Туберкулез и системная красная волчанка
Лечение туберкулеза с множественной лекарственной устойчивостью (МЛУ-ТБ) является клинически сложным, требующим как минимум 18 месяцев терапии. Его появление у пациента с системной красной волчанкой (СКВ) может осложнить управление как МЛУ-ТБ, так и СКВ. Это первый описательный отчет о МЛУ-ТБ у пациента с СКВ.
У 19-летней женщины, получавшей долгосрочный преднизолон для СКВ, был диагностирован МЛУ-ТБ. Она была начата в режиме лечения МЛУ-ТБ, а преднизолон был заменен азатиоприном. После первоначального ответа на терапию пациент испытывал вспышку симптомов волчанки. В исследованиях изображений выявлен аваскулярный некроз правой головки бедренной кости. Затем ее лечили внутривенным метил-преднизолоном, а затем поддерживали кортикостероидами. Азатиоприн был прекращен из-за гематологической токсичности и неконтролируемого СКВ. Ее симптомы волчанки регрессировали и не повторялись во время лечения МЛУ-ТБ. Пациент был объявлен излеченным от МЛУ-ТБ после 18 месяцев ATT. В настоящее время она запланирована для полной операции по замене тазобедренного сустава.
Этот случай освещает проблемы одновременного лечения МЛУ-ТБ и СКВ у пациента из-за их притирающих признаков и симптомов, взаимодействия с наркотиками и необходимости использования иммуномодулирующих средств в отсутствие стандартных рекомендаций и документированных предыдущих опытов. Наш опыт подчеркивает важность надлежащего выбора режимов лечения как МЛУ-ТБ, так и СКВ.
Системная красная волчанка — хроническое аутоиммунное заболевание. Заболеваемость туберкулезом и смертность у пациентов с СКВ высоки [1, 2]. С ростом туберкулеза с лекарственной устойчивостью во всем мире больные СКВ могут развиваться МЛУ-ТБ [3]. В этом случае мы показали успешное управление случаем МЛУ-ТБ у пациента с СКВ, несмотря на первоначальные проблемы с лечением.
В ноябре 2010 года 19-летняя этнически тибетская женщина с СКВ была обращена к нам с результатами исследований культуры мокроты и испытаний на чувствительность к лекарственным средствам (DST), которые продемонстрировали туберкулез с множественной лекарственной устойчивостью с резистентностью к изониазиду, рифампицину, этамбутолу, стрептомицину, этионамид и восприимчивость к канамицину, капреомицину, офлоксацину, моксифлоксацину, пиразинамиду, пара-аминосалициловой кислоте и клофазимину. Хотя не было четкой истории контакта с случаями ТБ, она проживала в школе-интернате, где в течение последних нескольких лет наблюдались случаи МЛУ-ТБ. До получения результата ДСТ она принимала противотуберкулезную терапию категории I (АТТ) изониазидом, рифампицином, пиразинамидом и этамбутолом в течение 45 дней без ответа. Она представила нам лихорадку, кашель и генерализованную слабость, и она была положительной мокротой для кислотоустойчивых бацилл. Рентгенограмма грудной клетки продемонстрировала двусторонние верхние и средние легкие инфильтраты с половыми поражениями (рис.1). 1Честная рентгенограмма, показывающая двусторонние верхние и средние легкие инфильтраты из-за МЛУ-ТБ у пациента, страдающего СКВ.
В 2006 году ей был поставлен диагноз СКВ после представления сыворотки, фоточувствительности и полисеросита (плевральный выпот, перикардиальный выпот, асцит). Тесты на антиядерные антитела и антитела против двухцепочечной ДНК были положительными. С тех пор она была на метилпреднизолон и гидроксихлорохин (HCQ). За год до презентации она принимала метил преднизолон 8 мг в альтернативные дни и HCQ 200 мг два раза в день.
24 ноября 2010 года мы начали лечение МЛУ-ТБ с помощью канамицина 600 мг, левофлоксацина 750 мг, пара-аминосалициловой кислоты — 8 г, циклосерина — 750 мг, пиразинамида — 1250 мг и клофазимина — 100 мг. Ее вес составлял 42 кг. Было начато снижение дозы метилпреднизолона и введена азатиоприн 50 мг с планом постепенного увеличения дозы до 100-125 мг. После постепенного конуса метилпреднизолон прекращают через 30 дней. Ее симптомы первоначально улучшались с разрешением лихорадки и опусканием кашля. Мазок мокроты стал отрицательным. Однако после 2 месяцев терапии МЛУ-ТБ она жаловалась на трудности с ходьбой с правым бедренной болью, излучающей колено, что еще хуже с движением, и развилось вяло. При осмотре наблюдалось заметное сокращение правой нижней конечности с мышечным истощением в бедрах и ногах. Через неделю у нее развилась сыпь бабочки на щеках, алопеция и повышенные трудности при ходьбе. Рентгенограмма тазобедренных суставов показала литические и склеротические поражения правой головки бедренной кости с нерегулярным контуром (рис.2). МРТ тазобедренных суставов проявляли несакальный некроз двусторонних бедренных головок, справа больше, чем левый, с минимальным выпотом правого бедра. Ее гемоглобин упал с 12 до 7,9 г%, а количество тромбоцитов снизилось с 260 000 до 68 000 мкл. Она была направлена на многодисциплинарную консультацию, которая не выявила признаков участия центральной нервной системы или волчаночного нефрита. Начали проводить импульсную терапию метилпреднизоном IV с последующим пероральным предсказанием преднизолона. Азатиоприн был остановлен с учетом возможной миелосупрессии, приводящей к анемии и тромбоцитопении. Пациент клинически улучшился, с разрешением кожной сыпи и артралгии. На нее вводили дозу преднизолона в дозе 7,5 мг, HCQ 200 мг два раза в день, добавки кальция и алендронат раз в неделю с витамином D3. Лечение МЛУ-ТБ продолжалось. Через два месяца после остановки азатиоприна уровень ее гемоглобина и количество тромбоцитов увеличились до 10,1 г / см3 и 139 000 мкмоль соответственно. Во время последующих ортопедических консультаций не наблюдалось прогрессирования остеонекроза тазобедренного сустава, и после завершения лечения МЛУ-ТБ была рекомендована полная замена тазобедренного сустава. Инъекционный канамицин прекращают через 9 месяцев ATT и пиразинамид прекращают через 1 год ATT. Последовательные мазки мокроты были отрицательными. У нее было 7 отрицательных культур для туберкулеза с начала лечения МЛУ-ТБ. После 18 месяцев ATT, она была объявлена вылеченной, и лечение ТБ было прекращено. В настоящее время она запланирована на операцию по замене тазобедренного сустава. 2Радиограмма с изображением поднятого правого полумесяца и нерегулярным контуром правого бедра с литическим и склеротическим поражением в головке бедренной кости у пациента с СКВ с диагнозом МЛУ-ТБ.
Насколько нам известно, это первый зарегистрированный случай МЛУ-ТБ у пациента с СКВ. Иммуносупрессия от хронической стероидной терапии и живущих в высокой распространенности ТБ и МЛУ-ТБ была важными факторами риска развития МЛУ-ТБ у нашего пациента с СКВ. Ранее сообщалось о высоком уровне МЛУ-ТБ в тибетском населении, проживающем в Индии [4]. Диагностика и лечение ТБ и особенно МЛУ-ТБ у пациента с СКВ создают несколько проблем. Мы считаем, что выделить четыре основных момента: (1) признаки / симптомы туберкулеза и СКВ могут имитировать друг друга, представляя собой диагностическую проблему, (2) токсичность лекарств от МЛУ-ТБ, включая кожную сыпь, артралгии, нефротоксичность, анемию, тромбоцитопения и симптомы ЦНС могут также имитировать признаки / симптомы СКВ и, таким образом, усложнять управление, (3) Взаимодействие лекарственных препаратов и перекрывающиеся токсичности могут усложнять управление СКВ и МЛУ-ТБ, особенно перед лицом микобактериальной устойчивости к фторхинолонам и / или аминогликозидам где может потребоваться использование более токсичных препаратов, таких как линезолид, которые имеют сходный профиль гематологической токсичности с иммуносупрессивными средствами, такими как азатиоприн, используемый для СКВ [5] и (4) Отсутствие четких рекомендаций, использование иммунодепрессантов и их доза корректировки у пациента с СКВ с МЛУ-ТБ могут быть клинически сложными для лечащего врача.
У этого пациента вовлечение тазобедренного сустава может быть вызвано длительной стероидной терапией, остеонекрозом из СКВ или МЛУ-ТБ тазобедренного сустава, хотя выявление аваскулярных некрозов двусторонних бедренных головок на МРТ и развитие ноги / сустава боли при приеме ATT предполагали хроническую стероидную терапию как этиологию. Трудно было четко различать хроническую стероидную терапию и СКВ как причину. Мы были обеспокоены использованием пиразинамида, учитывая ее участие в тазобедренном суставе и боли в ногах, поскольку пиразинамид может привести к гиперурикемии и артралгии [6]. Однако, поскольку симптомы нашего пациента утихали вскоре после повторного введения кортикостероида, мы решили продолжить пиразинамид в течение года, тщательно взвешивая риски и преимущества. Нашему пациенту повезло, что она восприимчива к основным противотуберкулезным препаратам второй линии: фторхинолонам и аминогликозидам. Вспышка SLE, которую она испытала во время лечения МЛУ-ТБ, вероятно, была вызвана попыткой отмены глюкокортикоидов, а не ухудшением ТБ, учитывая ее первоначальное улучшение после лечения МЛУ-ТБ, продолжающуюся отрицательную реакцию мокроты и быстрый ответ на перезапуск глюкокортикоидов. На протяжении всего курса лечения мы проявляли бдительность в отношении любых признаков и симптомов нейропсихиатрической волчанки, таких как депрессия, поскольку наш пациент также получал циклосерин для МЛУ-ТБ, который также может вызывать депрессию и вызывать суицидальные тенденции [7]. Таким образом, учитывая документированные более плохие результаты лечения МЛУ-ТБ в других иммунокомпромиссных состояниях [8, 9], становится важным, чтобы инициирование и корректировка дозы кортикостероидов и иммунодепрессантов для СКВ были осторожно выполнены, чтобы поддерживать соответствующий ответ к АТТ, а также для достижения длительной ремиссии СКВ. Кроме того, из-за перекрытия токсичности лекарств важно тщательный выбор режима лечения МЛУ-ТБ у пациента с СКВ.
Хотя СКВ и МЛУ-ТБ могут быть редкой комбинацией, рост глобальной заболеваемости МЛУ-ТБ может означать, что клиницисты во всем мире столкнутся с более подобными случаями [5]. Важно тщательно анализировать риски и преимущества при выборе компонентов лечения для МЛУ-ТБ и СКВ. Использование кортикостероидов, поддерживающих низкие дозы, было необходимо для контроля СКВ у нашего пациента, и это не отрицательно сказалось на результатах лечения МЛУ-ТБ. Частый и тщательный мониторинг очень важен. Фармакологическое управление должно быть индивидуализировано для достижения оптимального контроля болезни с минимальными неблагоприятными событиями с наркотиками. Разработка руководящих принципов для лечения МЛУ-ТБ при наличии хронических состояний, таких как СКВ, поможет врачам и пациентам во всем мире.
Письменное информированное согласие было получено от пациента для этого отчетного случая и любых сопроводительных изображений. Согласие доступно для просмотра Редакторами журнала.
KD и TS установили диагноз и управляли пациентом. К. Д. написал первый проект и провел обзор литературы. KD и AR отредактировали и внесли вклад в последующие проекты. Все авторы прочитали и утвердили окончательную рукопись.
Конкурирующие интересы Авторы заявляют, что у них нет конкурирующих интересов.
Полный текст:
- Аннотация
- Об авторах
- Список литературы
- Cited By
Высокая суммарная доза кортикостероидов при терапии системной красной волчанки (СКВ) и само заболевание являются факторами риска развития туберкулеза. Клинический случай освещает проблемы диагностики и одновременной терапии коморбидных заболеваний, сопровождающихся, с одной стороны, распространенным полиорганным туберкулезом, с другой, – чрезмерно выраженной активностью СКВ, усугубляющейся на фоне применения противотуберкулезных средств. Данный опыт подчеркивает важность назначения индивидуального режима химиотерапии туберкулеза с учетом переносимости противотуберкулезных препаратов и наличия побочных эффектов.
д-р мед. наук, доцент, зав. кафедрой фтизиатрии и пульмонологии
634050, г. Томск, Московский тракт, 2
зав. ревматологическим отделением терапевтических клиник
634050, г. Томск, Московский тракт, 2
канд. мед. наук, ассистент кафедры госпитальной терапии с курсом физической реабилитации и спортивной медицины, саркоидолог
634050, г. Томск, Московский тракт, 2
634009, г. Томск, ул. Р. Люксембург, 17/1
зам. главного врача по медицинской части
634009, г. Томск, ул. Р. Люксембург, 17/1
1. Falagas M.E., Voidonikola T.P., Angelousi A.G. Tuberculosis in patients with systemic rheumatic or pulmonary diseases treated with glucocorticosteroids and the preventive role of isoniazid: a review of the available evidence // International Journal of Antimicrobial Agents. 2007; 30: 477–486.
2. Yun J.E., Lee S.W., Kim T.H. The incidence and clinical characteristics of Mycobacterium tuberculosis infection among systemic lupus erythematosus and rheumatoid arthritis patients in Korea // Clin. Exp. Rheumatol. 2002; 20: 127–132.
3. Sayarlioglu M., Inanc M., Kamali S. Tuberculosis in Turkish patients with systemic lupus erythematosus: increased frequency of extrapulmonary localization // Lupus. 2004; 13: 274–278.
4. Белов Б.С., Соловьев С.К., Клюквина Н.Г., Тарасова Г.М., Полянская М.В. Коморбидные инфекции у больных системной красной волчанкой: современное состояние проблемы // Научно-практическая ревматология. 2016; (54) 4: 469–477.
5. Pasoto S.G., Borba E.F., Bonfa E., Shinjo S.K. Lupus pleuritis: a relevant risk factor for pulmonary tuberculosis // Lupus. 2010; 19: 1585–1590.
6. Клюквина Н.Г., Асеева Е.А., Никонорова Н.О. Поражение легких при системной красной волчанке: хорошо известные факты и нерешенные вопросы // Научно-практическая ревматология. 2016; (54) 5: 578–589.
7. Crispín C., Liossis S-N.C., Kis-Toth K. Pathogenesis of human systemic lupus erythematosus: recent advances // Trends in Мolecular Мedicine. 2010; 16 (2): 47–57.
8. Pathak S., Mohan C. Cellular and molecular pathogenesis of systemic lupus erythematosus: lessons from animal models // Pathak and Mohan Arthritis Research & Therapy. 2011, 13: 241–250.
9. Blanco P., Pitard V., Viallard J.F. Increase in activated CD8+ T lymphocytes expressing perforin and granzyme B correlates with disease activity in patients with systemic lupus erythematosus // Arthritis Rheum. 2005; 52: 201– 211.
10. Tam L.S., Li E.K., Wong S.M., Szeto C.C. Risk factors and clinical features for tuberculosis among patients with systemic lupus erythematosus in Hong Kong // Scand. J. Rheumatol. 2002; 31: 296–300.
11. Jick S.S., Lieberman E.S., Rahman M.U., Choi H.K. Glucocorticoid use, other associated factors, and the risk of tuberculosis // Arthritis. Rheum. 2006. 15; 55(1): 19–26.
12. Zhang L., Wang D.X., Ma L. Aclinical study of tuberculosis infection in systemic lupus erythematosus // Zhonghua Nei Ke Za Zhi. 2008; 47: 808–810.
13. Rovensky J., Kovalancik M., Kristufek P. Contribution to the problem of occurrence of tuberculosis in patients with systemic lupus erythematosus // Z. Rheumatol. 1996; 55 (3): 180–187.
14. Клюквина Н.Г. Проблема коморбидности при системной красной волчанке // РМЖ. 2015; 7: 370.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
Системные заболевания соединительной ткани — группа воспалительных аутоиммунных заболеваний неизвестной этиологии, характеризующаяся множественным поражением соединительной ткани различных органов и систем. В процесс могут вовлекаться, в том числе и все отделы дыхательной системы. В одних случаях патология легких связана непосредственно с системным поражением соединительной ткани в других носит вторичный характер. Нередко поражения разного характера сочетаются у одного пациента, и эта множественность повреждений лёгких является общей чертой системных заболеваний. В то же время каждое заболевание отличается своеобразием лёгочной патологии. Системные заболевания соединительной ткани имеют прогрессирующий характер и длительное, часто тяжёлое течение. Лёгочные проявления могут возникать на любой стадии или предшествовать болезни за несколько лет. Ведущими симптомами являются одышка, кашель и боли в грудной клетке. Самые частые синдромы — поражение плевры и интерстициальные болезни лёгких. Характерная этим заболеваниям дисфункция иммунной системы, а также использование в лечении глюкокортикостероидов и цитостатических препаратов повышают восприимчивость организма к инфекции, способствуют развитию тяжелых осложнений (пневмония, сепсис и туберкулёз). Наряду с обычными возбудителями пневмоний, осложнения нередко вызываются условно-патогенной флорой, микобактериями туберкулёза, вирусами и грибами.
Системная красная волчанка (СКВ)— аутоиммунное заболевание, характеризующееся системным поражением сосудов различного калибра. Для СКВ характерно наличие в сыворотке крови высоких титров антинуклеарных факторов (АНФ), антител к нативной ДНК и антигену Смитта (Sm-Ag), низкий уровень комплемента.
По сравнению с другими системными заболеваниями поражение лёгких при СКВ представлено самым широким спектром синдромов:
Клиническая картина поражения лёгких наблюдается в 1-6% случаев заболевания СКВ, по данным мультиспиральной компьютерной томографии (МСКТ) поражение легких отмечается уже в 30%, а на аутопсии — в 70% случаев СКВ сопровождается поражением легких.
Основа лечения системной красной волчанки — глюкокортикостероидные препараты и иммуносупрессивные средства. Без лечения прогноз неблагоприятный, при адекватной терапии возможно достижение ремиссии.
Ревматоидный артрит (РА) — симметричное хроническое воспаление в первую очередь суставов кистей и стоп, сопровождающееся постепенным разрушением (деструкцией) их структуры. Иммунологическая особенность РА — выработка аутоантител класса IgM к собственным иммуноглобулинам (ревматоидные факторы), которые обнаруживаются в сыворотке крови в умеренных или высоких титрах. Наряду с поражением суставов у 20-30% больных развиваются внесуставные проявления, к которым относят ревматоидные узелки и ревматоидный васкулит. Наиболее типичные проявления васкулита— дигитальный (пальцевой) артериит, язвы кожи, периферическая нейропатия и васкулит внутренних органов (лёгких, сердца, почек). Риск летального исхода при развитии внесуставных проявлений увеличивается в 5 раз. Для ревматоидного артрита характерны бронхоэктазы и бронхиолиты, а также поражение плевры, лёгочных сосудов (васкулит, лёгочная гипертензия), альвеолярные геморрагии, развитие интерстициальных заболеваний легкого (ИЗЛ). Плеврит — самое частое поражение лёгких при РА, протекает малосимптомно, с небольшим количеством выпота, отмечается примерно у 25% больных. У трети больных плеврит ассоциируется с ИЗЛ, течение которого при ревматоидном артрите может быть очень медленным (10 лет и более) или фульминантным (молниеносным, мгновенным). Ревматоидные узелки (РУ) в лёгких обнаруживаются редко (в 1-2%). У 10-15% больных развивается опасное осложнение — вторичный амилоидоз, в том числе с вовлечением лёгких. Доказано более частое развитие лимфом, миеломной болезни и лейкозов на фоне ревматоидного артрита.
Системная склеродермия (прогрессирующий системный склероз) — группа заболеваний, в ранней стадии которых превалируют нарушения микроциркуляции и воспаление, постепенно приводящие в дальнейшем к генерализованному фиброзу (склерозу). Типичные аутоиммунные нарушения при системной склеродермии — образование антицентромерных антител и антител к антигену топоизомеразы1 (Scl-70). Заболевание отличается разнообразием появлений, самым ярким из которых является уплотнение кожных покровов. Диффузная форма склеродермии характеризуется острым развитием и быстрым прогрессированием генерализованного фиброза кожи и внутренних органов (сердца, лёгких, почек). Относительно доброкачественная лимитированная форма дебютирует феноменом (синдромом) Рейно, кожные изменения имеют ограниченный характер, прогрессируют медленно и сопровождаются сосудистыми ишемическими расстройствами. Поражение лёгких при склеродермии встречается чаще, чем при других системных заболеваниях, у мужчин чаще, чем у женщин. Патология легких при мультиспиральной компьютерной томографии (МСКТ) у больных системной склеродермией отмечаются в 80-90% . Чаще всего это интерстициональное заболевание легких (ИЗЛ) и легочная гипертензия (ЛГ). Причиной ЛГ в 12-15% могут быть также фиброзные поражения левых отделов сердца (клапан, миокард). Легочная гипертензия чаще ассоциируется с лимитированной формой болезни и выявляется у больных с длительным анамнезом, ИЗЛ с диффузной формой. Инфекционные осложнения (пневмонии, абсцедирование) возникают реже, чем при других системных заболеваниях. Риск развития рака легкого на фоне системной склеродермии повышается в 3-5 раз.
Идиопатические воспалительные миопатии - группа заболеваний, в основе клинических проявлений которых лежит воспаление поперечнополосатой мускулатуры (полимиозит, дерматомиозит, ювенильный дерматомиозит и т.д.). Иммунологическими маркёрами являются миозит-специфические антитела, направленные к цитоплазматическим белкам и рибонуклеиновым кислотам. Чаще других встречаются антитела к аминоацилсинтетазам тРНК (Jo-1 и др.).
Поражение мышц проявляется симметричной слабостью проксимальных (расположенных ближе к туловищу) групп мышц верхних и нижних конечностей и мышц, участвующих в сгибании шеи, что проявляется затруднением при подъёме с низкого стула; при посадке в транспорт; при умывании и причёсывании. Характерно поражение мышц глотки, гортани и верхней трети пищевода (дисфония, дисфагия). Внутриорганные проявления разнообразны, наиболее часто встречается поражение дыхательной системы. Типично для миопатий поражение межрёберных мышц и диафрагмы, что приводит к затруднению дыхания, одышке. Пневмония осложняет течение полимиозита и дерматомиозита у 30-50% больных. Ведущую роль в её развитии играет аспирация пищи, связанная с поражением мышц глотки и верхней трети пищевода (аспирационный синдром). Наиболее тяжёлым поражением лёгких является интерстициональное заболевание (ИЗЛ), признаки которого в 10% случаев предшествует симптомам мышечного поражения.
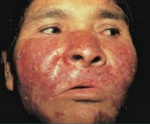
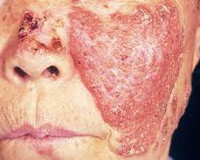
Туберкулёзная волчанка – это распространённая форма казеозно-некротического туберкулёзного поражения кожи, затрагивающая преимущественно лицо и верхнюю половину туловища. Проявляется образованием бугорков (люпом) с изъязвлениями, постепенно сливающихся воедино, частичным или полным обезображиванием лица. Диагностируется с помощью дерматологического осмотра, исследования отделяемого кожи (микроскопия, ПЦР), специфических тестов. Лечение проводят противотуберкулёзными антибиотиками, иммуностимуляторами и другими вспомогательными средствами.
МКБ-10
- Причины
- Патогенез
- Классификация
- Симптомы туберкулёзной волчанки
- Осложнения
- Диагностика
- Лечение туберкулёзной волчанки
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Туберкулёзная волчанка (туберкулёз кожи люпоидный, вульгарная волчанка) – самая распространённая, хронически протекающая форма локального туберкулёза со склонностью к расплавлению тканей. По данным официальной статистики, средний показатель выявления вульгарной волчанки составляет 0,43 больных на 100 000 населения (4,1% от частоты всего внелёгочного туберкулёза). Заболеванию подвержены дети и подростки, люди зрелого возраста страдают реже. Заболевание чаще обнаруживается у женщин. Люпоидный туберкулёз имеет длительное рецидивирующее течение и без лечения может прогрессировать на протяжении всей жизни.

Причины
Возбудитель заболевания - грамположительный микроорганизм (палочка Коха), не склонный к образованию спор, но обладающий высокой устойчивостью к химическими агентам и факторам окружающей среды. В большинстве случаев волчанка вызывается M. tuberculosis, иногда – M. bovis. В кожу и слизистые бактерии проникают эндогенно с током крови или лимфатической жидкости из других очагов туберкулёзной инфекции (лёгочная ткань, кости, суставы, периферические лимфатические узлы), имеющихся в организме. Случаи экзогенного заражения от других лиц через повреждённую кожу встречаются гораздо реже при плотном контакте с бактериовыделителем.
Вероятность развития туберкулёзного поражения кожных покровов увеличивается при отсутствии воздействия солнечного света (инсоляции). Прямое влияние ультрафиолетового излучения убивает микобактерии туберкулёза в течение нескольких минут. Факторами риска также считаются травмы, переохлаждения, снижающие активность иммунитета человека и способствующие активации латентной инфекции. Предрасположенность к аллергическим реакциям (крапивница, отёк Квинке) повышает вероятность более тяжёлого течения болезни.
Патогенез
После попадания возбудителя в кожу из первичного очага гематогенным или лимфогенным путём формируется люпома размером с булавочную головку. Она представляет собой первичный морфологический элемент вульгарной волчанки и является скоплением мелких туберкулёзных бугорков. При массивном инфицировании повреждённой кожи контактным путём возникает инфильтрат, напоминающий очаг Гона, сопровождающийся лимфаденитом и лимфангоитом.
При гистологическом исследовании в дерме обнаруживаются люпомы из эпителиодных клеток и клеток Лангханса, на периферии располагается зона из лимфоцитов и плазмоцитов. Творожистый некроз в бугорках отсутствует или выражен незначительно. Выявляются изменённые, деформированные сосуды (вплоть до полного заращения). В эпидермисе происходит чрезмерное утолщение рогового слоя, гиперпигментация, формирование папиллом.
Классификация
В зависимости от клинической картины заболевания выделяют несколько форм волчанки, которые различаются по интенсивности проявлений и внешним признакам. Различают: плоскую, язвенную, псориазиформную, птириазиформную, бородавчатую, опухолевидную и другие менее распространённые разновидности. Нередко язвенная и плоская формы могут сочетаться друг с другом.
- Плоская. Отдельные люпомы сливаются между собой, формируя очаг поражения. Он увеличивается в результате возникновения в периферических отделах новых бугорков. Поверхность очага ровная, шелушения незначительные или отсутствуют.
- Язвенная. Возникает при массивном изъязвлении поверхности люпом. Язвы неглубокие, кровоточат при прикосновении. Нередко развиваются деформации хрящей носа, ушной раковины, что способствует обезображиванию лица.
- Псориазиформная. Люпома внешне напоминает бляшку псориаза. На поверхности находятся серо-белые чешуйки с шелушением, кожа по периферии гиперемирована.
- Птириазиформная. Характеризуется отрубевидным крупным шелушением в зоне поражения.
- Бородавчатая. Типично образование разрастаний белесоватого цвета, внешне напоминающих бородавки.
- Опухолевидная. Представляет собой несколько слившихся бугорков. Они образуют большую мягко-эластичную опухоль, склонную к распаду или формированию язв.
В клиническом течении волчаночного процесса выделяют четыре стадии. Каждая имеет особенности течения, определяющие тяжесть состояния больного:
- Инфильтративная. Наблюдается отёк, гиперемия тканей, люпомы не выражены.
- Бугорковая. Формируются мелкие бугорки, которые соединяются и напоминают бородавчатые вегетации.
- Язвенная (может отсутствовать). Сверху на люпомах появляются кровоточащие язвы, нередко возникают папилломы.
- Рубцовая. Если процесс не проходил стадию изъязвления, рубцы ровные и блестящие. После эпителизации язв формируются плотные деформирующие рубцы.
Симптомы туберкулёзной волчанки
Болезнь развивается постепенно: сначала в дерме формируются бугорки размером 1-8 мм, имеющие жёлтую, коричневую, бурую, серую окраску. Люпомы имеют тестоподобную консистенцию, ровную блестящую поверхность, где впоследствии возникают шелушения. Бугорки всегда безболезненны, высыпают в количестве нескольких штук на расстоянии друг от друга, постепенно сливаясь: по периферии возникает застойная область. Патологический процесс чаще всего локализуется в области ушных раковин, носа, скул, верхней губы, может переходить на переднюю поверхность шеи и плечи, затрагивать слизистые оболочки с образованием грубых рубцов.
Люпомы соединяются между собой, увеличиваются в размерах, формируя неровные бляшки либо опухолеподобные очаги. Из-за процессов некроза в центре возникают глубокие язвы. При особенно тяжёлом течении волчанки у пациентов с ослабленным иммунитетом в деструкцию вовлекается не только кожа, но и хрящевые ткани. При разрушении перегородки носа он напоминает заострённый укороченный клюв птицы. Нарушается обоняние, страдает дыхательная функция.
Из-за деструкции выворачиваются веки, уменьшается в размерах ротовое отверстие, истончаются и обламываются хрящи ушных раковин. Поражение слизистой оболочки ротовой полости приводит к нарушению жевательной и глотательной функции: больные часто попёрхиваются, тяжело усваивают твёрдую пищу. При вовлечении в патологический процесс голосовых связок может изменяться голос: он становится глухим, осиплым.
В течение 4-6 недель наступает заживление повреждённых тканей. После завершения активного язвенного процесса на поверхности кожных покровов формируются плоские нежные рубцы, напоминающие папирус.
Осложнения
Формирующиеся рубцы вызывают контрактуры, ограничивают движение мимических мышц: это становится причиной полной или частичной потери артикуляционных способностей (при поражении лица, ротовой полости, гортани). При отсутствии своевременного лечения к туберкулёзной волчанке может присоединиться вторичная инфекция – рожистое воспаление. Если воспалительный процесс переходит на лимфатические сосуды, развивается лимфангит. В 4% всех случаев на фоне туберкулёзной волчанки возникает базальноклеточная карцинома.
Диагностика
Диагностика туберкулёзной волчанки проводится на основании данных общего осмотра и физикальных исследований. При выявлении заболевания необходимо сотрудничество дерматолога и фтизиатра, так как необходимо обнаружение и лечение первичного очага туберкулёза. Для диагностического поиска наиболее информативны:
- Физикальное обследование. С его помощью устанавливается распространённость бугорков, их цвет, консистенция. В результате гибели эластиновых волокон при прощупывании бляшки пуговчатым зондом он без сопротивления погружается внутрь неё (симптом Поспелова). Если же на люпому надавливают предметным стеклом, кожа обескровливается, а сами бугорки приобретают вид жёлто-коричневых пятен (признак Гентчинсона или феномен яблочного желе).
- Лабораторная диагностика возбудителя. Проводится окраска биологического материала (кожного отделяемого) по Цилю-Нильсену и последующее микроскопическое исследование с иммерсионной системой. Микобактерии имеют вид красных палочек на синем фоне. Полимеразная цепная реакция за 5-7 часов позволяет определить небольшое количество ДНК микобактерий в исследуемом образце.
- Проведение туберкулиновых проб. Проба Манту и Диаскинтест оцениваются, исходя из увеличения размеров инфильтрата и папулы более 5 мм, свидетельствующих о заражении. Реже используют скарификационные пробы (Пирке, градуированную пробу): они показывают положительный результат на наличие микобактерий.
- Квантифероновый тест. Обнаруживает в крови гамма-интерферон, появляющийся в организме человека в ответ на внедрение микобактерий. Метод обладает высокой специфичностью (99,1%) и чувствительностью (89%). Его аналог - T-SPOT.TB тест, выявляющий сенсибилизированные Т-лимфоциты.
- Инструментальные методы. Проводится рентгенография грудной клетки в прямой и боковой проекции, выявляющая первичный очаг туберкулёза в лёгких. Поражение костей и других внутренних органов можно обнаружить с помощью КТ или МРТ.
В общем анализе крови при туберкулёзной волчанке наблюдается понижение уровня лейкоцитов, связанное с основным заболеванием. Значительное уменьшение лимфоцитов и повышение СОЭ являются неблагоприятными прогностическими признаками. С целью оценки реактивности организма выполняется иммунограмма. Дифференциальный диагноз проводится с красной волчанкой, бугорковым сифилисом, туберкулоподопной лепрой.
Лечение туберкулёзной волчанки
В современной дерматологии предусмотрено использование комплексных методов терапии. Пациенты с туберкулёзной волчанкой должны лечиться в специализированном диспансере с соблюдением палатного или общего режима. Назначается диета с ограничением соли, быстрых углеводов, рекомендуется к употреблению пища, богатая белками. Следует также полностью отказаться от вредных привычек (они способствуют снижению иммунитета). Консервативная терапия включает в себя:
- Противотуберкулёзные препараты (химиотерапию). Для этого используется первая линия средств (изониазид, рифампицин, рифабутин, пиразинамид, этамбутол, стрептомицин), дозировки подбираются фтизиатром индивидуально. Другие линии применяются при развитии лекарственной устойчивости.
- Вспомогательную терапию. Для уменьшения побочных эффектов от противотуберкулёзных антибиотиков назначают симптоматические препараты: антиоксиданты, иммуностимуляторы, глюкокортикоиды, витамины, анаболики, гепатопротекторы.
- Физиотерапевтические процедуры. Особенно эффективно ультрафиолетовое облучение наружных покровов, которое стимулирует процессы регенерации, вызывает гибель микобактерий, уменьшает вероятность развития осложнений. Среди других методик часто используют лекарственный электрофорез с антибактериальными препаратами, лазерную терапию, индуктотермию, лечебную гимнастику, УВЧ-терапию.
Хирургическое удаление изъязвлённых участков кожных покровов и хрящей проводится только при риске вторичного инфицирования. При выраженном обезображивании для восстановления внешнего вида впоследствии могут быть использованы пластические операции по пересадке кожных лоскутов и хрящевых тканей. С их помощью восстанавливают целостность носовой перегородки, формируют ушные раковины, иссекают деформирующие рубцы.
Прогноз и профилактика
Туберкулёзная волчанка – хроническое заболевание. При своевременном выявлении и лечении прогноз благоприятный. Повторное возникновение болезни наблюдается только в случае нарушения схемы лечения или развития у микобактерий устойчивости к лекарственным препаратам. Профилактика туберкулёзной волчанки сводится к лечению основного заболевания, соблюдению правил личной безопасности при контакте с заражёнными (использование перчаток, масок) и укреплению иммунитета.
Читайте также:


