Иммунограмма при ревматоидном артрите

Ревматоидный артрит (РА) ‒ аутоиммунное ревматическое заболевание неизвестной этиологии, характеризующееся хроническим эрозивным артритом (синовитом) и системным поражением внутренних органов [5]. Известно, что в основе патогенеза РА лежат выраженные нарушения иммунного ответа, при этом важная роль в развитии и прогрессировании данного заболевания отводится лимфоцитарной и цитокиновой системам. За последние годы достигнут значительный прогресс в изучении патогенеза РА, а также в разработке современных средств диагностики и лечения данного заболевания. Однако изучение состояния молекулярных рецепторов лимфоцитарной системы и взаимосязи их с провоспалительными цитокинами при РА остается актуальной и недостаточно исследованной
проблемой.
Представления о содержании субпопуляций Т-лимфоцитов периферической крови и их значении при РА немногочисленны и противоречивы.
По данным исследователей, у больных РА по сравнению с группой здоровых лиц имеет место Т-лимфопения ‒ снижение относительного содержания CD3+ лимфоцитов [4].
В периферической крови у больных РА ряд авторов не обнаружили значительного изменения содержания CD4+ Т-лимфоцитов [4], другие выявили достоверное увеличение этих клеток [9]. По данным ряда исследователей, в периферической крови больных РА отмечается снижение содержания CD8+ Т-лимфоцитов как следствие нарушения сбалансированности иммунного ответа [3]. По другим данным, у больных РА содержание CD8+ Т-лимфоцитов нормальное или повышено [7]. По данным литературы, у больных РА в периферической крови повышено содержание CD8+ Т-лимфоцитов клеток памяти и понижено содержание соответствующих эффекторных клеток, что связано с ускоренной дифференцировкой Т-клеток памяти с фенотипами CD4+ и CD8+[6].
У больных РА выявлена активация гуморального звена иммунной системы, характеризующаяся увеличением содержания В-лимфоцитов периферической крови, что сопровождается увеличением Ig и ЦИК [4].
РА является системным аутоиммунным заболеванием, при котором преобладающая пусковая роль принадлежит Т-хелперам первого типа.
Важным последствием поляризации иммунного ответа по Th1 типу является нарушение баланса синтеза провоспалительных и противовоспалительных цитокинов.
Интерферон гамма (IFNγ) является важным медиатором как доиммунной защиты, так и развивающегося специфического иммунного ответа. Этот цитокин регулирует адаптивный иммунный ответ, влияя на антигенпрезентирующие фагоциты и антигенраспознающие лимфоциты. IFNγ является главным медиатором клеточного иммунитета, стимулируя поляризацию клеток в направлении Th1. Кроме того, IFNγ способствует дифференцировке Т и В-лимфоцитов, является основным активатором макрофагов, стимулирует синтез антител В-лимфоцитами, увеличивает синтез основных провоспалительных цитокинов ‒ TNF-α, IL-1, IL-6, рекрутирует CD4+ ‒Т-лимфоциты и другие клетки-эффекторы в очаг воспаления [2]. В связи с этим, IFNγ способен усиливать аутоиммунные реакции. Использование современных иммуноферментных методик показало, что концентрация IFNγ достоверно повышена в сыворотке крови и в синовиальной жидкости больных РА [8]. По данным других авторов, у больных РА снижена способность лейкоцитов и лимфоцитов к продукции IFNγ [3]. Рядом исследователей продемонстрирован отчетливый лечебный эффект антител к IFNγ у больных РА [1].
Цель работы
Изучить состояние молекулярных рецепторов иммунной системы: CD3+, CD4+, CD8+, CD19+, иммунорегуляторного индекса ‒ ИРИ (CD4+%/ CD8+%), а также регулятора иммунного воспаления IFNγ у больных РА, оценить взаимосвязи между Т-, В-лимфоцитами и IFNγ. Выявить состояние CD3+, CD4+, CD8+, CD19+, ИРИ, IFNγ в зависимости от активности заболевания.
Материал и методы
Нами обследовано 80 женщин, больных РА, у которых диагноз соответствовал критериям АРА 1987 года. Средний возраст пациенток составил ‒ 51,96±1,36 года, длительность заболевания ‒ в среднем 7,24±0,7 лет.
Первая степень активности воспалительного процесса выявлена у 6,2 % больных, вторая ‒ у 45 % и третья ‒ у 48,8 % пациентов. У 80 % больных была определена серопозитивная форма РА. Рентгенологические изменения I-II степени отмечались у 52,5 % больных, III-IV ‒ у 47,5 %. Системные проявления в виде амиотрофии (67,5), ревматоидных узелков (26,2 %), лихорадки (22,5 %), лимфоаденопатии (21,25 %), гепатоспленомегалии (17,5 %), сетчатого ливедо 10 %), дигитального артериита (6,2 %) были обнаружены у 48,8 % больных. Преобладали больные со II функциональным классом заболевания ‒ 40 % и III ‒ 55 %. Группу сравнения составили 25 здоровых лиц, репрезентативных по возрасту и полу.
Для оценки выраженности суставного синдрома и функциональной способности больного использовались: анамнез; оценка степени выраженности болевого синдрома больным с применением 100 мм визуальной аналоговой шкалы (ВАШ); продолжительность утренней скованности в мин.; число болезненных и припухших суставов (исходя из 68 и из 44 суставов соответственно); суставной индекс Ричи (оценка 53 суставов). Всем больным проводилось лабораторное и инструментальное исследование: общий анализ крови и общий анализ мочи, определение С-реактивного белка (СРБ) (полуколичественный латекс-тест); ревматоидного фактора (РФ) (твердофазный иммуноферментный анализ); рентгенологическое исследование пораженных суставов. Состояние молекулярных рецепторов лимфоцитарной системы CD3+, CD4+, CD8+, CD19+ определяли, используя иммуноцитохимический субпопуляционный анализ лимфоцитов крови. Субпопуляции лимфоцитов периферической крови идентифицировали как в процентном их соотношении, так и в пересчете на абсолютные показатели. IFNγ сыворотки крови определяли методом твердофазного иммунноферментного анализа.
Статистическую обработку материала производили на персональном компьютере с помощью программы Statistica 6,0.Данные представлены в виде средней арифметической величины (M) и стандартной ошибки среднего (m). Для определения статистической значимости различий использовали Т-критерий Стъюдента. Взаимосвязи между переменными вычислялись при помощи коэффициента корреляции Пирсона r. Различия считались достоверными при р 0,05), что, вероятно, связано с миграцией В-лимфоцитов из периферической крови в очаг воспаления. В группе больных РА по сравнению с группой здоровых лиц отмечена тенденция к увеличению процентного содержания CD8+ (24,82±0,42 % и 22,04±0,95 % соответственно, р>0,05) и тенденция к снижению ИРИ (1,46±0,03 и 1,54±0,07 соответственно, р>0,05). Вероятно, у больных РА нарушена функция цитотоксических лимфоцитов, неспособных контролировать аутоиммунное воспаление. Не определено изменение относительного содержания CD3+, CD4+, лимфоцитов крови у больных РА по сравнению с группой контроля (р>0,05, рис. 1).
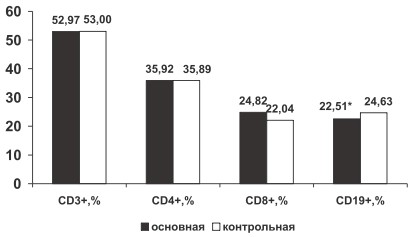
Рис. 1. Изменение относительного содержания CD3+, CD4+, CD8+, CD19+ крови у больных РА в основной и контрольной группах
* ‒ (р 0,05, рис. 2), что связано с активацией лимфоцитарной системы при хроническом иммуновоспалительном процессе.
Уровень IFNγ в периферической крови больных РА по сравнению с группой контроля был увеличен в 3 раза (249,92±33,84 пг/ мл и 73,89±6,55 пг/мл, р 0,05, таблица) при различных степенях активности РА достоверно
не изменялось.
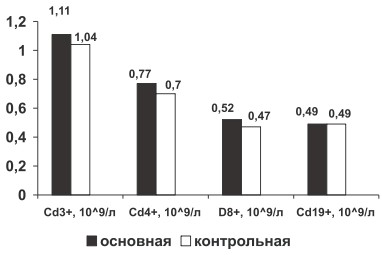
Рис. 2. Изменение абсолютного содержания CD3+, CD4+, CD8+, CD19+ крови у больных РА в основной и контрольной группах
У больных со 2-й степенью активности по сравнению с 1-й, наблюдается тенденция к увеличению абсолютного содержания изучаемых лимфоцитов крови CD3+, CD4+, CD8+, CD19+ и снижению ИРИ (р>0,05, таблица).
Изменение содержания молекулярных рецепторов лимфоцитарной системы крови и цитокинов в зависимости от активности РА (М ±m)
Ревматоидный артрит (РА) сокращает жизнь человека на 10-15 лет. Уже в первые 5-7 лет болезни половина пациентов утрачивает трудоспособность, а через 20 лет с момента заболевания число инвалидов увеличивается до 60-90%. Раннее выявление РА играет важную роль в оценке активности, стадии заболевания и течения патологии, а также в составлении прогноза болезни и эффективности лечения.
В статье мы рассмотрим, какие показатели крови при артрите повышены, узнаем, как снизить СОЭ при ревматоидном артрите, выясним причины повышения С-реактивного белка и укажем основные принципы лечения заболевания.
Значимость лабораторных исследований
РА —, распространенное и тяжелое аутоиммунное заболевание. Для него характерны такие признаки, как опухание и покраснение кожных покровов над пораженным суставов, тугоподвижность и утренняя скованность в суставе, болезненность, особенно после физической активности, местное повышение температуры и другие проявления в зависимости от формы болезни.
Чтобы определить ревматоидный артрит, выделяют широкий спектр биомаркеров или показателей крови.
Наиболее значимы для артрита:
- аутоантитела,
- показатели острой фазы воспалительного процесса,
- цитокины,
- показатели активации эндотелия,
- показатели активации субпопуляции лимфоцитов,
- показатели метаболизма костной и хрящевой ткани,
- генетические маркеры.
Для анализов на артрит и артроз используют кровь, синовиальную жидкость и синовиальную ткань.
Основные анализы
Какие анализы необходимо сдавать при ревматоидном артрите и болях в суставах, решают специалисты: терапевт, ревматолог, иммунолог и другие.
В большинстве клинических случаев назначают исследования, которые мы подробно рассмотрим ниже.
Диагностика РА требует дифференциального подхода, поскольку патология имеет похожие клинические признаки с рядом других заболеваний. Первоначально врач назначает общий анализ крови и мочи.
Например, количество лейкоцитов при РА редко превышает норму и свидетельствует об аутоиммунном характере заболевания. Если патология вызвана вирусом, то содержание лейкоцитов будет пониженным, а лимфоцитов – повышенным. Такой процесс наблюдается при вирусном поражении суставов, например, при гепатите.
Показатель уровня гемоглобина при РА снижен до 110 г/л, при норме в 120-140 г/л. Это вызвано тем, что при РА жизненный период эритроцитов снижается или уменьшается их выработка в костном мозге, впоследствии это приводит к уменьшению гемоглобина в крови. По мере ухудшения состояния больного, уровень гемоглобина понижается.
Анализ мочи необходим для исключения схожих патологий. У больного РА выявляется повышенный уровень белка и наличие лейкоцитов в моче, но эти показатели —, не специфические для РА.
СОЭ определяет наличие воспалительного процесса и его интенсивность. Чем выше показатель отклонения от нормы, тем интенсивнее процесс воспаления суставов. СОЭ определяется при общем анализе крови.
Индикатор используют для диагностики острой и хронической инфекции, аутоиммунных заболеваний, инфарктов внутренних органов. Уровень СОЭ увеличивается при злокачественных опухолях, по время беременности, при приеме некоторых лекарственных препаратов (например, салицилатов).
Норма СОЭ у женщин 2-15 мм/час, у мужчин 1-10 мм/час. Повышение СОЭ до 20-30 мм/час происходит при анемиях, в период беременности или менструации. Значительное повышение более 60 мм/час говорит о наличии воспаления, аутоиммунного заболевания, злокачественной опухоли, которая сопровождается распадом тканей, или лейкозе.
Показатель СОЭ не специфичен и его можно использовать только в совокупности с другими индикаторами. Однако это самый распространенный способ определения наличия и интенсивности воспаления.
Биохимический анализ крови устанавливает наличие воспаления и его интенсивность.
- белок гаптоглобин свидетельствует о сильном воспалительном процессе при РА,
- фибриноген выше нормы 2-4 г/л говорит об интенсивном аутоиммунном процессе, его превышение указывает на опасность образования тромбов,
- сиаловые кислоты в норме составляют 2-2,33 ммоль/л, превышенные показателя свидетельствует о наличии воспаления в соединительной ткани сустава и разрушении коллагена,
- кроме того, проводят лабораторные анализы на белки сыворотки (серомукоиды), иммуноглобулины и пептиды.
В зависимости от превышения нормы по указанным маркерам определяется интенсивность воспалительного процесса.
C-реактивный белок используется наряду с показателем СОЭ для определения воспалительного процесса. Чем выше показатель С-реактивного белка, тем тяжелее и интенсивнее процесс воспаления.
В норме его значение не превышает 5 мг/л, при РА показания бывают на уровне от 400 мг/л и больше. У детей С-реактивный белок выступает маркером наличия бактерий в крови при заболеваниях костей и суставов.
Повышенный уровень С-реактивного белка отмечается при бактериальных и вирусных инфекциях в остром периоде, инфаркте миокарда, злокачественных опухолях и аутоиммунных заболеваниях.
Уровень роста С-реактивного белка прямо пропорционален СОЭ , т.е. чем выше СОЭ, тем выше С-реактивный белок.
Но есть исключения:
- показатель С-реактивного белка резко повышается даже при незначительном заражении тканей, СОЭ при этом остается в пределах нормы,
- уровень С-реактивного белка не увеличивается, а СОЭ растет при некоторых вирусных инфекциях, тяжелой интоксикации, некоторых формах хронического артрита.
Уровень С-реактивного белка изменятся в течение суток, поэтому следует измерять его в динамике.
Ревматоидный фактор (РФ) представляет собой антитела, которые синтезируются клетками синовиальной оболочки сустава. Отсюда они попадают в кровь, образуют иммунные комплексы и повреждают стенки сосудов и синовиальную оболочку.
РФ используют для диагностики ряда заболеваний (опухоли, гельминтоз, васкулит). Его присутствие в крови еще не говорит о наличии РА.
У здорового человека РФ в крови отсутствует. При РА выявление РФ 25-50 МЕ/мл считается умеренным повышением, 50-100 МЕ/мл – высоким, более 100 МЕ/мл – предельно высоким.
У детей РФ может появляться из-за частых ОРВИ, гриппе или стафилококко-стрептококковой инфекции. После лечения РФ пропадает, если этого не происходит, значит, в организме протекает аутоиммунная реакция. Также РФ может повышаться в период полового созревания, в 13-15 лет из-за скачков половых гормонов.
РА имеет две формы по ревматоидному фактору: серопозитивную и серонегативную. При серопозитивной форме анализ на РФ будет положительным. От этого зависит тактика лечения больного.
Пациенты с серопозитивной формой РА страдают от более тяжелого течения болезни: сильного воспаления, более трудного достижения ремиссии, выраженностью деструктивного процесса в суставах и внесуставных проявлений.
Что такое АЦЦП? Расшифровка АЦЦП: антитела к циклическому цитруллинированному пептиду. 
АЦЦП —, специфический маркер РА. При ревматоидном артрите в анализе крови характерно их высокое содержание (до 95%), которое показывает наличие повреждений тканей суставной капсулы.
Если ткани находятся в здоровом состоянии, норма показателя находится в пределах от нуля до трех единиц/мл. При развитии патологии норма при анализе на АЦЦП при ревматоидном артрите возрастает от 58 до 87 Ед./мл.
Высокие показатели свидетельствуют о значительных процессах разрушения хряща сустава.
АЦЦП обнаруживаются уже на начальной стадии заболевания, это особенно ценно для ранней диагностики РА (до 6 месяцев). Они вырабатываются за год до появления первых признаков патологии.
Анализ на АЦЦП при ревматоидном артрите необходим при отрицательном РФ (серонегативная форма болезни).
Его показатели не изменяются в течение болезни, поэтому анализ не информативен для отслеживания динамики развития патологии или ухудшения патологического процесса.
Антинуклеарные тела воспроизводятся иммунной системой. Они работают против ядерных белков клеток. Анализ на антинуклеарные тела делают в случае выявления воспаления, происхождение которого не ясно, и считается самым распространенным в диагностике аутоиммунных заболеваний.
Такие тела выявляются более чем у 90% пациентов с заболеваниями соединительной ткани суставов. Кроме этого, анализ используют для диагностики множества инфекционных, воспалительных и онкологических патологий.
Для ревматоидного артрита они не специфические, но присутствуют в организме при таких патологиях, как системная красная волчанка, коллагенозы, гепатит, склеродермия и другие.
Анализы на маркеры гепатита В и С обусловлены тем, что болезнь может проявлять себя как аутоиммунное заболевание. В таком случае воспаление пораженных суставов выступает единственным признаком болезни.
Маркеры вирусных гепатитов делят на специфические и неспецифические. Специфические позволяют определить вид вируса, а неспецифические —, определить заболевание в процессе его развития.
Своевременная диагностика гепатита В позволяет вылечить заболевание до начала его прогрессирования, можно определить вид вирусного возбудителя, время заражения, этап болезни и ее течение. На основе полученных результатов исследования составляют наиболее эффективную схему лечения.
При гепатите С выявление индикаторов на начальном этапе позволяет избежать обострения и развития цирроза. Иногда можно избежать развития хронического течения болезни и устранить вирус полностью.
Для проведения качественного анализа на маркеры при гепатите проводится распределение иммуноглобулинов (Ig) по классам М и G. В случае когда в крови обнаружен IgM, в организме диагностируют хронические процессы. При наличии IgG говорят, что болезнь уже была перенесена.
К признакам, указывающим на острую форму заболевания, специалисты относят:
- выявление поверхностного HbsAg антигена,
- наличие белка HBeAg,
- присутствие иммуноглобулина анти-HBc.
HbsAg антиген – это наиболее ранний маркер вирусного заболевания, проходящего в острой фазе. Он обнаруживается в анализах по прошествии 4 или 6 недель после инфицирования, когда процесс проходит острую либо преджелтушную стадию. Такие маркеры обнаруживаются даже в случае отсутствия признаков вирусного возбудителя.
HbeAg антиген формируется на раннем этапе патологии и в преджелтушный период. Маркер свидетельсвует об активном процессе распространения вируса в организме. Если он обнаруживается на протяжении 4 и более недель, то это значит, что болезнь находится в хронической форме.
Наличие анти-Hbs говорит о патологии, находящейся в конце острого этапа развития. Эти маркеры могут обнаруживаться в течение 10 и больше лет, их наличие указывает на формирование иммунитета.
Анти-Hbe указывает на динамику заражения. Соотношение показателей (anti-Hbe:HbeAg) помогает контролировать течение болезни и прогнозировать ее исход.
Антитела anti-Hbc IgM к маркеру HbcAg могут находиться в крови от 3 до 5 месяцев, их обнаружение указывает на наличие острой формы гепатита В.
Антитела анти-HbcIgG к маркеру HbcAg указывают на настоящее присутствие патологии либо на то, что болезнь была перенесена ранее.
Однако в анализах могут присутствовать не только маркеры вирусных гепатитов, рассмотренные выше. Если речь идет о группе С, к результатам присоединяется HCV-RNA – рибонуклеиновая кислота, она свидетельствует о патологии, обнаруживается в печеночных тканях либо в крови.
Рассмотрим антитела к гепатиту С.
Анти-HCV total присутствуют в случае острой либо хронической формы патологии, они выявляются спустя 6 недель после инфицирования. Даже в случае успешного самоизлечения организма, что встречается в 5% случаев, их обнаруживают в течение 5-8 лет. 
Анти-HCV core IgG обнаруживаются на 11 неделе после заражения. При хронической стадии эти антитела выявляются постоянно, их количество снижается после выздоровления и с трудом определяется лабораторными исследованиями.
Анти-NS3 присутствуют в крови на начальном этапе формирования болезни, их повышенное количество указывает на острую стадию гепатита С.
Маркеры вирусного гепатита С анти-NS4, анти-NS5 выявляются только на последних этапах развития патологии, когда имеет место поражение печени. Их уровень после выздоровления падает, а после применения Интерферона в качестве лечения они могут полностью исчезнуть.
Антитела к гепатиту А IgM выявляются сразу после появления желтухи, представляя собой диагностический маркер гепатита А-группы в остром периоде болезни. Эти антитела присутствуют в крови на протяжении от 8 до 12 недель, а у 4 % пациентов могут выявляться на протяжении 12 месяцев.
Достаточно скоро после формирования IgM в крови начинают формироваться антитела IgG – после появления они сохраняются в течение всей жизни и гарантируют наличие стойкого иммунитета.
Если в крови обнаружены анти-HAV–IgG и отсутствуют анти-HAV–IgM, можно говорить об имеющемся иммунитете к гепатиту А на фоне перенесенной ранее инфекции, либо это указывает на проведенную вакцинацию против вируса.
Анти-HAV–IgG формируется в сыворотке примерно через 14 суток после проведения вакцинации и после того, как было произведено введение иммуноглобулинов. При этом количество антител больше если, пациент перенес инфекции, нежели после того, как произошла пассивная передача.
Важно! Антитела этого типа передаются от матери к плоду трансплацентарным способом и часто обнаруживаются у малышей, возраст которых превышает 1 год. Количество суммарных антител по отношению к HAV определяется и используется только с эпидемиологической целью или же чтобы выявить предвакцинальный статус.
Антитела IgM преобладают в случае острой инфекции и проявляются, как правило, на ранней стадии процесса. Затем они обнаруживаются на протяжении всей жизни, причем у 45% взрослых пациентов выявляется наличие антител в сыворотке.
Генетические анализы при РА назначаются для выявления антигенов, определяющих предрасположенность к аутоиммунным заболеваниям. Такие индикаторы могут подтвердить или опровергнуть диагноз. Обнаружение антигена у здорового человека не всегда будет свидетельствовать о потенциальной угрозе развития заболевания.
Интерпретация результатов анализов
Для диагностики врач проводит качественный и количественный анализ результатов лабораторных исследований. Он тщательно сопоставляет данные как в начале обращения пациента при дифференциальной диагностике, так и в динамике для контроля результатов терапии. Дать заключение на основе анализов способен только специалист.
Заключение
Своевременный и качественный анализ крови при ревматоидном артрите позволяет выявить болезнь на ранней стадии, предотвратить развитие тяжелых форм заболевания, а также дифференцировать подозрения на другие схожие патологии.
Для диагностики РА может потребоваться множество исследований. Они необходимы как для установки точного диагноза, так и для контроля эффективности лечения. С их помощью корректируют и подбирают наиболее подходящую терапию в динамике.
Анализы на ревматоидный артрит обязательны при проявлении симптомов патологии и для дифференциального обследования. Ревматоидный артрит — аутоиммунное заболевание, сопровождающееся воспалением, симптомы которого настолько расплывчаты и неспецифичны, что без дифференциальных исследований уточнить диагноз не представляется возможным. Какие анализы являются специфичными, а какие имеют значение только при рассмотрении совокупности всех показателей?

При уточнении диагноза такого сложного вида патологии анализы при ревматоидном артрите можно разделить на:
- специфические — позволяющие с высокой степенью достоверности подтвердить или опровергнуть предварительный диагноз;
- неспецифические — выявляют присутствие отдельных признаков и только в совокупности подтверждают диагноз.
Для лечения суставов наши читатели успешно используют СустаЛайф. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…

Анализ крови при ревматоидном артрите помогает обнаружить циркулирующие аутоантитела и маркеры острой фазы воспалительного процесса. Специфическим анализом является определение ревматоидного фактора и выявление антител к циклическому цитруллинированному пептиду (АЦЦП). Именно исследование на АЦЦП стало передовым шагом в диагностике ранних форм ревматоидного артрита и определении патологии при серонегативной форме заболевания или при отсутствии выраженных симптомов.
По данным исследования НИИР РАМН, у пациентов с выявленным Р-фактором признаки ревматоидного артрита отмечались уже через год после проведенного исследования у 56% обследованных. Среди тех, у кого результат был отрицательным, через тот же период времени патология развилась у 44%.
В то время как при позитивном результате на АЦЦП заболевание через год развилось у 70% обследованных, а при негативном — у 30%. Приведенные результаты убедительно доказывают высокую валидность, чувствительность и информативность метода, которым проводится исследование АЦЦП.

Неспецифическим исследованием на ревматоидный артрит является анализ на присутствие маркеров острого воспалительного процесса. Когда диагностируют ревматоидный артрит, анализ крови из пальца на СОЭ (РОЭ) показывает повышенный (по сравнению с нормой) результат. Величина интервала полученных показателей маркеров и их референсных значений свидетельствуют об активной фазе воспалительного процесса в организме.
При подозрении на наличие патологии и для дифференциации ревматоидного артрита врач обязательно назначит следующие анализы:
- крови: клинический, биохимический, иммунологический, АЦЦП;
- общий мочи;
- внутрисуставной жидкости;
- биоптата суставной оболочки и др.
Анализ крови помогает определить факторы наличия ревматоидного артрита даже на стадии, предшествующей появлению симптомокомплекса. При исследовании клинического анализа факторов крови обращают внимание на следующие показатели, которые являются острофазовыми маркерами:
- активность гемоглобина;
- СОЭ;
- лейкоцитарную формулу;
- число тромбоцитов;
- количество криоглобулинов.
Результаты этих исследований напрямую связаны со стадией, на которой находится патологический процесс в организме больного.

Биохимические исследования крови пациента проводятся для установления активности следующих составляющих:
- гаптоглобина — белка острой фазы, который контролирует течение и прогрессирование воспалительного процесса;
- фибриногена в плазме крови — при повышении активности указывает на воспаление и активную фазу аутоиммунного заболевания;
- сиаловых кислот — при превышении является диагностическим и прогностическим признаком активного воспалительного процесса;
- серомукоидов — сывороточных белков;
- пептидов;
- γ — глобулинов;
- криоглобулинов (IgM, IgG, IgA и др.).
Повышение уровня всех перечисленных факторов крови свидетельствует о том, что в организме протекает острый воспалительный процесс. Эти же факторы определяют и во внутрисуставной жидкости. Кроме того, эти белки вырабатываются не только клетками печени, но и органами иммунной системы, что косвенно может свидетельствовать и об ее уровне.
Определение уровня АЦЦП является самым информативным из современных методов раннего диагностирования заболевания, так как антитела к циклическому цитруллинированному пептиду вырабатываются задолго до того, как больной почувствует первые симптомы заболевания. Разница между возможными и существующими сроками установления патологии составляет более 10-15 лет, что дает надежду на быстрое начало лечения, то есть еще до возникновения необратимых изменений в суставах.
Так, например, в результате множества клинических исследований была установлена достоверная связь между наличием Р-фактора и внешним воздействием на организм внешних и внутренних факторов, что снижает прогностическую ценность этого показателя.
Диагностическая чувствительность тестов разная, поэтому для получения цельной картины анализируются результаты всех перечисленных исследований. Ниже в таблице приведены полученные в результате клинических исследований показатели чувствительности методов исследования:
| Принятое сокращение | Расшифровка | Показатель чувствительности (%) |
| АМЦВ | Аутоантитела к модифицированному цитруллинированному виментину | 78 |
| АЦЦП | антитела к циклическому цитрулиннированному пептиду | 77 |
| IgМ РФ | Р- фактор представленный иммуноглобулином IgМ | 71 |
| IgА РФ | Р- фактор представленный иммуноглобулином IgА | 43 |
| АКА | Антикератиновые антитела | 43 |
| ARA33 | Антитела к ядерному антигену RA33 | 31 |
| АНФ | Антинуклеарный фактор | 31 |
Обычно при подозрении на данную патологию должны сдаваться анализы АЦЦП и РФ. Но если они будут отрицательными, то может быть назначено углубленное обследование, которое включает АМЦВ и ARA33. Так, например, IgМ РФ определяется не только при остром воспалительном процессе, но и при злокачественных процессах в пожилом возрасте. Поэтому и разрабатываются комплексы анализов, которые помогут увеличить чувствительность методов исследования.
Иммунологические анализы проводят с помощью иммуноферментного анализа. В настоящее время апробируются и другие методы исследования, которые помогут повысить достоверность результатов и просчитать риск развития патологии еще до ее возникновения. Так, например, оцениваются методы генного, транскриптомного и протеомного анализов, которые позволяют проанализировать генетически обусловленные риски появления патологий суставов.
Для того чтобы установить диагностические признаки заболевания, необходимо полученные результаты анализов сравнить с нормой или референсными значениями исследуемых показателей.
Одним из исследуемых показателей является уровень гемоглобина. Установлено, что при ревматоидной патологии происходит снижение активности эритроцитов и количества гемоглобина за счет укорочения периода жизни эритроцитов или нарушения функции их продукции костным мозгом. В норме уровень гемоглобина в крови взрослого человека должен составлять 120–160г/л, но при данной болезни пороговое значение составляет 110 г/л. При прогрессировании патологии — гораздо меньше.

Норма АЦЦП — 3 Ед/мл. При ревматоидном артрите значение этого показателя может колебаться в интервале 58–87 Ед/мл. Увеличение интервала свидетельствует о прогрессирующем процессе разрушения хрящевой ткани. Чем больше эта разница, тем сильнее выражен дегенеративный процесс. Норма АМЦВ составляет менее 20 Ед/мл. О патологии свидетельствует повышение показателя, которое уже через несколько лет после появления первых признаков может достигать 62–86 Ед/мл.
Негативным проведенный анализ на Р-фактор считается при показателе менее 25МЕ/мл. При серопозитивной форме патологии это значение может составлять 59МЕ/мл, а при серонегативном — 18МЕ/мл. Норма ARA 33 составляет менее 25 МЕ/мл, но при патологии уровень возрастает — 30-32МЕ/мл.
Примечательно, что наблюдается отличие в этих показателях при ревматоидном артрите (РА) и других воспалительных заболеваниях суставов, что позволяет дифференцировать РА от подагры, остеоартроза, эрозивного артрита и др. Нормы показателей, которые определяются при биохимическом анализе крови, составляют:
- гаптоглобин — в крови 0,8-2,7 г/л, в моче 0,0–4,2 мг/л;
- фибриноген — 2–4 г/л;
- сиаловая кислота — 620–730 мг/л (2,0–2033 ммоль/л);
- серомукоиды — 1,2–1,6 ммоль/л;
- гамма-глобулин — 8–13,5 г/л .

Повышение этих показателей свидетельствуют не только о наличии воспалительного процесса. Так, например, увеличение количества сиаловых кислот возникает при разрушении коллагеновой ткани. Повышение количества гаптоглобина свидетельствует о процессе разрушения эритроцитов, характерном для данного заболевания.
Сравнение изменений составляющих протеинограммы помогает определить, на какой стадии находится патология, сколько времени прошло от возникновения дегенеративных нарушений. Сдать анализы требуется и для определения эффективности терапевтических методов, применяемых для лечения болезни.
Проходить исследования нужно при предрасположенности к данному заболеванию, а также при достижении возраста после 50 лет. Анализ полученных результатов и интерпретация их позволяют на начальных стадиях определить наличие заболевания или рассчитать с высокой степенью достоверности фактор риска.
Екатерина Юрьевна Ермакова
- Карта сайта
- Диагностика
- Кости и суставы
- Невралгия
- Позвоночник
- Препараты
- Связки и мышцы
- Травмы
Анализ крови при артрите
Артритом называется воспаление костных и хрящевых тканей сустава. Оно может быть вызвано инфекцией, травмой, аллергической реакцией или стать следствием другой патологии опорно-двигательного аппарата. В медицине различают реактивный, инфекционный, ревматоидный, ювенильный, травматический, псориатический и другие разновидности заболевания (всего их насчитывается больше 10).
В связи с таким количеством вариаций постановка точного диагноза является достаточно сложной, поскольку начальные клинические проявления многих видов системных заболеваний соединительной ткани отличаются мало, а типичные симптомы проявляются на поздних стадиях, когда для лечения требуется затратить намного больше времени и усилий. При дифференциальной диагностике заболеваний суставов, кроме аппаратных методов обследования (рентгенографии, МРТ, УЗИ, контрастная артрография) в обязательном порядке проводят лабораторные исследования крови.

Чтобы результаты исследований были объективными, пациенту нужно соблюдать следующие правила:
- за 2-3 дня перед сдачей анализа следует исключить из рациона жирные блюда;
- за 8 часов до проведения исследования пищу принимать нельзя;
- если это не представляет опасности для здоровья, в течение суток следует отменить прием лекарственных препаратов;
При диагностике артрита проводится несколько видов исследования крови, каждый из которых несет информацию о качественных и количественных отклонениях от нормы:
- Общий (клинический). При проведении ОАК определяют эритроциты, тромбоциты, лейкоциты, гемоглобин, СОЭ, гематокрит.
- Биохимический. Предполагает исследования физико-химических свойств компонентов крови: уровень сиаловой и мочевой органических кислот, а также белков ― гаптоглобина, фибриногена и С-реактивного белка.
- Иммунорферментный (ИФА). Представляет собой тестирование ферментов-маркеров ― ревматоидного фактора, антинуклеарных и других специфических антител.
На основании результатов анализов можно сделать выводы о наличии воспалительного заболевания, а также определить его принадлежность к тому или иному виду артрита.
Общий анализ крови позволяет обнаружить наличие очага воспаления, но не обеспечивает классификацию заболевания. Наиболее важными показателями при диагностике артрита являются скорость оседания эритроцитов (СОЭ), а также количество гемоглобина и лейкоцитов. Нормой считаются показатели:
- лейкоциты 4,0-9,0×109/л;
- гемоглобин 120-150 г/л;
- СОЭ не выше 25 мм/ч.
На видео ниже представлена более полная информация об основных показателях ОАК.

Самым надежным лабораторным методом, позволяющим обнаружить наличие воспалительного процесса, считается СОЭ. Помещенная в пробирку кровь постепенно разделяется: эритроциты, как более тяжелые частицы, оседают на дно, а легкие фракции остаются в верхнем слое. При воспалении белковый состав крови изменяется, и скорость оседания эритроцитов сразу же возрастает, достигая иногда 60 мм/ч и более.
Анализ крови на биохимию дает возможность выявить воспаление и степень его развития, а также характерные для того или иного вида артрита изменения состава плазмы и фирменных элементов крови.
Нормой считаются показатели:
- общий белок 63÷86 г/л;
- мочевая кислота 0,25÷0,50 ммоль/л;
- сиаловые кислоты 135÷200 у.е.;
- гаптоглобин 150÷2000 мг/л.
При артрите наблюдается рост количества вырабатывающихся в печени фибриногенов (они отвечают за свертываемость крови), повышается уровень участвующего в продуцировании красных кровяных телец гаптоглобина. Высокой чувствительностью обладает уровня С-реактивного белка в сыворотке крови: повышенное содержание этого элемента обнаруживается в первые сутки развития воспалительного процесса.
Для лечения суставов наши читатели успешно используют СустаЛайф. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…

Результаты биохимического исследования используются для дифференциальной диагностики заболеваний суставов. Так, увеличение концентрации сиаловых кислот, которые образуются при распаде тканей, могут свидетельствовать о наличии заболевания ревматоидного типа, превышение нормы мочевой кислоты ― о подагрическом артрите.
Основные показатели иммуноферментного исследования крови:
- Ревматоидный фактор. При проведении исследования выявляются антитела к изменившему при воспалении синовиальной оболочки сустава воспаления белку. В норме величина РФ не превышает 10÷14 ед/мл, резкое увеличение количества антител считается одним из характерных признаков ревматоидного артрита.
Высокий ревматоидный фактор обнаруживается в крови 5-7% здоровых людей, в то же время у 50% больных РА результат анализа на РФ отрицательный. Следовательно, данный метод диагностики не является абсолютно достоверным и служит для постановки предварительного диагноза.
- Антитела к циклическому цитруллинированному пептиду. Атипичное для здорового организма белковое соединение цитруллин вырабатывается в синовиальной оболочке сустава при аутоиммунных воспалительных заболеваниях соединительной ткани, в частности, при ревматоидном артрите. Для их уничтожения организм продуцирует особые иммуноглобулины, которые связывают и нейтрализуют чужеродный пептид.
- Антитела к ЦЦП обнаруживаются у 70-80% больных РА, и появляются в сыворотке намного раньше других маркеров заболевания, иногда за год до проявления первых симптомов. Поэтому измерение уровня АЦЦП считается одним из эффективных и достоверных методов ранней диагностики артрита. Норма содержания антител к циклическому цитруллинированному пептиду ― 0÷3 ед./мл.
- Антистрептолизин О. Данный метод лабораторного исследования основан на определении количества антител к стрептококкам, и применяется для дифференциальной диагностики. Норма АСЛО для взрослого человека ― до 200 ед./мл. В случае ревматоидного артрита этот показатель не превышает нормы, он увеличивается при ревматизме, а также реактивном артрите, который развивается как осложнение после перенесенного инфекционного заболевания.

Анализы крови при артрите являются одним из наиболее эффективных методов дифференциальной диагностики, позволяющим исключить другие, схожие по симптомам заболевания, и обнаружить патологию в самом начале развития, а иногда даже до появления ее первых внешних признаков.
Читайте также:







