Циклоп синдром коленного сустава что это
Циклоп-синдром – это осложнение после пластики передней крестообразной связки, возникающее вследствие рубцевания трансплантата в межмыщелковом пространстве.
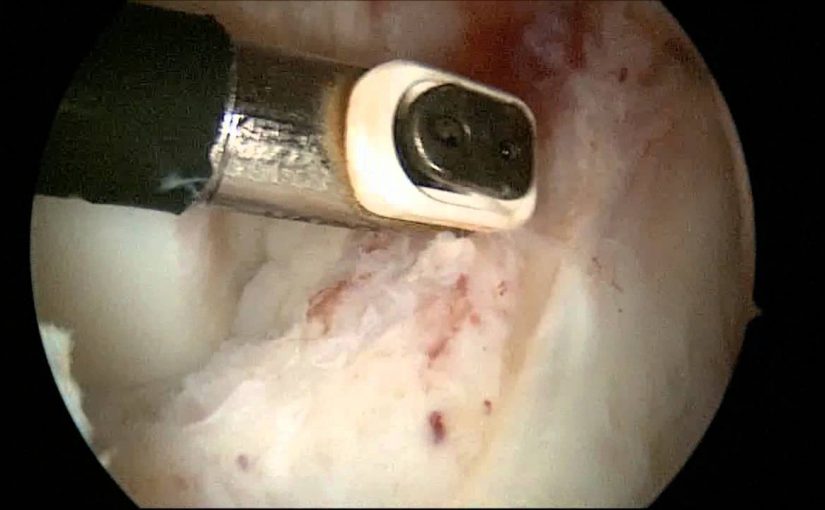
Этиология
При пластике ПКС трансплантатом из собственной связки надколенника (техника ВТВ) трансплантат значительно утолщается в результате ремоделирования и рубцовых процессов. Возникновению циклоп-синдрома способствуют следующие факторы:
- Переднее расположение большеберцового канала при пластике ПКС,
- Невозможность достижения полного разгибания в раннем послеоперационном периоде,
- Нотч-пластика (не подтверждено).
Значительно реже циклоп-синдром возникает после пластики ПКС с использованием сухожилия полусухожильной мышцы. В этом случае причиной является рубцевание дистальной культи ПКС, сохранённой в ходе операции.
Ведущий симптом – ограничение разгибания в коленном суставе, которое может быть постоянным или периодическим. Пациенты часто отмечают улучшение разгибания во время лечебной гимнастики, однако спустя примерно час объем движений возвращается к исходному уровню. Также может появится непостоянный блок в коленном суставе, вызванный разрывом мениска.
Доминирующим симптомом у пациентов с минимальным ограничением разгибания может стать боль в области бедренно-надколенникового сустава.
Основную диагностическую ценность имеют сбор анамнеза и клинический осмотр. Ограничение разгибания имеет пружинящую конечную точку.
Специфические клинические тесты для диагностики циклоп-синдрома отсутствуют. Тест Лахмана следует проводить во всех случаях. Наличие циклоп-синдрома не означает послеоперационной стабильности.
Для оценки большеберцового канала можно выполнить рентгенографию в боковой проекции. Рекомендовано также исследование в боковой проекции под нагрузкой в положении Лахмана (30° сгибания) или в положении максимального разгибания, выполняемое с целью документации. Переднее положение большеберцового канала легко определяется.
Чем более кпереди сформирован большеберцовый канал, тем выше вероятность развития симптоматичного рубцевания трансплантата ПКС.
По данным МРТ можно определить положение большеберцового канала (сформирован ли слишком кпереди) и наличие рубцовой ткани кпереди от ПКС, обычно имеющей образования с низкой интенсивностью сигнала.
У пациентов с характерным анамнезом и послеоперационным ограничением разгибания диагноз считается установленным, поэтому выполнение МРТ нецелесообразно.
При ревизии межмыщелкового пространства определяются узелки рубцовой ткани разных размеров. При попеременном сгибании и разгибании видно, как рубцовая ткань собирается между мыщелками бедренной и большеберцовой костей, создавая препятствие для полного разгибания.
Внешний вид рубцовой ткани различен. Нередко можно обнаружить объёмную однородную рубцовую массу, расположенную дистальнее трансплантата ПКС. В некоторых случаях рубцовая ткань пигментирована и состоит из множества образований меньших размеров. Как правило, в рубцовой ткани отмечаются голубоватые или багровые участки кровоизлияний, возникающих вследствие постоянной микротравматизации. Для рубцовой ткани характерна волокнистая структура, что требует её дифференцировки от волокон трансплантата.
Размеры волокнистого узелка различны, их диаметр может варьировать от 5 мм до 2-4 см и даже более.
Лечение
Консервативные методы лечения отсутствуют. Даже интенсивное восстановительное лечение не уменьшит ограничения разгибания.
Единственно эффективный метод лечения – артроскопическое иссечение рубцовой ткани, что в большинстве случаев приводит к полному восстановлению объёма движений. У большинства пациентов полное разгибание в коленном суставе возможно сразу после оперативного вмешательства. У остальных полный объем движений восстанавливается только после реабилитационной терапии, направленной на растяжение задней капсулы.
Если после реабилитационной терапии объем разгибания не восстановлен полностью, следует исключить фиброз задней капсулы, например, в случае её повреждения во время первичной травмы и недостигнутого полного разгибания в раннем реабилитационном периоде, либо в тех случаях, когда первичная пластика ПКС была выполнена в остром периоде травмы.
- Ревизия.
- Пальпация щупом.
- Резекция рубцовой ткани.
- Извлечение рубца.
- Очищение трансплантата от оставшейся рубцовой ткани.
- Тест на импиджмент.
- Мобилизация.
- Гемостаз.
После операции конечность помещается в ортез для сохранения разгибания и растяжения задней части капсулы. Гиперэкстензионные ортезы, 0° ортезы и этапные гипсовые повязки очень болезненны для некоторых пациентов и являются препятствием для реабилитационной терапии.
Есть сведения о хороших результатах, достигнутых при использовании ортезов, поддерживающих задние отделы сустава (PTS splint), которые используются при повреждениях ЗКС. Смещая большеберцовую кость кпереди по отношению к бедру, ортез помогает растянуть заднюю часть капсулы. Это переносится лучше, чем растяжение капсулы принудительным разгибанием.
Интенсивное восстановительное лечение начинается после удаления дренажа в первый послеоперационный день. При значительном и долговременном ограничении разгибания рекомендуется стационарное лечение в отделении реабилитации.
Пациент должен быть информирован о возможном рецидиве циклоп-синдрома, требующем повторного хирургического вмешательства.
Самое полезное по теме: "Циклоп синдром коленного сустава" от профессионалов. Здесь подготовлен полный тематический материал в удобном для чтения виде.

Циклоп синдром коленного сустава
БОЛЕЗНЬ ГОФФА КОЛЕННОГО СУСТАВА
(диагностика и лечение в амбулаторных условиях)

Берглезов М.А., Угнивенко В.И., Вялько В.В.
Колено является сложной биомеханической системой с большим количеством анатомических образований, способствующих выполнению функции. Связки колена являются главным стабилизирующим компонентом. Не менее важены мягкотканный вспомогательный аппарат коленного сустава, включающий слизистые сумки, жировые тела в области крыловидных складок, мениски, а также функциональное состояние мышц выполняющих движения в коленном суставе и стабилизирующих его.
Диагностика патологических процессов коленного сустава мо-жет быть затруднена по ряду причин, в частности, из-за недоста-точно пристального выяснения обстоятельств и механизма травмы или начала заболевания, невнимательного клинического обследова-ния сустава и неправильной оценки симптомов, недостаточно ква-лифицированной интерпретации рентгенограмм.
Одним из недифференцированных симптомов ряда заболеваний коленного сустава является боль, хромота, ощущение дискомфорта в суставе, хруст, припухлость, ограничение подвижности, контрак-туры и деформации, истинные и ложные блокады сустава.
Из наиболее распространенных сопутствующих, осложняющих течение деформирующего артроза, или самостоятельных заболеваний коленного сустава являются следующие: менископатия или хроничекий менисцит, болезнь Гоффа, хронический синовит различной этиоло-гии с нередким ущемлением синовиальных ворсин, пигментно-ворсинчатый синовит, бурсит или тендиноз в области нижнего полюса надколенника, наружный пателлярный компрессионный синдром с подвывихом надколенника или без него, наличие в полости коленного сустава свободных хрящевых и костно-хрящевых тел различного происхождения (Голикова Н.М., Ушакова О.А.,1988).
В сложных случаях, клинико-рентгенологическое исследование дополняется артропневмогафией и магнитой резонансной томографией (МРТ).
Одним из объективных методов исследования коленного сустава является артропневмография. Методика введения кислорода в коленный сустав не сложна и заключается в пункции коленного сустава тонкой иглой с последующим введением медленно под давлением 120 мм. рт. ст. медицинского кислорода в объеме от 60 до 120 мл. Рентгеновский снимок выполняют в ближайшие 10 — 15 минут после манипуляции. Особенного информативен рентгеновский снимок в боковой проекции. Методика артрографии коленного сустава позволяет оценить состояние суставной капсулы, наличие так называемых кист Беккера (Фанке К., 1981; Ricklin P.,1964). На снимке видны: заполненный кислородом верхний, задний завороты синовиальной сумки, состояние области крыловидных складок (Рис.1), что является достаточно надежным диагностическим признаком в случае гипертрофии жировых тел Гоффа (Н.М.Голикова,1975,1979).
Рисунок 1. Артропневмограмма коленного сустава в норме (после введения кислорода под давлением 100мм.рт.ст.). Хорошо выражен верхний заворот (А). Контуры тел Гоффа (Б) без признаков гипертрофии.

До появления методики магнитного резонансного изображения, оценка функции и морфологии коленного сустава ограничивалась медицинским осмотром, артрографией и данными компьютерной томографии. Появление методики анализа МРТ изображения со своей уникальной способностью изображать компоненты мягкой ткани революционизироло оценку связочного и мягкотканного аппарата коленного сустава (Nicholas JA, Frieberger RH, Killoran PJ ,1970; Brown DW, Allman FL Jr, Eaton SB, 1978; Crabtree SD, Bedford AF, Edgar MA, 1981; Thijn CJP,1982; Selesnick FH, Noble HB, Bachman DC, 1985). Наиболее легко оценивается изображение в сагитальной плоскости.

На МРТ передне-нижней области коленного сустава виден тонкий слой подкожной мягкой ткани, затем — накопление жира называемого препателлярной жировой подушкой (fat pad prepatellaris) или телами Hoffa. Наиболее локализованная область сигнальной интенсивности в норме определяется под нижним полюсом надколенника, что не должно рассматриваться как патологическое состояние (El-Khoury GY, Wira RL, Berbaum KS, et al, 1992). Сигналы внутреннего и наружного менисков соедияет связка Winslow (Watanabe AT, Carter BC, Teitelbaum GP, et al,1989). Жировые тела Гоффа выделяются на МРТ по величине и интенсивности проявления (Рис.2).
Рисунок 2. МРТ коленного сустава в сагитальной плоскости. Тела Гоффа.

В 1904 г. А. Гоффа описал заболевание крыло-видной складки коленного сустава, которое в настоящее время носит его имя. «Я обнаружил данное заболевание при операции па коленном суставе, когда я предполагал наличие поврежденного мениска. Но мениски при вскры-тии сустава оказались интактными. Однако я обратил внимание на обширную гиперплазию жи-ровой ткани под связкой надколенника. Это на-блюдение показало, что мы имеем дело с весьма типичной картиной заболевания. Если мы будем препарировать здоровый коленный сустав, то под связкой надколенника увидим две крыловидные и одну синовиальную складки. Пер-вые представлены жировой тканью, которая по-крыта синовиальной оболочкой, напоминающей собой мягкую липому, распространяющуюся от переднего края большеберцовой кости в полость сустава….Таким образом, речь идет о характерном заболевании, которое лучше всего обозначить как воспалительную гиперплазию жировой ткани с прорастанием ее плотной фиброзной соединительной тканью.
Этот воспалительный процесс, поскольку отсут-ствуют какие-либо другие этиологические момен-ты, обычно связан с травмой. Гипертрофированный тяж в дальнейшем ущемляются между мышелками бедренной и большеберцовой костей, что является новым стимулом для усугубления процесса воспаления.
Хроническое воспаление и дегенерация, известное как Hoffa болезнь, возникает в пределах препателлярной жировой подушки. Равномерная гипертрофия может провести к блокаде жировой ткани между бедренной костью и большой берцовой костью. Диагноз обычно устанавливается артроскопически (Ogilvie-Harris DJ and J. Giddens, 1994).
По данным современной литературы, лечение хронического воспаления жировой клетчатки и блокирования коленного сустава преимущественно хирургическое и заключается в иссечении жировых тел в области переднего отдела коленного сустава.
Синдром Гоффа часто встречается в молодом возрасте как результат прямой травмы переднего отдела коленного сустава и обычно сопровождается клиникой повреждения менисков. Проводимая в таких случаях артроскопия является методом радикального лечения этого заболевания. Однако, наибольшую проблему амбулаторной ортопедии представляют больные средних и старших возрастных групп, хирургическое лечение которых по различным причинам нежелательно.
По нашим наблюдениям, болезнь Гоффа чаще всего встречается у женщим в пре- и постменопаузальном периоде в возрасте от 45 до 65 лет, что указывает на очевидную связь гиперплазии жировой клетчатки коленного сустава с нарушением гормонального фона.
У всех больных отмечена характерная клиническая картина: неполное разгибание сустава без явной заинтересованности менисков и связочного аппарата, припухлость сустава в передне-нижнем отделе, псевдофлюктурирующее крепитирующее образование по обе стороны от собственной связки надколенника, гипоторофия, снижение функции 4-х главой мышцы бедра и ее внутренней головки, функциональная нестабильность коленного сустава. Среди всех случаев тяжелого нарушения функции нижних конечностей, вызванных ортопедической патологией, тяжелые нарушения функции, вызванные болезней Гоффа болезнь Гоффа составляют 12%, что указывает не только на рапространенность этой патологии, но и на тяжесть ее течения.
При рентгенологическом исследовании выявлены признаки артроза коленного сустава I-II стадий по Н.С.Косинской, что вероятно и явилось основанием ошибочного диагноза. На артропневмограммах определялись характерные изменения: уменьшение обьема и регидность верхнего заворота коленного сустава, увеличесние объема заднего заворота с развитием грыжевого выпячивания в подколенную область — кисты Беккера, гипертрофия жировой клетчатки в области нижнего полюса надколенника с внедрением ее в между бедренной и большеберцовой костями (Рис 3). Нередко на рентгеновских снимках в области крыловидных складок определяются отложения кальция — калькулезный бурсит.
Рисунок 3. Артропневмограммы коленного сустава больных с сндромом Гоффа. Гипертрофия жировых тел области крыловидных складок (А), уменьшение обьема и регидность верхнего заворота коленного сустава, увеличесние объема заднего заворота, киста подколенной области (киста Беккера).


Лечение синдрома Гоффа коленного сустава в амбулаторных условиях.
Циклоп синдром коленного сустава что это

Многие годы пытаетесь вылечить СУСТАВЫ?
Глава Института лечения суставов: «Вы будете поражены, насколько просто можно вылечить суставы принимая каждый день средство за 147 рублей.
При пластике ПКС трансплантатом из своей связки надколенника (техника ВТВ) трансплантат существенно утолщается в итоге ремоделирования и рубцовых действий. Появлению циклоп-синдрома содействуют последующие причины:
Для лечения суставов наши читатели успешно используют Sustalaif. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
- Переднее размещение большеберцового канала при пластике ПКС,
- Невозможность заслуги полного разгибания в ранешном послеоперационном периоде,
- Нотч-пластика (не доказано).
Существенно пореже циклоп-синдром возникает опосля пластики ПКС с внедрением сухожилия полусухожильной мускулы. В этом варианте предпосылкой является рубцевание дистальной культи ПКС, сохранённой в ходе операции.
Ведущий симптом – ограничение разгибания в коленном суставе, которое может быть неизменным или повторяющимся. Пациенты нередко отмечают улучшение разгибания во время целебной гимнастики, но спустя приблизительно час размер движений ворачивается к начальному уровню. Также может покажется непостоянный блок в коленном суставе, вызванный разрывом мениска.

Доминирующим симптомом у пациентов с наименьшим ограничением разгибания может стать боль в области бедренно-надколенникового сустава.
Основную диагностическую ценность имеют сбор анамнеза и клинический осмотр. Ограничение разгибания имеет пружинящую конечную точку.
Специальные клинические испытания для диагностики циклоп-синдрома отсутствуют. Тест Лахмана следует проводить во всех вариантах. Наличие циклоп-синдрома не значит послеоперационной стабильности.

Для оценки большеберцового канала можно выполнить рентгенографию в боковой проекции. Рекомендовано также исследование в боковой проекции под перегрузкой в положении Лахмана (30° сгибания) или в положении наибольшего разгибания, делаемое с целью документации. Переднее положение большеберцового канала просто определяется.
Чем наиболее кпереди сформирован большеберцовый канал (Вытянутое, искусственно ограниченное пространство, предназначенное для организации связи, передачи или перемещения чего-либо), тем выше возможность развития симптоматичного рубцевания трансплантата ПКС.
По отданным МРТ можно найти положение большеберцового канала (сформирован ли очень кпереди) и наличие рубцовой ткани (текстильное полотно, изготовленное на ткацком станке переплетением взаимно перпендикулярных систем нитей) кпереди от ПКС, традиционно имеющей образования с малой интенсивностью сигнала.
У пациентов с соответствующим анамнезом и послеоперационным ограничением разгибания диагноз считается установленным, потому выполнение МРТ нецелесообразно.
При ревизии межмыщелкового места определяются узелки рубцовой ткани различных размеров. При попеременном сгибании и разгибании видно, как рубцовая ткань собирается меж мыщелками бедренной и большеберцовой костей, создавая препятствие для полного разгибания.
Наружный вид рубцовой ткани разен. Часто можно найти большую однородную рубцовую массу, расположенную дистальнее трансплантата (в медицине пересадка какого-либо органа или ткани, например, почки, сердца, печени, лёгкого, костного мозга, стволовых гемопоэтических клеток, волос) ПКС. В неких вариантах рубцовая ткань пигментирована и состоит из множества образований наименьших размеров. Как правило, в рубцовой ткани отмечаются голубоватые или багровые участки кровоизлияний, возникающих вследствие неизменной микротравматизации. Для рубцовой ткани соответствующа волокнистая структура, что просит её дифференцировки от волокон трансплантата.
Размеры волокнистого узелка разны, их поперечник может варьировать от 5 мм до 2-4 см и даже наиболее.
К исцелению бедренно-надколенникового болевого синдрома, в особенности нередко встречающегося у юных женщин, следует подступать очень усмотрительно. Нужно учесть, что хрящ (один из видов соединительной ткани, отличается плотным, упругим межклеточным веществом, образующим вокруг клеток-хондроцитов и групп их особые оболочки, капсулы) бедренно-надколенникового сочленения не имеет нервных волокон и, что патогенез этого болевого синдрома до конца не узнан.
До недавнего времени (а в неких центрах и до сих пор) было принято отчасти резецировать размягченный хрящ, при этом разрушалась lamina splendence и инициировалось прогрессивное разрушение хряща. При сохранении жалоб рекомендовалось и выполнялись (также и в реальнее время) наиболее инвазивные вмешательства – пересадка бугристости большеберцовой кости, стягивающие операции, угловые остеотомии надколенника. В значимом числе вариантов эти операции быстрее усугубляют состояние пациента, чем уменьшают его жалобы.
Таковым образом, артроскопическое вмешательство при бедренно-надколенниковом болевом синдроме обязано быть отложено до тех пор, пока не будут исчерпаны все консервативные меры (упражнения на растяжение для напряженных мышечных групп: четырехглавая мускула, подвздошно-большеберцовый тракт, мышцы-сгибатели).
При гипермобильности связок используются упражнения, наведённые на постепенное повышение мышечной силы. Целебная физическая культура применяется и для исцеления многофункциональных нарушений осанки.
Пробный 4-6 недельный курс консервативного исцеления не является достаточным. Артроскопия показана минимум через 3 месяца консервативного исцеления.
При артроскопии можно исключить некие морфологические предпосылки болей, выявить томные повреждения хряща. В выраженных вариантах применяется соответственное действие на хрящ.
Циклоп – синдром после пластики передней крестообразной связки коленного сустава
Cyclope синдром – это одно из осложнений пластики передней крестообразной связки коленного сустава, является одной из форм артрофиброза. Чаще возникает при применении ВТВ трансплантата для пластики связки, реже при применении ST трансплантата.
Клинически характеризуется болью в переднем отделе сустава и ограничением разгибания в сроки более 4 месяцев после операции. Морфологически характеризуется рубцово- измененной соединительной тканью в переднем отделе сустава, которая ущемляется при разгибании и хронически травматизируется.
Решение проблемы — ревизионная артроскопия коленного сустава и резекция измененной ткани.
Попробуйте воспользоваться картой суставов, чтобы найти необходимый вам материал на Сустав Wiki
Причины возникновения и профилактика артрофиброза коленного сустава после артроскопической аутопластики передней крестообразной связки.

Рис. 1. Разрастания фиброзных масс вокруг дистальной части трансплантата.

Рис. 2. Ущемление фиброзных масс при разгибании коленного сустава.

Рис.3. Тотальное разрастание фиброзных масс вокруг трансплантата.
Всем больным была выполнена АС резекция фиброзных масс с мобилизацией ТР. Во всех случаях отмечено прорастание рубцовых формаций в сухожильную часть ТР. Нередко, после мобилизации, последний выглядел жизнеспособным и функциональным.

Рис. 4. Внешний вид трансплантата после его мобилизации.
В то же время, морфологическое исследование показало низкую структурную сохранность ТР во всех наших наблюдениях. В 7 случаях отмечены дистрофические изменения ТР, различной степени выраженности, проявляющиеся в нарушении архитектоники коллагеновых волокон; замены сухожильных клеток неспецифическими фибробластами с непосредственным переходом в рубцовую ткань; гиалинозе сухожилия с дистрофией клеточных элементов; увеличении количества сосудов со склерозом стенок и признаками пролиферативного васкулита; метаплазии сухожильной ткани в волокнистый хрящ и др. Еще в 1 наблюдении, через 10 месяцев после операции выявлен тотальный некроз трансплантата.
Клиника располагает опытом артроскопического (АС) восстановления передней крестообразной связки (ПКС) коленного сустава (КС) трансплантатом (ТР) из связки надколенника (СН) у 487 больных, со свежими и застарелыми повреждениями ПКС. Такой пластический материал является наиболее популярным среди подавляющего большинства ортопедов. Однако, с его применением связан ряд серьёзных послеоперационных проблем. И одной их них является артрофиброз (АФ), существенно влияющий не только на функцию КС, но и на процессы ремоделирования ТР [2,4,6,8]. С таким осложнением в различных формах его проявления мы встретились у 20 больных. В данной статье мы хотим изложить наши взгляды на проблему диагностики, лечения и профилактики артрофиброза, возникающего после АС стабилизации КС. Наш материал основан на данных клинического обследования 429 пациентов, результатов 94 магнитно - резонансных томографий (МРТ) и 49 ревизионных артроскопических операций.
У всех наших пациентов, макроскопически атрофиброз проявлялся разрастанием в полости КС рубцово - измененной соединительной ткани, различной степени выраженности. Одним из основных клинических проявлений АФ было выраженное снижение амплитуды движений в КС, сопровождающееся болевым синдромом различной степени выраженности. Основываясь на данных клинико - макроскопических проявлений, мы выделяем 4 типа АФ.
Тип 1 - ограниченный артрофиброз. С такой формой мы встретились у 6 больных. Во всех случаях он был представлен единичными спаечными тяжами различной толщины и степени плотности, с наиболее частой локализацией в области верхнего заворота. Хотим отметить, что это единственный тип АФ, который, не имел какой - либо специфической клинической симптоматики. Единственной, и довольно редкой жалобой больных был незначительный дискомфорт в передне - верхних отделах КС, не влияющий отрицательно на функцию КС в целом. У всех пациентов, наличие единичных спаек оказалось АС находкой.
Тип 2 - множественный артрофиброз. Был представлен множественными спайками в области верхнего заворота, пателло-феморального сустава (ПФС) и передних отделов КС. Такая форма АФ осложнила течение реабилитационного периода у 2 больных, и клинически проявлялась в умеренном ограничении движений и передними болями в КС различной интенсивности, снижении мобильности надколенника (Н), рецидивирующем синовите, ощущениями "дискомфорта" в области ПФС.
Тип 3 - тотальный артрофиброз. Проявлялся выраженным разрастанием патологических рубцовых формаций в области верхнего заворота, ПФС и передних отделов КС. С такой формой АФ мы встретились в 2-х наблюдениях, через 2,5 и 3 месяца после операции. Клинически тотальный АФ проявлялся в стойком ограничении как сгибания, так и разгибания в КС, уменьшении или отсутствии мобильности Н, интенсивной болью, гипотрофией четырехглавой мышцы бедра (ЧГМБ), рубцовыми изменениями в задних отделах фиброзной капсулы.
Тип 4 - локальный артрофиброз. Проявлялся разрастанием вокруг ТР рубцово-измененной соединительной ткани. С такой формой АФ, получившей в зарубежной литературе название "cyclop" синдром мы встретились у 8 больных. [3]. У всех пациентов это осложнение диагностировано при АС ревизии КС в сроки от 5 до 14 месяцев после операции. В 3-х наблюдениях диагноз "cyclop" синдром был установлен до операции, на основании данных МРТ. Локальный АФ - наиболее грозное позднее послеоперационное осложнение, от которого в целом зависит судьба ТР. Сегодня, это наименее изученная форма АФ, и мы хотим более подробно остановиться на ней.
Основными клиническими проявлениями "cyclop" синдрома у наших пациентов были: дефицит разгибания 10-15°; передние боли в КС; ощущения механического препятствия, инородного тела и дискомфорта в передних отделах КС при его разгибании.
АС находки свидетельствовали о разрастании рубцово-измененной соединительной ткани вокруг ТР, интимно спаянной с последним, округлой формы, плотной консистенции, укрытой синовиальной оболочкой, нередко с хорошо выраженным сосудистым рисунком. При разгибании КС эти рубцовые массы ущемлялись между "плато" большеберцовой кости и крышей межмыщелковой ямки бедра. Важно отметить, что чем больше времени прошло с момента первичной операции, тем более выраженными были клинико - макроскопические проявления "cyclop" синдрома.
Мы выделили 3 формы АС проявления "cyclop" синдрома. Так, у 5 больных обнаружено разрастание фиброзных масс вокруг дистальной части ТР. В 2-х наблюдениях отмечено тотальное разрастание фиброзных масс вокруг всей сухожильной части ТР. Еще в 1 случае фиброзная ткань была представлена несколькими фрагментироваными рубцовыми формациями, так же округлой формы и схожей консистенции.
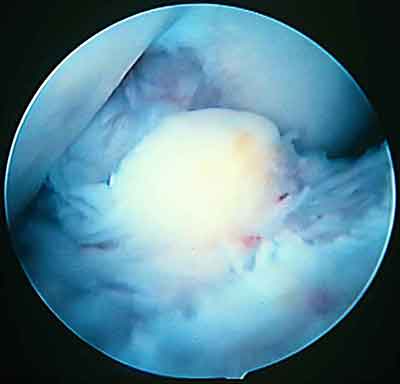
Рис. 1. Разрастания фиброзных масс вокруг дистальной части трансплантата.
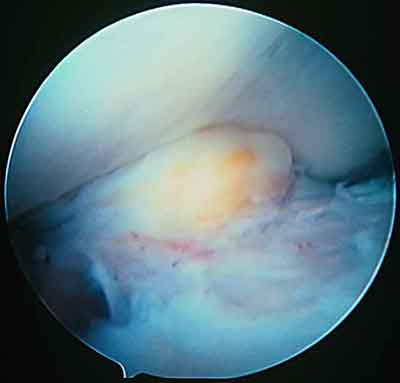
Рис. 2. Ущемление фиброзных масс при разгибании коленного сустава.
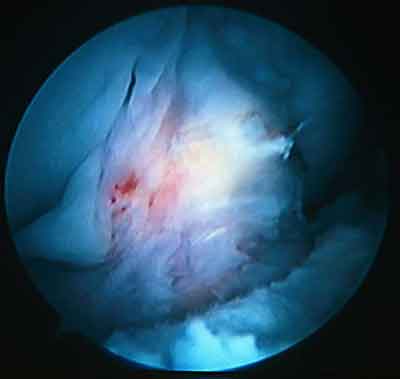
Рис.3. Тотальное разрастание фиброзных масс вокруг трансплантата.
Всем больным была выполнена АС резекция фиброзных масс с мобилизацией ТР. Во всех случаях отмечено прорастание рубцовых формаций в сухожильную часть ТР. Нередко, после мобилизации, последний выглядел жизнеспособным и функциональным.
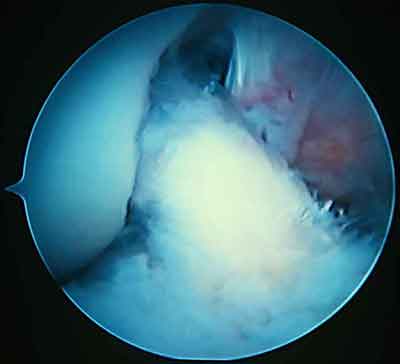
Рис. 4. Внешний вид трансплантата после его мобилизации.
В то же время, морфологическое исследование показало низкую структурную сохранность ТР во всех наших наблюдениях. В 7 случаях отмечены дистрофические изменения ТР, различной степени выраженности, проявляющиеся в нарушении архитектоники коллагеновых волокон; замены сухожильных клеток неспецифическими фибробластами с непосредственным переходом в рубцовую ткань; гиалинозе сухожилия с дистрофией клеточных элементов; увеличении количества сосудов со склерозом стенок и признаками пролиферативного васкулита; метаплазии сухожильной ткани в волокнистый хрящ и др. Еще в 1 наблюдении, через 10 месяцев после операции выявлен тотальный некроз трансплантата.
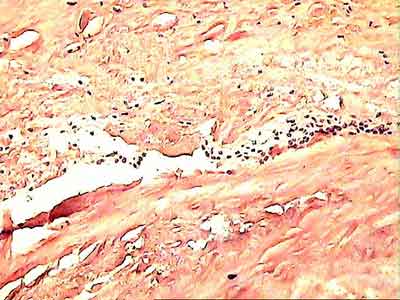
Рис. 5. Гистологическая картина некроза трансплантата. Окраска пикрофуксином по Ван-Гизону, увеличение Х 200
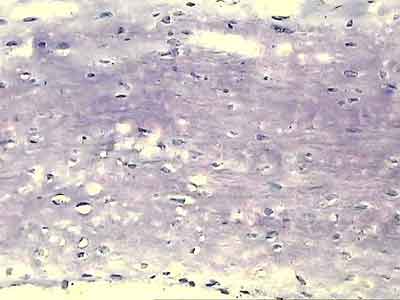
Рис. 6. Метаплазия хрящевой ткани в трансплантате. Окраска толуидиновым синим, увеличение Х 200
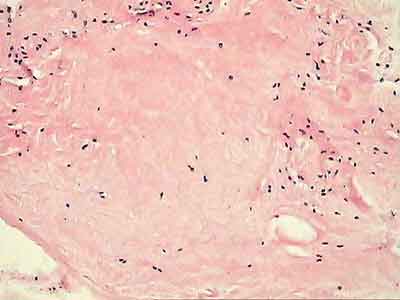
Рис. 7. Дезорганизация структуры трансплантата, выраженная дистрофия клеток, крупный бесклеточный участок некроза.Окраска гематоксилином и эозином, увеличение Х 200.
Тщательный анализ нашего клинического материала и данных зарубежной литературы позволил нам выделить ряд закономерных причин развития артрофиброза. Так, у 3-х больных реконструкция ПКС была выполнена в течение первых 3-х недель после травмы, на фоне сохраняющегося болевого синдрома и рефлекторного ограничения движений в КС, явлений гемартроза, выраженной отечности мягких тканей и др. Такая ошибочная тактика привела не только к увеличению степени уже имеющихся посттравматических воспалительных явлений в капсуле сустава и околосуставных тканях, но и к еще большему послеоперационному уменьшению амплитуды движений, при уже имеющихся изменениях кинематики КС. Поэтому считаем, что восстановление ПКС должно выполняться лишь после купирования острых посттравматических явлений и полного восстановления амплитуды движений в КС, что достигается к сроку 4-6 недель после травмы. В тоже время, операция в остром периоде может быть направлена на восстановление боковых стабилизаторов, коррекцию сопутствующих повреждений менисков, хряща, капсулы сустава, внутрисуставных переломов и др.
Мы не можем согласиться с мнением, что восстановление в остром периоде боковых стабилизаторов КС так же часто приводит к развитию артрофиброза. Наш опыт восстановления свежих повреждений боковых стабилизаторов показал, что использование функциональных ортезов и начало ранних движений в КС значительно снижают риск возникновение такого осложнения. В то же время, кальцификация или гетеротопическая оссификация в зоне повреждения большеберцовой коллатеральной связки могут привести к выраженному болевому синдрому и при консервативной тактике лечения, ограничивающему движения в КС, что в свою очередь и может привести к развитию артрофиброза. С нашей точки зрения, далеко не все повреждения боковых стабилизаторов требуют ранней хирургической коррекции.
К факторам риска мы так же отнесли необоснованную иммобилизацию КС с лимитированием как пассивных, так и активных движений, неадекватную раннюю послеоперационную реабилитацию, позднее начало движений в КС и др. Считаем целесообразным использование в послеоперационном периоде функциональных ортезов и раннее начало движений в КС. Особое внимание следует уделять профилактике дефицита разгибания, являющимся с нашей точки зрения одним из основных факторов риска развития локального АФ. Важно помнить, что длительно сохраняющееся ограничение разгибания может привести к рубцово - дегенеративным изменениям в задних отделах фиброзной капсулы сустава, и потребовать хирургической коррекции.
Так, у всех наших 8 пациентов с "cyclop" синдромом имелся дефицит разгибания КС в 10-15°. В 2-х наблюдениях нами были допущены тактические ошибки: мы искусственно лимитировали после операции разгибание, необоснованно опасаясь миграции заклиненного проксимального костного блока ТР. С целью профилактики ограничения разгибания особое внимание следует уделять выполнению так называемых, пассивных экстензионных упражнений. Для этого под пятку оперированной конечности следует подложить жесткий валик так, чтобы оперированная конечность располагалась над поверхностью кровати на 15-20см. При этом она должна провисать под действием силы тяжести и достаточной релаксации мышц конечности. Такие упражнения рекомендуем выполнять 3-4 раза в день по 15-20 минут.
К причинам развития локального АФ мы так же отнесли хроническую травматизацию ТР о край латерального мыщелка (ЛМБ) или крыши межмыщелковой ямки бедра (МЯБ) при разгибании КС. Как правило, такое осложнение обусловлено формированием большеберцового туннеля значительно кпереди от центра его изометрического расположения, и отказом от выполнения резекции ЛМБ при наличии его контакта с ТР. Важно помнить и возможности травматизации волокон ТР о краевые остеофиты ЛМБ. Вероятность развития такого осложнения достаточно высока у лиц с уже имеющимся остеоартрозом КС. Этот факт является одной из причин, по которой мы отказались от аутопластической стабилизации КС у пациентов с выраженными изменениями хрящевого покрова. Крайне важно во время операции оценить ширину МЯБ. В тех случаях, когда она узкая, или определяется её сужение из-за разрастания краевых остеофитов, необходимо выполнять резекцию ЛМБ или крыши МЯБ с расширением межмыщелкового пространства.
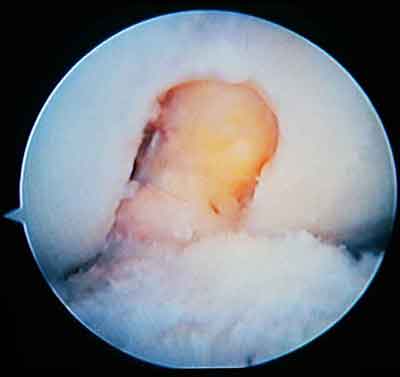
Рис. 8. Артроскопическая картина сужения межмыщелкового пространства.
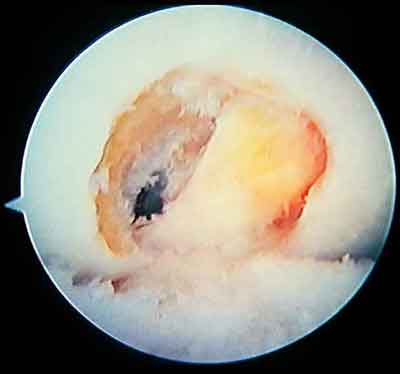
Рис. 9. Межмыщелковое пространство после резекции латерального мыщелка бедра.
К факторам риска развития "cyclop" синдрома, мы также отнесли несоответствие диаметров сухожильной части ТР и большеберцового туннеля, в результате чего происходят смещения ТР в переднее - заднем направлениях при сгибании - разгибании КС, приводящие к хронической травматизации волокон ТР о края стенок туннеля, и последующему разрастанию артрофибротических масс вокруг дистальной части ТР. Этот феномен получил название "эффект стеклоочистителя". Важно отметить, что он так же может явиться причиной изменения формы проксимальной части большеберцового туннеля.
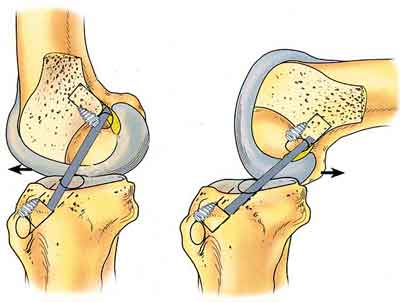
Рис. 10 Схема "эффекта стеклоочистителя
Следует помнить и о возможности травматизации ТР о внутрисуставные края большеберцового туннеля, когда после его формирования не удаляются остатки хряща и мелких костных фрагментов. С целью профилактики рекомендуем выполнять тщательную обработку туннеля.
Отдельно хотим остановиться на таком послеоперационном осложнении, как "синдром инфрапателлярной контрактуры" (infrapatellar contracture syndrome) КС, являющимся разновидностью артрофиброза [5]. Он проявляется в разрастании в области ПФС и передних отделов КС патологически измененной соединительной ткани. С таким осложнением мы встретились у 2-х пациентов. Тщательный анализ этих случаев, а так же данных зарубежной литературы позволили нам выделить 3 стадии течения этого осложнения.
Продромальная стадия проявляется в течение первых 2-8 недель после операции. К макроскопическим признакам этой стадии относятся отёк синовиальной оболочки, жировой подушки и "ретинакулярных" тканей. Клинически эта стадия проявляется в ограничении разгибания; передними болями; отечностью и болезненностью при пальпации мягких тканей вокруг, и самой СН; снижением мобильности Н и гипотрофией ЧГМБ.
Активная стадия - проявляется через 6-20 недель после операции. Она характеризуется интенсивными передними болями; степень отечности и инфильтрации мягких тканей передних отделов КС значительно увеличивается; появляются выраженная отечность, утолщение, инфильтрация и резкая болезненность при пальпации дистального места прикрепления СН; сама связка так же утолщена и отечна, но в меньшей степени; её пальпация сопровождается выраженными болевыми ощущениями и нередко крепитацией; отмечается ещё большее снижение мобильности Н и амплитуды движений в КС.
Хроническая стадия - наблюдается через 8-9 месяцев после операции. Основными клиническими проявлениями этой стадии могут быть: отсутствие мобильности Н; интенсивные передние боли в КС; пателло-феморальный артроз; гипотрофия и функциональная слабость ЧГМБ; амплитуда движений в КС характеризуется 40-50? сгибания, и дефицитом разгибания в 10-20? и др. Отечность и воспаление парапателлярных тканей сохраняется, но в значительно меньшей степени, чем при активной стадии. Рентгенологически может определяться стойкое патологическое смещение Н вниз (patella baja).
Неоценимую помощь в диагностике этого осложнения в обоих наших случаях оказала МРТ, позволившая верифицировать наличие, локализацию и степень выраженности артрофиброза.
Артроскопически этот синдром проявлялся наличием плотных рубцовых тканей в передних отделах КС, начинающихся от гипотрофированного жирового тела, и распространяющихся на ПКС и МЯБ.
В заключение хотим отметить, что наша клиника так же располагаем опытом АС восстановления ПКС аутосухожилиями полусухожильной и нежной мышц, прямой головки ЧГМБ. Уделяя особое внимание предоперационному планированию, мы стали более осторожно относиться к выбору пластического материала, учитывая как отрицательные, так и положительные стороны его применения. В последнее время все большее предпочтение отдаем свободному трансплантату из сухожилия m.rectus femoris с костным блоком от верхнего полюса Н, имеющему ряд неоспоримых преимуществ перед СН.
Мы надеемся, что данная статья позволит многим хирургам избежать вышеописанных ошибок и предотвратить развитие артрофиброза после артроскопической аутопластики ПКС.
Список литературы:
1. Dandy D.J., Edwards D. Problems in regaining full extension of the knee after anterior cruciate ligament reconstruction: does arthrofibrosis exist? // Knee Surg Sports Traumatol Arthrosc.- 1994.- vol.2.- № 2.- p. 76-79.
2. Delcogliano A., Franzese S., Branca A. et al Light and scan electron microscopic analysis of Cyclops syndrome: etiopathogenic hypothesis and technical solutions // Knee Surg Sports Traumatol Arthrosc.- 1996.- vol.4.- №4.- p.194-199.
3. Jackson D.W., Schaefer R.K. Cyclops syndrome: loss of extension following intra-articular anterior cruciate ligament reconstruction. // Arthroscopy.- 1990.- vol.6.-№3.- p.171-178.
4. Muellner T., Kdolsky R., Grosschmidt K. et al. Cyclops and cyclopoid formation after anterior cruciate ligament reconstruction: clinical and histomorphological differences // Knee Surg. Sports Traumatol. Arthrosc.- 1999.- vol.7.- №5.- p.284-289.
5. Paulos L.E., Rosenberg T.D., Drawbett J. et al. Infrapatellar contracture syndrome: an unrecognized cаuse of knee stifness with patella entrapment and patella infera // Am J Sports Med.- 1987.- vol.15.- p.331-341.
6. Shelbourne K.D., Wilckens J.H., Mollabashy J.L. Arthrofibrosis in acute anterior cruciate ligament reconstruction. The effect of timing of reconstruction and rehabilitation // Am J Sports Med.- 1991.- vol. 19.- №4.- p.332-339.
7. Shelbourne K.D., Patel D.V. Treatment of limited motion after anterior cruciate ligament reconstruction // Knee Surg. Sports Traumatol., Arthrosc.- 1999.- vol.7.- № 2.- p.85-92.
8. Strobel M.J. Limited motion and scarring, in: Manual of Arthroscopic surgery // Springer-Verlag- Berlin Heidelberg, 2002, p.345-366.
Список рисунков к статье Лазишвили Г.Д. с соавторами:
"Анализ причин возникновения и профилактика артрофиброза после артроскопической стабилизации коленного сустава."
Рис.1. Разрастания фиброзных масс вокруг дистальной части трансплантата.
Рис.2. Ущемление фиброзных масс при разгибании коленного сустава.
Рис.3. Тотальное разрастание фиброзных масс вокруг трансплантата.
Рис.4. Внешний вид трансплантата после его мобилизации.
Рис.5. Гистологическая картина некроза трансплантата. Окраска пикрофуксином по Ван-Гизону, увеличение Х 200.
Рис.6. Метаплазия хрящевой ткани в трансплантате. Окраска толуидиновым синим, увеличение Х 200.
Рис.7. Дезорганизация структуры трансплантата, выраженная дистрофия клеток, крупный бесклеточный участок некроза. Окраска гематоксилином и эозином, увеличение Х 200.
Рис. 8. Артроскопическая картина сужения межмыщелкового пространства.
Рис. 9. Межмыщелковое пространство после резекции латерального мыщелка бедра.
Рис. 10. Схема "эффекта стеклоочистителя".
Читайте также:


