Скрининг костей при раке простаты
Остеосцинтиграфия в онкологии (радионуклидная диагностика) — один из самых востребованных методов радиоизотопного исследования применительно к онкологическим больным. Сканирование скелета при онкологических заболеваниях производится на современном диагностическом оборудовании, которое представлено в виде гамма-камеры и дополнительных диагностических устройств.
Метод позволят получить очень четкое изображение костной системы и выявить те патологические изменения, которые произошли в результате болезни. К таким изменениям относятся первичные опухоли костной ткани, либо метастазы злокачественных опухолей в других локализациях (опухоли молочной железы, предстательной железы, легких, щитовидной железы).
Процедура остеосцинтиграфии заключается во введении специального вещества (радиофармпрепаратов), которое накапливается в определенных органах и тканях, имитируя процессы, происходящие в организме. Например, образование и выведение желчи или мочи. В состав этих препаратов входит радиоактивная метка, излучения которой регистрируются детекторами гамма-камеры. Далее компьютер формирует плоское или объемное изображение. Обработав это изображение, получают графики, индексы и показатели, отражающие работу органов.
Посмотрите информационное видео про кабинет радиодиагностики в Онкологическом Диспансере в г. Москва:
- Основные задачи исследования
- Преимущества диагностики
- Как проходит остеосцинтиграфия?
- Безопасность
- Показания для назначения исследования
Основные задачи исследования
Все, что нужно знать о процедуре остеосцинтиграфии, представляем на картинке:
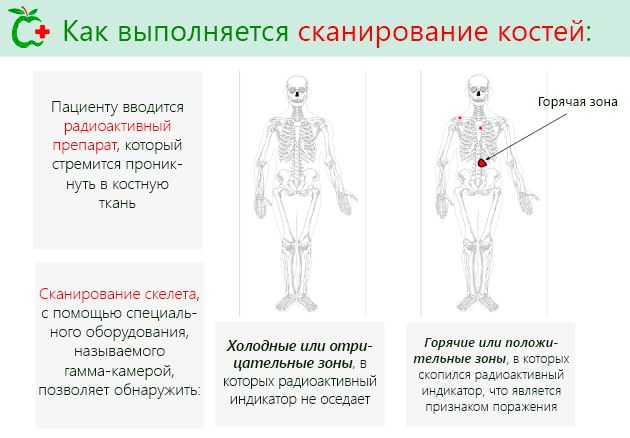
Остеосцинтиграфия — классический метод радионуклидной диагностики с возможностью визуализации всего тела за одно высокочувствительное исследование.
Порядка 30-40% больных, умерших от рака легких и предстательной железы, имели множественные метастазы в костях. Главная задача специалистов сводится к своевременному выявлению таких метастазов при проведении остеосцинтиграфии перед подготовкой к хирургическому вмешательству и лучевой терапии.
Если у больных уже имеется болевой синдром, следует ускорить этап проведения радионуклидной диагностики в целях проверки онкологии костей.
Основные задачи исследования:
- диагностика (скрининг) костей на наличие онкологии;
- диагностика доброкачественных изменений;
- определение функционального состояния органов и систем;
- определение степени распространенности опухолевого процесса.
Выполнение поставленных задач помогает специалистам определиться с тактикой лечения, объемами хирургического вмешательства и последующей лучевой терапией. Кроме того, за одно исследование представляется возможным ответить на все вопросы обследуемых пациентов.
Своевременная диагностика способна определить пути лимфооттока от опухоли к здоровым тканям, которые могут быть вовремя прооперированы.
Преимущества диагностики
Главное отличительное свойство данного метода — это функциональность. Применительно к онкологии, сцинтиграфия дает возможность определить патологические процессы в клетках опухоли, когда анатомические и морфологические изменения еще не видны и не могут быть обнаружены с помощью общепринятых методов лучевой диагностики (рентген скелета при онкологии, КТ).
Исследование достаточно безопасно для пациентов. За одну процедуру можно оценить не только состояние костей, органов грудной и брюшной полостей, но и патологические изменения лимфатических узлов и молочных желез. Тем самым возможно не упустить время пациента и предоставить ему возможность как можно раньше начать противоопухолевое лечение.
Современное и успешное лечение рака молочной железы немыслимо без метода радионуклидной диагностики.
Сканирование молочной железы дает возможность диагностировать опухоли размерами менее 1 см. Главные преимущества этого метода — это выявление масштабов распространенности опухолевого процесса и оценка эффективности противоопухолевого лечения.
Современные методы лучевой диагностики позволяют оценить не только форму, размеры и строение внутренних органов, но и их функциональное состояние. Определение функций и есть главная заслуга остеосцинтиграфии.
Изображения костной системы, получаемые в результате остеосцинтиграфии, очень четкие и наглядные. Ни один другой метод не может так обширно показать изменения в скелете, как метод остеосцинтиграфии.
Выявить костные метастазы при сканировании костей возможно на ранних сроках возникновения злокачественных изменений. Исследование позволяет зафиксировать патологию на несколько месяцев раньше по сравнению с рентгеном костей скелета при раке. Компьютерно-томографическое исследование так же уступает остеосцинтиграфии по своим функциональным возможностям. Радионуклидная диагностика охватывает весь скелет, не выделяя отдельные области, в то время как при компьютерной томографии, как правило, исследуется лишь одна область.
При этом, если с помощью КТ обследовать весь скелет в целом, лучевая нагрузка будет в 10 раз больше, чем при остеосцинтиграфии.
Ядерная медицина объединяет все диагностические и терапевтические вмешательства, связанные с введением в организм радионуклидов. Позволяет на молекулярном уровне оценивать физиологические изменения, происходящие в организме.
В ряде случаев, болевого симптома может не быть даже при обширном метастазировании костной системы, а стандартные снимки рентгенографии показывают патологические изменения только на поздней стадии заболевания. Поэтому, при быстрорастущих опухолях и смешанных поражениях радионуклидному исследованию нет равных.
Сцинтиграфия костей имеет очень большое значение при выборе препаратов и оценке их эффективности на каждом этапе лечения онкологического заболевания. Данный метод применяется как в онкологии, так и в ортопедии.
Радионуклидная диагностика характеризуется объективностью и имеет очень большое прогностическое значение. Процедура отличается невысокой стоимостью и возможностью динамического наблюдения.
Как проходит остеосцинтиграфия?
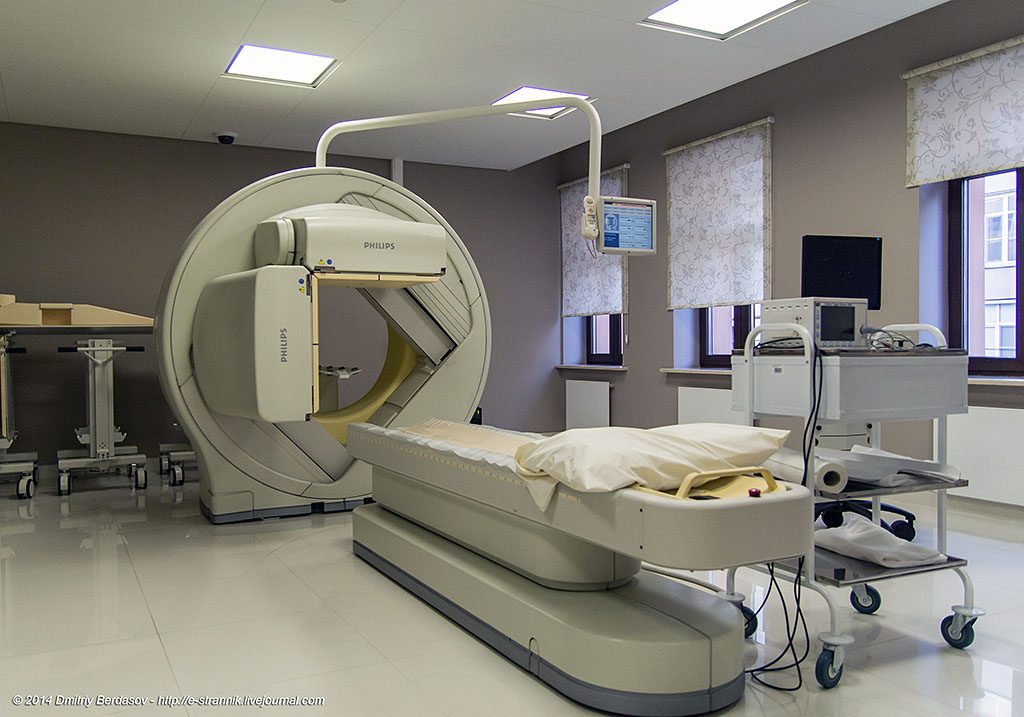
Перед началом исследования пациенту внутривенно вводится биологически активное вещество, на которое сажается метка. Наличие радиоактивной метки дает возможность проанализировать введенный состав с помощью специальных систем отслеживания. Данный метод диагностики позволяет визуализировать во времени и пространстве те или иные важные для специалистов физиологические процессы. В онкологии чаще всего используются препараты глюкоза и технетрил. Оба препарата отражают метаболическую активность опухоли, что дает очень много дополнительной информации.
После введения контрастного вещества, на мониторе отражается пространственно-временное распределение радиофармпрепаратов в клетках, тканях и органах обследуемого человека.
Основными инструментами для сцинтиграфического исследования являются:
- гамма-камера, состоящая из блоков отслеживания, предназначенных для улавливания гамма-излучений;
- место для пациента (ложе);
- био-синхронизатор;
- экран;
- компьютер для принятия данных исследования;
- компьютер, обрабатывающий изображение.
Для проведения остеосцинтиграфии в большинстве случаев не требуется специальной подготовки. Обследование не обременительно для детей и физически слабых граждан. Пациенту не нужно раздеваться и испытывать чувства голода. Требуется лишь снять одежду с металлическими элементами. Некоторые пациенты отзываются об этом исследовании как о достаточно приятной процедуре, поскольку обследуемый пребывает в покое около 20 минут.
Остеосцинтиграфия не вредна и не вызывает каких-либо болевых ощущений.
Безопасность
При сцинтиграфии в качестве радиоактивной метки используется технетрил (короткоживущий радионуклид с периодом полураспада 6 часов и низкой энергией радиоактивного излучения). Препарат практически полностью выводится из организма в течение суток. Исследование планируется таким образом, чтобы минимизировать лучевую нагрузку. Так, при одном исследовании она не превышает 1-го миллизиверта.
Вопрос о безопасном проведении сканирования беременных женщин является открытым, так как ответ на него неоднозначен. По некоторым данным, беременность не является абсолютным противопоказанием к проведению исследования. Однако, ряд специалистов не готовы взять на себя ответственность по утверждению факта безопасности данной процедуры.
Вопрос назначения сцинтиграфии беременным женщинам рассматривается сугубо индивидуально, исходя из клинического состояния пациентки.
Ни ранний возраст, ни общее тяжелое физическое состояние не являются абсолютными противопоказаниями к проведению сцинтиграфии. Внутривенное введение радиофармпрепаратов не превышает по объему 1 мл, не вызывает аллергических реакций и является химически безопасным для пациента. Для детей и беременных женщин возможно проведение сцинтиграфии без применения определенных видов медикаментов.
Показания для назначения исследования
Основные показания для проведения остеосцинтиграфии описаны на картинке:
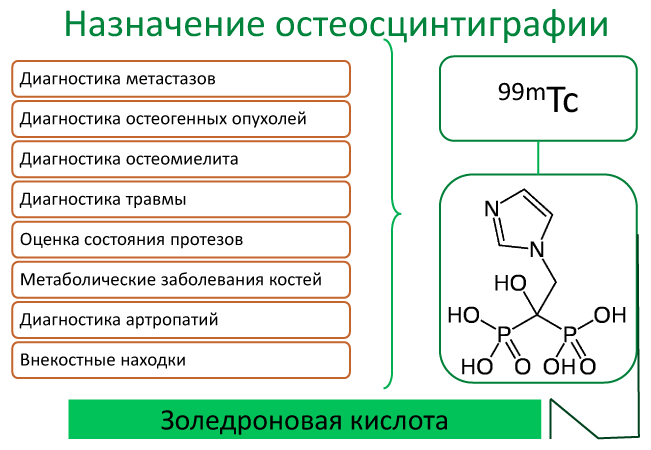
Сцинтиграфия является незаменимым исследованием, когда стоит вопрос об определении жизнеспособности органов. Например, показатель функционального резерва почки невозможно получить ни одним из существующих методов. При этом, в ряде случаев метод настолько чувствителен, что позволяет диагностировать изменения на ранних клинических стадиях.
Очень информативны радионуклидные исследования при врожденных патологиях позвоночника, хронических воспалительных заболеваниях почек, печени, при определении кровоснабжения легких и сердца. В исследовании костной системы остеосцинтиграфия применяется для поиска костных метастазов и очагов остеомиелита. Для пациентов с эндокринной патологией проводится сканирование простаты, щитовидной и паращитовидной желез.
Сцинтиграфия дает важную клиническую информацию для планирования методов лечения при любых новообразованиях.
Как проходит процедура сцинтиграфии и в чем ее важность, рассказывается в следующем видеорепортаже:

В чем заключается скрининг рака предстательной железы?
Скрининг рака предстательной железы заключается в регулярном измерении уровня простат-специфического антигена (ПСА) в крови у мужчин от 50 до 65-70 лет.
При повышении уровня ПСА выше определенного порогового значения (традиционно это 4 нг/мл) производится т.н. систематическая биопсия предстательной железы под контролем трансректального ультразвукового исследования. При биопсии забираются кусочки ткани простаты, которые исследуются под микроскопом на предмет выявления признаков рака простаты.
У каких мужчин скрининг рака предстательной железы не проводится?
Скрининг рака предстательной железы не проводится у молодых мужчин (до 40 лет), поскольку это заболевания в таком возрасте практически не встречается. В возрасте от 40 до 50 лет рак предстательной железы выявляется также редко, кроме случаев с наследственной предрасположенностью.
Поэтому в данном возрастном промежутке скрининг показан только при наличии рака простаты у близкого родственника пациента. У пожилых мужчин и мужчин с тяжелыми неизлечимыми заболеваниями, у которых вероятность прожить 10 лет и более невелика, скрининг может приносить больше вреда, чем пользы, поскольку выявление и лечение начальных форм рака предстательной железы никак не скажется на продолжительности жизни, но может ухудшить ее качество.
При помощи каких методов можно выявить рак предстательной железы?
Традиционно рак предстательной железы диагностировался при помощи пальпации простаты через прямую кишку. К сожалению, этот простой метод может выявить опухоль только в том случае, когда она достаточно большая и часто уже не подлежит радикальному лечению.
Поэтому, чтобы выявить опухоль на раннем этапе, когда она еще не пальпируется, требуется выполнить так называемую биопсию, которая заключается в заборе кусочков ткани простаты специальной иглой из определенных зон железы.
Чтобы не пропустить опухоль требуется выполнить от 6 до 10 (иногда и более) биопсий. Такая биопсия называется систематической и выполняется под контролем трансректального ультразвукового исследования. Обычно биопсия выполняется не всем мужчинам, а только тем, у которых имеется повышение уровня ПСА в крови.
Что такое Простат-специфический антиген (ПСА)
ПСА (простат-специфический антиген) – это опухолевый маркер рака предстательной железы. ПСА представляет собой белок, который вырабатывается исключительно в предстательной железе и в минимальных концентрациях попадает в кровь. При раке предстательной железы обычно в кровь попадает большее количество ПСА, что используется для раннего выявления этого заболевания.
Тем не менее, у такой методики имеется существенный недостаток, который заключается в том, что повышение уровня ПСА часто бывает при других, доброкачественных заболеваниях простаты (например, воспаление простаты или доброкачественная гиперплазия предстательной железы).
При помощи каких методов можно "увидеть" рак предстательной железы?
Использование магнитно-резонансной томографии (МРТ)
Перспективным является использование магнитно-резонансной томографии (МРТ) в определенных режимах, однако это пока является предметом научных исследований.
Есть ли недостатки скрининга рака предстательной железы?
Да, как и у любого скрининга, они имеются. Так, в ходе скрининга можно выявить так называемый "незначимый" рак, который в отсутствие скрининга никогда бы не был выявлен (а значит и пролечен). А "ненужное" лечение в таких случаях может приводить к осложнениям и стойким последствиям.
Кроме того из-за неспецифичности ПСА рак выявляется только у 20-30 % из числа мужчин с повышенным уровнем этого маркера, а значит оказывается, что биопсия не нужна большинству пациентов, которым она проводится.
Нужен ли скрининг рака предстательной железы?
В настоящее время западные ученые ведут дискуссии о необходимости скрининга рака предстательной железы, поскольку у ученых нет твердой уверенности, что польза от скрининга превышает его потенциальные недостатки. Что касается нашей страны, то в настоящее время ведется изучение вопроса о необходимости внедрения скрининга.
Тем не менее, внедрение в Беларуси элементов скрининга в форме так называемого "раннего выявления" принесло бы несомненную пользу, учитывая частое выявление этого заболевания в далеко зашедшей стадии.
Что надо знать о скрининге рака предстательной железы?
Если у Вас в семье были случаи рака предстательной железы у кровных родственников или Вы ответственно относитесь к своему здоровью и хотели бы принять участие в программе раннего выявления рака простаты, несмотря на возможные неудобства, обратитесь к своему урологу для выполнения исследования уровня ПСА в крови.
Помните, что только профессионально выполненная биопсия предстательной железы (а иногда несколько биопсий) может исключить наличие рака предстательной железы при повышенном уровне ПСА.
Ультразвуковое исследование с эластографией сдвиговой волны и мультипараметрическая магнитно-резонансная томография при заболеваниях предстательной железы
В современной онкоурологии актуальность проблемы заболевания раком предстательной железы обусловлена широкой распространенностью данной патологии и лидирующим местом в структуре онкологической заболеваемости мужчин большинства стран мира. По данным Белорусского канцер-регистра в структуре заболеваемости злокачественными новообразованиями мужчин предстательная железа занимает первое место.
Существующие стандартные методы диагностики злокачественных опухолей предстательной железы обладают высокой точностью при выявлении заболевания. В РНПЦ ОМР им.Н.Н.Александрова используются и новые методы исследования, позволяющие улучшить стандартный подход на основе применения трансректального ультразвукового исследования с эластографией сдвиговой волны, которая открыла новые возможности количественной оценки жесткости ткани и позволяет определить локализацию подозрительных очагов.
Для подтверждения или исключения наличия злокачественной опухоли предстательной железы выполняется биопсия под контролем трансректального ультразвукового исследования. Она состоит из целевого этапа получения материала из подозрительных очагов, которые выявлены при помощи мультипараметрической МРТ таза и трансректального УЗИ с эластографией сдвиговой волны (т.к. точность определения диагноза возрастает, когда биопсия ориентирована на более жесткие области) и рекомендуется в сочетании с систематическим многоточечным этапом по определенной схеме.
Эластография показывает преимущества при выявлении в области верхушки и средней части простаты, тогда как МРТ – в визуализации базальной и переходной зон.
На рисунке представлен клинический пример пациента с повышенным уровнем ПСА. Ему выполнены мультипараметическая МРТ и трансректальное УЗИ с эластографией сдвиговой волны по данным которых определялись подозрительные очаги (указано стрелками или красным цветом). В последующем выполнена биопсии предстательной железы, которая состояла из систематического и целевого этапов. По результатам биопсии установлен диагноз рак предстательной железы с суммой баллов Глисона 4+3 (ISUP Grade 3). Пациенту выполнена радикальная простатэктомия в результатах которой подтвердилась правильно установленная стадия и лечение проведено успешно.
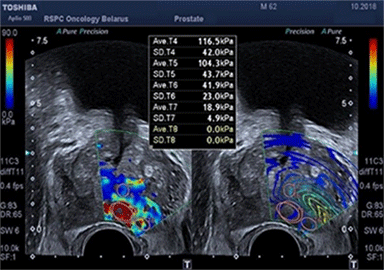
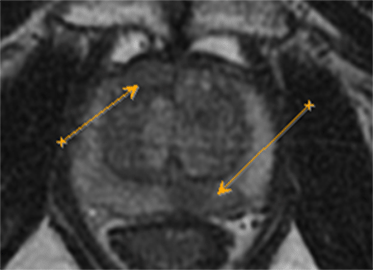
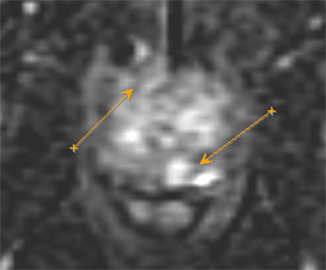
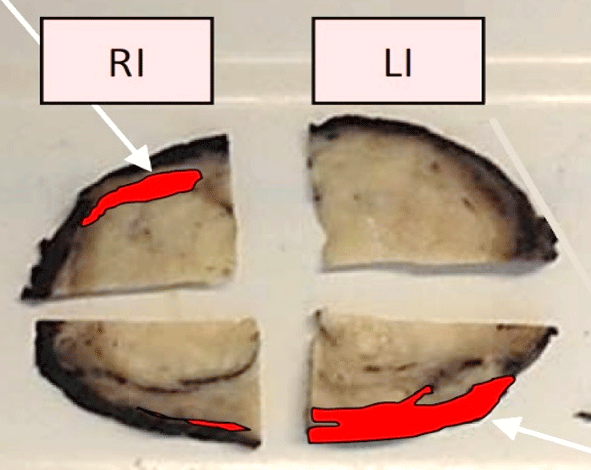
Установившийся тренд на изменение подходов к методике выполнения биопсии предстательной железы с включением целевого этапа при проведении систематической биопсии является результатом определенных успехов развития методов лучевой диагностики, в частности совместного использования при планировании биопсии результатов мультипараметрической МРТ и трансректального УЗИ с эластографией сдвиговой волны.

Одной из главных задач современной урологии является ранняя диагностика рака предстательной железы (РПЖ) и поиск более эффективных методов его лечения. Онкологическую опухоль важно вовремя отличить от доброкачественной гиперплазии и других новообразований. Каждый способ исследования имеет свою прогностическую ценность – вероятность реального наличия заболевания при положительном результате теста, достоверность предсказания. Важным показателем информативности диагностических методов также является чувствительность – количество истинно положительных результатов среди других тестов. Для постановки диагноза всегда требуется комплекс исследований.
Способы диагностики рака предстательной железы
Способы диагностики рака простаты включают лабораторные анализы, инструментальные исследования, лучевые и ультразвуковые методы визуализации.
ПСА (простатспецифический антиген) – это вещество, которое вырабатывается тканями простаты. Его количество в крови растет при аномальном увеличении объема железы на фоне нарушения целостности ее клеточной структуры (в норме простата защищена клеточным барьером). Простата увеличивается не только от рака, поэтому для диагностики применяют несколько показателей на основе ПСА, отражающих как его количество, так и динамку изменения, соотношение свободной и связанной форм, наличие сопутствующих веществ.
- При значении от 4 до 10 нг/мл рак выявляется в 20-35% случаев;
- При ПСА от 10 нг/мл – 42-80%;
- Если уровень антигена превышает 40 нг/мл, то опухоль с вероятностью 40-60% уже дала метастазы.

Более специфическим показателем является РСА3. Его называют истинным онкомаркером простаты. Это ген, который активизируется на фоне развития рака. Продуктом такой активности является мРНК, уровень которой измеряется при помощи специальных тест-систем.
Пальцевое исследование раньше было единственным методом обнаружения рака простаты. На ощупь опухоль отличается от других тканей повышенной плотностью, неподвижностью, от нее могут отходить тяжи к семенным пузырькам. В большинстве случаев такие образования находятся в периферической зоне, то есть доступны для пальца врача. Нащупать можно только опухоли объемом более 0,2 см 3 .
При пальцевом исследовании рак простаты легко спутать с камнями, гиперплазией, хроническим простатитом, аномалиями семенных пузырьков. Прогностическая ценность метода составляет от 4 до 11% при ПСА до 2,9 нг/мл и от 33 до 83% при ПСА от 3 нг/мл.

Процедура пальпации простаты
При помощи абдоминального УЗИ (через живот) рак простаты выявляется плохо. На пути ультразвуковых волн много помех в виде тканей и жировой прослойки. Более точным методом является трансректальная эхография (ТРУЗИ). Между ректальным датчиком и простатой только тонкая стенка прямой кишки.
На начальных стадиях раковая опухоль гипоэхогенна (более темного цвета, плохо отражает сигнал), но может быть и гиперэхогенной. Для ранней диагностики (скрининга) этот метод непригоден, поскольку рак можно спутать с гиперплазией или простатитом. Существенные изменения тканей простаты видны на УЗИ, но точно определить их характер сложно.
ТРУЗИ позволяет обнаружить только 60% раковых опухолей, в остальных случаях злокачественные образования легко перепутать с обычными тканями из-за схожей эхогенности (ответ на УЗ-волну). Допплеровское сканирование (цветная картинка с обозначением интенсивности кровоснабжения) несущественно добавляет точности. Основное преимущество ТРУЗИ – безопасность и небольшая стоимость.
Самостоятельно найти небольшую опухоль на УЗ-снимке не получится. Даже специалисты не всегда правильно интерпретируют увиденное на экране.



Более точным методом диагностики рака является эластометрия сдвиговой волной (эластография). Проводится при помощи специального ТРУЗ-датчика и определяет рак с точностью до 87%. Подозрение вызывают участки тканей с пониженной эластичностью. Коэффициент жесткости раковой ткани в 28 раз превосходит аналогичный показатель нормальной. Основной недостаток – зависимость от профессионализма врача.
Первая информация о гистосканировании как методе дифференциальной диагностики рака предстательной железы стала появляться в 2007 г. Этот способ подходит для раннего выявления рака, его чувствительность составляет 92% .
Внешне процесс гистосканирования практически не отличается от обычного ТРУЗИ. Датчик поворачивается вокруг магнитной катушки, сигнал передается в аппарат Histoscanning (специальный диагностический комплекс), который создает трехмерную модель простаты и обозначает подозрительные области. Анализируется плотность, текстура, упругость ткани. Это новый метод диагностики рака простаты, идеален для подготовки к биопсии.

Результаты гистосканирования 
Карта, составленная по результатам гистосканирования с обозначенными подозрительными на рак участками
МРТ – самый безопасный и достаточно точный метод диагностики рака простаты. Выполняется для уточнения результатов ТРУЗИ или гистосканирования. Для обследования простаты используют ректальную катушку. Мультипараметрическая МРТ позволяет максимально точно диагностировать рак без биопсии. Подробнее о диагностике простаты при помощи МРТ.

Рак простаты на снимках МРТ
КТ для диагностики рака простаты назначают нечасто, в основном для обнаружения метастаз в костях, легких, брюшной полости и для планирования точек облучения при лучевой терапии. Внутривенное контрастирование позволяет достаточно четко визуализировать опухоль. Подробнее о компьютерной томографии предстательной железы.
Более точным методом является ПЭТ-КТ. Он требует предварительного внутривенного введения радиофармпрепарата. Его тип зависит от исследуемого процесса. ПЭТ-КТ можно назвать самой точной диагностикой, которая позволяет не только выявить опухоль и ее метастазы, но и определить стадию рака, спрогнозировать эффективность различных видов терапии.

Сравнительная таблица точности диагностических методов рака простаты по данным МГМУ им. Сеченова (Москва)
Радиоизотопное сканирование при раке простаты применяют для поиска метастазов в костях. Предварительно в вену вводят радиоактивный препарат, который концентрируется на поверхности костей и захватывается опухолевыми клетками. Примерно через 3 часа тело пациента сканируют при помощи гамма-камеры. Информация поступает в компьютер, который обрабатывает ее и выдает общую картину скелета. Доза облучения при этом не превышает таковую при КТ.
Радиоизотопное сканирование на 50% точнее рентгена (на нем метастаз будет виден только тогда, когда кость утратит половину своего неорганического состава). Метод применяют для диагностики рецидивов метастазирования после применения радикальных способов лечения.

Биопсию назначают как конечный исчерпывающий метод диагностики рака. Простату под видеоконтролем в нескольких местах прокалывают специальными иглами, в которые забирают столбики ткани. Чем больше проколов, тем точнее диагностика. Каждую из проб помещают в отдельный контейнер и отправляют на анализ. Качество полученных клеток оценивают по шкале Глисона.
Видеоконтроль за направлением игл осуществляют при помощи ректального датчика. Области забора тканей планируют заранее.

Лимфаденэктомия – это удаление тазовых лимфоузлов с целью оценки их поражения метастазами. Метод применяют перед удалением простаты, а также для планирования области облучения перед радиотерапией.
Операция чаще всего выполняется малоинвазивным лапароскопическим методом. В зависимости от объема удаляемой ткани выделяют ограниченную, стандартную и расширенную лимфаденэктомию.
Молекулярная диагностика рака простаты заключается в обнаружении особых веществ-маркеров, которые появляются в организме на фоне развития онкологического процесса. Открыто уже более 90 генов и их производных, которые тем или иным образом связаны со злокачественными опухолями простаты. Самым известным является ПСА. Кроме него, существуют, например, p2PSA, CYP3A4, Ki67 LI, PSMA, ЕРСА, PSCA. Изменения ДНК, характерные для рака простаты, выявляют при помощи методов ПЦР (в том числе в режиме реального времени), флуоресцентной гибридизации.

Краткая схема метода ПЦР
Примеры маркеров:
- Показателем опухолевого процесса является снижение синтеза Е-кадгеринов. Это вещества, которые обеспечивают межклеточные связи.
- По мере своего развития опухоль начинает активно продуцировать коллагеназу 4 типа. Чем ее больше, тем агрессивнее ведет себя рак.
- При злокачественной опухоли снижается активность гена р63 и его функционального аналога Р53, который препятствует развитию раковой клетки с поврежденной ДНК.
Молекулы опухолевых маркеров обнаруживают во время иммуногистохимического исследования тканей (ИГХ), полученных при биопсии. Обычного гистологического анализа бывает недостаточно для диагностирования онкологии. ИГХ позволяет не только точно поставить диагноз, но и выявить первичную опухоль, оценить ее характер, спрогнозировать рост образования, определить оптимальный вид терапии на основании исследования чувствительности клеток.
Ранняя диагностика рака предстательной железы: классика и последние европейские рекомендации
Задачей ранней диагностики рака простаты является обнаружение опухоли практически в зачаточной стадии. На первой стадии она излечима на 100%. На настоящий момент не существует специального метода ранней диагностики, который точно определил бы наличие рака. Классическая схема скрининга (обследование здоровых на вид людей по определенной схеме) включает в себя:
- Пальпацию железы;
- Анализ на ПСА;
- ТРУЗИ.
Это так называемая диагностическая триада.
Скрининг может спасти жизнь, а может привести к гипердиагностике и ненужной операции. Сначала берут кровь на ПСА. Точное пороговое значение, при котором имеет смысл делать биопсию, до сих пор не определено. При повышении верхнего предела есть риск пропустить рак на ранней стадии, при понижении – зря сделать биопсию (процедура с неприятными последствиями).

Риск развития рака при низком уровне ПСА 
Прогностическая ценность и чувствительность различных методов при скрининге 
Схема исследования ПСА при скрининге
Обычно при настораживающих значениях ПСА делают ТРУЗИ, но, согласно исследованиям европейских специалистов, для раннего скрининга рака простаты предпочтительнее МРТ. Этот метод снижает риск гипердиагностики на 50%, а ненужных операций – на 70%. Если МРТ выявляет подозрительный участок, то берут биопсию под МР-контролем.
Целевые группы для скрининга
Сколько бы ни говорили о массовом скрининге как о способе снижения смертности от рака простаты, он себя не оправдывает. Тотальные проверки всех мужчин экономически нецелесообразны и малоэффективны. Исследования для обнаружения рака простаты на ранней стадии следует проводить среди лиц, сформированных в целевые группы риска. На сегодняшний момент в них попадают следующие категории мужчин:
- В возрасте от 50 до 70 лет. Меняется гормональный уровень, обостряются хронические заболевания, что создает предпосылки для патологического деления клеток простаты. После 70 лет ранняя диагностика не имеет смысла.
- В возрасте после 40 лет при неблагоприятной наследственности (если отец или братья болели раком простаты).
- Больные гиперплазией простаты перед назначением длительного медикаментозного курса лечения (важно убедиться, что разрастание тканей не злокачественно и лечение не усугубит ситуацию).
Обязательное обследование на рак также рекомендуется всем мужчинам, имеющим проблемы с мочеиспусканием.
Минусы массового скрининга рака простаты:
- Часто выявляются медленно растущие опухоли, лечение которых приводит к ухудшению состояния пациента и снижает выживаемость;
- Бывают ложноположительные результаты, которые крайне негативно действуют на психологическое состояние мужчины;
- Высокая стоимость дополнительных исследований, далеко не всегда оправданная;
- В 2% случаев после биопсии под контролем ТРУЗИ развивается инфекционное воспаление.
Очень желательно, чтобы все исследования проводил один и тот же специалист, который после пальцевого осмотра точно будет знать, каким областям простаты уделить особое внимание на УЗИ.

Общая схема диагностики рака простаты с применением различных методов
Диагностика рака простаты в пожилом возрасте
У мужчин после 70 лет чаще всего обнаруживается медленно прогрессирующий рак простаты, который может никогда и не доставить серьезных неприятностей. В таких случаях врач должен принять важное решение относительно дальнейшей тактики диагностики и лечения.
Если сделать биопсию, то высока вероятность развития побочных эффектов в виде инфекции, затруднения мочеиспускания, недержания мочи, болей. Нередко именно биопсия дает толчок росту опухоли, после чего состояние больного резко ухудшается. Европейские урологи рекомендуют ориентироваться не на уровень ПСА, а на сопутствующие симптомы. При их слабой выраженности лучше отказаться от инвазивных методов диагностики и лечения, а наблюдать за опухолью при помощи МРТ и анализа на ПСА (динамика роста, соотношение свободного и общего).
На ТРУЗИ-снимках простаты пожилых мужчин сложно выявить небольшие раковые очаги, поскольку железа увеличена, в ней много участков гиперплазии. Это также не является причиной для активного лечения.
Диагностика рецидива рака простаты
Целью радикальных методов лечения рака простаты является полное удаление опухолевого очага, однако в ряде случаев развиваются рецидивы. Зафиксировать активизацию онкопроцесса можно при помощи следующих методов:
- Анализ на ПСА и другие биомаркеры. Повышение их уровня говорит о биохимическом рецидиве. Через 20-30 дней после операции количество антигена должно снизиться до неопределяемых значений. Рост в пределах 0,1-0,3 нг/мл может свидетельствовать о функционировании оставшихся доброкачественных тканей.
- МРТ и остеосцинтиграфия. Методы позволяют выявить метастазы.
- ПЭТ-КТ с холином обнаруживает мелкие очаги роста.
- Биопсия под контролем ТРУЗИ.
Диагностика выявляет характер роста опухоли, в зависимости от этого подбирают тип терапии.
Какой способ диагностики рака предстательной железы неверен
Ошибка диагностики рака может быть при любом методе, если специалист не обладает должной квалификацией. К ложному диагнозу приводит неправильная интерпретация результатов или низкое качество оборудования. Опытный врач с точностью до 80% может определить рак и при пальпации.
Чаще всего ошибается УЗИ. После этого метода больше всего ложных биопсий.
В настоящее время урологи все меньше полагаются на значение ПСА, на смену этому маркеру приходят более точные − b-PSA и p2-PSA.
Заключение
Большинство стандартных методов диагностики рака простаты, которые доступны по полису ОМС, допускают ложноположительные и ложноотрицательные результаты. Играет роль и человеческий фактор, и качество оборудования. В частных клиниках нередко закупают списанные томографы и УЗ-аппараты, снимки которых неинформативны для специалистов. Максимально точную диагностику могут провести только в специальных онкоцентрах, например, в СПб это можно сделать в подразделении НМИЦ онкологии им. Петрова – консультативно-диагностическом центре на ул. Красного Текстильщика. В других городах ведущие онкоцентры также предоставляют подобные услуги.
Читайте также:


