Можно ли вылечиться от дерматомиозита
МНЕ СМЕНИЛИ ДИАГНОЗ НА ХРОНИЧЕСКИЙ АУТОИММУННЫЙ ПОЛИМИОЗИТ С ТЯЖЕЛЫМ НИЖНИМ ПЕРИФЕРИЧЕСКИМ ПАРАПАРЕЗОМ… ТОЖЕ НЕ АЙС КОНЕЧНО НО ЗАТО ЛЕЧИТСЯ МЕДИКАМЕНТОЗНО ))))))))))))))
ну и кому интересно .
Полимиозит — системное заболевание соединительной ткани, характеризующееся воспалительным и дегенеративным изменением мышц, приводящее к их слабости, атрофии и сопутствующим поражениям кожи при дерматомиозите.
Этиология полимиозита изучена недостаточно, предполагается роль вирусов, генетических факторов, непереносимость лекарств.
Развитие полимиозита (дерматомиозита) связывают с аутоиммунным процессом и образованием специфических антител к мышечной ткани, а также с нарушением клеточного иммунитета, что подтверждается накоплением большого количества Т- и В-лимфоцитов в пораженных мышцах.
Полимиозитом (дерматомиозитом) чаще болеют женщины (соотношение 2,5: 1), выделяют ювенильный (детский) дерматомиозит. Частота заболевания от 2 до 10 случаев на 100000 населения.
Симптомы полимиозита
Выделяют несколько клинических вариантов полимиозита (дерматомиозита): 1) первичный идиопатический полимиозит; 2) детский дерматомиозит; 3) первичный идиопатический дерматомиозит взрослых; 4) паранеопластический дерматомиозит.
Начало полимиозита (дерматомиозита), как правило, постепенное, в виде прогрессирующего нарастания мышечной слабости преимущественно проксимальных групп мышц. Иногда (особенно у лиц молодого возраста и детей) наблюдается начало с болями и слабостью в мышцах, лихорадкой, потерей массы тела. При дерматомиозите наряду с поражением мышц отмечают характерные изменения кожи.
Ведущим признаком является симметричная слабость проксимальных групп мышц конечностей, шеи, спины: больной не может присесть, самостоятельно подняться с кровати, войти в транспорт, в тяжелых случаях — причесаться, оторвать голову от подушки, держать ложку. Поражение мышц глотки, гортани и пищевода приводит к дисфагии, поперхиванию, иногда к невозможности самостоятельно глотать пищу, могут поражаться мышцы мягкого неба, языка — развивается псевдобульбарная симптоматика. Поражение межреберных мышц и диафрагмы приводит к нарушению дыхания, осложняется развитием пневмонии. При поражении мышц гортани появляются дисфония, осиплость голоса, вплоть до афонии. При пальпации часто определяются болезненность и инфильтрация мышц.
При дерматомиозите типичны изменения кожи чаще в виде эритемы на открытых участках тела; характерны периорбитальный отек и эритема, имеющая своеобразный лиловый оттенок цвета гелиотропа, яркая эритема локализуется также на лице, шее, в зоне декольте, над суставами, особенно над проксимальными межфаланговым и пястно-фаланговыми; типичны капилляриты.
Поражение внутренних органов при полимиозите (дерматомиозите) встречается относительно редко.
Поражение сердца проявляется изменениями миокарда с нарушением ритма, проводимости и иногда сердечной недостаточностью преимущественно в острую фазу болезни. При обследовании обнаруживают тахикардию, глухость тонов, аритмию и увеличение размеров сердца.
Поражение легких может протекать с развитием интерстициального легочного фиброза у 5—10% больных, что проявляется нарастающей одышкой, непродуктивным кашлем, снижением диффузионной функции легких. В тяжелых случаях возможно развитие фатальной легочной недостаточности.
Поражения ЖКТ проявляются чаще всего нарастающей дисфагией. В отличие от склеродермии поражаются верхние отделы пищевода и глоточное кольцо, в связи с чем имеются затруднения при глотании как твердой, так и жидкой пищи, которая выливается через нос.
Особый вариант дерматомиозита — опухолевый (паранеопластический), который клинически может не отличаться от идиопатического, однако, как правило, отмечается торпидность к проводимой терапии, глюкокортикостероидами. Дерматомиозит может вызвать злокачественная опухоль любой локализации; удаление опухоли приводит к излечению от дерматомиозита. Поэтому при заболевании дерматомиозитом (полимиозитом) очень важно тщательное и иногда повторное обследование больных для исключения неоплазмы.
Из лабораторных признаков активного полимиозита (дерматомиозита) помимо неспецифических признаков воспаления (лейкоцитоз, увеличение СОЭ, диспротеинемия) диагностическое значение имеет появление креатина в моче, повышение в крови уровня креатинфосфокиназы, аминотрансфераз и альдолазы.
Диагноз полимиозита (дерматомиозита) ставится на основании типичных кожных изменений, нарастающей проксимальной мышечной слабости, повышения мышечных ферментов; типичной картины полимиозита при биопсии мышцы; миопатических изменений при электромиографии.
Дифференциальный диагноз проводят с целым рядом заболеваний: вирусным или бактериальным миозитом, поражением мышц при паразитарных заболеваниях (трихинеллез, цистицеркоз); алкогольной миопатией; ревматической полимиалгией; эндокринными заболеваниями (гиперкортицизм, гипо- или гипертиреоз).
К осложнениям полимиозита (дерматомиозита) относятся развитие мышечных контрактур, кальциноза мышц.
К смертельным осложнениям может привести развитие аспирационной пневмонии, дыхательных расстройств, поражение сердца; опухоль.
Лечение полимиозита
Основным лечением полимиозита (дерматомиозита) являются глюкокортикостероидные гормоны, назначаемые в острый период болезни в высоких дозах (60—100 мг/сут) с постепенным снижением до поддерживающих в течение 1—2 лет. Иммунодепрессанты (чаще метотрексат или азатиоприн) используют при неэффективности терапии глюкокортикостероидами.
Прогноз при ранней диагностике, адекватной терапии и отсутствии осложнений благоприятный, возможно полное излечение.
Лечение дерматомиозита направлено па устранение проксимальной мышечной слабости и кожных изменений. Кожные проявления не всегда реагируют на терапию одновременно с реакцией мышц. При лечении миопатии эффективно применение пероральных кортикостероидов, иммуносупрессоров, биологических агентов и/или иммуноглобулина. Эффективными средствами в отношении кожных проявлений заболевания являются солнцезащитные препараты, местные кортикостероиды, антималярийные средства, метотрексат и/или иммуноглобулин. В рутинной клинической практике эти методы терапии используются отдельно и в комбинации, однако оптимальные терапевтические режимы не установлены, поскольку отсутствуют высококачественные рандомизированные исследования с группами контроля.
• В начале лечения применяются кортикостероиды с высокой фармакологической активностью. Мазь триамцинолона может применяться для менее выраженных очагов или при их локализации на лице.
Короткий курс стероидов сверхвысокой активности, таких как клобетазол, рекомендуется при более тяжелом поражении различных участков тела, за исключением лица.
• Местный такролимус 0,1% применяется как вспомогательная терапия при торпидпых кожных проявлениях.
• Системная терапия направлена на мышечные проявления заболевания и начинается с приема системных кортикостероидов в комбинации с иммуносупрессивными препаратами (метотрексатом, циклоспорином А или азатиоприном), либо без них.
• Препаратом первой линии является преднизон в дозе 0,5-1,0 мг/кг массы тела в день (или 60 мг в день) до тех пор, пока повышенный уровень мышечных ферментов не продемонстрирует тенденцию к нормализации показателей, после чего доза стероидов должна постепенно снижаться.

• Метотрексат вызывает положительный эффект у детей и взрослых с торпидным дерматомиозитом, у пациентов, нуждающихся в стероид-сберегающих препаратах, а также при вторичных побочных эффектах стероидов:
- Недавние исследования показали, что назначение метотрексата в ранней стадии заболевания способствует более быстрому выздоровлению, ограничению количества применяемых лекарственных препаратов и уменьшению осложнений.
- Комбинированная терапия с преднизопом и метотрексатом становится общепринятой и позволяет уменьшить дозу кортикостероидов до 5 мг в день и менее.
- Прием метотрексата предлагается начинать с 7,5-10 мг в педелю. Затем дозировка повышается на 2,5 мг в педелю до достижения общей дозы 15-25 мг в неделю. Общая доза метотрексата зависит также от того, насколько хорошо пациент может переносить этот препарат.
- По мере повышения дозы метотрексата постепенно снижается доза преднизона.
• Комбинация циклоспорина А и метотрексата показала некоторое преимущество при лечении торпидного ювенильного дерматомиозита.
• Азатиоприн обычно применяется при хронической форме заболевания как стероидсберегающий препарат; однако исследования с применением азатиоприна в дозе 2 мг/кг в день не показали значительного улучшения силы мышц по сравнению с плацебо.
• Гидроксихлорохин является еще одним препаратом стероид-сберегающей терапии, который рекомендуется для молодых женщин с незначительными проявлениями заболевания.
• Эмпирически изучались различные парные комбинации следующих препаратов: азатиоприн, циклоспорин А, внутримышечный метотрексат и пероральный метотрексат.
• Крайне важно изучить профиль побочных эффектов этих препаратов и в соответствии с ним регулировать лечение пациента. Во время их приема следует исключить беременность, а также регулярно проводить контрольные лабораторные исследования. У пациентов, принимающих метотрексат, после кумулятивной дозы 1,5 г необходима биопсия печени.

• Внутривенная пульс-терапия метилпредпизолона считается предпочтительной для тяжелого течения болезни и при торпидных случаях миозита.
• Отмечается значительное число пациентов, резистентных или частично реагирующих па стероиды или иммуносупрессивные препараты. Недавние исследования выявили эффективность внутривенного иммуноглобулина как препарата второй линии.
- При лечении пациентов с дерматомиозитом с помощью внутривенного введения иммуноглобулина было показано статистически достоверное улучшение мышечной силы и некоторое улучшение кожных проявлений заболевания.
- Пациенты получали 1 г/кг/день иммуноглобулина в течение двух дней каждые 4 недели.
• Для восстановления мышечной силы рекомендуются физиотерапия и/или специальные методы лечения.
• Фотозащитные мероприятия включают применение солнцезащитных препаратов широкого спектра, ношение защитной одежды и ограничение времени пре бывания на солнце.
• Новые биологические препараты, включая ингибиторы фактора некроза опухолей-альфа, испытываются в настоящее время для применения при дерматомиозите у детей и взрослых.

• У пациентов старше 50 лет после начала лечения необходимо исключить признаки малигиизации.
• Для женщин без факторов риска достаточно полного ежегодного обследования яичников, молочных желез и прямой кишки.
• С учетом возраста пациента и семейного анамнеза выполняется маммография и/или колоноскопия. Некоторые специалисты рекомендуют полное обследование пациентов старше 50 лет с дерматомиозитом.
• Если с момента установления диагноза прошло более двух лет, поиск злокачественной опухоли не обязателен. В течение первого года наблюдения диагноз первичной злокачественной опухоли устанавливается в шесть раз чаще. После первого года риск становится таким же, как в общей популяции.
Рекомендации пациентам с дерматомиозитом. Пациенту необходимо разъяснить всю важность солнцезащитных мероприятий. Следует указать на серьезный характер заболевания и его прогноз, поскольку у многих пациентов мышечная слабость сохраняется даже тогда, когда течение заболевания удается взять под надежный контроль. Пациенты должны понимать, что принимаемые ими лекарственные препараты наряду с пользой увеличивают риск нежелательных побочных эффектов, поэтому врача следует информировать о возникновении любых неблагоприятных явлений. В связи с приемом целого ряда препаратов женщинам детородного возраста необходимо предохраняться от беременности.
Пациенты нуждаются в очень внимательном и регулярном наблюдении для контроля медикаментозного лечения и общего состояния. Это необходимо потому, что высокие дозы стероидов и стероид-сберегающих препаратов, таких как метотрексат, обладают потенциалом многочисленных побочных эффектов. Необходимы лабораторные тесты по всем параметрам, связанным с приемом токсических медикаментов, используемых при лечении. Для профилактики некоторых побочных эффектов сильнодействующих медикаментов пациенты также нуждаются в физиотерапии и специальных добавках, таких как кальций и фолиевая кислота.
Клинический пример дерматомиозита. 55-летняя латиноамериканка обратилась к врачу по поводу распространенной сыпи и повышенной мышечной слабости. Сыпь появилась у нее два месяца назад, предположительно как фоточувствительная реакция на новый назначенный препарат гидрохлоротиазид. Пациентка прекратила прием гидрохлоротиазида, и после применения местных кортикостероидов выраженность сыпи уменьшилась. В последнее время женщина испытывала затруднения при вставании со стула, ходьбе и поднимании рук над головой. При осмотре была выявлена гелиотропная сыпь, натогномоничная для дерматомиозита, и папулы Готтрона.
Отмечалась также околоногтевая эритема и чешуйки красного цвета па волосистой части кожи головы. При неврологическом исследовании была выявлена проксимальная миопатия. Больная также жаловалась на затруднения при глотании хлеба. Активность ферментов мышечной ткани была повышена в незначительной степени. Лечение, заключавшееся в ежедневном приеме 60 мг преднизона и аппликации местных стероидов на пораженные участки, оказалось эффективным и две недели спустя самочувствие пациентки улучшилось, при этом сыпь побледнела. После шестинедельного ежедневного приема преднизона в дозе 60 мг больной назначен метотрексат еженедельно по 10 мг с целью последующего постепенного снижения дозы стероидов. Некоторое время улучшение продолжалось, по после снижения дозы стероидов высыпания рецидивировали.
Была назначена физиотерапия и начато лечение микроэлементами кальция для предупреждения стероид-индуцированного остеопороза. Для минимизации побочных действий метотрексата больная также принимала по I г фолиевой кислоты ежедневно. Шесть месяцев спустя она чувствовала себя хорошо, принимая 7,5 мг метотрексата еженедельно и 20 мг преднизолона ежедневно.

Общие сведения
Дерматомиозит или по-другому — болезнь Вагнера является тяжелым диффузным прогрессирующим системным заболеванием соединительной ткани, поражающим скелетную и гладкую мускулатуру, микроциркуляторную систему сосудов, внутренние органы и кожные покровы. Приводит к замене функциональных структур на фиброзные.
Клиническая картина выражается в виде двигательной дисфункции, васкулита, отеков, эритемы, гиперкератоза и может быть:
- острой, начинающейся с лихорадки и запоминающегося развития симптомов, без лечения приводит к летальному исходу спустя 2-3 мес., вызванному полным обездвиживанием и тяжелой сердечно-легочной недостаточностью;
- подострой– с постепенным нарастанием на протяжении нескольких лет мышечной слабости, артралгии, эритемы, изменений во внутренних органах;
- хронической– с доброкачественным исходом, имеющим циклическое течение и длительные ремиссии, отличается наличием локальных атрофических и склеротических изменений мышц и кожных покровов, причем во внутренних органах происходят компенсированные изменения.
В результате дерматополимиозит приводит к осложнениям – фиброзу, кальцинозу, атрофии и гнойным инфекциям.
Болезнь Вагнера встречается редко – 2-6 взрослых особей и 1-2 ребенка на 100 тыс. человек. Патология более распространена в странах на юге Европы. Заболеваемость повышается в весенне-летний сезон, что связывают с инсоляцией — более интенсивным облучением солнечным светом.
Патогенез
Начинается патогенетический процесс с неспецифического воздействия — переохлаждения, избыточной солнечной инсоляции, вакцинации, острой интоксикации, травм и прочих экзогенных факторов. Он связан с наличием инфекционных агентов, внедренных в геном мышечных клеток, изменениями нейроэндокринной реактивности или генетической предрасположенностью — наличием антигенов гистосовместимости HLA, связанных с B8 либо DR3.
При дерматомиозите происходит развитие иммунновоспалительной реакции, направленной на деструкцию измененных внутриядерных структур клеток мускулатуры и кожи. Благодаря перекрестным реакциям в иммунное поражение вовлекаются родственные по антигенам клеточные популяции. Микрофагальные механизмы элиминации из организма иммунокомплексов приводят к активации фиброгенеза и системного воспаления мелких сосудов. Гиперреактивность иммунной системы направлена на разрушение внутриядерного строения вириона, она проявляется наличием в кровотоке антител Mi2, Jo1, SRP, а также аутоантител к ядерным белкам и другим антигенам растворимого типа.
Классификация
Примерно в 25-30% случаев отсутствуют кожные симптомы и тогда говорят о частном случае этого системного заболевания – полимиозите.
В зависимости от происхождения и течения выделяют:
- первичный идиопатический дерматополимиозит;
- вторичный паранеопластический или опухолевый тип встречается у особ старше 55 лет на фоне рака молочной железы, легких, яичников, предстательной железы, матки, желудка, толстой кишки, при гемобластозах и прочих злокачественных новообразованиях;
- ювенильный – детский;
- полимиозит, сочетающийся с прочими диффузными заболеваниями соединительных тканей.
Отличается очаговым кальцинозом таких мягких тканей как мышцы, эпидермис и подкожная жировая клетчатка. Депозиты солей кальция – гидроксиапатиты могут откладываться на поверхности и глубоко, образуя ограниченные единичные или диффузно расположенные узелки и псевдоопухоли. Поверхностные бляшки с кальцинатами вызывают воспалительные реакции окружающих тканей, они нагнивают и отторгаются в виде крошковатой массы.
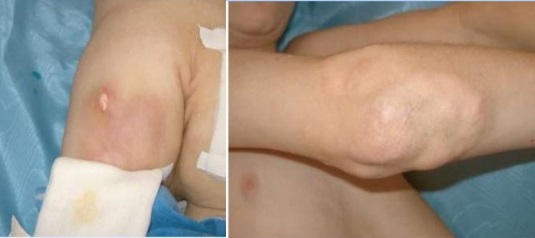
Как и у взрослых наблюдаются классические высыпания и симптом Готтрона. Постепенно нарастающая мышечная слабость начинается с причудливой походки ребенка, которая в дальнейшем еще больше сковывает движения, не давая возможности играть, бегать и обслуживать себя.
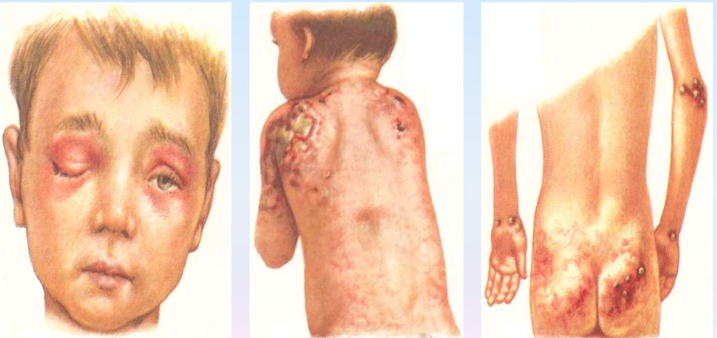
Причины
Патология полиэтиологическая, ей предшествует множество факторов:
- латентные инфекционные агенты: вирусы гриппа, парагриппа, гепатита B, пикорнавирусы, парвовирусная инфекция, бактериологические возбудителиболезни Лайма и бета-гемолитические стрептококкигруппы А, простейшие, например, токсоплазмы;
- злокачественные новообразования;
- вакцинирование от тифа, кори, паротита, холеры, краснухи;
- терапия Д-пеницилламинами, гормонами роста.
Симптомы дерматомиозита
Болезнь Вагнера представляет собой целый симпатокомплекс, обусловленный прежде всего генерализованными нарушениями микроциркуляторного кровяного русла и проявляющийся со стороны различных органов и систем, больше всего – со стороны эпидермиса и мускулатуры.
Симптом Готтрона – наличие розовых и ярко-красных шелушащихся папул, бляшек, локализованных на разгибательных поверхностях суставов, таких как: межфаланговые и пястнофаланговые складки, локтевые и коленные сгибы. Неяркие покраснения могут самопроизвольно регрессировать и оказываться полностью обратимыми.
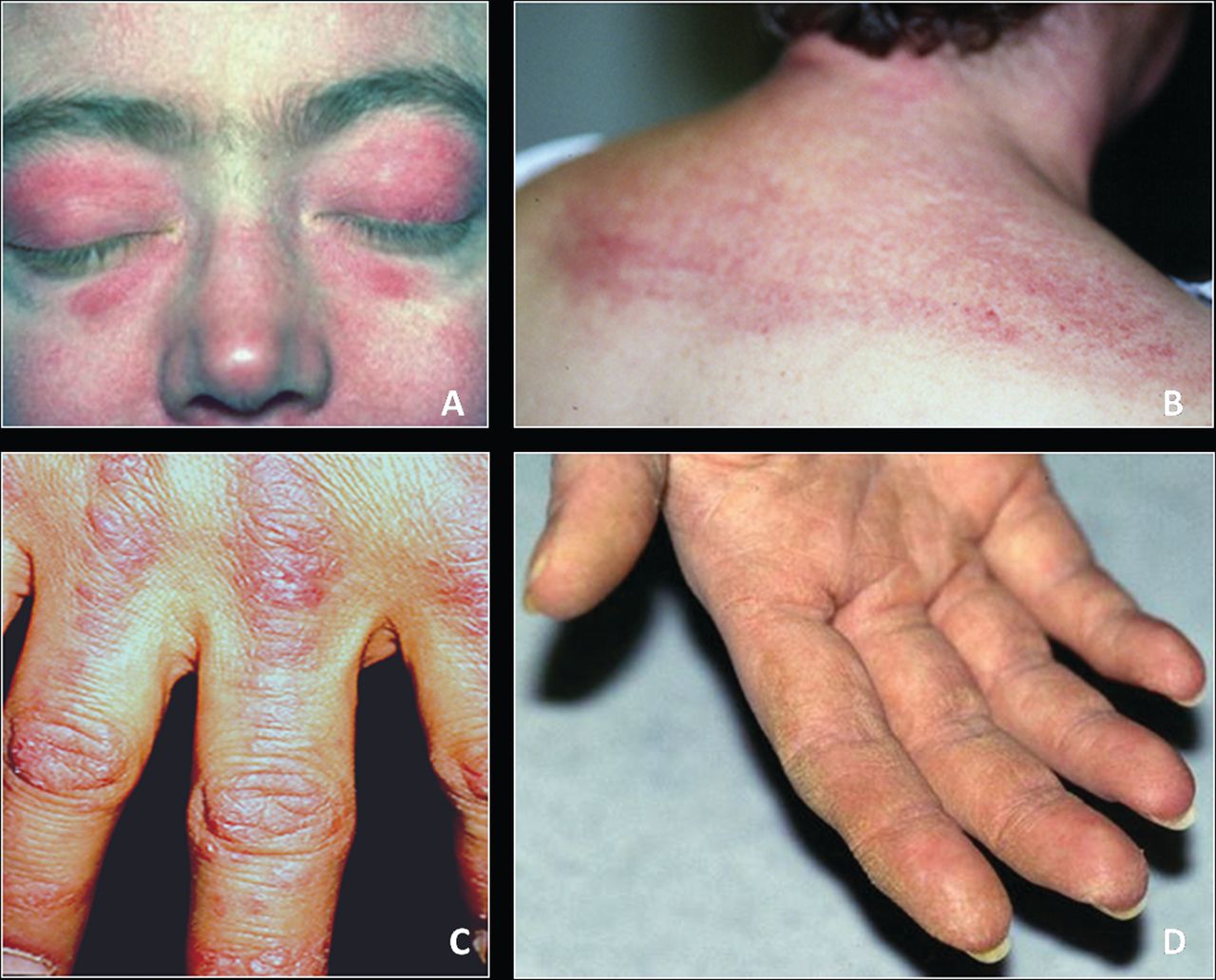
У больных развивается фотодерматит – повышение чувствительности к солнечным лучам открытой поверхности кожи.
Ранним симптомом дерматомиозита считается изменения ногтей – покраснение и разрастание кожи вокруг ногтевой пластинки.
Главные симптомы полимиозита – это атрофия и мышечная слабость, которая обычно симметрична и вовлекает в патологический процесс плечевой и тазовый пояс, сгибатели шеи и мышцы брюшного пресса, проявляется сложностью подъема по лестнице, вставания со стула, удержания головы.
Опаснее всего, когда задеты дыхательные, глазодвигательные и глотательные мышцы, ведь это провоцирует дыхательную недостаточность, дезориентацию и диплопию, трудности во время акта глотания (дисфагия), охриплость и изменения голоса. Воспалительный процесс в мускулатуре может сопровождаться болевым синдромом — миалгией. Нарушения кровоснабжения и трофики вызывает уменьшение мышечной массы, развитие тяжелого некротического миозита, в результате происходит разрастание соединительной ткани в мышечных волокнах и образование уплотнений, а также сухожильно-мышечных контрактур.
Влияние на сердечно-сосудистую систему вызывает не только патологию миокарда — миокардит, но и коронарных сосудов и всех трех оболочек сердца, провоцируя тахикардию, артериальную гипотензию, приглушенность тонов, дилатационную кардиопатию, нарушения сердечного ритма, вплоть до AV-блокады и инфаркта.
Обычно это вторичные осложнения, вызванные гиповентиляцией в результате слабости дыхательных мышц и диафрагмы, развитием инфекции, аспирацией при глотании. Чаще всего они приводят к фиброзирующему альвеолиту, базальному пневмофиброзу, интерстициальной пневмонии и даже метастатическим новообразованиям. Главными проявлениями являются такие симптомы как:
- одышка;
- хрипы;
- непродуктивный кашель;
- цианоз;
- крепитация– хрустящий звук, выявляющийся при аускультации;
- уменьшение объемов и диффузионных характеристик легких.
- скованность движений – вследствие поражения суставов ( артралгии и артрита), что может сопровождаться их припухлостью и болями;
- субфебрильная температура – до 38° в острых фазах;
- развитие гастрита, колита, эрозивно-язвенных поражений и геморрагиипрактически в 50% случаев приводят к утрате веса и спровоцированы изменениями сосудов и нарушениями питания слизистых ЖКТ, проходимости нервных импульсов и перистальтики;
- синдром Рейно – онемение рук и холодные пальцы после действия холода, эмоционального стрессалибо без явных причин, что в итоге вызывает боль и отечность, багрово-красный цвет кожных покровов;
- конъюнктивит, стоматит и другие поражения слизистых;
- умеренная гепатомегалия и незначительные нарушения функции печени;
- лимфаденопатия– наличие плотных распространенных отеков;
- нарушения чувствительности — гиперестезии, гипералгезии, арефлексии, чаще всего вызванные полиневритом;
- гормональный дисбаланс, сопровождающийся функциональными нарушениями работы половых желез и гипофизарно-надпочечниковой системы.
Анализы и диагностика
При подозрении на дерматомиозит необходим первичный осмотр и изучение состояния больного, сбор данных анамнеза и жалоб. В анализах крови можно выявить:
- незначительное повышение СОЭ;
- умеренный лейкоцитоз;
- увеличенное количество миоглобина, фибриногена, креатина, мочевой кислоты, гаптоглобинов, серомукоида, α-2-иγ-глобулинов;
- повышение ферментативной активности, вызванной мышечным распадом, наибольшее диагностическое значение имеет креатинфосфокиназа, лактатдегидрогеназа, АЛТ, АСТ, альдолаза.
При полимиозите важны электромиографические исследования нормальной электрической активности расслабленных мышц, низкоамплитудной — при их произвольных сокращениях, а также изучение коротких, полифазных потенциалов моторных единиц, выявляющих спонтанные потенциалы фибрилляции.
Для подтверждения диагноза следует провести:
- биопсию мышц;
- иммунологические пробы антител Jo 1 к гистидил-транспортной РНКсинтетазе;
- рентгенографию и УЗИ для выявления альвеолита, пневмонии, кальцинатов, остеопорозаили других глубинных изменений.
Лечение дерматомиозита
В основном лечение дерматомиозита медикаментозное. Обычно для ликвидации иммунновоспалительного фиброзирующего процесса назначают:
- глюкокортикоиды;
- цитостатики.
Кроме того, лечение полимиозита может включать симптоматическую коррекцию нарушений работы органов и систем – прием сердечных гликозидов, гепатопротекторов, поливитаминных комплексов, нестероидных противовоспалительных препаратов и средств, улучшающих нервно-мышечную передачу и повышающих метаболические процессы в мышечных тканях. При обнаружении глубинного или поверхностного отложения кальцинатов вводят внутривенно с 5%-раствором глюкозы динатриевую соль этилендиаминтетрауксусной кислоты, которая образует комплексы с ионами кальция, и они выводятся из организма.
В ходе лечения важно сохранять объем движений и препятствовать мышечной слабости, образованию контрактур, к примеру, при помощи лечебной физкультуры. Больным категорически противопоказана иммобилизация.
- Свежие записи
- Архив
- Друзья
- Личное дело
- Избранное
Практические подходы к лечению полимиозита
Е.Ю. Мененкова 1 , Ю.А. Капитонова 1 , В.И. Соколова 2
Полимиозит (ПМ) – аутоиммунное заболевание, патоморфологическим субстратом которого являются поперечно-полосатая мускулатура, с системным поражением центральной и периферической нервной системы, полиморфной висцеральной патологией [2, 3]. Частота заболеваемости полимиозитом составляет 0,5–0,8 на 100 тыс населения. Подвержены болезни популяции всех возрастов, но пик заболеваемости приходится на 5–15 и 40–60 лет. Женщины болеют в 2 раза чаще. Несмотря на 150-летнюю историю изучения ПМ, до настоящего времени не выявлено пусковых механизмов заболевания, не существует ни единых схем лечения, ни специфических маркеров прогнозирования и оценки проводимой терапии.
Целью настоящей работы была разработка подходов к лечению больных ПМ с высокой степенью активности процесса, проявляющейся тяжёлыми двигательными нарушениями.
Материал и методы исследования
В исследовании приняли участие 9 пациентов женского пола больных полимиозитом в возрасте от 21 до 56 лет, средний возраст составил 40 ± 9,6 лет. Диагноз был установлен на основании:
Всем пациентам была проведена пульс-терапия кортикостероидами (КС) (метипред или преднизолон) внутривенно капельно из расчёта 10–15 мг на 1 кг массы тела больного в течение трёх дней, с последующим назначением преднизолона перорально в дозе 1 мг/кг/сут через день.
Эффективность проводимой терапии оценивалась через 10 дней после окончания пульс-терапии на основании динамики неврологического статуса, динамики показателей КФК, уменьшения или исчезновения электромиографических признаков воспалительного процесса в мышцах (потенциалов фибрилляций и положительных острых волн), снижения выраженности спонтанной активности и увеличения параметров ПДЕ.
Результаты
В нашем исследовании длительность заболевания ПМ составила 6,28 ± 1 мес. До начала лечения все пациенты предъявляли жалобы на боли в проксимальных мышцах конечностей, возникающие при движении и в покое, при пальпации, слабость в проксимальных мышцах плечевого и тазового поясов, похудание за время болезни на 5,12 ± 1,74 кг, периодические затруднение при дыхании. У одной больной наблюдалась эритема лица, шеи, периорбитальный отёк.
Приводим наиболее типичный клинический случай (собственное наблюдение).
Следует отметить, что у всех 9 пациентов при использовании пульс-терапии КС (метипред или преднизолон) внутривенно капельно было достигнуто увеличение силы в скелетных мышцах и снижение уровня КФК и ЦИК (табл. 1). Уменьшение степени выраженности спонтанной активности по данным ЭМГ наблюдалось у 8 пациентов. Пульс-терапия кортикостероидами способствовала быстрому регрессу неврологических нарушений, улучшению двигательных функций у пациентов и восстановлению способности к самообслуживанию. Кроме того, удалось сократить длительность стационарного лечения в среднем на 20 %. Побочные эффекты имели место лишь у троих больных и проявлялись в основном тошнотой, которую удалось купировать назначением антацидных препаратов (альмагель).
Для постановки определённого диагноза полимиозита необходимо сочетание не менее ТРЁХ критериев диагностики полимиозита:
- клинический симптомокомплекс
- повышение уровня мышечных ферментов
- изменения параметров ПДЕ по данным ЭМГ
- морфологические изменения в мышцах.
Кортикостероиды являются основной патогенетической терапией при полимиозите. По данным литературы, полный или частичный ответ на КС удаётся достигнуть у 75–90 % больных [6].
В настоящее время КС используются по двум методикам. Первая – это пульс-терапия КС (метипред или преднизолон) внутривенно капельно в течение трёх дней из расчета 10–15 мг на 1 кг массы тела больного [4, 5].
Вторая схема: назначение преднизолона в однократной дозе из расчёта не менее 1 мг на 1 кг массы тела больного утром через день. В особо тяжёлых случаях доза увеличивалась до 2 мг на 1 кг массы тела [4].
Нашим больным с острым развитием заболевания и выраженной мышечной слабостью мы применили первую схему. Пульс-терапия была проведена в течение 3 дней, с последующим назначением преднизолона перорально в дозе 1 мг/кг/сут через день. Ни в одном клиническом наблюдении значимых побочных эффектов в лечении ПМ не отмечалось. Известно, что улучшение у больных с ПМ на фоне лечения адекватными дозами КС наступает в среднем через 2–4 месяца после проведённой терапии. Поддерживающая доза преднизолона зависит от течения болезни, индивидуальной переносимости. Вопрос об отмене препарата можно решить лишь в том случае, если в течение, по крайней мере, 12 месяцев не наблюдалось клинико-биохимической активности (КФК) процесса, исчезновение спонтанной активности по данным ЭМГ [4]. В большинстве случаев, даже при самом благоприятном течении заболевания, общая продолжительность лечения составляет 2–3 года, при этом только 25 % больных могут полностью отказаться от КС, но многие вынуждены в течение длительного времени принимать поддерживающие дозы препарата.
Цитостатическая терапия (ЦТ) должна обсуждаться при необходимости включения в схему лечения в следующих случаях:
Клиническое улучшение наступает в течение 2–5 дней после инфузии, а спустя 10–14 дней достигает своего максимума (доза 2–4 г на 1 кг массы тела ежедневно в течение 5 дней). Лечение ВВИГ способствует повышению общей сопротивляемости организма больных и более быстрому разрешению интеркурентных инфекций, что особенно важно у больных с угнетённой иммунной системой.
После 2–3 курсов, проводимых ежемесячно, улучшение достигает степени, дающей возможность снижения дозы КС. Однако, учитывая дороговизну препарата, решение о целесообразности применения ВВИГ должно обсуждаться в каждом конкретном случае.
Таким образом, полученные нами результаты позволяют рекомендовать проведение пульс-терапии высокими дозами КС (преднизолон) больным с острым развитием ПМ для достижения более быстрого регресса неврологических нарушений, восстановления способности к самообслуживанию и улучшения качества жизни пациентов, а также позволяют сократить длительность стационарного пребывания больных, что особенно важно в условиях страховой медицины.
Читайте также:


