Лечение очаговой склеродермии метотрексатом
- КЛЮЧЕВЫЕ СЛОВА: склеродермия, лейкоз, хориокарцинома, метотрексат
Ограниченная склеродермия – хроническое заболевание соединительной ткани, которое характеризуется нарушением микроциркуляции и синтеза коллагена, воспалением, аутоиммунной и тканевой реконструкцией. Патологией чаще страдают женщины в возрасте от 20 до 50 лет.
Этиология ограниченной склеродермии остается не до конца понятной. На ее развитие могут влиять генетические факторы, сопутствующие заболевания. В настоящее время большое значение отводится нарушению клеточного и гуморального иммунитета, а также выработке аутоантител против компонентов клетки. Именно поэтому для лечения данного дерматоза применяются иммуносупрессанты.
Согласно стандартам оказания медицинской помощи больным с ограниченной склеродермией, утвержденным приказом Министерства здравоохранения и социального развития Российской Федерации от 28.12.2012 № 1591н, в качестве препаратов первой линии показаны глюкокортикостероиды. Несмотря на то что данный метод лечения позволяет достичь хорошего результата, назвать его идеальным невозможно. Поэтому поиск новых терапевтических опций продолжается. Метотрексат может стать достойным претендентом на эту роль. Необходимо также отметить, что в педиатрической практике при ограниченной склеродермии метотрексат успешно применяется достаточно широко и давно.
Метотрексат
Метотрексат является цитостатиком, который блокирует синтез ДНК, угнетает продукцию провоспалительных и усиливает продукцию противовоспалительных цитокинов, что и обусловливает его противовоспалительный и иммуномодулирующий эффект. Если иммунная теория патогенеза ограниченной склеродермии является главной, то назначение препарата оправданно.
Применение при разных видах ограниченной склеродермии
M. Řiháček и соавт. [1] описали фармакокинетические и фармакодинамические характеристики метаболитов метотрексата, который является антионкологическим препаратом и применяется для лечения тяжелых процессов, в том числе детского острого лимфобластного лейкоза и хориокарциномы.
Низкие дозы метотрексата используют при ревматоидном артрите, псориазе, системном склерозе и других аутоиммунных заболеваниях.
Побочные эффекты данного препарата хорошо изучены и описаны. Однако их появление может быть непредсказуемым из-за отсутствия специфических биомаркеров токсичности.
Уровень метотрексата в плазме должен регулярно контролироваться при помощи проведения лабораторных анализов.
S. Kafaja и соавт. [2] предположили, что уплотнение кожи является одним из ранних проявлений системного склероза и оказывает большое влияние на качество жизни больных. В связи с этим они рекомендовали применять метотрексат на начальном этапе диффузного кожного заболевания.
J.S. Mertens и соавт. [3] исследовали эффективность и безопасность метотрексата у 107 взрослых, страдавших ограниченной склеродермией. Через один и два года 26 и 63% больных соответственно прекратили терапию в связи с ремиссией процесса. Из-за неэффективности в течение первого года препарат был отменен только в 24% случаев. Пациенты с поверхностной ограниченной склеродермией в отличие от лиц с другими формами ограниченной склеродермии труднее соглашались на такое лечение. Чтобы свести к минимуму неэффективность метотрексата при ограниченной склеродермии, наиболее важными мерами признаны назначение фолиевой кислоты и уменьшение времени отсрочки с лечением.
S.B. Couto и соавт. [6] использовали метотрексат при лечении пациентки с почечным синдромом в качестве первого проявления ювенильной системной склеродермии с фокально-сегментарным гломерулосклерозом. В 12 лет у больной развился стероидочувствительный почечный синдром. В 14 лет появились отеки орбитальных областей и нижних конечностей, склеродактилия. Пациентка получала 25-гидроксивитамин D (800 МЕ/сут), метотрексат (0,5 мг/кг/нед) и амлодипин (0,15 мг/кг). Преднизолон в дозе 60 мг/м 2 /сут вводили в течение четырех недель, затем через день по 40 мг/м 2 в течение двух месяцев со снижением дозы в течение четырех месяцев. По окончании терапии пациентка продолжила получать метотрексат 15 мг/нед. Отеков и протеинурии не зафиксировано.
M. Spalek и соавт. [7] сделали обзор литературы с 1989 г. в отношении 66 случаев склеродермии, вызванной радиацией. Необходимо отметить, что склеродермия, вызванная радиацией, – редкое осложнение после радиотерапии. Она часто неправильно диагностируется – как другие дерматологические заболевания или злокачественные новообразования, поскольку имеет сходные клинические характеристики. Методы лечения данной патологии неизвестны. Обычно применяются топические и системные глюкокортикостероиды, ингибиторы кальциневрина, системные супрессанты, такие как метотрексат, такролимус, гепарин, гиалуронидаза, системные антибиотики, Имиквимод, микофенолата мофетил, фототерапия (UVA, UVA1, UVB, PUVA), фотофорез.
За последнее время в клинике им. В.Г. Короленко комплексное лечение с метотрексатом получил 41 пациент. У 15 женщин и пяти мужчин диагностирована распространенная форма ограниченной склеродермии. У 12 пациенток в анамнезе – оперативное вмешательство по поводу онкопроцесса разной локализации. Девять мужчин страдали аденомой предстательной железы. У таких пациентов существует ограничение для применения глюкокортикостероидов и физиотерапии, в связи с чем был назначен метотрексат. Метотрексат вводили внутримышечно в дозе 10–15 мг в зависимости от веса пациента. Курс терапии предполагал не менее десяти инъекций. Его можно было повторить через четыре-пять месяцев. Уже после первого курса наблюдалось уменьшение активности кожного процесса, площади очагов склеротических изменений и отсутствие новых высыпаний.
Клинический случай
Под нашим наблюдением находилась пациентка Г., 67 лет. Больна предположительно в течение трех лет. Именно тогда появились высыпания на коже передней поверхности правой голени и ограничение движения в голеностопном и коленном суставах. За это время получила пять курсов комбинированной терапии (пенициллин, сосудистые препараты, топические глюкокортикостероиды).
С марта по апрель 2018 г. принимала преднизолон в дозе 40 мг/сут с постепенным снижением дозы и ультрафонофорез с гидрокортизоном на очаги поражения. Однако кожный процесс не регрессировал, появились новые высыпания.
Пациентке были назначены внутримышечные инъекции метотрексата 20 мг один раз в неделю под контролем лабораторных показателей. В дальнейшем доза метотрексата снижалась до 7,5 мг.
Общая длительность терапии – 18 недель.
На фоне лечения отмечался регресс высыпаний и практически полное восстановление подвижности правого коленного сустава (рис. 1 и 2).
Метотрексат показан в комплексной терапии распространенных форм ограниченной склеродермии. В тех случаях, когда применение глюкокортикостероидов или физиотерапии невозможно, он остается единственным эффективным методом лечения.
Владельцы патента RU 2627153:
Изобретение относится к медицине, а именно к дерматологии, и может быть использовано для лечения очаговой склеродермии. Для этого на очаги поражения воздействуют низкоэнергетическим лазерным излучением инфракрасного диапазона частотой следования импульсов - 1500 Гц, длительностью импульса 110-160 нс, импульсной мощностью 4-6 Вт/имп, по 1-3 минут на поле. Общая продолжительность воздействия составляет не более 15 минут. Непосредственно перед воздействием лазерным излучением на очаги склеродермии накладывают гель для тела NOLLA naturelle®. При этом воздействие лазерным излучением чередуют через день с аппликациями парафина на очаги склеродермии, температурой 48-52°C, временем 20 минут. Курс лечения составляет 8-10 комплексных процедур. Способ обеспечивает многофакторное воздействие на все звенья обменных процессов в патологически изменённых фиброзированных кожных очагах при снижении побочных эффектов и противопоказаний к проведению лечения. 2 пр.
Изобретение относится к медицине, а именно к физиотерапии, дерматологии, медицинской реабилитации и предназначено для лечения очаговой склеродермии.
В основе патогенеза очаговой склеродермия лежат несколько основных механизма: сосудистые изменения, активация иммунной системы и нарушение ее регуляции, а также изменения в метаболизме коллагена и фибробластов. Современные принципы терапии при локальной склеродермии предполагают назначение различных групп лекарственных средств (метотрексата, глюкокортикостероидов, такролимуса, циклоспорина, иматиниба, микофенолата мофетила, ретиноидов и др.), а также проведение физиотерапевтического лечения.
Все же разнообразие методов лечения в данном случае не всегда приводит к должному клиническому эффекту. Так, из уровня техники известны различные схемы применения лекарственных средств для лечения очаговой склеродермии: метотрексат - наиболее широко используемый препарат; глюкокортикостероиды, применяемые в виде как пероральной, так и наружной формы. В качестве топической терапии чаще всего назначают метилпреднизолона ацепонат, бетаметазон, клобетазола пропионат в виде аппликаций, курс лечения 4-12 недель, или окклюзионных повязок, курс 2-3 недели. (Шостак Н.А. и др. Локализованная (очаговая) склеродермия в общей медицинской практике. Лечебное дело. - 2015 г. - №4. - С. 45-52). Возможно применение антигипоксантов и антиоксидантов (Старовойтова М.Н. Опыт применения актовегина при очаговой склеродермии // Современная ревматология. - 2011 г. - №3. - С. 42-45).
Другим перспективным направлением лечения очаговой склеродермии является физиотерапия в комплексе с лекарственными средствами с учетом формы заболевания и возраста больных.
Достаточно известен способ лечения очаговой склеродермии, включающий применение гиалуронидазы в очагах склеродермии, путем ультрафонофореза (Диденко И.Г. Терапевтическая эффективность ультразвука и фонофореза лидазы при различных формах склеродермии. Вестник Дерматологии и венерологии. - 1978 г. - №6. - С. 76-79) или электрофореза (Ананьева К.А. и др. Новый метод лечения различных форм склеродермии электрофорезом с лидазой. Методики по диагностике, лечению и профилактике заболеваний, разработанные и усовершенствованные в МОНИКИ им. М.Ф. Владимирского. М.: 1970 г. - С. 148-149). Однако применение гиалуронидазы не всегда высокоэффективно при данной патологии: клинический эффект ограничивается одним-двумя месяцами, а также возможны аллергические реакции. В настоящее время отмечается высокий рост числа аллергических реакций, который отчасти связан с применением лекарственных средств, в том числе ферментных (согласно сводным данным по ряду стран, лекарственная аллергия встречается у 8-12% больных). Смертность от осложнений лекарственной терапии вышла на 4-е место в мире. Во многих странах функционируют национальные центры по контролю безопасности лекарств, работа которых координируется ВОЗ. В ее базе данных имеется около 2 млн сообщений о нежелательных побочных эффектах лекарств. Ежегодно поступает около 200000 сообщений из разных стран, причем по свидетельству многих авторов, это количество постоянно растет. При использовании лонгидазы такие реакции также отмечались. С учетом важной роли микроциркуляторных нарушений, носящих системный характер, в развитии патологического процесса при очаговой склеродермии, действия лонгидазы недостаточны. Все это ограничивает продолжительность ремиссии после курса лечения, предложенного в данной и аналогичных методиках, до одного-двух месяцев.
Пероральный прием фотосенсибилизирующих препаратов ограничен у больных, имеющих выраженную дисфункцию печени и почек, катаракту, афакию. При этом наружное применение псораленов в виде спиртовых растворов и кремов вызывает трудности при наличии у больных распространенных поражений кожи.
Из уровня техники известен способ лечения очаговой склеродермии с помощью ультразвуковой терапии (Волнухин В.А. Федеральные клинические рекомендации по ведению больных локализованной склеродермией. - М.: 2013 г. - 21 с.), включающий в себя озвучивание очагов поражения с частотой колебаний 880 кГц, интенсивностью 0,05-0,8 Вт/см 2 , экспозицией 5-10 мин на поле, по лабильной методике в непрерывном или импульсном режиме. Курс составляет 10-15 ежедневных процедур. Лечение ультразвуком эффективно на начальных стадиях заболевания, но при интенсивном склерозировании очага необходимо повышение мощности воздействия, что может привести к подавлению регенерации кожи, поэтому данный способ воздействия нельзя считать оптимальным.
Оптимальным является выбор фактора физиотерапевтического воздействия, лишенного вышеуказанных осложнений. Так, известно, что низкоинтенсивная лазерная терапия способна стойко улучшить микроциркуляцию в очагах склеродермии. В отдельных работах показана эффективность применения низкоинтенсивной лазерной терапии в комплексном лечении ограниченных форм локализованной склеродермии (Волнухин В.А. и др. Опыт применения сочетанных методов низкоинтенсивной лазеротерапии при лечении заболеваний с проявлениями склероза и атрофии кожи // Лазерная медицина. - 1997 г. - Том 2. - №1. - С. 12-15).
В результате проведенного патентно-информационного поиска был выявлен наиболее близкий по технической сущности к предлагаемому изобретению способ лечения очаговой склеродермии (Гайдина Т.А. Фотофорез лонгидазы в восстановительном лечении ограниченной склеродермии // Дис. канд. мед. наук - 2011 г. - 107 с.), заключающийся в воздействии на очаги поражения низкоэнергетическим лазерным излучением инфракрасного диапазона, частотой следования импульсов 1500 Гц, длительностью импульса 110-160 нс, импульсной мощностью 4-6 Вт/имп, по 1-3 мин на поле, общей продолжительностью воздействия не более 15 мин, на курс - 15 ежедневных процедур.
Применение низкоинтенсивного лазерного излучения позволяет добиться противовоспалительного эффекта, улучшения периферического кровообращения; активации обменных и трофических процессов, метаболизма биологически активных веществ, стимуляции ряда защитных механизмов (фагоцитоз и др.), но, в целом, данный способ обладает и существенными недостатками. Так, известно, что низкоэнергетическое лазерное излучение рекомендуется назначать больным с очаговой склеродермией в стадию стабилизации процесса (Гайдина Т.А. Фотофорез лонгидазы в восстановительном лечении ограниченной склеродермии. // Дис. канд. мед. наук - 2011 г. - 107 с.), тогда как для достижения стабилизации применение только низкоэнергетического лазера недостаточно.
Таким образом, существует потребность в способе лечения очаговой склеродермии, лишенном недостатков вышеуказанных аналогов.
Техническим результатом настоящего изобретения является повышение эффективности лечения больных с очаговой склеродермией за счет комбинированного воздействия низкоэнергетической лазерной терапии с аппликациями геля для тела NOLLA naturelle® и парафинотерапии с оптимальными параметрами.
Этот технический результат достигается тем, что в предлагаемом способе лечения больных, включающем воздействие на очаги поражения низкоэнергетическим лазерным излучением инфракрасного диапазона, частотой следования импульсов - 1500 Гц, длительностью импульса 110-160 нс, импульсной мощностью 4-6 Вт/имп, по 1-3 минуте на поле, общей продолжительностью воздействия не более 15 минут, непосредственно перед воздействием лазерным излучением на очаги склеродермии накладывают аппликации геля для тела NOLLA naturelle® и чередуют через день воздействие лазерным излучением с аппликациями парафина на очаги склеродермии, температурой 48-52°, временем 20 мин; курсом лечения 8-10 комплексных процедур.
Предлагаемый способ осуществляют следующим образом.
Перед воздействием лазерным излучением на предварительно очищенные мягким моющим средством очаги склеродермии накладывают аппликации геля для тела NOLLA naturelle®. Оказывают воздействие на очаги поражения низкоэнергетическим лазерным излучением инфракрасного диапазона с помощью установки низкоэнергетического лазерного воздействия, частотой следования импульсов 1500 Гц, длительностью импульса 110-160 нс, импульсной мощностью 4-6 Вт/имп, по 1-3 минуте на поле, общей продолжительностью воздействия не более 15 мин, чередуют через день воздействие лазерным излучением с аппликациями парафина на очаги склеродермии, температурой 48-52°С, временем 20 мин, курсом лечения 8-10 комплексных процедур. Одна процедура в комплексном лечении включает в себя низкоэнергетическое лазерное воздействие через аппликации геля NOLLA naturelle® и воздействие парафиновыми аппликациями, т.е. занимает 2 дня.
Помимо выраженного дефиброзирующего действия, сопоставимого и существенно превышающего эффективность лонгидазы, аппликации парафина оказывают тепловое действие, которое переходит в другие виды энергии в организме больного, что улучшает его биоэнергетический потенциал.
Температура является важным естественным стимулирующим фактором, необходимым для поддержания теплового баланса человека, а воспринимающие его рецепторы находятся как на периферии, так и в центральной нервной системе. Этим можно объяснить влияние аппликаций парафина и на некоторые системы организма, не вовлеченные в процесс тепловосприятия, такие как иммунная, эндокринная и др. Диапазон температур парафиновых аппликаций - 48-52°С - оптимально способствует возрастанию внутрикожного, мышечного кровотока, а также увеличению кислородного транспорта, что активирует процессы репарации кожи.
Аппликации парафина оказывают выраженное механическое действие (при застывании парафин кристаллизуется, а его объем, уменьшаясь, способствует компрессии поверхностных тканей), что эффективно усиливает лимфатический дренаж, способствуя детоксикации организма.
Для регенерации кожи важным является наличие в геле микро- и макроэлементов, аминокислот, витаминов в соотношении и количествах, близких к суточной потребности организма человека, без которых восстановление патологически измененных тканей невозможно.
Таким образом, процедуры низкоэнергетического лазерного излучения с аппликациями геля для тела NOLLA naturelle®, чередующиеся с парафинотерапией, обладающей оптимально выбранным температурным диапазоном, способствуют существенному повышению эффективности лечения очаговой склеродермии. Такое многофакторное воздействие охватывает все звенья обменных процессов в патологически измененных фиброзированных кожных очагах. Гуморальное действие биологически активных веществ, оказывет общее воздействие на организм больного, стимулируя ряд защитных механизмов, которые существенно потенциируются активными компонентами геля. Кроме того, компоненты геля для тела NOLLA naturelle® являются достаточно гипоаллергенными.
Пример 1. Больная Л., 83 года, больна 1,5 года. Жалобы на наличие высыпаний в области живота, бедер и ягодиц, сопровождающихся зудом и чувством стягивания кожи. Считает себя больной с 2015 г., когда впервые заметила появление пятен розового цвета на коже бедер и ягодиц. В марте 2016 г. заметила появление новых пятен в области живота и появление участков уплотнения в прежних бляшках. Госпитализирована в отделение дерматовенерологии и дерматоонкологии ГБУЗ МО МОНИКИ им. М.Ф. Владимирского для дальнейшего обследования и лечения.
При обследовании отмечались патологический кожный процесс подостровоспалительного характера, распространенный и несимметричный. Локализован на коже в областях живота, бедер и ягодиц и представлен сиренево-розовыми отечными пятнами размером 2-10 см. В центре некоторых из них визуализируются участки атрофии желтовато-белого цвета с гладкой блестящей поверхностью. При обследовании выявлена эозинофилия, при этом антитела Scl-70 не обнаружены. Гистологическое исследование: периваскулярные воспалительные инфильтраты в ретикулярном и подкожном слоях дермы, отек верхнего слоя дермы. В биоптате преобладают клетки лимфоцитов, гистиоцитов, а также эозинофильных гранулоцитов.
Диагноз: Бляшечная склеродермия, индуративно-атрофическая форма, впервые выявленная.
Больная Л., помимо стандартной лекарственной терапии получала лечение по предлагаемому способу. Непосредственно перед воздействием лазерным излучением на очаги склеродермии накладывали аппликации геля для тела NOLLA naturelle®. При этом воздействие на очаги поражения осуществляли низкоэнергетическим лазерным излучением инфракрасного диапазона, частотой следования импульсов 1500 Гц, длительностью импульса 110-160 нс, импульсная мощностью 5 Вт/имп, по 1-3 минуты на поле. Общая продолжительность воздействия составила 15 минут. Воздействие лазерным излучением чередовали через день с аппликациями парафина на очаги склеродермии, температурой 48°С, временем 20 мин. Таким образом, одна комплексная процедура включала в себя низкоэнергетическое лазерное воздействие через аппликации геля NOLLA naturelle® и воздействие парафиновых аппликаций. Курс лечения составил 8 комплексных процедур за 16 дней.
После курса комплексного лечения у больной Л. отмечено улучшение в виде разрешения высыпаний, практически полного разрешения плотности в очагах, зуд и чувство стягивания пациентку не беспокоят. Больной было проведено контрольное гистологическое исследование, при этом отек уменьшился, структура слоев дермы близка к нормальной.
Контрольный осмотр через 6 месяцев показал устойчивую ремиссию заболевания.
Диагноз: Линейная склеродермия, впервые выявленная.
Больной М., помимо стандартной лекарственной терапии получал лечение по предлагаемому способу. После наложения аппликаций геля для тела NOLLA naturelle® на очаги склеродермии воздействовали в этих зонах поражения низкоэнергетическим лазерным излучением инфракрасного диапазона, частотой следования импульсов 1500 Гц, длительностью импульса 110-160 нс, импульсной мощностью 6 Вт/имп, по 1-3 минуты на поле. Общая продолжительность воздействия составила 15 минут. Воздействие лазерным излучением чередовали через день с аппликациями парафина на очаги склеродермии, температурой 50-52°С, на подбородке - 48°С, временем 20 мин. Таким образом, одна комплексная процедура включала в себя низкоэнергетическое лазерное воздействие через аппликации геля NOLLA naturelle® и воздействие парафиновых аппликаций. Курс лечения составил 10 комплексных процедур в течение 20 дней.
После курса комплексного лечения у больного М. отмечено улучшение в виде разрешения высыпаний, практически полного разрешения венчиков гиперемии, значительного размягчения бляшек, уменьшения чувства стягивания. Больному было проведено контрольное гистологическое исследование: отек значительно уменьшился, структура слоев дермы близка к нормальной, отмечаются единичные утолщенные пучки коллагеновых волокон в соединительной тканей.
Таким образом, предлагаемый способ позволяет повысить эффективность лечения больных с очаговой склеродермией за счет тщательно подобранного комбинированного воздействия низкоэнергетической лазерной терапии с аппликациями геля для тела NOLLA naturelle® и парафинотерапии с оптимальными параметрами. Способ прост, экономичен и практически лишен побочных эффектов и противопоказаний.
Способ лечения очаговой склеродермии, включающий воздействие на очаги поражения низкоэнергетическим лазерным излучением инфракрасного диапазона, частотой следования импульсов 1500 Гц, длительностью импульса 110-160 нс, импульсной мощностью 4-6 Вт/имп, по 1-3 мин на поле, общей продолжительностью воздействия не более 15 минут, отличающийся тем, что непосредственно перед воздействием лазерным излучением на очаги склеродермии накладывают аппликации геля для тела NOLLA naturelle® и через день чередуют воздействие лазерным излучением с аппликациями парафина на очаги склеродермии, температурой 48-52°C, временем 20 мин, курсом лечения 8-10 комплексных процедур.
Очаговая склеродермия – это хроническое прогрессирующее аутоиммунное заболевание соединительной ткани, характеризующееся появлением на различных участках тела очагов локального воспаления (эритемы и отека), с последующим формированием в них склероза и/или атрофии кожи и подкожной жировой клетчатки. Данная патология встречается у представителей любой расы. Женщины болеют чаще, чем мужчины (2,7:1). Заболевание может возникать в любом возрасте, даже у новорожденных, начинаясь без какой-либо симптоматики и ухудшения общего состояния. Согласно эпидемиологическим данным, очаговая склеродермия (см. фото №1) занимает второе место по распространённости среди аутоиммунных заболеваний соединительной ткани. За последнее десятилетие увеличилась тенденция к более агрессивному течению данной патологии, что, возможно, связано с несоблюдением норм диспансеризации и сроков лечения.
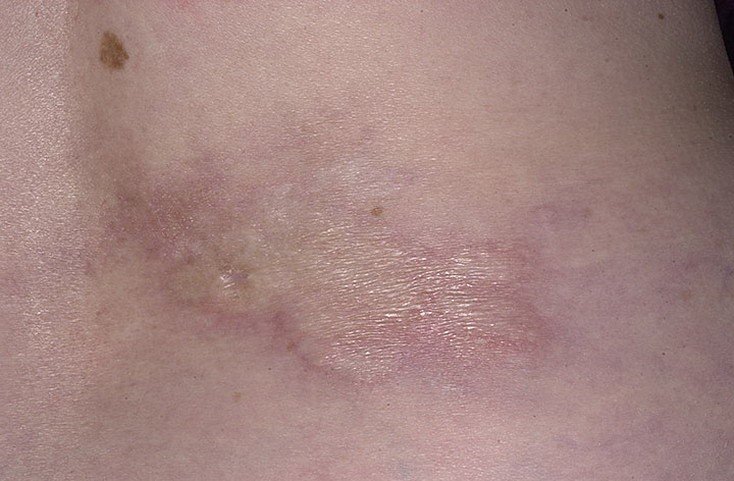
Очаговая склеродермия(фото№1)
У больных со склеродермией всегда есть риск перехода локализированного процесса в системный. Выделяют четыре основных прогностические фактора, которые говорят о вероятности диффузного течения данного заболевания, а именно:
- Дебют заболевания в возрасте до 20 лет или после 50 лет;
- Множественная бляшечная или линейная формы заболевания;
- Локализация очагов поражения над суставами конечностей;
- Дисиммуноглобулинемия.
В Юсуповской больницы диагностикой и лечением различных аутоиммунных заболеваний соединительной системы занимаются врачи-ревматологи. Для своевременного обследования и проведения дальнейшего лечения клиника оснащена мощной диагностической базой, которая представлена целым рядом инновационного медицинского оборудования европейского образца. В дневном стационаре клиники пациент сможет пройти быстро и комфортно все необходимые процедуры, минуя часовые стояния в очереди.
Очаговая склеродермия: этиология и патогенез
В большинстве случаев причины возникновения очаговой склеродермии остаются неизвестные. В патогенезе заболевания основную роль играют аутоиммунные нарушения, повышение синтеза и отложение в коже и подкожной жировой клетчатке коллагена и других компонентов соединительной ткани, микроциркуляторными расстройствами. Шифр по очаговой склеродермии по Международной классификации болезней МКБ-10соответствует L94.0
Очаговая склеродермия: классификация
На данном этапе общепринятой классификации не разработано. Наиболее приемлема классификация С.И. Довжанского (1979) очаговой склеродермии (см. фото № 2) у взрослых, которая включает в себя все клинические формы:
- Бляшечная склеродермия; очаговая, узловатая;
- Линейная склеродермия;
- Генерализованная склеродермия
- Глубокая склеродермия;
- Пансклеротическая склеродермия;
- Буллезная склеродермия;
- Идиопатическая атрофодермия Пазини-Пьерини;
- Прогрессирующая гемиатрофия лица Парри-Ромберга;
- Склероатрофический лихен.

Очаговая склеродермия (фото №2) у взрослого. Линейная форма.
Очаговая склеродермия: клиническая картина
Клиническая картина очаговой склеродермии разнообразна. Больные на приеме у врача-ревматолога могут предъявлять жалобы на зуд, болезненность, чувство покалывания и стянутости кожи, ограничение движения в суставах, деформацию пораженных участков кожи.
Классически принято выделять три стадии развития данной патологии соединительной ткани:
- Эритема (отек) – появление покраснения кожи в области поражения;
- Склероз – появление уплотнения кожи;
- Атрофия кожи – истончение кожи и подкожно-жирового слоя.
Наиболее распространенной формой очаговой склеродермии является бляшечная склеродермия, которая характеризуется появлением на туловище или конечностях очагов эритемы и индурации (уплотнение) кожи. Центр очагов со временем светлеет, приобретает оттенок слоновой кости, и все больше затвердевает. Процесс склерозирования продолжается пока не сформируется блестящий атрофический пласт. В течение месяца он разрешается, приобретая коричневатую гиперпигментацию.
При узловатой склеродермии появляются единичные или множественные узелки, внешне похожие на келоидные рубцы. Как правило, они появляются у больных, не имеющих склонности к развитию келоидов. Кожа в области склеродермии имеет телесный цвет.
При линейной склеродермии на кожи появляются очаги эритемы линейной формы. Характерная локализация очагов по ходу сосудисто-нервного пучка или на одной половине тела.
Очаговая склеродермия: диагностика
Диагностика очаговой склеродермии основывается на данных анамнеза заболевания, анамнеза жизни, жалоб и клинической картине заболевания. Данную патологию следует лечить и наблюдать у врача-ревматолога. Для исключения сопутствующих заболеваний и противопоказаний пациент должен быть проконсультирован следующими специалистами:
- Терапевтом;
- Кардиолог;
- Эндокринологом;
- Гинекологом;
- Невропатологом;
- Гастроэнтерологом;
- Отоларингологом.
Для уточнения активности патологического процесса, а также исключения системной гипертермии назначают проведение следующих исследований:
- Лабораторные обследования: ОАК, ОАМ, биохимический анализ крови;
- Гистологическое исследование кожи;
- Определение в крови антинуклеарного фактора;
- УЗИ органов брюшной полости, почек, щитовидной железы;
- ЭКГ;
- Рентгенография грудной клетки;
- Компьютерная томография;
- Магнитно-резонансная томография.
Очаговая склеродермия: лечение
Лечение очаговой склеродермии в Юсуповской больнице подбирается в индивидуальном порядке каждому пациенту в зависимости от формы, стадии и тяжести течения заболевания, а также локализации очагов поражения. Терапия при данном заболевании соединительной ткани должна быть направлена на:
- Снижение активности патологического процесса и прогрессирование заболевания;
- Уменьшение площади поражения кожи и выраженность клинических симптомов заболевания;
- Предотвращение развития осложнений;
- Улучшение качества жизни больных.
При наличии сгибательных контрактур, деформаций скелета и косметических дефектов кожи необходима консультация хирурга для решения вопроса о проведении хирургической коррекции.
Больные с активным, быстро прогрессирующим течением заболевания показано введение в медикаментозную терапию глюкокортикостероидных препаратов системного действия.
Больным с тяжелыми формами очаговой склеродермии со сформированными глубокими поражениями кожи и подлежащих тканей назначают цитостатические препараты (метотрексат) в виде монотерапии или в комбинации с глюкокортикоидными препаратами системного действия. Иногда может наблюдаться спонтанный регресс склерозирующего процесса кожи или полное разрешение очагов поражения.
В Юсуповской больнице ведущие специалисты с многолетним стажем работы ведут пациентов с различными формами очаговой склеродермии. В стенах стационара пациент окунется в комфортабельную и уютную атмосферу, благодаря профессиональной работе высокоспециализированного медицинского персонала. После курса лечения для каждого больного разрабатывается программа реабилитации. Звоните по телефону для записи на прием к врачу-ревматологу.
Читайте также:


