Гигантоклеточная опухоль коленного сустава лечение
Гигантоклеточная опухоль — распространенная онкологическая болезнь, с которой чаще всего сталкиваются люди в возрасте от 15 до 40 лет. Заболевание характеризуется доброкачественным течением, а сама опухоль образуется в тканях костей.
С другой стороны, под воздействием некоторых факторов возможно злокачественное перерождение, которое чревато опасными последствиями. Так что представляет собой недуг и на какие симптомы стоит обращать внимание?
Что такое остеобластокластома? Особенности строения
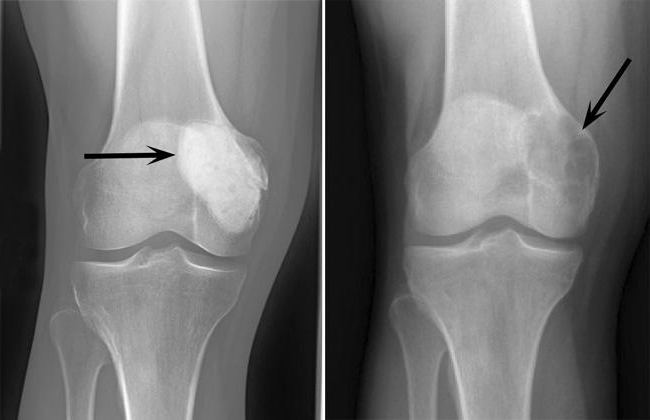
Гигантоклеточная опухоль представляет собой довольно специфическую структуру, которая образуется в костных тканях. Известно, что остеобластокластома состоит из двух типов клеток: мелких одноядерных (клетки округлой или овальной формы со светлым ядром и небольшим количеством хроматина) и гигантских многоядерных (содержат 20-30 ядер и внешне напоминают нормальные остеокласты; они равномерно распределены в толще новообразования и изолированы друг от друга).
В разрезе можно увидеть, что внутри опухоли имеется мягкая ткань бурого цвета со следами мелких геморрагий (кровоизлияний) и некроза.
Классификация новообразований
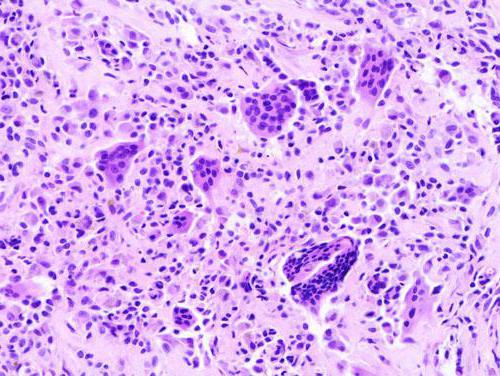
В современной медицине подобные новообразования классифицируют в зависимости от структуры, формы и прочих характеристик. Если говорить об особенностях строения, то гигантоклеточная опухоль может быть:
- ячеистой (состоит из мелких ячеек, разделенных неполными костными перегородками);
- кистозной (опухоль представляет собой полость в кости; она заполнена жидкостью, поэтому внешне напоминает кисту);
- литическая (это агрессивный вид опухоли, рост которой сопровождается быстрым разрушением костных тканей; специфический костный рисунок определить невозможно).
Во время диагностики обращают внимание и на локацию новообразования. Опухоль может быть центральной (образуется в толще кости) или периферической (поражает поверхностные костные структуры и надкостницу).
Примерно в 50 % случаев новообразование располагается в тканях костей вокруг коленного сустава. Часто опухоль обнаруживают в дистальной части лучевой кости. Тем не менее остеобластокластома может поражать практически любую кость, включая позвонки, крестец, большеберцовую, бедренную и плечевую кость, нижнюю челюсть. Иногда патологический процесс распространяется на сухожилия и мягкие ткани.
Основные причины развития заболевания
К сожалению, на сегодняшний день причины появления и роста опухоли неизвестны. Считается, что имеет место наследственный фактор, особенно если закладка и развитие костного аппарата ребенка с самого начала протекали неправильно.
Некоторые специалисты утверждают, что вероятность развития гигантоклеточной опухоли возрастает в том случае, если у пациента имелись воспалительные заболевания, затрагивающие кость и надкостницу. К факторам риска также можно отнести частые переломы и прочие травмы опорного аппарата.
На какие симптомы стоит обратить внимание?
На начальных этапах развития гигантоклеточная опухоль редко дает о себе знать. К ранним признакам можно отнести лишь ноющую боль, которая возникает периодически. Более выраженные симптомы возникают в результате интенсивного роста новообразования.
Костная ткань начинает разрушаться. Возможны спонтанные переломы в месте локализации новообразования. По мере роста опухоли под кожей появляется припухлость, иногда с четкими очертаниями. На наружных покровах в области поражения прорисовывается сетка сосудов.
Если новообразование расположено близко к суставу, то возможна частичная или полная потеря его подвижности. Болезненность также становится более выраженной — дискомфорт беспокоит пациента и во время физической активности, и в состоянии покоя.
Злокачественный процесс и его признаки
Гигантоклеточная опухоль кости считается сравнительно безопасной. Тем не менее всегда существует риск злокачественного перерождения новообразования. На сегодняшний день точные причины, запускающие процесс, неизвестны. Некоторые ученые считают, что виной всему - изменения гормонального фона и частые травмы. Есть врачи, которые утверждают, что перерождение является результатом ранее проведенной лучевой терапии.
В любом случае стоит понимать, что злокачественное новообразование опасно. Кстати, процесс сопровождается рядом симптомов, на которые стоит обратить внимание. Наблюдается интенсивный рост образования. Нередко патологический процесс выходит за пределы кости — в таких случаях образуется гигантоклеточная опухоль мягких тканей или сухожилий.
Во время обследования можно опередить изменение структуры новообразования — оно становится литическим, костные перемычки между ячейками исчезают, контуры кистозной опухоли становятся размытыми. Увеличивается диаметр очага поражения — недуг сопровождается интенсивным разрушением костной ткани.
Диагностические процедуры
Наличие тех или иных симптомов должно натолкнуть врача на мысль о наличии ракового заболевания. Разумеется, гигантоклеточная опухоль требует тщательной диагностики. После сбора анамнеза пациенту назначают:
- Биохимический анализ крови, который позволяет не только проверить работу всего организма, но и обнаружить маркеры, свидетельствующие о разрушении костной ткани.
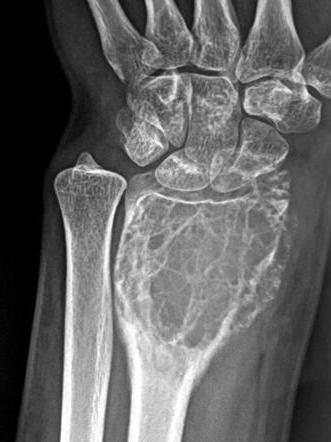
- Обязательным является рентгенологическое исследование. На снимках врач может увидеть опухоль, оценить ее размеры, изучить состояние кости. Оборудование для подобной диагностики имеется практически в каждой больнице, да и стоимость процедуры доступная.
- Самым информативным методом является магнитно-резонансная томография (столь же точные результаты можно получить с помощью компьютерной томографии). У врача есть возможность определить размеры и структуру опухоли, оценить состояние костной ткани, увидеть имеющиеся метастазы. К сожалению, это достаточно дорогое исследование.
- После обнаружения опухоли рекомендуется биопсия. Во время процедуры врач проводит забор тканей из новообразования — образцы затем отправляются в лабораторию. Анализ биоптата помогает проверить, содержит ли опухоль злокачественные клетки.
На основе полученных данных врач может определить, является ли новообразование опасным, после чего выбрать максимально эффективный способ лечения.
Гигантоклеточная опухоль: лечение
Сразу же стоит сказать, что терапия напрямую зависит от размера новообразования, наличия злокачественного процесса, локации метастазов и т. д.
Удаление гигантоклеточной опухоли обязательно. Во время операции проводится резекция не только новообразования, но и участка пораженной кости. Удаленную часть опорного аппарата заменяют протезом. При воспалении или инфицировании опухоли врач может принять решение об ампутации всей конечности. Если в теле пациента были обнаружены метастазы (например, в легком или печени), то проводится частичное удаление пораженных тканей.
Довольно часто в схему включается лучевая терапия. Такое лечение необходимо в том случае, если опухоль невозможно удалить (например, она образовалась внутри бедренной кости, позвонка или крестца). Облучение проводят и при наличии злокачественного процесса, даже если во время хирургического вмешательства удалось избавиться от всех патологических формирований. В некоторых случаях пациенты осознанно отказываются от резекции кости.
Выбор метода лечения нужно доверить врачу. Для лечения остеобластокластомы применяют дистанционную гамма-терапию, ортовольтную рентгенотерапию, тормозное или электронное излучение.
Гигантоклеточная опухоль: прогноз для пациентов и возможные осложнения

В большинстве случаев прогнозы для больных положительные. Безусловно, новообразование нужно удалить, нередко и вместе с участком пораженной кости. Но рецидивы регистрируются редко.
А вот злокачественная гигантоклеточная опухоль опасна, ведь заболевание сопровождается образованием метастазов, которые могут быть расположены практически в любом органе. Далеко не всегда хирургу удается провести резекцию всех новообразований.
Гигантоклеточная опухоль – это новообразование остеогенной природы. Синоним термина – бурая опухоль, гигантома, остеобластокластома, остеокластома, т. е. опухоль, образованная из клеток, формирующих (остеобласты) и разрушающих (остеокласты) костную ткань. Встречается заболевание у представителей обоих полов с одинаковой частотой, преимущественно у работоспособного населения от 20 до 40 лет.
Локализация патологии — это зона метафиза, а также эпифиза длинных трубчатых костей, расположенных у коленного сустава. Частая локализация – трубчатые кости, чаще всего встречается заболевание большеберцовой или бедренной кости. Нередко диагностируют патологию в челюсти, тазу, плече, позвоночнике.
Доброкачественная или злокачественная?
Современные медики выделяют два типа гигантоклеточной опухоли кости – доброкачественную и злокачественную.
Гигантоклеточная опухоль провоцирует истончение кости, на поздних и запущенных стадиях происходит полноценное разрушение коркового слоя.
О причинах и симптомах
Предполагать от чего образуются опухоли кости или мягких тканей можно, однако до сегодняшнего дня не установлены точные причины их образования.
- Травмы, ушибы.
- Наследственные особенности.
- Предшествующие воспалительные заболевания.
- Гормональные изменения, в т. ч. беременность для женщин, наступление климакса.
- Очаги воспалений в области костной ткани, а также надкостницы.
Те же факторы способствуют малигнизации (перерождению) доброкачественных образований в злокачественные.
Если доброкачественную гигантоклеточную опухоль лечить неправильно, то она преобразуется в злокачественное новообразование. Новообразования с малигнизацией встречаются в 15% случаев, после этого назвать остеокластому доброкачественной уже нельзя.
Заболевание известно медицине давно, но до настоящего времени точные причины ее развития так и не сформулированы.
В зависимости от строения, а также от склонности к росту, выделяется 2 вида остеокластомы:
- Литическая — характеризуется быстрым ростом и значительным разрушением коркового слоя кости.
- Ячеисто-трабекулярная — определена наличием очагов разрушения костной ткани, полость которых разделена перегородками. Данный вид опухоли классифицируется на 2 подвида — активно-кистозную и пассивно-кистозную.
Активно-кистозная не обозначена четкими границами, быстро растет, при этом значительно разрушает корковый слой кости, данный процесс провоцирует веретенообразное раздутие кости. Пассивно-кистозная имеет четкие и ясные границы, не имеет склонности к росту.
Теперь рассмотрим симптомы, обнаружив которые, нельзя пренебрегать походом к врачу и подробным обследованием. Проявления болезни напрямую зависят от конкретного расположения новообразования, в таком и ключе их и разберем.
При локализации в костях черепа гигантоклеточная опухоль чаще всего располагается в нижней челюсти, хотя и верхнее положение не исключено. Нередко обнаруживается у пациентов, начиная с 10 – летнего и до 30-летнего возраста. Формируется опухоль внутри челюстной кости, иногда заключена в фиброзную капсулу.
Кровоснабжение опухоли проходит интерстициально, т. е. между соседними тканями. Такой кровоток вызывает разрушение красных телец крови и гемосидероз – окружающие ткани окрашиваются в бурый цвет из-за избытка железа, подтверждая одно из названий патологии, бурая опухоль. Морфологически любая остеобластокластома состоит из гигантских клеток, напоминающих остеокласты, однако имеющих до 10 ядер в своем строении.
Бессимптомное начало приводит к тому, что пациент не обращается к врачу своевременно. В более поздних стадиях отмечается болезненность при нажатии на пораженную область, незначительная асимметрия лица. Зубы в области гигантомы могут сместиться, стать подвижными.
В области пальцев стоп и кистей, реже в суставах колена, бедра, лодыжки превалирует теносиновиальная гигантоклеточная опухоль, представляющая собой плотный узел, расположенный в мягких тканях, близко от сухожилия. Размеры дольчатого серовато — белого узла могут достигать 4 см. Постепенно гигантоклеточная опухоль сухожилия распространяется на кость сустава, разрушая ее.
Злокачественный вариант данного новообразования встречается крайне редко, но при ее возникновении она протекает подобно низкодифференцированной саркоме с возможными метастазами в легкие и лимфоузлы.
Начальные проявления бессимптомны, позже клинка болезни напоминает картину артрита.
Среди многообразия глиом (опухолей головного мозга) выделяется гигантоклеточная глиома, которая может иметь две формы – доброкачественную и злокачественную. В зависимости от того, в какой области мозга располагается образование, каковы его размеры и степень компрессии на мозг, возникает неврологическая симптоматика.
Среди злокачественных астроцитом встречается гигантоклеточная глиобластома – агрессивная форма, имеющая неблагоприятный прогноз. Любые новообразования мозга проявляются головными болями, нарушениями слуха и зрения, чувствительности, рефлексов. Конкретные признаки опять же зависят от конкретной локализации процесса.
Клиническая картина
Определить момент, когда остеокластома только начала свое развитие, практически невозможно, так как заболевание в начальной стадии не имеет никаких ярко-выраженных симптомов.
Диагностика
Для подтверждения диагноза врач используется следующие методы:
- Сбор анамнеза.
- Визуальный осмотр.
- Пальпация пораженной части тела.
- Рентген исследование (определение локализации новообразования и ее вида).
- КТ или МРТ (исследование глубины поражения костей).
- Биопсия пораженной ткани (чаще всего данный вид исследования назначается перед проведением хирургического лечения).
В международном классификаторе заболеваний (мкб 10) остеобластокластома определена кодом D 16.
Как лечить
Остеобластокластома лечится только хирургическим путем, перед тем, как определить план проведения операции, выясняется вид и локализация опухоли, ее размер.
Методы лечения:
- Удаление в процессе операции участка пораженной кости.
- Химиотерапия.
- Лучевая терапия.
- На 1 и 2 стадиях при остеокластоме малой берцовой кости, ребра, локтя, пяточной кости, а также при остеобластокластоме лопатки проводится сегментарная или же краевая резекция пораженного участка. Операция может быть проведена без замещения дефекта, а также с установлением протеза или же трансплантата.
- На 3 стадии проводится расширенная резекция или удаление всей части пораженной кости. Если в патологический процесс вовлечены сосуды, нервные окончания или обширный участок конечности, а также при наличии признаков инфицирования, проводится ампутация.
После операции показана местная криотерапия, а также электрокоагуляция.
Лучевая терапия показана в следующих случаях:
- для уменьшения риска рецидива;
- на ранних стадиях развития патологии;
- если локализация опухоли находится в труднодоступном для хирургической операции месте (позвоночник);
- при получении от пациента отказа на проведение оперативного лечения.
Важно определить, что эффективность лечения лучевой терапией мала по сравнению с хирургическим вмешательством.
В большинстве вариантов прогноз при гигантоклеточной опухоли благоприятный. Но не стоит забывать и о возможных осложнениях.
Прогноз доброкачественных форм хороший, чего не скажешь о злокачественном варианте. Продолжительность жизни пациентов со злокачественной гигантоклеточной глиобластомой 2 стадии достигает 5 лет, при выявлении на более поздних этапах не превышает 2 года.
Аннотация научной статьи по клинической медицине, автор научной работы — Горячев А. Н., Резник Леонид Борисович, Гейко Алексей Иванович, Еремеев Олег Владимирович, Тютюников Александр Валерьевич
Обобщен опыт лечения 98 больных с гигантоклеточными опухолями дистального отдела бедра и проксимального отдела большеберцовой кости доброкачественного течения. Диагностика основывалась на данных клиники, лучевых методах (рентгенография, КТ, МРТ), а также морфологических данных. Хирургическое лечение состояло в выполнении органосохраняющих операций. Низкая частота рецидивов позволяет считать основным методом лечения гигантоклеточных опухолей костей с доброкачественным течением резекцию опухоли . При литическом характере течения опухоли показана резекция сегмента конечности и замещение его онкологическим эндопротезом .
Похожие темы научных работ по клинической медицине , автор научной работы — Горячев А. Н., Резник Леонид Борисович, Гейко Алексей Иванович, Еремеев Олег Владимирович, Тютюников Александр Валерьевич
Management of giant-cell tumors in the knee
The authors have summed up the experience of treatment of 98 patients with benign giant-cell tumors of distal femur and proximal tibia . The diagnostics was based on clinical and morphological data, as well as on those of radiation methods (roentgenography, CT, and MRT). Operative treatment consisted in making organ-saving surgeries. Low incidence of relapses allows to consider tumor resection as a basic method for treatment of giant-cell bone tumors. Resection of segment and its replacement with oncologic endoprosthesis is indicated in case of lytic tumor process.
Лечение гигантоклеточных опухолей в области коленного сустава
А.Н. Горячев|, Л.Б. Резник, А.И. Гейко, О.В. Еремеев, А.В. Тютюников
Management of giant-cell tumors in the knee
A.N. Goriachev|, L.B. Reznik, A.I. Geiko, O.V. Yeremeyev, A.V. Tutunikov
(главный врач - В.Г. Бережной)
Обобщен опыт лечения 98 больных с гигантоклеточными опухолями дистального отдела бедра и проксимального отдела большеберцовой кости доброкачественного течения. Диагностика основывалась на данных клиники, лучевых методах (рентгенография, КТ, МРТ), а также морфологических данных. Хирургическое лечение состояло в выполнении органосохраняющих операций. Низкая частота рецидивов позволяет считать основным методом лечения гигантоклеточных опухолей костей с доброкачественным течением резекцию опухоли. При литическом характере течения опухоли показана резекция сегмента конечности и замещение его онкологическим эндопротезом. Ключевые слова: гигантоклеточная опухоль, дистальный отдел бедра, проксимальный отдел большеберцовой кости, резекция опухоли, онкологический эндопротез.
The authors have summed up the experience of treatment of 98 patients with benign giant-cell tumors of distal femur and proximal tibia. The diagnostics was based on clinical and morphological data, as well as on those of radiation methods (roentgenography, CT, and MRT). Operative treatment consisted in making organ-saving surgeries. Low incidence of relapses allows to consider tumor resection as a basic method for treatment of giant-cell bone tumors. Resection of segment and its replacement with oncologic endoprosthesis is indicated in case of lytic tumor process. Keywords: giant-cell tumor, distal femur, proximal tibia, tumor resection, oncologic endoprosthesis.
Гигантоклеточные опухоли (Международная гистологическая классификация костных опухолей) являются доброкачественными, но прогрессирующими агрессивными костными новообразованиями. Они состоят из веретенообразных и овоидных клеток с многочисленными гигантскими клетками по типу остеокластов, равномерно распределенных по опухолевой ткани. Опухоль возникает чаще у лиц в возрасте до 30 лет, поражает эпифиз и метафиз трубчатой кости, на их долю приходится до 5 % всех первичных опухолей костей. По данным литерату-
ры, основным методом лечения гигантоклеточ-ных опухолей является хирургический [1, 3]. Применявшееся лучевое лечение [4] в настоящее время практически оставлено вследствие непредсказуемого исхода, длительной перестройки облученных тканей, длительных сроков иммобилизации конечности, ведущих к потере функции коленного сустава.
Цель исследования: изучить ближайшие и отдалённые результаты хирургического лечения больных с гистологически подтверждёнными вариантами гигантоклеточной опухоли.
MАTЕPИАЛЫ И МЕТОДЫ
Под нашим наблюдением находились 98 больных с гигантоклеточными опухолями проксимального отдела большеберцовой и дистального отдела бедренной кости. Первичная диагностика основывалась на данных клиники (боль, припухлость, местное повышение температуры, нарушение функции конечности) и лучевых методов -рентгенография, КТ, МРТ. Дифференциальная диагностика проводилась с аневризмальными и солитарными костными кистами, фиброзной дис-плазией, бурой опухолью гипертиреоидизма и
даже с хондро- и остеогенной саркомой. КТ, МРТ позволяли уточнить локализацию, распространённость опухолевого процесса и состояние стенок костных опухолей, а также спланировать объём и характер оперативного вмешательства (резекция опухоли, сегментарная резекция, ампутация).
Всем больным выполнялась дооперационная биопсия. При выборе методики биопсии пункци-онная и трепанобиопсия подкупают простотой и доступностью, однако малый объем полученного материала и неуверенность в результате морфоло-
гического заключения снижает их значимость. Для получения достоверных результатов морфологического исследования предпочтительна до-операционная открытая биопсия с обязательным поиском наиболее агрессивных участков опухоли. Доступ осуществляли в зоне предполагаемого последующего оперативного вмешательства, под жгутом. Кроме того, для минимизации отрицательных последствий биопсии на окружающие ткани костную полость вскрывали путём выкраивания костного фрагмента с сохранением мягкот-каной ножки. После забора тканей для морфологического исследования место биопсии обрабатывали спиртом и 5 % раствором йода, после чего костный лоскут помещали на место.
При определении характера процесса мы выделяли три основные формы: доброкачественную, литическую и злокачественную [1]. В группе из 98 пациентов, находившихся под нашим наблюдением, доброкачественный характер течения гиган-токлеточной опухоли отмечен у 78 больных, ли-тический - у 12, злокачественный - у 8 больных.
Основными хирургическими методами лечения доброкачественных гигантоклеточных опухолей проксимального отдела большеберцовой и дистального отдела бедренной кости были краевая резекция или резекция в границах опухоли. После расширенного иссечения биопсийного рубца над опухолью откидывали костный фрагмент в виде фартука. Мягкотканный компонент опухоли удалялся с применением кюретажа. Недостатком этого приёма [1] является отсутствие радикальности, поскольку часть опухолевых клеток остается на стенках костной полости. Для усиления санирующего эффекта после выполнения кюретажа полость обрабатывали фрезой, что обеспечивало условную радикальность операции. В случае расположения опухоли в субхондраль-ной зоне вблизи суставного хряща особое внимание уделяли его сохранению. Необходимость такого подхода, на наш взгляд, обусловлена, с одной стороны, желанием сохранить сустав, а с другой - способностью хрящевой ткани блокировать распространение опухоли на элементы сустава, и в своей практике мы не наблюдали такого распространения. После резекции полость промывали физиологическим раствором, вакуу-мировали, обрабатывали спиртом и 5 % раствором йода. Поскольку используемые мероприятия не в состоянии обеспечить достаточного абла-стического эффекта, с целью его достижения нами применялась обработка полости высокам-плитудным низкочастотным ультразвуком частотой 42 кГц. Возникающие в процессе ультразвуковой обработки кавитации, ультразвуковые микропотоки и течения удаляют опухолевые клетки не только с поверхности кости, но и из приповерхностного слоя губчатой кости.
После высокоинтенсивной ультразвуковой обработки полость заполняли пластическим материалом.
Рис. 1. Ультразвуковая обработка полости после резекции опухоли
В группе из 78 больных с доброкачественным характером течения опухолевого процесса всем пациентам операция выполнялась согласно описанной технологии с обязательным применением ультразвуковой обработки полости после выполнения её кюретажа. Для заполнения образовавшейся полости использовали различные материалы.
Современная реконструктивная хирургия располагает разными пластическими материалами для заполнения костных полостей как биологически инертными, включая акриловый костный цемент [3], пористую керамику, пористый никелид титана [5], так и биодеградирую-щими, такими как аутотрансплантаты, деминерализованные аллотрансплантаты, структурные аллотрансплантаты (Tutoplast), ксенотрансплан-таты, кальций-фосфатные комплексы [6], композитные биодеградирующие материалы (Ignite, Miig, Allomatrix, Osteoset).
В случае выявления литического характера опухоли методом выбора для хирургического лечения являлись радикальные операции, заключавшиеся в резекции поражённого сегмента и замещении дефекта онкологическим эндопротезом, либо ампутации. В этой группе нами у 11 больных с литической формой течения выполнено тотальное замещение резекционных дефектов онкологическими эндопротезами. Ещё в одном случае в процессе подготовки к операции произошло озло-качествление опухоли, и в ходе операции было обнаружено метастазирование процесса. Хирур-
гическая тактика была изменена и выполнена ампутация конечности на уровне верхней трети бедренной кости.
У 8 больных с гистологически подтверждённым первично злокачественным течением опухоли выполнены ампутации конечности.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Значительное количество разработанных и применяемых сегодня материалов для замещения полостей, остающихся после внутрикостной резекции гигантоклеточной опухоли, ставит перед ортопедом вопрос о выборе, исходя из преимуществ того или иного материала, показаний к применению, эффективности.
К преимуществам использования костных ау-тотрансплантатов мы отнесли быструю перестройку, невысокий риск развития местных инфекционных осложнений, достаточную механическую прочность. При разрушении опухолью субхондрального слоя аутотрансплантация абсолютно показана для укрепления изнутри суставной поверхности хряща. К недостаткам метода отнесем дополнительную травму при заборе материала и ограниченный объем трансплантата. У 35 больных, прооперированных с применением аутотрансплантатов, отмечен положительный результат с быстрой перестройкой кости.
Использование деминерализованных костных аллотрансплантатов не сопровождается дополнительной травмой и ограничением объема кости, однако прочностные и структурные возможности таких трансплантатов уступают аутокостным. А отсутствие механической прочности, в свою очередь, ограничивает их использование при замещении костных дефектов, особенно субхонд-ральных. Так, у 8 из 11 больных, которым применялась данная методика, в дополнение использовались другие материалы, обладающие механической прочностью
Рис. 2. Больной Ш. Рентгенография правого коленного сустава. Гигантоклеточная опухоль проксимального отдела большеберцовой кости
Рис. 3. Больной Ш. Данные МРТ проксимального отдела большеберцовой кости правой голени. Гигантоклеточная опухоль проксимального отдела большеберцовой кости
Рис. 4. Больной Ш. 16 месяцев после операции. Рентгенография правого коленного сустава. Результаты замещения дефекта и перестройки костной ткани
Рис. 5. Больной Ш. Данные КТ проксимального отдела большеберцовой кости правой голени. Результаты замещения дефекта и перестройки костной ткани
Неорганические материалы использовались нами реже. В случае замещения большого дефекта проксимального отдела большеберцовой кости небиодеградирующими материалами дополнительно использовали аутотрансплантат, размещая его субхондрально, что обеспечивало сохранность хряща. В 10 случаях из 12 имплантаций пористого никелида титана нами применялась такая хирургическая тактика. Применение пористой керамики в 2 случаях также успешно сочетали с костной аутотрансплантацией. С целью иллюстрации такой тактики приводим следующее клиническое наблюдение
Рис. 6. Больной Н. Рентгенография правого коленного сустава. Гигантоклеточная опухоль большеберцовой кости
Рис. 7. Больной Н. Рентгенография правого коленного сустава после операции. Замещение полости аутотрансплан-татом и стержнем из пористого никелида титана
Рис. 8. Больной Н. Рентгенография правого коленного сустава через 18 месяцев после операции. Перестройка костной ткани вокруг имплантата
Таким образом, при поражении субхонд-ральной кости важным элементом хирургического вмешательства мы считаем формирование субхондральной поддержки, сохраняющей целостность плато большеберцовой кости под нагрузкой. Такая технология использовалась нами и в случае применения керамических имплантатов. У больного К. с субтотальным поражением проксимального отдела левой большеберцовой кости (рис. 9.) для замещения дефекта была использована структурированная пористая керамика и аутокостный трансплантат (рис. 10).
Рис. 9. Больной К. Рентгенография левого коленного сустава. Гигантоклеточная опухоль большеберцовой кости
Рис. 10. Больной К. Рентгенография левого коленного сустава после операции. Замещение полости пористой керамикой и костным аутотрансплантатом
Через 4 года произошла остеоинтеграция в керамический трансплантат и перестройка костного аутотрансплантата (рис. 11). Рецидива заболевания не отмечено.
Рис. 11. Больной К. Рентгенография левого коленного сустава через 4 года после операции. Перестройка аутотрансплантата, остеоинтеграция керамики
Больному В. с поражением проксимального отдела большеберцовой кости и разрушением суставного хряща (рис. 12), с гистологически подтвержденной литической формой течения гигантоклеточной опухоли выполнена резекция проксимального отдела большеберцовой кости на длину до 15 см с замещением дефекта индивидуальным онкологическим эндопротезом (рис. 13). Результаты операции оценены нами как удовлетворительные, через год после операции стояние элементов эндопротеза удовлетворительное (рис. 14).
Рис. 12. Больной В. Рентгенография правого коленного сустава. Гигантоклеточная опухоль больше-берцовой кости
Рис. 13. Больной В. Резекция проксимального отдела большеберцовой кости. Имплантация онкопротеза
Рис. 14. Больной В. Рентгенография правого коленного сустава. Результаты онкологического эндопро-тезирования через 1 год после операции
Основной задачей ортопеда при выполнении резекции гигантоклеточной опухоли в проксимальном отделе большеберцовой кости и дис-тальном отделе бедра считаем сохранение функции коленного сустава. Однако на период заживления послеоперационной раны необходима иммобилизация конечности. После снятия швов разрешаются сначала пассивные, а затем активные движения в коленном суставе. Умеренные нагрузки на ногу разрешаются через 4-6 недель с постепенным увеличением.
Таким образом, после резекции опухоли у 98
больных положительные исходы отмечены у 95. Рецидив опухоли имеет место у одного больного, у которого выполнена интраоперационная биопсия, констатировано озлокачествление процесса и в итоге выполнена ампутация на
уровне верхней трети бедренной кости. Ещё у 1 больного выполнена ампутация по поводу септической нестабильности эндопротеза, у 1 больного произошел перелом ножки эндопроте-за, конечность неопорная.
Диагностика и лечение гигантоклеточных опухолей является серьёзной проблемой, обусловленной гистологической вариабельностью их течения, что подтверждает опыт лечения 98 больных с гигантоклеточными опухолями дис-тального отдела бедра и проксимального отдела большеберцовой кости. Такие опухоли характеризуются прогрессирующим агрессивным течением. Диагностика основывается на данных клиники, лучевых методах (рентгенография, КТ,
МРТ) и морфологии. Основным методом лечения при доброкачественном течении процесса являются органосохраняющие операции (краевые и внутриопухолевые резекции кости). Современная реконструктивная ортопедия располагает обширным выбором пластических материалов для заполнения полостей после резекции опухоли, а правильный выбор таких материалов обеспечивает хорошие долговременные результаты.
1. Доброкачественные варианты течения ги-гантоклеточныой опухоли нуждаются в хирургическом лечении в объёме внутрикостной резекции.
2. Для замещения дефектов и полостей, образующихся после удаления опухоли, с положительным результатом могут применяться различные пластические материалы.
3. С целью субхондральной поддержки сус-
тавной поверхности в проксимальном отделе большеберцовой кости рекомендуется использовать костные аутотрансплантаты.
4. Литический вариант течения гигантокле-точной опухоли с истончением кортикального слоя и наличием мягкотканного компонента требует выполнения радикального оперативного вмешательства, включая сегментарную резекцию кости и эндопротезирование.
1. Зацепин С. Т. Костная патология взрослых : руководство для врачей. М. : Медицина, 2001. 638 с.
2. Имамалиев А. С., Хабижанов Б., Жуковский И. Я. Костная ксенопластика. М. : Медицина, 1974. 216 c.
3. Куропаткин Г. В. Костный цемент в травматологии и ортопедии. Самара, 2006. 74 с.
4. Лагунова И. Г. Опухоли скелета. М. : Медицина, 1962. 267 c.
5. Новые технологии в лечении онкопатологии / Г. Ц. Дамбаев [и др.] // Бюллетень ВСНЦ СО РАМН. 2004. № 2(112). C. 64-69.
6. Общие закономерности биотрансформации и остеоинтеграции кальций фосфатных материалов / А. В. Карлов, В. Л. Шахов, И. А. Хлусов, В. И. Савенко // Клинические фундаментальные аспекты травматологии. Томск, 2003. С. 123 -134.
7. Persson B. M., Wouten H. M. Curettage and acryl fixation cement age of surgery on giant cell tumor of bone // J. Bone Joint Surgery. 1976. Vol. 58, No 13. P. 120-125.
Рукопись поступила 07.06.10.
Сведения об авторах:
Читайте также:


