Ювенильный остеопороз что это такое
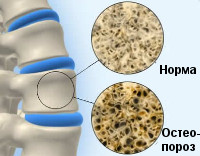
Под остеопорозом мы чаще всего понимаем возрастное нарушение минерального обмена, приводящее к уменьшению минеральной плотности и истончению костей. Однако ювенильный, то есть юношеский, остеопороз уже далеко не редкое явление в современном мире.
Причиной для обращения юных пациентов к специалистам в области остеопороза зачастую являются повторные компрессионные переломы . Остеопороз у детей так же, как и у взрослых, может иметь серьезные последствия, но своевременная диагностика и правильное лечение могут остановить потерю костной массы.
Проблема в том, что остеопороз – это коварное заболевание, которое долго может не проявляться. Детский остеопороз протекает еще более скрытно, чем взрослый. Распознать его можно только после того, как кости уже потеряли значительное количество костной массы и стали склонными к переломам . Исследования показывают, что чаще всего переломы происходят у детей в возрасте с 5 до 7 и с 12 до 15 лет.
Классификация детского
остеопороза
Как и у взрослых, остеопороз у детей также может быть первичным или вторичным. Первичный остеопороз — это когда остеопороз не связан с другими патологиями или приемом каких-либо препаратов, способных оказывать негативное влияние на метаболизм костной ткани.
Вторичный остеопороз — когда он сопутствует заболеваниям эндокринной системы.
Причины развития
остеопороза у детей
Врожденные факторы риска:
1. Генетика. Статистика говорит о том, что от 75% до 85% минеральной плотности костей зависит от состояния костей родителей. При первичном осмотре врач спрашивает, были ли в семье больного ребенка случаи остеопороза или переломов шейки бедра.
2. Внутриутробная патология. Остеопороз у ребенка может возникнуть в следствие недоношенности, несоблюдения матерью режима, гипоксии, куренияи или употребления матерью наркотических средств или ее различных хронических заболеваний.
Внешние факторы:
1. Вскармливание искусственными неадаптированными смесями.
2. Болезни желудочно-кишечного тракта.
3. Различные костные заболевания (рахит, сколиоз и др.)
4. Гормональные нарушения. Понижение уровня стероидных женских гормонов (эстрогенов) уменьшает пик костной массы. Эта причина сходна с механизмом постменопаузального остеопороза у женщин. У мальчиков снижение минеральной плотности костей часто связана с задержкой пубертата и недостаточным уровнем гормона роста.
5. Заболевания обмена веществ (лейкоз, сахарный диабет и др.)
7. Неправильное питание , которое не дает необходимого для костного матрикса количества кальция .
8. Гиподинамия, связанная с малоподвижным образом жизни. Отсутствие физических нагрузок препятствует высокому пику костной массы.
9. Вредные привычки: употребление спиртных напитков и курение.
Симптомы остеопороза
у детей
* Болевой синдром возможен, но не обязателен. Боль, как правило, локализуется в пояснице и носит хронический характер.
* Снижение роста, которое происходит из-за деформации позвонков.
* Костные деформации, например, сутулость, изменения в грудной клетке или плоскостопие.
* Основной симптом – переломы при незначительных нагрузках и падениях. Зачастую это компрессионные переломы позвонков или нижних конечностей.
Диагностика ювенильного остеопороза
1. Осмотр специалиста, сбор анамнеза, в ходе которого выясняется наличие переломов, болевого синдрома, различных факторов, которые могли оказать негативное влияние на формирование минеральной плотности костей и физическую активность.
2. Делается рентгенографический снимок позвоночника и шейки бедра для определения индекса клиновидности, то есть выясняют, как высота вентрального края тел позвонков соотносится с дорсальным краем.
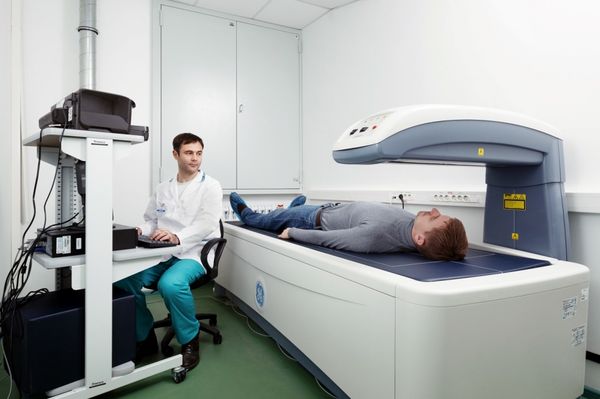
3. Проводится анализ минеральной плотности кости – денситометрия . Эта диагностика при помощи некоторых аппаратов способна показать наличие полостей в костях.
4. Биохимический анализ мочи и крови, который показывает уровни кальция и фосфора, а также маркеры костного образования и резорбции.
Лечение остеопороза
у детей
Важно понимать, что не существует какого-то универсального метода лечения детского остеопороза. Остеопороз – это заболевание, которое связано с нарушением минерального обмена в организме. Поэтому первый шаг в лечении — устранение причин, если это возможно, которые привели к сбою кальциевого обмена.
Физические нагрузки способны значительно повысить плотность костной ткани. Детям с остеопорозом обязательно назначается комплекс упражнений или рекомендуется какой-либо не травмоопасный вид спорта, например, ходьба или плавание.
Диета, которая исключает все жирное и копченое, так как лишний вес провоцирует остеопороз. Обязательными в рационе детей должны быть молочные продукты, особенно это касается детей с остеопорозом. Молоко можно пить до пол-литра в день, не боясь последствий, излишки полностью выводятся с мочой.
Инсоляция, то есть нахождение ребенка на солнце, необходима для выработки витамина D, чтобы кальций всасывался организмом в достаточном количестве.
Остеопороз – хроническое заболевание, поэтому для того, чтобы предотвратить его появление вновь, пациент должен соблюдать такой образ жизни и в старшем возрасте. И не допускать факторов, которые могут вредить усвоению кальция, например, табакокурение или алкогольную зависимость.

Ювенильный остеопороз – это заболевание костной ткани у детей до 18 лет с нарушением костного метаболизма, приводящим к значительному снижению минерализации костей. Проявляется болями различной интенсивности, обычно в поясничном отделе позвоночника. Также характерны частые переломы, в том числе компрессионные переломы тел позвонков. Ювенильный остеопороз диагностируется с учетом анамнеза и клинических данных, подтверждается результатами инструментального обследования скелета. Используются различные рентгенологические методы и биопсия. Лечение комплексное, направлено на повышение степени минерализации костей, устранение болей, профилактику дальнейшего развития заболевания.
МКБ-10
- Причины
- Симптомы ювенильного остеопороза
- Диагностика
- Лечение ювенильного остеопороза
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Ювенильный остеопороз относится к группе первичных остеопорозов, это означает, что патология развивается без видимых внешних причин: эндокринных нарушений, инфекций, ревматических поражений и т. д. Как правило, заболевают дети в возрасте 8-14 лет, что связано со спецификой общего метаболизма и обмена веществ в костной ткани в препубертате. В этот период достигается пик костной массы, и любое уже имеющееся нарушение обмена чаще всего дебютирует на этом фоне. Девочки страдают примерно в два раза чаще мальчиков, что объясняется особенностями гормонального фона.
Всего к настоящему времени в педиатрии описано около 100 случаев ювенильного остеопороза, однако заболевание не теряет своей актуальности, поскольку невозможно устранить причину нарушений костного метаболизма, а значит, лечение часто оказывает только временный эффект. Остеопороз различной этиологии является причиной более половины от общего числа диагностируемых компрессионных переломов тел позвонков. Именно этот перелом значительно осложняет течение заболевания и прогноз для здоровья ребенка. Кроме того, заболеваемость в последние годы неуклонно растет из-за неправильного рациона детей, часто с самого рождения.

Причины
Этиология ювенильного остеопороза в настоящее время неизвестна. Существуют различные врожденные и средовые факторы риска, взаимодействие которых провоцирует развитие симптоматики. В семьях детей, страдающих ювенильным остеопорозом, обнаруживаются случаи частых переломов (в том числе шейки бедра) у родителей и других близких родственников. Обследование показывает, что минеральная плотность костей может быть снижена у братьев и сестер пациента.
Ювенильный остеопороз во многом обусловлен нарушением обмена кальция и фосфора в организме, центральная регуляция метаболизма этих минералов может нарушаться при любом патогенном воздействии во внутриутробном периоде. Что касается факторов внешней среды, здесь большую роль играют:
- заболевания кишечника, поскольку метаболизм кальция тесно связан с ЖКТ, особенно с тонким кишечником, где кальций в норме всасывается в кровь;
- нерациональное питание ребенка;
- гиподинамия, т. к. недостаток физических нагрузок приводит к активации остеокластов, разрушающих костную ткань.
Симптомы ювенильного остеопороза
Долгое время заболевание развивается незаметно для родителей и окружающих ребенка людей. Пациент поначалу желается на быструю утомляемость, особенно в мышцах спины. Чаще всего ребенка беспокоит дискомфорт или боль в пояснице. Характерным для ювенильного остеопороза является волнообразное течение, поэтому неприятные ощущения долгое время то усиливаются, то ослабевают. Болезнь протекает скрыто. Первым симптомом, на который обращают внимание, часто становится перелом костей предплечья, например, лучевой кости. После госпитализации проводится обследование, в ходе которого и выявляется заболевание.
Ювенильный остеопороз также можно заподозрить при нарушении осанки у ребенка, особенно если это сочетается с замедлением роста. К сожалению, часто первым симптомом патологии становится компрессионный перелом тел позвонков. Что характерно, даже такой серьезный признак может оставаться незамеченным. Ребенок начинает жаловаться на боли в области перелома, заметно напряжение мышц спины. Родителям стоит обратить внимание на возможно предшествовавшее появлению жалоб падение на спину. В целом для болей при ювенильном остеопорозе характерно то, что нестероидные противовоспалительные препараты оказываются неэффективными в купировании болевого синдрома.
Диагностика
Тщательно собранный анамнез и клинические проявления позволяют педиатру заподозрить остеопороз. Если исключаются эндокринные, инфекционные и другие причины, тогда, вероятнее всего, речь идет о ювенильном остеопорозе. Диагноз подтверждается на основании комплексного обследования, включающего неинвазивные и инвазивные методы:
- Обзорная рентгенография. Обнаруживает снижение плотности костей, очаги просветления и расширение костномозгового канала, однако эти признаки появляются при снижении минерализации на 20-30%, то есть являются поздними. На компьютерной томограмме можно визуализировать места компрессионных переломов.
- Денситометрия. При ювенильном остеопорозе требуется подтверждение сниженной минерализации костей. Для этого чаще всего проводится двойная энергетическая рентгеновская абсорбциометрия. Метод является разновидностью денситометрии и позволяет с высокой точностью (до 2%) определить плотность костной ткани. Показатель сравнивается с нормой для данного возраста, и у пациентов оказывается ниже нормы.
- Биопсия. Достаточно часто приходится прибегать к инвазивным методам диагностики, то есть к биопсии подвздошной кости. Это наиболее точный метод, позволяющий оценить гистологическую структуру кости и достоверно подтвердить ювенильный остеопороз.
Лечение ювенильного остеопороза
Терапия включает в себя диету, а также повышение минеральной плотности костной ткани до уровня, максимально приближенного к норме. Рациональная диета, сбалансированная по содержанию белка, кальция и фосфора, также является обязательным компонентом терапии.
- Медикаментозная терапия. Нарушения метаболизма костной ткани можно устранить двумя путями: повышение остеогенеза или снижение скорости костной резорбции. Часто применяются лекарственные средства, влияющие на оба этих процесса (как правило, гормональные). Кроме того, обязательно используются препараты витамина D и кальций. Медикаменты для купирования болевого синдрома подбираются индивидуально. Патогенетическая терапия также способствует уменьшению болей.
- Коррекция переломов. Лечение переломов только хирургическое, далее показана диета с высоким содержанием кальция и физиотерапия. В период ремиссии назначается ЛФК
- Ортопедическая коррекция. Пациентам с ювенильным остеопорозом показано ношение корсета, поскольку даже при успешном лечении возможно прогрессирование сутулости, что в дальнейшем значительно ухудшает качество жизни во взрослом возрасте. Помимо этого, корсеты разгружают позвоночник, снижая риск компрессионных переломов.
Прогноз и профилактика
Прогноз ювенильного остеопороза сомнительный в связи с невозможностью этиотропного лечения, даже при своевременной комплексной терапии сохраняется риск инвалидизации. Важно постоянно соблюдать рекомендованную диету, проходить курсовое лечение, выполнять все назначения лечащего врача. Профилактика включает, главным образом, устранение модифицируемых факторов риска: ведение активного образа жизни, лечение болезней ЖКТ, рациональное питание.
Особенности и причины возникновения
В зависимости от причины возникновения выделяют две разновидности заболевания:
- Первичная (идиопатическая) форма. Ювенильный идиопатический остеопороз развивается по неизвестным причинам. Определенную роль играет генетическая предрасположенность. Фактором риска является также питание с недостаточным поступлением кальция и гиподинамия. Обычно остеопороз манифестирует в период активного роста ребенка, причем девочки болеют чаще.
- Вторичная форма возникает как следствие других заболеваний. Причиной может быть патология пищеварительного тракта, которая характеризуется поражением слизистой оболочки тонкого кишечника. При этом снижается всасываемость кальция, что и приводит к деминерализации костей. Гормональный дисбаланс также является причиной развития вторичного остеопороза в молодом возрасте. Может нарушаться продукция половых гормонов или наблюдаться дисфункция щитовидной железы. Кроме того, вторичный ювенильный остеопороз может развиваться при заболеваниях крови, поражении почек, или как симптом патологии соединительной ткани.
В этом видео эксперты расскажут, как укреплять кости при остеопорозе.
Симптомы и диагностика
Остеопороз в детском возрасте развивается постепенно, и имеет хронический характер. Довольно длительное время заболевание может протекать бессимптомно, и начальные признаки уловить чрезвычайно сложно.
Первые неспецифические симптомы обычно связаны с поражением позвоночного столба. Ребенок может жаловаться на боль в спине, которая появляется после нагрузки. Чаще поражается поясничный отдел позвоночника, что связано с его высокой подвижностью. Изменяется осанка, характерно появление сколиоза или грудного кифоза. Родители могут заметить отставание в росте.
Однако намного чаще остеопороз манифестирует с появления спонтанных переломов. Из-за того, что костная ткань приобретает повышенную хрупкость, переломы могут возникать даже при легком ударе или незначительном падении.
Поставить окончательный диагноз по клинической картине можно только в запущенных стадиях при наличии рецидивирующих спонтанных переломов. Для диагностики в начальной стадии используются дополнительные методы исследования. Лабораторная диагностика включается в себя оценку состояния кальций-фосфорного обмена и эндокринного статуса. Для этого назначаются следующие анализы:
- Биохимический анализ крови. Для оценки состояния минерализации определяют общий уровень кальция и фосфора. Исследуется уровень активности образования костной ткани (уровень щелочной фосфатазы).
- Для оценки кальций-фосфорного обмена определяют также суточную экскрецию этих микроэлементов с мочой.
- Гормональный анализ крови. При подозрении на вторичный остеопороз исследуют уровень половых гормонов и состояния щитовидной железы (кальцитонин).
Более специфическим методом диагностики является применение инструментального исследования:
- Обзорная рентгенография. Применяется для диагностики переломов, у детей особенно опасен компрессионный перелом тел позвонков. Для оценки минерализации костной ткани рентгенография назначается редко, поскольку изменения появляются только при значительном снижении плотности костей.
- Компьютерная томография (КТ). Как и рентгенография используется для диагностики переломов. Является более специфическим методом, позволяет выявить даже краевой перелом позвонков.
- Денситометрия. Может применяться как рентгеновская, так и ультразвуковая. Наиболее информативный метод при остеопорозе, поскольку позволяет определить даже незначительное снижение плотности. Полученные показатели сравниваются со средними значениями для данного возраста.
Правила лечения
Лечение при ювенильном остеопорозе направлено, прежде всего, на профилактику переломов, стабилизацию состояния и уменьшение болевых проявлений. Терапия при остеопорозе имеет длительный, а часто и пожизненный характер:
В случае возникновения перелома трубчатой кости необходимо иммобилизовать конечность при помощи шины или повязки. Лечение переломов должно осуществляться врачом-травматологом в хирургическом стационаре.
Для уменьшения риска развития компрессионного перелома позвоночника необходимо носить специальные корсеты.

Профилактика
Профилактические меры включают в себя раннюю диагностику и здоровый образ жизни. Предупредить развитие заболевания можно, если придерживаться правильного питания (с повышенным содержанием кальция и витамина Д) и соблюдать умеренную физическую нагрузку. Особенно это касается детей в период активного роста костей. Вторичная профилактика включает в себя избегание травмирующих факторов.
Остеопороз – заболевание, затрагивающее костные ткани скелета человека, при котором отмечается резкая потеря костной массы, снижение плотности костей, нарушение их архитектоники. Это приводит к тому, что кости становятся менее прочными, возрастает риск вн

Безболезненная, уникальная методика доктора Бобыря
Дешевле, чем мануальная терапия
Мягко, приятно, нас не боятся дети
Только с 20 по 30 июня! Записывайтесь сейчас!

Многие считают, что лечение остеопороза – удел пожилых людей и в большинстве случаев женского пола. Но в медицинской практике встречаются случаи развития болезни у детей или подростков. Ювенильный (юношеский) остеопороз – достаточно редкая форма патологии, возникающая у ранее здоровых детей в период между 7-13 годами (перед началом полового созревания) и в большинстве случаев полностью излечима.
Детский ювенильный остеопороз, так же как и взрослый подразделяется на первичный (идиопатический) и вторичный. В первом случае видимых и достаточно объяснимых причин возникновения недуга не выявляется (таких случаев достаточно мало).
Чаще всего консультация остеопата необходима маленьким пациентам с вторичными признаками остеопороза. Беспокоящие симптомы возникают на фоне других патологических состояний, болезней или медикаментозной терапии, которые негативным образом отражаются на метаболизме костных тканей.
Заболевания, при которых велика вероятность развития вторичного ювенильного остеопороза:
- Эндокринная система – сахарный диабет, гипотиреоз, синдром Иценко-Кушинга, тиреотоксикоз и пр.
- Ревматические патологии – системная красная волчанка, ревматоидный артрит и пр.
- Органы пищеварения, почки и печень – хронические патологии печени, гепатит, мальабсорбция, почечная недостаточность.
- Заболевания крови – лейкемия, лейкоз, лимфома, системный мастоцитоз.
- Хронические заболевания органов дыхания и легких.
- Длительная иммобилизация, травматические повреждения, хирургические вмешательства, пересадка органов и пр.
Ятрогенные факторы, вызывающие ювенильный остеопороз, – лечение проводимое кортикостероидами, иммунодепрессантами, антикоагулянтами, антиконвульсантами и некоторыми другими лекарственными препаратами, химиотерапия, проводимая при онкологических заболеваниях.
Выделяют две группы факторов риска, которые могут спровоцировать развитие идиопатического ювенильного остеопороза: генетические и факторы внешней среды.
Генетическая предрасположенность: пиковая величина костной массы, пол, раса.
Коэффициент пиковой массы костей – максимальное количество костных тканей, достигнутое человеком к моменту завершения роста и формирования скелета, предопределенное генетически. Определение этой величины стало возможным с внедрением в клиническую практику двухэнергетических рентгеновских аппаратов с низкой лучевой нагрузкой, позволяющих делать денситометрию детям регулярно в процессе роста. Метод основан на высокоточном измерении потерь костной массы по ее минеральной насыщенности.
Статистические данные и исследования показали, что коэффициенты костной массы выше у девочек в сравнении с мальчиками такого же возраста, роста и веса. Значительно выше минеральная плотность кости у чернокожих по сравнению с белыми, и значительно ниже ее показатели у азиатов. Большую роль в формировании заниженного пика костной массы играет генетическая предрасположенность. Если родители имеют низкую минерализацию скелета, то у следующего поколения высока вероятность развития ювенильного остеопороза, причем, как правило, доминант передается по женской линии.
Факторы внешней среды: недостаточное потребление кальция с пищей, малая физическая активность, чрезмерные физические нагрузки, недостаточное пребывание на солнце, вредные привычки.
Заниженные показатели костной массы отмечаются у вегетарианцев и девушек, следующих диете для похудения, что отображает их прямую связь с дефицитом потребляемого с пищей кальция. Подавляющее большинство медиков подчеркивают необходимость полноценного кальциевого приема для нормального формирования пика костной массы.
Благотворно на интенсивность прироста коэффициента костей влияет физическая активность. Ряд исследований зафиксировал повышенную минеральную плотность костных тканей в позвонках у детей, занимающихся каким-либо подвижным видом спорта, по сравнению со сверстниками, не имеющими физических нагрузок. Причем показатели не падали даже при снижении частоты и интенсивности тренировок. Однако чрезмерное физическое перенапряжение перед и/или в период полового созревания может негативно отразиться на формировании пика массы кости, особенно у девочек.
Отрицательное воздействие на формирование архитектоники кости оказывает недостаточная инсоляция (пребывание на солнце), так как только на солнечном свету в коже вырабатывается витамин D, отвечающий за всасывание кальция в кишечнике. Раннее привыкание подростков к табакокурению, потреблению алкоголя и наркотиков также вредит усвоению кальция и существенно повышает риск развития остеопороза и идиопатических переломов.
Исследования подтвердили взаимосвязь недостаточности показателей пиковой массы костной ткани и дальнейшего лечения заболеваний позвоночника в зрелом и преклонном возрасте. Плохая минерализация скелета в детском и юношеском возрасте может стать причиной лечения нестабильности позвоночника, позвоночных грыж, остеохондроза, люмбалгии и других заболеваний.
Самыми первыми признаками ювенильного остеопороза, как правило, становятся боли в нижней части спины (пояснице). Они носят хронический характер, усиливаются после длительного пребывания в вынужденных позах (сидя, стоя) и непривычных физических нагрузок. Болевой синдром может распространяться на бедра и ноги, коленный сустав, голеностопную часть, часто сопровождается затруднениями при ходьбе, хромотой.
Среди физических пороков, сопровождаемых остеопорозное заболевание, наблюдаются кифоз Шейермана Мау (сутулость верхней части спины), кифосколиоз, распрямление поясничного лордоза, резкое снижение роста (за счет деформации позвонков), впалая грудная клетка или наоборот клиновидная и выпирающая (напоминает киль птицы), плоскостопие. Общее состояние организма ребенка ослабленное, отмечается вялость, перепады настроения, угнетенность.
Перечисленные симптомы не являются специфичными, нередко встречаются в периоды интенсивного роста организма и причиной обращения родителей в клинику остеопатии становятся переломы. Травматические повреждения трубчатых костей нижних конечностей, небольших костей стоп или компрессионные переломы тел позвонков могут происходить при незначительных нагрузках, а иногда даже при резких движениях.
При наличии у детей беспокоящих симптомов и факторов риска (генетическая предрасположенность, малая физическая активность, недостаточное потребление молочных продуктов) следует безотлагательно провести:
- рентгенографию грудного и поясничного сегментов позвоночника, а также шеек бедренных костей;
- денситометрию костных тканей;
- биохимический анализ крови и мочи на содержание в них кальция, фосфора и других микроэлементов;
- гистоморфометрическое исследование биоптата крыла подвздошной кости при трудностях или невозможности проведения дифференциальной диагностики.
В большинстве случаев идиопатический ювенильный остеопороз проходит спонтанно, так же как и начинается, ничем не проявляя себя в зрелом возрасте пациента. Тем не менее, физические патологии, сопровождаемые заболевание требуют ранней диагностики особенно у детей и подростков. Эти меры необходимы для защиты позвоночных сочленений и других костей скелета несовершеннолетних больных от неожиданных переломов и их последствий.
При этом не существует единых консервативных или хирургических методов лечения остеопороза у малолетних пациентов. Каждый случай рассматривается индивидуально, также назначается и специфическое лечение.
Важной детерминантой в достижении пика костной массы (лечении и профилактики остеопорозного заболевания) является физическая активность. Кроме ЛФК, плавания в острый период могут быть порекомендованы длительные пешие прогулки на свежем воздухе (не менее двух часов в день), йога, танцы, аэробика, соразмерная с возрастом и физическим состоянием пациента посильная физическая работа.
Благоприятное воздействие при лечении оказывает физиотерапия, сеансы мануальной терапии. Следует избегать небезопасной физической деятельности и экстремальных видов спорта. При переломах практикуется поддерживающая терапия (костыли, шины, эластичные и жесткие корсеты).
При лечении ювенильного остеопороза оправдана сбалансированная диета, богатая на кальций и витамин D. Передозировки не следует опасаться, так как количество всасываемого кальция в организме всегда меньше потребляемого, излишки выводятся почками с мочой. Одобренные лекарственные препараты (бисфосфонаты) при терапии остеопороза у взрослых в экспериментальных целях были предложены детям, но не показали ожидаемых результатов.
В большинстве случаев после адекватного лечения заболевания происходит полное восстановление костных тканей, нарушения роста компенсируются после окончания острого периода. Однако, в некоторых случаях идиопатический остеопороз, к сожалению, остается неизлеченным, что приводит к инвалидной группе, лечению нарушений осанки и нестабильности позвоночника.
А.А. Дударева, А.И. Метальников, Е.В. Калашникова, К.В. Лукьянов, г. Барнаул
Введение
Остеопороз – системное заболевание, характеризующееся низкой массой кости и микроструктурной перестройкой костной ткани, приводящей к повышенной ломкости кости и, как следствие этого, повышению риска перелома. Это определение патологии было принято в 1990 г. на конференции по остеопорозу в Копенгагене. Уменьшение массы кости влечет за собой снижение механической прочности, поэтому переломы при остеопорозе возникают при незначительной травме или даже статической нагрузке. Частота переломов, связанных с остеопорозом, во всем мире увеличивается. Риск переломов шейки бедра на протяжении жизни у женщин белой расы составляет 15%, что приближается к уровню заболеваемости раком молочной железы, эндометрия и яичников, вместе взятых Риск перелома шейки бедра на протяжении жизни у мужчин составляет 5%, что приближается к уровню заболеваемости раком предстательной железы. Переломы шейки бедра в 20% случаев становятся причиной смерти, а 50% выживших остаются инвалидами. Каждый третий пациент с переломами этой локализации нуждается в дорогостоящих реабилитационных мероприятиях. Частота переломов тел позвонков у взрослых за последние 30 лет увеличилась в 4 раза. По данным ряда исследователей, почти 20% ортопедических приемов приходится на больных с переломами тел позвонков, возникших, главным образом, на фоне остеопороза (С.С Родионова, 1997). Не менее драматична ситуация с переломами у детей и подростков. По данным г. Барнаула, за последние 15 лет частота переломов тел позвонков у детей возросла в 6 раз, причем у 70% пострадавших механизм травмы был не адекватен тяжести повреждения. По данным Российского НИИ травматологии и ортопедии им. Вредена, анализ результатов обследования подростков с патологией позвоночника выявил у 13,95% наличие остеопороза (С А. Михайлов, 1997).
Благодаря широкомасштабным исследованиям, проводимым в ряде стран Европы и Америки, разработаны методы диагностики и лечения ОП. До окончательного решения проблемы, судя по данным литературы, еще далеко. Тем не менее, совершенно очевидно, что предотвращение потери костной массы может быть гораздо эффективнее, чем лечение осложнений остеопороза. Поэтому основной целью профилактических мероприятий в группах риска развития остеопороза является увеличение костной массы, близкой к максимуму, приобретаемому к 18-20 годам.
БМЕ – участок костной ткани, в котором протекают сопряженные по времени процессы локальной резорбции и образования кости, что обозначается как ремоделирование. БМЕ образует остеокласты, остеобласты, активные мезенхимальные клетки, капиллярные петли. Размер БМЕ – 0,05-0,1 мм3. В организме взрослого одновременно функционирует 105х106 БМЕ. Длительность жизни БМЕ и сроки рождения или формирования новых БМЕ имеют постоянную величину, что поддерживает состояние образования и резорбции кости. Интенсивность ремоделирования достигает максимума в юношеском возрасте, затем постепенно снижается. Возрастное снижение интенсивности ремоделирования лежит в основе физиологической атрофии костной ткани. Большинство исследователей считают, что потеря массы кости в норме зависит от пола и составляет у мужчин 0,4-1,2%, у женщин 0,75-2,4% в год. Причем у женщин этот процесс начинается с 35, у мужчин с 50 лет.
Регуляторный механизм БМЕ неизвестен, но есть предположения, что основную роль при этом играют активные метаболиты витамина D. Интермедиарная организация скелета несет ответственность не только за ремоделирование, но и за моделирование (процесс, контролирующий форму и размер кости) и восстановление микропереломов. В норме в костной ткани постоянно происходят микропереломы трабекул, которые запускают механизмы ремоделирования, что, в свою очередь, способствует их заживлению.
25-40% фосфора взрослый человек получает с мясом и рыбой, 20-30% – с молочными продуктами и 12-20% – с хлебом. Хотя его всасывание происходит по всей длине тонкого кишечника, основное количество усваивается в тощей кишке. Главным образом всасывание происходит за счет системы Na-зависимого активного транспорта, в меньшей мере – путем пассивной диффузии. Не исключается также возможность поступления фосфора вместе с кальцием под влиянием 1,25-(ОН)2D3. Причем метаболит действует непосредственно на проницаемость мембран энтероцитов. 90% фосфора накапливается в кости. Содержание фосфора крови, в отличие от кальция, меняется в течение суток, что связывают с приемом пищи и действием паратиреоидного гормона (ПТГ). Резорбция фосфора под влиянием ПТГ происходит в проксимальных почечных канальцах. Активные метаболиты витамина D на этот процесс не влияют.
Основное регулирующее влияние на гомеостаз кальция, фосфора и метаболизм костной ткани оказывают ПТГ, активные метаболиты витамина D3, кальцитонин (КТ). Их взаимодействие осуществляется по принципу обратной связи, характерной для функционирования саморегулирующейся системы
Секреция ПТГ регулируется изменением уровня ионизированного кальция в крови. Тканями-мишенями гормона являются почки и костная ткань. В клеткахмишенях ПТГ связывается со специфическими рецепторами на их мембране. Сигнал, транслируемый мембранным сопрягающим белком, активизирует аденилатциклазу, что в свою очередь приводит к образованию циклических нуклеотидов, модулирующих клеточные компоненты и их функцию. При действии ПТГ кальций экстрагируется из кости. Гормон увеличивает число остеокластов за счет ускорения созревания их клеток-предшественников и повышает их метаболическую активность ПТГ способен также оказывать влияние на функцию остеобластов. Влияние гормона на почки связано с реабсорбцией кальция и фосфора. Большинство исследователей считают, что рецепторы к ПТГ располагаются преимущественно в проксимальных почечных канальцах. С возрастом в норме продукция ПТГ увеличивается.
Человек получает витамин D в виде холекальциферола (D3), который вырабатывается в коже, и эргокальциферола (D2), поступающего с пищей. Суточная потребность в витамине D – 2,5 мг (100 ME). Однако ни витамин D2, ни D3 не обладают биологической активностью. Превращение витамина D в активные метаболиты представляется следующим образом. Витамин D3 в крови связывается с витамин D-связывающим белком и в таком виде транспортируется в печень, где после гидроксилирования образуется 25оксихолекальциферол (25-OH/D3). Процесс гидроксилирования происходит с участием фермента витамин D-25-гидроксилазы и весьма чувствителен к воздействию медикаментов и повреждается при гепатобилиарной патологии. Из печени 25-(ОН-)D3 поступает в кровь, где снова связывается с витамин D-связывающим белком. Это соединение представляет собой основную циркулирующую в крови форму витамина D. Второе гидроксилирование происходит в почках и, в меньшей степени, в костях, с участием фермента 1-а-гидроксилазы или 24гидроксилазы. Образуется, соответственно, активный метаболит 1,25-(ОН)2D3 (кальцитриол) и 24, 25-(OH)2D3. Наиболее изучено влияние 1,25-(ОН)2D3, который стимулирует всасывание кальция из кишечника, его реабсорбцию в почечных канальцах, обеспечивает процесс минерализации и стимулирует образование кости в участках ее резорбции.
Являясь антагонистом ПТГ, угнетает процесс резорбции костной ткани, уменьшая число и активность остеокластов, оказывает тормозящее влияние на синтез 1,25-(ОН)20з, снижает реабсорбцию кальция в почечных канальцах. Кроме того, КТ устраняет гиперкальциемию, возникающую после приема пищи. Участие КТ в ремоделировании костной ткани признается не всеми исследователями.
Имеются многочисленные данные о влиянии эстрогенов на всасывание кальция в кишечнике. По мнению большинства исследователей, воздействие эстрогенов па метаболизм кальция и костной ткани осуществляется через увеличение продукции ПТГ, который, в свою очередь, влияет на метаболизм 1,25-(ОН)2D3. Дефицит эстрогенов уменьшает продукцию КТ, изменяет чувствительность костных клеток к ПТГ.
На метаболизм костной ткани, помимо кальцийрегулирующих гормонов, оказывают влияние системные и локальные факторы роста Системным медиатором, регулирующим число и активность остеокластов, является остеокластактивирующий фактор. Последний в определенных количествах вырабатывается в норме лимфоцитами в присутствии макрофагов, продуцирующих простагландины группы Е. Костная ткань сама является богатым источником факторов роста, которые влияют на процессы резорбции и образования кости. Эти факторы роста главным образом действуют как локальные регуляторы метаболизма костной ткани. Более того, исходная костная клетка, синтезирующая фактор роста, может оказаться и его клеткой-мишенью. К настоящему времени из костного матрикса или культуры кости выделены следующие факторы роста: фактор роста фибробластов, который разделяется на кислотный и щелочной и индуцирует остеогенез; инсулиноподобный фактор роста, повышающий способность костно-мозговых клеток (предшественники) образовывать костную ткань in vitro; трансформирующий фактор роста присутствует в костном матриксе и высвобождается в процессе резорбции. Этот фактор ингибирует действие остеокластов и стимулирует остеобласты. Существует еще ряд факторов, изученных в меньшей степени.
Таким образом, регуляция метаболизма костной ткани в норме является многофакторным процессом, и нарушение одного из компонентов этой системы может привести к развитию остеопороза.
Патогенез системного остеопороза
До настоящего времени нет единого мнения в отношении механизмов нарушения ремоделирования и моделирования при ОП.
Таким образом, в основе развития ОП лежит нарушение внутрикостных механизмов – моделирования и ремоделирования. Как пример ОП, связанного с нарушением моделирования, описывается несовершенный остеогенез, ОП при нарушении питания, при билиарном циррозе и прочих причинах. Остеопороз как следствие нарушения ремоделирования развивается при кратковременной гипокинезии, тиреотоксикозе, приеме стероидов и пр. причинах.
В развитии заболевания выделяют два момента: остеопению и механическую несостоятельность костной ткани. При остеопении механическая прочность остается достаточной, чтобы выдержать физиологические нагрузки. Появление перестроечных переломов связывается с развитием механической несостоятельности из-за замедленного заживления микропереломов. В норме в костной ткани происходят микропереломы трабекул, которые активизируют ремоделирование, а это, в свою очередь, способствует их заживлению. В силу ряда причин, действующих на клетки БМЕ, этот механизм при ОП нарушается, число переломов костных балок увеличивается. При этом срабатывает принцип обратной связи; накопление микропереломов усугубляет механическую несостоятельность кости.
Данные относительно уровня ПТГ при остеопорозе противоречивы. Наряду с нормальным или даже повышенным содержанием нередко описывается и снижение его уровня. Снижение секреции ПТГ отмечено при ОП на фоне гипокинезии. По мнению ряда авторов, единичные сообщения об увеличении уровня ПТГ у больных ОП, например при постменопаузальной форме, объясняются тем, что не учитывается возможность возрастного, характерного для нормы его увеличения. Известные данные о способности остеобластов влиять на синтез ПТГ в какой-то мере объясняют снижение уровня гормона у больных ОП с выраженной клеточной депрессией.
Большую частоту ОП у женщин белой расы связывают с более низким, чем у черных женщин, уровнем КТ. Как считают некоторые исследователи, КТ влияет на развитие ОП только после наступлении менопаузы. В то же время сообщения о влиянии КТ на созревание хондроцитов свидетельствуют о более широком спектре его действия. Данные относительно изменений уровня КТ при ОП противоречивы. Отмеченное снижение подтверждается не всеми авторами.
Нарушение процессов моделирования, ремоделирования и функции клеток, участвующих в гистогенезе, связывают с недостатком активных метаболитов витамина D. Данные об изменении уровня метаболитов витамина D при ОП, так же как и сведения, относительно изменения уровня ПТГ и КТ, носят противоречивый характер.
О возможном влиянии недостатка эстрогенов на развитие ОП впервые высказался Albright. Однако до настоящего времени их воздействие на костную ткань остается предметом дискуссии. Мнение о способности эстрогенов тормозить резорбцию и тем самым предотвращать потерю костной ткани больных ОП, не является общепризнанным В ведущей роли эстрогенов в генезе заболевания заставляет усомниться то, что ОП не является неизбежностью для каждой женщины в менопаузе, и увеличение в последние годы числа больных среди женщин молодого и среднего возраста с нормальным менструальным циклом и сохранением детородной функции, а также значительный рост числа больных среди мужчин.
Таблица 1. Суточная потребность в кальции в разные возрастные периоды, а также при некоторых физиологических состояниях
| Группы здоровых лиц | Потребность в кальции, мг/сут |
| Дети | 800-1000 |
| Подростки | до 1300 |
| Предменопаузальный и период | 1000 |
| Постменопаузальный период | 1500 |
| Беременность | 1500 |
| Гипокинезия | 2000 |
Недостаточное потребление кальция. По данным В.А. Тутельтяна и Б.П. Суханова, суточная потребность кальция (мг/сут) составляет для детей в возрасте 3 мес. 400, 4-6 мес. – 500, 7-12 мес. – 600, 1-3 года – 800, 4-6 лет – 900-1000, 7-10 лет – 1100 и 11-17 лет – 12001300 мг/сут.
Ограничение физической нагрузки нивелирует процессы моделирования и ремоделирования, изменяя функцию БМЕ, и приводит к остеопении. При гипокинезии снижается число остеобластов, они теряют свое упорядоченное расположение. У молодых людей полная неподвижность в течение 4 месяцев может вызвать снижение минеральной плотности до 20%.
Увеличение потребления фосфора с пищей приводит к гиперфосфатемии и может стать причиной ОП, вызывая, с одной стороны, гипокальциемию, с другой – оказывая непосредственное тормозящее воздействие на костеобразование. К увеличению уровня фосфора в крови может привести и инсулинотерапия, так как под влиянием инсулина увеличивается поглощение фосфора в тонком кишечнике.
Повышенное содержание алкоголя в крови оказывает повреждающее влияние на остеобласты, усиливает (кратковременно) функцию коры надпочечников. Глюкокортикоиды, оказывая прямое действие на околощитовидные железы, способствуют увеличению секреции ПТГ. Кроме того, глюкокортикоиды угнетают всасывание Са из кишечника, нарушают метаболизм витамина D и усиливают экскрецию Са с мочой. Многократное повторение этого воздействия приводит к развитию остеопороза.
Потенциально важны генетические исследования для выявления риска остеопорозных переломов. Если будет возможным идентифицировать полиморфизм, который предскажет низкую плотность кости или остеопорозные переломы, это может быть использовано как скрининговый инструмент для идентификации людей с таковым риском и для назначения им профилактического лечения. Это также может дать основу для составления тестов для проверки эффективности лечения. Например, показано, что ответ костной массы на добавление в диету витамина D и кальция в значительной мере зависит от полиморфизма рецептора для витамина. Подобным образом применение полиморфных маркеров для других генов-кандидатов может выявить лучшую реакцию на заместительную гормонотерапию, бифосфонаты и изменения в образе жизни.
Таблица 2. Изучение генетического влияния в процессе остеопороза
| Изучаемый ген | Значение для определения |
| Рецептор витамина В | Через рецептор витамин регулирует дифференцировку клеток кости, оборот кости и гомеостаз кальция |
| Рецептор эстрогенов | Через рецептор эстрогены регулируют оборот кости и рост скелета |
| Трансформирующий фактор | Присутствует в матриксе кости и обеспечивает связь между резорбцией кости и рост костеобразованием |
| Интерлейкин 6 | Регулирует дифференцировку остеокластов и медиирует некоторые влияния половых гормонов на кость |
| Ген коллагена тип I | Тип I коллагена преобладает среди белков кости |
| Коллагеназа | Энзим, участвующий в резорбции костного матрикса |
Читайте также:


