Ревматоидный фактор и щитовидная железа
Казанский государственный медицинский университет
Введение. Ревматоидный артрит (РА) – распространенное (около 1% населения планеты) аутоиммунное ревматическое заболевание, характеризующееся симметричным эрозивным артритом (синовитом) и широким спектром внесуставных (системных) проявлений. Характерными проявлениями РА являются боли, нарушение функции суставов и неуклонно прогрессирующая деформация суставов, необратимое поражение внутренних органов, приводящие к ранней потере трудоспособности (около трети пациентов становятся инвалидами в течение 20 лет от начала болезни) и сокращению продолжительности жизни пациентов (в среднем на 5–15 лет) [1].
В последние годы взгляд на РА как на неизлечимое заболевание пересматривается. Это cвязано с расширением возможностей ранней диагностики РА, что позволяет начинать активную, тщательно контролируемую (tight control) терапию базисными противовоспалительными препаратами (БПВП), в первую очередь метотрексатом (МТ), в ранней стадии болезни и разработкой нового класса генно-инженерных биологических препаратов (ГИБП), которые селективно блокируют важные звенья иммунопатогенеза РА [2].
Пациенты с РА подвергнуты повышенной частоте развития патологии щитовидной железы, что объясняется общностью иммунологических механизмов развития этих заболеваний. Распространенность тиреоидной патологии в целом среди больных РА достигает 28% [3].
Работы отечественных авторов по изучению функционального состояния щитовидной железы у больных РА на фоне современной терапии немногочисленны [4]. Особый интерес представляет изучение функционального состояния ЩЖ в эру лечения больных РА генно-инженерными биологическими препаратами. Зарубежные и отечественные исследования по этой теме отсутствуют, что и предопределило актуальность данной работы.
Цель. Оценить функциональное состояние щитовидной железы у больных РА на фоне терапии БПВП и ГИБП.
Терапия ГИБП проводилась по стандартной схеме [5,6].
На момент начала лечения ритуксимабом 11 пациентов находились на базисной терапии РА, 9 из них получали метотрексат в дозе 7,5 – 15 мг в неделю, 2 – лефлуномид в дозе 20 мг в день. На момент назначения тоцилизумаба и абатацепта все пациенты получали метотрексат (в дозе 7,5 – 20 мг и 10 – 15 мг в неделю соответственно), инфликсимаба – 1 пациент получал метотрексат в дозе 12,5 мг в неделю, 2 – лефлуномид в дозе 10 и 20 мг в день.
В группе больных, начавших впервые получать лечение БПВП, 14 пациентам назначен метотрексат в дозе 7,5-15 мг в неделю, 3 пациентам - лефлуномид в дозе 20 мг в день, 2 пациентам - сульфасалазин в дозе 2000 мг в день, 2 пациентам - плаквенил в дозе 200 мг в день.
Эффект терапии оценивали по критериям ACR и EULAR (DAS 28). Оценку эффективности проводили через 24 недели терапии.
Возраст больных РА составил 44 [32,5; 52] года, длительность заболевания – 2,3 [0,2; 4,4] года. Серопозитивный РА диагностирован у 38 (80,9%) больных, серонегативный – у 9 (19,1%). Средняя степень активности РА определена у 8 (17%) больных, высокая - у 39 (83%). I рентгенологическая стадия РА установлена у 2 (4,3%) пациентов, II – у 21 (44,7%), III – у 14 (29,8%), IV - у 10 (21,3%) пациентов. Медленно-прогрессирующее течение заболевания было у 31 (66%) пациента, быстропрогрессирующее – у 16 (34%). Системные проявления были выявлены у 38 (80,9%) больных. Индекс HAQ составил 1,5 [1,1;1,9]. ФК I - II был диагностирован у 18 (38,3%) пациентов, ФК III - IV – у 29 (61,7%) пациентов.
Статистическая обработка полученных результатов осуществлялась с использованием пакета программ Excel, Statististica 6,0 для Windows. Достоверность различий при сравнении количественных параметров оценивали с помощью критерия Уилкоксона. Для сравнения долей применялись таблицы сопряжённости, с последующим использованием точного критерия Фишера или критерия χ кв. Пирсона. Различия считались достоверными при p 0,05).
Таблица 2. Динамика основных клинических и лабораторных показателей у больных РА на фоне терапии абатацепта и инфликсимаба
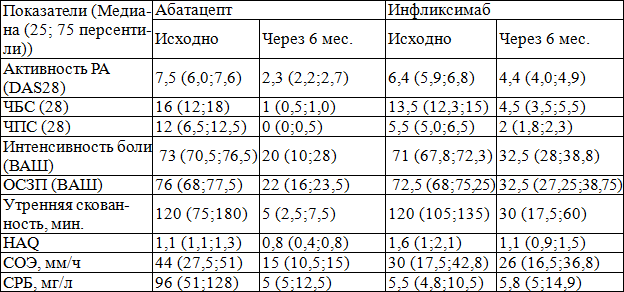
Примечание: в группе пациентов, получающих абатацепт и инфликсимаб, достоверных различий нет
Оценка эффективности терапии абатацептом по критериям EULAR (рис. 1) показала, что через 6 месяцев лечения хороший эффект достигнут у всех пациентов (3 (100%)). Оценка эффективности терапии по критериям ACR (рис. 2) показала, что через 6 месяцев лечения у всех пациентов наблюдалось уменьшение параметров на 20%, на 50% и на 70%.
В начале исследования в группе пациентов, получавших абатацепт (n=3) у 2 (66,7%) пациентов были выявлены повышенные уровни антител к щитовидной железе (у одного пациента – АТ к ТПО и АТ к ТГ, у другого – только АТ к ТПО).
У пациента с исходно высоким уровнем антител к щитовидной железе на фоне лечения абатацептом уровень АТ к ТПО снизился, уровень АТ к ТГ нормализовался. У данного пациента была достигнута ремиссия РА по критериям EULAR и 70% улучшение по ACR. У другого пациента с исходно высоким уровнем АТ к ТПО через 6 месяцев лечения их уровень уменьшился, но произошло увеличение уровня АТ к ТГ. У пациента достигнут хороший эффект по EULAR, 70 % улучшение по ACR.
Таким образом, на фоне улучшения клинических и лабораторных параметров РА произошло снижение уровня антител к щитовидной железе.
Среди обследованных больных, начавших получать инфликсимаб (n=4) было 3 (75%) женщины, 1 (25%) мужчина в возрасте 45 [39,3;50,3] лет с длительностью РА 5 [4,5;10,5] лет. Серопозитивный РА был диагностирован у 3 (75%) пациентов, серонегативный - у 1 (25%). У 2 (50%) пациентов было медленно - прогрессирующее течение РА. III рентгенологическая стадия РА установлена у 1 (25%) пациента, IV – у 3 (75%) пациентов. Системные проявления РА были выявлены у 2 пациентов (50%). Высокая степень активности РА была диагностирована у всех больных (4 (100%)).
На фоне терапии инфликсимабом отмечена положительная динамика ЧБС, ЧПС, интенсивности боли и ОСЗП по ВАШ, длительности утренней скованности, СОЭ, индекса HAQ, активности заболевания по индексу DAS 28 (p>0,05).
Оценка эффективности терапии инфликсимабом по критериям EULAR (Рис. 1.) показала, что через 6 месяцев лечения хороший эффект достигнут у 1 (25%) пациента, удовлетворительный эффект – у 2 (50%) пациентов, у 1 (25%) пациента эффект отсутствовал. Оценка эффективности терапии по критериям ACR (рис. 2) показала, что через 6 месяцев лечения уменьшение параметров на 20% отмечалось у всех пациентов (4 (100%)), на 50% - у 2 (50%) и на 70% - у 1 (75%) пациента.
При клинической оценке тиреоидного статуса у пациентов, получавших инфликсимаб (n=4) исходно не наблюдалось нарушений функции щитовидной железы или повышенного уровня антител к щитовидной железе.
Через 6 месяцев лечения инфликсимабом у одного пациента впервые был диагностирован субклический гипотиреоз. У данного пациента эффект по критериям EULAR отсутствовал. Эффективость терапии по критериям ACR составила 20%. Возникновение субклинического гипотиреоза можно объяснить неэффективностью проводимой терапии вследствие того, что пациенту не были назначены БПВП из–за наличия противопоказаний. Инфликсимаб одобрен для применения при РА только в комбинации с БПВП.
Среди обследованных больных, начавших получать БПВП (n=21) было 18 (85,7%) женщин, 3 (14,3%) мужчин в возрасте 46 [33;52] лет с длительностью РА 0,2 [1,5;2] года. Серопозитивный РА был диагностирован у 15 (71,4%) пациентов, серонегативный – у 6 (28,6%). Медленно - прогрессирующее течение РА было у 13 (61,9%) пациентов, быстро-прогрессирующее – у 8 (38,1%). I рентгенологическая стадия РА установлена у 2 (9,5%) пациентов, II – у 14 (66,7%) пациентов, III – у 3 (14,3%) пациентов, IV – у 2 (9,5%) пациентов. Системные проявления РА были выявлены у 13 (61,9%) пациентов. Средняя степень активности РА была диагностирована у 5 (23,8%) больных, высокая – у 16 (76,2%) больных.
Изучение динамики активности заболевания по индексу DAS 28 показало его достоверное снижение через 6 месяцев от начала терапии (p 0,05).
При сравнительной оценке эффективности терапии между разными биологическими агентами по критериям EULAR и ACR различия в эффективности не были выявлены.
Проведенное исследование показало улучшение функции щитовидной железы у пациентов с исходно выявленным субклиническим гипотиреозом, снижение или нормализацию титра антител к щитовидной железе на фоне проводимой терапии.
Современная базисная терапия оказывает положительное влияние на функциональное состояние щитовидной железы у пациентов с РА.
Список использованных источников:
1. Насонов Е.Л. Новые аспекты фармакотерапии ревматоидного артрита – блокада ко–стимуляции Т–лимфоцитов// Русский медицинский журнал. – 2009. – Т. 17, №3. – С. 150-155.
2. Насонов Е.Л., Лукина Г.В., Сигидин Я.А. Комбинированная терапия ритуксимабом и лефлуномидом при ревматоидном артрите (предварительные результаты российского регистра АРБИТР)// Научно–практическая ревматология. – 2011. - №1. – С. 16-20.
3. Мягкова М.А. Естественные антитела к гормонам. – М.: Материя - Медика, 2001. – 260 с.
4. Зиннетуллина Н.Х. Особенности тиреоидного статуса у больных ревматоидным артритом: Автореф. дис. … канд. мед. наук. – Чебоксары, 2003. – 23 с.
5. Насонов Е.Л. Ревматология: Клинические рекомендации. – М.: ГЭОТАР-Медия, 2010. – 752 с.
6. Биологическая терапия в ревматологии/ Я.А. Сигидин, Г.В. Лукина. – М.: Практическая медицина, 2009. – 302 с.


Простой и информативный анализ, который покажет проблемы с суставами в начале заболевания.

Думаю, каждый человек хоть раз в жизни испытывал неприятные ощущения в суставах. А если посмотреть на мировую статистику, то многие заболевания суставов диагностируют в достаточно молодом возрасте. Есть точный анализ, который покажет, есть ли у вас предрасположенность к заболеваниям суставов. Это анализ крови на ревматоидный фактор.
Что такое ревматоидный фактор?
Ревматоидный фактор (РФ) – это аутоантитела, которые ошибочно атакуют собственные ткани организма, принимая их за чужеродные. Мишенью для аутоантител служат FC- фрагменты иммуноглобулинов класса IgG. Анализ крови на ревматоидный фактор используется в качестве маркера воспалительной и аутоиммунной активности.
Для диагностики каких заболеваний назначают анализ крови на ревматоидный фактор?
Чаще всего данный тест применяется для диагностики ревматоидного артрита и синдрома Шегрена, однако уровень РФ в крови может повышаться и при других воспалительных и аутоиммунных заболеваниях, таких как системная красная волчанка, склеродермия, дерматомиозит.
Почему я решила сдать анализ крови на ревматоидный фактор?
Не могу сказать, что меня по жизни как-то особенно беспокоили суставы. Даже с учётом того, что у меня было две беременности и даже сейчас я иногда ношу младшую дочку на руках, на колени, например, я совсем не жалуюсь. Единственное, в последние пару месяцев я начала замечать болезненные ощущения в суставах пальцев рук. Но опять же это может быть и не симптомом какой-то болезни, просто я часто пользуюсь смартфоном (чем ещё заняться на самоизоляции?). Раньше я так много в телефоне не сидела, поэтому может быть руки просто устают. Но ладно бы если просто дискомфорт в суставах. У меня около трех недель держалась субфебрильная температура. Пару дней даже 37.5 была, но в основном 37.1-37.2. Никаких симптомов простуды у меня не было. А вот одним из первых и иногда даже единственных симптомов болезни суставов является повышение температуры до субфебрильных показателей.
Поэтому я решила сдать общий анализ крови, анализ крови на с-реактивный белок (чтобы исключить в организме воспалительной процесс) и как раз анализ крови на ревматоидный фактор.
Платно или по полису ОМС?
С учётом сложившейся эпидемиодогической обстановки в стране мне совсем не хотелось идти в поликлинику к терапевту и просить у неё направление на этот анализ. Поэтому я решила сдать анализ платно в частной лаборатории. Цена, кстати, адекватная. В Инвитро стоимость данного анализа - 330 рублей.

Подготовка к сдаче анализа.
Анализ крови на ревматоидный фактор нужно сдавать натощак. Либо должно пройти минимум 3 часа с последнего приёма пищи. Больше никакой специальной подготовки нет. Воду перед сдачей анализа пить можно.
Сам анализ.
Нужно сдать кровь из вены. Для меня не проблема - я не боюсь сдать кровь. Как я уже писала не раз, дело это минутное и самое неприятное, что может произойти - это попадётся неопытный лаборант, после забора крови которым на руке может остаться синяк.
Результат.
В лаборатории обещали, что результат будет готов на следующий день после сдачи анализа. Так и вышло - в районе обеда мне на электронную почту пришло письмо от Инвитро с моими результатами анализов.

Ревматоидный фактор у меня ниже референсных значений, а это значит, что речи об аутоимунном процессе не идет. Это меня порадовало, одной проблемой меньше.
Выводы.
Простой и информативный анализ, не требующий сложной специальной подготовки. Результат готовится быстро. Да и цена доступная. В некоторых случаях он просто необходим, так как может показать проблемы с суставами в самом начале заболевания.
5 звёзд и РЕКОМЕНДУЮ.
Возможно вам будет интересно прочитать другие мои отзывы на медицинские услуги:
Спасибо за внимание к моему отзыву!
Полный текст:
- Аннотация
- Об авторах
- Список литературы
- Cited By
В обзоре литературы рассматриваются различные аспекты сочетания ревматоидного артрита (РА) с аутоиммунными заболеваниями щитовидной железы (тиреоидитом Хашимото и болезнью Грейвса). Обсуждаются распространенность, генетическая предрасположенность, сходство патогенеза и клинических симптомов, а также способность органоспецифичных аутоантител (антител к тиреоидной пероксидазе, антител к тиреоглобулину) и гипотиреоза влиять на течение РА и риск кардиоваскулярых осложнений.
1. Насонов ЕЛ, редактор. Ревматология. Клинические рекомендации. Москва: ГЭОТАР-Медиа; 2010 [Nasonov EL, editor. Revmatologiya. Klinicheskie rekomendatsii [Rheumatology. Clinical guidelines]. Moscow: GEOTAR-Media; 2010].
2. Александрова ЕН, Авдеева АС, Лукина ГВ и др. Клинико- иммунологические эффекты анти-В-клеточной терапии у больных ревматоидным артритом. Научно-практическая ревматология. 2012;50(1):14-21. [Aleksandrova EN, Avdeyeva AS, Lukina GV, et al. The clinical and immunological effects of anti-B-cell therapy in patients with rheumatoid arthritis. Nauchno-Prakticheskaya Revmatologiya = Rheumatology Science and Practice. 2012;50(1):14-21 (In Russ.)]. doi: 10.14412/1995- 4484-2012-498
3. Авдеева АС, Новиков АА, Александрова ЕН и др. Связь уровней цитокинов с активностью заболевания, уровнем аутоантител и деструктивными изменениями суставов при раннем ревматоидном артрите. Научно-практическая ревматология. 2015;53(4):385-90. [Avdeeva AA, Novikov AA, Aleksandrova EN, et al. An association of cytokine levels with disease activity, autoantibody levels, and joint destructive changes in early rheumatoid arthritis. Nauchno-Prakticheskaya Revmatologiya = Rheumatology Science and Practice. 2015;53(4):385-90 (In Russ.)]. doi: 10.14412/1995-4484-2015-385-390
4. Duraes C, Moreira CS, Alvelos I, et al. Genetic susceptibility to autoimmune thyroid disease: past, present, and future. Thyroid. 2010 Jul;20(7):715-25. doi: 10.1089/thy.2010.1644
5. Barton A, Worthington J. Genetic susceptibility to rheumatoid arthritis: an emerging picture. Arthritis Rheum. 2009 Oct 15;61(10):1441-6. doi: 10.1002/art.24672
6. Tomer Y, Huber A. The etiology of autoimmune thyroid disease: a story of genes and environment. J Autoimmun. 2009 MayJun;32(3-4):231-9. doi: 10.1016/j.jaut.2009.02.007
7. Kä llberg H, Ding B, Padyukov L, et al. EIRA Study Group. Smoking is a major preventable risk factor for rheumatoid arthritis: estimations of risks after various exposures to cigarette smoke. Ann Rheum Dis. 2011 Mar;70(3):508-11. doi: 10.1136/ard.2009.120899
8. Dayan CM, Daniels GH. Chronic autoimmune thyroiditis. N Engl J Med. 1996 Jul 11;335(2):99-107. doi: 10.1056/NEJM199607113350206
9. Ngo ST, Steyn FJ, McCombe PA. Gender differences in autoimmune disease. Front Neuroendocrinol. 2014 Aug;35(3):347-69. doi: 10.1016/j.yfrne.2014.04.004
10. Heuer M, Aust G, Ode-Hakim S, Scherbaum WA. Different cytokine mRNA profiles in Graves' disease, Hashimoto's thyroiditis, and nonautoimmune thyroid disorders determined by quantitative reverse transcriptase polymerase chain reaction (RT-PCR). Thyroid. 1996 Apr;6(2):97-106. doi: 10.1089/thy.1996.6.97
11. Nanba T, Watanabe M, Inoue N, Iwatani Y. Increases of the Th1/Th2 cell ratio in severe Hashimoto's disease and in the proportion of Th17 cells in intractable Graves' disease. Thyroid. 2009 May;19(5):495-501. doi: 10.1089/thy.2008.0423
12. Giordano C, Richiusa P, Bagnasco M, et al. Differential regulation of Fas-mediated apoptosis in both thyrocyte and lymphocyte cellular compartments correlates with opposite phenotypic manifestations of autoimmune thyroid disease. Thyroid. 2001 Mar;11(3):233-44. doi: 10.1089/105072501750159615
13. Ajjan RA, Watson PF, McIntosh RS, Weetman AP. Intrathyroidal cytokine gene expression in Hashimoto's thyroiditis. Clin Exp Immunol. 1996 Sep;105(3):523-8. doi: 10.1046/j.1365- 2249.1996.d01-784.x
14. Gianoukakis AG, Khadavi N, Smith TJ. Cytokines, Graves' disease, and thyroid-associated ophthalmopathy. Thyroid. 2008 Sep;18(9):953-8. doi: 10.1089/thy.2007.0405
15. Helen Kemp E, Ajjan RA, Metcalfe RA, et al. IL-14 and IL-16 are expressed in the thyroid of patients with either Graves' disease or Hashimoto's thyroiditis. Clin Endocrinol (Oxford). 2015 May 4. doi: 10.1111/cen.12810
16. Ajjan RA, Weetman AP. Cytokines in thyroid autoimmunity. Autoimmunity. 2003 Sep-Nov;36(6-7):351-9. doi: 10.1080/08916930310001603046
17. Mikos H, Mikos M, Obara-Moszynska M, Niedziela M. The role of the immune system and cytokines involved in the pathogenesis of autoimmune thyroid disease (AITD). Endokrynol Pol. 2014;65(2):150-5. doi: 10.5603/EP.2014.0021
18. Segni M, Pucarelli I, Truglia S, et al. High prevalence of antinuclear antibodies in children with thyroid autoimmunity. J Immunol Res. 2014;2014:150239. doi: 0.1155/2014/150239
19. Tagoe CE, Zezon A, Khattri S, Castellanos P. Rheumatic manifestations of euthyroid, anti-thyroid antibody-positive patients. Rheumatol Int. 2013 Jul;33(7):1745-52. doi: 10.1007/s00296-012- 2616-9
20. Tektonidou MG, Anapliotou M, Vlachoyiannopoulos P, Moutsopoulos HM. Presence of systemic autoimmune disorders in patients with autoimmune thyroid diseases. Ann Rheum Dis. 2004 Sep;63(9):1159-61. doi: 10.1136/ard.2004.022624
21. Perez-Moreiras JV, Alvarez-Lopez A, Gomez EC. Treatment of active corticosteroid-resistant Graves' orbitopathy. Ophthal Plast Reconstr Surg. 2014 Mar-Apr;30(2):162-7. doi: 10.1097/IOP.0000000000000037
22. Salvi M. Immunotherapy for Graves' ophthalmopathy. Curr Opin Endocrinol Diabetes Obes. 2014 Oct;21(5):409-14. doi: 10.1097/MED.0000000000000097
23. Figueroa-Vega N, Alfonso-Perez M, Benedicto I, et al. Increased circulating pro-inflammatory cytokines and Th17 lymphocytes in Hashimoto's thyroiditis. J Clin Endocrinol Metab. 2010 Feb;95(2):953-62. doi: 10.1210/jc.2009-1719
24. Ruggeri RM, Saitta S, Cristani M, et al. Serum interleukin-23 (IL-23) is increased in Hashimoto's thyroiditis. Endocr J. 2014;61(4):359-63. doi: 10.1507/endocrj.EJ13-0484
25. Насонов ЕЛ, Александрова ЕН, Новиков АА. Аутоиммунные ревматические заболевания: итоги и перспективы научных исследований. Научно-практическая ревматология. 2015;53(3):230-7 [Nasonov EL, Aleksandrova EN, Novikov AA. Autoimmune rheumatic diseases: Results and prospects for researches. Nauchno-Prakticheskaya Revmatologiya = Rheumatology Science and Practice. 2013;53(3):230-7 (In Russ.)]. doi: 10.14412/1995-4484-2015-230-237
26. Nakano A, Watanabe M, Iida T, et al. Apoptosis-induced decrease of intrathyroidal CD4(+)CD25(+) regulatory T cells in autoimmune thyroid diseases. Thyroid. 2007 Jan;17(1):25-31. doi: 10.1089/thy.2006.0231
27. Vanderpump MPJ, Tunbridge WMG, French JM, et al. The incidence of thyroid disorders in the community: a twenty-year follow-up of the Whickham survey. Clin Endocrinol. 1995;43(1):55- 68. doi: 10.1111/j.1365-2265.1995.tb01894.x
28. Cardenas Roldan J, Amaya-Amaya J, Castellanos-de la Hoz J, et al. Autoimmune thyroid disease in rheumatoid arthritis: a global perspective. Arthritis. 2012;2012:864907. doi: 10.1155/2012/864907
29. Atzeni F, Doria A, Ghirardello A, et al. Anti-thyroid antibodies and thyroid dysfunction in rheumatoid arthritis: prevalence and clinical value. Autoimmunity. 2008 Feb;41(1):111-5. doi: 10.1080/08916930701620100
30. El-Sherif WT, El Gendi SS, Ashmawy MM, et al. Thyroid disorders and autoantibodies in systemic lupus erythematosus and rheumatoid arthritis patients. Egypt J Immunol. 2004;11(2):81-90.
31. Przygodzka M, Filipowicz-Sosnowska A. Prevalence of thyroid diseases and antithyroid antibodies in women with rheumatoid arthritis. Pol Arch Med Wewn. 2009 Jan-Feb;119(1-2):39-43.
32. Raterman HG, Jamnitski A, Lems WF, et al. Improvement of thyroid function in hypothyroid patients with rheumatoid arthritis after 6 months of adalimumab treatment: a pilot study. J Rheumatol. 2011 Feb;38(2):247-51. doi: 10.3899/jrheum.100488
33. Pan XF, Gu JQ, Shan ZY. Increased risk of thyroid autoimmunity in rheumatoid arthritis: a systematic review and metaanalysis. Endocrine. 2015 Sep;50(1):79-86. doi: 10.1007/s12020- 015-0533-x
34. Shiroky JB, Cohen M, Ballachey ML, Neville C. Thyroid dysfunction in rheumatoid arthritis: a controlled prospective survey. Ann Rheum Dis. 1993 Jun;52(6):454-6. doi: 10.1136/ard.52.6.454
35. McCoy SS, Crowson CS, Gabriel SE, Matteson EL. Hypothyroidism as a risk factor for development of cardiovascular disease in patients with rheumatoid arthritis. J Rheumatol. 2012 May;39(5):954-8. doi: 10.3899/jrheum.111076
36. Парамонова ОВ, Русанова ОА, Гонтарь ИП. Взаимосвязь органоспецифической аутоиммунной патологии щитовидной железы с неорганическими аутоиммунными ревматическими заболеваниями. Клиническая и экспериментальная тиреоидология. 2012;8(1):46-50 [Paramonova OV, Rusanova OA, Gontar IP. Interrelation specific autoimmune pathologies of a thyroid gland with inorganic autoimmune rheumatic diseases. Klinicheskaya i Eksperimental'naya Tireoidologiya = Clinical and Experimental Thyroidology. 2012;8(1):46-50 (In Russ.)]. doi: 10.14341/ket20128146-50
37. Delamere JP, Scott DL, Felix-Davies DD. Thyroid dysfunction and rheumatic diseases. J R Soc Med. 1982 Feb;75(2):102-6.
38. Boelaert K, Newby PR, Simmonds MJ, et al. Prevalence and relative risk of other autoimmune diseases in subjects with autoimmune thyroid disease. Am J Med. 2010 Feb;123(2):183.e1-9. doi: 10.1016/j.amjmed.2009.06.030
39. Andonopoulos AP, Siambi V, Makri M, et al. Thyroid function and immune profile in rheumatoid arthritis. A controlled study. Clin Rheumatol. 1996 Nov;15(6):599-603. doi: 10.1007/BF02238551
40. Chan AT, Al-Saffar Z, Bucknall RC. Thyroid disease in systemic lupus erythematosus and rheumatoid arthritis. Rheumatology (Oxford). 2001 Mar;40(3):353-4. doi: 10.1093/rheumatology/40.3.353
41. Al-Awadhi AM, Olusi S, Hasan EA, Abdullah A. Frequency of abnormal thyroid function tests in Kuwaiti Arabs with autoimmune diseases. Med Princ Pract. 2008;17(1):61-5. doi: 10.1159/000109592
42. Raterman HG, van Halm VP, Voskuyl AE, et al. Rheumatoid arthritis is associated with a high prevalence of hypothyroidism that amplifies its cardiovascular risk. Ann Rheum Dis. 2008 Feb;67(2):229-32. doi: 10.1136/ard.2006.068130
43. Santos MJ, Vinagre F, Silva JJ, et al. Cardiovascular risk profile in systemic lupus erythematosus and rheumatoid arthritis: a comparative study of female patients. Acta Reumatol Port. 2010 JulSep;35(3):325-32.
44. Kerola AM, Nieminen TV, Kauppi MJ, et al. Increased risk of levothyroxine-treated hypothyroidism preceding the diagnosis of rheumatoid arthritis: a nationwide registry study. Clin Exp Rheumatol. 2014 Jul-Aug;32(4):455-9.
45. Bengtsson C, Padyukov L, Kä llberg H, Saevarsdottir S. Thyroxin substitution and the risk of developing rheumatoid arthritis; results from the Swedish population-based EIRA study. Ann Rheum Dis. 2014 Jun;73(6):1096-100. doi: 10.1136/annrheumdis-2013-203354
46. Никитина НМ, Афанасьев ИА, Романова ТА, Ребров АП. Особенности коморбидности у больных ревматоидным артритом в разные годы наблюдения. Современная ревматология. 2015;9(1):39-43. [Nikitina NM, Afanasyev IA, Romanova TA, Rebrov AP. Specific features of comorbidity in rheumatoid arthritis patients in different follow-up years. Sovremennaya Revmatologiya = Modern Rheumatology Journal. 2015;9(1):39-43 (In Russ.)]. doi: 10/14412/1996-7012-2015-1- 39-43
47. LeRiche NGH, Bell DA. Hashimoto's thyroiditis and polyarthritis: a possible subset of seronegative polyarthritis. Ann Rheum Dis. 1984 Aug;43(4):594-8. doi: 10.1136/ard.43.4.594
48. Punzi L, Michelotto M, Pianon M, et al. Clinical, laboratory and immunogenetic aspects of arthritis associated with chronic lymphocytic thyroiditis. Clin Exp Rheumatol. 1997 JulAug;15(4):373-80.
49. Blake DR, McGregor AM, Stansfield E, Smith BR. Antithyroidantibody activity in the snyovial fluid of patients with various arthritides. Lancet. 1979 Aug 4;2(8136):224-6. doi: 10.1016/S0140-6736(79)90238-1
50. Punzi L, Schiavon F, Ramonda R, et al. Anti-thyroid microsomal antibody in synovial fluid as a revealing feature of seronegative autoimmune thyroiditis. Clin Rheumatol. 1991 Jun;10(2):181-3. doi: 10.1007/BF02207661
51. Bourji K, Gatto M, Cozzi F, et al. Rheumatic and autoimmune thyroid disorders: a causal or casual relationship? Autoimmun Rev. 2015 Jan;14(1):57-63. doi: 10.1016/j.autrev.2014.10.007
52. Hezarkhani S, Sedighi S, Aghaei M, et al. Rheumatologic manifestations in Iranian patients with autoimmune thyroid diseases. J Clin Diagn Res. 2014 Oct;8(10):MC06-8. doi: 10.7860/JCDR/2014/7974.4981
53. Punzi L, Sfriso P, Pianon M, et al. Clinical manifestations and outcome of polyarthralgia associated with chronic lymphocytic thyroiditis. Semin Arthritis Rheum. 2002 Aug;32(1):51-5. doi: 10.1053/sarh.2002.33722
54. Ahmad J, Blumen H, Tagoe CE. Association of antithyroid peroxidase antibody with fibromyalgia in rheumatoid arthritis. Rheumatol Int. 2015 Aug;35(8):1415-21. doi: 10.1007/s00296-015-3278-1
55. Серебряков ВГ, Алекберова ЗС, Корешков ГГ, Зеновко ЕИ. Особенности течения ревматоидного артрита, сочетающегося с патологией щитовидной железы. Терапевтический архив. 1990;62(5):48-51. [Serebriakov VG, Alekberova ZS, Koreshkov GG, Zenovko EI. The characteristics of the course of rheumatoid arthritis combined with thyroid pathology. Terapevticheskii arkhiv = Therapeutic Archive. 1990;62(5):48-51 (In Russ.)].
56. Koszarny A, Majdan M, Suszek D, et al. Relationship between rheumatoid arthritis activity and antithyroid antibodies. Pol Arch Med Wewn. 2013;123(7-8):394-400.
57. Raterman HG, Voskuyl AE, Simsek S, et al. Increased progression of carotid intima media thickness in thyroid peroxidase antibodies-positive rheumatoid arthritis patients. Eur J Endocrinol. 2013 Oct 21;169(6):751-7. doi: 10.1530/EJE-13-0394
58. Dessein PH, Joffe BI, Stanwix AE. Subclinical hypothyroidism is associated with insulin resistance in rheumatoid arthritis. Thyroid. 2004 Jun;14(6):443-6. doi: 10.1089/105072504323150750
59. Raterman HG, van Eijk IC, Voskuyl AE, et al. The metabolic syndrome is amplified in hypothyroid rheumatoid arthritis patients: a cross-sectional study. Ann Rheum Dis. 2010 Jan;69(1):39-42. doi: 10.1136/ard.2008.100776
60. Dessein PH, Joffe BI, Veller MG, et al. Traditional and nontraditional cardiovascular risk factors are associated with atherosclerosis in rheumatoid arthritis. J Rheumatol. 2005 Mar;32(3):435-42.
61. Dessein PH, Norton GR, Woodiwiss AJ, et al. Influence of nonclassical cardiovascular risk factors on the accuracy of predicting subclinical atherosclerosis in rheumatoid arthritis. J Rheumatol. 2007 May;34(5):943-51.
62. Marchiori RC, Pereira LA, Naujorks AA, et al. Improvement of blood inflammatory marker levels in patients with hypothyroidism under levothyroxine treatment. BMC Endocr Disord. 2015 Jun 23;15:32. doi: 10.1186/s12902-015-0032-3

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
Симптомы и способы диагностики хронического тиреоидита Хашимото
При ультразвуковой и рентгенологической денситометрии устанавливается степень выраженности остеопороза. А выявление пониженного содержания тиреотропного гормона в сыворотке крови позволяет предполагать вторичную природу гипотиреоза, при высоком уровне ТТГ предполагают первичный гипотиреоз. Также при необходимости проводят определение содержания кальция в сыворотке крови, метаболитов витамина D и других биохимических показателей.
Тиреоидит Хашимото – это хроническое воспаление щитовидной железы аутоиммунного характера. Вызвано заболевание сбоем работы иммунной системы. Патология приводит к снижению функции шитовидки, недостаточной выработке гормонов и нарушению обменных процессов в организме.
При развитии аутоиммунных процессов в организме начинают вырабатываться антитела к здоровым клеткам щитовидной железы, что приводит к деструкции тканей и снижению функции эндокринного органа. Клетки насыщаются лейкоцитами, что приводит к развитию воспалительного процесса. В результате железа меньше вырабатывает тиреоидных гормонов, развивается гипотиреоз, а секреция тиреотропина повышается.
Патологические антигены приводят к разрушению фолликулярных клеток щитовидки, которые секретируют тироксин и трийодтиронин. Т-лимфоциты также могут оказывать негативное влияние на ткани гипофиза и рецепторы периферических тканей.
Аутоиммунный тиреоидит Хашимото является наследственным заболеванием. Провоцирующими факторами могут послужить:
- перенесенные воспалительные, инфекционные заболевания;
- механические травмы щитовидной железы;
- длительное лечение гормональными препаратами;
- дефицит или переизбыток йода;
- стресс;
- послеродовой период;
- тяжелая форма сахарного диабета;
- другие аутоиммунные заболевания: ревматоидный артрит, гепатит;
- плохая экологическая обстановка;
- перенесенные операции на щитовидной железе.

Аутоиммунный тиреоидит чаще встречается в регионах с неблагоприятной экологической обстановкой. Страдает недугом около 4% населения, острые клинические проявления диагностируются у 1% больных.
Тиреоидит Хашимото проявляется следующими признаками:
- увеличение или уменьшение объема щитовидной железы;
- при пальпации железа плотная, прощупываются узловые уплотнения;
- болезненные ощущения в области шеи;
- затруднения во время глотания, разговора.
К симптомам острого воспаления относится повышение температуры тела, головная боль, миалгия, ломота в теле и суставах. Может наблюдаться покраснение кожи над щитовидной железой, увеличение регионарных лимфоузлов.
Заболевание развивается постепенно в течение нескольких лет. На начальных стадиях появляются признаки тиреотоксикоза из-за деструкции фолликулярных клеток. Позже возникают характерные симптомы гипотиреоза:
- выпадение волос;
- ломкость, слоение ногтей;
- раздражительность;
- быстрая утомляемость, общая слабость;
- зябкость;
- снижение температуры тела;
- гипотония;
- отечность лица, конечностей;
- заторможенность, снижение интеллектуальных способностей;
- мышечная слабость, снижение чувствительности тканей;
- увеличение массы тела при плохом аппетите;
- метеоризм, частые запоры;
- нарушение менструального цикла у женщин, маточные кровотечения.
У больных обнаруживается анемия, повышенный уровень вредного холестерина в крови, нарушение толерантности к глюкозе. В некоторых случаях развивается сахарный диабет.
При остром течении тиреоидита Хашимото клинические симптомы развиваются в течение 2–3 месяцев, проявляются более выраженно, вызывают сильное недомогание, высокую температуру тела.
После этого наступает субклиническая фаза, при которой повышается секреция ТТГ, а уровень Т4 находится в пределах нормы или незначительно понижен. Выраженных симптомов заболевания нет.
Следующая стадия – тиреотоксическая. Т-лимфоциты разрушают клетки щитовидной железы, при этом происходит выброс резервных запасов тироксина в кровь, развиваются симптомы тиреотоксикоза. Отмершие фолликулярные клетки воспринимаются иммунной системой, как чужеродные тела, что приводит к еще большей выработке Т-лимфоцитов. Пациента беспокоит:
- тошнота;
- частая диарея;
- желтушность кожи;
- гипертония;
- тахикардия;
- снижение массы тела.
Может наблюдаться выпучивание глаз.
Аутоиммунные процессы постепенно приводят к деструкции значительного количества клеток щитовидки, развивается гипотиреоз на фоне выраженного дефицита тироксина. Функция эндокринного органа может восстановиться через некоторое время, или гипотиреоз сохраняется пожизненно.
АИТ в некоторых случаях протекает только в фазе тиреотоксикоза или сопровождается исключительно симптомами гипотиреоза.
Хронический тиреоидит Хашимото бывает нескольких видов:
- При атрофической форме происходит уменьшение размеров щитовидной железы, присутствуют симптомы гипотиреоза, наблюдается дефицит тироксина, трийодтиронина.
- Гипертрофическая форма характеризуется диффузным увеличением щитовидки, орган плотный, подвижный. Присутствуют симптомы тиреотоксикоза или гипотиреоза.
По клиническим признакам АИТ бывает латентный и манифестный. Скрытая форма заболевания характеризуется повышенным уровнем ТТГ при нормальных показателях Т4, клинические симптомы заболевания могут отсутствовать. Размер щитовидки не изменен или наблюдается незначительное диффузное увеличение, узлы отсутствуют.
Явный гипотиреоз подтверждается при высокой концентрации тиреотропина, выраженном дефиците Т4 и наличии признаков снижения функции щитовидной железы.
По морфологическим признакам аутоиммунный тиреоидит классифицируют:
- Очаговый АИТ поражает одну долю щитовидной железы.
- Диффузный АИТ вызывает значительное увеличение объема щитовидки.
- Перитуморальный АИТ развивается при отеке головного мозга. Нарушается работа гипофиза, секреция ТТГ.
- Ювенильный АИТ наблюдается у подростков. В основе заболевания лежит гиперплазия щитовидной железы.
В зависимости от формы заболевания подбирают необходимое лечение.
Ультразвуковое исследование помогает оценить структуру тканей щитовидной железы, степень патологических процессов, выявить наличие узловых образований. Чтобы подтвердить диагноз, и правильно определить характер уплотнений, назначается тонкоигольная аспирационная биопсия. При аутоиммунном тиреоидите в биоматериале отсутствуют раковые клетки, могут содержаться некротические массы, аутоиммунные лимфоциты.
Перечень лабораторных анализов:
- общий анализ крови на уровень лимфоцитов;
- определение показателей свободного Т3 и Т4;
- иммунограмма: АТ к ТПО, АТ к ТГ, антитела к коллоидному антигену и тиреоидным гормонам.
Проводят дифференциальную диагностику аутоиммунного заболевания с другими формами тиреоидитов, раком щитовидной железы, узловым зобом.
- Артропатия встречается у четверти всех больных с микседемой, поражая при этом в основном суставы нижних конечностей и мелкие суставы кисти.
- У многих пациентов при длительном течении гипотиреоза развивается диффузный системный остеопороз.
- Проявления гипотиреозного артрита обычно неспецифичны: боли и отечность в суставах, ограничение объема движений в них, скопление выпота в полости сустава.
- У 10% больных возникает синдром указательного пальца (боль при его сгибании), у 22% больных гипотиреозом развивается контрактура Дюпюитрена, у трети больных развивается синдром карпального канала. Это связано с отеком параартикулярных тканей, сопутствующими явлениями теносиновита, отложением в параартрикулярных тканях мукополисахаридов, а при длительном существовании и хондрокальциноза.
- В некоторых случаях изменения в суставах предшествуют проявлению типичных симптомов гипотиреоза со стороны других органов и систем. Но при этом может прослеживаться миалгия (боли в мышцах), общая слабость, повышенная утомляемость.
Диагностика артропатий при гипотиреозе
Связывая отклонения от нормы в своем состоянии с патологией щитовидки, пациенты задаются вопросом о том, где находится щитовидная железа, так как с этого начинается диагностика – с пальпации.
Железа расположена под гортанью, на уровне пятого-шестого шейного позвонка. Она охватывает своими долями верх трахеи, а перешеек железы приходится прямо на середину трахеи.
По массе щитовидная железа достигает 25-ти грамм, а по длине не более 4 см. Ширина в среднем 1,5 см, аналогичная толщина. Объем измеряется в миллилитрах и равен до 25 мл у мужчин и до 18 мл у женщин.
Щитовидная железа – это орган внутренней секреции, отвечающий за выработку гормонов. Функции щитовидной железы заключены в гормональной регуляции посредством выработки определенного типа гормонов. Гормоны щитовидки включают в своем составе йод, так как еще одной функцией железы является хранение и биосинтез йода в более активную органическую функцию.
Пациенты, которых направляют на лабораторную диагностику заболеваний щитовидки, ошибочно считают, что исследуются гормоны щитовидной железы ТТГ, АТ-ТПО, Т3, Т4, кальцитонин. Важно различать, какие гормоны вырабатывает щитовидная железа, а какие – другие органы внутренней секреции, без которых щитовидка просто не будет работать.
- ТТГ – это тиреотропный гормон, который вырабатывается гипофизом, а не щитовидкой. Но он регулирует работу щитовидной железы, активизирует захват йода из плазмы крови щитовидкой.
- АТ-ТПО – это антитела к тиреопероксидазе, вещество негормональной природы, которое продуцируется иммунной системой в результате патологических процессов и аутоиммунных заболеваний.
Непосредственно гормоны щитовидной железы и их функции:
- Тироксин – Т4 или тетрайодтиронин. Представляет тиреоидные гормоны, отвечает за липидный метаболизм, понижение концентрации триглицеридов и холестерина в крови, поддерживает метаболизм костных тканей.
- Трийодтиронин – Т3, основной гормон щитовидной железы, так как тироксин также имеет свойство преобразовываться в трийодтиронин путем присоединения еще одной молекулы йода. Отвечает за синтез витамина А, понижение концентрации холестерина, активизацию метаболизма, ускорение пептидного обмена, нормализацию сердечной деятельности.
- Тиреокальцитонин – не является специфическим гормонов, так как может вырабатываться еще вилочковой и паращитовидной железой. Отвечает за накопление и распределение кальция в костной ткани, по сути, укрепляя ее.
Исходя из этого, единственное, за что отвечает щитовидная железа – это синтез и секреция тиреоидных гормонов. А вот продуцируемые ею гормоны выполняют ряд функций.
- Сначала гипофиз и гипоталамус получают сигнал от рецепторов о том, что в крови уровень тироксина и трийодтиронина занижен.
- Гипофиз вырабатывает ТТГ, который активизирует захват йода клетками щитовидной железы.
- Железа, захватывая полученный с пищей йод в неорганической форме, начинает его биосинтез в более активную, органическую форму.
- Синтезирование происходит в фолликулах, из которых состоит тело щитовидки, и которые наполнены коллоидной жидкостью, содержащей тиреоглобулин и пероксидазу для синтеза.
- Полученная органическая форма йода присоединяется к тиреоглобулину и высвобождается в кровь. В зависимости от количества присоединенных молекул йода, образовывается тироксин – четыре молекулы йода, или трийодтиронин – три молекулы.
- В крови Т4 или Т3 высвобождается отдельно от глобулина, а он снова захватывается клетками железы для использования в дальнейшем синтезе.
- Рецепторы гипофиза получают сигнал о достаточном количестве гормонов, выработка ТТГ становится менее активной.
Соответственно, обнаружив признаки заболевания щитовидной железы, врач назначает исследование не только концентрации гормонов щитовидки, но и гормонов, которые ее регулируют, а также антител к важной составляющей коллоида – пероксидазе.
На данный момент все патологии щитовидки медицина подразделяет на три состояния:
- Гипертиреоз – нарушение функции щитовидной железы, при котором повышается активность секреции и в кровь поступает избыточное количество тиреоидных гормонов, обменные процессы в организме увеличиваются. К заболеваниям также причисляется тиреотоксикоз.
- Гипотиреоз – нарушение функции щитовидной железы, при котором вырабатывается недостаточное количество гормонов, вследствие чего обменные процессы замедляются из-за недостатка энергии.
- Эутиреоз – заболевания железы, как органа, которые не имеют никаких проявлений в гормональном плане, но сопровождаются патологией самого органа. Среди заболеваний сюда относится гиперплазия, зоб, узловые образования.
Болезни щитовидной железы у женщин и мужчин диагностируют через показатель ТТГ, понижение или повышение которого свидетельствуют о реактивности или гипоактивности железы.
Только такой отвар запустит РЕГЕНЕРАЦИЮ щитовидной железы
Зоб пропадет уже через 3 дня! Это средство стало сенсацией в лечении щитовидной железы!
У женщин симптомы заболевания щитовидной железы проявляются чаще, так как гормональные колебания отражаются на менструальном цикле, что заставляет пациентку обращаться за помощью к врачу. Мужчины чаще списывают типичные симптомы щитовидки на усталость и перенапряжение.
Основные и самые распространенные заболевания:
- Гипотиреоз;
- Гипертиреоз;
- Тиреотоксикоз;
- Узловой, диффузный или смешанный зоб;
- Злокачественные образования железы.
Каждое из этих заболеваний характеризуется особенной клинической картиной и стадиями развития.
Врачи пока что не знают основную причину возникновения артрита, но определенно он возникает от травмы или инфекции. Наиболее частой причиной развития и является попадание инфекции в суставы. Это случается, когда щитовидная железа плохо справляется со своими обязанностями и иммунитет человека ослабевает. Именно сбой функционирования иммунной системы может привести к артриту.
Ревматоидный артрит представляет собой структурное заболевание соединительной ткани, где происходит первоначальное поражение мелких суставов. При ревматоидном артрите наблюдаются значительные отклонения в структуре гипофиза щитовидной железы. Во время данного заболевания имеются симптомы глубокого тиреоидного сбоя и симптомы аутоиммунных изменений щитовидной железы.
Возникновение артрита в височно-нижнечелюстной области
Артрит височно-нижнечелюстного сустава представляет собой болезнь, которая напоминает заболевания уха. В ухе начинает происходить процесс, который напоминает воспаление острый отит. Для артрита височно-нижнечелюстного сустава в области уха характерны такие симптомы, как:
- Болевые ощущения в ухе в области поражения. Человек может испытывать различную боль уха. От легкой боли до сильной боли, которая приносит значительное беспокойство.
- Отмечается малая потеря слуха. Ухо плохо слышит, иногда слух полностью пропадает.
- Наблюдается скованность в нижней части челюсти в утреннее время, иногда больной не может сделать движения, чтобы открыть рот.
- В период двигательных манипуляций в части нижней челюсти заболевший чувствует шум разнообразного характера, возможно щелканье, хруст или даже шуршание.
Если человек заболевает гнойным артритом, то данное заболевание сопровождается сильными болевыми ощущениями уха. Зачастую присутствует симптом заложенности в ушах. В височно-нижнечелюстной части сустава может появиться краснота кожного покрова, припухлость. Обычно у человека поднимается температура тела при артрите.
Причины болевых ощущений уха может констатировать только опытный ЛОР-врач. Чтобы болевые ощущения уха от артрита не беспокоили заболевшего, врач назначает специализированные повязки, антибактериальные или противовоспалительные препараты. Если врач диагностирует выраженный гнойный процесс, то требуется немедленное хирургическое вмешательство.
Возникновение артрита челюсти
1. Острый артрит;
2. Хронический артрит;
В основном симптомами заболевания являются сильные болевые ощущения в области зубов, наблюдаются припухлости в области височно-нижнечелюстного сустава. При запущенной стадии болезни больной не может двигать челюстью, движения могут быть полностью ограничены. Течение болезни может проходить с интоксикацией, высокой температурой тела, ознобом. К причинам образования височно-нижнечелюстного сустава можно отнести следующие параметры:
- Травма зубов, механическое повреждение челюсти;
- Удары, ушибы, резкое открывание полости рта;
- Проникновение инфекции в области зубов, челюсти;
- Наличие гормональной дисфункции в организме;
Что касается средств лечения артрита в области зубов и всей челюсти, то врач использует эластичную повязку, которую накладывает на челюсть. Таким образом, осуществляется полное обездвиживание и покой пораженному суставу. Болевые ощущения зубов перестают беспокоить. После повязки назначается медикаментозное лечение разнообразными противовоспалительными препаратами.
Если болевые ощущения зубов продолжаются или имеется запущенная стадия заболевания челюсти, то врач немедленно назначает хирургическое вмешательство. Особенно оно происходит часто, когда имеется гнойное воспаление челюсти. Если вы испытываете только боли зубов, то стоит обратиться к врачу-стоматологу, который осмотрит вас и назовет точную причину болезни зубов. Иногда болевые ощущения зубов не означают, что человек болеет артритом челюсти. Поэтому стоит проконсультироваться с врачом-стоматологом.
1. Острый артрит;
Лечение височно-нижнечелюстного артрита
Лечение начинается с того, что врач первым делом снимает болевые ощущения, которые беспокоят больного. Затем, в зависимости от вида заболевания, назначается медикаментозное лечение. Прописывается курс анальгетиков, массаж жевательных мышц. Эффективной процедурой, которая дает отличные результаты, называют миогимнастику.
Ревматоидный артрит лечится при помощи консервативных методов. Назначаются специальные противовоспалительные лекарственные препараты, осуществляется санация рта. Иногда больному может понадобиться протезирование зубов, чтобы достичь нормальной высоты прикуса.
Читайте также:


