Остеолиз при сахарном диабете
Что такое стопа Шарко? В чем трудность диагностики диабетической остеоартропатии? Диабетическая остеоартропатия (ОАП, стопа Шарко, сустав Шарко) — редкое, но крайне тяжелое осложнение сахарного диабета, при неадекватном лечении приводящее к необратимо
Диабетическая остеоартропатия (ОАП, стопа Шарко, сустав Шарко) — редкое, но крайне тяжелое осложнение сахарного диабета, при неадекватном лечении приводящее к необратимой инвалидизации. Это осложнение можно назвать одной из самых загадочных форм синдрома диабетической стопы, так как предсказать развитие ОАП и выделить группы риска среди пациентов с сахарным диабетом крайне трудно. С этим осложнением диабета встречаются врачи разных специальностей — хирурги, эндокринологи, ортопеды, но далеко не всегда оно вовремя распознается.
Деструктивная остеоартропатия была описана в ХIХ веке французским неврологом Шарко [2], но не при сахарном диабете (в доинсулиновую эру поздние осложнения диабета практически не встречались), а при сифилитическом поражении проводящих путей спинного мозга (tаbеs dоrsаlis). Впоследствии было установлено, что подобные изменения суставов стоп также встречаются при различных заболеваниях, приводящих к нарушению иннервации нижних конечностей (сирингомиелии, диабетической полинейропатии и др.). В настоящее время наиболее частой формой остеоартропатии является диабетическая.
Распространенность данного осложнения среди больных сахарным диабетом составляет менее 1% [3], хотя в литературе встречаются данные о поражении костной ткани стоп у 0,1-55% больных [4]. Такая противоречивость сведений, очевидно, связана с различиями в методике обследования и разными критериями диагностики остеоартропатии.
В подавляющем большинстве случаев ОАП поражает кости и суставы стоп. В 1991 году была предложена классификация ОАП [3] в зависимости от локализации процесса (рис. 1). У 20-25% пациентов ОАП поражает обе стопы, но обычно не одновременно. Встречаются случаи ОАП с поражением других суставов: коленного и даже локтевого.
Остеоартропатия — это по сути поражение костной ткани в отличие от типичных форм остеопороза, имеющих исключительно локальный характер. Причиной такого поражения кости является нарушение иннервации нижних конечностей вследствие диабетической нейропатии.
Известно, что ОАП не развивается у пациентов с нарушениями кровоснабжения нижних конечностей. Это объясняется тем, что при ишемической и нейроишемической формах синдрома диабетической стопы невозможно аномальное усиление кровотока в костной ткани.
После манифестации ОАП процесс проходит четыре стадии [4].
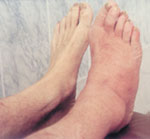 |
| Рисунок 2. |
Первая (острая) стадия характеризуется отеком стопы, умеренной гиперемией и местной гипертермией (рис. 2). Боли и лихорадка нехарактерны. Рентгенография может не выявлять деструктивных изменений (на этой стадии они представлены лишь микропереломами); обнаруживается остеопороз костей стоп.
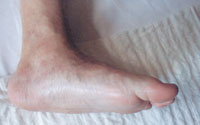 |
| Рисунок 3. |
Вторая (подострая): фрагментация костей и начало деформации стопы. В типичных случаях происходит уплощение свода стопы на пораженной стороне (рис. 3). Отек и воспалительные явления в этой стадии уменьшаются. Рентгенологически определяются фрагментации костных структур.
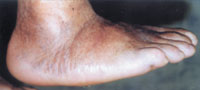 |
| Рисунок 4. |
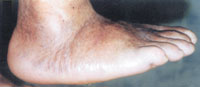 |
| Рисунок 5а. |
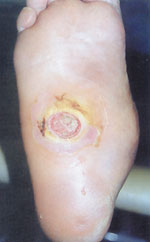 |
| Рисунок 5б. |
Четвертая (стадия осложнений): перегрузка отдельных участков деформированной стопы приводит к образованию язвенных дефектов (рис. 5); при их инфицировании возможно развитие флегмоны стопы, остеомиелита, гангрены.
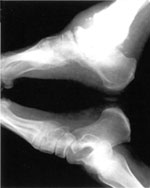 |
| Рисунок 6. |
ОАП диагностируется на основании клинической картины, анамнеза (небольшая травма, хирургическое вмешательство) и рентгенологических признаков, соответствующих той или иной стадии. Очень часто из-за недостаточной информированности врачей общей практики об ОАП это осложнение ошибочно диагностируется как лимфостаз, тромбофлебит, флегмона стопы и др.
Наиболее затруднен дифференциальный диагноз в острой стадии, когда несвоевременное начало адекватного лечения приводит к необратимой инвалидизации.
 |
| Рисунок 7. |
Дифференциальная диагностика ОАП в острой фазе включает два основных вопроса:
- Являются ли воспалительные изменения следствием поражения костных структур или их следует рассматривать как проявление другого заболевания (флегмоны стопы, острого тромбофлебита, подагрического артрита, ревматических поражений суставов и др.)?
- При наличии рентгенографических признаков деструкции кости имеет она неинфекционную (ОАП) или инфекционную (остеомиелит) природу?
Для решения первого вопроса необходимы данные рентгенографии стоп (хотя в острой фазе могут присутствовать лишь неспецифические изменения в виде остеопороза). Магнитно-резонансная томография и сцинтиграфия скелета стопы выявляют микропереломы, воспалительные изменения, усиление кровотока в пораженных костях.
Возможна оценка биохимических маркеров распада костной ткани (гидроксипролина, дезоксипиридинолина, фрагментов коллагена и др.). С аналогичной целью могут использоваться и маркеры перестройки костной ткани, отражающие активность остеобластов (то есть остеосинтеза), — костный изофермент щелочной фосфатазы и др. Но уровень этих веществ во многом зависит от активности процессов распада костной ткани в скелете в целом.
Очевидно, что изменения, характерные для других заболеваний: признаки острого тромбофлебита при УЗДГ венозной системы, типичная клиника подагрического артрита (с болевым синдромом и лихорадкой, соответствующей рентгенологической и биохимической картиной) и прочие — делают диагноз ОАП менее вероятным.
Для остальных случаев наиболее приемлемым на сегодняшний день алгоритмом диагностики ОАП в острой фазе можно считать следующий [9]:
При возникновении у больного сахарным диабетом одностороннего отека стопы (особенно при неповрежденной коже) следует обязательно исключить возможность ОАП. При подозрении на ОАП и при повышенном риске ее развития (длительное течение сахарного диабета, выраженная диабетическая нейропатия) целесообразнее назначить лечение сразу, чем через несколько месяцев наблюдать необратимую деформацию стопы.
В острой фазе цель лечения — остановка процессов остеолиза, предотвращение патологических переломов или их консолидация.
Наиболее частая ошибка — назначение вазоактивных препаратов. Эти средства показаны далеко не при всех формах синдрома диабетической стопы (только при ишемической и нейроишемической), а при ОАП способны усилить и без того избыточный кровоток в костной ткани.
Основой лечения ОАП в острой стадии является полная разгрузка конечности до исчезновения признаков воспаления (отека, локальной гипертермии). Адекватная разгрузка обеспечивает консолидацию костных отломков и более важна, чем медикаментозное лечение [3]. Если разгрузка не проводится, наиболее вероятны смещение костных отломков и развитие прогрессирующей деформации стопы, представленной на рис. 2-5. В первые дни и недели заболевания показан строгий постельный режим. В дальнейшем возможна ходьба, но только в специально изготовленном ортезе, переносящем значительную часть нагрузки со стопы на голень. Временная разгрузка в период изготовления ортеза может выполняться с помощью тутора, который отличается от ортеза стандартной формой (продается в готовом виде) и менее плотной фиксацией конечности.
После разрешения отека (обычно через 4 месяца) от ношения ортеза постепенно отказываются, а пациенту разрешают ходить в индивидуально изготовленной ортопедической обуви (рис. 7).
Стандартным методом разгрузки конечности при ОАП в большинстве зарубежных стран, особенно англоязычных (США, Великобритания, Австралия и др.), является применение фиксирующих повязок из полимерных материалов, по свойствам аналогичных гипсу (Тоtаl Соntасt Саst). Но даже при наличии высококвалифицированного персонала, проводящего эту процедуру, метод чреват развитием повреждений кожи (пролежней) под иммобилизирующей повязкой в 10% случаев.
В острой фазе ОАП применяются лекарственные препараты, влияющие на метаболизм костной ткани.
Тормозят процесс резорбции костной ткани бифосфонаты и кальцитонин.
Отечественный бифосфонат первого поколения ксидифон (этидронат) отличается доступной ценой. Назначается по 15-25 мл готового раствора натощак прерывистыми курсами (например, первые 10 дней каждого месяца), так как постоянный его прием создает риск остеомаляции. Современные бифосфонаты — фосамакс (алендронат) и другие — применяются в постоянном режиме и более эффективны. Доза фосамакса — 10,0 мг (одна таблетка) натощак ежедневно. Имеются сообщения о внутривенном применении бифосфонатов [бонефос (клодронат)] при ОАП.
Кальцитонин (миакальцик) применяется подкожно или внутримышечно по 100 МЕ один раз в день (обычно 1-2 недели), далее — в виде назального аэрозоля по 200 МЕ ежедневно.
Образование костной ткани стимулируют активные метаболиты витамина Д3 (альфа Д3-Тева и др.) и анаболические стероиды.
Альфа Д3-Тева применяется по 0,5-1 мкг/сут (2-4 капсулы) после еды. Альфа Д3-Тева способствует улучшению абсорбции кальция в кишечнике и активации процессов костного ремоделирования, обладает способностью подавлять повышенный уровень паратиреоидного гормона, усиливать нервно-мышечную проводимость, уменьшая проявления миопатии. Длительная терапия Альфа Д3-Тева способствует уменьшению болевого синдрома, повышению мышечной силы, координации движений, снижению риска падений и переломов костей. Частота побочных реакций на фоне длительной терапии Альфа Д3-Тева остается низкой.
Анаболические стероиды (ретаболил, неробол) назначают в виде инъекций один раз в неделю в течение 3-4 недель.
Препараты кальция самостоятельного действия на метаболизм костной ткани не оказывают, поскольку включение кальция в состав костной ткани регулируется соответствующими гормонами. Эти препараты применяются как вспомогательные для обеспечения достаточного потребления кальция при лечении патологии костной ткани (которое должно составлять с учетом всех пищевых продуктов 1000-1500 мг/сут). Наибольшей биодоступностью обладают лактат и карбонат кальция. Они входят в состав препаратов кальций-Сандоз форте, витрум-кальциум и кальций-Д3-Никомед, которые можно назначать по одной таблетке в день (около 500 мг элементарного кальция). Последний из названных препаратов содержит также витамин Д3, но в профилактических дозах, поэтому это средство следует рассматривать в первую очередь как источник кальция. Препараты кальция принимают во второй половине дня, так как именно в это время происходит их максимальное усвоение. Глюконат кальция (таблетки по 100 мг) стоит недорого, но отличается низкой биодоступностью, из-за чего необходимая суточная доза препарата составляет 10 таблеток.
Кальцитонин и бифосфонаты способны вызывать гипокальциемию, витамин Д3 и препараты кальция — повышать уровень кальция в крови. Поэтому необходимо определение уровня ионизированного кальция до начала лечения и ежемесячно на его фоне (в современных лабораториях этот показатель определяется в капиллярной крови). Обычно применяется комбинация какого-либо из ингибиторов резорбции, витамина Д3 и препаратов кальция. В зависимости от уровня ионизированного кальция дозы тех или иных препаратов увеличиваются или уменьшаются. Продолжительность лечения составляет 4-6 месяцев.
Вспомогательные средства (НПВС, эластичное бинтование конечности, иногда диуретики) применяются в целях устранения отека.
Рентгенотерапия пораженных суставов позволяет достаточно быстро купировать воспалительные явления. Однако, по данным ряда плацебо-контролируемых исследований, факт улучшения прогноза течения ОАП после рентгеновского облучения не подтвердился. Поэтому рентгенотерапию следует применять только в сочетании с адекватной разгрузкой конечности.
Оптимальным результатом лечения, начатого в острой фазе, является предотвращение переломов или консолидация отломков. О результатах лечения позволяют судить изменения клинической картины и контрольная рентгенография через 4-6 месяцев от манифестации заболевания.
После стихания воспалительных явлений сохраняется повышенный риск ОАП (в этой же или других зонах). Помимо общих профилактических мер (см. ниже) целесообразно носить ортопедическую обувь, уменьшающую нагрузку на суставы стопы (в первую очередь, предплюсны) при ходьбе.
В том случае, если процесс находится на второй или третьей стадии, основной целью лечения становится предотвращение осложнений ОАП. При наличии деформаций стопы необходима сложная ортопедическая обувь с внутренним рельефом, повторяющим аномальную форму стопы. Ригидная подошва с так называемым перекатом — приподнятой передней частью — препятствует дальнейшему смещению костных отломков при ходьбе. Постоянное ношение качественной ортопедической обуви предотвращает развитие трофических язв в местах повышенного давления. Попытки ортопедической коррекции деформаций при ОАП (супинаторы и т. п.) бесперспективны и чреваты быстрым развитием язв.
Предложен ряд методов оперативного вмешательства, направленных на коррекцию деформации стопы при ОАП (артродез, резекция костных структур, создающих повышенное давление на подошвенную поверхность и приводящих к образованию незаживающей язвы), но в России опыт их применения невелик. Несомненным условием использования этих методов является полное стихание воспалительного процесса и остеолиза (так как в противном случае оперативное вмешательство может способствовать появлению новых очагов деструкции). Вероятно, лечение препаратами, укрепляющими костную ткань, создает более благоприятные условия для проведения операции. Однако вопрос о показаниях к хирургическому лечению и его безопасности при ОАП по-прежнему остается спорным. Чаще всего показанием к такому лечению служит тяжелая деформация стопы, делающая невозможным изготовление адекватной ортопедической обуви. В любом случае после оперативного вмешательства необходимо обеспечить полную 3-месячную разгрузку пораженной конечности (постельный режим, далее — Total Contact Cast или его аналог) [3].
Вопрос о методах профилактики в группах риска окончательно не решен. Своевременное выявление остеопении в дистальных отделах конечностей позволило бы восстанавливать костную плотность с помощью соответствующих препаратов. Однако остеопороз скелета стоп при рентгенографии у больных диабетом встречается в десятки раз чаще, чем ОАП, в связи с чем группа пациентов, имеющих показания для профилактического лечения, становится неоправданно большой. Кроме того, недостаточно разработаны методы количественной оценки костной плотности (денситометрии) скелета стоп, без которых невозможно составить представление об изменениях плотности костной ткани на фоне лечения, а также выбрать наиболее эффективные препараты и т. п.
Одиночные или множественные дефекты
Одиночные остеолитические дефекты могут вызываться любым из этиологических факторов, указанных выше. Поэтому при оценке одиночного дефекта необходимо использовать весь диапазон диагностических методов.
При множественных очагах остеолиза круг возможных диагнозов обычно гораздо уже. У молодых людей причиной множественных дефектов костей обычно являются врожденные аномалии или инфекция; эту патологию следует искать в первую очередь.
У больных старше 40 лет причиной множественных дефектов обычно бывают метастазы злокачественных опухолей, миеломная болезнь или метаболические расстройства.
При оценке любых случаев остеолиза следует принимать во внимание следующие факторы: возраст больного, тип пораженной кости и локализацию анатомического дефекта, характер краев и субстрата дефекта, множественный или одиночный характер поражения.
Отдельные формы остеолиза
Как указано выше, установление диагноза заболевания костей проходит обычно по пути создания на основе рентгенологической картины списка возможных диагнозов, а затем постепенного исключения отдельных диагнозов с учетом возраста больного, анамнеза, данных физикального обследования, дополнительных методов исследования.
Кистозный ангиматоз костей (рис.119). Впервые описанный Jacobs и Kimmelstiel в 1953 г., кистозный ангиматоз костей является редким заболеванием, вызывающим остеолиз. Этиология заболевания неизвестна, диагноз обычно ставится в подростковом возрасте (10—15 лет). Мужчины болеют в 2 раза чаще, чем женщины, причем более чем у половины больных в анамнезе имеются переломы костей.
Ангиоматозным дефектам костей могут сопутствовать аналогичные изменения в других органах, в частности в селезенки. Ангиоматозным дефектам костей могут сопутствовать аналогичные изменения в других органах, в частности в селезенке.
Обычно диагноз кистозного ангиоматоза поставить трудно. Этим процессом может поражаться любая кость, но чаще всего он встречается в осевых костях скелета. Поражение обычно представлено центральными кистозными просветлениями диаметром от 1—2 мм до нескольких сантиметров с хорошо очерченными склеротическими краями.
В типичных случаях дефекты круглые или овальные и расположены в костно-мозговом канале. Субстрат дефекта не определяется. Дифференциальный диагноз в этих случаях проводится с эозинофильной гранулемой, полиостозной фиброзной дисплазией, метастазами и множественной миеломой. Для подтверждения диагноза требуется биопсия.
Приобретенные повреждения костей
Воспалительные изменения
Это заболевание может проявляться в двух формах: острый гематогенный остеомиелит и вторичный, или хронический, остеомиелит вследствие распространения инфекции на кость из мягких тканей.
Острый гематогенный остеомиелит (рис. 120). Это заболевание чаще встречается у детей младшего и школьного возраста, распространенность его возросла в связи С широким использованием внутривенных катетеров.
Чаще всего источником инфекции является золотистый стафилококк, реже — возбудители туберкулеза, сифилиса, стрептококк. Чаще всего процесс локализуется в позвонках, крестцово-подвздошном сочленении, симфизе, грудино-ключичном сочленении, хотя нередко встречается и поражение длинных костей.
Очаг остеомиелита обычно возникает в области дистальных метафизов, или аналогичных зонах в костях, не имеющих собственных метафизов. В этих участках обычно мало артериальных и венозных коллатералей, поэтому кровоток замедлен. Бактерии эмболизируют мелкие ветви сосудов, вызывая инфекционный процесс.
В первые три дня заболевания не обнаруживается рентгенологически достоверных изменений костей. В подозрительных случаях на этих ранних сроках можно попытаться использовать сканирование костей с радиоактивными изотопами. У взрослых прежде всего возникает отечность в глубине мягких тканей, прилежащих к пораженной кости.
У детей эпифизарная пластинка часто служит барьером для распространения инфекции в соседний состав, но у взрослых к остеомиелиту нередко присоединяется септический артрит. Разумеется, как упоминалось выше, клиническая картина может оказать большую помощь при постановке диагноза острого гематогенного остеомиелита.
Иногда в случаях острого гематогенного остеомиелита сразу, без острой фазы, может сформироваться хроническая костная полость (абсцесс Броди). В этом случае ведущей жалобой является боль в пораженной области, рентгенологическая картина может быть разнообразной. Дефект обычно полиостью прозрачен, размеры его колеблются.
Он располагается в диафизе или метафизе кости, края могут не дифференцироваться или же, наоборот, определяется плотная граница склероза вокруг абсцесса (рис. 121). Кроме того, вокруг полости может определяться широкая полоса периостальной реакции, которая рентгенологически напоминает остеоидную остеому.
Вторичный остеомиелит (рис. 122). Эта форма инфицирования кости встречается чаще всего у больных сахарным диабетом или с сосудистой недостаточностью. В этом случае костная ткань, прилежащая к участку инфицированных мягких тканей, также подвергается вторичной инфекции, разрушается или лизируется.
Травмы
При этой патологий редко встречаются истинные участки остеолиза. Разумеется, при любом переломе происходит определенный остеолиз в рамках реорганизации костной ткани перед образованием костной мозоли. Обычно в анамнезе больного обнаруживаются указания на травму.
При повторной травме могут возникать значительная резорбция и лизис костной ткани, чаще всего они наблюдаются при острой нейропатической артропатии.
Острая нейропатическая артропатия (рис. 123). Первое описание нейропатической артропатии было сделано Шарко в 1868 г. Первичную причину заболевания связывают с двумя основными процессами: нарушением чувствительной иннервации и повторной травмой.
В свое время одним из основных заболеваний, предрасполагающих к этой патологии, был сифилис. В последние годы это место занял сахарный диабет. Нейропатические изменения в суставах встречаются приблизительно у 6% больных диабетом. Картина нейропатической артропатии обычно развивается в течение нескольких лет.
Острая нейропатическая артропатия является одним из вариантов артрита Шарко, характеризуется фрагментацией суставных концов кости и подвывихом, которые развиваются менее чем за 2 мес. Из-за быстрой динамики этот процесс часто путают с травмой и инфекцией и оценивают ошибочно.
Рентгенологические изменения включают разрушение кости, фрагментацию ее и исчезновение суставного хряща. В окружающих мягких тканях можно обнаружить кальцифицированные продукты распада костей, иногда они распространяются по межмышечным щелям. Чаще всего острой нейропатической артропатии подвержены тазобедренные, коленные суставы.
Диагноз острой нейропатической артропатии можно заподозрить на основании известных предрасполагающих факторов и быстрого развития типичной рентгенологической картины.
Диабетическая остеоартропатия представляет собой деструктивное поражение костной и хрящевой суставной ткани на фоне сахарного диабета. При длительном повышенном уровне сахара в крови возникает метаболическая патология, при которой происходит прогрессирующее и нередко безболезненное разрушение суставов. Отсутствие боли связано с иннервацией сочленения – повреждением нервных окончаний из-за заболевания. В основном поражаются стопы, плюсневые и предплюсневые кости (90%), но патологический процесс может охватить любые суставы (коленный, тазобедренный), хотя и гораздо реже. В 20% случаев наблюдается двустороннее поражение. Вероятность развития диабетической остеоартропатии повышается, если человек болен диабетом более 8 лет и лечение не осуществлялось либо проводилось неэффективно.
Поражение костной системы наблюдается у 58% больных диабетом 1 типа, у 24% с диабетом 2-го типа. Рентген показывает нарушения только после того, как 20-40% костной ткани уже утрачено. КТ более информативна, поскольку позволяет выявить содержание минеральных веществ как в трубчатой, так и в компактной костной ткани. Своевременное распознавание первых признаков позволит эффективно остановить разрушение и избежать инвалидизации, которой часто заканчивается поражение суставов на фоне диабета.
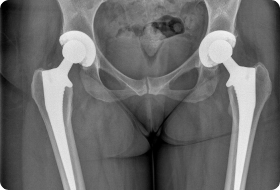
Механизм поражения суставов
Причинами поражения суставов при диабете называют нарушение иннервации и аномально ускоренный кровоток в костной ткани, приводящий к остеопении локального масштаба. Также провоцирующую роль играют рецидивирующие травмы: даже самые незначительные способны запустить процесс остеолиза, разрушающий сустав. Протеингликановый состав костной, а также хрящевой ткани изменяется при дефиците инсулина. Основным механизмом, формирующим патологические нарушения в костях и сосудах, является гликирование белков.
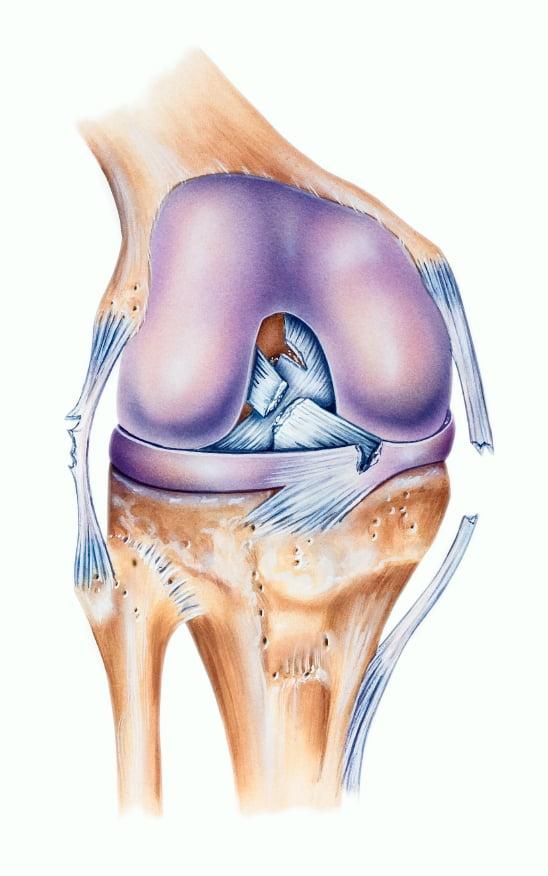
На первой стадии наблюдается отек, умеренная гиперемия. Боль и лихорадка отсутствуют. Рентгенологическое исследование не выявляет деструктивных изменений. Наблюдается остеопороз.
На второй стадии рентген выявляет нарушения в виде:
- умеренного остеопороза эпифизов;
- субхондрального склероза, сопровождающегося появлением краевых остеофитов;
- остеолиза и секвестрации;
- разрастаний соединительной ткани;
- асептических некрозов;
- патологической перестройки тканей кости, ее фрагментации.
Нарушение чувствительности провоцирует растяжение связочного аппарата, от чего сустав расшатывается. На третьей стадии начинается выраженная деформация, вывихи, возможны спонтанные переломы костей. Сустав буквально распадается на части, остается только заменить его на искусственный. Другими способами подвижность не восстановить.
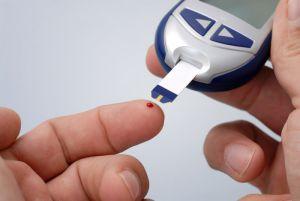
Лечение
Основой терапии при сахарном диабете является постоянный контроль над уровнем сахара. Для этого существуют специальные приборы, позволяющие быстро определить его уровень. Только при условии нормализации сахара можно рассчитывать на результат при лечении суставов, если степень их разрушения еще позволяет проводить консервативную терапию.

Больному необходимо регулярно заниматься гимнастикой, проводить сеансы массажа и самомассажа, а также использовать аппаратную физиотерапию для восстановления чувствительности.
Хондропротекторы при выраженных дегенеративных процессах в суставе не помогут, поэтому их использование в большинстве случаев бессмысленно. Для снятия боли назначаются противовоспалительные и обезболивающие средства, с их помощью спадает отечность и немного улучшается подвижность. Применяются кортикостероидные препараты путем инъекционного введения непосредственно в сустав.
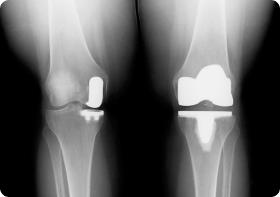
Хирургическое лечение
Хирургическое вмешательство при сахарном диабете возможно только при нормализации уровня сахара. Если диабет скомпенсирован и противопоказаний со стороны сердечно-сосудистой системы и внутренних органов не выявлено, то можно проводить замену сустава. Заключение дает эндокринолог по результатам обследования. При нормализации уровня сахара все процессы заживления у больных диабетом происходят также, как и у здоровых людей, но контроль очень важен не только перед операцией, но и сразу же после нее.
Есть риск отторжения, если у пациента преклонный возраст, заболевание продолжается более 10 лет. Однако современные технологии позволяют свести его к минимуму. Эндопротезирование производится при помощи фиксации на цемент, в котором содержится антибиотик (например, цифуроксим). Частота осложнений при введении данного метода существенно сократилась.
Существенно осложняет процедуру эндопротезирования лишний вес, который часто превышает все нормы при сахарном диабете. Это может стать противопоказанием к операции, поскольку не только затрудняется доступ к суставу, УЗИ-навигация и последующее закрытие тканей, но и ухудшается приживаемость из-за высокой нагрузки. Часты случаи развития ранних инфекций и смещения эндопротеза, велика вероятность, что произойдет перипротезный перелом, повредятся связки сустава, может развиться тромбоз конечности, тромбоэмболия, асептическая нестабильность, вывих головки имплантата.
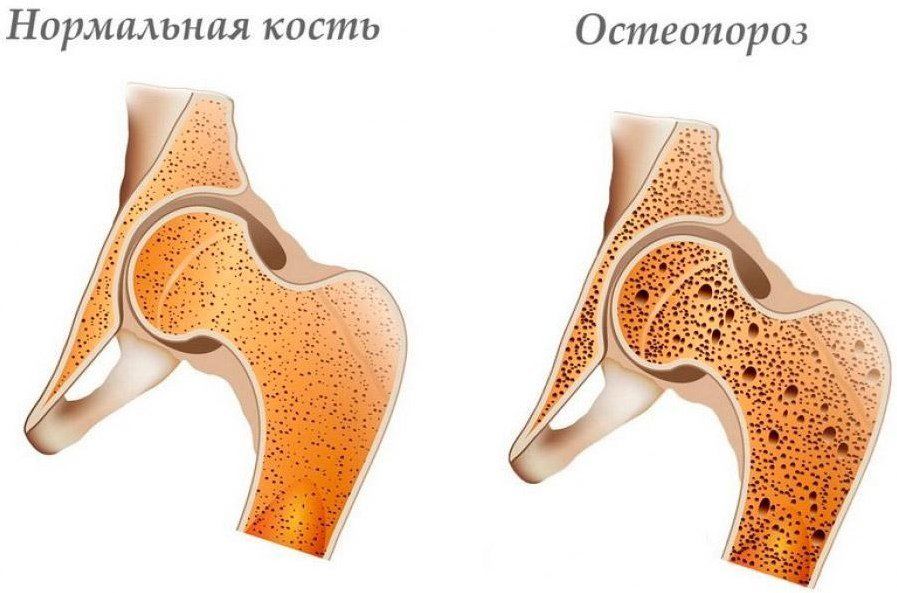
Осложнение сахарного диабета нередко может быть коварнее основного заболевания. В последние годы список таких осложнений пополнила ещё одна болезнь – остеопороз костей. Медики обратили внимание на то, что низкая плотность костей часто диагностируется у пациентов с недостатком инсулина в организме. Профессор, доктор медицинских наук, руководитель Центра остеопороза в Поволжье Виллорий Иванович Струков уверен: остеопороз вторичен, поэтому залогом его успешного лечения является устранение основного, первичного заболевания. В данном конкретном случае – сахарного диабета.
Как недостаток инсулина влияет на плотность костей
Каким образом недостаток инсулина влияет на плотность костей?
Установлено, что инсулин играет весьма важную роль в процессах костного ремоделирования:
При снижении уровня инсулина в крови развиваются остеопения – небольшое снижение минеральной плотности кости — и более тяжёлая патология – остеопороз, характеризующаяся значительной потерей костной массы и увеличенным риском переломов .
Остеопороз как осложнение сахарного диабета. Механизм развития заболевания
Рассмотрим механизм развития остеопороза при сахарном диабете.
Недостаток инсулина и связанные с ним нарушения обменных процессов создают благоприятные условия для снижения плотности костей. Запускается сразу несколько механизмов, влияющих на метаболизм костной ткани и повышающих риск переломов.
Дополнительными факторами риска развития костных патологий и возникновения переломов при сахарном диабете являются неправильное питание , низкая масса тела, ухудшение зрения при тяжёлых поражениях сетчатки глаза и диабетической катаракте, нарушение координации движений и способности организма поддерживать обычный уровень артериального давления в вертикальном положении, мышечная слабость, особенно часто встречающиеся у пациентов с заболеванием I типа.
Ряд специалистов (Schwait A. V., Pittas A. G., Lau J., Hu F., Dawson-Hughes B.) отмечают, что у женщин с сахарным диабетом I типа, чей возраст перешагнул рубеж в 50 лет, риск перелома шейки бедра в 7 раз выше, чем у их сверстниц, не страдающих этим заболеванием. У тех же представительниц прекрасной половины человечества, у кого в период менопаузы диагностирован сахарный диабет II типа, риск перелома шейки бедра почти вдвое выше, чем у здоровых дам.
Признаки остеопороза при сахарном диабете
Какие признаки остеопороза могут проявиться при сахарном диабете?
Осложнение сахарного диабета, прежде всего, даёт о себе знать ноющей болью в области крестца и поясницы или за грудиной, которая усиливается при ходьбе и нагрузке. Могут также беспокоить болевые ощущения в суставах, нарушения походки, осанки, деформация грудной клетки, хромота, невозможность полностью распрямить спину, беспричинная усталость, постоянное желание полежать на спине, затруднённость дыхания, изжога, запоры. Возможно уменьшение роста на пару сантиметров в год.
Особенности заживления переломов при диабете
Заживление остеопоротических переломов при диабете протекает гораздо тяжелее, чем при его отсутствии, и отличается рядом особенностей.
Первое, к чему нужно быть готовым — это гораздо более длительный период срастания костей. Причина тому – нарушение процессов регенерации в организме. Скорейшему выздоровлению нередко препятствует и присоединившаяся инфекция, с которой не под силу справиться ослабленной при диабете иммунной системе. При этом возможно неправильное срастание костей, замещение костных тканей непрочными соединительными и развитие деформаций повреждённой конечности. Бактерии и микобактерии, проникнувшие в кость и костный мозг , могут также стать виновниками развития гнойно-некротического процесса – остеомиелита. Но даже если фрагменты сломанной кости всё-таки успешно срастутся, костные ткани в месте перелома по-прежнему останутся слабыми и хрупкими, возникнет риск их повторного травмирования. К тому же перелом кости способен спровоцировать обострение диабетической болезни.
Гимнастика для профилактики остеопороза при сахарном диабете
Специальных схем лечения остеопороза при сахарном диабете не существует. Основные задачи больного, у которого диагностировано осложнение сахарного диабета – держать под контролем основное заболевание, не допускать кризисных состояний, резкого повышения или понижения уровня сахара в крови, попытаться снизить факторы риска (курение, злоупотребление алкоголем или кофе, низкая физическая активность, длительное состояние неподвижности, лишний вес и прочие). Американская ассоциация антивозрастной медицины разработала комплекс гимнастики для профилактики остеопороза при сахарном диабете. Выполнять её нужно медленно и неторопливо.
- Исходное положение (И. п.) — стоя, спина прямая, плечи и грудь расправлены, руки – вдоль туловища, ноги – на ширине плеч. Выдох: поднять руки через стороны вверх, потянуться за ними всем телом, подняться на носки, голову чуть поднять (не запрокидывать!). Вдох: медленно вернуться в исходное положение, сначала – туловище, затем – руки. Повтор упражнения – 4-5 раз.
- И. п. – как в предыдущем упражнении. Одну руку поднять вверх над головой, другая по-прежнему внизу. Менять положение рук. Важно не задерживать дыхание. Повтор – 8-10 раз.
- И. п. как в первом упражнении. Выдох: поднять руки в стороны до уровня плеч, ладони повёрнуты вниз, пальцы вместе. Вдох: медленно опустить руки. Повтор – 5-7 раз.
- И. п. как в первом упражнении. Поднять руки на уровень груди и согнуть их перед грудью, ладони смотрят вниз, пальцы соединены между собой. Вдох: локти — в стороны. Выдох: локти — перед грудью. Повтор – 6-8 раз.
- И. п. как в первом упражнении. Поднять прямые руки перед собой на уровень груди, пальцы вместе ладони — вниз. Выдох: поворот туловища вместе с руками вправо. Вдох: туловище возвращается в прямое положение. Выдох: поворот туловища влево. Повтор: 8-10 раз.
- И. п. – стоя прямо, ноги – на ширине плеч, руки – на поясе. Вдох: развести прямые руки в стороны, слегка повернуть туловище вправо. Выдох: медленно вернуться в исходное положение. Повтор – 3-4 раз в каждую сторону.
- И. п. – стоя прямо, плечи расправлены. Выдох: наклон вперёд (не слишком низко), вдох – вернуться в исходное положение. Повтор – 8-10 раз.
- И. п. – сидя на стуле, спина прямая, руки опираются на сиденье. Выдох – поднять согнутую ногу к груди. Вдох: опустить ногу. Затем – то же самое другой ногой. Повтор – 10-12 раз каждой ногой.
- И. п. – как в предыдущем упражнении. Выдох: выпрямить одну ногу перед собой, потянуть носок вперёд, вверх. Вдох: опустить ногу. Затем – повторить движение другой ногой. Повтор – 10-20 раз каждой ногой.
- Неторопливая ходьба на месте. Можно на вдохе поднимать руки вверх, на выдохе опускать. Повтор – 5-10 минут.
Регулярное выполнение перечисленных упражнений позволит повысить тонус мышц спины, живота, ног, сформировать мышечный корсет, поддерживающий позвоночник, избавиться от болей в спине, улучшить подвижность суставов , обмен веществ, кровоснабжение и работу сердца.
Физические нагрузки необходимы для нормального костного ремоделирования и поддержания баланса мышц. Они благоприятно влияют на уровень глюкозы в крови, позволяют держать под контролем массу тела. Всё это вкупе способствует уменьшению риска падения.
Стандартная терапия снижения плотности костей включает в себя применение препаратов на основе бисфосфонатов , направленных на торможение процессов разрушения старой костной ткани, заместительной гормональной терапии , а также кальцийсодержащих препаратов с (или без) витамином D. Все названные группы лекарственных средств грубо воздействуют на естественные физиологические процессы, происходящие в человеческом организме и отличаются большим количеством тяжелейших побочных эффектов вплоть до онкологии. Между тем на современном фармацевтическом рынке появилась серия натуральных средств от остеопороза, позволяющих эффективно и безопасно укрепить костную ткань, предупредить переломы .
Читайте также:


