Остеоартроз вторичный синовит диагноз
Воспалительные процессы внутри суставов, чаще всего в коленном суставе, могут приводить при артрозе к синовиту. Причем, если говорить о коленном синовите, то поражается правое колено, реже – левое, и, крайне редко – оба коленных суставах. Это объясняется частым травмированием нижних конечностей, где после травм попадают инфекции, скапливается жидкость в синовиальной оболочке, ведущая к деформации тканей.

Виды синовита
Помимо распространенного коленного синовита при артрозе случаются:
- Тазобедренный синовит;
- Голеностопный;
- Плечевой;
- Локтевой;
- Крайне редко локализуется в височно-нижнечелюстном суставе (ВНЧС), лучезапястных суставах.
Причины и симптомы патологии

Этиология синовита и артроза во многом схожа. На развитие болезни влияют такие факторы, как инфекции, полученные травмы (растяжения, вывихи, переломы) костей, особенно, нижних конечностей; нарушение обмена веществ и иммунной системы. Артрит и подагра также провоцируют возникновение синовита коленного или тазобедренного сустава при артрозе.
Распознать синовит можно по тупой боли в коленном суставе, где скопилась жидкость. Впрочем, далеко не всегда болевой симптом проявляется сразу. Заметными признаками будут скованность суставов, повышение температуры тела, припухлость колена или другого поражённого сочленения костей. При обследовании у врача для подтверждения диагноза придется пройти пункцию – взятию внутрисуставной жидкости из синовиальной оболочки для анализа.
Синовит при артрозе довольно легко спутать с другими заболеваниями, поэтому требуется тщательное обследование.
Лечение недуга
После подтверждения диагноза и выяснения причин, вызвавших артроз с синовитом, следует немедленно начать лечение. Оно должно быть комплексным и многосторонним, чтобы не привести к печальным последствиям.

Первым делом, обычно лечащий врач назначает противовоспалительные нестероидные препараты (НПВП): диклофенак, ибупрофен, кетопрофен, индометацин и др. Проводят так называемую иммобилизацию больных суставов, т.е. ограничение подвижности, дабы сохранить хрящевые и мягкие ткани опорно-двигательного аппарата. При запущенном синовите потребуется лечение с помощью кортикостероидов.
Нетрадиционное лечение синовита
Народная медицина тоже вносит свой незаменимый вклад для борьбы с воспалением синовиальной оболочки. Обычно это физиотерапевтические средства, основанные на компрессах, примочках, настоев на лекарственных травах и растений: чистотел, окопник, чабрец, душица, омела, зверобой, сабельник, корни аира и солодки и др.

Например, известен такой рецепт с использованием березовых листьев и пижмы, омелы, а также грецких орехов, которые берутся в одинаковых частях. Заливают кипятком, дают постоять час. Принимают в течение дня по нескольку раз. Полезный отвар, который повышает ослабленный иммунитет, насыщает организм нужными веществами, усиливает проникаемость в капиллярах.
Простой способ помочь суставам при синовите и артрозе связан с лавровым маслом, которое можно получить в домашних условиях. Для этого измельчают две-три столовых ложки лаврового листа, заливают стаканом оливкого или подсолнечного масла. Плотно закрывают полученную смесь и оставляют настаиваться на семь дней. Настойку процеживают, используют по назначению в качество растирочного средства ежедневно.
Заключение
На синовит артроз оказывает значительное влияние, и наоборот: синовит очень часто провоцирует артроз, особенно, гонартроз коленных и тазобедренных суставов. Причины и признаки могут напоминать другие болезни, вследствие чего диагностика должна быть проведена достаточно масштабно и профессионально. Исходя из этиологии синовита, общего состояния организма пациента, врач назначит лечение. Не стоит пренебрегать этим банальным советом: не занимайтесь самодиагностикой и самолечением! Однако помочь своему организму народными методами вместе с консервативным лечением будет не лишним.
Весьма распространенным заболеванием стал синовит – воспалительный процесс, поражающий синовиальную оболочку суставов. При нем возникает выпот, он дальнейшем собирается внутри полости соединения. Чаще вторичный синовит возникает у людей с диагнозом остеоартроз. Больше всего возникновению данного заболевания подвергается коленный сустав. Такая частотность связана с сильными нагрузками, приходящимися именно на данное соединение.
Синовит коленного сустава бывает различных сложностей. Это зависит от многих причин:
- Развитие воспаления на основе аутоиммунных, метаболических болезней (бурсита, артрита);
- Развитие воспаления, исключая проявления наружных повреждений (малого количества суставной жидкости, травмы мениска, хряща).

Симптомы заболевания
Характерными признаками наличия заболевания являются:
- Наличие выпота, который имеет светло-желтый оттенок, умеренную вязкость;
- Возникновение припухлости;
- Деформация соединения;
- Тянущая болезненность сустава;
- Ограничение движения;
- Подопревание.
Вышеперечисленные симптомы длятся примерно 3-4 дня, но в исключительных случаях — 10-15 дней. Возникшее повторное нагноение в воспаленном суставе может возникать через 2-3 месяца. Во избежание рецидива необходимо своевременное постановление диагноза и прохождение курса лечения под наблюдением специалиста. Из-за подобных осложнений развиваются склеротические изменения внутри пораженной оболочки. При этом ухудшается состояние хряща, синовиальной жидкости.
Последствием развития вторичного синовита является возникновение фиброзных изменений внутри периартикулярных тканей. Конечные этапы воспалительного процесса характеризуются отрывом фрагментов остеофитов. В дальнейшем они будут располагаться в полости соединения. Если же они попадают в щель сустава, то больной может лишиться способности двигаться и возникнут резкие боли.
При наличии диагноза синовит коленного сустава наблюдается смещение оси конечности. Больной жалуется на ограничение движения, наблюдается гипотрофия региональных мышц, смещение надколенника, утолщение периартикулярных тканей. Вследствие этих процессов возникает деформация соединения.
Диагностика
Исследование заключается в нескольких этапах.
На первом этапе проводится осмотр доктором для определения следующих пунктов:
- Изменение величины сустава;
- Деформация соединения;
- Болезненность при движении;
- Деформация соединения.
- Второй этап включает лабораторные исследования:
- Общий анализ крови;
- Определение биохимических маркеров.
Третий этап заключается в рентгенологическом методе. Он состоит из:
- КТ;
- УЗИ;
- МРТ.
На последнем, четвертом этапе, проводится пункция. Именно она является основным вариантом диагностики, способным обнаружить воспаление в соединении, определить инфекционного возбудителя, а затем степень его чувствительности по отношению к применяемым средствам от бактерий.

Пункция коленного сустава выполняется таким образом:
- Внутрь воспаленного соединения, для взятия жидкости, вводится специальная игла;
- Выполнение анализа отобранной жидкости;
- Определение в изъятом экссудате уровня белка, количества кровяных телец, а также присутствие инфекции.
В роли дополнительных вариантов диагностики также применяют:
- Биопсию;
- Артрографию;
- Артропневмографию.
Лечение
Изначально, для определения причины, спровоцировавшей возникновения коленного синовита, врач назначает комплексное обследование. На его основании он устанавливает курс лечения для каждого отдельного случая заболевания.
Курс лечения включает такие этапы:
- Проведение пункции воспаленного сустава. С использованием специальной иглы (без анестезии) отсасывается синовиальная жидкость;
- Выполняется иммобилизация коленного сустава (шины, давящие повязки, гипсовые лонгеты). Этот этап длится до 7 дней;
- Медикаментозное лечение;
- Хирургическое вмешательство (при необходимости).


Начнут восстанавливаться хрящевые ткани, снизится отечность, вернется подвижность и активность суставов. И все это без операций и дорогостоящих лекарственных препаратов. Достаточно лишь начать.
Остеоартроз — хроническое невоспалительное заболевание суставов неизвестной этиологии, характеризующееся прогрессирующей дегенерацией суставного хряща, структурными изменениями субхондральной кости и сопутствующим реактивным синовитом
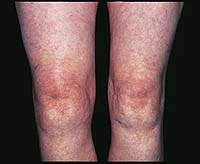 |
| Рисунок 1. Синовит (припухлость, гиперемия, локальное повышение температуры) правого коленного сустава при ОА |
При прогрессировании ОА в результате происходящих дегенеративных процессов хрящ размягчается, разрыхляется. В нем появляются трещины, простирающиеся до кости.
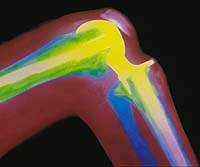 |
| Рисунок 2. Эндопротез коленного сустава. Рентгенограмма |
Особая роль в патогенезе ОА отводится синовиту, морфологически характеризующемуся умеренно выраженными пролиферативными и экссудативными реакциями (гиперплазией синовиальной оболочки и ее мононуклеарной инфильтрацией), наиболее выраженными в местах прикрепления синовии к хрящу с последующим исходом в склероз и липоматоз. В субхондральной кости выявляются микропереломы, утолщение костных трабекул и остеофитоз. Экссудативно-пролиферативные реакции как в субхондральной кости, так и в синовиальной оболочке протекают на фоне нарушений региональной гемодинамики и микроциркуляции с развитием тканевой гипоксии. В последующем прогрессирование болезни принимает, по сути, необратимый характер.
Боль, деформация и тугоподвижность сустава являются основными клиническими проявлениями ОА.
Боль в суставе — наиболее частый и выраженный симптом при ОА, носит неоднородный характер. Причинами ее могут быть деструктивные процессы в хрящевых и субхондральных структурах, нарушения микроциркуляции, особенно при затруднении венозного кровотока в спонгиозной части кости, фиброз капсулы сустава, воспалительный процесс в мягких околосуставных тканях, спазм близлежащих мышц и реактивный синовит.
В целом для заболевания характерен механический ритм болей — возникновение боли под влиянием дневной физической нагрузки и стихание за период ночного отдыха, что связано со снижением амортизационных способностей хряща и костных подхрящевых структур к нагрузкам. При этом происходит прогибание костных балок в сторону спонгиозной кости.
Возможны непрерывные тупые ночные боли, связанные с венозным стазом в субхондральной спонгиозной части кости и повышением внутрикостного давления.
Рефлекторный спазм близлежащих мышц, а также развитие реактивного синовита вызывают постоянные боли.
Реактивный синовит и воспалительный отек параартикулярных тканей усугубляют клиническую картину. При наличии синовита, помимо боли в суставе как при движении, так и в покое, характерны утреннняя скованность, припухлость сустава, локальное повышение кожной температуры. С прогрессированием заболевания рецидивы синовита учащаются.
Обычно ОА развивается медленно и начинается как моноартикулярное заболевание, но через некоторое время в патологический процесс включаются и другие суставы, чаще всего те, которые компенсаторно брали на себя повышенную механическую нагрузку, чтобы разгрузить первоначально заболевший сустав.
Клинически значимыми и инвалидизирующими формами ОА являются гонартроз и коксартроз. Клиническая картина ОА определяется конкретным суставом и группой суставов, вовлеченных в патологический процесс.
Среди неинвазивных методов диагностики гонартроза ведущее место по информативности занимает ультразвуковое двумерное сканирование коленных суставов, которое используют для объективизации и детализации характеристики вторичного синовита, являющегося прогностически неблагоприятным фактором, усугубляющим процессы дегенерации хряща. Наряду с диагностикой наличия синовиальной жидкости можно определить ее характер, особенно над bursa suprapatellaris и появлением жидкости над мыщелками бедренной кости, толщину и характер синовиальной оболочки; при этом ее утолщение при 0,4 см и более, а также контуры суставных поверхностей с учетом однородности контуров хряща на мыщелках бедренной кости и толщину хряща принимают за патологию. Ультразвуковое исследование суставов позволяет также уточнить характер и степень воспалительного процесса для выработки адекватного лечения.
Артроскопия в артрологии для диагностики воспалительных и дегенеративных заболеваний суставов, к сожалению, применяется недостаточно широко и, более того, не выявляет качественных отличий от воспаления синовии при других артритах. Существенно расширяет диагностические возможности артроскопии использование прицельной биопсии, а визуальный контроль позволяет получить фрагмент синовиальной ткани или хряща, наиболее адекватно отражающих развивающийся в суставе патологический процесс, но при этом данная процедура редко показывает распространенность патологического процесса. Артроскопия используется и с лечебной целью — с целью промывания полоски коленного сустава, при которой удаляется хрящевой детрит, а также фрагменты мениска, утолщенной и воспалительной синовии; выполняется аброзивная артропластика при гонартрозе. При коксартрозе ультразвуковое исследование отмечает, наряду с наличием и характером синовиальной жидкости, эхоуплотнение капсулы синовиальной оболочки, хрящевой губы, остеофиты. Однако следует сказать, что как ультразвуковые, так и эндоскопические признаки не могут считаться специфическими при гонартрозе и коксартрозе, поскольку они встречаются и при других заболеваниях суставов, как воспалительного, так и дегенеративного характера.
Основными целями терапии ОА являются: замедление прогрессирования дегенерации хряща и максимально возможное сохранение функции сустава. Терапевтическая тактика при ОА состоит из трех компонентов:
- механическая разгрузка пораженных суставов;
- купирование синовита;
- предотвращение прогрессирования заболевания.
Задачи, которые ставятся при составлении комплекса лечебных мероприятий, можно решать с учетом следующей шкалы приоритетов: болевой синдром, синовит, нарушение трофики суставов и местного кровотока, гипотрофия и гипотония мышц, контрактура.
Режим. Механическая разгрузка сустава является определяющим фактором как в уменьшении болевого синдрома, так и в лечении ОА в целом. Сюда входят рекомендации по исключению длительного пребывания в фиксированной позе, долгого стояния на ногах, длительной ходьбы, повторяющихся стереотипных движений, переноса больших тяжестей, ведущих к механической перегрузке определенных зон суставов. В далеко зашедших стадиях заболевания пациенту полезно ходить с тростью, костылями. При выраженных болях в фазу обострения может быть назначен полупостельный режим.
Диета. Четких патогенетических рекомендаций по диете ОА на настоящий момент не существует. Важным условием в лечении ОА коленных суставов является снижение избыточной массы тела. В последнее время рекомендуются пищевые добавки (глюкозамин, хондроитин и др.), но эффективность их требует клинических подтверждений.
В терапии ОА наиболее часто применяются обезболивающие препараты, нестероидные противовоспалительные препараты (НПВП) и средства с хондропротективными свойствами.
В терапии ОА, который сопровождается болевым и воспалительным синдромами, широко применяются НПВП. В настоящее время известно около 100 НПВП различных классов, но поиск новых лекарственных средств этой группы продолжается. Это связано с потребностью в медикаменте, имеющем оптимальное соотношение обезболивающего и противовоспалительного действия и характеризующемся высокой степенью безопасности. В этом плане большой интерес представляет появившийся на российском рынке препарат ксефокам.
Ксефокам — новый НПВП класса оксикамов.
Подобно другим НПВП, ксефокам обладает обезболивающей и противовоспалительной активностью, связанной с подавлением синтеза простагландинов посредством ингибирования циклооксигеназы (ЦОГ).
Так как большинство НПВП подавляют, как правило, и ЦОГ-1 и ЦОГ-2, то развитие гастропатий, а также нарушение функции почек и агрегации тромбоцитов являются запрограммированным фармакологическим эффектом этих препаратов.
Существует достоверная связь между приемом НПВП и развитием патологии верхних отделов ЖКТ: геморрагий, эрозий, язв в желудке (гастропатий), а также эзофагопатий и дуоденопатий, что проявляется болями или чувством тяжести в эпигастральной области, тошнотой, иногда рвотой, изжогой, дисфагией, метеоризмом, диареей и др. Возможно бессимптомное течение гастропатий, в связи с чем увеличивается риск развития таких серьезных осложнений, как кровотечение и перфорация, нередко ведущих к летальному исходу. Кроме того, длительный прием НПВП вызывает энтеропатии и колонопатии с последующим развитием железодефицитной анемии и гипоальбуминемии.
К образованию эрозий и язв приводит подавление НПВП синтеза простагландинов слизистой ЖКТ, что вызывает:
- уменьшение секреции слизистого геля;
- снижение секреции бикарбонатов;
- ухудшение кровотока в слизистой ЖКТ.
Высокий риск возникновения язв ЖКТ отмечается при продолжительной терапии НПВП, но максимален в первый месяц приема препарата. Снижение риска в дальнейшем объясняется, по-видимому, адаптационными механизмами, благодаря которым гастродуоденальная слизистая приобретает способность противостоять повреждающему действию НПВП.
Полагают, что при приеме НПВП нарушается репарация хряща и субхондральной кости за счет угнетения синтеза простагландинов, в частности в зонах микропереломов, с образованием очагов деструкции и кист. При этом, купируя болевой синдром и явления синовита, НПВП не задерживают дегенеративно-дистрофических изменений в суставных тканях пациента.
Установлено, что селективное ингибирование ЦОГ-2 оказывает незначительный эффект при острой боли. В то же время при острой боли концентрация ЦОГ-1 увеличивается в три-четыре раза, поэтому для анальгетического эффекта может иметь значение ингибирование именно этого изофермента. Таким образом, оптимальным сочетанием анальгетического и противовоспалительного эффекта обладают препараты, ингибирующие как ЦОГ-1, так и ЦОГ-2. Ксефокам является наиболее мощным ингибитором обоих изоферментов. Эта способность ксефокама в 100-200 раз превышает таковую у эталонных НПВП, например у диклофенака и пироксикама. При этом соотношение ингибиторной активности ксефокама в отношении ЦОГ-1 и ЦОГ-2 (мера селективности) занимает срединное положение по сравнению с аналогичными показателями других НПВП, что и обеспечивает баланс анальгетической и противовоспалительной активности ксефокама.
Ксефокам угнетает высвобождение свободных радикалов кислорода из активированных лейкоцитов, что усиливает его анальгетическую и противовоспалительную активность.
Обезболивающий эффект ксефокама отчасти связан с его влиянием на центральную нервную систему. Это подтверждается тем, что внутривенное введение лорноксикама (ксефокама) больным с болями в пояснице повышало уровень эндогенных морфинов при одновременном улучшении состояния. Активация системы нейропептидных опиоидов может быть одним из путей реализации анальгетического эффекта ксефокама. По анальгетическому эффекту ксефокам приравнивается к 20 мг морфина, при этом он не оказывает опиатоподобного действия на ЦНС и не вызывает лекарственной зависимости.
Исследования показали, что в терапевтических дозах ксефокам стимулирует синтез протеогликанов, предотвращая дегенерацию суставного хряща. Эта важная особенность ксефокама делает его препаратом выбора при ОА, поскольку известно, что многие НПВП, напротив, отрицательно влияют на хрящ.
Ксефокам практически весь (на 99%) связывается с белками плазмы, тем не менее он активно проникает в суставные полости, где длительное время (10-12 часов) сохраняется в достаточной терапевтической концентрации — даже когда в плазме его концентрация снижается. Это позволяет принимать препарат всего лишь два раза в день. Благодаря короткому периоду полувыведения из плазмы крови (примерно 4 часа) прием ксефокама сопровождается меньшей выраженностью побочных эффектов, так как в период между введениями доз возможно восстановление протекторных физиологических уровней простагландинов, необходимых для защиты слизистой желудка и поддержания нормального кровотока в почках.
Ксефокам полностью метаболизируется в печени, при этом одна треть его неактивных метаболитов выводится почками, а две трети — печенью и кишечником. Такой двойной путь экскреции снижает нагрузку на данные органы и улучшает переносимость ксефокама. После многократного введения ксефокама не наблюдается его кумуляция в плазме, что снижает риск побочных эффектов по сравнению с НПВП, имеющими более длительный период полувыведения. Фармакокинетика ксефокама примерно одинакова у пожилых людей и лиц молодого или зрелого возраста, поэтому не требуется какой-либо коррекции дозы препарата у пожилых.
Клинические испытания подтвердили высокую эффективность и хорошую переносимость ксефокама у больных ОА. В результате месячного приема лекарства в суточной дозе 16 мг уменьшались боль, длительность утренней скованности, улучшалась функция суставов.
К средствам, модифицирующим течение ОА, относятся препараты, в основе действия которых лежат:
- активация анаболических процессов в матриксе хряща
- подавление активности лизосомальных ферментов
- стимуляция синтетических функций хондроцитов.
Традиционно для лечения ОА использовались парентеральные гликозаминогликаны, однако в последнее время предпочтение отдается пероральным препаратам, а именно глюкозаминсульфату и хондроитинсульфату.
При некупируемом реактивном синовите показана пункция сустава, удаление синовиальной жидкости и внутрисуставное введение глюкокортикоидов, которые ингибируют синтез интерлейкина-1 и фактора некроза опухоли-α, участвующих в воспалении и деградации хряща. Широко используются при этом гидрокортизон, метипред, кеналог и дипроспан. Последние препараты характеризуются более выраженным и пролонгированным лечебным действием. Вместе с глюкокортикоидами возможно введение анестетиков (новокаина, лидокаина), действие которых при этом потенцируется. Введение ингибиторов медиаторов воспаления — контрикала (трасилола) или гордокса — благотворно влияет на метаболизм хряща.
В настоящее время рассматривается вопрос о широком внедрении в практику для подавления локального воспаления внутрисуставного введения ксефокама.
Широко применяемые для восстановительного лечения ОА физиотерапевтические методы уменьшают болевой синдром, а также воспалительные процессы и мышечный спазм, улучшают микроциркуляцию, благоприятно воздействуют на метаболические процессы в тканях сустава. При этом используются ультрафиолетовое облучение, электрические токи, переменные магнитные поля, электрофорез и фонофорез лекарственных средств на суставы. При пролиферативных явлениях, вазотрофических расстройствах и контрактурах показаны тепловые процедуры, включая аппликации парафина, озокерита, иловой и торфяной грязи. При отсутствии синовита эффективны морские, радоновые, сульфидные, бишофитные и йодобромные ванны. Для укрепления мышц рекомендуется применение электромиостимуляции.
При выполнении лечебного массажа больным ОА следует избегать механического раздражения суставной капсулы, обращая особое внимание на работу с прилегающими к суставу мышцами. Тогда снижается болевой мышечный спазм, повышается тонус ослабленных групп мышц, усиливается трофика пораженных суставов и улучшаются функциональные способности больного.
При выраженном длительном болевом синдроме, не купируемом традиционными средствами, а также при значительных нарушениях функции сустава применяется хирургическое лечение чаще всего на коленных и тазобедренных суставах. Кардинальной операцией является эндопротезирование сустава. Хорошо зарекомендовали себя эндопротезы, в которых узел скольжения состоит из пары металл–полиэтилен.
Важную роль в профилактике ОА играет выявление и своевременная ортопедическая коррекция врожденных аномалий: вывиха бедра, варусной и вальгусной установки голеней, плоскостопия и др. В профессиональной деятельности необходимо исключить длительные статические и стереотипные механические перегрузки суставов. Существенным условием профилактики ОА коленных суставов является нормализация избыточной массы тела.
Лабораторные данные при остеоартрозе.
Клинический анализ крови и мочи обычно нормальные. При синовите может быть ускорение СОЭ до 20-25 мм/ч. Биохимические и иммунологические показатели соответствуют норме. Увеличение СРБ, α2-глобулина и фибриногена, обычно отсутствующее при остеоартрозе, может выявляться при наличии синовита, однако повышение обычно незначительное.
При исследовании синовиальной жидкости определяется ее нормальная вязкость с хорошо формирующимся муциновым сгустком, количество клеток нормальное или слегка увеличено (не более 5 • 103). Количество нейтрофилов при развитии реактивного синовита обычно не превышает 50 %.
При морфологическом исследовании биопсированной синовиальной оболочки наблюдается ее фиброзно-жировое перерождение без пролиферации покровных клеток, с атрофией ворсин и наличием небольшого количества сосудов. Увеличение количества сосудов, небольшая очаговая пролиферация покровных клеток, очаги слабо выраженной лимфоидной инфильтрации выявляются только при развитии синовита.
Рентгенография суставов является важным методом диагностики остеоартроза.
Основные рентгенологические признаки остеоартроза:
- остеофиты - костные краевые разрастания, увеличивающие площадь соприкосновения и изменяющие конгруэнтность суставных поверхностей;
- сужение суставной щели, более выраженное в сегментах, испытывающих бульшую нагрузку (в коленных суставах - в медиальных отделах, в тазобедренных суставах - в латеральных отделах);
- субхондралъный склероз (уплотнение костной ткани).
Необязательными рентгенологическими признаками при остеоартрозе являются:
- кисты (обычно расположены по оси наибольшей нагрузки);
- подвывихи и вывихи;
- эрозии.
Для определения рентгенологических изменений и степени выраженности остеоартроза наиболее часто используется классификация). Kellgren и J. Lawrence (1952), оценивающая степень выраженности основных рентгенологических признаков остеоартроза.
Стадии остеоартроза (по J. Kellgren и J. Lawrence, 1952):
- 0 - отсутствие рентгенологических признаков;
- I - сомнительные рентгенологические признаки;
- II - минимальные изменения (небольшое сужение суставной щели, единичные остеофиты;
- III - умеренные проявления (умеренное сужение суставной щели, множественные остеофиты);
- IV - выраженные изменения (суставная щель почти не прослеживается, выявляются грубые остеофиты).
Для более точной оценки рентгенологических изменений при остеоартрозе в 1987 г. A. Larsen предложил усложненную методику, позволяющую количественно оценить степень остеоартроза.
Рентгенологические критерии остеоартроза (Larsen А., 1987):
- 0 - отсутствие рентгенологических признаков;
- I - сужение суставной щели менее чем на 50 %;
- II - сужение суставной щели более чем на 50 %;
- III - слабая ремодуляция;
- IV - средняя ремодуляция;
- V - выраженная ремодуляция.
Следует учитывать, что динамика рентгенологических изменений при остеоартрозе отличается медленным темпом: скорость сужения суставной щели у больных гонартрозом составляет приблизительно 0,3 мм в год, поэтому в целях более точной диагностики, оценки динамики заболевания и эффективности лечения используются компьютерная томография, магнитно-ядерная томография, артросонография, остеосцинтиграфия и артроскопия. С помощью указанных методик можно оценивать толщину хряща и синовиальной оболочки, выявить наличие эрозий в хряще, определить характер и количество жидкости в различных отделах суставов. В последние годы артроскопия рассматривается как метод ранней диагностики остеоартроза, поскольку позволяет выявить отмеченные изменения хряща даже в случае отсутствия рентгенологических признаков болезни.
На рисунках представлены рентгенограммы больных остеоартрозом различной локализации.

Рентгенограмма кистей. Определяется ужение рентгенологических суставных щелей. Субхондральный склероз в ДМФС и ПМФС

Рентгенограмма кистей. Определяется сужение рентгенологических суставных щелей. Субхондральный склероз, остеофиты в ДМФС и ПМФС

Рентгенограмма стоп. Определяется сужение суставных щелей. Субхондральный склероз и краевые остеофиты в ПФС 1-х пальцев стоп.

Рентгенограмма правого коленного сустава. Определяется неравномерное сужение суставной щели. Субхондральный склероз, выраженные краевые остеофиты
Для постановки диагноза остеоартроза можно пользоваться критериями, предложенными различными авторами.
Критерии диагноза остеоартроза (по Л. И. Беневоленской [и др.], 1993):
- боли в суставах, возникающие в конце дня и (или) в первую половину ночи;
- боли в суставах, возникающие после механической нагрузки и уменьшающиеся в покое;
- деформация суставов за счет костных разрастаний (включая узелки Гебердена и Бушара).
- сужение суставной щели;
- остеосклероз;
- остеофитоз.
Для постановки диагноза остеоартроза наличие первых двух клинических и рентгенологических критериев обязательно.
Диагностика остеоартроза в большинстве случаев, особенно в развернутой стадии заболевания, не представляет больших трудностей и основывается на клинико-рентгенологических проявлениях заболевания. Для постановки диагноза остеоартроза целесообразно использовать вышеприведенные критерии заболевания.
Однако в ранней стадии остеоартроза, когда отсутствуют характерные рентгенологические признаки заболевания, диагностика остеоартроза может быть затруднена. В этих случаях должны учитываться клинические особенности болезни, такие как механический характер болей, медленное прогрессирование, локализация болей в тазобедренных или коленных суставах, анамнестические указания на перегрузку сустава.
В некоторых случаях находят рентгенологические изменения суставов, характерные для остеоартроза. У лиц с такими изменениями при отсутствии клинических проявлений заболевания диагноз остеоартроз не ставится.
Течение остеоартроза.
Выделяют остеоартроз с быстрой генерализацией процесса и костно-суставной деструкцией (эрозивный артроз). Такое течение чаще наблюдается при полиостеоартрозе с наличием узелков Гебердена и наследственной предрасположенностью, а также у женщин в период менопаузы.
Читайте также:


