Эндопротезирование при дефектах вертлужной впадины

Переломы вертлужной впадины составляют от 7% до 25% от повреждений таза [1]. Частота встречаемости подобной патологии составляет 3 случая на 100 000 населения в год [2]. За последние 100 лет, в связи с ростом количества ДТП, их количество увеличилось в 20 раз. Последствия подобных травм значительно снижают качество жизни и являются причиной стойкой утраты трудоспособности. Несмотря на успехи современной травматологии, разработку новых алгоритмов и методов оперативного лечения, устройств для остеосинтеза и способов их применения, по данным современной литературы можно сделать заключение, что даже проведение стабильного остеосинтеза с анатомическим восстановлением суставной поверхности вертлужной впадины в раннем посттравматическом периоде не гарантирует удовлетворительного результата [3; 4].
Дегенеративно-дистрофические изменения тазобедренного сустава, требующие хирургического лечения, развиваются у 12-88% пострадавших [1; 2; 5]. При развитии посттравматического коксартроза возможности оперативного лечения ограничены артродезированием и эндопротезированием тазобедренного сустава. Формирование анкилоза тазобедренного сустава приводит к нарушению не только позвоночно-тазовых отношений, но механических осей дистальных суставов нижних конечностей, что приводит к развитию гонартрозов и крузартрозов, значительному нарушению походки, снижению качества жизни. В связи с этим наиболее предпочтительным способом хирургического лечения является тотальное эндопротезирование тазобедренного сустава [6; 7]. Однако, несмотря на широкое использование данной методики, результаты лечения посттравматического коксартроза хуже, чем при лечении идиопатического коксартроза [2; 8; 9]. К основным сложностям, с которыми сталкивается хирург в ситуации лечения посттравматического коксартроза, в первую очередь относятся дефекты костной ткани вертлужной впадины, не позволяющие достичь прочной первичной фиксации стандартных вертлужных компонентов. В тех случаях, когда перелом вертлужной впадины сросся, высока вероятность порочной консолидации отломков, что приводит к нарушению анатомических взаимоотношений в суставе. Предшествующие многократные и объемные операции приводят к наличию выраженного мягкотканного рубцового процесса не только в проекции доступа, но и в области параартикулярных тканей, что увеличивает время оперативного вмешательства, снижает реабилитационный потенциал, повышает риск септических осложнений. Наличие металлоконструкций также ограничивает варианты использования имплантатов, увеличивает риск развития параимплантной инфекции, при необходимости удаления металлоконструкций увеличивается тяжесть интраоперационного травматического воздействия. Вследствие выраженного изменения анатомических осложнений у пациентов с посттравматическим коксартрозом определяется сформированный порочный мышечный стереотип ходьбы, что также снижает реабилитационный потенциал. Асептический некроз головки бедренной кости, развившийся вследствие перенесенной травмы, ограничивает возможность замещения посттравматических дефектов путем аутоостеопластики [1; 10]. Выбор метода оперативного лечения зависит от величины костных дефектов, качества костной ткани, наличия интактных колонн вертлужной впадины или нарушенной целостности тазового кольца, что определяет возможность обеспечения надежной фиксации и достаточной площади контакта с жизнеспособной костью [11].
Цель исследования: оценить результаты лечения пациентов с посттравматическим коксартрозом 3 стадии в сочетании с дефектами вертлужной впадины.
Материал и методы исследования. За 2012-2018 гг. в ННИИТО был пролечен 221 пациент с коксартрозом 3 стадии и посттравматическими дефектами вертлужной впадины. Учитывая отсутствие общепринятой классификации посттравматических дефектов вертлужной впадины, оценку дефектов мы проводили по одной из самых распространенных и наиболее цитируемой в современной литературе – классификации W.G. Paprosky. Выбор данной классификации был обусловлен не только ее распространенностью, но и относительной универсальностью, которая позволяет использовать данную классификацию для оценки дефектов любой этиологии и определить тактику оперативного лечения согласно алгоритму, предложенному авторами [12]. При проведении анализа также учитывали тип перелома вертлужной впадины по классификации АО, способ предшествующего лечения (восстановление суставной поверхности вертлужной впадины, проведение стабильного остеосинтеза, сроки проведения оперативного вмешательства), срок, прошедший после травмы до проведения эндопротезирования, тип дефекта по классификации W.G. Paprosky. Критериями включения в исследование были следующие параметры: возраст старше 18 лет, наличие посттравматического коксартроза 3 стадии и дефекта вертлужной впадины IIa и обширнее по классификации W.G. Paprosky. Критерием исключения являлись пациенты младше 18 лет, а также пациенты с наличием хронического инфекционного процесса в области тазобедренного сустава. Пациенты были разделены на 2 группы: в I группу включены 189 пациентов, которым оперативное лечение по поводу перелома вертлужной впадины либо не проводилось, либо суставная поверхность не была восстановлена, либо операция была выполнена в срок более 21 дня с момента травмы. Во II группу включены 32 пациента, которым в срок до 21 дня с момента травмы был проведен стабильный остеосинтез с восстановлением суставной поверхности вертлужной впадины.
Половой состав групп был неоднороден, в обеих группах преобладало количество мужчин – соотношение женщины/мужчины: 1 к 5.
В I группе было 46 женщин и 143 мужчины, средний возраст составил 49+1 год (min 24, max 78, медиана 51), во II группе 4 женщины и 28 мужчин, средний возраст составил 50+2 года (min 28, max 79, медиана 53).
При анализе типа и характера переломов вертлужной впадины было выявлено, что в группе I чаще всего были диагностированы переломы типа A, а в группе II – чаще всего встречались переломы типа B по классификации AO (табл. 1).
Распределение пациентов в группах по типу перелома по шкале AO ASIF
В случае ревизионной артропластики тазобедренного сустава, когда уже имеются значительные костные дефектывертлужной впадины, не всегда представляется возможным использовать обычную ауто- и аллоостеопластику. Одной из причин этого является значительная потеря костной ткани вокруг первично установленного эндопротеза. Первоначально остеолиз может наблюдаться уже вокруг установленного эндопротеза. Процесс значительно прогрессирует в случае инфекционных осложнений, а также если имеются ошибки первичного эндопротезирования, ведущие к нарушению биомеханики установленного сустава и раннему проявлению его нестабильности.
Для фиксации компонентов эндопротеза и закрытия образовавшихся дефектов кости может производиться забор собственной кости больного, например из тазовой кости, и установка его взамен разрушенной кости. Но данный метод требует дополнительных разрезов, что повышает травматичность операций, самого аутоматериала зачастую просто недостаточно для проведения операции, а установленные трансплантаты, лишенные питающих сосудов, могут подвергаться лизису, особенно после гнойных осложнений.
Поставленную задачу можно также решать путем аллоостеопластики (деминерализованные, декальцинированные, структурные и неструктурные костные аллотрансплантаты). Однако в этом случае приходится рассчитывать лишь на их остеокондуктивные свойства, которые в отсутствие питающих сосудов в значительной степени ослабевают при увеличении размера трансплантата более 1,2 см.
Существуют и различные искусственные (металлические) конструкции, формирующие вертлужную впадину. Но использование их носит ограниченный характер вследствие отсутствия индивидуальности, дополнительной травматичности при установке, а также невозможности применения в случаях обширных костных дефектов.
Результатом многочисленных испытаний различных способов решения этой проблемы в ситуациях с дефектами вертлужной впадины от 2В типа по W. G. Paprosky (1991) стала разработка метода закрытия дефекта стенки вертлужной впадины при помощи аутотрансплантата из большого вертела бедренной кости на питающей ножке в целях создания во впадине надежного костного ложа для установки вертлужного компонента эндопротеза.
Разработанный способ осуществлялся следующим образом. После удаления эндопротеза, рубцов, патологических грануляций и выявления дефекта дна вертлужной впадины с целью подготовки к пластике с помощью долота и осцилляторной пилы формировался костный фрагмент из большого вертела на питающей ножке, соответствующий по форме и размеру дефекту вертлужной впадины.
Питающая ножка аутотрансплантата в большинстве случаев выкраивалась из пучков средней и малой ягодичных мышц. Оптимальным являлось формирование питающей ножки из части сухожилия одной мышцы - малой ягодичной, поскольку она лежит в самом глубоком слое и позволяет весьма удобно перенести фрагмент большого вертела в вертлужную впадину без натяжения и перегибов. Однако выделение малой ягодичной мышцы зачастую бывает весьма затруднительно, поэтому обычно для формирования питающей ножки использовали пучки сухожилий двух мышц - малой и средней ягодичных. Соответственно, питание осуществляется за счет ветвей первого порядка верхней ягодичной артерии.
Затем трансплантат перфорировался и временно фиксировался к своему ложу. Для адаптации регенерата к новым условиям кровоснабжения рана ушивалась на 3-4 недели.
На втором этапе, после обработки дефекта вертлужной впадины, подготовленный аутотрансплантат перемещали на питающей ножке, укладывали во впадину таким образом, чтобы максимально закрыть дефект, и фиксировали его при помощи 2-3 винтов. Далее впадина обрабатывалась для установки вертлужного компонента эндопротеза, причем в некоторых случаях возникала необходимость использования укрепляющих колец (Мюллера, Ганса) или антипротрузионной системы (Бурх - Шнайдера).
По описанному и запатентованному способу было прооперировано 12 больных с различными дефектами вертлужной впадины. Сроки наблюдения после операции составили от 1 до 7 лет. У 91,9 % + 1,3 % пациентов получены хорошие и отличные результаты (от 84 до 93 баллов по шкале Харриса) - отмечена желаемая функциональная перестройка остеотрансплантатов, вертлужные компоненты эндопротезов за все время наблюдения остаются стабильными, отсутствует их дислокация, больные не жалуются на боли, движения в оперированных суставах не ограничены, ходят без помощи костылей и трости.
Современный метод эндопротезирования тазобедренного сустава
С широким распространением метода эндопротезирования тазобедренного сустава и увеличением числа оперированных пациентов растет и количество больных с нестабильными эндопротезами. Эти пациенты нуждаются в ревизии и частичной или полной (тотальной) замене имплантата.
Асептическая нестабильность эндопротеза, в зависимости от способа фиксации, возникает по трем основным причинам: резорбция кости вокруг имплантата, дестабилизация цементной мантии и износ пары трения эндопротеза. Замена вертлужного компонента эндопротеза тазобедренного сустава при ревизионном эндопротезировании, наряду с заменой бедренного компонента, является основной задачей при восстановлении функции конечности в целом.
Основными проблемами при ревизии вертлужного компонента эндопротеза являются степень потери костной массы в области ацетабулярной впадины в результате асептического расшатывания ранее установленного компонента и нарушение целостности вертлужной впадины.

С января 1990 по январь 2009 г. в отделении эндопротезирования ЦИТО им. Н.Н. Приорова выполнено 603 операции ревизионного эндопротезирования тазобедренного сустава. В 526 случаях производилась ревизия вертлужного компонента.
Ревизии подверглись эндопротезы различных производителей. Средний возраст пациентов составил 55 лет (от 17 до 81 года). Также выполнялась повторная установка вертлужного компонента при дефектах впадины, возникших после удаления ранее установленных эндопротезов.
В 422 случаях первичная установка чашки была бесцементной, в 104 - проводилась с помощью костного цемента. После удаления ранее установленного вертлужного компонента практически все пациенты имели дефекты стенок или полостные дефекты.
За основу оценки дефектов впадины авторами взята классификация W. Paprosky. Будучи достаточно трудной для восприятия и описания, она является наиболее распространенной и часто употребляемой в литературе.
По классификации W. Paprosky пациенты распределились следующим образом. Дефекты типа 1-2В были у 116 человек. Дефекты 2С и выше - у 410.
Столь выраженный дефицит костной массы вертлужной впадины у большинства пациентов заставил искать новые пути решения данной проблемы в двух направлениях. Во-первых, для восполнения дефицита костной массы совместно с костным банком ЦИТО, начиная с 1996 г., авторы начали использовать обработанный и консервированный костнопластический материал для пластики стенок и дна впадины (до 1996 г. применялась только аутокость, взятая из крыла подвздошной кости).
Укрепления дна впадины при лечении суставов
В 1996 г. впервые для укрепления дна впадины использовали кортикальные трансплантаты, с 1997 г. - костную стружку, с 2000 г. - губчатую лиофилизированную аллокость и с 2003 г. - лиофилизированные фрагменты головок бедренных костей. Во-вторых, для сохранения механической прочности вертлужной впадины авторы пошли по пути создания усиливающей чашки типа реконстуктивного кольца "Schneider-Burch", ацетабулярного поддерживающиго коль¬ца Muller и других конструкций.
Два этих направления легли в основу метода восстановления вертлужной впадины при ревизионном эндопротезирований у пациентов с выраженным дефицитом костной массы и нарушением механической прочности кости.
Данная методика костной пластики впадины в сочетании с использованием укрепляющей металлической чаши или кольца была применена в 84 случаях. У остальных пациентов костная пластика не выполнялась или при использовании костнопластического материала не применялось усиление впадины путем установки металлической конструкции в виде чаши или кольца.
Все пациенты имели дефекты впадины типа 2С-ЗВ по принятой классификации, то есть имели сегментарные или смешанные сегментарные и полостные дефекты вертлужной впадины. Возраст пациентов был от 29 до 78 лет (средний - 55 лет). Сроки наблюдения после ревизионного эндопротезирования составили от 4 месяцев до 8,5 лет (первая установка - июль 2000 г.).
К интраоперационным осложнениям авторы отнесли 2 случая из 84: перелом верхнего края вертлужной впадины при установке усиливающей чаши и парез седалищного нерва. В первом случае была переустановлена усиливающая чаша, во втором - парез выявлен сразу после операции и был связан с повышенной травматичностыо манипуляций. После проведенного лечения функция нерва восстановилась.
Послеоперационные осложнения после эндопротезирования суставов
К ранним послеоперационным осложнениям отнесены 2 случая поверхностного нагноения, в 2 случаях произошло отхождение гематомы. К поздним послеоперационным осложнениям авторы отнесли глубокое нагноение - 4 случая, хронический болевой синдром - 2, дестабилизацию чаши - 3 случая и миграцию винтов - 1.
Изучение результатов проводилось по стандартной методике осмотра пациента, путем выполнения контрольных рентгенограмм, оценки по шкале Харриса и субъективной оценки пациента по принципу: отлично, хорошо, удовлетворительно, плохо.
На 84 случая применения данной методики удовлетворительный, хороший и отличный результаты получены в 74 случаях (88%). Неудовлетворительный результат - 10 случаев (12%).
К неудовлетворительным отнесены: глубокое нагноение - 4 случая, дестабилизация чашки -3, хронические боли - 2, миграция винтов - 1.
Выводы
Использование данной методики восстановления вертлужной впадины с выраженным дефицитом костной массы при ревизионном эндопротезировании тазобедренного сустава является эффективным способом лечения пациентов с нестабильностью вертлужного компонента.

исунок 1. Рентгенологические примеры несостоятельности вертлужного кубка эндопротеза:
a. расшатывание и подвывих вертлужного кубка,
б. полный вывих и протрузия вертлужного кубка.


Рисунок 3. Рентгенологические примеры вывиха и расшатывания имланта:
a. вывих ацетабулярного кубка,
б. причина вывиха – вертикаллизация (до 80о) ацетабулярного компонента,
в. расшатывание ацетабулярного кубка.
При реконструкции костного дефекта вертлужной впадины при эндопротезировании тазобедренного сустава, на наш взгляд, использование аутологичной или аллогенной кости нецелесообразно. В процессе перестройки трансплантата происходит его резорбция и частичная или полная секвестрация, что приводит к расшатыванию вертлужного компонента эндопротеза. Наиболее оптимальным, на наш взгляд, является использование металлических конструкций и армированного металлом костного цемента. Ниже приведен (рис. 4) клинический пример реконструкции вертлужной впадины с помощью реконструктивной пластины.


Рисунок 4. Клинический пример реконструкции вертлужной впадины при несосоятельности крыши и заднего края, после несросшегося перелома и порочного остеосинтеза:
а. рассасывание заднего края (контуром обозначен костный дефект крыши и и заднего края),
б. реконструированная крыша и задний край, имплантированый кубок (интраоперационно),
в. рентгенограмма до операции – порочный остеосинтез, задне-верхний подвывих в Т.Б.С.,
г. послеоперационная рентгенограмма – видна имплантированная реконструктивная пластина, аутотрансплантат укрепленный винтами.
На наш взгляд, решение о реконструкции вертлужной впадины должно приниматься на операционном столе, т. к. пунктом отсчета должна являться позиция кубка эндопротеза в вертлужной впадине. Только после пробного расположения кубка во впадине решается вопрос о несостоятельности крыши или всего верхне-заднего комплекса (рис.5).

Рисунок 5. Схема принятия решения о реконструкции вертлужной впадины:
б. определение дефекта конфигурации вертлужной впадины (верхне-
в. реконструкция дефекта вертлужной впадины,
г. окончательная имплантация вертлужного кубка.
Мы отошли от стандартных техник с использованием аутотрансплантатов из-за высокой вероятности резорбции трансплантата и в дальнейшем возможности расшатывания эндопротеза. Нами в НЦТО для небольших дефектов заднего края вертлужной впадины разработан способ реконструкции вертлужной впадины заполнением костным цементом, армированным винтами. Способ реконструкции вертлужной впадины заполнением костным цементом, армированным винтами запатентован в Республике Армения (патент на изобретение No 1759). Ниже приведен (рис. 6 и 7) клинический пример заполнения дефекта заднего края вертлужной впадины цементным массивом, укрепленным металлическими винтами.




Рисунок 7. Схема реконструкции цементным массивом, укрепленным металлическими винтами:
а. виден дефект заднего края вертлужной впадины - помечено серым (желтаястрелка),
б. примерка ацетабулярного кубка, для планирования реконструкции,
в. имплантация армировочных винтов в подвздошную кость (синие стрелки),
г. примерка ацетабулярного кубка с имплантированными винтами, д. окончательная обработка костного ложа, нанаесение анкорных отверстий (желтые стрелки), т.е. заливка цемента и имплантация ацетабулярного кубка, виден массив цемента.
Рисунок 9. Оригинальнальная пластина для реконструкций костных дефектов вертлужной впадины:
а. большая пластина,
б. малая пластина
Листовая форма пластины позволяет моделировать ее в гемисферический купол во время операции, для придания формы вертлужного кубка, лишняя часть пластинки может откусываться. Имеется возможность моделирования пластинки в любую сложную форму и поверхность - практически без ограничения (рис. 10). Имеется два размера пластинок – большая и малая: малая имеет диапазон полусфер от 45мм до 51мм, а большая - от 52мм до 64мм (рис. 9). Оригинальная пластина для реконструкции вертлужной впадины запатентована в Республике Армения (патент на изобретение No 1758).

Рисунок 10. Оригинальнальная пластина в согнутом состоянии

Рисунок 11. Схема имплантации оригинальнальной пластины и техника реконструкции дефектов вертлужной впадины:
а. виден дефект заднего края вертлужной впадины - помечено серым (желтая стрелка),
в. примерка ацетабулярного кубка в искусственной впадине,
г. заливка цемента и имплантация кубка, виден массив цемента (голубой).
Рисунок 12. Пример использования реконструктивной пластины с аутотрансплантатом:
а. снимки больной после коррегирующей остеотомии, головка левой бедренной кости в положении подвывиха - более 1/3 вне суставной впадины (синяя стрелка),
б. интраоперационный снимок: реконструкция вертлужной впадины аутотрансплантатом и реконструктивной пластиной, фиксированными винтами,
в. интраоперационный снимок: имплантирован цементный кубок,
г. послеоперационный снимок: тотальное эндопротезирование левого Т.Б.С.

Рисунок 13. Пример использования реконструктивной пластины без аутотрансплантата:
а. предоперационная рентгенограмма: остаточные явления перенесенной болезни Пертеса, левосторонний деформирующий коксартроз,
б. ослеоперационная рентгенограмма: тотальное эндопротезирование левого ТБС с рекон-струкцией вертлужной впадины малой пластинкой ЦТОР,
в. тот же снимок, увеличенный: малая реконструктивная пластина, фиксированная винтами (синие стрелки), виден массив цемента заполняющий дефект задне-верхнего края (желтые стрелки).
Имеющийся клинический материал представлен результатами 149 реконструкций несос-тоятельной вертлужной впадины за период с 2006 по 2010 г.г. У указанного контингента больных в 88 случаях была произведена реконструкция вертлужной впадины оригинальной пластиной ЦТОР. Среди произведенных операций: в 12 случаях осуществлялась реконструкция аутотрансплантатом из резецированной головки для пластического восстановления крыши; в 6 случаях производилось укрепление дна вертлужной впадины антипротрузионной сеткой без использования аутотрансплантата, а в 4 – с использованием последнего; в 7 случаях было использовано укрепляющее кольцо вертлужной впадины без аутотрансплантата, а в 8 – с использованием; в 24 случаях использовалась техника реконструкции массивом цемента, укрепленного винтами, так же разработанная в ЦТОР. Из 88 случаев реконструкции вертлужной впадины оригинальной пластиной ЦТОР в 10 случаях использовался аутотрансплантат из резецированной головки бедренной кости, а в остальных случаях он не использовался и был заменен цементным массивом. Далее в виде таблицы (таб. 1) более развернуто представлены различные способы реконструкций несостоятельности костного ложа вертлужной впадины при эндопротезировании тазобедренного сустава.
Как видно из приведенной выше таблицы, большая часть осложнений и, соответственно, выполненных по их поводу ревизий, связана с использованием аутотрансплантатов. В категориях без использования аутотрансплантатов нами наблюдались лишь 2 осложнения (одно подверглось ревизии с отличным результатом, а второе не нуждалось в таковой вследствие скудной клинической картины). В случаях использования реконструктивной пластины с аутотрансплантатом результативность была 90%, в случаях же без аутотрансплантата (цементным массивом) результативность - 100%.
Заключение и выводы.
При реконструкции костного дефекта вертлужной впадины при эндопротезировании тазобедренного сустава использование аутологичной или аллогенной кости нецелесообразно. В процессе перестройки трансплантата происходит его резорбция и частичная или полная секвестрация, что приводит к расшатыванию вертлужного компонента эндопротеза. Наиболее оптимальным, на наш взгляд, является использование металлических конструкций и армированного металлом костного цемента. Для этой цели эффективной является, разработанная нами специальная реконструктивная пластина для дефектов вертлужной впадины. Эффективность данного метода при правильной технике исполнения может приближаться к 90-100%.
Таблица 1 Различные способы реконструкций костного ложа вертлужной впадины при
эндопротезировании ТБС, произведенные в НЦТО за период 2006-2010 г.г.
Описание патента на изобретение RU2637105C1
Изобретение относится к медицине, а именно к ортопедии и травматологии, может быть использовано при оперативном лечении диспластического и посттравматического коксартроза, лечении больных с повреждениями и последствиями повреждений вертлужной впадины.
Травмы, а также посттравматические и врожденные дефекты тазобедренного сустава часто являются причинами инвалидности. Известны различные методики лечения повреждений и дефектов вертлужной впадины. В общедоступных источниках представлены способы чрескостного, накостного, комбинированного остеосинтеза, реконструктивное эндопротезирование.
Из уровня техники известен способ пластики вертлужной впадины при ее дисплазии ([1], патент RU 2207076), включающий отсечение головки бедренной кости и введение ее в вертлужную впадину. Отсеченную головку бедра и вертлужную впадину освобождают от хрящевого слоя. Задне-боковым разрезом обнажают вертельную область бедренной кости и заднюю стенку капсулы тазобедренного сустава. Последнюю П-образно рассекают. Выкроенный лоскут капсулы берут на держалки. Вывихивают из сустава и резецируют головку и шейку бедренной кости. Головку бедра и вертлужную впадину освобождают от хрящевого покрова. Головку бедра маятниковой пилой рассекают вдоль оси шейки на две, а затем на четыре равных фрагмента. Последовательно адаптируют каждый из сегментов головки бедра по периметру вертлужной впадины. Суставной стороной прижимают к подлежащей части края вертлужной впадины и фиксируют винтом, причем губчатой стороной каждый трансплантат должен незначительно выходить в полость вертлужной впадины. Обрабатывают вертлужную впадину булавовидными фрезами. Фрезой срезают и выступающую во впадину часть каждого трансплантата, чем формируют округлое ложе для установки чашки эндопротеза. Устанавливают чашку эндопротеза, которая прижимает трансплантат к дефекту края вертлужной впадины. Устанавливают ножку эндопротеза в диафиз бедра. Восстанавливают целостность капсулы сустава. Рану послойно ушивают с установкой дренажной системы.
Недостаток данного способа [1] - это полное удаление хряща с головки бедренной кости, из которой формируют трансплантат, отсутствие обработки костного ложа в области дефекта вертлужной впадины, направленной на стимуляцию регенеративных процессов. В результате не создается достаточных условий для адекватного кровоснабжения области дефекта, условий для приращения и органотипической перестройки трансплантата, что приводит к неудовлетворительному качеству формирующегося регенерата костной ткани и увеличивает риск развития нестабильности вертлужного компонента эндопротеза в послеоперационном периоде.
Известен способ эндопротезирования тазобедренного сустава при костном дефекте вертлужной впадины ([2], патент RU 2475202). Осуществляют доступ к тазобедренному суставу. После капсулотомии выполняют вывих головки бедренной кости. Обрабатывают головку бедренной кости вогнутой фрезой с максимальным сохранением аутопластического материала головки в форме полусферы, с удалением хряща и субхондральной пластинки. Пересекают шейку бедренной кости. Извлекают головку вместе с шейкой из сустава. Отсекают сформированный аутотрансплантат. В области дефекта вертлужной впадины формируют выгнутой фрезой ложе сферической формы, соответствующее диаметру аутотрансплантата. Аутотрансплантат устанавливают в область дефекта и временно фиксируют спицами. Формируют вертлужную впадину. Удаляют спицы. Фиксируют аутотрансплантат спонгиозными винтами. Устанавливают вертлужный компонент эндопротеза. Имплантируют бедренный компонент эндопротеза. Проводят вправление головки эндопротеза. Рану ушивают.
В данном способе [2] также производят полное удаление хряща и субхондральной пластинки с головки бедренной кости, из которой формируют трансплантат, не производят перфорирование в области дефекта вертлужной впадины. Не создается достаточных условий для адекватного кровоснабжения области дефекта, условий для приращения и органотипической перестройки трансплантата, что приводит к неудовлетворительному качеству формирующегося регенерата костной ткани и увеличивает риск развития нестабильности вертлужного компонента эндопротеза в послеоперационном периоде.
Известен способ двухэтапного эндопротезирования тазобедренного сустава ([3], патент RU 2171643), который предполагает применение внешней фиксации костных отломков и последующую имплантацию компонентов эндопротеза. Первым этапом производится низведение головки бедренной кости до уровня вертлужной впадины с последующей фиксацией. Вторым этапом выполняется эндопротезирование тазобедренного сустава.
Однако способ [3] адаптирован для лечения больных со смещением головки бедренной кости в проксимальном направлении относительно вертлужной впадины. Способ [3] предполагает длительное двухэтапное лечение. Трудно добиться прочного сращения костей таза, которое необходимо для сохранения стабильности имплантированного протеза тазобедренного сустава. Стабильное положение костей таза, фрагментов вертлужной впадины является необходимым условием для последующей стабильной имплантации протеза тазобедренного сустава.
Известен способ пластики дна вертлужной впадины ([4], патент RU 2157669). Производят отсечение головки бедренной кости, освобождение ее и вертлужной впадины от хрящевого слоя, отсечение проксимальной части головки. Из части головки формируют трансплантат. Диаметр плоскости сечения фрагмента должен превышать диаметр дефекта дна вертлужной впадины. Трансплантат вводят в вертлужную впадину, плоскостью сечения прижимая к дефекту со стороны суставной впадины. Во впадине и выступающей в нее части головки округлой фрезой диаметром, меньшим диаметра вертлужной впадины, формируют ложе для чашки эндопротеза.
Известен способ эндопротезирования вертлужной впадины при дефекте ее дна ([5], патент RU 2474394), включающий удаление головки бедренной кости, обработку вертлужной впадины, отсечение части головки с последующим формированием из нее трансплантата, причем диаметр плоскости сечения фрагмента должен превышать диаметр дефекта дна вертлужной впадины, помещение сформированного трансплантата в дефект дна вертлужной впадины. Из дефекта дна вертлужной впадины формируют многогранник с максимально возможным количеством граней, затем из половины трансплантата со стороны его выпуклой поверхности формируют многогранник таким образом, чтобы форма и размеры формируемого многогранника соответствовали форме и размерам многогранника в дне вертлужной впадины, а при помещении сформированного трансплантата в дефект дна вертлужной впадины совмещают оба многогранника.
Недостаток данных способов [4; 5] заключается в том, что не обеспечена достаточно прочная фиксация трансплантата к дефекту вертлужной впадины. Не производится туннелизация костного ложа в области дефекта вертлужной впадины. В результате не создается достаточных условий для адекватного кровоснабжения области дефекта, условий для приращения и органотипической перестройки трансплантата, что приводит к неудовлетворительному качеству формирующегося регенерата костной ткани и увеличивает риск развития нестабильности вертлужного компонента эндопротеза в послеоперационном периоде. Тазовый компонент при установке проявляет тенденцию к расшатыванию, эндопротез становится нестабильным и возникает необходимость в реконструктивном эндопротезировании.
Известен способ эндопротезирования тазобедренного сустава при переломах и посттравматических дефектах вертлужной впадины ([6], патент RU 2360627). Сущность способа состоит в расширенном доступе к суставу, удалении головки, имплантации тазовых и бедренных компонентов протеза, проведении проб на вправление и стабильность протеза, замене рашпиля на бедренный компонент протеза, вправлении головки протеза во впадину и послойном ушивании раны. При этом выполняют остеотомию шейки бедренной кости и удаление головки без применения винтового экстрактора. Затем обрабатывают впадину до губчатой кости и определения размеров локализации вертлужной впадины. Кроме того, обрабатывают резецированную головку бедра с удалением хряща и субхондральной пластинки. После чего ее располагают в обработанной впадине с перекрытием зоны ее дефекта. Затем моделируют из головки имплантационное ложе тазового компонента, которое фиксируют спонгиозными винтами к вертлужной впадине. Осуществляют примерку и установку стандартного тазового компонента. Использование данного изобретения позволяет обеспечить надежную первичную фиксацию компонентов стандартного эндопротеза при переломах и посттравматических дефектах вертлужной впадины.
Недостаток данного способа [6] это полное удаление хряща и субхондральной пластинки с головки бедренной кости, из которой формируют трансплантат, отсутствие обработки костного ложа в области дефекта вертлужной впадины, направленной на стимуляцию регенеративных процессов, например остеперфорации (туннелизации). В результате не создается достаточных условий для адекватного кровоснабжения области дефекта, условий для приращения и органотипической перестройки трансплантата, что приводит к неудовлетворительному качеству формирующегося регенерата костной ткани и увеличивает риск развития нестабильности вертлужного компонента эндопротеза в послеоперационном периоде.
Из уровня техники видно, что разработка и внедрение новых, комбинированных, органосберегающих способов лечения врожденной и приобретенной патологии тазобедренного сустава является актуальной задачей современной травматологии, так как способов, полностью удовлетворяющих всем потребностям, нет.
Задача изобретения заключаются в необходимости расширения существующего оперативного набора способов пластики дефекта передне- и задне-верхнего края вертлужной впадины структурной аутокостью при эндопротезировании тазобедренного сустава с целью повышения качества и эффективности лечения. Обеспечение восполнения дефекта вертлужной впадины структурной аутокостью, обеспечение условий для сращения трансплантата с тазовой костью, формирования регенерата, органотипической перестройки трансплантата и прилежащей костной ткани с формированием полноценного костного массива. Обеспечение возможности осуществить имплантацию и заклинивание тазового компонента эндопротеза (чашки) за счет плотной посадки (press-fit) в истинную вертлужную область, с восстановлением точки ротации тазобедренного сустава.
Технический результат заключается в обеспечении приращения и перестройки аутотрансплантата, заполняющего дефект вертлужной впадины, обеспечении полной остеоинтеграции и стабильности тазового компонента эндопротеза, восстановлении нормальных биомеханических условий функционирования тазобедренного сустава. В целом техническое решение позволяет решить поставленную задачу. Снижается риск появления нестабильности тазового компонента эндопротеза после его имплантации. Обеспечивается выживаемость эндопротеза тазобедренного сустава.
Способ обеспечивает получение аутотрансплантата с минимальной потерей костной массы, создание полноценного контакта по всей поверхности между аутотрансплантатом и костным ложем в области дефекта вертлужной впадины. Остеоперфорация активирует кровоток, ускоряет обменные процессы, контакт с губчатой поверхностью аутотрансплантата способствует органотипической перестройке костной ткани, образованию костного регенерата, полноценному врастанию трансплантата и формированию костного массива вокруг чашки эндопротеза тазобедренного сустава. Что в сочетании с центрацией в истинную вертлужную область обеспечивает стабильную установку тазового компонента эндопротеза, снижается его микроподвижность, повышается выживаемость эндопротеза и снижается вероятность необходимости ревизионного эндопротезирования, сокращается время костной пластики.
Изобретение поясняется графическими материалами, на которых показано:
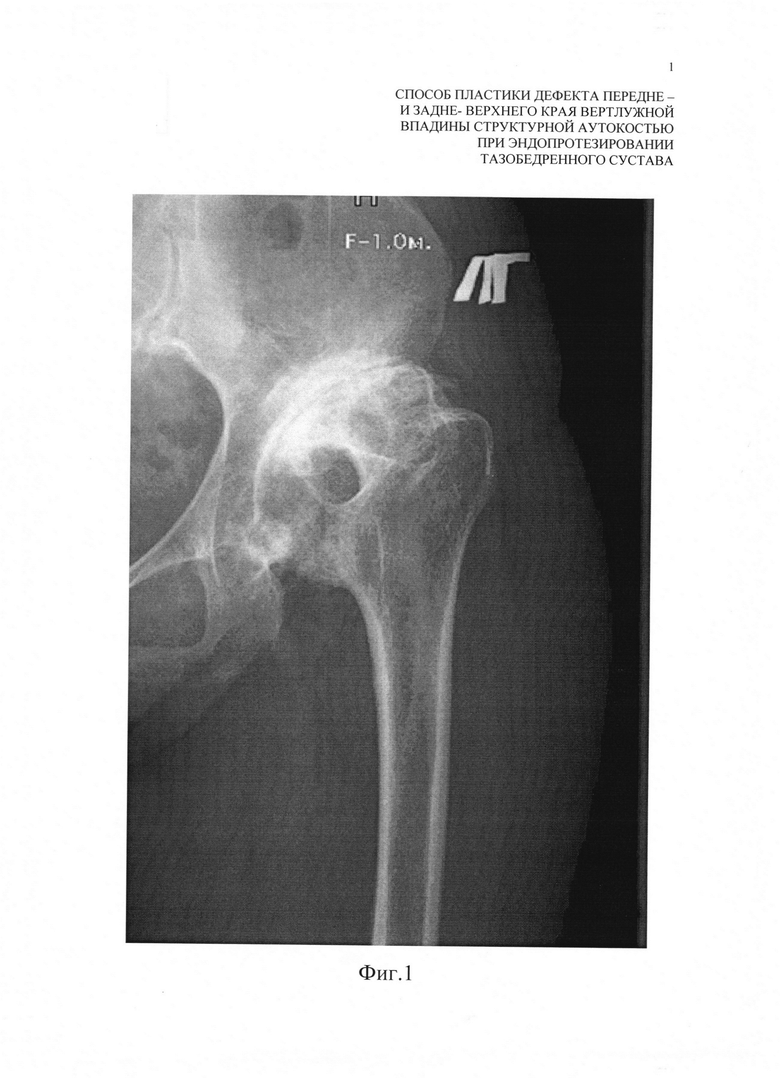
Фиг. 1 - Копия рентгенограмы левого тазобедренного сустава пациента до лечения;
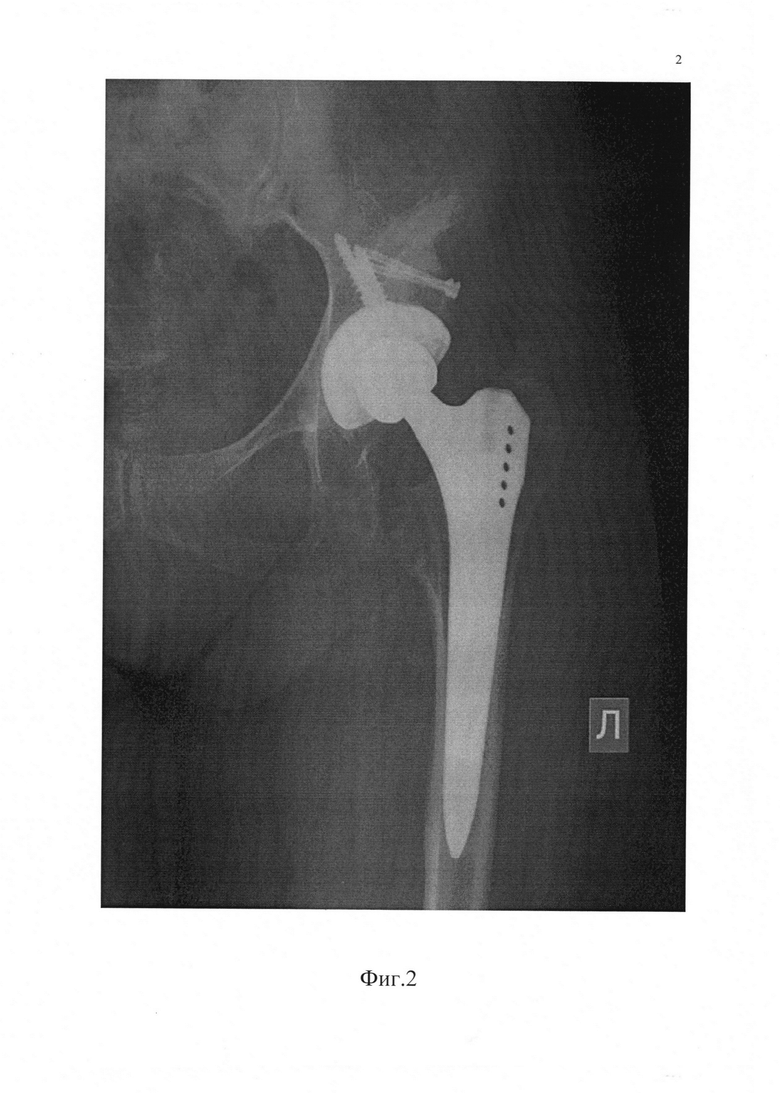
Фиг. 2 - Копия рентгенограмы левого тазобедренного сустава пациента после лечения.
Способ осуществляется следующим образом.
Пациент К. 57 лет.
Диагноз: левосторонний коксартроз III стадии, субтотальный дефект крыши и переднего края вертлужной впадины, подвывих бедра Crowe III стадии (фиг. 1). При осмотре пациента определили наличие боли и ограничение движений в области левого тазобедренного сустава.
Похожие патенты RU2637105C1
Иллюстрации к изобретению RU 2 637 105 C1
Реферат патента 2017 года СПОСОБ ПЛАСТИКИ ДЕФЕКТА ПЕРЕДНЕ - И ЗАДНЕ - ВЕРХНЕГО КРАЯ ВЕРТЛУЖНОЙ ВПАДИНЫ СТРУКТУРНОЙ АУТОКОСТЬЮ ПРИ ЭНДОПРОТЕЗИРОВАНИИ ТАЗОБЕДРЕННОГО СУСТАВА
Формула изобретения RU 2 637 105 C1
Читайте также:


