Чем лечить артрит у ребенка какие антибиотики
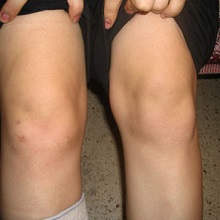
Реактивный артрит у детей, он же инфекционно-аллергический артрит – это патология, провоцирующая воспаление в различных суставах организма, не сопровождается гнойными очагами.
Болезнь является весьма распространённой, так как появляется вследствие поражения тела инфекцией, сбоев в иммунитете, респираторных нарушений и других причин. Медицинская статистика показывает большую склонность к реактивному артриту у ребенка мужского пола, но риск остаётся высоким и у девочек.
Болезнь не угрожает жизни, но приносит серьёзные сложности для жизнедеятельности, её важно начать вовремя лечить.
Что это такое?
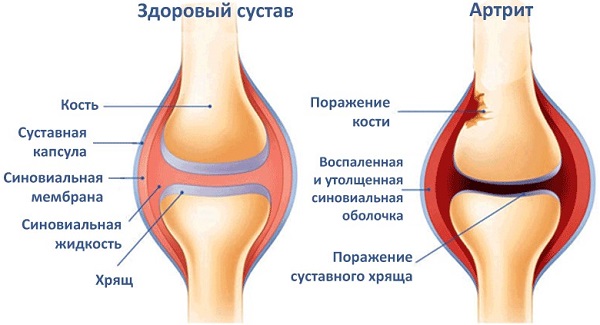
Реактивный артрит (РА) – воспаление суставов, которое носит вторичный характер и развивается после перенесенной внесуставной инфекции. Ранее считалось, что при этом заболевании микробы в полости сустава не обнаруживаются. Современная наука доказала, что при РА можно выявить антигены возбудителей в синовиальной оболочке или жидкости с помощью специальных методов исследования.
Среди детей до 18 лет РА впервые развивается примерно у 30 человек из 100000. Распространенность этого заболевания – 87 случаев на 100000 детского населения. Среди всех ревматических заболеваний в детском возрасте доля РА составляет 40 – 50%. Таким образом, реактивный артрит (не путать с ревматоидным!) – достаточно распространенная болезнь суставов у детей.
Причины развития
Аномальная реакция иммунной системы – основная причина возникновения реактивного артрита у детей. В результате иммунного ответа на внедрение болезнетворных микроорганизмов вырабатываются антитела, которые уничтожают чужаков. Иногда организм перестает понимать разницу между рецепторами клеток внутреннего слоя, выстилающего сустав и клетками микробов. Поэтому вместе с микроорганизмами иммунитет по ошибке уничтожает ткани суставов собственного организма. Ненормальная иммунная реакция запускает реактивный воспалительный процесс, разрушающий сустав.
Инфекции, которые могут спровоцировать заболевание:
- Инфекции дыхательных путей и неспецифические чаще приводят к реактивному артриту у ребенка, чем урогенитальные или кишечные. Ему в половине случаев предшествуют болезни дыхательных путей: ангина, ОРЗ, бронхит, фарингит;
- На втором месте – возбудители кишечных инфекций: иерсинии, сальмонеллы, шигеллы, кампилобактер;
- Реже всего у детей встречается воспаление суставов, вызванное возбудителями урогенитальных инфекций: хламидий, уреаплазмы, гонококков, микоплазмы.
По разным данным, связь с возбудителем удается точно установить в 50-60% случаев.
У дошкольников чаще развивается артрит тазобедренного сустава. У школьников и подростков – голеностопного или коленного сустава. Мелкие суставы рук и ног у детей при реактивном артрите нечасто оказываются повреждены.
Развитие реактивного артрита зависит не столько от инфекции, сколько от предрасположенности. 85% больных имеют отягощенную наследственность – являются носителями антигена HLA-B27. Для них риск развития реактивного артрита в 50 раз выше.
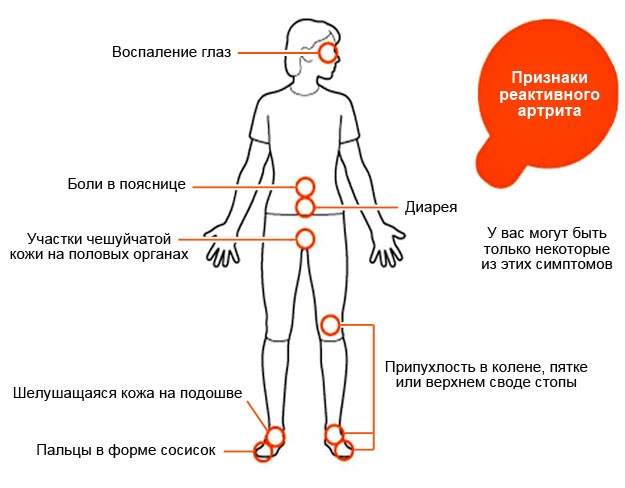
Симптомы и первые признаки
Реактивный артрит у детей Комаровский Е. О. описывает следующей симптоматикой:
- лихорадочное состояние, температура часто достигает 38-39°С;
- глюмерулонефрит;
- тошнота с приступами рвоты, но рвотные позывы появляются не всегда;
- болевые ощущения в любой части головы с головокружением;
- плеврит;
- быстрая утомляемость, слабость;
- признаки болезни проявляются спустя 2-3 недели после инфекционного заболевания;
- ухудшение аппетита и похудание;
- аортальная недостаточность;
- увеличение объёмов лимфоузлов в паху;
- патологии сердечно-сосудистой системы.
Наиболее эффективно лечение реактивного артрита у детей при обнаружении патологии на первом этапе, но в этот период мало характерных симптомов. Недуг полностью излечим на начальной стадии. Если не лечиться или использовать неправильный курс, развивается хроническая форма.
Диагностика
В домашних условиях можно заподозрить реактивный артрит, если воспалению сустава предшествовало какое-либо инфекционное заболевание, а также судя по характерной клинической картине, описанной выше. Далее следует показать ребенка врачу, не начиная самостоятельно никакого лечения, ведь точный диагноз реактивного артрита ставится только после проведения анализов и инструментальных исследований. Все дети с подозрением на реактивный артрит должны быть направлены к ревматологу.
- Сбор анамнеза.
- Визуальный осмотр.
- Клинический анализ крови (возможно повышение количества лейкоцитов, СОЭ).
- Анализ мочи (также могут быть повышены лейкоциты).
- Ревмопробы (биохимический анализ крови на антистрептолизин О (антитела к стрептококку), СРБ, сиаловые кислоты, общий белок, фибриноген, мочевая кислота, циркулирующие иммунные коплексы), ревматоидный фактор.
- Мазки из мочеиспускательного канала, цервикального канала, конъюнктивы глаза (в случае перенесенной мочеполовой инфекции могут быть выделены хламидии.
- Посев кала на дизгруппу (после кишечной инфекции возможен высев патогенных микроорганизмов – сальмонелл, шигелл, иерсиний).
- Серологические реакции на выявление антител к возбудителям кишечных инфекций.
- Реакция иммунофлюоресценции на обнаружение антигенов хламидий в сыворотке крови и синовиальной жидкости.
- Иммуноферметный анализ – выявляет антитела к хламидиям в сыворотке крови и суставной жидкости.
- Анализ синовиальной жидкости. Может быть повышено количество различных видов лейкоцитов (нейтрофилов – при остром процессе, моноцитов и лимфоцитов – при хроническом).
- Выявление антигена HLA-B27 – в 90 % случаев.
- Рентгенография сустава. Признаки реактивного артрита – кисты в эпифизах, околосуставной остеопороз, воспаление надкостницы, мест крепления сухожилий.
- УЗИ сустава, МРТ – позволяет визуализировать мягкотканые структуры, не видимые на рентгене, наличие суставного выпота.
- Артроскопия – проводится при трудностях в выявлении возбудителя. Врач осматривает сустав изнутри и имеет возможность взять ткани для микроскопического исследования.
К врачу нужно обратиться немедля, если:
- у ребенка покраснение, отек, горячие кожные покровы в области сустава;
- если он жалуется на выраженную боль в суставе;
- при наличии лихорадки.
Последствия реактивного артрита
Без надлежащего лечения реактивные артриты способны вызвать ряд серьезных осложнений. Прежде всего, это касается людей с хроническим течением болезни. Осложнения связаны с частыми обострениями и длительным вяло текущим воспалительным процессом. Чаще всего они встречаются у пациентов, которые обладают генетической предрасположенностью (антигеном HLA-B27).
Наиболее распространенными являются следующие последствия реактивных артритов:
- Хронизация воспалительного процесса . Встречается в среднем у 20% пациентов с реактивными артритами. Она может считаться самым распространенным последствием данного заболевания, так как накладывает отпечаток на жизнь пациента. Человек вынужден длительное время (более года) принимать противовоспалительные препараты, что отражается на его работоспособности.
- Снижение остроты зрения . Является довольно редким последствием синдрома Рейтера. Чаще всего оно вызвано не самой болезнью (которая обычно проходит без последствий самостоятельно), а неправильным приемом препаратов. Без консультации врача-офтальмолога это приведет к обострению хронических заболеваний, если таковые имеются. В частности, речь идет о скрытых формах глаукомы или ускоренном прогрессировании катаракты. Это и становится причиной снижения остроты зрения.
- Ограничение подвижности в суставе . Возникает после интенсивного воспалительного процесса. Отчасти оно объясняется слабостью мышц, если сустав был обездвижен, отчасти – изменениями в полости самого сустава. Наиболее заметно это осложнение при поражении крупных суставов (коленный, локтевой, лучезапястный). При аналогичных проблемах с суставами пальцев ног, например, это не сильно отразится на уровне жизни пациента.
- Хронические болезни внутренних органов . Как уже упоминалось выше, воспалительный процесс при реактивных артритах в редких случаях затрагивает и некоторые внутренние органы. Если пациент поздно обратился к врачу, это может привести к некоторым структурным изменениям и нарушению функции этих органов. В частности, речь идет об утолщении листков плевры и ухудшении фильтрации почек. Наиболее тяжелым осложнением является амилоидоз – отложение патологического белка, которое серьезно нарушает функцию органа.
- Хронические боли в суставе . После перенесенного реактивного артрита остаются редко, но могут беспокоить пациента еще долгие годы. Даже после стихания воспалительного процесса и клинического выздоровления боль иногда остается. Это объясняется структурными изменениями в полости сустава (например, костными наростами на суставных поверхностях или нарушениями выработки суставной жидкости). В результате этих нарушений при движении кости будут сильно тереться друг о друга, что и проявится болевыми ощущениями. Такие боли плохо поддаются медикаментозному лечению и иногда требуют хирургического вмешательства.
Как лечить?
Главной задачей при лечении реактивного артрита у детей в домашних условиях является устранение инфекции.
Если вовремя обратиться к врачу и своевременно начать лечение, то в результате наступает полное выздоровление. К сожалению, некоторые малыши с наследственной предрасположенностью не справляются с болезнью, и реактивный артрит переходит в хроническую форму. При частых рецидивах воспаление может затронуть позвоночник и тем самым вызвать тяжелое заболевание – спондилоартрит.
Лечение реактивного артрита подразумевает комплексный подход:
- для борьбы с возбудителем заболевания назначают антибиотики, подобранные с учетом вида инфекции;
- для устранения болевых ощущений пациенту рекомендуется принимать нестероидные противовоспалительные препараты (Нурофен, Ибупрофен);
- при острых и длительных болях применяют Нимесулид или Диклофенак;
- в осложненных случаях необходимы гормональные препараты – глюкокортикоиды.
При остром течении коленного артрита деткам в полость сустава вводят гормональные препараты (подробнее в статье: лечение артрита коленного сустава у ребенка). Метод достаточно эффективный, но его нельзя применять, если в полости суставной сумки присутствуют бактерии.
На этапе ремиссии отсутствуют выраженные симптомы реактивного артрита. Иногда могут возникать слабые дискомфортные ощущения после подвижных игр, переохлаждения. Для их устранения применяются отвлекающие, местнораздражающие наружные средства, например, бальзамы Ким и Барсучок. Во время ремиссии основные усилия врачей направлены на профилактику болезненных рецидивов за счет укрепления защитных сил организма. Для этого детям показан прием сбалансированных комплексов витаминов и микроэлементов: Витамишки, Супрадин Кидс, Мультитабс.
Восстановлению всех функций суставов способствуют физиопроцедуры. Используются магнитотерапия, электрофорез с диметилсульфоксидом, аппликации с парафином и озокеритом, грязелечение, санаторно-курортное лечение. Обязательны ежедневные занятия физкультурой и гимнастикой для укрепления мышц, улучшения кровоснабжения тканей питательными веществами. Также полезны прогулки на свежем воздухе, плавание, аквааэробика.
Профилактика
Ребенка с детства следует приучать к здоровому образу жизни и соблюдению норм личной гигиены. В качестве профилактических мер родителям рекомендуется выполнять следующие рекомендации:
- Своевременно лечить инфекции и хронические заболевания у взрослых членов семьи.
- При планировании беременности женщине следует обследоваться на хламидиоз и при обнаружении инфекции пройти соответствующее лечение, которое предотвратит внутриутробное заражение ребенка.
- Своевременно лечить и вакцинировать домашних животных.
- Приучать ребенка соблюдать личную гигиену( вовремя мыть руки, не брать в рот грязные игрушки, не пользоваться чужими вещами и т.д.).
- Закаливать малыша, повышать его иммунитет, обеспечить ему правильное, полноценное питание, соблюдать режим дня.
- В подростковом возрасте разъяснять вопросы половой гигиены.
Обязанностью каждого родителя является обеспечение ребенку здорового и полноценного образа жизни, а профилактических мер нужно придерживаться не только в периоды болезни, но и на протяжении всей жизни.
Прогноз
У детей с реактивным артритом прогноз в большинстве случаев благоприятный, потому что детский организм быстро восстанавливается. Главным условием является своевременность лечения. В противном случае возможно развитие хронической формы, рецидивы, поражение других органов, развитие ревматоидного артрита и даже слепота.
Одной из актуальных проблем современной педиатрии является диагностика и лечение воспалительных заболеваний суставов. Наиболее распространен среди ревматических заболеваний детского возраста реактивный артрит (РеА), который встречается
Одной из актуальных проблем современной педиатрии является диагностика и лечение воспалительных заболеваний суставов. Наиболее распространен среди ревматических заболеваний детского возраста реактивный артрит (РеА), который встречается у 86,9 на 100 000 детского населения [1].
В настоящее время к РеА относят воспалительные негнойные заболевания суставов, развивающиеся вследствие иммунных нарушений, после кишечной или урогенитальной инфекции. В преобладающем большинстве случаев РеА ассоциируется с острой или персистирующей кишечной инфекцией, вызываемой энтеробактериями (Yersinia enterocolitica, Yersinia pseudotuberculosis, Salmonella enteritidis, Salmonella typhimurium, Shigella flexneri, Shigella sonnei, Shigella Newcastle, Campylobacter jejuni), и с острой или персистирующей урогенитальной инфекцией, вызываемой Chlamydia trachomatis. Инфекции респираторного тракта, связанные с Mycoplasma pneumoniae, и особенно Chlamydophila pneumonia, также могут служить причинами развития РеА. Имеются также данные о связи РеА с кишечной инфекцией, вызванной Clostridium difficile и некоторыми паразитарными инфекциями.
РеА, ассоциированный с кишечной инфекцией и инфекцией, вызванной Chlamydia trachomatis, развивается преимущественно у генетически предрасположенных лиц (носителей HLA-B27) и относится к группе серонегативных спондилоартритов [2, 3, 6]. Было обнаружено, что антитела к ряду микроорганизмов перекрестно реагируют с HLA-B27. Это объясняется феноменом молекулярной мимикрии, согласно которой белки клеточной стенки ряда кишечных бактерий и хламидий имеют структурное сходство с отдельными участками молекулы HLA-B27. Предполагается, что перекрестно реагирующие антитела способны оказывать повреждающее действие на собственные клетки организма, которые в наибольшей степени экспрессируют молекулы HLA-B27. Но при этом считают, что такое перекрестное реагирование может препятствовать осуществлению адекватного иммунного ответа, способствуя персистированию и хронизации инфекции. Имеются данные, что у носителей НLA-B27 после перенесенной кишечной и урогенитальной инфекции РеА развивается в 50 раз чаще, чем у лиц, не имеющих этого антигена гистосовместимости.
Диагноз РеА ставится в соответствии со следующими диагностическими критериями, принятыми на III Международном совещании по РеА в Берлине в 1996 г. [7].
– Олигоартрит (поражение до 4 суставов).
– Преимущественное поражение суставов ног.
– Время возникновения: за 2–4 нед до развития артрита.
Лабораторное подтверждение инфекции:
– Необязательно, но желательно при наличии клинических проявлений инфекции.
– Обязательно, при отсутствии явных клинических проявлений инфекции.
Критерии исключения — установленная причина развития моно- или олигоартрита:
Вместе с тем в реальной практике термин РеА ошибочно используется ревматологами гораздо шире и включает артриты после перенесенной вирусной инфекции, поствакцинальные артриты, постстрептококковый артрит и некоторые другие.
В настоящее время одной из наиболее распространенных причин развития РеА является хламидийная инфекция.
В структуре РеА хламидийные артриты составляют до 80% [8, 9, 10]. Это связано с пандемией хламидиоза в мире, особенностями путей передачи хламидийной инфекции, цикла развития хламидий и реакции на терапию. Восприимчивость к хламидиям всеобщая, существует множество путей передачи инфекции в том числе и контактно-бытовой путь (в отношении Chlamydia pneumonia). Триггерная роль кишечной инфекции в развитии РеА также остается актуальной.
Классическим проявлением РеА является болезнь Рейтера или уретро-окуло-синовиальный синдром, впервые описанный Бенджамином Броди, а затем Гансом Рейтером, под именем которого синдром и вошел в медицину. Болезнь Рейтера в настоящее время рассматривается как особая форма РеА и характеризуется классической триадой клинических симптомов: уретрит, конъюнктивит, артрит. При наличии кератодермии говорят о тетраде болезни Рейтера. Синдром Рейтера чаще всего начинается с симптомов поражения урогенитального тракта через 2–4 нед после перенесенной инфекции или предполагаемого заражения хламидиями или бактериями кишечной группы. При синдроме Рейтера триггерными инфекционными факторами чаще всего являются Chlamydia trachomatis, Shigella flexneri 2а, либо их сочетание.
Болезнь Рейтера, ассоциированная с хламидийной инфекцией, характеризуется менее выраженной остротой клинической картины [8, 10]. Поражение урогенитального тракта характеризуется стертостью клинической картины. У мальчиков могут развиваться баланит, инфицированные синехии, фимоз. У девочек поражение урогенитального тракта может ограничиваться вульвитом, вульвовагинитом, лейкоцитурией и/или микрогематурией, а также клиникой цистита. Поражение урогенитального тракта может на несколько месяцев опережать развитие суставного синдрома.
Поражение глаз характеризуется развитием конъюнктивита: чаще катарального, невыраженного, непродолжительного, но склонного к рецидивированию. У 1/3 больных может развиться острый иридоциклит, угрожающий слепотой. Поражение глаз также может на несколько месяцев или лет опережать развитие суставного синдрома.
Экссудативный артрит (моно- или олигоартрит) при болезни Рейтера хламидийной этиологии может протекать без боли, скованности, выраженного нарушения функции, но с большим количеством синовиальной жидкости и непрерывно рецидивируя. Поражение суставов при этом характеризуется длительным отсутствием деструктивных изменений, несмотря на рецидивирующий синовит.
Нередко РеА протекает без отчетливых внесуставных проявлений, относящихся к симптомокомплексу синдрома Рейтера (конъюнктивит, уретрит, кератодермия). В таких случаях ведущим является суставной синдром, который также характеризуется преимущественным поражением суставов нижних конечностей, асимметричного характера. Несмотря на отсутствие внесуставных проявлений у этих детей также имеется высокий риск развития ювенильного спондилоартрита. Наличие характерного суставного синдрома, сопровождающегося выраженной экссудацией и связанного с перенесенной кишечной или урогенитальной инфекцией или с наличием серологических маркеров кишечной или урогенитальной инфекции, позволяет с большой долей вероятности отнести заболевание к разряду реактивных артритов.
Диагностика РеА основывается на клинико-анамнестических данных, включающих наличие характерного суставного синдрома, связанного с инфекционным процессом. В связи с тем, что инфекция, предшествующая развитию РеА, не всегда бывает ярко выражена, в процессе диагностики особую значимость приобретают данные дополнительных лабораторных исследований. Для постановки точного диагноза необходимо выделение возбудителя, вызвавшего инфекцию, и/или обнаружение в сыворотке крови высоких титров антител к нему. Для идентификации триггерных инфекций используют различные микробиологические, иммунологические и молекулярно-биологические методы. Этиологическая диагностика включает следующее.
1.1. Выявление антигена хламидий в эпителиальных клетках, полученных в результате соскобов из уретры и конъюнктивы, а также в синовиальной жидкости (прямой иммунофлюоресцентный анализ и др.).
1.2. Выявление антител к антигенам хламидий в сыворотке крови и в синовиальной жидкости (реакция связывания комплемента, прямая и непрямая иммунофлюоресценция):
- острая фаза хламидиоза или обострение хронического процесса — наличие иммуноглобулин (Ig) M в течение первых 5 дней, IgA — в течение 10 дней, IgG — через 2–3 нед;
- реинфекция или реактивация первичной хламидийной инфекции — повышение уровня IgG, определяются IgA, могут быть единичные IgM;
- хроническое течение хламидиоза — наличие постоянных титров IgG и IgA;
- бессимптомное течение хламидиоза, персистенция возбудителя — низкие титры IgA;
- перенесенная хламидийная инфекция — низкий титр IgG.
1.3. Выявление антител к бактериям кишечной группы в сыворотке крови (при помощи реакции прямой гемагглютинации и реакции связывания комплемента).
Наиболее доказательным является выделение триггерных микроорганизмов классическими микробиологическими методами (посевы кала, перенос соскоба с эпителия уретры и/или конъюнктивы на культуру клеток). Чаще удается выделить хламидии из урогенитального тракта, значительно реже — энтеробактерии из кала.
Трудности диагностики РеА часто обусловлены стертым субклиническим течением первичного инфекционного процесса. Артрит развивается чаще при нетяжелых формах кишечной или урогенитальной инфекций, и к моменту развития артрита признаки триггерной инфекции в большинстве случаев проходят. Кроме того, в условиях нарушенного иммунного ответа возможно развитие хронических персистирующих форм инфекции. Поэтому в дебюте суставного синдрома необходимо в первую очередь исключить скрытую кишечную и хламидийную инфекции. Кроме того, диагностику РеА затрудняет сочетание предшествовавших инфекционных процессов различной локализации. Установлено также, что поражение кишечника и мочевыводящих путей может быть как первичным по отношению к РеА, так и развиваться одновременно с ним и даже позже, что нередко затрудняет определение причинно-следственных связей.
Дифференциальный диагноз РеА от других видов ювенильных артритов часто бывает затруднен. Наиболее распространенной патологией, требующей дифференциальной диагностики с РеА, являются инфекционные артриты, заболевания, связанные с инфекцией, сопровождающиеся артритами, а также ортопедическая патология и разные формы ювенильного идиопатического артрита.
Вирусный артрит. В настоящее время известно, что около 30 вирусов могут вызывать развитие острого артрита. К ним относятся: вирусы краснухи, парвовирус, аденовирус, вирус гепатита В, вирусы герпеса различных типов, вирус паротита, энтеровирусы, Коксаки-вирусы и др. Диагностика основана на связи с вирусной инфекцией или проведенной вакцинацией. Клиническая картина чаще представлена артралгиями, чем артритами. Клинические симптомы наблюдаются в течение 1–2 нед и исчезают без остаточных явлений.
Диагностические критерии постстрептококкового артрита включают:
- появление артрита на фоне или спустя 1–2 нед после перенесенной носоглоточной инфекции (стрептококковой этиологии);
- одновременное вовлечение в процесс преимущественно средних и крупных суставов;
- возможную торпидность суставного синдрома к действию нестероидных противовоспалительных препаратов (НПВП), нерезкие сдвиги в лабораторных показателях;
- наличие повышенных титров постстрептококковых антител;
- выявление хронических очагов инфекции в носоглотке (хронический тонзиллит, фарингит, гайморит).
Клещевой боррелиоз (болезнь Лайма). Диагностика боррелиоза основана на данных анамнеза: пребывание пациента в эндемичной зоне, наличие в анамнезе факта укуса клеща, а также характерную клиническую картину. Подтверждают диагноз серологическими методами, которые выявляют антитела к Borrelia burgdorferi.
Диагноз септического артрита ставится на основании клинической картины инфекционного процесса, определения характера синовиальной жидкости, результатов посева синовиальной жидкости на флору с определением чувствительности к антибиотикам, а также рентгенологических данных (в случае развития остеомиелита).
Клиническая картина туберкулезного артрита представлена общими симптомами туберкулезной инфекции: интоксикацией, субфебрильной температурой, вегетативными нарушениями и локальными симптомами — боли в суставах, преимущественно в ночное время, явления артрита. Для подтверждения диагноза необходимы рентгенологические данные, анализ синовиальной жидкости, биопсия синовиальной оболочки.
Ювенильный спондилоартрит. Данное заболевание является возможным исходом хронического течения РеА у предрасположенных лиц (HLA-B27 носителей). Суставной синдром так же, как и при РеА, представлен асимметричным моно- или олигоартритом с преимущественным поражением суставов ног. Кардинальными признаками, позволяющими поставить диагноз ювенильного спондилоартрита, являются рентгенологические данные, свидетельствующие о наличии сакроилеита (одно- или двустороннего).
Выделяют три вида терапии: этиотропную, патогенетическую, симптоматическую.
Этиотропное лечение РеА, ассоциированного с хламидийной инфекцией. Поскольку хламидии являются внутриклеточными паразитами, то выбор антибактериальных препаратов ограничивается только теми, которые способны накапливаться внутриклеточно. К таким препаратам относятся макролиды, тетрациклины и фторхинолоны. Однако тетрациклины и фторхинолоны достаточно токсичны, их применение ограничено в детской практике. В связи с этим для лечения хламидийного артрита у детей используются макролиды. Азитромицин — для детей в первый день приема доза препарата составляет 10 мг/кг, а в последующие 5–7 дней — 5 мг/кг в один прием. Лучший эффект достигается при использовании антибиотика в течение 7–10 дней. Рокситромицин — для детей суточная доза составляет 5–8 мг/кг массы тела. Джозамицин (вильпрафен) суточная доза препарата составляет 30–50 мг/кг массы тела, разделенные на три приема. Кларитромицин используется у детей старше 6 мес — 15 мг/кг/сут в 2 приема, спирамицин — детям массой более 20 кг из расчета 1,5 млн МЕ/10 кг массы тела в сутки. Кратность приема — 2–3 раза.
У подростков возможно применение тетрациклинов и фторхинолоновых препаратов.
В отношении РеА, связанных с кишечной инфекцией, однозначных рекомендаций по антибактериальной терапии не существует. Наличие антител к бактериям кишечной группы и особенно бактериологическое подтверждение кишечной инфекции является основанием для назначения антибиотиков. Используются аминогликозиды — амикацин в/м или в/в — до 15 мг/кг/сут в одно-два введения, 7 сут, гентамицин в/м или в/в 5–7 мг/кг/сут в два введения, 7 сут, фторхинолоновые препараты (для детей старше 12 лет).
Патогенетическая терапия. Монотерапия антибиотиками оказывает недостаточный эффект при затяжном и хроническом течении РеА, неадекватности иммунного ответа. Целесообразно для лечения хронического хламидийного артрита использовать различные иммуномодулирующие средства (тактивин, ликопид, полиоксидоний) в сочетании с антибиотиками.
Наиболее эффективной, по результатам многолетних контролируемых исследований, оказалась схема с использованием ликопида [8, 10, 13].
Схема комбинированной терапии ликопидом и антибиотиками у больных с хроническим течением РеА, ассоциированного с хламидийной инфекцией, следующая.
- Ликопид применяется в виде сублингвальных таблеток. Детям до 5 лет целесообразно назначать ликопид по 1 мг 3 раза в день, дети старше 5 лет — ликопид по 2 мг 3 раза в день. Курс лечения составляет 24 дня.
- На 7-й день приема ликопида назначается антибиотик. Возможно использование любого антибиотика, обладающего противохламидийной активностью. Так как необходимо перекрыть 2–3 жизненных цикла хламидий, курс лечения антибиотиком должен составлять не менее 7–10 дней.
- После завершения курса антибактериальной терапии дети продолжают получать ликопид до 24 дня.
Использование иммуномодуляторов противопоказано при трансформации РеА в спондилоартрит, высокой иммунологической активности.
Симптоматическая терапия. С целью лечения суставного синдрома при РеА применяют НПВП. Диклофенак внутрь 2–3 мг/кг/день в 2–3 приема или напроксен внутрь 15–20 мг/кг/день в 2 приема или ибупрофен внутрь 35–40 мг/кг в 2–4 приема или нимесулид внутрь 5 мг/кг в 2–3 приема или мелоксикам внутрь 0,3–0,5 мг/кг в 1 прием.
Глюкокортикостероиды как наиболее мощные противовоспалительные средства используются в период обострения суставного синдрома. Их применение ограничивается преимущественно внутрисуставным способом введения. При необходимости можно воспользоваться коротким курсом пульс-терапии метилпреднизолоном, который предполагает быстрое (в течение 30–60 мин) внутривенное введение больших доз метилпреднизолона (5–15 мг/кг в течение 3 дней).
При тяжелом и торпидном течении заболевания, появлении признаков спондилоартрита, высокой клинической и лабораторной, в том числе иммунологической, активности возможно применение иммуносупрессивных препаратов. Наиболее часто используется сульфасалазин (в дозе 30–40 мг/кг массы в сутки), реже метотрексат ( в дозе 10 мг/м 2 в неделю).
У большинства детей РеА заканчивается полным выздоровлением. У части больных эпизоды РеА рецидивируют и в дальнейшем появляются признаки спондилоартрита, особенно у HLA-B27 позитивных больных. Мерами профилактики являются своевременное выявление хламидийной инфекции у ребенка и членов его семьи, адекватная терапия урогенитальной инфекции.
Е. С. Жолобова, доктор медицинских наук, профессор
Е. Г. Чистякова, кандидат медицинских наук, доцент
Д. В. Дагбаева
ММА им. И. М. Сеченова, Москва
Читайте также:


