Амиотрофия при ревматоидном артрите
Ревматоидный артрит представляет собой системное иммуновоспалительное заболевание соединительной ткани, проявляющееся хроническим эрозивно-деструктивным полиартритом с преимущественно симметричным поражением суставов кистей и стоп и сопровождающееся у бо
Ревматоидный артрит представляет собой системное иммуновоспалительное заболевание соединительной ткани, проявляющееся хроническим эрозивно-деструктивным полиартритом с преимущественно симметричным поражением суставов кистей и стоп и сопровождающееся у большинства больных образованием особого вида аутоантител (ревматоидный фактор). Женщины болеют в 3–4 раза чаще мужчин, причем заболевание у них начинается обычно в возрасте 35–45 лет.
Болезненные, тугоподвижные суставы не только мешают выполнять самые простые повседневные движения, но и значительно нарушают ритм нормальной жизни.
Ревматоидный полиартрит — тяжелое системное заболевание, которое проявляется прогрессирующим воспалительным синовитом, симметрично поражающим периферические суставы конечностей.
В соответствии с рекомендациями Американской ревматологической ассоциации (1987) при диагностике ревматоидного артрита целесообразно придерживаться следующих критериев:
- утренняя скованность суставов или вблизи суставов длительностью не менее 1 ч до ее полного исчезновения;
- опухание мягких тканей (артрит) трех суставов или более, наблюдаемое врачом (т. е. в период осмотра или в анамнезе под наблюдением врача);
- опухание (артрит) проксимальных межфаланговых, пястно-фаланговых или запястных суставов;
- симметричное опухание (артрит) как минимум в одной паре суставов;
- ревматоидные узелки;
- наличие ревматоидного фактора;
- обнаружение при рентгенологическом исследовании эрозий и (или) периартикулярного остеопороза в суставах кистей и стоп.
При длительно текущем заболевании деформируются пораженные суставы. Помимо суставов, при ревматоидном полиартрите нарушаются околосуставные структуры (связки, сухожилия и др.), развиваются ревматоидный васкулит (поражение мелких сосудов), остеопороз, происходит поражение внутренних органов.
В пользу иммунопатологического/аутоиммунного характера воспалительного процесса при ревматоидном артрите свидетельствует обнаружение у большинства больных в сыворотке крови и синовиальном выпоте из пораженных суставов аутоантител — ревматоидного фактора.
Большое значение в развитии ревматоидного артрита имеет генетическая предрасположенность. Это подтверждается выраженной семейной агрегацией заболевания, наличием у части больных ревматоидным артритом антигенов II класса главного комплекса гистосовместимости HLA DR4 и Dw4 (с носительством которых связывают тяжелое течение артрита и быстрое прогрессирование эрозивных изменений суставов). Рассматривается роль наследственных или приобретенных нарушений Т-супрессорной регуляции иммунных реакций, недостаточной функции моноцитарно-макрофагальной системы. Пусковую роль в развитии ревматоидного артрита могут играть: хронические очаги инфекции, гормональная перестройка организма, пищевая аллергия, предшествующие травмы суставов, длительное воздействие влажного холода и физическое перенапряжение.
При хроническом воспалении у края суставного хряща в месте прикрепления к эпифизам суставной капсулы происходит разрушение и замещение паннусом участков субхондральной костной ткани с образованием эрозий. Иногда разрастающиеся грануляции проникают через субхондральную замыкательную пластинку в костную ткань. Продукты костно-хрящевой деструкции, в свою очередь, оказывают раздражающее воздействие на синовиальную оболочку, что способствует поддержанию в ней воспалительного процесса. Одновременно возникают воспалительные изменения в капсуле сустава, связках, синовиальной выстилке сухожилий и синовиальных сумках с последующим их склерозированием, приводящему к стойкому ограничению подвижности пораженных суставов, подвывихам и контрактурам. Иногда наблюдается некроз и разрыв сухожилий, синовиальных сумок. Нередко отмечается развитие вторичного остеоартроза.
Воспалительный процесс при ревматоидном артрите характеризуется неуклонным прогрессированием, темпы которого зависят от активности воспалительного процесса. Даже в периоды клинической ремиссии в синовиальной оболочке сохраняются признаки воспаления. Постепенно паннус разрушает хрящ на значительной поверхности эпифиза, а замещающая его грануляционная ткань соединяет между собой противоположные суставные поверхности и в последующем трансформируется вначале в фиброзную, а затем в костную ткань, что приводит к образованию соответственно фиброзного и костного анкилоза, обусловливающего полную неподвижность пораженных суставов.
При рентгенологическом исследовании суставов отмечается асимметричность эрозивных изменений с частым и ранним анкилозированием суставов запястий.
Течение серонегативного ревматоидного артрита менее тяжелое, в прогностическом плане более благоприятное, чем при серопозитивной форме заболевания: слабее выражены деструктивные (эрозивные) изменения и функциональные нарушения суставов, реже наблюдаются ульнарная девиация пальцев кистей, контрактуры и анкилоз (за исключением анкилоза суставов запястья). Вместе с тем серонегативный ревматоидный артрит хуже, чем серопозитивный, поддается терапии базисными и иммуносупрессивными препаратами. Чаще развивается вторичный амилоидоз.
При лечении ревматоидного артрита используются НПВП, в тяжелых случаях применяются глюкокортикостероиды, иммуносупрессоры, с целью профилактики остеопороза обычно назначают комбинацию препаратов кальция и витамина D.
Несмотря на все успехи фармакологии, ревматоидный артрит до настоящего времени остается тяжелым заболеванием с неблагоприятным прогнозом.
Приведем пример из личного опыта ведения больной с ревматоидным артритом, представляющим, по мнению автора, научный интерес.
Больная В., возраст — 71 год, обратилась к неврологу в августе 2006 г. с жалобами на боли в суставах кистей, коленных суставах, в пояснице. Боль в суставах беспокоила днем и ночью, обычно была выраженной, нередко мигрирующей, обусловливала ограничение всех активных и пассивных движений в пораженных суставах. Артралгия зачастую сочеталась с выраженной миалгией, оссалгией, болями в сухожилиях. Из анамнеза: проявления полиостеоартроза в течение 15 лет, дебют суставного синдрома воспалительного характера в июне 2002 г. (отек и воспаление в области суставов, фебрильная лихорадка, подтвержденная лабораторно активность воспалительного процесса). Амбулаторно (сначала периодически, в последние 3 года постоянно) получала НПВП (ибупрофен, индометацин, диклофенак, ацеклофенак). С 2004 г. регулярно принимала кальций D3 (1 г кальция в сутки).
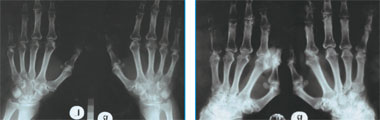 |
| Рис. 1. Рентгенограмма кистей больной В. 2003 г.: проявления полиостеоартроза, явных эрозий нет. Рис. 2. Рентгенограмма кистей больной В. 2006 г.: множественные кисты и эрозии, отрицательная динамика с 2003 г. |
Стационарно проходила лечение в городском ревматологическом центре г. Санкт-Петербурга (апрель 2003 г., июнь–июль 2006 г.) с диагнозом: ревматоидный артрит, серопозитивный, с системными проявлениями (субфебрилитет, амиотрофия, миалгии), активность 2-й степени, функциональная недостаточность суставов 1–2-й степени. Сопутствующая патология: ишемическая болезнь сердца, стенокардия II ФК. Гипертоническая болезнь 3-й степени, ОНМК (декабрь 2002 г.). Хронический бронхит вне обострения. Диффузный зоб второй стадии. Эутиреоз. Полиостеоартроз. Желчно-каменная болезнь.
С 2003 г. постоянно получает метотрексат в дозировке 2,5 мг 2 раза в неделю. Несмотря на проводимое лечение, суставной болевой синдром нарастал, учащались обострения, ухудшалось состояние костей (остеопороз, эрозии). Показательна рентгенография кистей (рис. 1–2).
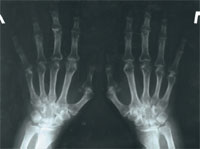 |
| Рис. 3. Рентгенограмма кистей больной В. 2007 г.: проявления полиостеоартроза, положительная динамика с 2006 г. |
С августа 2006 г. на фоне лечения метотрексатом неврологом был дополнительно назначен Структум в дозировке 500 мг 2 раза в день. Больная ориентирована врачом на длительный, до полугода, прием препарата. Некоторое уменьшение интенсивности (непрекращающегося в течение 2 последних месяцев) болевого синдрома наступило через 3 нед. Эпизоды обострений ревматоидного артрита были в течение 4 мес. К концу 5-го месяца комбинированной терапии (метотрексат + Структум) болевой синдром значительно снизился, уменьшилась утренняя скованность, спала отечность лучезапястных и коленных суставов.
В феврале 2007 г. была сделана рентгенография кистей (рис. 3). Результат сравнения с предыдущими рентгенографиями оказался более чем положительным (уменьшились эрозии костей). Прием структума продлен на 3 мес. По состоянию на май 2007 г. обострений суставного синдрома не наблюдалось в течение 4 мес, сохранялась небольшая отечность на лучезапястных (больше слева) и коленных суставах. С целью коррекции противоревматической терапии (снижение дозы метотрексата) больной рекомендована консультация в городском ревмоцентре.
И. Н. Бабурин
СПбНИПНИ им. В. М. Бехтерева, Санкт-Петербург
Мышцы поражаются у большинства больных РА. Мышечная слабость и атрофия отмечаются не менее чем у 75% больных. Причиной этих симптомов служит уменьшение мышечной активности в связи с болью в суставах и особенно их контрактурами. Эта причина, однако, не может считаться единственной. Еще в 1873 г. J. Paget писал, что мышечная атрофия при РА пропорциональна не столько ограничению движений, сколько выраженности боли.
Спустя почти столетие J. De Andrade (1968) доказал в эксперименте, что атрофия мышц у животных с артритами выражена сильнее, чем вызванная иммобилизацией. О том же свидетельствуют частые клинические наблюдения, касающиеся быстро развивающейся амиотрофии при тяжелом РА. Темпы ее развития при этом более быстрые, чем при обычной иммобилизации, тем более что в подобных случаях общий объем движений часто остается немалым.
Поэтому основными причинами мышечной патологии у больных РА следует считать как ограничение мускульной активности, так и катаболическое влияние воспалительного процесса (возможно, опосредуемое эффектом интерлейкина-1 и фактором некроза опухоли, вырабатываемых макрофагами). Последнее может значительно усугубляться сопутствующей лихорадкой, частым ухудшением аппетита, нерациональным питанием (в частности, бедным белками).
Трактовка данных биопсий вне связи с клиническими и биохимическими показателями должна быть очень осторожной. Микроскопический анализ мышечной ткани нередко обнаруживает сосудистые изменения и клеточные инфильтраты, формально соответствующие представлениям о воспалении, у лиц без какой-либо мышечной патологии. Возможно, что речь идет о реакции на транзиторные физиологические сдвиги (большее накопление молочной кислоты и т. д.).
Не подтвердилось также мнение об относительной специфичности для РА так называемого узелкового полимиозита, представляющего собой узелковые клеточные инфильтраты диаметром 1—2 мм, обильно рассеянные в эндомизии и перимизии и состоящие из скоплений лимфоцитов и плазматических клеток, в редких случаях — тучных клеток, нейтрофилов и эозинофилов. L. Sokoloff и соавт. (1950) показали, что подобные изменения наблюдались у 56% больных РА, у 29% больных неревматическими заболеваниями и у 23% здоровых.
Повышение уровня мышечных ферментов в крови имеет большое значение для диагноза ревматоидного миозита. Однако необходимо принимать во внимание, что содержание этих ферментов у больных РА может повыситься также вследствие внутримышечных инъекций, мышечной биопсии, индивидуальных реакций на некоторые лекарства (хлорохин, ацетилсалициловая кислота, D-пеницилламин) и даже значительной физической нагрузки. В связи с этим диагностика ревматоидного миозита надежна лишь при сочетании клинических симптомов с ферментемией и гистологическими воспалительными изменениями или (что менее убедительно) при комбинировании двух компонентов этой триады.
Четко очерченный синдром миозита у больных РА редок. Относительно чаще он встречается при ревматоидном васкулите, однако и в этих случаях (при локализации васкулита в мышцах) его клиническое значение обычно невелико. Поэтому особый интерес вызывает наблюдение Г. Н. Жуковской (1987) больного классическим серопозитивным и эрозивным РА (без васкулита), у которого миозит в течение длительного времени настолько превалировал над суставными проявлениями, что правильный диагноз был поставлен более чем через год.
Необходимо иметь в виду, что заметная мышечная патология у больных РА в редких случаях может быть связана с влиянием некоторых лекарств. Так, глюкокортикостероиды (прежде всего содержащие фтор — триамцинолон, дексаметазон), особенно при их длительном назначении в больших дозах, вызывают у отдельных больных так называемую стероидную миопатию. Ее симптомы обычно развиваются постепенно и относятся преимущественно к проксимальным мышцам ног, а затем и рук (боли, быстрая утомляемость, затруднения при подъеме на лестницу и при вставании с низкого стула).
Эти симптомы нередко оцениваются как признаки обострения основного заболевания, что ведет к увеличению дозы стероидов и тем самым к усугублению миопатических проявлений. Уровень сывороточных мышечных ферментов при стероидной миопатии нормален. Ценный лабораторный признак — повышенное выделение креатина с мочой. При гистологическом исследовании мышц не обнаруживают достоверных воспалительных изменений; отмечаются лишь неспецифические дистрофические симптомы — потеря поперечной исчерченности, атрофия волокон и т. д. После уменьшения дозы гормональных препаратов и особенно полной отмены их признаки стероидной миопатии исчезают, чему способствует лечебная физкультура, направленная на упражнения для соответствующих мышц.
Назначение D-пеницилламина у некоторых больных может вызвать патологию мышц двух различных типов. Относительно чаще встречается синдром миастении (myasthenia gravis). Он проявляется в постепенном нарастании слабости различных мышечных групп с соответствующими функциональными нарушениями (слабость, утомляемость, диплопия, нарушения глотания и речи, птоз, затруднения при выполнении простых движений).
Повышения уровня мышечных ферментов в крови и гистологической картины миозита не наблюдается. У некоторых больных . определяются антитела к тканевым компонентам мышечных поперечных полос и к ацетилхолиновым рецепторам мышц (последнее обстоятельство может быть непосредственной причиной мышечной слабости). После отмены D-пеницилламина симптомы миастении постепенно исчезают; при недостаточном восстановлении мышечной силы назначают прозерин.
У единичных больных при назначении D-пеницилламина описано развитие истинного полимиозита с миалгиями, слабостью проксимальных мышц конечностей, нарастанием уровня мышечных ферментов и характерной гистологической картиной (инфильтрация лимфоцитами и макрофагами, участки дегенерации и регенерации мышечных волокон). Для лечения этого осложнения необходимо отменить D-пеницилламин, в серьезных случаях — назначить глюкокортикостероиды.
Хлорохиновая миопатия также представляет собой очень редкое лекарственное осложнение. Она характеризуется постепенно прогрессирующей слабостью проксимальных мышц ног, затем — рук, позже — более дистальных мышечных групп. Уровень мышечных ферментов в крови может быть повышен. Характерный гистологический признак — вакуолизация мышечных волокон. Отмена хлорохина приводит к полному, но медленному выздоровлению.
Назначение гидроксихлорохина (плаквенила) не вызывает миопатии. Таким образом, в основе изменений мышц при РА могут лежать принципиально различные причины: миозит, атрофия вследствие недостаточных упражнений, вызванные воспалительным процессом катаболические сдвиги в обмене веществ, недостаточное белковое питание и, наконец, редкие и сугубо индивидуальные (возможно, генетически обусловленные) реакции на определенные лекарственные препараты.
Поэтому в каждом конкретном случае явной мышечной патологии у больного РА необходим соответствующий клинический и анамнестический анализ с определением в крови уровня мышечных ферментов; по показаниям проводят биопсию наиболее пораженных отделов мышц.
Ревматоидный артрит – тяжелое, с трудом поддающееся лечению заболевание. Причины развития его установлены не полностью, тем не менее, при проведении правильно назначенного комплексного лечения качество жизни пациента может быть вполне удовлетворительным. Но это при условии неукоснительного выполнения больным всех рекомендаций лечащего врача.
Что такое ревматоидный артрит
Ревматоидный артрит (РА) – хроническое системное прогрессирующее заболевание, проявляющееся в виде воспаления в основном мелких суставов. Связано оно не с инфекцией, а с поломкой иммунной системы. Поражается соединительная ткань, поэтому данное заболевание называется системным. Патологический процесс часто распространяется и внутренние органы (сердце, сосуды, почки) – это внесуставные проявления болезни.
Всего в мире ревматоидным артритом болеет около 1% населения. Заболеть можно в любом возрасте, но чаще это случается в 35 – 55 лет у женщин и немного позже (в 40 – 60 лет) у мужчин. Ревматоидный артрит у женщины диагностируют в три раза чаще, чем мужчины.
Причины
Точные причины начала данного заболевания не установлены. Но известны основные причинные факторы:
- Наследственная предрасположенность – встречаются случаи семейных заболеваний.
- Влияние внутренних (эндогенных) факторов – у большинства больных женщин и мужчин отмечается низкий уровень мужских половых гормонов; научно подтверждено, что после использования оральных контрацептивов (ОК) риск развития болезни снижается.
- Влияние факторов внешней среды (экзогенных). Возбудители инфекции запускают аутоиммунную реакцию – аллергию на собственные ткани организма. Это связано с тем, что некоторые инфекционные возбудители имеют в составе своих клеток белки, схожие с белками тканей человека. При попадании этих возбудителей в организм иммунная система вырабатывает антитела (IgG), которые по неизвестной науке причине становятся антигенами (чужеродными для организма веществами). На них вырабатываются новые антитела IgM, IgA, IgG (ревматоидные факторы), уничтожающие их. Нарастание количества антител сопровождается усилением воспаления. Некоторые возбудители выделяют вещества, способствующие разрастанию суставной синовиальной оболочки и ферменты, повреждающие ткани.
В результате целого комплекса причин клетки синовиальной оболочки начинают выделять воспалительные цитокины – белковые молекулы, инициирующие и поддерживающие воспаление. Развивается длительно протекающий воспалительный процесс, происходит разрушение хрящевой и костной суставной ткани, деформация конечности. Хрящевая ткань заменяется соединительной, появляются костные разрастания, нарушается функция сустава. Очень часто причиной развивающегося аутоиммунного поражения суставов является герпетическая инфекция – вирусы простого герпеса 1, 2 типа, цитомегаловирус, вирус Эпштейна – Барр (вызывает мононуклеоз) и другие возбудители, например, микоплазмы.
Предрасполагающие (запускающие, триггерные) факторы:
- травмы, заболевания суставов;
- переохлаждения, постоянное пребывание в сыром помещении или в сыром климате;
- нервные перенапряжения, стрессы;
- имеет значение наличие хронических очагов инфекции – тонзиллиты, кариозные зубы, любые инфекционно-воспалительные процессы;
- прием некоторых лекарств с мутагенными свойствами.
Симптомы
Заболевание протекает волнообразно, в виде периодов обострений (рецидивов) и ремиссий.
Начало в большинстве случаев подострое и имеет связь с перенесенной инфекцией, переохлаждением, травмой или нервным перенапряжением, беременностью, родами.
Одновременно появляются незначительно выраженные боли в пораженных суставах, сначала преходящие, а затем постоянные. Еще один из первых симптомов, на который стоит обратить внимание, - легкая припухлость в суставной области. Она может проходить в течение дня, но затем становится постоянной.
В большинстве случаев при ревматоидном артрите поражается сначала небольшое количество суставов стоп и кистей. На ранней стадии могут также поражаться коленные суставы. Поражения симметричны. При подостром течении первые признаки нарушений появляются через несколько недель, при медленном, хроническом – через несколько месяцев.
Острое начало, высокая активность патологического процесса и системные проявления характерны для ювенильного ревматоидного артрита у детей и подростков. Он может начинаться с высокой температуры, изначального поражения сразу нескольких суставов и признаков поражения внутренних органов.
Ревматоидный артрит сопровождается признаками общей интоксикации. Это слабость, недомогание, небольшое повышение температуры тела, головные боли. Нарушается аппетит, больной теряет массу тела.
Суставной синдром. Поражаются сначала мелкие суставы кисти (число их увеличивается), а затем и крупные суставы (плечевые, коленные). Они опухают, становятся очень болезненными, постепенно теряют свою функцию, обездвиживаются. Длительное обездвиживание приводит к выраженной атрофии (уменьшению в объеме) мышц. Ревматоидный артрит характеризуется также тем, что поражения разных суставов могут быть неодинаковыми: в одних могут преобладать признаки воспаления (отек), в других – пролиферации (разрастания соединительной ткани с деформацией и нарушением функции).
Появляются подкожные ревматоидные узелки – небольшие, умеренно плотные, безболезненные образования, располагающиеся на поверхности тела, чаще всего на коже локтей.
Поражается периферическая нервная система. Из-за поражения нервов больные ощущают онемение, жжение, зябкость в конечностях.
При ревматоидном васкулите происходит поражение различных мелких и частично средних кровеносных сосудов. Часто это проявляется в виде точечных очагов некроза в области ногтей или безболезненных язв в области голени. Иногда васкулит может проявляться в виде микроинфарктов.
При частых обострениях и прогрессировании ревматоидного артрита происходит поражение внутренних органов - сердца (эндокардит), почек (нефрит), легких (узелковое поражение легочной ткани) и т.д.
К врачу следует обращаться при появлении следующих симптомов:
- Болей в суставах, легкой скованности движений по утрам, если:
- кто-то из близких родственников болеет ревматоидным артритом;
- вы недавно перенесли какое-то инфекционно-воспалительное заболевание (ОРВИ, ангину), затяжной стресс или просто переохладились;
- вы проживаете в холодной сырой местности.
- Небольшого повышения температуры, недомогания, снижения аппетита, потери массы тела, сопровождающихся легкой утренней скованностью движений.
Локализации процесса
При ревматоидном артрите вначале обычно поражаются мелкие суставы кистей, пальцев рук и стоп. Внешний вид верхних х конечностей:
Хруст в суставах - когда стоит беспокоиться
Внутрисуставные инъекции гиалуроновой кислоты
Внешний вид нижних конечностей:
- пальцы стоп приобретают молоточковидную форму;
- подвывихи мелких суставов приводят к развитию плоскостопия;
- для ревматоидной стопы характерно также вальгусное (кнаружи) отклонение стопы, связанное с поражением голеностопа;
- при поражении коленных суставов появляется сгибательная контрактура (неподвижность).
Тазобедренные суставы поражаются редко.
Стадии ревматоидного артрита
Ревматоидный артрит протекает в три стадии:
- Начальная, воспаления– поражение синовиальных сумок сопровождается болями, отеком околосуставных тканей.
- Прогрессирующая, пролиферации – быстрое деление клеток синовиальной оболочки, приводящее к ее уплотнению.
- Завершающая, деформации – при длительном течении воспаленные клетки начинают выделять фермент, разрушающий хрящевую и костную ткань, что приводит к изменению суставной формы и тяжелому нарушению их функции.
По длительности течения выделяют следующие стадии ревматоидного артрита:
- очень ранняя – до полугода;
- ранняя – от полугода до года;
- развернутая – до 2-х лет;
- поздняя – после 2-х лет.
- Околосуставной остеопороз – разрежение, истончение костной ткани;
- Сужение суставной щели и единичные эрозии на хрящевой суставной поверхности;
- Множественные глубокие эрозии суставных хрящей и костей;
- Присоединяется анкилоз - неподвижность сустава из-за сращения суставных поверхностей.
Стадии ревматоидного артрита
Существует несколько типов классификаций ревматоидного артрита по разным критериям.
По клинико-анатомическим признакам выделяют следующие формы ревматоидного артрита:
- суставная форма;
- суставно-висцеральная (системная) – поражаются не только суставы, но и внутренние органы;
- ювенильная форма – развивается у детей до 16 лет, характеризуется острым началом, лихорадкой и выраженными внесуставными проявлениями.
- медленнопрогрессирующий РА – самая частая форма, может продолжаться годами;
- быстропрогрессирующий РА – характеризуется злокачественным течением;
- без признаков прогрессирования – встречается редко.
По иммунологическим признакам:
- Наличие или отсутствие содержания в крови ревматоидного фактора (РФ) – антител к собственному иммуноглобулину G:
- серопозитивные – РФ обнаружен;
- серонегативные – РФ не обнаружен.
- Наличие или отсутствие в крови антител к циклическому цитрулинсодержащему пептиду – анти-ЦЦП или АЦЦП (цитрулин – продукт обмена, в норме полностью выводящийся из организма; при РА выделяются ферменты, встраивающие цитрулин в белки и превращающие его в чужеродный белок – антиген; на этот антиген иммунная система вырабатывает антитела):
- серопозитивные – АЦЦП обнаружен;
- серонегативные – АЦЦП не обнаружен.
Выделяют следующие критерии сохранности функций опорно-двигательного аппарата:
- Выполнение движений в полном объеме.
- Снижение двигательной активности. Появляются трудности, не позволяющие выполнять движения в полном объеме, особенно в профессиональной сфере.
- Нарушение подвижности, возможно только самообслуживание.
- Невозможны любые виды двигательной активности, в том числе самообслуживание.
Что будет, если не лечить
Если ревматоидный артрит не начать лечить своевременно, в дальнейшем он начнет быстро прогрессировать, что увеличивает риск развития возможных осложнений:
- деформации и утрата суставных функций, приводящие к инвалидности;
- изменению нервно-мышечной системы с нейропатиями и уменьшением объема мышц;
- поражению сердечно-сосудистой системы в виде васкулитов, эндокардитов, микроинфарктов;
- нарушениям со стороны почек с постепенным формированием хронической почечной недостаточности;
- поражениям органов зрения, в том числе язвенного характера;
- поражению плевры и легких - развитию плеврита и интерстициальной пневмонии;
- развитию анемии и системных тромбозов мелких кровеносных сосудов.
Диагностика
Диагноз ревматоидного артрита подтверждается данными дополнительного обследования. Диагностика ревматоидного артрита включает:
- Лабораторные исследования:
- общий анализ крови – выявляет воспалительный процесс (ускоряется СОЭ, изменяется число лейкоцитов);
- биохимия – позволяет уточнить причины воспаления и нарушения обменных процессов;
- иммунологические исследования – наличие или отсутствие специфических антител.
- Инструментальные исследования:
- рентгендиагностика – выявляет патологию суставов;
- компьютерная и магнитно-резонансная томография (КТ, МРТ) – позволяют провести оценку ранних суставных изменений;
- УЗИ – выявляет увеличение объема суставной жидкости и наличие участков некроза.
Как лечат ревматоидный артрит
Лечение ревматоидного артрита начинается с устранения воспаления и боли. Затем присоединяется комплексное лечение:
- диета;
- медикаментозная терапия (базисное лечение);
- средства народной медицины;
- физиотерапевтические процедуры;
- лечебная гимнастика и массаж;
- новые методики;
- хирургические методы лечения.
Питание при ревматоидном артрите должно быть регулярным и полноценным. В суточном рационе должны присутствовать продукты, богатые кальцием (творог, сыр, кефир), овощи, фрукты, овощные супы, нежирное мясо и рыба.
Из рациона должны быть исключены: концентрированные бульоны, овощи, богатые эфирными маслами (свежий лук, чеснок, редис), жирные, копченые, консервированные продукты, сладости, сдоба, сладкие газированные напитки. Должен быть полностью исключен прием алкоголя.
Это индивидуально подобранная терапия, включающая в себя применение нестероидных противовоспалительных препаратов (НПВП), глюкокортикоидных средств (ГКС), базисных препаратов и биологических агентов.
Чтобы облегчить состояние больного, лечение начинают с назначения НПВП. Современные лекарственные препараты этого ряда (нимесулид, целекоксиб, мелоксикам) снимают воспаление и боль в суставах, не вызывая выраженных побочных явлений, характерных для ранних НПВП (диклофенака и др.).
Если воспаление и боль носят выраженный характер и НПВП не помогают, назначают глюкокортикоидные гормоны (ГКС - преднизалон, дексаметазон, триамсинолон). Они быстро снимают отек, боль, устраняют повышенное содержание синовиальной жидкости, но имеют много побочных эффектов, поэтому их стараются назначать короткими курсами. Препараты этой группы назначают также для того, чтобы подавить разрастание синовиальной оболочки сустава. Иногда ГКС вводят в суставную полость. При сильных болях и воспалении ГКС назначают в виде пульс-терапии: внутривенно большими дозами на протяжении не более трех дней.
При тяжелом течении ревматоидного артрита назначают плазмаферез – очищение крови от антител. С этой же целью назначают сорбенты, например, Энтеросгель, очищающий организм от токсинов.
Препараты базисной терапии подавляют аутоиммунный воспалительный процесс и пролиферацию (размножение) клеток соединительной ткани, оказывающих разрушающее действие на суставы. Базисные средства действуют медленно, поэтому их назначают длительными курсами и подбирают индивидуально. Эффективные, проверенные временем базисные препараты метотрексат, сульфасалазин и лефлуномид (Арава). Последний препарат относится к новому поколению и имеет меньше побочных эффектов.
В последнее время для лечения ревматоидного артрита стали применять биологические агенты – антитела, цитокины и другие активные вещества, играющие значительную роль в иммунных реакциях. Одним из таких препаратов является ритуксимаб (Мабтера, Реддитукс). Активным действующим веществом препарата являются антитела мыши и человека, которые подавляют иммунные реакции. Назначение этого препарата позволяет реже назначать курсы комплексной медикаментозной терапии.
Народные средства при ревматоидном артрите применяют в основном наружно. Вот некоторые из них:
- кору вяза высушить, растереть в порошок, развести водой, разложить на салфетке над пораженной поверхностью в виде компресса на всю ночь; хорошо лечатся воспаление и боль;
- спиртовые растирания с экстрактами растений (корня лопуха, хмеля, цветков одуванчика, чабреца); в стеклянную банку помещают измельченные растения, заливают водкой, настаивают в темном месте 10 дней и используют как растирание.
Физиотерапевтические процедуры помогают быстрее избавить больного от воспаления и боли. С этой целью назначают:
- электрофорез с диклофенаком;
- фонофорез с дексаметазоном;
- аппликации с димексидом.
Хондропротекторы что это как выбрать, насколько они эффективны
Читайте также:


