Поражение позвонков при лгм
Что важно знать о лимфоме
- Возрастной пик лимфомы: 30-70 лет
- 85% - симптомы неходжкинской лимфомы (более 80% — В-клеточные лимфомы)
- Первичное поражение костей (составляет 4% от первичных опухолей костей)
- Вторичное поражение (30% лимфом метастазируют в кости) при различных стадиях лимфомы Ходжкина.
Лимфома Ходжкина- что это за болезнь
- Лимфопролиферативное заболевание
- Вторичные поражения (кости и мозговые оболочки)
- Локализация в порядке увеличения частоты: кости, эпидуральное пространство, интрадурально и в костном мозге
- Картина поражения очень изменчива, дифференциальная диагностика и прогноз крупноклеточной лимфомы затруднены.
Какой метод диагностики эффективнее при лимфоме: МРТ, КТ, рентген, ПЭТ
- ПЭТ
- Рентгенография и КТ (кости) при лимфоме Беркитта и Т-лимфоме
- МРТ с контрастированием (поражение мозговых оболочек и костного мозга).
Внимание: в связи с большой изменчивостью данных методов визуализации лимфомы могут имитировать другие заболевания.
- Остеолиз
- Редко - остеосклероз (тело позвонка напоминает слоновую кость).
- Диффузная деструкция кости (остеолитическая и, реже, склеротическая)
- Обычно мелкоячеистая с инфильтрацией межпозвоночного пространства
- Мягкотканный компонент.
- Слабый сигнал на Т1-взвешенном изображении, усиленный сигнал на Т2- взвешенном изображении
- При динамической МРТ с контрастированием выявляется быстрое накопление контраста
- Мягкотканный компонент
- Гомогенное усиление сигнала после введения контраста.
- Повышенное накопление изотопа
- ПЭТ с ФДГ используется для определения стадии и наблюдения в ходе лечения.
- Солидное объемное образование, возможна инфильтрация кости
- Гомогенное усиление после введения контраста.
- На Т1-взвешенном изображении: дает сигнал меньшей или равной интенсивности, чем нормальные ткани.
- На Т2-взвешенном изображении: дает сигнал равной или большей интенсивности, чем нормальные ткани (опухоль и отек);
- На Т1-взвешенном изображении е контрастированием: выраженное накопление контраста.
- Утолщение нервных корешков.
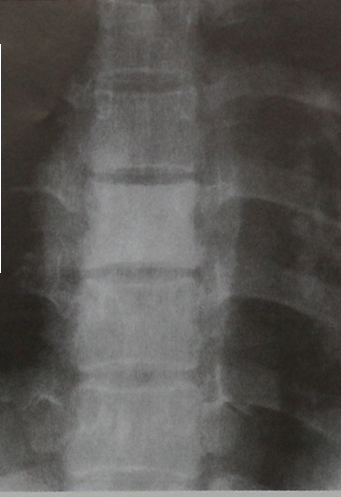
Рентгенограмма грудного отдела позвоночника, прямая проекция. Остеосклероз пораженного лимфомой позвонка Thy (тело позвонка напоминает слоновую кость). Расширена тень околопозвоночных мягких тканей.
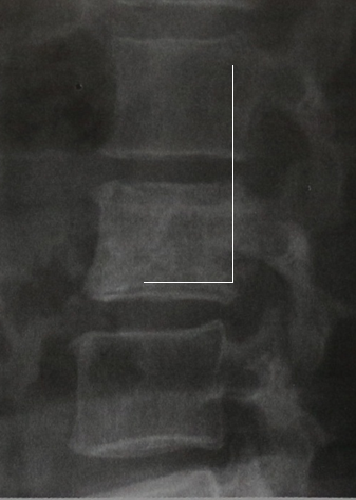
Рентгенограмма поясничного отдела позвоночника, боковая проекция. Остеосклероз пораженного лимфомой позвонка L| (тело позвонка напоминает слоновую кость). Остеосклероз имеет выраженную неоднородность. Определяются отдельные очаги остеолиза.
Клинические проявления
- Боль в спине без характерных особенностей.
Лечение лимфомы
- Обычно лечение лимфомы хорошо поддаются химио- и/или лучевой терапии
- При возникновении острой неврологической симптоматики при лимфоме 4 стадии показана хирургическая декомпрессия.
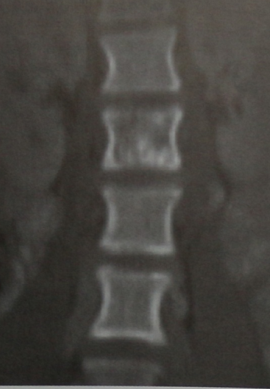
КТ пояснично-грудного отдела позвоночника (прямая проекция). Смешанная лимфома.
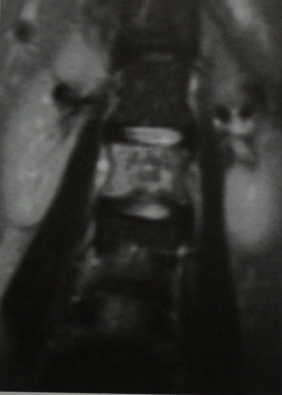
МРТ пояснично-грудного отдела позвоночника (фронтальная проекция, последовательность STIR). Лимфома позвонка дающая сигнал повышенной интенсивности.
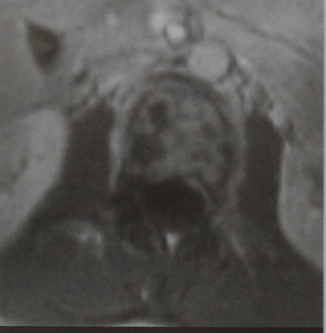
MPT позвонка ThXII (горизонтальная проекция, Т1-взвешенное изображение с контра¬стированием). Значительное накопление контраста в солидных участках лимфомы. Определяются остеолитические очаги (участки некроза). Тело позвонка окружено тонким ободком мягкотканной опухоли. С левой стороны опухоль распространяется на дугу позвонка.
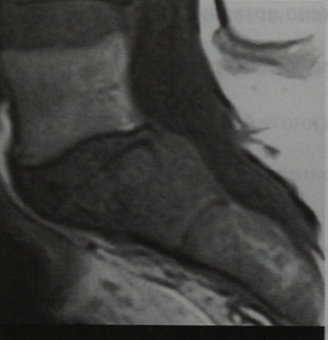
МРТ крестца (сагиттальная проекция, Т1-взвешенное изображение). Эпидуральное мягкотканное образование и деструкция компактного вещества.
С чем можно спутать поражение позвоночника при лимфоме
Кости
- Метастазы
- Болезнь Педжета (тело позвонка напоминает сло¬новую кость)
- Гистиоцитоз из клеток Лангерганса
Мозговые оболочки, костный мозг
- Гематома
- Метастазы
- Менингит
- Астроцитома
- Эпендимома
Лимфогранулематоз - злокачественная гиперплазия лимфоидной ткани, характерным признаком которой является образование гранулем с клетками Березовского-Штернберга. Для лимфогранулематоза специфично увеличение различных групп лимфатических узлов (чаще нижнечелюстных, надключичных, медиастинальных), увеличение селезенки, субфебрилитет, общая слабость, похудание. С целью верификации диагноза осуществляется биопсия лимфоузлов, диагностические операции (торакоскопия, лапароскопия), рентгенография грудной клетки, УЗИ, КТ, биопсия костного мозга. В лечебных целях при лимфогранулематозе проводится полихимиотерапия, облучение пораженных лимфоузлов, спленэктомия.


- Причины лимфогранулематоза
- Классификация лимфогранулематоза
- Симптомы лимфогранулематоза
- Диагностика лимфогранулематоза
- Лечение лимфогранулематоза
- Прогноз при лимфогранулематозе
- Цены на лечение
Общие сведения
Лимфогранулематоз (ЛГМ) – лимфопролиферативное заболевание, протекающее с образованием специфических полиморфно-клеточных гранулем в пораженных органах (лимфоузлах, селезенке и др.). По имени автора, впервые описавшего признаки заболевания и предложившего выделить его в самостоятельную форму, лимфогранулематоз также называют болезнью Ходжкина, или ходжкинской лимфомой. Средний показатель заболеваемости лимфогранулематозом составляет 2,2 случая на 100 тыс. населения. Среди заболевших преобладают молодые люди в возрасте 20-30 лет; второй пик заболеваемости приходится на возраст старше 60 лет. У мужчин болезнь Ходжкина развивается в 1,5-2 раза чаще, чем у женщин. В структуре гемобластозов лимфогранулематозу отводится втрое место по частоте возникновения после лейкемии.
Причины лимфогранулематоза
Этиология лимфогранулематоза до настоящего времени не выяснена. На сегодняшний день в числе основных рассматриваются вирусная, наследственная и иммунная теории генеза болезни Ходжкина, однако ни одна из них не может считаться исчерпывающей и общепризнанной. В пользу возможного вирусного происхождения лимфогранулематоза свидетельствует его частая корреляция с перенесенным инфекционным мононуклеозом и наличием антител к вирусу Эпштейна-Барр. По меньшей мере, в 20% исследуемых клеток Березовского-Штернберга обнаруживается генетический материал вируса Эпштейна-Барр, обладающего иммуносупрессивными свойствами. Также не исключается этиологическое влияние ретровирусов, в т. ч. ВИЧ.
На роль наследственных факторов указывает встречаемость семейной формы лимфогранулематоза и идентификация определенных генетических маркеров данной патологии. Согласно иммунологической теории, имеется вероятность трансплацентарного переноса материнских лимфоцитов в организм плода с последующим развитием иммунопатологической реакции. Не исключается этиологическое значение мутагенных факторов - токсических веществ, ионизирующего излучения, лекарственных препаратов и других в провоцировании лимфогранулематоза.
Предполагается, что развитие лимфогранулематоза становится возможным в условиях Т-клеточного иммунодефицита, о чем свидетельствует снижение всех звеньев клеточного иммунитета, нарушение соотношения Т-хелперов и Т-супрессоров. Главным морфологическим признаком злокачественной пролиферации при лимфогранулематозе (в отличие от неходжкинских лимфом и лимфолейкоза) служит присутствие в лимфатической ткани гигантских многоядерных клеток, получивших название клеток Березовского-Рид-Штернберга и их предстадий – одноядерных клеток Ходжкина. Кроме них опухолевый субстрат содержит поликлональные Т-лимфоциты, тканевые гистиоциты, плазматические клетки и эозинофилы. При лимфогранулематозе опухоль развивается уницентрически - из одного очага, чаще в шейных, надключичных, медиастинальных лимфатических узлах. Однако возможность последующего метастазирования обусловливает возникновение характерных изменений в легких, ЖКТ, почках, костном мозге.
Классификация лимфогранулематоза
В гематологии различают изолированную (локальную) форму лимфогранулематоза, при которой поражается одна группа лимфоузлов, и генерализованную – со злокачественной пролиферацией в селезенке, печени, желудке, легких, коже. По локализационному признаку выделяется периферическая, медиастинальная, легочная, абдоминальная, желудочно-кишечная, кожная, костная, нервная формы болезни Ходжкина.
В зависимости от скорости развития патологического процесса лимфогранулематоз может иметь острое течение (несколько месяцев от начальной до терминальной стадии) и хроническое течение (затяжное, многолетнее с чередованием циклов обострений и ремиссий).
На основании морфологического исследования опухоли и количественного соотношения различных клеточных элементов выделяют 4 гистологические формы лимфогранулематоза:
- лимфогистиоцитарную, или лимфоидное преобладание
- нодулярно-склеротическую, или нодулярный склероз
- смешанно-клеточную
- лимфоидное истощение
В основу клинической классификации лимфогранулематоза положен критерий распространенности опухолевого процесса; в соответствии с ним развитие болезни Ходжкина проходит 4 стадии:
I стадия (локальная) – поражена одна группа лимфоузлов (I) либо один экстралимфатический орган (IE).
II стадия (регионарная) - поражены две или более группы лимфатических узлов, расположенных с одной стороны диафрагмы (II) либо один экстралимфатический орган и его регионарные лимфоузлы (IIE).
III стадия (генерализованная) – пораженные лимфоузлы расположены с обеих сторон диафрагмы (III). Дополнительно может поражаться один экстралимфатический орган (IIIE), селезенка (IIIS) либо они вместе (IIIE + IIIS).
IV стадия (диссеминированная) – поражение затрагивает один или несколько экстралимфатических органов (легкие, плевру, костный мозг, печень, почки, ЖКТ и др.) с одновременным поражением лимфоузлов или без него.
Для обозначения наличия или отсутствия общих симптомов лимфогранулематоза на протяжении последних 6 месяцев (лихорадки, ночной потливости, похудания) к цифре, обозначающей стадию болезни, добавляются буквы А или В соответственно.
Симптомы лимфогранулематоза
К числу характерных для лимфогранулематоза симптомокомплексов относятся интоксикация, увеличение лимфатических узлов и возникновение экстранодальных очагов. Часто заболевание начинается с неспецифических симптомов – периодической лихорадки с температурными пиками до 39°С, ночной потливости, слабости, похудания, кожного зуда.
У 15-20% пациентов лимфогранулематоз дебютирует с увеличения лимфоузлов средостения. При поражении медиастинальных лимфоузлов первыми клиническими признаками болезни Ходжкина могут служить дисфагия, сухой кашель, одышка, синдром ВПВ. Если опухолевый процесс затрагивает забрюшинные и мезентериальные лимфоузлы, возникают абдоминальные боли, отеки нижних конечностей.
Лимфогранулематоз (ЛГМ, болезнь Ходжкина, лимфома Ходжкина) – заболевание лимфатической системы, особый тип лимфомы, то есть злокачественного заболевания, где опухолевая ткань возникает из лимфоцитов. Для ЛГМ характерно прежде всего опухолевое поражение лимфатических узлов с постепенным распространением заболевания от одной группы лимфоузлов к другой. Могут поражаться также другие органы, прежде всего селезенка, а также печень, легкие, кишечник, костный мозг и т.п.
Отличительной чертой ЛГМ по сравнению с другими лимфомами является присутствие в пораженных болезнью лимфоузлах особого типа клеток, называемых клетками Березовского-Штернберга-Рид. Это гигантские клетки, возникшие из B-лимфоцитов.
В зависимости от распространенности процесса различают четыре стадии ЛГМ.
- Стадия I – вовлечены лимфоузлы только одной области или один орган вне лимфоузлов.
- Стадия II – вовлечены лимфоузлы в двух или более областях с одной стороны диафрагмы или одна группа лимфоузлов и один орган также с одной стороны диафрагмы.
- Стадия III – вовлечены лимфоузлы с обеих сторон диафрагмы; возможно также поражение селезенки и других органов вне лимфоузлов.
- Стадия IV – наблюдается распространенное поражение одного или более внутренних органов – таких как печень, костный мозг, легкие, кишечник; оно может сопровождаться или не сопровождаться поражением лимфоузлов.
В обозначении стадии заболевания могут использоваться также дополнительные символы: А (системные клинические симптомы отсутствуют), В (присутствуют), E (вовлечены не только лимфоузлы, но и другие органы), S (вовлечена селезенка).
Различают несколько гистологических вариантов ЛГМ: с нодулярным склерозом (40-50% всех случаев ЛГМ), смешанноклеточный (около 30% всех случаев ЛГМ), с лимфоидным преобладанием и с истощением лимфоидной ткани (редкие варианты).
ЛГМ имеет два возрастных пика заболеваемости: один в молодом возрасте (15-35 лет), второй в пожилом. ЛГМ встречается в среднем с частотой около 1 случая на 25 тысяч населения в год, при этом дети и подростки составляют около 10-15% заболевших, а у детей дошкольного возраста болезнь встречается редко. Мужчины болеют несколько чаще женщин.
Факторы, влияющие на риск заболевания ЛГМ, постоянно изучаются. Могут играть роль как генетическая предрасположенность, так и некоторые вирусные инфекции. Так, считается, что риск развития ЛГМ повышен у людей, инфицированных вирусом Эпштейна-Барр (широко распространенным вирусом из группы герпетических вирусов). Риск развития ЛГМ увеличивается при иммунодефицитных состояниях, включая СПИД.
При ЛГМ наблюдается безболезненное увеличение лимфатических узлов – чаще всего шейных и надключичных, лимфоузлов грудной полости (области средостения), порой подмышечных, паховых и лимфоузлов брюшной полости. Это самый характерный симптом болезни. Взрослые больные иногда отмечают, что увеличенные лимфоузлы становятся болезненными после приема алкоголя.
По мере развития опухолевого процесса самочувствие больного ухудшается. На поздних стадиях развития болезни может наблюдаться желтуха, если опухоль распространилась в печень и перекрывает желчные протоки. Могут возникать отеки лица, шеи и рук (так называемый синдром сдавления верхней полой вены), отеки ног.
Чтобы отличить ЛГМ от других онкологических и неонкологических заболеваний, необходимо провести исследование опухоли – увеличенного лимфатического узла или очага в других тканях тела. Для этого производят его хирургическое удаление или биопсию с микроскопическим и иммуногистохимическим исследованием образца. Обнаружение клеток Березовского-Штернберга-Рид (крупных клеток особого вида, специфичных для ЛГМ) и их предшественников (клеток Ходжкина) является важным признаком ЛГМ; эти опухолевые клетки окружены другими клетками – лимфоцитами, эозинофилами и др.
Для обнаружения конкретных пораженных опухолью участков – лимфатических узлов и/или внутренних органов – используют различные методы визуализации: рентгенографию, ультразвуковое исследование (УЗИ), компьютерную томографию (КТ) и позитронно-эмиссионную томографию (ПЭТ). Именно ПЭТ считается самым эффективным тестом для определения стадии ЛГМ и оценки ответа на лечение. Возможны и другие исследования.
Производится костномозговая пункция и/или трепанобиопсия с последующим исследованием образца костного мозга, чтобы понять, поражен ли болезнью этот орган.
Лечение ЛГМ основано на сочетании химиотерапии и облучения. Выбор конкретной терапии зависит от варианта болезни, возраста пациента, стадии (локальное или распространенное поражение организма), сопутствующих заболеваний и других факторов.
В химиотерапии ЛГМ у детей и подростков в России успешно используют протоколы, предложенные немецкими онкогематологами. Эти протоколы позволяют получить высокий процент излечения с минимальными побочными эффектами, что очень важно при этой болезни. Также могут применяться курсы ABVD (адриабластин, блеомицин, винбластин, дакарбазин), BEACOPP (блеомицин, этопозид, адриамицин, циклофосфамид, винкристин, прокарбазин, преднизон) и другие химиотерапевтические курсы, количество которых определяют в зависимости от стадии болезни.
За химиотерапией следует лучевая терапия. Дозу облучения определяет врач-онкогематолог в зависимости от стадии заболевания, используемого протокола и облучаемого органа.
При оценке предпочтительности различных протоколов следует учитывать не только их эффективность в лечении основного заболевания, но также токсичность и повышение вероятности возникновения новых (вторичных) онкозаболеваний после терапии. Больные, излечившиеся от ЛГМ, и врачи, их наблюдающие, должны помнить о риске развития вторичных опухолей и о необходимости регулярных осмотров.
В сложных случаях (устойчивость болезни к терапии, рецидивы) может применяться высокодозная терапия с аутологичной трансплантацией костного мозга. Аллогенная трансплантация используется лишь в редких случаях.
ЛГМ относится к числу тех опухолевых заболеваний, которые наиболее эффективно излечиваются на современном уровне развития медицины. Среди молодых пациентов выздоравливают около 90% больных. У пожилых пациентов выживаемость хуже, но в среднем прогноз все равно достаточно хороший. Даже в случае рецидива можно излечивать около половины пациентов.
Прогноз, разумеется, зависит также от стадии заболевания: среди пациентов, у которых болезнь была диагностирована на стадиях I-II, доля излечивающихся превышает 90%, тогда как при обнаружении ЛГМ на стадии IV эта доля снижается до 65-70%.
После пятилетней ремиссии болезнь, как правило, считается излеченной. Однако и после излечения от ЛГМ необходима пожизненная онкологическая настороженность, так как вторичные опухоли иногда развиваются даже через 10-20 лет после окончания лечения. Могут возникнуть и другие отдаленные последствия – например, кардиомиопатия (поражение миокарда) как следствие химиотерапии. Благодаря разработке новых протоколов вероятность побочных эффектов уменьшается, однако полностью исключить их нельзя.
Первичные опухоли возникают в позвоночнике, чаще всего в молодом возрасте (1 - 3 декаде жизни). Они растут либо из кости, либо из фиброзных тканей, мышц, нервов и сосудов, окружающих позвонок. Первичные опухоли позвоночника довольно редки и растут, как правило, медленно. Первичными новообразованиями позвоночника [по гистологической структуре] являются: остеохондрома, эозинофильная гранулема (или Х-гистиоциоз), гемангиома, аневризмальная костная киста, остеоид-остеома, остеобластома, гигантоклеточная опухоль, остеогенная саркома (остеосаркома; наиболее распространенная злокачественная опухоль костей̆), хондросаркома, саркома Юинга, хордома (наиболее часто встречающаяся злокачественная опухоль позвоночника, причем в отличие от других опухолей локализуется только в позвоночнике). Первичные опухоли встречаются лишь в 5 % случаев в отличие от метастатических новообразований в позвоночнике.

Метастатические опухоли являются одной из наиболее распространенных форм опухолей скелета вообще и позвоночника в частности (неуклонный рост которых обусловлен увеличением продолжительности жизни и, соответственно, увеличением доли пожилого населения в популяции). Позвоночник при этом занимает второе место после головного мозга по локализации метастатического поражения центральной нервной системы. Группа риска – пациенты в возрасте 40 – 65 лет (средний возраст пациентов – около 60 лет), мужчины страдают чаще женщин. По данным аутопсии опухоли, метастазирующие в позвоночник, можно распределить в следующем порядке: миелома, рак молочной железы и легкого, рак предстательной железы и желудка, лимфома, меланома, злокачественные новообразования мочевого пузыря и почек, щитовидной и поджелудочной желез и некоторых других органов. Излюбленным местом локализации метастазов является грудной отдел позвоночника - до 68% случаев (отмечается определенная зависимость между исходным ростом первичной опухоли и локализацией метастазов в позвонки; так, опухоли желудочно-кишечного тракта чаще метастазируют в пояснично-крестцовый отдел, а опухоли молочной железы – в грудной отдел позвоночника). У женщин наиболее часто метастазирует в кости рак молочной̆ железы и рак легких, у мужчин – рак предстательной̆ железы и рак легких. По данным AAOS (Americal Academy of Orthopedic Surgeons), метастатическое поражение позвоночника встречается примерно у 20% пациентов с онкологическими заболеваниями, причем [ . ] от 5 до 10 % таких поражений сопровождаются компрессией спинного мозга.

Общее состояние больного на стадии появления первых клинических признаков опухолевого (неопластического) поражения позвоночника, как правило, не меняется. При доброкачественных опухолях оно не изменяется вообще (исключая остеоид-остеому). Даже появление метастазов в позвоночнике на начальной стадии не меняет общей соматический статус пациента. В то же время, хороший внешний вид пациента не исключает наличия у него злокачественного новообразования, так как кахексия развивается только в терминальной стадии процесса.
Наиболее частым симптомом при опухолях позвоночника является боль (в т.ч. нелокализованная) [в области спины и/или в конечности] - ведущий клинический признак (симптом). Длительность и выраженность боли во многом зависит от агрессивности опухоли. В отличие от боли при других патологиях позвоночника, боль при новообразованиях (боль биологического характера) особенно проявляется в ночное время (или, при ее невыраженной степени в начальных стадиях, проявляется в вечернее и утреннее время), регрессирует на фоне кортикостероидной и лучевой терапии (не купируется стандартными НПВС). Объяснение ночных болей, возможно, заключается в напряжении надкостницы в силу отека стромы опухоли. Боли также могут быть обусловлены нестабильностью (боль механического характера) - ассоциированы с движением и проявляются в зоне, которая соответствует пораженному сегменту позвоночного столба. В группе пациентов с доброкачественными опухолями характерны внезапное появление болей на фоне увеличения физической нагрузки и прогрессивно рецидивирующий тип течения заболевания (медленно растущие доброкачественные опухоли характеризуются нарастанием болевого синдрома от нескольких месяцев до нескольких лет). При этом на начальных стадиях процесса значительная часть больных отмечает длительные ремиссии (до нескольких месяцев), боли нередко проходили самостоятельно, и пациенты не спешили обращаться к врачам. Острые боли являются следствием патологического перелома позвонка, среди пациентов со злокачественными опухолями, и напрямую зависят от степени нагрузки на позвоночник, носят постоянный характер, нарастают по мере прогрессирования заболевания. Внезапное усиление боли часто свидетельствует о патологическом переломе.

Обратите внимание! Остеопорозные переломы встречаются в 2 раза чаще опухолевых переломов. Остеонекроз при опухолевых переломах встречается чаще, что может быть связано с особенностями лечения. Для переломов на фоне опухолевого поражения наиболее характерна III степень снижения высоты тела (снижение высоты более 40%), в то время как вид деформации не несет существенного диагностического значения (Неред А.С. и соавт., 2013).

Обратите внимание! Опухолевый процесс костно-суставного аппарата характеризуется следующей классической клинической картиной-триадой симптомов: [ 1 ] боль, [ 2 ] увеличение объема (наличие опухоли), [ 3 ] нарушение функции. Однако вследствие анатомических особенностей позвоночного столба клинически увеличение объема можно отмечать только при локализации опухоли в остистом отростке при выраженном процессе. А нарушение функции вообще нередко свидетельствует о его декомпенсации. Мало того, данная симптоматика [ . ] характерна не только для злокачественного опухолевого процесса. Она может иметь место и при доброкачественных новообразованиях и опухолеподобных заболеваниях (аневризмальная костная киста, остеоид-остеома, солитарная костная киста), а также при псевдоопухолевых процессах и при целом ряде неопухолевых заболеваний опорно-двигательного аппарата. По-видимому, этим можно объяснить большое число диагностических ошибок при первичном врачебном осмотре.
Другим частым симптомом опухолевого процесса позвоночника является неврологическая симптоматика, которая обусловлена сдавлением корешковых (и спинальных) нервов, корешков или спинного мозга вследствие распространения опухоли или ретропульсии кости из-за патологического перелома (частота развития изолированной боли в спине, как основной жалобы при поступлении пациентов, равна частоте возникновения боли в сочетании с проводниковыми нарушениями: парезами, расстройствами чувствительности и функции тазовых органов различной выраженности). В зависимости от локализации и размеров опухоли неврологическая симптоматика может быть представлена симптомами ирритации и выпадения (дефицита - чувствительного, двигательного и др.). В некоторых случаях пациенты не ощущают неврологической дисфункции, однако в момент осмотра необходимо неврологическое обследование. Неврологические изменения при первичном осмотре выявляются [примерно] у 1\2 больных со злокачественными опухолями и [примерно] у 1/3 - с доброкачественными (при этом однако не все пациенты предъявляют жалобы).
В основе стандартизованной оценки неврологических нарушений у больного с опухолевым процессом в позвоночнике лежит анализ выраженности эпидуральной компрессии спинного мозга (ESCC - Epidural Spinal Cord Compression), и его структур. Для объективизации этого показателя группой по изучению опухолей позвоночника (Spine Oncology Study Group – SOSG) принята система классифицирования ([ . ] определяющая тактику лечения), базирующаяся на анализе аксиальных T2-взвешенных МРТ-изображений в месте наиболее грубой компрессии:



Запомните! С целью верификации диагноза и выявления повреждения спинного мозга необходимо ([ . ] первостепенная задача врача) назначение [рентгеновской] компьютерной томографии (КТ) и магнитно-резонансной томографии (МРТ) позвоночника при появлении первых подозрительных симптомов. В качестве первичного исследования рекомендуется выполнение КТ вовлеченного отдела позвоночника, которое позволяет оценить степень разрушения кортикального слоя и кальцификацию опухоли (стандарт). Значимую информацию представляет также МРТ позвоночника (стандарт), позволяющее выявить: [ 1 ] наличие мягкотканого компонента в костной структуре; [ 2 ] изменения в окружающих параспинальных тканях; [ 3 ] компрессию нервных структур; [ 4 ] инфильтрацию губчатого вещества позвонков; [ 5 ] эпидуральный компонент. Традиционное выполнение рентгеновского исследования (опция) при первичном обращении пациентов, имеющих боли в позвоночнике в случае первичного новообразования позвоночника, [ . ] не является диагностически значимым, так опухоль не имеет патогномоничных флюроскопических симптомов. Самым важным методом диагностики онкологического процесса является гистология. Ведь без понимания гистологического характера опухоли невозможно назначить адекватное лечение (химио-терапия, лучевая терапия или операция).

Обратите внимание! Опухоли позвоночника, особенно на начальной стадии заболевания, не обладают какими-либо особенными, свойственными только им симптомами. Даже при возникновении патологических переломов позвонков, часто осложняющих опухолевый процесс, могут отсутствовать специфические клинические и рентгенологические признаки. Это приводит к диагностическим ошибкам у трети больных и задержке правильной диагностики на срок до двух лет. Нередко лечение начинается тогда, когда больного уже парализовало.
Другие симптомы возникают значительно реже, но могут играть важную роль при планировании лечения. Так, по данным ряда авторов, сколиотическая деформация встречается почти у 70% больных с остеоидостеомой и остебластомой. Полный анамнез не должен ограничиваться обследованием по звоночника и включать данные о наличии общих симптомов (слабость, температура, потеря веса и т.д.), историю заболевания, семейный анамнез. Обследование должно включать неврологическое исследование, которое позволит выявить уровень поражения позвоночника. Нельзя забывать, что некоторые заболевания могут носить мультифокальный характер. Как правило, многоуровневое поражение встречается при метастатическом процессе, миеломной болезни. Однако описаны случаи мультифокальной гигантоклеточной опухоли; для злокачественных опухолей (саркома Юинга, остеосаркома) более характерны skip метастазы (skip-MTS) и/или отдаленные [прыгающие, отстоящие] метастазы (W.F. Enneking впервые предложил определять метастазы в кость, уже пораженную первичной опухолью, как skip-MTS, которыепредставляют собой опухолевые очаги, располагающиеся в пределах той же самой кости, но не имеющие непосредственной связи с первичной опухолью; как правило, они небольших размеров, с относительно четкими контурами и выявляются в губчатом веществе кости проксимальнее основного очага; частота обнаружения skip-MTS составляет менее 1%). Многоочаговое поражение также может наблюдаться при доброкачественных опухолях (остеохондромы, нейрофибромы, эозинофильные гранулемы, фиброзные дисплазии).

Все решения, касающиеся выбора метода лечения пациента, основываются на его способности перенести соответствующую процедуру, что, в частности, зависит от [1] распространенности опухолевого процесса, [2] его гистологического типа, а также [3] сопутствующей соматической патологии. Так как продолжительность жизни пациента напрямую связана с гистологическим типом опухоли, [ . ] выбор оптимального объема операции рекомендовано проводить совместно с врачом-онкологом. Немелкоклеточный рак легкого, рак толстой кишки и карциномы неизвестной первичной локализации имеют показатели выживаемости в среднем около 4 месяцев с момента операции, таким пациентам не рекомендуется проводить агрессивных вмешательств, которые могут потребовать длительного восстановления. Если сопутствующая соматическая (коморбидная) патология исключает возможность хирургического вмешательства, радиационные и медицинские терапевтические средства рекомендуется использовать даже на поздних стадиях онкологического процесса.
Читайте также:


