Операция по стентированию позвоночной артерии
Используйте навигацию по текущей странице
- О методе
- Заболевания
- Стоимость
- Врачи
- Вопросы/ответы
- Советы и статьи
- Видеосюжеты

Кратко о методе лечения
Эндоваскулярная операция при сужении позвоночной артерии, позволяющая восстановить проходимость сосуда и предупредить развитие инсульта в вертебро-базилярном бассейне.
Каротидные и позвоночные артерии проходят через шею, поставляя кровь в мозг. Вертебральные (позвоночные) артерии расположены в области шеи и в основном содержатся в костных каналах шейного отдела позвоночника.
Процедура стентирования позвоночных артерий является минимально-инвазивным методом, который обеспечивает альтернативу хирургии.
При стентировании саморасширяющаяся сетчатая трубка помещается в артерию в месте сужения. При размещении в сосуде внешняя сила стента уменьшает или полностью устраняет сужение в сосуде. Этот метод может быть применен к сужению сосуда как в области шеи, так и внутри черепа.
Стент — трубчатая металлическая сетка, задача которой, поддерживать проходимость сосудов. Активно их стали применять с 90-х годов.
В зависимости от того, из чего стенты изготовлены, они бывают двух видов: расправляемые баллоном и саморасправлящиеся.
Расправляемые представляют собой сетку, изготовливаются из нержавеющей стали или других металлических сплавов (кобальт и хром), которые противостоят ржавчине. Современные сетки имеют сложную конструкцию и могут адаптироваться под форму кровеносного сосуда и распределяются внутри него равномерно и точно.
Саморасправляющиеся стенты изготавливаются из тонкой проволоки, сделанной из стали или нитинола (сплав никеля и титана), и отличаются тем, что имеют память формы. Их реже применяют для стентирования позвоночной артерии, так как при имплантации они укорачиваются до 20% и не могут удерживаться прочно в определенной позиции.
Каротидные и позвоночные стенты остаются на месте и не обнаруживаются металлоискателями.
Стентирование каротидной и вертебральной артерии гораздо менее инвазивно, чем операция. Пациенты обычно имеют более короткое время восстановления.
Для позвоночных и подключичных артерий лечение только ангиопластикой или ангиопластикой со стентированием может быть подходящей терапией первой линии.
Показания и противопоказания
Показания к стентированию:
Артерии могут сужаться (стенозироваться) или полностью блокироваться при атеросклерозе. Атеросклероз — это заболевание, при котором жировые отложения, называемые бляшками, собираются внутри кровеносных сосудов. По мере развития атеросклероза происходит постепенное сужение сосуда и снижение притока крови к мозгу. Это может привести к инсульту или временным ишемическим атакам. Путем восстановления или усиления кровотока через суженные артерии риск потенциально опасного для жизни удара может быть уменьшен или предотвращен.
Псевдоаневризма: образует вторичную травму стенки сосуда, что приводит к периартериальной гематоме.
Артериовенозные свищи, связанные с позвоночными артериями, редкое явление. Подобно псевдоаневризмам, эти поражения чаще всего встречаются вторично с тупой или проникающей травмой шеи.
Ятрогенные поражения вызваны артериальной пункцией с сопутствующим повреждением соседней вены.
Симптомы вертебробазилярной недостаточности.
Патологическая извитость артерии.
Противопоказания
Хотя стентирование может быть лучшим вариантом, чем операция для многих пациентов, однако подходит не всем. Процедуру не проводят если диаметр артерии менее 3мм; у пациента тяжелая почечная и дыхательная недостаточность; у пациента заболевания сосудов, непозволяющие проводить эндоваскулярное вмешательство; при сильной извитости артерии; недавний инсульт или внутричерепное кровоизлияние.
Малоинвазивные операции не так давно внедрились в медицинскую практику. И одним из таких хирургических вмешательств стало стентирование сосудов. Для его проведения не требуется больших разрезов, общей анестезии, длительного периода реабилитации. Операция в среднем занимает до 40–60 минут, чаще всего осуществляется в процессе рентгеноконтрастного исследования сосудистого просвета, прооперированный больной может покинуть клинику уже через несколько дней.
Стентирование — что это такое
Суть вмешательства сводится к внедрению в просвет суженного сосуда специального каркаса (стента), который уже не дает ему менять свои размеры. Стенты изготавливаются из специального металла или пластика, не притягивающего факторы свертывания крови, и неспособного осложняться тромбозом. Это такой себе цилиндр с цельной, сетчатой, или стенкой из колечек. Он расправляется с помощью раздуваемого баллончика, на котором, собственно, и подводится к месту сужения. Но существуют и саморасправляющиеся стенты.

Кроме того, разработаны имплантаты с медикаментозным напылением. В качестве лекарства используются антиагреганты и иммунодепрессанты. Они еще сильнее снижают риск тромбообразования на внутренней поверхности стента и угнетают иммунный ответ на инородное тело. Но самым последним новшеством стали биодеградируемые каркасы, начинающие через полгода после установки постепенно растворяться. Тем не менее специалисты из Швейцарии, вплотную изучающие отдаленные результаты стентирования разными материалами, лучшими на сегодняшний день признали внутрисосудистые стенты с лекарственным покрытием.

Стентирование артерий является достаточно простой манипуляцией для подготовленных ангиохирургов. Все они выполняют один и тот же алгоритм действий.
- Сначала выбирается периферический сосуд, через который будет заводиться стент. Обычно это – бедренная, плечевая или лучевая артерия.
- Место в ее проекции обрабатывается антисептиком. Осуществляется инъекция местного анестетика, на который была предварительно проведена аллергологическая проба.
- Затем сосуд пунктируется, в него устанавливается катетер, в который вводится проводник с баллончиком.
- Перед ним впрыскивается антиагрегант, обычно – Гепарин. Затем – контрастное вещество. Оба препарата подхватываются кровью и опережают баллончик, разжижая кровь и заполняя просвет артерии, который становится виден при рентгеноскопии.
- Баллончик под контролем рентгенаппарата подводится к суженому участку, из него выходит временный фильтр для улавливания случайно оторвавшихся элементов атеросклеротической бляшки и тромбов. Затем баллончик раздувается, сдавливая атеросклеротические бляшки и расширяя просвет артерии.
- После дилятации сосуда баллончик сдувается, и проводник с ним и временным фильтром извлекаются.
- Затем к механически расширенному сосудистому отрезку подводится второй проводник с фиксированным на баллончике стентом.
- Баллончик медленно раздувается, расправляя металлический каркас, придавливая бляшку к сосудистой стенке, и расширяя просвет. Каркас фиксирует атероматозные массы, предотвращая их попадание в общий кровоток.
- После фиксации имплантата для окончательного его укрепления на месте баллончик несколько раз сдувается-раздувается и извлекается из сосудистого русла.
- Удаляется и катетер.
- Место оперативного вмешательства обрабатывается антисептиком, на рану накладывается давящая повязка. Иногда может потребоваться наложение одного узлового шва.
Имплантат остается в организме человека навсегда, его форма не меняется, он пожизненно способствует нормальному кровоснабжению соответствующих тканей. Постепенно внутренняя поверхность стента покрывается размножающимися клетками сосудистой выстилки, и иммунная система не распознает чужеродное тело. В артерии, склонные к чрезмерному разрастанию внутренней оболочки, а, следовательно, — к повторному возникновению атеросклеротической бляшки, вводится имплантат с соответствующим лекарственным покрытием. Оно предотвращает рост и новое образование эндотелия. Без использования таких каркасов нового поколения в 20% случаев происходил бы рецидив, и просвет артерии снова бы сужался.

Количество стентов, их размер и вид определяет ангиохирург в зависимости от конкретной ситуации:
- числа пораженных сосудов, нуждающихся в стентировании;
- длины стенозированного участка;
- степени сужения артериального просвета;
- способности внутренней оболочки к гиперплазии.
Состояние после стентирования нашло свое место в Международной классификации болезней и имеет собственный код по МКБ 10 пересмотра – Z 95.5. Это свидетельствует о том, что оно играет важную роль в медицине, предотвращая смертельные осложнения атеросклероза, и увеличивая продолжительность жизни прооперированным пациентам. Благодаря чрескожному коронарному вмешательству (ЧКВ), стентированию прецеребральных, почечных артерий, сосудов нижних конечностей, аорты процент смертности от инфаркта миокарда, инсульта, гангрены и разрыва аневризмы значительно снизился.
Бывают случаи, когда стентирование проводить необязательно и пациентам показана только баллонная ангиопластика. Это похожий метод оперативного вмешательства, при котором сосудистый просвет увеличивают раздуванием баллончика без последующей имплантации стента. Но в этой ситуации без выполнения пациентом предписаний врача возникает риск рецидива. Тогда врачи повторно делают ангиопластику, или, если нет противопоказаний, назначают стентирование.
Установка еще одного каркаса в месте уже существующего невозможна: имплантат призван выполнять свои функции на протяжении всей жизни. Повторное стентирование показано при прогрессировании атеросклероза в других участках сосудистого русла, в т. ч. находящихся далеко от места первого оперативного вмешательства. При запущенных изменениях сосудистой стенки и невозможности имплантации каркаса выполняют более травматическую операцию – шунтирование.
Показания для проведения стентирования
Главным показанием к стентированию является атеросклеротическое сужение того или иного участка артериальной магистрали более чем на 60%. Реже операция назначается при аневризматическом расширении сосуда, гиперплазии его мышечной оболочки или облитерирующем эндартериите. Установку стента врачи рекомендуют и при невозможности проведения открытой ангиопластики или эндартерэктомии, противопоказаниях у больного к общей анестезии.
Перед операцией обязательно назначают дополнительные исследования, главное из которых – ангиография (коронарография, аортография и т. д.). Именно этот метод позволяет объективно оценить степень изменения сосудистого просвета и выбрать наиболее адекватную тактику. Не обходится и без стандартных предоперационных анализов, функциональной диагностики, консультаций кардиолога, сосудолога, анестезиолога.
Предоперационная подготовка включает прием антиагрегантов в течение нескольких дней и запрет на прием пищи вечером накануне и утром непосредственно перед вмешательством. При правильной подготовке осложнения после стентирования развиваются редко. Ранними осложнениями могут стать аллергические реакции на вводимые препараты, в том числе и на рентгеноконтрастное вещество. Во время прокола периферического сосуда возможна его сквозная перфорация с последующим образованием местной гематомы.
Не исключены и осложнения, непосредственно связанные с наличием в просвете сосуда самого стента. Так, С-реактивный белок и лимфоциты крови могут быть повышены пару месяцев после операции с применением имплантата, содержащего иммунодепрессант. А вот пониженное артериальное давление может носить стойкий характер. В позднем послеоперационном периоде иногда возможно наслоение тромботических масс на внутренних стенках стента, что снижает его проходимость. Крайне редко, при непрочной установке, возможно смещение сосудистого каркаса по направлению тока крови.
Противопоказания
Каким бы удачным ни был малоинвазивный метод восстановления кровотока в суженых сосудах, у него есть свои противопоказания:
- диаметр просвета менее 0,3 см;
- большая длина стенозированного участка;
- субкомпенсированная и декомпенсированная легочная недостаточность;
- тяжелая аритмия;
- выраженная почечная недостаточность;
- нарушение свертываемости крови.
Виды стентирования по локализации
Атеросклероз носит генерализованный характер, он поражает все сосуды эластического и мышечно-эластического типа (простыми словами – аорты и крупных артерий). Но никто не будет ставить стенты во все суженые участки. Врачи спасают ткани, которые страдает больше всех, и гибель которых может угрожать жизни пациента. У одних больных на первый план выступает далеко зашедшее кислородное голодание вещества головного мозга, у других – сердечной мышцы, у третьих – почек, у четвертых – мягких тканей конечносте. Поэтому стентирование классифицируется по локализации установки стентов.
После перенесенного острого нарушения мозгового кровообращения эта малоинвазивная операция противопоказана в течение 2 месяцев. По истечению 8–10 недель врачи тщательно выбирают метод восстановления кровотока в ишемизированных участках головного мозга. И стентирование сонной или позвоночной артерии не всегда в приоритете, особенно при их кальцинозе или значительной извитости сосудов. В группе риска оказываются и пациенты в пожилом и старческом возрасте, гипертоники, аллергики.

При восстановлении проходимости прецеребральных артерий кровоснабжение головного мозга значительно улучшается, и пациент может почувствовать временное тепло в области головы. Такое часто встречается в практике анестезиолога, поэтому перед вмешательством он предупреждает больного о возможных ощущениях. Но, исходя из отзывов пациентов, чувство тепла длится недолго и не приносит особого дискомфорта.
Цена стентирования в первую очередь зависит от типа стента, степени поражения сосуда, тяжести сопутствующей патологии, требующей дополнительных процедур и манипуляций. Зависит стоимость и от вида применяемой ангиографии, контролирующей ход операции.
Показаниями к реконструкции просвета коронарных артерий являются:
- прединфарктные состояния в виде нестабильной или тяжелой стабильной стенокардии;
- непосредственно острый инфаркт миокарда;
- приступы ишемических атак после перенесенного инфаркта.
Стенты устанавливают как в крупных сосудах, так и в их ветвях, а также в ранее подведенных шунтах. Причем в последнем случае часто бывает показано одномоментное множественное стентирование, например, 1 стент заводят в правую коронарную артерию (ПКА), 2–й – в шунт, подведенный к правой межжелудочковой артерии (ПМЖА), 3–й – в шунт, подведенный к ветви тупого края (ВТК). Такие операции длятся намного дольше обычных, и требуют особого мастерства от кардиохирурга.
Показанием к стентированию сосудов ног является облитерирующий атеросклероз, приводящий к перемежающей хромоте, критической ишемии или гангрене мягких тканей. Устанавливая стент и возобновляя адекватное кровоснабжение врачи спасают пациентов от ампутации конечности. Иногда катетеризацию для введения стента приходится осуществлять на здоровой ноге. Проводник заводится к месту бифуркации аорты, а затем подводится против тока крови к пораженному участку сосуда больной ноги.

Каким бы ни казалось абсурдным, но вмешательство через локтевой доступ предпочтительнее, так как осложнения после него встречаются намного реже, чем при бедренном. При этом продолжительность операции увеличивается, а риск возникновения послеоперационных кровотечений снижается в разы. Зато доступ через бедренную артерию удобнее и сокращает время операции.
Стентирование грудной или брюшной аорты проводят не только при ее атеросклеротическом сужении, но и при расширении (аневризме). В последнем случае восстанавливается нормальный кровоток без завихрений и расслоения оболочек главной артерии, что предотвращает внезапный разрыв сосуда при скачке артериального давления.
Стентирование аорты подразумевает более тщательную предоперационную подготовку. Связано это с тем, что хирурги должны быть готовы к немедленному расширению операции и переходу на открытое вмешательство в связи с техническими сложностями или развитием внутриоперационных осложнений.
Стентирование внутричерепных сосудов головного мозга – пока что редкая операция, так как ее эффективность еще не имеет доказательной базы, хотя положительные результаты уже зафиксированы. Вмешательство имеет много трудностей: для контроля установки стенка необходимо облучать голову, сосуды мозга достаточно извиты, механические воздействия при продвижении имплантата могут навредить ЦНС.
Послеоперационный период длится до 4–5 суток, и основная цель врачей на этом этапе – предотвратить воспалительный процесс и тромбирование инородного тела в артерии. Поэтому назначается соответствующая терапия. А на будущее пациентам рекомендуют поменять образ жизни, следить за холестерином, принимать статины, повысить физическую активность. Только с такими условиями повторная операция им не грозит.
ЭНДОВАСКУЛЯРНОЕ ЛЕЧЕНИЕ (СТЕНТИРОВАНИЕ) СТЕНОЗИРУЮЩЕЙ ПАТОЛОГИИ БРАХИОЦЕФАЛЬНЫХ АРТЕРИЙ
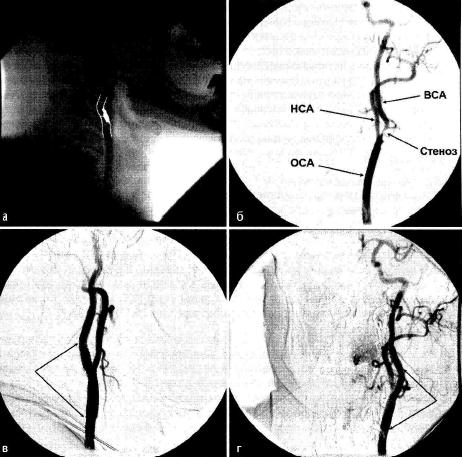
В последние годы в хирургическом лечении стенозирующей патологии брахиоцефальных артерий наряду с широко распространённой каротидной эндартерэктомией всё большее распространение получает эндоваскулярный метод - ангиопластика и стентирование. Эта операция, как и каротидная эндартерэктомия, направлена на восстановление просвета сосуда и адекватного кровотока по нему (рис. 19-8).
Эндоваскулярное лечение стенозирующей патологии брахиоцефальных артерий (ангиопластика и стентирование) имеет следующие преимущества перед каротидной эндартерэктомией:
- отсутствие необходимости проводить операцию под общей анестезией, что позволяет оценивать неврологический статус больного в течение всей операции;
- более короткий восстановительный период после операции;
- отсутствие хирургической раны на шее, что исключает риск поражения ЧН, инфицирования раны, образования гематомы на шее;
- возможность одновременных вмешательств на сонной, позвоночной, подключичной артериях;
Рис. 19-8. Ангиограммы в боковой (цифровая обработка) и прямой проекциях: а, б - критический стеноз левой внутренней сонной артерии атеросклеротической бляшкой (>80%); в, г - восстановление просвета сосуда после стентирования (стрелками указаны границы стента) .
- более низкую смертность и вероятность осложнений у пациентов:
- с высоким хирургическим риском (стенокардия напряжения III-IV функционального класса и/или фракция выброса левого желудочка менее 30%, нестабильная стенокардия, острый инфаркт миокарда в анамнезе, хронические обструктивные заболевания лёгких, почечная недостаточность, окклюзия контралатеральной внутренней сонной артерии);
- параличом контралатерального гортанного нерва;
- рестенозами после каротидной эндартерэктомии;
- двусторонними стенозами высокой степени;
- • возможность оперировать больных со стенозами в труднодоступных или недоступных для прямой хирургии зонах (сегменты C1-Cz внутренней сонной артерии, проксимальные отделы общей сонной артерии, стенозы подключичных и позвоночных артерий).
Показаниями к стентированию брахиоцефальных артерий считают симптоматические стенозы более 50% и бессимптомные стенозы более 75%.
Противопоказания к про ведению ангиопластики и стентирования таковы:
- тотальная окклюзия сосуда (применительно к внутренней сонной артерии);
- сосудистые заболевания, препятствующие использованию эндоваскулярных инструментов:
- выраженный атероматоз дуги аорты;
- выраженная извитость и петлеобразование сосудов;
- наличие внутрипросветного тромба в области стеноза (для сонных артерий);
- острый период ишемического инсульта или завершённый инсульт с выраженным неврологическим дефектом;
- внутричерепное кровоизлияние в сроки до 1 мес.
ПРЕДОПЕРАЦИОННАЯ ПОДГОТОВКА
Перед операцией необходимо использовать неинвазивные методы обследования, позволяющие определять степень стеноза: цветное дуплексное сканирование брахиоцефальных артерий, спиральную КТ в ангиографическом режиме. При этом важно иметь данные о состоянии всех экстракраниальных сосудов (ветвей дуги аорты) и виллизиева круга. Помимо этого необходимо проводить тщательный неврологический осмотр, а также КТ - и/или МРТ -исследование головного мозга, чтобы оценить динамику изменений после операции. У больных с тяжёлыми сопутствующими заболеваниями необходимо дополнительно обследовать органы и системы (ЭКГ, ЭхоКГ, консультация терапевта и пр.). За 2-3 дня до операции пациентам назначают антиагреганты (клопидогрел по 75 мг в день).
МЕТОДИКА ПРОВЕДЕНИЯ
Операцию осуществляют под местной анестезией с внутривенной седацией. Это позволяет проводить мониторинг неврологического статуса на протяжении всей операции. Для контроля за динамикой линейной скорости кровотока по средней мозговой артерии, а также прохождения микроэмболов необходимо проводить операцию под допплерографическим мониторингом. Окончательное суждение о степени стеноза можно вынести после получения ангиографических данных.
В большинстве случаев используют трансфеморальный доступ, и только при наличии причин, препятствующих этому доступу, можно использовать иной (через лучевую или подмышечную артерии) . Непосредственно после пункции артерии внутривенно вводят 5000 ЕД гепарина (далее каждые 40-60 мин под контролем активированного времени свёртывания гепарин вводят повторно). При тотальной селективной ангиографии ветвей дуги аорты можно выявить мультифокальные поражения брахиоцефальных артерий и наметить (или изменить) тактику лечения.
Для того чтобы оценить состояние коллатералъного кровообращения мозга, необходима визуализация как экстра- так и интракраниальных отделов брахиоцефальных артерий.
Стентирование сонных артерий
Сонные артерии стентируют, применяя устройства защиты мозга от эмболии (фильтры-ловушки) . Операцию в этих случаях начинают с установки фильтра. Его проводят через зону стеноза и раскрывают в дистальном сегменте артерии.
Это один из опасных в плане эмболии этапов операции. Если степень стеноза не позволяет беспрепятственно провести фильтр-ловушку через зону стеноза, целесообразно использовать проксимальнеe устройства защиты мозга от эмболии (баллоны-катетеры) . При этом все манипуляции на артерии проводят при её предварительной окклюзии баллоном-катетером в проксимальных отделах. Отсутствие кровотока в сосуде предотвращает попадание эмболов в мозговые сосуды. Однако эти устройства неприменимы у больных с разобщённым виллизиевым кругом и/или истощёнными резервами коллатерального кровообращения.
В некоторых случаях возникает необходимость в про ведении предварительной дилатации артерии (раздувание баллона на уровне стеноза перед имплантацией стента). Она показана при выраженном сужении сосуда, когда проведение системы доставки стента не представляется возможным. При раздувании баллона в области бифуркации общей сонной артерии за счёт раздражения барорецепторов синокаротидной зоны нередко развиваются выраженная брадикардия (вплоть до асистолии) и артериальная гипотензия. Для профилактики этих нежелательных реакций перед проведением предварительной и последующей дилатации вводят 0,3-0,5 мл раствора атропина внутривенно.
Следующий этап - доставка и имплантация стента. В настоящее время для стентирования сонных артерий используют нитиноловые стенты, обладающие памятью формы. Они практически не подвержены деформации и оказывают постоянное радиальное давление на стенку сосуда после имплантации. Стент позиционируют таким образом, чтобы дистальная и проксимальная его части перекрывали зону стеноза не менее чем на 5 мм. Сразу после имплантации стента про водят контрольную ангиографию, позволяющую определить степень резидуального стеноза. последующая дилатация (раздувание баллона внутри имплантированного стента) показана в тех случаях, когда степень резидуального стеноза превышает 30%. После завершения ангиопластики и стентирования фильтр-ловушку извлекают с помощью специального устройства. После удаления фильтра про водят контрольную ангиографию экстра- и интракраниального отделов церебральных артерий.
Стентирование подключичных и позвоночных артерий
Методика стентирования подключичных и позвоночных артерий не имеет принципиальных отличий от стентирования сонных артерий. Следует отметить, что при стентировании этих сосудов можно использовать как саморасширяемые (нитиноловые) , так и баллонрасширяемые стенты. Устройства для защиты мозга от эмболии обычно не используются, так как при значимых стенозах позвоночной и подключичной артерий создаются условия, при которых кровоток по позвоночной артерии становится ундулирующим или ретроградным. После ангиопластики и стентирования кровоток по позвоночНой артерии восстанавливается в несколько отсроченном промежутке времени (от 20 с до 20 мин).
ПОСЛЕОПЕРАЦИОННОЕ ВЕДЕНИЕ
После операции больным на протяжении последующих 2-4 ч следует проводить мониторинг АД и ЧСС для их коррекции, поскольку возникшие при дилатации брадикардия и артериальная гипотензия могут носить продолжительный характер. В течение последующих 3 сут больным назначают эноксапарин натрий (0,4 мл подкожно) . Клопидогрел следует принимать в течение 6 мес после операции (75 мг/сут) , ацетилсалициловую кислоту - в течение всей жизни (100 мг/cyт).
При стабильном состоянии пациента и отсутствии нарастания неврологической или сопутствующей соматической симптоматики больного можно выписать на следующие сутки после операции.
В дальнейшем пациентам проводят контрольные обследования через 1, 3, 6, 12 мес после операции, а затем каждые полгода. Эти обследования включают оценку неврологического статуса, дуплексное исследование брахиоцефальных артерий при каждом обследовании, спиральную кт в ангиографическом режиме и КТ головного мозга через 6 мес после операции, а также при выявлении клинических и ультразвуковых признаков рестеllоза.
РЕЗУЛЬТАТЫ
Результаты операции необходимо оценивать в следующих временных промежутках:
- периоперационный период (непосредственные результаты операции) - подготовка больного к операции, операция и ближайшие 1-3 сут после неё;
- ранний послеоперационный период (ближайший исход) - первые 30 дней после операции;
- поздний послеоперационный период (отдалённые результаты) - 12 мес после операции.
Критериями оценки в периоперационном периоде (непосредственные результаты операции) служат технический (или ангиографический) и процедурный успех.
- Техническим успехом считают степень остаточного (резидуального) стеноза, определяемого при контрольной ангиографии, менее 30%.
- Процедурный успех включает технический успех при отсутствии серьёзных осложнений (ишемический или геморрагический инсульт, инфаркт миокарда) или летального исхода.
В раннем послеоперационном периоде критериями оценки считают ишемические нарушения мозгового кровообращения (например, транзиторная ишемическая атака, малый или большой инсульт), инфаркт миокарда, рестеноз артерии, летальность.
В отдалённом периоде исход лечения оценивают по критериям, используемым в раннем послеоперационном периоде (инсульт, рестеноз, инфаркт миокарда, летальность), а также критериям, учитывающим изменение клинической картины заболевания (улучшение, без перемен, ухудшение) . Для оценки динамики неврологического статуса оптимальна шкала инсульта, разработанная Национальным институтом здоровья США (NIНSS).
ОСЛОЖНЕНИЯ
Одними из основных осложнений сосудистых (как прямых, так и внутрисосудистых) операций на брахицефальных артериях бывают нарушения мозгового кровообращения по ишемическому типу (транзиторная ишемическая атака, малый инсульт, большой инсульт). Ишемические расстройства могут произойти и на стороне оперируемого сосуда, и на противоположной стороне. В первом случае инсульт может быть следствием эмболии мозговых сосудов атеpоматозными или тромботическими массами, отрывающимися во время манипуляций при незащищённой артерии (манипуляции на артерии до установки устройств защиты).
Применение внутрисосудистых фильтров-ловушек при стентировании сонных артерий значительно уменьшает риск развития интраоперационных эмболических осложнений. При этом необходимо учитывать, что в некоторых случаях возможна макроэмболия самого фильтра. В условиях разобщённого виллизиева круга обусловленное эмболией фильтра длительное прекращение кровотока по внутренней сонной артерии может также привести к ипсилатеральному инсульту. При стенозах сонной артерии, сочетающихся с контралатеральной каротидной окклюзией, длительное прекращение кровотока на оперируемой сонной артерии может привести как к ипсилатеральному, так и к контралатеральному инсульту (гемодинамический инсульт) . Допплерографический мониторинг (динамика линейной скорости кровотока по средней мозговой артерии, эмболодетекция) помогает выявлять изменения церебральной гемодинамики в ходе операции в режиме реального времени, тем самым позволяя предотвратить развитие ишемических осложнений.
В некоторых случаях при ангиопластике и стентировании сонных артерий ишемический инсульт бывает следствием длительной брадикардии и артериальной гипотензии, возникшей в результате барорефлекса при манипуляциях в синокаротидной зоне. Профилактика этого осложнения крайне важна. В большинстве случаев бывает достаточно предварительного внутривенного введения 0,3-1,0 мг раствора атропина за 3-5 мин до баллонной дилатации. Однако в некоторых случаях брадикардия и артериальная гипотензия прогрессируют, несмотря на
стр 399 пропущена
• Окклюзии сонных артерий при субкомпенсации мозгового кровообращения в бассейне окклюзированной артерии (ундулирующий неврологический дефицит, ретроградный кровоток по глазничной артерии, асимметрия кровотока по интракраниальным артериям по данным ТКДГ, отсутствие или уменьшение цереброваскулярных резервов при функциональных пробах).
• в комбинации с реваскуляризирующей операцией при множественном поражении брахиоцефальных артерий.
ПРЕДОПЕРАЦИОННОЕ ОБСЛЕДОВАНИЕ
Принципы обследования больных те же, что и при проведении реконструктивных операций на сонных и позвоночных артериях. При планировании экстраинтракраниального микроанастомозирования необходимо также ультразвуковое исследование интракраниальных артерий.
ТКДГ проводят датчиком с частотой 2 МГц в пульсовом режиме. Больной лежит на спине или на боку в зависимости от лоцируемой артерии. Артерии основания головного мозга, а также магистральные артерии в их экстракраниальных сегментах идентифицируют по данным глубины эхолокации в соответствии с общепринятой методикой. При исследовании необходимо оценить величину линейной скорости кровотока, направление кровотока, его спектральные характеристики в средней (сегменты Мl, М2), передней и задней мозговых артериях, глазничной артерии с обеих сторон. При планировании операции по созданию экстраинтракраниального микроанастомоза обязательным в оценке состояния коллатерального кровообращения считают исследование цереброваскулярных резервов (мониторирование линейной скорости кровотока в средней мозговой артерии на стороне окклюзии на фоне перорального приёма ацетазоламида в дозе 1 г или задержки дыхания) . Для выявления при знаков субкомпенсации кровообращения в вертебробазилярном артериальном бассейне про водят исследование динамики линейной скорости кровотока в задней мозговой артерии с обеих сторон на фоне фотостимуляции зрительного коркового анализатора.
МЕТОДИКА ПРОВЕДЕНИЯ
Операцию проводят под эндотрахеальным наркозом с использованием операционного микроскопа, микрохирургического инструментария и атравматического шовного материала.
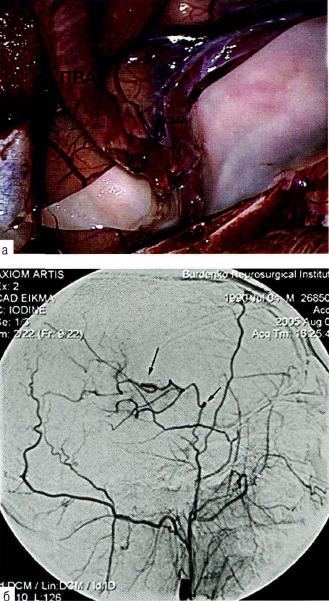
Реваскуляризацию головного мозга осуществляют наложением экстраинтракраниального сосудистого анастомоза между ветвью поверхностной височной артерии и корковой ветвью средней мозговой артерии на стороне тромбоза внутренней сонной артерии (рис. 19-9а) .
Рис. 19-9. 3кстра-интракраниальный анастомоз: а - вид анастомоза между поверхностной височной артерией ( ПВА) и ветвью средней мозговой артерии (СМА) на операции; 6 - ангиография (боковая проекция) после создания экстра-интракраниального анастомоза (стрелками указаны зона анастомоза и заполняющиеся через него вторичные ветви средней мозговой артерии).
Донорскую артерию выделяют на протяжении 5-6 см в соединительнотканном футляре шириной 3-4 мм после подковообразного или линейного разреза кожи и мягких тканей в височно-теменной области. В качестве донорской чаще всего используют теменную ветвь поверхностной височной артерии. Использование лобной ветви поверхностной височной артерии оправдано лишь при отсутствии функционирующего естественного каротидно-офтальмического анастомоза, питающегося из лобной ветви поверхностной височной артерии. После костнопластической трепанации височно-теменной области диаметром 2,5-3,0 см, вскрытия твёрдой и арахноидальной мозговых оболочек выделяют корковую артерию.
После сопоставления донорской артерии с корковой создают микроанастомоз по типу "конец в бок" под углом 450 , накладывая отдельные микрососудистые швы (от 9 до 11). Твёрдую мозговую оболочку сопоставляют наложением наводящих швов. После выпиливания канала для прохождения донорской артерии костный лоскут фиксируют отдельными швами. Подкожный дренаж, как правило, не устанавливают во избежание возможного повреждения микрососудистого анастомоза.
При гемодинамически значимом стенозе наружной сонной артерии или окклюзии общей сонной артерии на стороне тромбоза внутренней сонной артерии перед созданием экстра-интракраниального микроанастомоза показана этапная пластика устья наружной сонной артерии или подключично-наружносонное шунтирование.
Одномоментные реконструктивные и реваскуляризирующие вмешательства нецелесообразны.
ПОСЛЕОПЕРАЦИОННОЕ ВЕДЕНИЕ
В послеоперационном периоде медикаментозное лечение про водят п о тем же принципам, что и после реконструктивных вмешательств. Снятие швов после создания экстра-интракраниального микроанастомоза про водят на 9- 10-е сут. Чтобы оценить функционирование анастомоза, используют ТКДГ и прямую ангиографию.
При хорошо функционирующем анастомозе объёмная скорость кровотока по нему составляет около 30-35 млjмин, достигая в отдельных случаях 40-60 млj мин. При ангиографическом исследовании можно видеть степень заполнения васкуляризированного бассейна (рис. 19-9б).
ОСЛОЖНЕНИЯ
Основным осложнением операции бывает тромбирование анастомоза. Оно, как правило, развивается непосредственно или в ближайшие сроки после операции.
Читайте также: