Лечение травм спинного мозга новинки лечения

Препарат на основе двух генов поможет восстановить двигательную активность пациента после травмы спинного мозга. Революционная разработка российских ученых защищает нейроны от гибели, стимулирует рост кровеносных сосудов и новых нервных волокон. Эффективность препарата показали проведенные на крысах эксперименты — спустя несколько месяцев после начала лечения животные смогли ходить на прежде парализованных конечностях. Для того чтобы начать доклинические испытания, исследователям осталось решить проблемы с финансированием.
Травма спинного мозга, возникшая в результате аварии, несчастного случая или падения с высоты, нередко приводит к потере чувствительности и способности двигать частями тела ниже места поражения. Сейчас помочь мышцам усилить сигнал может только экзоскелет и нейропротезы, и то при условии, что не полностью утрачена связь между спинным и головным мозгом. Исследователи из Казанского федерального университета (КФУ) создали препарат, который позволяет успешно бороться с травмами спинного мозга, несмотря на наличие осложняющих выздоровление факторов.
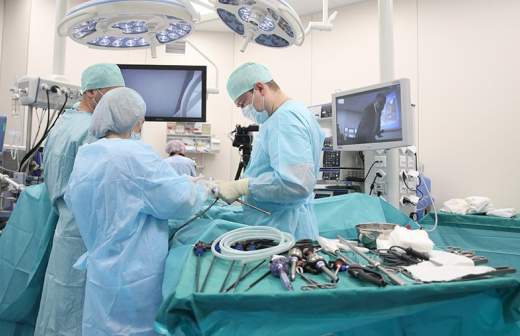
Дело в том, что при повреждении спинного мозга организм постепенно наращивает в месте травмы рубец, состоящий из соединительной ткани. Он необходим для своеобразной фиксации места повреждения, но в дальнейшем препятствует росту аксонов, отростков нервных клеток, с помощью которых осуществляется связь с другими клетками.
Перед исследователями стояла задача создать такой препарат, который снижал бы скорость образования рубца и восстанавливал нервную ткань.
Исследователи из института фундаментальной медицины и биологии КФУ создали такой препарат, взяв за его основу два гена (VEGF и FGF2). Первый ген нормализует кровоснабжение при нейротравме, поддерживает выживаемость нейронов, стимулирует нейрогенез, рост новых сосудов и аксонов. Второй ген представляет собой фактор роста, обладает выраженным нейротрофическим действием — поддерживает выживаемость клеток в области повреждения, способствует развитию нервных волокон. Получившийся препарат содержит и регуляторные элементы, которые контролируют работу этих генов.
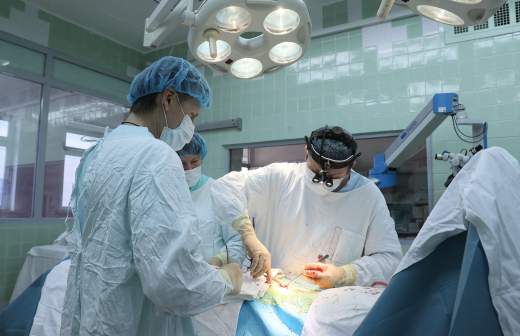
Испытания препарата на животных проходили следующим образом. Чтобы смоделировать повреждение спинного мозга, у подопытных вскрывали позвоночник и по нему с помощью специального молоточка наносили удар строго определенной силы. После операции животные теряли чувствительность задних конечностей и способность ими двигать. Во время всего эксперимента за животными тщательно ухаживали, помогая справляться с гигиеной и приемом пищи.
После нанесения травмы ученые переходили к лечению. Опытной группе животных вводили генный препарат, а контрольной позволяли восстанавливаться без стороннего вмешательства.
У крыс контрольной группы через два месяца после травмы наблюдалось частичное восстановление двигательных функций — животные сгибали лапы в одном или двух суставах. Однако полноценно передвигаться, удерживать вес тела и координировать движения грызуны не могли. Крысы в опытной группе в этот же период стали уверенно вставать на лапы, ходить, контролируя движения передних и задних конечностей.
— Помимо применения генного препарата мы проводим исследования эффективности лечения травм спинного мозга с помощью мезенхимных стволовых клеток, — рассказал старший научный сотрудник лаборатории генных и клеточных технологий института фундаментальной медицины и биологии КФУ Яна Мухамедшина. — Результаты обеих работ обнадеживают и показывают, что мы можем эффективно восстанавливать травмированный спинной мозг и его функции у крупных животных, в частности свиней, а в дальнейшем и у человека.
В перспективе ученые планируют сочетать эти методики для лечения травм головного мозга и терапии нейродегенеративных заболеваний.
Несмотря на то что гены в составе препарата и так присутствуют в человеческом организме, некий элемент риска всё равно есть и его невозможно предсказать, считает директор Института молекулярной медицины Научно-технологического парка биомедицины Сеченовского университета Андрей Замятнин.
— В составе генетической конструкции, которая используется, есть части (регуляторные элементы), которые в человеческом организме отсутствуют, — пояснил он. — Их влияние на организм абсолютно непредсказуемо. Поэтому для доказательства безопасности препарата необходимо провести клинические испытания.
Ученые готовы начать доклинические испытания в течение года, если решат вопрос финансирования.
Электрическая стимуляция спинного мозга вернула парализованным способность ходить. С этого года такие же операции будут проводить в России.
Не хуже швейцарских часов
Несколько лет в инвалидном кресле из-за травмы спинного мозга провели трое мужчин, прежде чем стать добровольцами в эксперименте доктора Грегуара Куртина. Этот швейцарский невролог задался целью вернуть подвижность их парализованным ногам с помощью электричества.
В госпитале Университета Лозанны нейрохирург Джоселин Блох имплантировала в позвоночник каждого по электрическому стимулятору. Стимулятор работает от пульта, включается врачом или самим пациентом и посылает импульсы к определенным группам мышц в ногах. При этом добровольцы параллельно проходили обычный курс реабилитации, состоящий из массажа и специальных упражнений.
Результаты превзошли все ожидания реабилитологов: через неделю парализованные пациенты смогли ходить с механической поддержкой, а еще через пять месяцев двое из них сумели сделать несколько шагов, даже не включая нейростимулятор,— поврежденные нейронные связи начали восстанавливаться. Само собой, тут же во весь рост встал вопрос о степени уникальности эксперимента. Попросту говоря, получат ли другие обездвиженные шанс вновь ходить на своих ногах?
Животным с частично пересеченным спинным мозгом точно так же вживляли в позвоночник электроды — оснащенная электростимулятором крыса при поддержке начинала резво передвигаться на задних лапах. Правда, в лабораторных условиях проводить такие опыты проще, ведь в реальности не бывает двух абсолютно идентичных травм позвоночника, каждый случай уникален, и к каждому пациенту приходится искать особый подход. Тем не менее метод сработал и на людях. Ученые объясняют результативность своих усилий высокой точностью установки и прицельным воздействием имплантатов.
— Мы стремились к тому, чтобы нейростимуляция была такой же точной, как швейцарские часы,— говорит нейрохирург Джоселин Блох.— Особые конфигурации электродов, установленных нами, активируют специфические области спинного мозга, имитируя команды мозга, которые запускают ходьбу.
А руководитель исследования Грегуар Куртин объясняет, почему он уже в первую неделю после установки имплантатов понял, что ступил на правильный путь.
— За годы испытаний этого метода на животных мы добились глубокого понимания того, как происходит активация спинного мозга естественным образом,— объясняет он.— Мы поняли, что решающую роль в способности пациента двигаться играет точное время и место электростимуляции. Именно это вызывает рост новых нервных связей.
По нужному адресу

Предшественники Куртина и Блох использовали непрерывную электростимуляцию. Но она не давала стойкого результата: как только ее отключали, пациенты возвращались к обездвиженному состоянию. Принцип действия новой нейротехнологии пока до конца непонятен, да и выборка пациентов пока что мала, однако первые успехи вдохновили швейцарцев на новые опыты. Теперь они хотят испытать действие электростимулятора на раннем этапе после травмы, когда нервно-мышечная система еще не атрофировалась после хронического паралича, и потенциал для выздоровления больший.
— По сути, мы создаем нейротехнологию следующего поколения,— говорит невролог Куртин.— Наша цель — разработать лечение, доступное в клиниках по всему миру.
Российские реабилитологи пока не могут оценить преимущества использования нейростимуляторов при работе с парализованными и комментируют достижения Грегуара Куртина с долей профессионального скепсиса.
— Мы сможем обсуждать применение этой технологии, когда она покажет статистически значимый результат, будет детально изучена и обоснована,— говорит заведующий отделением реабилитации Междисциплинарного центра реабилитации Василий Купрейчик.— Пока то, что делает доктор Куртин, требует осмысливания.
Впрочем, их коллеги нейрохирурги более оптимистичны. Дело в том, что спинальные электростимуляторы в мире используются довольно давно: в США сегодня живут около 250 тысяч человек с имплантированными системами электростимуляции. В России нейростимуляцией на научном уровне занимаются 30 медицинских учреждений. До недавнего времени за год в нашей стране устанавливалось 800 спинальных электростимуляторов, сейчас эта цифра выросла до 1200 — такова сейчас квота государства на бесплатные операции. Но до сих пор эту технологию использовали не для лечения парализованных. Она помогала решить другие задачи, прежде всего проблему хронических болей, а также симптоматическое лечение сложных генетических заболеваний, связанных с потерей подвижности. Швейцарские неврологи сделали ставку на факторы, которые прежде считались побочными эффектами в борьбе с другими болезнями. Теперь ученым остается только подтвердить свою разработку в более масштабных исследованиях.
Лечение электрической рыбой
Первым нейростимуляцию использовал, как ни странно, еще Гиппократ. Он описывал метод лечения невралгии тройничного нерва с помощью прикладывания электрического ската к больной половине лица. Вряд ли Гиппократ понимал механизм действия своей терапии, но он видел, что удар электричества способен переключить боль.
Алексей Кащеев в год делает 400–450 операций на спинном мозге, позвоночнике и периферических нервах. Из них 20 — по установке нейростимуляторов. Сам имплантат стоит около 1,5 млн рублей, и большая часть этой суммы приходится на стоимость генератора тока, который отдельно устанавливается под кожу и соединяется со стимулятором тонким проводом. Врачи не могут гарантировать, что нейростимуляция сработает для каждого пациента, поэтому проводят недельный тестовый период: провод от стимулятора выводят наружу и соединяют с источником тока, которым управляет пациент. Если выясняется, что электростимуляция помогает, под местным наркозом проводят вторую операцию — вживляют маленькую заряжающуюся батарею. Пациент получает пульт управления, которым можно включать и выключать устройство, или убавлять силу тока, если, например, стимуляция усилилась, из-за того что электрод слишком крепко прижался к спинному мозгу, когда человек лег на спину.
— Нейромодуляция — одно из самых перспективных направлений в нейрохирургии,— утверждает Алексей Кащеев из Научного центра неврологии.— Я не удивлюсь, если она заменит очень многие способы лечения, потому что она избавляет человека непосредственно от того, что его беспокоит, и при этом лишена серьезных рисков или побочных эффектов. Метод может не сработать, или у человека может сместиться электрод и нарушится зона стимуляции — вот и все риски. Их не сравнить с возможностью большой кровопотери, с нарушением каких-то функций или с формированием хронической боли, которая возникает при повреждении нерва.
Жизнь в пять раз лучше
Как мы уже говорили, точный механизм действия нейростимуляции до сих пор не раскрыт, и потому метод постоянно преподносит ученым сюрпризы. Например, выяснилось, что этим способом можно спасать конечности у больных с критической ишемией — когда нога гибнет из-за сахарного диабета или из-за непоправимого нарушения артериального кровообращения. От безысходности им стали устанавливать электростимуляторы, чтобы облегчить хроническую боль, и вдруг выяснилось, что, воздействуя на конечность, можно добиться не только обезболивания, но и расширения сосудов. У Алексея Кащеева есть пациенты, которым благодаря нейростимуляции удалось спасти ногу от ампутации: ограничились ампутаций нескольких пальцев.

В середине 80-х годов имплантаты на позвоночник стали устанавливать больным с рассеянным склерозом — ноги у них и болят, и теряют подвижность. Врачи рассчитывали только на обезболивание, но выяснилось, что эти пациенты стали лучше ходить. Нейрохирурги подчеркивают: чуда — полного излечения парализованного — они пока обеспечить не могут. Но параметры ходьбы у таких больных стали объективно лучше.
— Российские врачи первыми в мире описали использование спинальной стимуляции у пациентов с болезнью Штрюмпеля,— рассказывает нейрохирург Алексей Кащеев.— Это неизлечимое генетическое заболевание начинает проявляться в 20–30 лет в виде судорог в ногах и ведет к разрушению спинного мозга, утрачивается способность ходить. Так вот, статья вышла в 2015 году, с тех пор мы регулярно устанавливаем имплантаты таким больным. Первым пациентом у нас был дирижер и аранжировщик — утрата возможности нажимать на клавиши стала для него настоящей трагедией. Нет, он не излечился, но стал гораздо лучше ходить и двигаться. Прошло еще слишком мало времени, чтобы сделать вывод, тормозит ли стимуляция развитие самой болезни. Но мы установили: со стимулятором качество жизни наших пациентов улучшается в разы.
И надеется, что часть из них ходить сможет. Возможно, электростимуляция продемонстрирует врачам и другие неожиданные эффекты.
— Важно, чтобы пациенты не строили иллюзий: не существует людей, которым метод помог на 100 процентов,— предостерегает нейрохирург Кащеев.— Но он существенно улучшает качество жизни и его можно использовать в комплексе с другими методами — с лекарствами, с физиотерапией, потому что ограничений немного. Подходит даже пожилым — самому старшему моему пациенту 91 год. А другой пациент — он перенес 17 операций на голени, одну на позвоночнике, постоянно принимал обезболивающие — после операции два года назад снова активно занимается спортом, дайвингом: в год — до 50 прыжков с парашютом. Можно сказать, он вернулся к обычной жизни! Только это не значит, что я могу каждому гарантировать такой результат.
В любом случае метод будет развиваться. Параллельно с выяснением новых эффектов воздействия нейростимуляции на организм ученые совершенствуют и само устройство. На Западе, к слову, уже создан имплантат, в котором электрод совмещен с генератором тока. Таким образом устройство становится более компактным, а главное — беспроводным. Это дает возможность устанавливать имплантат на подвижной части тела и не опасаться, что при движении провод выдернется из генератора.
В будущем, считают медики, для подобных больных станет доступен нейроинтерфейс, то есть прямая связь головного мозга с электронным устройством. Пациенты с нейростимуляторами откажутся от пультов управления, так как работа имплантата будет согласована непосредственно с командами головного мозга.
Сейчас это кажется фантастикой, но, как свидетельствует множество научных примеров, будущее часто приходит, когда его не ждут.
Новый метод лечения травм спинного мозга
Наука часто апеллирует к интуитивной прозорливости. Прорывы в медицине иногда происходят из слухов и легенд (Эдвард Дженнер слышал, что доярки, инфицированные коровьей оспой, не болеют оспой – так и появилась первая вакцинация от оспы); от случайного заражения экспериментального материала (открытие пенициллина и неопрена); и от неожиданных побочных эффектов лекарств (Виагра изначально предназначалась для лечения заболеваний сердца).
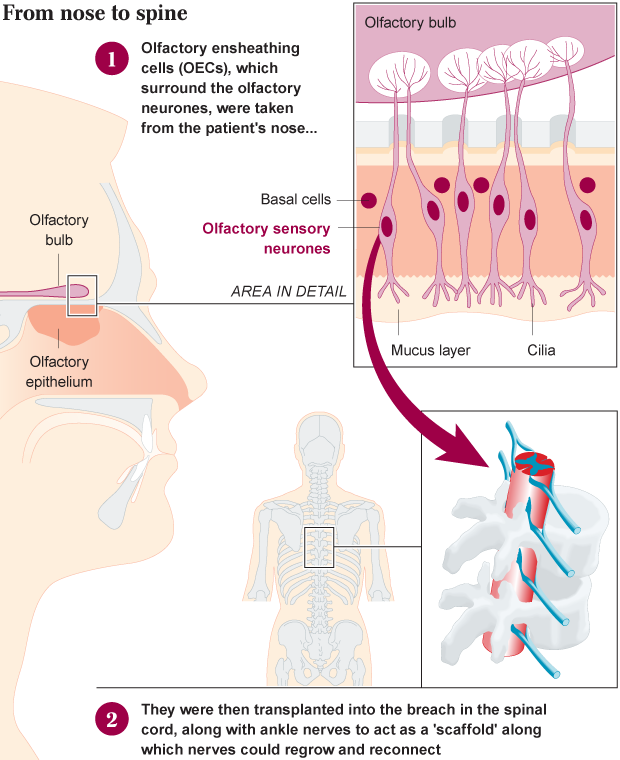
И мог ли предполагать Дарек Фидика , 38-летний польский пожарный, болеющий синуситом, что попадет в историю медицины как первый парализованный больной, который стал ходить после трансплантации нервных клеток. Восстановление движений в ногах дало пациенту невероятные ощущения и стало фактически вторым рождением. У пациента Фидика спинной мозг был полностью перерезан ножом во время драки с бывшим мужем жены, и Фидика согласился на пересадку клеток, полученных из носа. Клетки, которые называются обонятельные оболочечные (глиальные) клетки , как известно, влияют на регенерацию обонятельных нервов, которые транспортируют сигналы с обонятельных рецепторов в мозг и восстанавливаются каждые 30 дней.
Вместо этих специальных клеток, - которые не являются стволовыми клетками, а взрослыми функционирующими клетками – были получены нервные клетки с помощью операции на головном мозге. Нейрохирурги в университетской больнице Вроцлава в Польше проникли в череп Фидика, экстрагировали левую обонятельную луковицу и подготовили готовую к трансплантации культуру клеток ООК. Эти культивированные клетки затем пересадили в спинной мозг в область разрыва, вместе с полосками нервов лодыжки, чтобы задействовать их в качестве каркаса, по которому нервы могли бы вырасти.
В течение полутора лет появились результаты новаторской операции: пожарный, который также получал физиотерапию, ЛФК, смог частично перемещать свои нижние конечности, появились ощущения в ногах, выросли мышцы на левом бедре и в некоторой степени восстановились функции мочевого пузыря и кишечника, а также половые функции.
При таких тяжелых травмах спинного мозга как у Фидика (класса А), как правило, пациенты остаются парализованными на всю жизнь. Благодаря этому революционному вмешательству пациент стал передвигаться с помощью ходунков, и тяжесть его состояния перешла в класс С., Кроме того, как ни удивительно, он не потерял обоняние.
Операция была проведена в Польше, но была провозглашена в качестве прорыва британской медицины, так как проводилась под руководством профессора Джеффри Райзмана, из отделения нейрохирургии Университетского колледжа неврологии Лондона Профессор Райзман заявил. "Я считаю, что мы стоим на пороге исторического переломного момента в медицине "
В финансировании также участвовали UK Stem Cell Foundation и Nicholls Spinal Injury Foundation.NSIF это благотворительный британский фонд, который был создан Дэвидом Николсом, чей сын Дэниел был парализован после травмы позвоночника во время купания. Организация Spinal Injuries Association встретила известие о проведенной успешной операции с "осторожным оптимизмом", так как в настоящее время в Великобритании почти 40 000 человек с травмой спинного мозга.
Профессор Райзман еще в 1985 году исследовал клетки ООК и в 1997 году показал , что они могут повернуть вспять паралич у крыс. Теперь же свидетельствует Кевин Шейксшеф, профессор инженерии тканей из Университета Ноттингема, настойчивость стала давать плоды. "Это успех не в одночасье ," говорит профессор Shakesheff, который сотрудничал с профессором Райзманом в начале девяностых. "Джефф достиг таких блестящих результатов длительной работой в течение последних 20 лет, и он наблюдал за клиническими исследованиями в течение последнего десятилетия. Он знает о ООК больше, чем кто-либо в мире ".
Несмотря на то, что периферическая нервная система, в конечностях, может самовосстанавливаться - порезка пальца кухонным ножом, например, не будет, как правило, приводить к необратимому повреждению - то же самое не возникает при повреждении спинного мозга. Этот огромное слепое пятно в системе регенерации организма стало мотивацией для многих тысяч ученых, работающих в области регенерации тканей. Также интерес к регенерации спинного мозга стимулировал сбор средств для проведения научных изысканий: Фонд Кристофера и Дана Рив был организован после того, как актер, сыгравший последнего Супермена, был парализован после травмы во время верховой езды и этот фонд за короткое время собрал более $ 110 млн.
Мало того, что исследования могут помочь спинальным больным, но они имеют и долгосрочные цели: болезни старения, такие как заболевания сердца, рак и болезнь Паркинсона, являются в значительной степени результатом дегенерации и гибели клеток. Возможность создания здоровых клеток, которыми можно заменить старые клетки, очевидно, будет приоритетом медицины в ближайшем будущем.
В последние десять лет надежда восстановления тканей, в том числе и регенерации нервов, в значительной степени подогревалась ажиотажем вокруг стволовых клеток. Стволовые клетки делятся на два типа: эмбриональные - те, что могут быть собраны из ранних эмбрионов, со всеми вытекающими этическими проблемами; и взрослые стволовые клеток, которые могут быть извлечены из костного мозга и некоторых других тканей организма взрослого.
Ключевой особенностью стволовых клеток является их потенциальная возможность превращаться в определенные типы клеток; и давняя мечта ученых разблокировать этот потенциал так, чтобы он был аналогичен потенциалу эмбриональных клеток, который гораздо выше.
Именно невысокий потенциал взрослых стволовых клеток был причиной многочисленных неудачных клинических испытаний применения их для лечения сердечно-сосудистых заболеваний, диабета, болезни Паркинсона и травм спинного мозга.
В отличие от этого, ООК являются не стволовыми клетками, а взрослыми клетками, которые уже имеют окончательную специализизацию. Но именно их окончательная функция - как-то обучать и стимулировать рост нервных клеток в носовых ходах - была успешно использована в проведенном клиническом эксперименте.

Но наука все еще далека от полного лечения травм спинного мозга. Фидику повезло, и он больше не прикован к инвалидной коляске и через некоторое время сможет жить полноценно. Его восстановление, отчет о которых был опубликован в журнале трансплантации журнал Cell, может быть обусловлено целым рядом факторов. Его спинной мозг был разрезан относительно чисто; что, возможно, облегчило растущим нервным клеткам, преодолеть зазор в8 мм. У большинства же пациентов травмы спинного мозга гораздо более сложные .
Вполне возможно, что у хирурга было достаточное количество ООК клеток и ему удалось ввести их в нужное место. Для того чтобы убедиться в реальной эффективности такой методики лечения, необходимо провести ряд исследований на достаточно большой группе пациентов, и только затем можно говорить о реальной эффективности методики.
Но прорывы когда- то должны начинаться. Дэвид Николс потратил почти миллион фунтов на фундаментальные медицинские исследования, которые могли бы помочь его парализованному сыну Даниилу. Николс был предупрежден врачами, не предаваться ложным надеждам. Не испугавшись, он передал деньги, которые он собрал, профессору Райзману со словами: «Все говорили, я теряю время, но что такое жизнь без надежды?"
Профессор Райзман, обнадежил своего спонсора и сделал именно то, что делают ученые экспериментаторы: он следовал за наукой везде, куда она приводила, несмотря на обескураживающие трудности. Он сделал очень простой научный расчет- это то, что врачи могли изъять клетки из одной части тела, вставить их в другую часть тела, и те же клетки могут просто выполнять свою обычную работу. Если такое работает у крыс и собак; кто скажет, что это не может работать в организме человека?
Не всегда врачи могут сразу определить, приходится ли им иметь дело с полным либо с частичным повреждением. При частичном повреждении спинной мозг может передавать некоторые сигналы в головной мозг и наоборот, поэтому такие пациенты обладают некоторой чувствительностью и даже некоторыми моторными функциями ниже пораженной области.
Полное повреждение спинного мозга сопровождается полной или почти полной потерей моторной функции и чувствительности ниже области поражения. И хотя даже при тяжелой травме спинной мозг почти никогда не является полностью перерезанным, обширность повреждения приводит к тому, что восстановление пациента становится делом практически безнадежным. Во всяком случае, так считалось до сравнительно недавнего времени.
Несколько фактов

Больница Крейга в штате Колорадо, США, специализирующаяся на лечении и реабилитации пациентов с параличом, предлагает на своем сайте несколько фактов, позволяющих больным и их близким сориентироваться в новой для них реальности.
– Почти всегда остается надежда на восстановление по крайней мере некоторых из утраченных функций.
– При неполном параличе шансы восстановления выше. Анализ медицинской статистики штата Колорадо показал, что только 1 из 7 полностью парализованных после травмы пациентов смог добиться значительной степени восстановления движения. Для тех, кто сразу после травмы сохранил хотя бы слабую способность к движению конечностей, эта пропорция значительно выше: 3 из 4 таких пациентов добиваются существенных улучшений.
– При полном параличе неплохой шанс есть у того, кто сохранил чувствительность в нижней части туловища сразу после травмы. Примерно 2/3 пациентов с повреждением спинного мозга в шейном отделе после длительной реабилитации смогли нарастить достаточную силу мышц в ногах для того, чтобы ходить, при условии, что сразу после травмы они ощущали укол ноги иголкой. Что касается тех, кто ощущал только легкое прикосновение, ходить сможет примерно 1 из 8 таких пострадавших.
– Чем скорее после травмы начнут работать мышцы, тем выше шанс на прогресс, тем реальнее перспектива встать и пойти. Как правило, если мышцы становятся способны функционировать лишь через несколько недель, это с большей вероятностью будут мышцы рук, а не ног.
Сколько длится тот период, в который можно надеяться на существенное улучшение, будь то пациент с неполным или полным повреждением спинного мозга? Как долго можно жить надеждой? На этот вопрос нет однозначного ответа. Понятно, что после двух или трех лет паралича, шансы на то, что мышцы заработают без посторонней помощи, практически ничтожны.
Что же касается месяца, двух, полугода после травмы – прогноз сделать сложнее, однако есть два правила, которые помогут сориентироваться:
– Если есть постоянные улучшения, если все новые мышцы постепенно восстанавливают функцию, значит, высок шанс дальнейшего значительного прогресса.
– Чем дольше период без улучшений, тем ниже шанс на восстановление.
Что ж, эти факты внушают умеренный оптимизм даже тем, кто пострадал от обширного поражения спинного мозга. Еще больший оптимизм внушают научные разработки, которые в перспективе могут сделать паралич излечимым или, по крайней мере, создать условия для значительной адаптации пострадавших от травм спинного мозга к нормальной жизни.
Почва для оптимизма

Роб Саммерс в свои 20 лет был полон надежд: он должен был начать обучение в Университете штата Орегон, активно занимался бейсболом. Все изменилось 12 июля 2006 года: его сбила машина, после чего он оказался полностью обездвижен. И хотя у него сохранялась некоторая чувствительность в нижней части туловища, прогноз был неутешительным. Врачи сказали, что ходить Роб никогда не сможет.
В конце XX века история на этом бы и закончилась, но в наше время медицина все быстрее переходит от научной теории к практике. Робу Саммерсу и еще трем молодым людям с повреждениями спинного мозга предложили инновационную терапию – эпидуральные стимуляторы, имплантируемые в спинной мозг. Все четыре пациента, парализованные, по крайней мере, от груди и до кончиков ног, теперь в состоянии двигать ногами.
Роб Саммерс первым получил экспериментальное лечение, разработанное доктором Регги Эдгертоном из Калифорнийского университета (Лос-Анджелес) и доктором Сьюзан Харкема из Университета Луисвиля (Кентукки) при участии наших соотечественников из Института физиологии имени Павлова (Санкт-Петербург). Они опубликовали свою историю успеха в 2011 году в журнале Lancet.
В чем суть терапии?
Стимулятор подает непрерывный электрический импульс на разных частотах и разной интенсивности нижнему спинному мозгу, то есть в пояснично-крестцовую зону, и тем самым имитирует мозговые сигналы, которые инициируют движения.
Все четыре пациента приобрели способность двигать ногами сразу же после имплантации и активации стимулятора, при этом движения были произвольными. Исследователи пришли к выводу, что некоторые сигнальные пути могли остаться неповрежденными после травмы, и именно они облегчают совершение произвольных движений. Мозг воспринимает сигнал стимулятора как свой собственный, и мгновенно начинает контролировать и направлять движения мышц.
Экзоскелеты, стволовые клетки и даже носовые нейроны!
Две недели назад в журнале Scientific Reports была опубликована статья международного коллектива бразильских, американских и немецких ученых, добившихся восстановления некоторых двигательных функций у пациентов, которые в результате тяжелых травм спинного мозга были полностью парализованы в течение очень длительных сроков – от 3 до 15 лет.
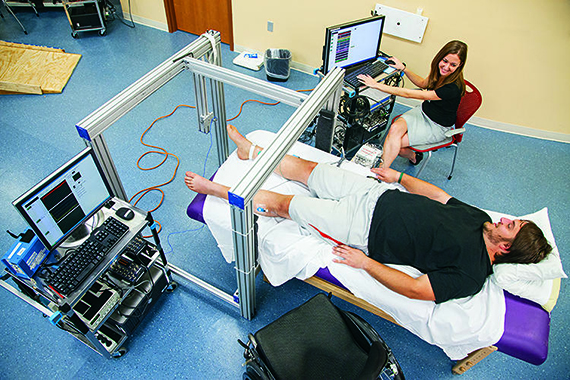
Метод реабилитации включал 3 компонента: виртуальную реальность, нейроинтерфейс и роботизированный экзоскелет.
Нейроинтерфейс представляет собой электроэнцелограф, регистрирующий активность мозга и передающий данные в компьютер для анализа. Когда пациент представлял себе, что он ходит, сигналы мозга, обрабатываемые компьютерной программой, приводили к тому, что аватар на экране двигался. Когда этот этап был пройден, пациенты перешли к занятиям с экзоскелетом, также управляемым нейроинтерфейсом.
Летом 2014 года член научной команды, нейробилог Мигель Николелис, представил на чемпионате мира по футболу одного из своих парализованных подопечных в экзоскелете, и тот на глазах у изумленной публики ударил по мячу.
Научное сообщество отнеслось к этой демонстрации весьма скептически: глядя со стороны, трудно было понять, действительно ли человек в экзоскелете самостоятельно контролировал свое футуристического вида оснащение.

Эти результаты кому-то могут показаться скромными, но ведь речь идет о пациентах, у которых чувствительность и минимальные моторные функции отсутствовали годами, а, как мы знаем, даже небольшой прогресс вселяет надежду на прогресс дальнейший.
Важно заметить также, что экзоскелеты с нейроинтерфейсом и ранее использовались в экспериментах по реабилитации парализованных людей, но подобный результат был достигнут впервые благодаря тому, что начинался эксперимент с обучения действиям в виртуальной реальности.
Было бы нелогично, если паралич не попробовали бы лечить стволовыми клетками. На сегодняшний день в арсенале ученых-медиков немало экспериментов, проведенных на животных.


Ученые считают, что новая методика поможет и парализованным людям, потерявшим подвижность после травм. Впрочем, пока о клинических испытаниях терапии на людях говорить преждевременно. В ближайшее время авторы протестируют разработанную ими технологию на более крупных животных.
Чуть раньше были опубликованы результаты исследований австралийских ученых из Университета Нового Южного Уэльса. Им удалось перепрограммировать клетки костной и жировой тканей в индуцированные мультипотентные стволовые клетки, способные участвовать в регенерации любых тканей.
Команда ученых уже успешно испытала полученные стволовые клетки на мышах. Теперь ученые считают, что в 2017 году они смогут протестировать клетки на людях. С помощью новых клеток авторы планируют лечить паралич и справиться с другими заболеваниями, например, с хроническими болями в спине или последствиями травм.
В октябре 2014 года в журнале Cell Transplantation был опубликован отчет о еще одной инновационной медицинской технологии, разработанной группой польских и английских медиков во главе с нейрохирургом Павлом Табаковым.
Сорокалетний Дерек Фидика в 2010 году после удара ножом в спину оказался парализован от груди и ниже. После двух лет безуспешной терапии медики решились на экспериментальный вид лечения.
Врачи провели операцию по извлечению обонятельной луковицы пациента, затем в специальных условиях были выращены особые клетки обонятельной выстилки носа, известные своей способностью проводить нервные импульсы. После этого были сделаны микро-инъекции клеток в область повреждения спинного мозга. Наконец, в ту же область были имплантированы четыре полоски нервной ткани.
По словам врачей, пересаженные клетки, прижившись в спинном мозге, стали выполнять функцию по проведению нервных импульсов между клетками самого мозга, таким образом способствуя их регенерации и восстановлению активности.
Уже спустя три месяца после вмешательства пациент почувствовал первые изменения, ощутив мышцы собственной ноги. Спустя еще полгода он смог сделать первые шаги при поддержке специального устройства и при помощи врача.
Важное преимущество метода заключается в том, что пациенту пересаживаются клетки из его собственной обонятельной луковицы, а значит, не произойдет реакции отторжения, как это бывает с донорскими органами и клетками.
Трудно сказать, какая из описанных терапий наиболее перспективна. Важно, что их несколько, что они развиваются, и каждая дает основания для надежды на то, что в будущем паралич станет полностью излечимым заболеванием.
Читайте также:


