Ферменты и межпозвонковая грыжа
Пожалуй, нельзя припомнить ни одного случая, чтобы доказанная межпозвонковая грыжа у пациента не требовала рано или поздно применения лекарственных препаратов. Медикаментозное лечение с помощью тех или иных средств грыжи позвоночника обычно проводится на начальном этапе ее возникновения, когда пациента внезапно сковывает сильная и острая боль, а также в периоды ее обострения. Каковы особенности лечения грыж лекарствами, и для чего нужны эти медикаменты?
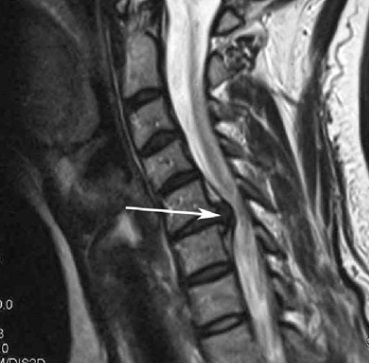
Грыжа шейного отдела на МРТ.
Особенности и цели лечения грыж лекарствами
Каковы же цели лечения межпозвоночной грыжи с помощью лекарств? Эти цели можно перечислить ниже:
- снятие болевого синдрома, цель симптоматическая. Пациент при достижении цели начинает обслуживать себя в быту, передвигаться, и может самостоятельно посетить лечебное учреждение;
- купирование воспаления и отека, который вызван компрессией грыжевым образованием различных мягкотканых структур. Уменьшение симптомов воспаления также снимает боль, и позволяет пациенту улучшить качество жизни. К счастью существует целая группа нестероидных противовоспалительных препаратов — НПВС, которые соединяют в себе и обезболивающие, и противовоспалительные свойства;
- уменьшение мышечного спазма, который развивается в глубоких мышцах спины в ответ на раздражающее влияние грыжи и формирует так называемый вторичный миофасциальный синдром.
Это такое состояние, когда в спине существует длительный, хронический источник боли, связанный с уплотненными мышцами. Эти уплотнения являются источником нарушенного кровообращения. Как известно, любая мышца может реагировать на боль и раздражение только одним известным ей способом — это резким сокращением. Грыжа вызывает постоянную боль, поэтому мышца находится в сокращении длительное время.
В результате сосуды, снабжающие мышцу кровью, сужаются, и от мышечной ткани затрудняется венозный отток. В мышцах накапливаются продукты обмена, в том числе и молочная кислота, и это приводит к вторичному хроническому спазму, формируя замкнутый круг. Такие уплотнения может легко обнаружить врач-невролог во время пальпации мышц спины. Они располагаются паравертебрально, то есть рядом с позвоночной линией справа и слева.
Обезболивание, противовоспалительные препараты, а также средства, снимающие хронический мышечный спазм (или миорелаксанты) и составляют три кита медикаментозного лечения межпозвонковых протрузий и грыж при их появлении и обострении.
Все эти препараты средства или лекарства (которые иногда не совсем правильно называют – медикаменты) в самом начале, при возникновении особо острой боли, применяются, как правило, парентерально, то есть в виде внутримышечных инъекций. Затем, обычно, через 3-4 дня, начинается переход на таблетированные формы, и присоединяется местное лечение. Пациенту назначается различные кремы, гели и мази, которые втираются или наносятся на необходимую область спины в проекции межпозвонковой грыжи, а также окружающих мышечных массивов.
Чем не лечат обострение протрузий и грыж
Сразу следует уточнить, что в Российской Федерации нет никакой возможности лечить даже очень сильную острую боль в спине, вызванную грыжей наркотическими анальгетиками, например с помощью накладывания пластыря Дюрогезик. То, что применяется в развитых странах, таких как США, Великобритания, Израиль, Чехия, где лечение грыж проводится по современным стандартам и с большой эффективностью, в России практически невозможно. Врач, назначивший при грыже Дюрогезик, по меньшей мере, рискует остаться без должности, а, в крайнем случае, обратить на себя пристальное внимание соответствующих органов.
Также не принято лечить межпозвонковые грыжи с помощью средств, которые называются спазмолитиками. Например, Баралгин или Но-шпа будут неэффективными, поскольку расслабляют в основном гладкую мускулатуру внутренних органов, и не имеют отношения к мышцам спины, хотя они обезболивают спазмы при желчнокаменной болезни.
Если на фоне боли в спине возникает лихорадка, то это, возможно, серьезный признак обострения пиелонефрита, наличия нетипичных форм холецистита и аппендицита с иррадиацией в спину, и других серьезных заболеваний.
Не лечат протрузии и грыжи, применяя различные ангиопротекторы, такие как пентоксифиллин, трентал и другие. Их задача — улучшать капиллярную микроциркуляцию при таких болезнях, как сахарный диабет, синдром Рейно и так далее. Поскольку межпозвонковые хрящи вообще лишены всяких сосудов, то их применять бессмысленно. А улучшать микроциркуляцию в спазмированных мышцах не имеет смысла, поскольку вначале следует снять мышечный спазм (применяя миорелакспнты), а дальше мышца сама справиться без дополнительных средств.
Перечень популярных и эффективных препаратов
Ниже перечислены лучшие популярные препараты для лечения острой боли в спине, вызванной в том числе, наличием протрузий и грыж межпозвонковых дисков. Вначале приводится международное непатентованное наименование (МНН), общее для всех коммерческих аналогов (или дженериков) этого лекарства. Затем — оригинальный препарат с этим МНН. Затем приводятся некоторые популярные дженерики.
Для каждого лекарства приводится средняя стоимость, актуальная для аптек всех форм собственности на территории Российской Федерации для конца июня 2019 года. Никакого рейтинга, занятия первых и последних мест не предусматривается.
Средства из группы НПВС
Препараты из группы НПВС обладают тремя важными лечебными качествами: они уменьшают воспалительный процесс, снижают боль и уменьшают лихорадку, или температуру. Последних качество при протрузиях и грыжах нас не интересует.
Важно знать, что все без исключения препараты НПВС имеют противопоказания, а наиболее старые средства первого поколения, такие как Диклофенак или Вольтарен, вообще нельзя применять дольше двух-трех дней. Все они способны обострять течение язвенной болезни желудка и двенадцатиперстной кишки, а в исключительных случаях вызывать даже язвенные кровотечения. Они приводят к обострению эрозивного гастрита, а при длительном бесконтрольном применении в течение нескольких недель могут привести к лекарственному токсическому гепатиту.
Мовалис, или оригинальный препарат мелоксикам, впервые полученный немецкой компанией Берингер Ингельхайм, является одним из лучших в своей группе. Кроме снятия острой боли в спине он показан при различных формах артритов, при болезненности суставов, при ревматологических заболеваниях, и при прочих воспалительных поражениях опорно-двигательного аппарата.
Мелоксикам оказывает сильное противовоспалительное действие, колоть его нужно по 1,5 мл внутримышечно ежедневно в течение 3 дней, Затем он применяется в таблетках, по одной таблетке 7,5 мг один раз в день. Но приём даже таблетированной формы не должен быть длительным. Лекарство противопоказано у пациентов с бронхиальной астмой, полипозом носа, при обострении эрозивного гастрита и язвенной болезни желудка, при тяжелой печеночной почечной недостаточности, в период беременности, грудного вскармливания, а также до 12-летнего возраста.
Выпускает Мовалис компания Берингер Ингельхайм, и упаковка из 3 ампул (для короткого курса) по 1,5 мл, в среднем, стоит 610 руб.
Препарат кетопрофен, представителем которого является Кетонал, также очень популярен, и выпускается не только в растворе для внутримышечного введения, но также и в виде геля для местного применения, который будет описан далее, в таблетках, а также в виде ректальных суппозиториев.
Показан кетопрофен при той же патологии с некоторыми изменениями: при артритах, обострении остеохондроза позвоночника — протрузиях и грыжах, при мигрени и головной боли, различных формах невралгии и радикулитах, при подагре, а также при послеоперационном болевом синдроме, в том числе и после микродискэктомии.
Внутримышечное введение предполагает по одной ампуле (100 мг) один-два раза в сутки, максимальная суточная доза — 2 ампулы. Препарат также обладает выраженным спектром противопоказаний. Кроме перечисленных выше противопоказаний к Мовалису, Кетонал нельзя применять при гемофилии, при декомпенсированной сердечной недостаточности. Его нельзя применять у детей до 15 летнего возраста. Стоит Кетонал, выпускаемый компанией Sandoz из Австрии 225 руб. за упаковку из 10 ампул.
Наконец, третий препарат, широко применяемый при протрузиях и грыжах — это диклофенак, и, пожалуй, самым чистым и высокоэффективным является оригинальный Вольтарен, производимый швейцарской компанией Novartis. Его стоимость составляет, в среднем, 260 руб. за упаковку из 3 ампул по 5 мл. Но есть и более доступные аналоги. Так, диклофенак, выпускаемой сербской компанией Хемофарм, будет стоить за ту же упаковку всего лишь 40 руб. Это говорит о высокой популярности этого препарата.
Вольтарен — эффективное обезболивающее: эффект наступает уже через 20-30 минут. Этот препарат также широко применяется при различных воспалительных и дегенеративных поражениях опорно-двигательного аппарата, при болевом синдроме в спине, при люмбаго, цервикалгии, ишиалгии, в том числе при протрузиях и грыжах. Также показан он при тяжелых приступах мигрени.
Внутримышечно его следует вводить глубоко, дозировка — один раз в день, а в случае особо тяжелой боли можно провести инъекции дважды в день, с промежутком в несколько часов. Рекомендуется применять как можно меньшую дозу, и как можно более коротким курсом лечения.
Миорелаксанты
Лечение острой боли в спине будет неполным без назначения миорелаксантов. Устраняя вторичный мышечный спазм, они улучшают кровообращение, и помогают уменьшить выраженность хронической боли в спине, которая часто в большей или меньшей степени сопровождает даже состояние ремиссии при протрузиях и грыжах.
Толперизон — оригинальный препарат Мидокалм, выпускает венгерская фармацевтическая компания Гедеон Рихтер, в упаковках по 5 ампул (1 мл). Кроме толперизона, в раствор добавлен лидокаин для облегчения боли, поскольку один толперизон является достаточно болезненным при внутримышечном введении. Стоит такая упаковка 475 руб.
Лидокаин относится к группе центральных мышечных релаксантов, и влияет на особые рефлексы спинного мозга. В результате рефлекторная готовность в ретикулоспинальном тракте уменьшается, и периферическое кровообращение в мышцах усиливается. Попутно толперизон обладает незначительным антиадренергическим и спазмолитическим эффектом.
Показан этот препарат при всех состояниях, при которых наблюдается спазм и повышенный тонус поперечно-полосатых мышц. Это не только острая и хроническая боль в спине, но также инсульт, рассеянный склероз, мышечная спастика при артрозах крупных суставов. Также он применяется в комплексном лечении после травматологических операций. Применять Мидокалм необходимо внутримышечно по одному миллилитру дважды в сутки. Противопоказан Мидокалм при тяжелых формах миастении, при беременности, кормлении грудью, а также в детском возрасте вплоть до 18 лет.
Сирдалуд выпускается только в таблетках, а это значит, что его нежелательно использовать в первые дни при особо сильном болевом синдроме. Его задача — мягкая, поддерживающая терапия в период затухающего обострения, когда боль уже не такая сильная, а вторичный миофасциальный синдром еще сохранен.
Сирдалуд производит заметный побочный эффект: его желательно не применять лицам, которые водят автомобиль, поскольку Сирдалуд вызывает сонливость, и очень часто. Но если он назначается тем, которым боль в спине мешают уснуть, то это довольно эффективное решение.

Нужно помнить, что Тизанидин следует отменять медленно, особенно в том случае, если лечение было длительное. Если его отменить резко, то у пациента может повыситься артериальное давление, и развиться приступ тахикардии. Если знать об этих особенностях препарата, то его можно применять при протрузиях и грыжах в течении 10-12 дней, а затем переводить пациента на аппаратную, или ручную физиотерапию и плавание. Выпускает Сирдалуд компания Novartis, и упаковка из 30 таблеток по 4 мг стоит 300 руб.
Местные средства для лечения острой боли в спине применяются очень широко. Это различные мази, кремы и гели, лечебные пластыри. Применять эти средства можно спустя 2-3 дня после возникновения острой боли в спине, когда интенсивность болевого синдрома стала снижаться вследствие терапии лекарственными препаратами. То есть в начале — инъекции, а затем вместе с таблетками можно назначать мази и кремы.
Почему это так? Дело в том, что среди мазей есть много представителей с согревающим эффектом. Например, Капсикам, содержащий капсаицин (экстракт кайенского перца) или мазь Финалгон. Если применять эти препараты сразу, то, напротив, отек будет усиливаться, поскольку они способствуют притоку крови к месту нанесения, а также и в глубокие ткани. Соответственно, усилится и выраженность болевого синдрома. А вот спустя несколько дней, когда интенсивность воспаления начнёт спадать и отечность рассасываться, тогда согревающие мази будут, напротив, своим притоком крови способствовать улучшению кровообращения в очаге и ликвидации болевого синдрома.
В первые дни появления очень острой боли, в принципе, можно пользоваться местными средствами, которые не согревают. Это охлаждающие мази и кремы, содержащие ментол и камфору, и другие. Для того чтоб не навредить себе случайно неправильным выбором — обязательно необходима консультация врача. Рассмотрим три характерных местных средства, применяемых при острой боли в спине, в том числе при протрузиях и грыжах. Это гель, мазь, и это особый согревающий пластырь.
Випросал В — это лечебная мазь, эффективными ингредиентами которой являются: живичный скипидар, салициловая кислота, камфора и яд гадюки. Эти ингредиенты подобраны очень удачно. Скипидар раздражает кожу и усиливает приток крови к коже от глубоких мышц, салициловая кислота расширяет сосуды, камфора обладает отвлекающим и охлаждающим эффектом. Яд гадюки улучшает реологические свойства крови и трофику тканей.

Показан Випросал В при различных формах невралгии, миозитах, а также при симптомах острой боли в спине. У этой мази довольно много противопоказаний. Так, нельзя ее применять в случае туберкулеза легких, склонности к возникновению сосудистых спазмов, детям, беременным и кормящим женщинам, при тяжелом нарушении функции печени и почек, и в некоторых других случаях.
На участок в проекции болезненности, наносят не больше, чем одну чайную ложку мази и втирают в кожу, не чаще, чем 2 раза в сутки. Продолжительность лечебного курса не должна продолжаться дольше двух недель без консультации врача. Выпускает Випросал В таллиннский химфармзавод (Эстония), одна туба массой 50 граммов стоит 286 руб.
Фастум-гель — это популярное, несогревающее средство, содержащее кетопрофен. По сути дела, это тот же самый Кетонал, только применяемый не в инъекциях, а местно. Его механизм действия также связан с противовоспалительным эффектом, который реализуется через ингибирование синтеза простагландинов. Кроме этого он обезболивает. Кроме остеохондроза, протрузий и грыж, он показан при ревматизме, подагре, различных травмах, таких как вывихи и растяжения, в случае тендовагинита, а также при тромбофлебите поверхностных вен. Положительные отзывы о нем дают не только неврологи, но и сосудистые хирурги.
Применять его необходимо, нанеся тонкий слой геля на кожу и слегка растереть, до 2 раз в сутки. Как и в прошлом случае, лечение не должно продолжаться более 2 недель. У Фастум-геля такие же противопоказания, как и у кетопрофена, но их меньше, ведь при местном применении он очень медленно всасывается в кровь, и практически не кумулирует в организме. Выпускает Фастум-гель итальянская группа Менарини, одна туба массой 50 грамм будет стоить 350 руб.
Этот пластырь является, по сути, не лекарственным веществом, а средством для домашней физиопроцедуры. В его состав входит железный порошок, активированный уголь, соль и вода. При соединении этих компонентов на одной поверхности (что происходит после удаления защитной пленки с пластыря) происходит его быстро разогревание до эффективной температуры 45 градусов. Это позволяет ему длительно прогревать необходимый участок поясницы на протяжении 10 часов.
Показан термопластырь при хроническом болевом синдроме в спине на стадии затихающего обострения при протрузиях и грыжах. Напомним, поскольку он согревает, то в первые дни применять его нельзя. У пластыря, несмотря на всю простоту сухого тепла, есть тоже множество противопоказаний. Но не имеет смысла их здесь описывать все полностью. Производит этот пластырь китайская компания под руководством Сандоз фармасьютикалз в Словении. Относительным минусом этого пластыря является его достаточно высокая цена. За одну упаковку из 10 полос, каждая из которых предназначено только для одноразового использования, следует заплатить 800 рублей.
В заключение следует сказать, что все эти средства должны назначаться только лечащим врачом в комплексе, в определённой последовательности, для того, чтобы скорейшим образом улучшить качество жизни, увеличить объем движений в спине и снять выраженный болевой синдром. Лекарственные препараты имеют противопоказания и побочные эффекты, поэтому все перечисленные в данной статье средства должны назначаться только лечащим врачом.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Высокая распространенность боли в спине, преимущественно в поясничном отделе позвоночника, обусловленной наличием межпозвонковых грыж в этом отделе, диктует необходимость глубокого изучения механизмов патогенеза данного заболевания с целью оптимизации профилактических и лечебных мероприятий. Грыжи поясничного отдела позвоночника и воспалительная реакция взаимосвязаны. На сегодняшний день считается, что воспаление обусловлено неблагоприятными симптомами, вызванными стимулированием нервных волокон, что приводит к появлению болевых ощущений. Однако воспаление также рассматривают как один из основных факторов регресса грыж поясничного отдела позвоночника. В статье рассмотрены молекулярные и клеточные механизмы, участвующие в регрессе грыж поясничного отдела позвоночника, в т. ч. ремоделирование матрикса и неоваскуляризация. Особое внимание уделяется воспалительной реакции, наблюдаемой при грыжах поясничного отдела позвоночника, в частности роли моноцитов/макрофагов. Изучение вклада цитокинов и клеток иммунной системы в процесс дегенерации межпозвонковых дисков, воспалительной реакции и ноцицепции может помочь обнаружить потенциальные терапевтические мишени у пациентов с симптоматическим поражением межпозвонковых дисков, что, в свою очередь, позволит улучшить качество жизни данной категории больных.
Ключевые слова: грыжа поясничного отдела позвоночника, межпозвонковый диск, воспаление, макрофаги, моноциты.
Для цитирования: Ткачев А.М., Епифанов А.В., Акарачкова Е.С. и др. Роль воспаления в спонтанном регрессе грыж межпозвонковых дисков. РМЖ. Медицинское обозрение. 2019;7:30-33.
Inflammation contributes to the spontaneous regression of spinal disc herniation
A.M. Tkachev 1,2 , A.V. Epifanov 3 , E.S. Akarachkova 4 , A.V. Smirnova 1 , A.V. Iljushin 1 , D.S. Archakov 2
1 Sergey Berezin Medical Institute, Volgograd
2 Tkachev Medical Clinic, Volgograd
3 Doctor Epifanov Clinic, Samara
4 International Society for Stress “Stress under control”, Moscow
High prevalence of low back pain (predominantly, lumbar backache) resulting from herniated discs requires careful study of the pathogenesis of this disorder to improve preventive and therapeutic interventions. Lumbar disc herniation is associated with inflammation. Currently, inflammation is considered to be associated with unfavorable symptoms resulting from nerve ending stimulation which leads to pain. However, inflammation is also regarded as one of the key factors of the regression of lumbar disc herniation. The paper discusses molecular and cellular mechanisms involved in the regression of lumbar disc herniation including matrix remodeling and neovascularization. Inflammatory response in lumbar disc herniation and, in particular, the role of monocytes and macrophages are highlighted. Investigati on of cytokine and immune cell contribution to intervertebral disc degeneration, inflammation, and nociception may provide potential therapeutic targets in patients with symptomatic disc herniation. As a result, their quality of life will be improved.
Keywords: lumbar disc herniation, intervertebral disc, inflammation, macrophages, monocytes.
For citation: Tkachev A.M., Epifanov A.V., Akarachkova E.S. et al. Inflammation contributes to the spontaneous regression of spinal disc herniation. RMJ. Medical Review. 2019;7:30–33.
В статье рассмотрены молекулярные и клеточные механизмы, участвующие в регрессе грыж поясничного отдела позвоночника, в т. ч. ремоделирование матрикса и неоваскуляризация. Особое внимание уделяется воспалительной реакции, наблюдаемой при грыжах поясничного отдела позвоночника.
Введение
Основной причиной боли в поясничном отделе позвоночника являются грыжи межпозвонковых дисков (МПД), которые наблюдаются примерно у 9% людей во всем мире [1]. При проведении диагностических нейровизуализационных исследований бессимптомные межпозвонковые грыжи (МПГ) обнаруживаются у 30–40% населения [2]. Грыжи поясничного отдела позвоночника обычно связывают с разрывом фиброзного кольца (ФК), выпадением студенистого ядра (СЯ) и стимуляцией нервных волокон, что приводит к появлению болевых ощущений. Однако в своем недавнем исследовании S. Rajasekaran et al. (2013) предположили, что МПГ чаще всего являются результатом повреждения замыкательных пластинок, а не разрыва ФК [3].
Предполагают, что основным молекулярным механизмом грыжи МПД является аномальное образование провоспалительных молекул, секретируемых СЯ и ФК, а также макрофагами, Т-лимфоцитами и нейтрофилами [4, 5]. Эти цитокины запускают спектр патологических клеточных реакций, включая аутофагию, старение и апоптоз [6, 7]. Регистрируется секреция таких провоспалительных медиаторов, как фактор некроза опухоли-альфа (TNF-α), ИЛ-1α/β, ИЛ-6, ИЛ-17, ИЛ-8, ИЛ-2, ИЛ-4, ИЛ-10, интерферон-гамма (IFN-γ), хемокины, простагландин E2 (PGE2) [8]. Показана роль TNF-α в образовании грыжи дисков, раздражении и прорастании нервных окончаний [9, 10], кроме того, TNF-α и ИЛ-1β вызывают активацию генов, кодирующих ферменты, разрушающие внеклеточный матрикс [11]. Продемонстрировано увеличение экспрессии ИЛ-1β и ИЛ-1R в ткани диска, подвергшегося дегенерации. В процессе дегенерации отмечается значительное увеличение уровня матриксных металлопротеиназ (MMP)-1, -3, -7, -9 и -13 и ADAM-протеаз (ADAMTS) -1, -4, -5, -9 и -15 в СЯ, что ставит вопрос о роли регуляции этих протеолитических ферментов в процессе заболевания [12].
Методы лечения МПГ и дегенеративного заболевания МПД в целом можно разделить на две группы: консервативные и хирургические. Лечение пациентов с секвестрированным видом МПГ на начальном этапе может проводиться консервативно в связи с более высокой вероятностью и скоростью рассасывания грыжи [13, 14]. Пациенты с некупируемой болью, неврологическими расстройствами или нарушениями функции кишечника либо мочевого пузыря являются кандидатами на проведение раннего хирургического вмешательства. Однако пока еще трудно прогнозировать, какие пациенты получат пользу от консервативного лечения [15] и у кого выше вероятность спонтанного регресса МПГ.
Механизмы спонтанного регресса МПГ
В настоящее время существует три теории, объясняющие резорбцию грыжевого материала. Согласно первой фрагменты грыжевого диска уменьшаются в размере из-за постепенного обезвоживания и сжатия, что может объяснить уменьшение интенсивности сигнала на МРТ [18]. По другой гипотезе напряжение, влияющее на заднюю продольную связку, приводит к ретракции фрагмента диска обратно в межпозвонковое пространство. Этот механизм может объяснить те случаи, когда ФК грыжевого диска остается нетронутым, но это не объясняет варианты с полным пролапсом МПД или миграцией фрагментов диска [14]. Третья теория заключается в том, что постепенная резорбция грыжи через деградацию ферментов и фагоцитоз индуцируется реакцией воспаления и неоваскуляризацией [19, 20]. Такая воспалительная реакция предположительно запускается, когда содержимое МПД попадает в эпидуральное пространство и организм воспринимает его как нечто чужеродное. Относительно каждого отдельного клинического состояния есть вероятность, что один конкретный механизм или комбинация трех механизмов приводит к спонтанному регрессу грыжевой ткани МПД.
Неприкосновенный иммунитет МПД. МПД — это самый большой аваскулярный орган в теле человека, который считается иммунологически привилегированным [21]. СЯ особенно сильно изолировано от иммунной системы, учитывая его расположение между двумя хрящевыми замыкательными пластинками и внутри плотной коллагеновой фиброзной структуры ФК. Кроме этого физиологического барьера, клетки МПД также активно противостоят вторжению иммунных клеток за счет экспрессии Fas-лиганда (FasL) [22]. FasL принадлежит семейству TNF, и известно, что он индуцирует апоптоз, связываясь со своим рецептором Fas. Хотя Fas экспрессируется в самых разных клетках, экспрессия FasL ограничена поверхностью цитотоксических Т-лимфоцитов, естественных NK-клеток, опухолевых клеток и стволовых клеток некоторых иммунологически привилегированных областей. Иммунологически привилегированная область клеток студенистого ядра — это основа теории о воспалительной реакции, способствующей резорбции МПГ. По данной теории экструзия СЯ в эпидуральное пространство запускает аутоиммунную реакцию, что приводит к инфильтрации иммунными клетками, которые вступают во взаимодействие с клетками МПД и вырабатывают разные молекулы, инициируя процесс резорбции грыжи [23].
Факторы нейрональной сенситизации могут включать рекрутмент цитокинов в области воспаления иммуномодулирующими клетками, в т. ч. сателлитные клетки глии или шванновские клетки, а также резидентные макрофаги [24]. В связи с тем, что в процессе эмбриогенеза с момента образования ткани СЯ отделены от кровотока [25] и не взаимодействуют с иммунной системой, при возникновении грыжи активируется иммунологически опосредованная воспалительная реакция [26]. Предполагается участие различных модуляторов и/или каскадов иммунологически опосредованного воспаления. В пользу этого свидетельствует клиническая эффективность иммуносупрессантов широкого спектра, таких как стероиды, а также результаты исследований, указывающих на более эффективное облегчение болевого синдрома при применении доксициклина, влияющего на экспрессию нескольких цитокинов, по сравнению с блокадой специфическими провоспалительными цитокинами [27].
Макрофаги как ключевые участники регресса МПГ. Макрофаги считаются самыми важными участниками процесса резорбции МПГ [28, 29]. Эти клетки обладают способностью активно фагоцитировать грыжевую ткань в лизосомы, заполненные коллаген-деградирующими ферментами. Макрофаги также выделяют ферменты лизосом посредством экзоцитоза, после чего они расщепляют межклеточные вещества, такие как компоненты матрикса диска (протеогликаны и коллагены) [30].
Рекрутинг моноцитов в ткань МПД. Точный механизм рекрутинга моноцитов в МПД остается пока неясным [31], однако известно, что МПД включает в себя клетки, подобные воспалительным (например, клетки с фагоцитарной способностью), и они способны продуцировать медиаторы воспаления [31], которые могут инициировать рекрутинг других иммунных клеток в область, пораженную грыжей. В частности, моноцитарный хемоаттрактантный белок-1 (MCP-1), хемокин подсемейства CC, способствует активизации и рекрутингу моноцитов [32, 33]. Инфильтрирующие макрофаги моноцитарного происхождения также продуцируют MCP-1, усиливая рекрутинг моноцитов в МПД. Кроме макрофагов в резорбции МПГ также участвуют плазмоцитоидные дендритные клетки [34]. Дендритные клетки преобладают над макрофагами при секвестрации транслигаментозного типа, что указывает на то, что они могут участвовать в инициации иммунной реакции [34].
Воспалительные каскады в МПГ. В ходе многочисленных исследований проводился анализ медиаторов иммунного ответа при МПГ, особое внимание уделяли роли макрофагов, участвующих в регрессе МПГ. Так, M.F. Shamji et al. [29] продемонстрировали высокий уровень продуктов макрофагов (IL-4, IL-6, IL-12 и IFN-γ) в тканях МПД, пораженных грыжей. Результаты других исследований показали, что ткани МПД также могут спонтанно продуцировать другие молекулы, например хемокины IL-8 и MCP-1, основная функция которых заключается в хемотаксисе макрофагов и ангиогенезе [32]. Более того, J.D. Kang et al. [35] выявили, что диск, пораженный грыжей, выделяет в большом количестве матриксную металлопротеиназу, оксид азота, IL-6 и PGE2. Продукция IL-6 индуцируется, когда происходит сокультивирование клеток МПД и макрофагов [36]. В недавнем исследовании T. Takada et al. [37] показали, что сокультивирование клеток МПД и макрофагов повышает активность IL-8, PGE2 и циклооксигеназы 2. По результатам обоих исследований, вышеупомянутые биохимические медиаторы продуцируются преимущественно макрофагами.
Аутоиммунная реакция — это намного более сложный процесс, чем рекрутинг макрофагов и неоваскуляризация. В ткани МПД при грыжах присутствуют не только макрофаги, но и другие иммунные клетки. Исследования in vivo на животных моделях способствовали более полному пониманию иммунного ответа, связанного с регрессом МПГ. Спонтанный регресс МПГ был продемонстрирован на моделях крыс с поврежденным позвоночником [38–41]. В этом исследовании МПГ были индуцированы уколом иглы. Выяснилось, что размер образованной грыжи пропорционален калибру используемой иглы. Грыжи значительно уменьшились в объеме через 2–6 нед. после повреждения. Также было выявлено, что количество CD68+ макрофагов, а также апоптоз в ткани грыжи были пропорциональны ее объему. В другом исследовании животным вводили иглу, проникающую через заднюю продольную связку, и искусственно создавали МПГ в эпидуральное пространство. МПГ постепенно, в течение 12 нед. после операции, спонтанно уменьшились в размере. Клеточный инфильтрат, состоявший преимущественно из макрофагов, наблюдался на 3-й день. Иммуногистохимический анализ показал, что клетки МПД с грыжей продуцировали TNF-α и IL-1β на 1-й день и MCP-1 на 3-й день.
Подтверждено наличие T- и B-лимфоцитов в изолированных МПД человека, пораженных грыжей [39]. В грыжевых тканях МПД человека при секвестрированных грыжах было обнаружено в 3 раза больше лимфоцитов, чем при экструзии диска, при которой не наблюдалось никаких других воспалительных клеток, кроме макрофагов [40–43]. В другом исследовании воспалительный инфильтрат характеризовался иммунным окрашиванием тех областей дисков с грыжей, на которых была проведена операция [41–44].
Роль неоваскуляризации в резорбции МПГ. Проведенные к настоящему моменту исследования доказывают, что механизм резорбции МПГ связан с каскадом воспаления, ремоделированием матрикса и ангиогенезом. Однако исследований, посвященных роли неоваскуляризации, проведено недостаточно. Обычно в МПД взрослого человека содержится мало кровеносных сосудов. Однако главным, определяющим фактором спонтанного регресса МПГ считается рост новых сосудов, который наблюдается на внешнем крае грыжевой ткани [42]. Было выдвинуто предположение, что в неоваскуляризации МПГ участвуют несколько молекулярных медиаторов, в т. ч. TNF-α, фактор роста эндотелия сосудов (VEGF) и основной фактор роста фибробластов (bFGF). Как упоминалось ранее, TNF-α может способствовать экспрессии VEGF, который играет важнейшую роль в образовании новых кровеносных сосудов, и некоторые исследования подтверждают присутствие VEGF и его рецепторов в тканях МПД, пораженных грыжей [43, 44]. Взаимодействие между макрофагами и тканями диска приводит к генерации воспалительных цитокинов, а как известно, эти цитокины участвуют в индукции ангиогенеза. Результаты этих исследований подчеркивают важность взаимовлияния ангиогенеза и воспаления, что в конечном итоге приводит к регрессу МПГ.
Патогенез болевого синдрома при дегенерации МПД
Возникновение дискогенной боли связано с врастанием нервных волокон в ткани, не имеющие иннервации [45–47]. Этот процесс может регулироваться взаимодействием провоспалительных цитокинов и нейтрофилов, продуцируемых клетками диска и инфильтрирующими ткань иммунными клетками, а также рецепторами нейротрофинов и их модуляторов. В здоровом состоянии врастанию нервных волокон препятствует барьерная функция тканей диска, определяющаяся высокой концентрацией хондроитинсульфатного компонента аггрекана и других матриксных молекул, которые подавляют рост нервных окончаний. Следует отметить, что в процессе дегенерации отмечается увеличение отношения кератана сульфата к хондроитина сульфату. Протеолитическое расщепление аггрекана под воздействием цитокин-зависимой активности ADAMTS4/5 может способствовать прорастанию нервных волокон в ткани диска [48]. Кроме того, в норме во внешних слоях ФК отмечается высокий уровень экспрессии Sema3A (белка семейства семафорина 3 класса), который подавляет рост аксонов. У пациентов с дискогенной болью отмечается снижение уровня экспрессии этого белка, наряду с увеличением степени дегенерации, что позволяет предположить, что Sema3A может подавлять врастание нервных волокон в ткань диска.
Продемонстрирована прямая взаимосвязь врастания нервных волокон и кровеносных сосудов в ткани МПД, это позволило предположить, что для выживания нейронов и врастания их в ткань диска необходим фактор роста нервов (NGF), вырабатываемый эндотелиальными клетками [47]. Следует отметить, что СЯ и ФК характеризуются низким уровнем экспрессии NGF и нейротрофического фактора мозга (BDNF), а также рецепторов нейротрофина TrkA, TrkB и p75NGFR [49]. Кроме того, отмечается увеличение экспрессии нейротрофина в МПД при болевом синдроме и в стадии дегенерации [49, 50]. Таким образом, NGF в тканях МПД может не только участвовать во врастании нервных волокон, но и напрямую влиять на межпозвоночные ганглии и активировать экспрессию кислоточувствительных ионных каналов (ASIC3), pH-чувствительного Na + -канала, связанного с ишемическим и воспалительным болевым синдромом [31, 51]. Цитокины также могут влиять на межпозвоночный ганглий, способствовать апоптозу [52], а также усиливать экспрессию TrpV1, ноцицептивного катионного канала [53]. Следует отметить, что нервные волокна, иннервирующие МПД, относятся к ноцицептивным и происходят из межпозвоночного ганглия: они экспрессируют ацетилхолинэстеразу, белок PGP 9.5, субстанцию P, BDNF, TrpV1, пептид, кодируемый геном кальцитонина (CGRP), белок нейрофиламентов (NFP) [54, 55]. Имеющиеся данные указывают на прямую связь уровней провоспалительных цитокинов, нейротрофинов и ноцицепции.
Выводы
Дегенерация МПД — широко распространенное состояние во взрослой популяции, связанное со значительными социально-экономическими потерями. Необходимо пробовать разные нехирургические способы лечения, прежде чем назначать хирургическое вмешательство на острой стадии МПГ. Это не касается случаев, когда консервативное лечение противопоказано, например при неврологических расстройствах и боли, неутихающей несмотря на прием медицинских препаратов.
Очевидно, что воспалительная реакция, которая возникает в связи с образованием МПГ, играет немаловажную роль в ее спонтанной резорбции. Таким образом, воспаление в данном конкретном клиническом контексте является положительным прогностическим фактором, и мы не должны препятствовать этому процессу. Хирурги, проводящие операции на позвоночнике, признают этот феномен, и многие считают его полезным для консервативного лечения МПГ. Несмотря на сказанное, именно воспалительная реакция оказывает негативное влияние на прилегающие нервные корешки, вызывая боль. Контроль воспалительной реакции в этих условиях — это важная и сложная задача при лечении пациентов с МПГ. Нужны знания о биологических механизмах, лежащих в основе резорбции МПГ, и персонализированный подход, чтобы назначать оптимальное лечение каждому отдельному пациенту. Такой подход в конечном итоге может приводить к значительной экономии социально-экономических ресурсов.
Только для зарегистрированных пользователей
Читайте также:


