Дозы метилпреднизолона при спинальной травме
Данная статья "Фармакотерапия при травме спинного мозга" написана в 2017 г.. На основании 85 ссылок авторы обобщили имеющиеся знания о метилпреднизолоне, других стероидах, ганглиозидах, антагонистах опиатов, блокаторах кальциевых каналов, антиоксидантах и свободных радикалах. Хотя некоторые исследования на животных показали потенциальное улучшение при использовании этих препаратов, убедительных доказательств существенного улучшения неврологических функций для введения этих препаратов в рутинную практику получено не было.
Использование высоких доз метилпреднизолона (МП) было рекомендовано после публикации Braken et al. национального исследования острой травмы спинного мозга (NASCIS II и III), включая четыре статьи о 6-ти и 12-ти месячных исследованиях в 1990-1998 гг.
NASCIS II состоял из 24 часовой терапии: 30 мг/кг МП болюсно, плюс 5,4 мг/кг внутривенно в течение следующих 23 часов или 5,4 мг/кг налоксона болюсно и последующая 24-часовая инфузия в дозе 4 мг/кг против плацебо, не позднее 12 часов после травмы. У пациентов, получавших МП в течение 8 часов, неврологический статус был лучше, чем в группе плацебо.
Меньшее восстановление двигательных функций наблюдалось в группе 48ТМ при начале лечения от 3 до 8 часов после травмы, но пациенты группы 48МП показали лучшее восстановление через один год (баллы восстановления 13,7 и 19 соответственно, р=0,053).
Однако как заявили Casha et al. после прочтения опубликованных результатов NASCIS, репутация метилпреднизалона кажется не заслуженной: значимых улучшений функций у пациентов не было описано ни в одном из исследований, а риск смерти от респираторных осложнений был в 6 раз выше в группе 48МП по сравнению с группой 24МП (NB: 6 против 1 из 166 рандомизированных пациентов в группе).
Этот неблагоприятный эффект был упомянут et al., призывавших к осторожности, означающей отказ от ненужного назначения в течение 48 часов в тех случаях, когда есть возможность применения МП в течение 24 часов, т. е. с началом в первые три часа после травмы. МП влияет на перекисное окисление липидов и гидролитическую деструкцию нейронов и микрососудистой мембраны, и его положительный эффект утрачивается после 8 часов, после чего его действие связано с подавлением иммунной активности клеток и доминированием прорастания аксонов.
В 2002 г. 83% канадских спинальных хирургов назначали МП из-за давления коллег или страха перед судебными преследованиями, по сравнению с 17%, считавших, что он действительно эффективен.
Позже Fehlings заявил, что положительный эффект назначения МП скромнее, чем показал анализ испытаний NASCIS. Его критическое резюме NASCIS II включает:
• Общий анализ 487 пациентов
• Положительный эффект при анализе постфактум был у 193 пациентов, получавших лечение МП в течение 8 ч.
• Малый уровень эффективности
• Функциональное значение и влияние на длинные проводящие пути вызывает сомнения.
• Сомнения по поводу влияния МП на заживление ран и сепсис.
Его критика NASCIS III включала:
• Отсутствие группы плацебо.
• Отрицательный результат общего анализа.
• Влияние ограничено при оценке постфактум от 0 до 3 часов и от 3 до 8 часов.
• Умеренное улучшение (р=0,08) по одному из показателей (уход за собой, функция сфинктеров, мобильность, общение, социальное познание) (48 ч метипреднизолона (МП)).
• Повышение случаев развития сепсиса и пневмонии в группе 48 метипреднизолона (МП).
Несмотря на обоснованную критику, следует рассмотреть возможность применения этого препарата, учитывая последствия позвоночно-спинномозговой травмы (ПСМТ) и доказательства положительного эффекта метилпреднизолона. Показаниями к назначению МП являются:
• NASCIS II протокол для острой, непроникающей ПСМТ 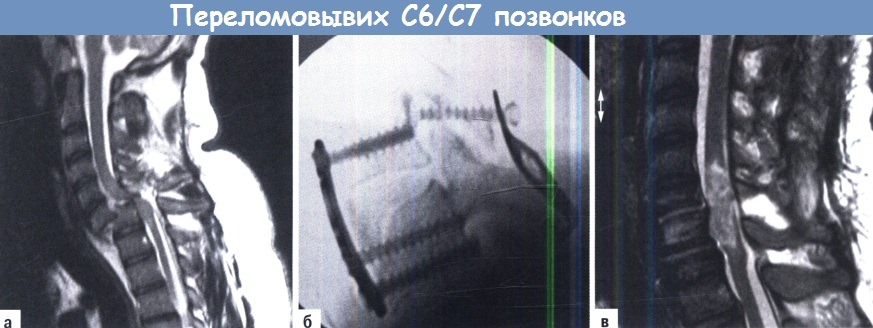
A-В. С6/С7 переломовывих с полным повреждением спинного мозга:
А. МРТ до удаления перелома.
Б. Ситуация после комбинированной процедуры: тракция и задняя редукция с фиксацией крюком Magerl, передняя дискэктомия, трансплантация и фиксация пластиной.
В. Послеоперационная МРТ, Т2-взвешенное изображение в сагиттальной проекции, показывающее степень повреждения спинного мозга.






На сколько я понимаю - философия введения метпреда в данной ситуации (как можно раньше) - минимизировать отек спинного мозга - мост к оперативному вмешательству. Если Вы живете на крайнем Севере или Ваши нейрохирурги из этого региона (здесь уж не географически конечно), то, наверное, целесообразности в метилпреднизолоне нет.
Теоритически Вы можете использовать другой ГКС, однако практически это не возможно - чтобы соблюсти эквивалентную дозу - уверен, что просто нет столько дексаметазона, преднизолона в вашей больнице
Я никогда не понимал тактики нейрохирургов, когда поступала спинальная травма + пневмония (аспирационная) и пациент на декомпрессионную операцию не брался - т.к. у него была пневмония - рекомендовалось лечение последний и через 2 недели (!) операция.
The National Acute Spinal Cord Injury Studies (NASCIS) II and III, a Cochrane review of all randomized clinical trials and other published reports, have verified significant improvement in motor function and sensation in patients with complete or incomplete SCIs who were treated with high doses of methylprednisolone within 8 hours of injury. The NASCIS II study evaluated methylprednisolone administered within 8 hours of injury. The NASCIS III study evaluated methylprednisolone 5.4 mg/kg/h for 24 or 48 hours versus tirilazad 2.5 mg/kg q6h for 48 hours. (Tirilazad is a potent lipid preoxidation inhibitor.) High doses of steroids or tirilazad are thought to minimize the secondary effects of acute SCI. In the NASCIS III trial, all patients (n = 499) received a 30-mg/kg bolus of methylprednisolone intravenously. The study found that in patients treated earlier than 3 hours after injury, the administration of methylprednisolone for 24 hours was best. In patients treated 3-8 hours after injury, the use of methylprednisolone for 48 hours was best. Tirilazad was equivalent to methylprednisolone for 24 hours.Both NASCIS studies evaluated the patients' neurologic status at baseline on enrollment into the study, at 6 weeks, and at 6 months. Absolutely no evidence from these studies suggests that giving the medication earlier (eg, in the first hour) provides more benefit than giving it later (eg, between hours 7 and 8). The authors only concluded that there was a benefit if given within 8 hours of injury following the NASCIS trials.
The use of high-dose methylprednisolone in nonpenetrating acute SCI had become the standard of care in North America. Nesathurai and Shanker revisited these studies and questioned the validity of the results. These authors cited concerns about the statistical analysis, randomization, and clinical endpoints used in the study. Even if the benefits of steroid therapy are valid, the clinical gains are questionable. Other reports have cited flaws in the study designs, trial conduct, and final presentation of the data. The risks of steroid therapy are not inconsequential. An increased incidence of infection and avascular necrosis has been documented.
A number of professional organizations have therefore revised their recommendations pertaining to steroid therapy in SCI. The Canadian Association of Emergency Physicians is no longer recommending high-dose methylprednisolone as the standard of care. The Congress of Neurological Surgeons has stated that steroid therapy "should only be undertaken with the knowledge that the evidence suggesting harmful side effects is more consistent than any suggestion of clinical benefit." The American College of Surgeons has modified their Advanced Trauma Life Support guidelines to state that methylprednisolone is "a recommended treatment" rather than "the recommended treatment."
In a recent survey conducted by Eck and colleagues, 90.5% of spine surgeons surveyed used steroids in SCI, but only 24% believed that they were of any clinical benefit. Note that the authors discovered that approximately 7% of spine surgeons do not recommend or use steroids at all in acute SCI. The authors reported that most centers werefollowing the NASCIS II trial protocol.
Overall the benefit from steroids is considered modest at best, but for patients with complete or incomplete quadriplegia, a small improvement in motor strength in one or more muscles can provide important functional gains.
The administration of steroids remains an institutional and physician preference in spinal cord injury. Nevertheless, the administration of high-dose steroids within 8 hours of injury for all acute SCI patients is practiced by most physicians.
The current recommendation is to treat all SCI patients according to the local/regional protocol. If steroids are recommended, they should be initiated within 8 hours of injury with the following steroid protocol: methylprednisolone 30 mg/kg bolus over 15 minutes and an infusion of methylprednisolone at 5.4 mg/kg/h for 23 hours beginning 45 minutes after the bolus.
Local policy will also determine if the NASCIS II or NASCIS III protocol is to be followed.
Two North American studies have addressed the administration of GM-1 ganglioside following acute SCI. The available medical evidence does not support a significant clinical benefit. It was evaluated as a treatment adjunct after the administration of methylprednisolone.
Активность корикостероидов обычно сравнивается с преднизолоном.
Метилпреднизолон.
По противовоспалительной активности превышает гидрокортизон в 5 раз, практически не обладает минералокортикоидной активностью.
Дексаметазон.
По противовоспалительной активности превышает гидрокортизон в 30 раз, не обладает минералокортикоидной активностью.
Преднизолон.
По сравнению с гидрокортизоном противовоспалительная активность преднизолона в 4 раза больше, минералокортикоидная активность в 0.6 раза меньше.
Триамцинолон.
По противовоспалительной активности в 6 раз активнее гидрокортизона, минералокортикоидная активность практически отсутствует.
Данные по эффективности/неэффективности кортикостероидов при спинальной травме весьма противоречивы. В некоторых странах от него отказались, в некоторых – нет.
Метилпреднизолон приблизительно в два раза активнее обычного преднизолона, т.е доза должна быть увеличена в два раза.






всем спасибо за ответы.

alpeli (5.3.2009, 13:10) писал:
Метилпреднизолон.
По противовоспалительной активности превышает гидрокортизон в 5 раз, практически не обладает минералокортикоидной активностью.
Преднизолон.
По сравнению с гидрокортизоном противовоспалительная активность преднизолона в 4 раза больше, минералокортикоидная активность в 0.6 раза меньше.
получается преднизолон : метилпреднизолон = 1 : 1,25






коллеги, а какова тактика ведения таких больных в вашем стационаре?
что с оперативным лечением такого контингента?

Sergei (5.3.2009, 12:47) писал:
Эквивалентные дозы стероидов
При отсутствии метипреда, тогда уж лучше декс используйте - нет минералокортикоидного эффекта (вам-то нужен только противоотёчный)
Важно ВСЕМ больных с травмой лечить как с потенциально нестабильным шейным отделом, until proven otherwise
Проблемы возникают с больными в коме - когда снимать ошейник? 100%-ного соглашения по этому поводу нет - пример рекомендаций
На этой странице - разные рекомендации по лечению спинальных больных из нашего регионального спинального центра в Salisbury. Кликабельно



Эльдар (5.3.2009, 19:06) писал:
коллеги, а какова тактика ведения таких больных в вашем стационаре?
что с оперативным лечением такого контингента?

Эльдар (5.3.2009, 2:10) писал:

alpeli (5.3.2009, 19:25) писал:
Источник я нашел – одна из наших книг по травме. Но, конечно, это не правильно. Приношу извинения.
За все годы работы только у трех больных со спинальной травмой я назначал высокие дозы стероидов. Впрочем, без видимого эффекта. В настоящее время рутинно назначаем магния сульфат – из серии: вдруг поможет, хуже не будет. В опытах на животных в свое время были получены весьма обнадеживающие результаты.
Но наиболее перспективным в плане фармакопротекции мне представляется назначение достаточно больших доз прогестерона. Но это в будущем – пока такие работы на людях, насколько я знаю, не выполнялись.

zubarew (15.3.2009, 7:06) писал:
Известно, что в дополнение к первичному повреждению спинного мозга непосредственно в результате травмы, развивается замедленный аутодеструктивный процесс, последствия которого еще более катастрофичны. Механизмы патофизиологического ответа на первичную травму и осуществление регулируемого контроля за аутодеструктивными процессами в спинном мозге являются предметами интенсивного изучения.
Существуют две теории, пытающиеся объяснить концепцию вторичного повреждения спинного мозга: сосудистая и нейрональная.
Согласно сосудистой теории, снижение или остановка кровотока вследствие повреждения эндотелия сосудов микроциркуляторного русла и образование тромбов приводят к ишемии в центральном сером веществе. Утрачивается сосудистая ауторегуляция, следствием чего является ишемия в белом веществе. Ишемические процессы захватывают несколько смежных сегментов спинного мозга. Кроме этого, присоединяются общие сосудистые эффекты острой травмы — артериальная гипотензия и снижение сердечного выброса, что усугубляет ишемические процессы в зоне травмы.
Нейрональная теория аутодеструктивных процессов предполагает травматическое повреждение цитоплазматической мембраны аксона с образованием каскада вторичных повреждений.
Ведущая роль в механизме клеточного повреждения отводится ионам кальция. Повреждение липопротеидов клеточных мембран сопровождается резким увеличением трансмембранного потока кальция и повышение его внутриклеточной концентрации в нейронах и клетках глии. Неконтролируемый приток кальция вызывает вазоспазм, высвобождается большое количество арахидоновой кислоты, которая также разрушает клеточную мембрану или метаболизируется с образованием, в том числе и свободных радикалов, они либо прямо разрушают анатомические структуры спинного мозга, либо усиливают агрегацию тромбоцитов и вазоспазм.
Независимо от того, развивается ли цепь реакций в соответствии с нейрональной или сосудистой теорией, необходима своевременная коррекция гипоперфузии и обеспечение стабилизации клеточных мембран — это и является главными целями раннего терапевтического вмешательства.
Коррекция посттравматической гипотензии преследует цель восстановления среднего артериального давления до нормотензивного уровня, чтобы предотвратить развитие вторичных интрамедуллярных кровоизлияний. Это достигается с помощью сосудорегупирующих препаратов, одним из важных в этом ряду является допамин, его применяют по 5 - 6 мг в сутки.
Одним из самых главных достижений в лечении спинномозговых повреждений последних лет является применение метилпреднизолона.
Программа NASCIS-2 (Национальные Исследования Острых Травм Спинного Мозга), проведенная с 1985 по 1988 годы в десяти нейрохирургических центрах США, позволила сделать выводы, что у больных с поврежденным спинным мозгом метилпреднизолон при его применении по рекомендуемой методике:
способствует восстановлению 20% утерянных двигательных функций у больных с параличами;
способствует восстановлению 75%-удерянных моторных .функций у больных с парезами. (В группе больных, леченных плацебо, параличи восстановились у 8%, а парезы - у 59% наблюдаемых).
Действие метилпреднизолона заключается в том, что он:
ингибирует перекисное окисление липидов, вызываемое свободными радикалами;
ингибирует гидролиз липидов;
поддерживает кровоснабжение ткани спинного мозга и аэробный энергетический метаболизм;
улучшает выведение из клетки кальция;
усиливает возбудимость нейронов и проведение импульсов.
Метилпреднизолон в виде водорастворимой лекарственной формы SOLU-MEDROL вводится внутривенно в дозе 30 мг/кг веса больного в течение первых 15 мин, затем через 45 мин препарат вводится в дозе 5,4 мг/кг/h в течение последующих 23 часов. Препарат эффективен, если его вводить только в первые 8 часов после травмы.
Solu-medrol рекомендуют применять даже при сочетанных повреждениях, несмотря на риск вторичных кровотечений и образования язв, т.к. соотношение пользы и риска весьма велико. Относительным противопоказанием является наличие сильно загрязненных ран.
Вот как, к примеру, оценивается результат применения метилпреднизолона в остром периоде травмы у больных с грубым повреждением шейного отдела спинного мозга: восстанавливается в среднем 12-15 двигательных баллов, а, как известно, разница в три балла во флексорах кисти — это разница между способностью и неспособностью самостоятельно есть.
Несмотря на высокую стоимость препарата, следует учитывать, что применение других видов терапии может стоить значительно дороже, а уменьшение потери неврологического дефицита на 12 - 15% позволит нивелировать эти расходы.
С целью преодоления нежелательного системного действия стероидов предприняты попытки синтезировать аналоги метилпреднизолона, у которых нет этого отрицательного эффекта. Создана группа лазароидов, которые превосходят solu-medrol по своей аитиоксидантной активности. Приступили к клиническим испытаниям тирилазада мезилата, который в эксперименте себя зарекомендовал с очень хорошей стороны.
Кроме медикаментозного, благоприятное воздействие на течение травмы оказывает локальная гипотермия, назначением которой является локальное снижение метаболизма и потребления кислорода в тканях спинного мозга, что приводит к уменьшению отека и блокированию биохимического каскада вторичных повреждений.
Гипотермия является необходимым компонентом при проведении операций по декомпрессии спинного мозга, она наиболее эффективна в остром периоде в первые 8 часов после травмы. Осуществить гипотермию можно как с помощью специальных устройств, в которых охлаждается физиологический раствор до необходимой температуры, так и с помощью примитивно замороженного физиологического раствора и разовой капельницы, через которую в момент операции на обнаженный спинной мозг подается капельно или струйно оттаявшая жидкость, имеющая температуру 4-7°С; экспозиция — не менее 40 минут.
В раннем периоде, особенно после декомпрессии спинного мозга, положительное воздействие оказывает гипербарическая оксигенация, которая позволяет компенсировать сниженную спинальную перфузию повышением уровня кислорода в крови.
Одним из самых грозных осложнений или проявлений травмы спинного мозга являются дыхательные нарушения. Возникающие в остром периоде травмы спинного мозга, они в значительной степени обуславливают тяжесть состояния больных и нередко становятся причиной смерти. Выраженность и характер нарушений дыхания зависят от уровня, тяжести спинномозговых повреждений, а также от времени, прошедшего после травмы.
Функция дыхания при травме шейного отдела спинного мозга страдает по двум причинам: во-первых, денервированные межреберные мышцы не в состоянии обеспечить нормальные движения грудной клетки, во-вторых, при повреждении диафрагмального центра на уровне CIV нарушается экскурсия диафрагмы.
При повреждении спинного мозга выше CIV сегмента дыхательные расстройства становятся угрожающими по обеим причинам; при поражении ниже этого уровня значительно снижается жизненная емкость легких. Поэтому больным в первую очередь требуется нормализовать функцию дыхания, для этого приходится прибегать к ИВЛ, которую лучше всего производить через трахеостому, поскольку интубация больных с травмой шейных позвонков через естественные пути противопоказана из-за возможности вторичного смещения позвонков.
Трахеостому следует наложить еще и потому, что быстрым вторичным осложнением травмы шейного отдела спинного мозга является присоединение пневмонии. Через трахеостомическое отверстие легче санировать трахео-бронхиальные пути, производить бронхоскопию, проводить наркоз во время оперативных вмешательств.
Больным с травмой спинного мозга в обязательном порядке с первых дней назначают антибактериальную терапию; сразу используются антибиотики широкого спектра действия превентивно, либо их следует подбирать с учетом чувствительности микрофлоры.
Хорошо зарекомендовали себя в последние годы фторхинолоны — ципрофлоксацин (ципробай, цифран), офлоксацин, темафлоксацин и др. Для спинальных больных ципробай (ципрофлоксацин, фирма Вауег) предпочтителен еще и потому, что это самый сильный антибиотик для лечения инфекций мочевыводящих путей, поскольку именно в моче обнаруживается его наибольшая концентрация, даже после перорального применения.
Для лечения инфекций дыхательных путей ципробай применяют по 200 мг внутривенно 2 раза в день, для лечения инфекций мочевыводящих путей можно применять по 250 мг 2 раза в день перорально. Курсы лечения составляют 7—14 дней. Основным условием высокой эффективности действия препарата является обеспечение нормального пассажа мочи.
Кроме расстройств дыхательных функций травма спинного мозга вызывает выраженные изменения в деятельности сердечно-сосудистой системы. Чаще всего это наблюдается при поражении шейных сегментов, но и при более низких локализациях у больных может наблюдаться стенокардитический синдром, часто развивается ортостатический коллапс, нарушается сердечный ритм, возникает миокардиодистрофия с недостаточностью кровообращения различной степени выраженности, нередки ишемия миокарда и кардиопульмональная недостаточность, выражающаяся в отеке легких. Больные могут погибать от внезапной остановки сердца. Важно вовремя диагностировать эти изменения и проводить симптоматическую терапию.
Практически у всех спинальных больных обнаруживаются изменения показателей функционального состояния печени, и как следствие, нарушение белкового обмена. В сыворотке крови наблюдается либо гипопротеинемия, либо при нормальном содержании белка изменяется его фракционный состав в стороны уменьшения альбуминов и возрастания глобулинов. Если у таких больных возникают гнойновоспалительные осложнения, то фракционные белковые сдвиги становятся еще более выраженными. Коррекцию этих состояний проводят с помощью введения 25% альбумина, нативной или замороженной плазмы.
Наблюдаются серьезные нарушения в системе свертывания крови, которые выражаются в повышенной кровоточивости из пролежней, мочевого пузыря и почек, тромбоэмболии легочной артерии и др. Это связано с гиперфибриногенемией и снижением толерантности плазмы к гепарину. Особенно высоко содержание фибриногена в крови, взятой из сосудов парализованных конечностей; выраженность этих коагулопатий тем больше, чем выше поражение спинного мозга.
С целью профилактики тромбоэмболических осложнений необходима антикоагулянтная терапия гепарином по 2,5 тыс ЕД 4 раза в день в течение 3 — 5 дней, антифибринолитическая терапия эпсилон-аминокапроновой кислотой.
Кроме вышеперечисленных происходят грубые изменения функции надпочечников, уменьшается количество вырабатываемого ими гормона 17-кетостероидов; резко снижается иммунитет; нарушается кислотно-щелочное состояние и т.д. Все эти патологические ситуации требуют коррекции, которую приходится проводить не только в остром, но и в течение всех периодов травматической болезни спинного мозга.
Несмотря на то, что одним из неблагоприятных осложнений травмы спинного мозга является его отек, нельзя допускать гиповолемии, которая в условиях депонирования крови в паретичных конечностях может привести к грубым расстройствам кровообращения. Спинальный больной должен получать не меиее 2,5 л жидкости в день и столько же выделять. В лечении должны использоваться низкомолекулярные декстраны.
Царенко С.В., НИИ скорой помощи им. Н.В.Склифосовского, Москва.
В силу ряда не до конца выясненных причин психологического порядка существуют четыре проблемы, вызывающие неизменный интерес реаниматологов, занимающихся лечением поражений и заболеваний нервной системы:
- Когда и кому производить трахеостомию?
- Есть ли лекарства, ускоряющие восстановление функций мозга?
- Не оказывает ли негативного действия на мозг глюкоза?
- Надо ли применять кортикостероиды?
Последняя проблема является последней только по списку, но не по значению. Имеется много предпосылок к применению кортикостероидов для лечения и предупреждения отека мозга. Теоретически возможна стабилизация мембран нейронов, что приводит к предупреждению проникновения жидкости внутрь клетки и выхода из нее лизосомальных ферментов. Кроме того, кортикостероиды могут подавлять избыточную активацию воспалительного цитокинового каскада, развивающегося вследствие некроза ткани мозга. Давно известно, что большие дозы этих препаратов эффективно уменьшают вазогенный отек, возникающий вокруг опухолей и абсцессов мозга (6).
Существует огромное количество экспериментальных данных и клинических наблюдений, свидетельствующих о возможных перспективах кортикостероидной терапии при тяжелой церебральной и спинальной травме, а также при сосудистой патологии мозга. Перечисление только авторов и названий этих работ заняло бы не одну страницу. Однако если быть объективным, то исследований, убедительно доказывающих положительную роль стероидов при указанной патологии, не существует. Все экспериментальные работы к разряду клинических доказательств не относятся. Большинство клинических исследований, указывающих на эффективность кортикостероидов у нейрохирургических больных, тоже не выдерживают критики, так как выполнены на небольших группах больных, часто с большими проблемами в дизайне работы и в статистической обработке полученных данных. Среди клинических работ наибольшего внимания заслуживают только несколько многоцентровых исследований, выполненных на хорошем методологическом уровне. Рассмотрим подробнее результаты работ, посвященных применению кортикостероидов при спинальной и черепно-мозговой травме. Многоцентровых исследований эффективности кортикостероидов при сосудистой патологии мозга не проводилось.
Наиболее масштабными работами по использованию кортикостероидов при спинальной травме являются исследования NASCIS II и NASCIS III. В обеих работах проводили лечение пострадавших со спинальной травмой большими дозами метилпреднизолона (30мг/кг – в первый час с последующей постоянной инфузией в течение 23 часов со скоростью 5,4 мг/кг ч). В первом исследовании (2) сделан вывод, что такое лечение приводило к улучшению отдаленных функциональных исходов по сравнению с пациентами, которые получали плацебо. Условием эффективности терапии было введение начальной дозы кортикостероидов не позже, чем через 8 часов после травмы. При введении начальной дозы в период от 8 до 12 часов эффекта метилпреднизолона не было. Серьезных осложнений кортикостероидной терапии не отмечено.
В исследовании NASCIS III (3) сравнивали введение тех же доз метилпреднизолона в течение 24 часов и 48 часов, а также стероидного производного тирилазада мезилата в течение 48 часов. Лечение начинали в течение 8 часов после спинальной травмы. Исследование имело практически те же проблемы, что и NASCIS II. Лучшие результаты получили, если лечение проводили в первые 3 часа по сравнению с интервалом 3-8 часов. Осталось неясной также существенность для больных полученных положительных результатов.
При черепно-мозговой травме (ЧМТ) вера врачей в кортикостероиды оказалась настолько велика, что не хватило нескольких исследований I класса (1, 4, 7, 9), чтобы ее разрушить. Во всех проведенных работах было показано, что отрицательные эффекты кортикостероидов нивелируют все их возможные положительные воздействия. Негативное влияние было связано с увеличением частоты септических осложнений из-за угнетения иммунитета, с нарастанием числа желудочно-кишечных кровотечений вследствие увеличения частоты стрессовых эрозий желудка и двенадцатиперстной кишки, а также с развитием гипергликемии.
Несмотря на убедительные результаты, по данным различных опросов от 14 до 64% травматологических центров в Великобритании и США продолжали использовать кортикостероиды при повреждениях мозга. Для окончательного решения этого вопроса было предпринято беспрецедентное по своим масштабам рандомизированное проспективное исследование I класса, посвященное по сверхраннему применению кортикостероидов при черепно-мозговой травме, CRASH (5). В исследовании приняло участие 239 госпиталей в 49 странах. Предполагалось набрать около 20000 больных! В исследование были включены только больные, которым по оценке лечащего врача, возможно, были показаны кортикостероиды в первые 8 часов после травмы. Если, по мнению врача, больной точно нуждался в кортикостероидах или, наоборот, он в них не нуждался, его в исследование не включали. Пациенты случайным образом были разделены на основную и контрольную группы. В основной группе в течение часа вводили 2 г метилпреднизолона и далее в течение 24-48 часов продолжали постоянную инфузию этого препарата со скоростью 0,4 г в час. Пациенты контрольной группы получали плацебо. Исследование пришлось в мае 2004 года прервать после того, как были проанализированы результаты лечения 10008 больных. Летальность к концу 2 недели после травмы в основной группе составила 21,1%, тогда как в контрольной группе – только 17,9%. Относительный риск лечения составил 1,18 при 95% доверительном интервале 1,09 – 1,27 (р = 0,001). Результаты лечения кортикостероидами были хуже во всех проанализированных подгруппах больных: при разной тяжести состояния и с разными сроками начала лечения. Самая большая разница в летальности была при относительно позднем начале лечения (от 3 до 8 часов) и среди пациентов с тяжестью состояния 12 и ниже баллов по шкале комы Глазго.
Причина повышения летальности осталась неясна, так не зарегистрировано увеличения числа септических и геморрагических осложнений.
Список литературы.
Читайте также:


