Что такое неспецифические боли в спине
О статье
- О статье
- Резюме
- Abstract (eng)
Ключевые слова: боль в спине, дегенеративно-дистрофическое поражение позвоночника, спондилоартроз, нестероидные противовоспалительные препараты.
Для цитирования: Бородулина И.В., Супонева Н.А., Бадалов Н.Г. Неспецифическая боль в спине: клинико-патогенетические особенности и возможности терапии // РМЖ. 2016. №25. С. 1699-1704
Nonspecific back pain: clinical pathogenic features and therapeutic modalities Borodulina I.V. 1 Suponeva, N.A. 2 Badalov, N.G. 1 1 Russian Scientific Center for Medical Rehabilitation and Balneology, Moscow 2 Scientific Center of Neurology, Moscow Currently, nonspecific back pain is generally recognized as a global health issue due to its high occurrence in the population. Degenerative dystrophic spine conditions which affect disc, facet joints, muscles, ligaments, and nerves are pathogenic basis of nonspecific back pain. Tonic muscle (or myofascial) syndrome is one of the most common pathogenic mechanisms of back pain. The treatment of nonspecific (primary) pain requires rational strategy depending on the dominant clinical sign. Non-steroidal anti-inflammatory drugs (NSAIDs) remain the “gold standard” for this disorder. Nimesulide characterized by good safety and efficacy (moderate quality of evidence) can be considered as a first-choice therapy. Complex treatment should include measures to reduce risk factors and to prevent exacerbations. The patient should also be educated to begin the treatment early since it prevents back pain chronicity.
Key words: nonspecific back pain, degenerative disk disorder, spondyloarthrosis, non-steroidal anti-inflammatory drugs.
For citation: Borodulina I.V., Suponeva N.A., Badalov N.G. Nonspecific back pain: clinical pathogenic features and therapeutic modalities // RMJ. 2016. № 25. P. 1699 –1704.
Статья посвящена вопросам неспецифической боли в спине

Неспецифическая (первичная) боль в спине может развиваться вследствие дегенеративно-дистрофических изменений в МПД, дугоотростчатых (фасеточных) суставах, кроме того, может быть обусловлена вовлечением в патологический процесс связок, мышц, сухожилий, фасций и невральных структур. Таким образом, боль в спине − следствие патологии костно-мышечной системы и соединительной ткани невисцеральной этиологии. Терминологически эти нозологии объединены в группу дорсопатий [3].
Клинические типы неспецифической боли в спине могут быть классифицированы по проявлениям (фенотипу):
− локальная боль − имеет распространение в пределах пораженного ПДС;
− проекционная (рефлекторная) боль − распространяется за пределы пораженного ПДС в смежные области позвоночника или в конечности, однако не сопровождается симптомами повреждения нервного корешка;
− радикулярная (корешковая) боль − всегда распространяется в зоне иннервации компримированного нервного корешка, сопровождается неврологическими симптомами радикулопатии.
Функциональной единицей позвоночника является ПДС, состоящий из двух позвонков, МПД и суставного комплекса между ними, окруженный мышечно-связочным аппаратом и нервными структурами. Правильное функционирование ПДС определяет нормальную биомеханику позвоночника, при этом МПД несет основную осевую нагрузку. Изменения хрящевой ткани МПД, представляющей собой пульпозное студенистое ядро, окруженное фиброзным кольцом, составляют морфологическую основу дегенеративного поражения позвоночника. Дегенеративно-дистрофическое поражение МПД влечет за собой механические внутридисковые изменения – происходит смещение диска с формированием протрузии или грыжи (в зависимости от степени выбухания в просвет спинномозгового канала) (рис. 1).

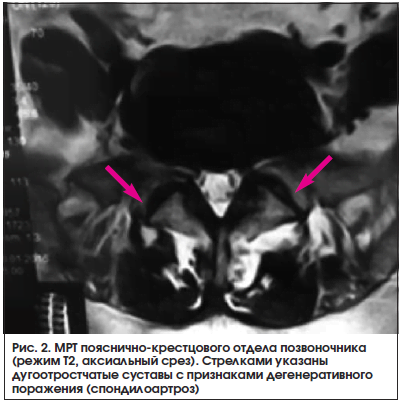
Боль при фасеточом синдроме имеет следующие признаки [14]:
− локализуется в спине (преимущественно в паравертебральных точках – проекции ДС);
− усиливается при длительном пребывании в положении сидя, с началом движения и при ходьбе;
− уменьшается в горизонтальном положении;
− ограничивает разгибание (усиливается при отклонении туловища назад) и ротацию;
− дебютирует в возрасте старше 35 лет.
В литературных источниках отмечают два основных патофизиологических механизма возникновения боли: дегенеративные изменения сустава, приводящие к раздражению медиальных ветвей задней порции иннервирующего спинномозгового нерва, и гиперплазия суставных отростков, влекущая за собой сужение межпозвонковых отверстий [12, 13]. Опираясь на биомеханическую взаимосвязанность комплекса диск − два межпозвонковых сустава, описан так называемый дегенеративный каскад: сегментарная дисфункция, нестабильность и стабилизация. На уровне ДС дегенеративный каскад представлен схемой на рисунке 3 [12].
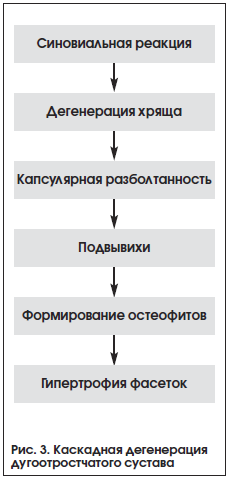
Неспецифическая боль в спине с вовлечением дискогенного, суставного и мышечно-связочного компонентов клинически проявляется локальным или рефлекторным (отраженным) болевым синдромом. Иная картина складывается в случае вовлечения нервного корешка при диско-радикулярном конфликте. Сдавление смещенным МПД нервного корешка обусловливает развитие компрессионной радикулопатии, а в патологический процесс оказываются вовлеченными твердая мозговая облочка, эпидуральная жировая клетчатка, сосуды, периневральная соединительная ткань. Компрессия нервного корешка патогенетически связана с возникновением асептического воспалительного процесса и микроциркуляторными расстройствами [17].
Клиническая картина при компрессионной пояснично-крестцовой радикулопатии характеризуется синдромом радикулопатии:
− боль преимущественно в нижней конечности или в спине и нижней конечности;
− сенсорные нарушения в зоне иннервации нервного корешка;
− гипорефлексия в соответствующем сегменте;
− положительный симптом натяжения (Ласега), выявляемый в пораженной конечности.
Диагностика фенотипа неспецифической боли в спине складывается из следующих подходов.
1. Клинико-неврологический осмотр с использованием функциональных тестов (проба Форестье, Отто, Шобера, Томайера и др.).
2. Основные инструментальные методы диагностики:
• рентгенологическое исследование: в переднезадней и боковой проекциях; функциональная спондилограмма в положении максимального сгибания и разгибания;
• МРТ или компьютерная томография (КТ).
3. Дополнительные инструментальные методы исследования:
• электронейромиография;
• миелография;
• остеоденситометрия.
Инструментальные методы диагностики дополняют данные клинико-неврологического осмотра, позволяют визуализировать поврежденную структуру, верифицировать диагноз и дать прогноз течения заболевания.
Локальный воспалительный процесс, являющийся ответной реакцией на сдавление нервного корешка диском, сопровождается активацией гуморальной системы, в которой большое значение придается интерлейкинам 17 и 21 [17, 18]. В литературных источниках описаны случаи спонтанного регресса компримирующего субстрата – грыжи МПД, что подтверждается клинически и результатами нейровизуализационных исследований [19]. Данный феномен остается не до конца изученным. Некоторые авторы высказывают предположение, что наиболее вероятным механизмом регресса служит активация фагоцитоза и ферментных систем [19, 20]. Мы наблюдали трех пациенток с описанным феноменом. Рисунки 4 и 5 представляют магнитно-резонансные томограммы пояснично-крестцового отдела позвоночника с визуализированной латеральной грыжей МПД на уровне IV и V поясничных позвонков, компримирующей нервный корешок. На рисунках 6 и 7 представлены контрольные томограммы спустя полтора года, на которых отмечается регресс грыжи диска.




Литература
Похожие статьи в журнале РМЖ
- Нестероидные противовоспалител.
- Современное состояние проблемы.
Статьи на эту же тему
- Грамотное лечение спины
- На страже благополучия
В статье представлены торакалгические синдромы и безболевые торакальные биомеханические ди.
Особенности первичных болей в спине.
БОЛЕВЫЕ СИНДРОМЫ в области спины разделяют на:
- первичные (неспецифические);
- вторичные (специфические).
Этиология НЕСПЕЦИФИЧЕСКОЙ БОЛИ В СПИНЕ обусловлена вовлечением в патологический процесс следующих структур:
- мышечно-связочного комплекса;
- межпозвонкового диска;
- межпозвонковых суставов;
- невральных структур (нервный корешок, твердая мозговая оболочка).

Неспецифическая (первичная) боль в спине может развиваться вследствие дегенеративно-дистрофических изменений в межпозвонковых дисках, дугоотростчатых (фасеточных) суставах, вовлечением в патологический процесс связок, мышц, сухожилий, фасций и невральных структур. Таким образом, боль в спине − следствие патологии костно-мышечной системы и соединительной ткани невисцеральной этиологии. Терминологически эти нозологии объединены в группу ДОРСОПАТИЙ.
Причинами ВТОРИЧНОГО БОЛЕВОГО СИНДРОМА В СПИНЕ служат:
- первичные и метастатические опухоли позвонков, оболочек спинного мозга;
- переломы позвонков;
- инфекционные поражения позвонков и межпозвонковых дисков (туберкулез, бруцеллез и проч.);
- неинфекционные воспалительные заболевания (анкилозирующий спондилоартрит, ревматоидный артрит);
- метаболические поражения костей (остеопороз, остеомаляция);
- острые нарушения спинального кровообращения;
- отраженные боли при патологии внутренних органов (почечная колика, гинекологические заболевания).
Результаты метаанализа 165 клинических исследований за период последних 30 лет, представленного в Arthritis & Rheumatism, показали, что распространенность боли в спине в популяции всех стран планеты составляет в среднем 31% (при этом у 38% населения выраженная боль в спине сохраняется не менее 1 года). Также отмечается, что чаще всего болью в спине страдают женщины в возрасте 40+ лет.
Проблема боли в спине имеет широкое распространение + не имеет однозначной стратегии терапии. Таким образом, проблема неспецифической боли в спине выходит за рамки чисто медицинских патологий, имея в том числе социальные, экономические и психологические аспекты. Факторы риска развития неспецифической боли в спине разнородны и множественны: наследственность, женский пол, ожирение, курение, тяжелые физические нагрузки, длительное пребывание в статической позе, которые приводят к дегенерации межпозвонковых дисков. Однако! Определяющими аспектами являются:
- нарушение трофики хрящевой ткани;
- повторяющиеся перегрузки позвоночно-двигательного сегмента.
Все ФАКТОРЫ ВОЗНИКНОВЕНИЯ БОЛИ В СПИНЕ можно разделить на корригируемые и некорригируемые, внешние и внутренние:
- внешние факторы: тяжелая физическая нагрузка, резкие движения, подъем тяжестей, низкая физическая активность, вредные привычки, сидячую работу, особенно выражено у офисных работников, что влечет за собой уменьшение выраженности поясничного лордоза, перераспределение нагрузки на диски, растяжение связок и капсул фасеточных суставов, нарушение гидратации и кровоснабжения диска, снижение тонуса мышц спины и брюшного пресса.
- внутренние факторы: избыточная масса тела, высокий рост, генетическая предрасположенность, беременность, депрессия, старение.
КЛИНИЧЕСКИЕ ТИПЫ НЕСПЕЦИФИЧЕСКОЙ БОЛИ В СПИНЕ могут быть классифицированы по проявлениям:
- локальная боль (распространение в пределах пораженного позвоночно-двигательного сегмента);
- проекционная (рефлекторная) боль (распространяется за пределы пораженного позвоночно-двигательного сегмента в смежные области позвоночника или в конечности, однако не сопровождается симптомами повреждения нервного корешка);
- радикулярная (корешковая) боль (всегда распространяется в зоне иннервации компримированного нервного корешка, сопровождается неврологическими симптомами радикулопатии).
БОЛЕВОЙ СИНДРОМ ПРИ ПОРАЖЕНИИ МЕЖПОЗВОНКОВОГО ДИСКА. Функциональной единицей позвоночника является позвоночно-двигательный сегмент, состоящий из 2 позвонков, межпозвонкового диска и суставного комплекса между ними, окруженный мышечно-связочным аппаратом и нервными структурами. Правильное функционирование сегмента определяет нормальную биомеханику позвоночника, при этом диск несет основную осевую нагрузку. Изменения хрящевой ткани диска, представляющей собой пульпозное студенистое ядро, окруженное фиброзным кольцом, составляют морфологическую основу дегенеративного поражения позвоночника. Дегенеративно-дистрофическое поражение межпозвонкового диска влечет за собой механические внутридисковые изменения – происходит смещение диска с формированием протрузии или грыжи (в зависимости от степени выбухания в просвет спинномозгового канала). Болевой синдром при поражении межпозвонкового диска имеет следующие признаки:
- локализуется преимущественно в проекции диска (межостистое пространство);
- усиливается в вертикальном положении, при длительном пребывании в положении сидя, при кашле и чихании;
- уменьшается в горизонтальном положении;
- сопровождается трудностями при наклоне вперед и разгибании из согнутого положения (ограничение движений, усиление боли).
- локализуется в спине (преимущественно в паравертебральных точках – проекции дугоотростчатого сустава);
- усиливается при длительном пребывании в положении сидя, с началом движения и при ходьбе;
- уменьшается в горизонтальном положении;
- ограничивает разгибание (усиливается при отклонении туловища назад) и ротацию.
МИОФАСЦИАЛЬНЫЙ СИНДРОМ. Отмечают два основных патофизиологических механизма возникновения боли:
- дегенеративные изменения сустава, приводящие к раздражению медиальных ветвей задней порции иннервирующего спинномозгового нерва;
- гиперплазия суставных отростков, влекущая за собой сужение межпозвонковых отверстий.
Опираясь на биомеханическую взаимосвязанность комплекса диск − два межпозвонковых сустава, описан так называемый дегенеративный каскад: сегментарная дисфункция, нестабильность и стабилизация. В патологический процесс при развитии дегенеративно-дистрофических изменений позвоночника неизбежно оказываются вовлечены мышечно-связочные структуры. Мышечный компонент боли в спине может быть представлен спазмом, характеризующимся болезненностью в местах прикрепления мышцы к кости и ограничением амплитуды движения, либо миофасциальным синдромом. Последнему свойственно формирование локальных болезненных уплотнений в пораженных мышцах с перегруппировкой сократительных элементов, которые являются одновременно триггерными точками. Мышечно-связочные нарушения имеют место в 100% случаев неспецифической боли в спине и служат самым частым источником ноцицепции. Диагностика мышечно-тонического (миофасциального) синдрома складывается из:
ПОЯСНИЧНО-КРЕСТЦОВАЯ РАДИКУЛОПАТИЯ. Неспецифическая боль в спине с вовлечением дискогенного, суставного и мышечно-связочного компонентов клинически проявляется локальным или рефлекторным (отраженным) болевым синдромом. Иная картина складывается в случае вовлечения нервного корешка при диско-радикулярном конфликте. Сдавление смещенным диском нервного корешка обусловливает развитие компрессионной радикулопатии, а в патологический процесс оказываются вовлеченными твердая мозговая оболочка, эпидуральная жировая клетчатка, сосуды, периневральная соединительная ткань. Компрессия нервного корешка патогенетически связана с возникновением асептического воспалительного процесса и микроциркуляторными расстройствами. Клиническая картина при радикулопатии:
- боль преимущественно в нижней конечности или в спине и нижней конечности;
- сенсорные нарушения в зоне иннервации нервного корешка;
- гипорефлексия в соответствующем сегменте;
- положительный симптом натяжения (Ласега), выявляемый в пораженной конечности.
Источник: Nurs Times / Pain management is still not being taken seriously
Lancet / Non-specific low back pain
Arthritis & Rheumatism / A Systematic Review of the Global Prevalence of Low Back Pain
РМЖ / Бородулина И.В. Неспецифическая боль в спине: клинико-патогенетические особенности и возможности терапии
Ревматология / Дубовская С.С.,Боль в спине: актуальные вопросы
Новости медицины и фармации / Куприненко Н. Синдром боли в спине: дифференциальная диагностика и терапия
Сак Л.Д., / Фасетный синдром позвоночника: клинико-диагностическая структура и малоинвазивные методики лечения //
Косинская Н.С. / Дегенеративно-дистрофические поражения костно-суставного аппарата.
Богачева Л.А. / Дорсалгии: классификация, механизмы патогенеза, принципы ведения (опыт работы специализированного отделения боли)
Современная ревматология / Шостак Н.А. Миалгии: подходы к дифференциальной диагностике, лечение
Exp Ther Med / Tian P. Role of interleukin-17 in chondrocytes of herniated intervertebral lumbar discs

Боль в спине (или дорсалгия) расценивается как неспецифическая (скелетно-мышечная), если не обнаруживается компрессии спинномозгового корешка или нерва, спинного мозга, корешков конского хвоста, а также нет специфических причин боли: перелома позвонков, опухоли, инфекционного поражения, спондилоартрита или других заболеваний, которые могут приводить к ее развитию. К факторам риска появления дорсалгии относят тяжелый физический труд, частые наклоны туловища, подъем тяжестей, а также сидячий образ жизни, вибрационные воздействия.

Обратите внимание ! Международные рекомендации разработаны преимущественно для люмбалгии (боли в нижней части спины - между XII парой ребер и нижними ягодичными складками с иррадиацией или без иррадиации в нижние конечности), которая наиболее часто встречается в клинической практике. Однако врачебная тактика существенно не меняется при цервикалгии и торакалгии, поэтому большинство рекомендаций, касающихся люмбалгии, применимы и при болевых синдромах другой локализации.

Обратите внимание! СМБ - это боль, связанная с физической нагрузкой и вызванными этой нагрузкой повреждением и асептическим воспалением различных мягкотканных элементов опорнодвигательного аппарата. СМБ характеризуется четкой локализацией и связью с движением определенной анатомической структуры. Целесообразно отделить понятие СМБ от боли, связанной с онкологическими и инфекционными заболеваниями структур опорно-двигательного аппарата (хотя при этой патологии появление боли также связано с активацией периферических болевых рецепторов), а также заболеваниями, при которых появление боли связано с дисфункцией ноцицептивной системы (фибромиалгия), поскольку при этой патологии отсутствует прямая связь с функциональной активностью (движением).


Обратите внимание! Необходимо информировать пациентов о [ . ] вероятности благоприятного прогноза при острой (неспецифической) боли в спине, в т.ч. о степени вероятности улучшения спустя 1 месяц от начала лечения. Следует объяснить больному, что ранняя нейровизуализация и другие диагностические тесты обычно не позволяют точно установить причину болевого синдрома, не улучшают результатов терапии и ведут к дополнительным расходам.

Обратите внимание! Обязателен анализ неблагоприятных психосоциальных факторов и эмоционального стресса, т.к. они служат более значимыми предикторами в отношении прогноза болевого синдрома, чем выводы, которые можно сделать из физического обследования, знаний об интенсивности и продолжительности боли или данных магнитно-резонансной томографии (МРТ). Оценка психосоциальных факторов позволяет выявить пациентов, у которых возможно медленное, плохое восстановление, и подобрать для них более эффективную, в том числе, мультидисциплинарную программу реабилитации. К психосоциальным факторам, ухудшающим прогноз, а также затрудняющим реабилитацию, относят: [1] высокая тревожность, депрессия, катастрофизация; [2] пассивная копинг-стратегия; [3] неудовлетворенность работой; а также [4] повышение уровня инвалидности, соматизацию.
Для купирования боли при острой и подострой дорсалгии рекомендуется использование нестероидных противовоспалительных препаратов (НПВП) [1] в терапевтических дозах и [2] относительно коротким курсом (при существенном снижении боли рекомендуется прекращение приема НПВП - в среднем через 10 - 14 дней). НПВП эффективнее плацебо как при острой, так и при хронической неспецифической боли в спине (миорелаксанты целесообразно применять в комплексном лечении СМБ только лишь при наличии болезненного гипертонуса мышц; к препаратам этого ряда, зарегистрированным в России, относятся толперизон, тизанидин и баклофен). При острой дорсалгии не доказано положительного влияния методов физиотерапии, рефлексотерапии, массажа и мануальной терапии, которые часто назначаются пациентам в нашей стране и существенно повышают стоимость лечения (применение мануальной терапии ассоциируется с возможностью увеличения грыжи межпозвонкового диска, на что особо указывают спинальные нейрохирурги).
[ 1 ] Максимальный эффект НПВП достигается при их регулярном использовании в средних и высоких терапевтических дозах. Оценка эффективности НПВП должна проводиться через 7 - 14 дней от начала приема полной терапевтической дозы препарата.
[ 2 ] Выбор [1] лекарственной формы НПВП и [2] конкретного препарата определяется клинической ситуацией. Наиболее целесообразным способом применения НПВП является пероральный прием. Использование инъекционных форм НПВП показано для кратковременного лечения очень интенсивной острой СМБ и/или при невозможности перорального приема. Длительное (более трех дней) применение инъекционных форм НПВП [ . ] НЕ оправдано с точки зрения эффективности и безопасности.
[ 3 ] Локальные формы НПВП (мази, гели или спреи) могут использоваться в качестве дополнительного анальгетика или самостоятельного обезболивающего средства при слабой или умеренно выраженной СМБ, а также в случае невозможности системного применения этих препаратов из-за высокого риска осложнений.
[ 4 ] В эквивалентных дозах и при достаточном времени наблюдения (хотя бы несколько дней) все НПВП - как селективные, так и неселективные - демонстрируют одинаковую эффективность (не установлено достоверного превосходства какого-либо одного НПВП над другими при лечении неспецифической СМБ); выбор конкретного НПВП должен быть основан на класс-специфических осложнениях того или иного НПВП, прежде всего со стороны желудочно-кишечного тракта и сердечно-сосудистой системы, поскольку именно риск развития этих побочных эффектов является основным фактором, ограничивающим применение НПВП. Таким образом, Выбор НПВП должен основываться на критериях безопасности и определяться наличием тех или иных факторов риска. Однако у некоторых пациентов отмечается положительный эффект после приема определенного НПВП, поэтому при отсутствии эффекта одного НПВП целесообразно попробовать другой.

читайте также пост: Принципы рационального выбора НПВП (на laesus-de-liro.livejournal.com) [читать]

читайте также пост: Хроническая неспецифическая поясничная боль (на laesus-de-liro.livejournal.com) [читать]
Аннотация научной статьи по клинической медицине, автор научной работы — Кукушкин М.Л.
Похожие темы научных работ по клинической медицине , автор научной работы — Кукушкин М.Л.
Diagnosis and treatment of nonspecific back pain
The article tells about recent algorithms for diagnosis and treatment of patients with back pain . In primary outpatient care, patients with back pain can be classified into one of two categories: "non-specific" musculoskeletal pain and "specific" pain caused by a potentially dangerous disease. This helps general practitioners to perform adequate diagnostics and prescribe effective therapy.
М.Л. КУКУШКИН, д.м.н., профессор, Научно-исследовательский институт общей патологии и патофизиологии, Лаборатория фундаментальных и прикладных проблем боли, Москва
ДИАГНОСТИКА И ЛЕЧЕНИЕ
НЕСПЕЦИФИЧЕСКОЙ БОЛИ В СПИНЕ
Ключевые слова: боль в спине, диагностика, лечение.
M.L. KUKUSHKIN, MD, Prof., Institute of General Pathology and Pathophysiology, Laboratory of fundamental and applied problems of pain, Moscow
DIAGNOSIS AND TREATMENT OF NONSPECIFIC BACK PAIN
■ начало стойкой боли в спине в возрасте до 15 лет и после 50 лет;
■ немеханический характер боли (боли не уменьшаются в покое, в положении лежа, в определенных позах);
■ связь боли с травмой;
■ постепенное усиление болей;
■ наличие онкологии в анамнезе;
■ возникновение боли на фоне лихорадки, снижения массы тела;
■ жалобы на длительную скованность по утрам;
■ симптомы поражения спинного мозга и его корешков (параличи, тазовые нарушения, расстройства чувствительности);
■ изменения в анализах мочи, крови.
Методы визуализации и консультации соответствующих специалистов рекомендуется назначать пациентам с болями в спине в неясных случаях, когда возникают подозрения на специфический характер боли, который может быть следствием опухолевого, воспалительного или травматического поражения позвоночника, инфекционных процессов, метаболических нарушений, заболеваний внутренних органов, повреждения мышц, поражения нервной системы и т. д.
Наличие лихорадки, локальной болезненности в паравертебральной области характерны для инфекционного поражения позвоночника. Его риск повышен у пациентов, получающих иммуносупрессивную терапию, страдающих ВИЧ-инфекцией, туберкулезом, инфекционными заболеваниями мочевыводящих путей. Причинами инфекционных осложнений могут быть недавно перенесенные инфекционные заболевания, туберкулез, саркои-доз, опоясывающий герпес, операции на позвоночнике, очаги в глубоких отделах мягких тканей. Лейкоцитоз может быть единственным лабораторным признаком, указывающим на дисцит или эпидуральный абсцесс.
Сохранение боли в покое и ночью, беспричинное снижение массы тела, наличие онкологического заболевания в анамнезе, а также возраст пациента старше 50 лет могут свидетельствовать о наличии первичной или метастатической опухоли позвоночника. Метастатическое поражение структур позвоночника встречается чаще, чем первичные опухоли. Метастазы в позвоночник обнаруживаются у 70%
пациентов с первичными опухолями. Среди опухолей, которые наиболее часто метастазируют в структуры позвоночника, - опухоли молочных желез, легких, предстательной железы, почек, лимфома, меланома и опухоли желудочно-кишечного тракта. Боль в спине, которая будит пациента ночью, может также указывать на опухоль.
В половине всех случаев у пациентов с аневризмой брюшной аорты первым симптомом является боль в спине. Поэтому наличие пульсирующего объемного образования в области живота при пальпации - серьезный повод для проведения дополнительных диагностических процедур.
Компрессионный перелом позвоночника можно заподозрить при наличии травмы позвоночника, а также у лиц с остеопорозом вследствие возрастных нарушений кальциевого обмена. Остеопороз наиболее часто выявляется у женщин в постклимактерическом периоде, у лиц, принимающих глюкокортикоиды. Факторами риска также являются курение, прием алкоголя и сидячий образ жизни.
Наличие выраженной скованности в спине, особенно по утрам, постепенное появление болей, усиление боли ночью может свидетельствовать о ревматическом заболевании.
Если же пациент жалуется на слабость в ногах, нарушение мочеиспускания и у него отмечаются снижение чувствительности в аногенитальной области и тазовые нарушения, следует заподозрить компрессию конского хвоста.
При осмотре пациента важно обращать внимание на возможные высыпания на кожных покровах, изменение позы, осанки, походки, объема движений в позвоночнике, тазобедренных суставах, на степень напряжения и болезненность мышц, локализацию миофасциальных триггер-ных точек. При этом слабо выраженная ортопедическая симптоматика при сильных болях может служить признаком серьезной сопутствующей патологии. Неврологическое обследование позволяет выявить повреждение корешков и структур спинного мозга.
Клинически НБС - это скелетно-мышечная боль, в которой традиционно выделяют мышечно-тонический (рефлекторный) болевой синдром, миофасциальный и артропатический болевой синдром [1, 8, 9, 21].
Мышечно-тонический болевой синдром возникает вследствие ноцицептивной импульсации, идущей от пораженных дисков, связок и суставов позвоночника при статической или динамической перегрузке. Более чем в половине случаев источником ноцицептивной импульсации являются дугоотростчатые (фасеточные) суставы, что подтверждается положительным эффектом блокад проекции этих суставов местными анестетиками. Ноцицепторы, содержащиеся в футлярах спинномозговых корешков, в твердой мозговой оболочке, задних и передних продольных связках, также могут участвовать в формировании боли. Вследствие ноцицептивной импульсации происходит рефлекторное напряжение мышц, которое вначале имеет защитный характер и иммобилизирует пораженный сегмент. Однако в дальнейшем тонически напряженная мышца сама становится источником боли. При этом обнаруживаются участки кожной и мышечной гиперальгезии, мышечное напряжение, ограничение движения в соответствующем сегменте позвоночника. При наклонах в передне-заднем или боковом направлениях болевые ощущения могут усиливаться. Облегчение боли отмечается в положении лежа на боку с согнутыми ногами в коленных и тазобедренных суставах.
Формирование миофасциального болевого синдрома (МФБС) происходит в условиях действия избыточной нагрузки на мышцы. При МФБС пальпируемая мышца ощущается спазмированной в виде тугого тяжа. В мышце обнаруживаются болезненные уплотнения (триггерные зоны), давление на которые вызывает локальную и отраженную боль.
Развитие МФБС во многом обусловлено сенситизацией (повышением возбудимости) ноцицепторов, локализованных в мышцах [2]. При сенситизации ноцицепторов нервное волокно становится более чувствительным к повреждающим стимулам, что клинически проявляется развитием мышечного напряжения и гиперальгезии.Неврологические нарушения не характерны при данной патологии.
Лечение пациентов с НБС должно быть направлено в первую очередь на регресс болевой симптоматики, способствующей восстановлению активности пациента и снижению риска хронизации боли [1, 9, 11, 19]. Важным является активное вовлечение пациента в процесс лечения, убеждение его в доброкачественном течении его болезни, разъяснение ему причин возникновения заболевания и тактики лечения. Разъяснение больным с НБС причин возникновения их состояния, тактики лечебных мероприятий позитивно влияет на результаты лечения, снижает количество повторных обращений и вероятность хронизации заболевания.
В острый период необходимо ограничить физические нагрузки, следует избегать подъема тяжестей, длительного пребывания в сидячем или лежачем положении. При НБС нет необходимости в соблюдении постельного режима. Небольшая физическая нагрузка не только не опасна, более того, - полезна, т. к. ранняя двигательная активность способствует улучшению трофики тканей и выздоровлению. Согласно рекомендациям, основанным на результатах многочисленных рандомизированных контролируемых исследований, эффективными при лечении НБС являются [1, 8-11, 19]:
Сохранение физической активности (уровень доказательности В); польза от сохранения постельного режима не доказана.
■ Использование парацетамола и нестероидных противовоспалительных препаратов (уровень доказательности А).
■ Использование центральных миорелаксантов (уровень доказательности В).
Острую болевую симптоматику у пациентов с неспецифической болью в спине рекомендуется купировать парацетамолом и нестероидными противовоспалительными препаратами (НПВП). Сочетание анальгетического и противовоспалительного действия, доказанная эффективность, наличие различных лекарственных форм и дозировок, ценовая доступность определяют первоочередной выбор НПВП при назначении больным с неспецифической болью в спине. Анальгетические и противовоспалительные свойства НПВП обусловлены ослаблением синтеза простагландинов вследствие ингибирования активности циклооксигеназ (ЦОГ-1 и ЦОГ-2) как в периферических тканях, так и в структурах ЦНС. Практически все НПВП, используемые в медицинской практике, апробированы при боли в спине и показали хороший обезболивающий эффект [4, 5]. Нет данных, свидетельствующих об анальгетических преимуществах какого-либо представителя группы НПВП при купировании НБС. Максимальный эффект НПВП достигается при их регулярном использовании в средних и высоких терапевтических дозах. Оценка эффективности НПВП должна проводиться через 7-14 дней от начала приема полной терапевтической дозы препарата. Выбор НПВП должен основываться на критериях безопасности и определяться наличием тех или иных факторов риска [4].
Среди класс-специфических осложнений, напрямую связанных с основным механизмом действия НПВП и возникающих наиболее часто, относятся поражение слизистой желудочно-кишечного тракта (ЖКТ), риск развития сердечно-сосудистых нарушений и функции почек [4, 5]. Проблема развития осложнений при назначении НПВП актуализируется у больных среднего и пожилого возраста, имеющих сопутствующие заболевания сердечно-сосудистой системы (артериальной гипертензии, ишемической болезни сердца (ИБС), сердечной недостаточности), ЖКТ (наличие в анамнезе язвы и желудочно-кишечного кровотечения), а также хронической болезни почек. По данным исследования КОРОНА-2, проведенного в России и странах СНГ, количество пациентов с жалобами на скелетно-мышечную боль и имеющих коморбидные сердечно-сосудистые или желудочно-кишечные заболевания, на приеме у ревматологов составляло более 90%, у неврологов -54,2%, у травматологов - 60,0%, у терапевтов - 34,3% [3].
Поэтому тактика лечения НПВП должна быть связана с безопасностью пациента и зависеть от возраста пациента, индивидуальной переносимости препарата пациентом и спектра сопутствующих заболеваний. Выбранное средство должно максимально устранять боль и не вызывать серьезных побочных эффектов. Согласно рекомендациям Ассоциации ревматологов России, Российского общества по изучению боли, Российской гастроэнтерологической
ассоциации, Российского кардиологического общества, Ассоциации травматологов-ортопедов России, Ассоциации междисциплинарной медицины, Российской ассоциации паллиативной медицины, клинически выраженная ИБС, хроническая сердечная недостаточность £ второго функционального класса (NYHA), острый и ранее перенесенный инфаркт миокарда, ишемический инсульт, сахарный диабет II типа с поражением органов-мишеней и систем должны рассматриваться как противопоказания для применения НПВП [4]. В этих случаях в качестве альтернативы НПВП могут быть использованы трамадол и флупиртин, обладающие доказанной эффективностью у больных с болями в спине [15, 20]. Вместе с тем основными средствами патогенетического лечения больных с НБС остаются НПВП.
Ксефокам (лорноксикам) относится к группе НПВП с выраженным анальгетическим действием. В основе механизма действия лорноксикама лежит угнетение синтеза простагландинов вследствие сбалансированного угнетения активности изоферментов ЦОГ-1 и ЦОГ-2 [13]. Угнетение активности ЦОГ не вызывает увеличения выработки лейко-триенов. Лорноксикам не обладает опиатоподобным действием на центральную нервную систему. Данный препарат существует в различных лекарственных формах: в виде парентеральных форм для внутримышечного и внутривенного введения, а также в виде таблеток, в т. ч. и в виде инновационной таблетированной формы Ксефокам Рапид, предназначенной для быстрого и эффективного лечения острой боли. Рекомендуемая доза для однократного приема Ксефокама составляет 8 мг, максимальная суточная -16 мг (в 2 приема с интервалом 8-12 ч). Ксефокам Рапид
обеспечивает быстрое (в течение первых 30 мин) обезболивающее действие, сопоставимое по скорости развития с формами для внутримышечного введения. Эффективность обезболивающего действия лорноксикама доказано в нескольких хорошо организованных рандомизированных контролируемых исследованиях у хирургических больных, при хронических ревматических заболеваниях, у больных с острой НБС [14, 16, 18, 22]. Кроме этого, высокая анальге-тическая эффективность лорноксикама у больных с дорсал-гиями по сравнению с диклофенаком, мелоксикамом и нимесулидом доказана в оригинальном российском рандомизированном исследовании [6].
Использование центральных миорелаксантов устраняет мышечное напряжение, способствует регрессу боли и восстановлению двигательной активности пациента с НБС [1, 7, 8, 9, 17]. В клинической практике при лечении таких больных используются в первую очередь толпери-зон, тизанидин и баклофен. Существуют также доказательства того, что комбинация НПВП и миорелаксантов у пациентов с НБС более эффективна, чем монотерапия этими препаратами. Эта комбинация позволяет сократить сроки лечения и уменьшить риск развития побочных эффектов НПВП за счет снижения продолжительности использования последних.
В комплексную терапию целесообразно также включать лечебную физкультуру, методы рефлексотерапии, мануальной терапии (постизометрическая релаксация), массаж. Как правило, такое сочетание медикаментозных и немедикаментозных методов лечения способствует ускорению выздоровления пациентов с НБС.
1. Алексеев А.В., Аринина Е.Е., Арсеньев А.О.
и др. Неспецифическая боль в нижней части спины. Клинические рекомендации для терапевтов и врачей общей практики. М.: ООО «КомплексСервис, 2008, 70 с.
2. Боль. Практическое руководство для врачей. Под ред. Н.Н. Яхно, М.Л. Кукушкина. М.: Издательство РАМН, 2011, 565 с.
3. Каратеев А.Е. Болезни костно-мышечной системы в практике 2102 врачей разных специальностей: структура патологиии мнение специалистов об эффективности НПВП (предварительные данные эпидемиологического исследования КОРОНА-2). Consilium medicum. 2013, (9): 95-100.
5. Каратеев А.Е., Яхно Н.Н., Лазебник Л.Б., Кукушкин М.Л., Дроздов В.Н., Исаков В.А., Насонов Е.Л. Применение нестероидных про-тивововспалительных препаратов. Клинические рекомендации. М.: ИМА-ПРЕСС, 2009. 168 с.
6. Ковальчук В.В., Ефимов М.А. Сравнительная характеристика эффективности и переносимости кратких курсов терапии (6 сут) различными нестероидными противовоспалительными препаратами при лечении пациентов с дорсалгиями. Ж. неврологии и психиатрии им. С.С. Корсакова, 2010, 110(1): 61-64.
7. Кукушкин М.Л. Алгоритмы диагностики и лечения больных с болью в спине. Российский журнал боли, 2014, (3-4): 3-6.
8. Павленко С.С. Боли в нижней части спины (эпидемиология, клинико-диагностическая классификация, современные направления в диагностике, лечении и стандартизации медицинской помощи. Новосибирск: Сибмедиздат НГМУ, 2007. 172 с.
9. Подчуфарова Е.В., Яхно Н.Н. Боль в спине. 2009. М.: ГЕОТАРМедиа. 356 с.
10. Atlas SJ, Deyo RA. Evaluating and managing acute of low back pain in the primary care setting. J. Gen. Intern Med, 2001, 16: 120-131.
11. Chou R, Huffman LH. Medications for Acute and Chronic Low Back Pain: A Review of the Evidence for an American Pain Society/ American College of Physicians Clinical Practice Guideline. Ann Intern Med, 2007, 147: 505-514.
12. Global Burden of Disease Study 2013 Collaborators. Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet, 2015 Aug 22, 386(9995): 743-800.
13. Hamza Yel-S, Aburahma MH. Design and in vitro Evaluation of novel sustained-release double-layer tablets of Lornoxicam: Utility of cyclodextrin and xanthan gum combination. AAPSPharm Sci Tech., 2009, 10: 1357-1366.
14. Kidd B, Frenzel W. A multicenter, randomized, double blind study comparing lornoxicam with diclofenac in osteoarthritis. J Rheumatol, 1996, 23(9): 1605-1611.
15. Li C, Ni J, Wang Z, Li M et al. Analgesic efficacy and tolerability of flupirtine vs. tramadol in patients with subacute low back pain: a double-blind multicentre trial. Curr Med Res Opin. 2008, 24(12): 3523-30.
16. Rose P, Steinhauser C. Comparison of Lornoxicam and Rofecoxib in Patients with Activated Osteoarthritis (COLOR Study). Clin Drug Investig, 2004, 24(4): 227-236.
17. Ross E. Back pain. In: Current diagnosis and treatment of pain. Eds.:von Roenn JH, Paice JA, Preodor ME. Large Medical Books. McGraw-Hill, 2006, p. 172-208
18. Sener M, Yilmazer C, Yilmaz I et al. Efficacy of lornoxicam for acute postoperative pain relief after septoplasty: a comparison with diclofenac, ketoprofen, and dipyrone. J Clin Anesth, 2008, 20(2): 103-108.
19. Tulder M, Becker A, Bekkering T et al. European guidelines for the management of acute nonspecific low back pain in primary care. Eur. Spine J, 2006, 15(suppl. 2): 169-191.
20. Uberall MA, Mueller-Schwefe GH, Terhaag B. Efficacy and safety of flupirtine modified release for the management of moderate to severe chronic low back pain: results of SUPREME, a prospective randomized, double-blind, placebo- and active-controlled parallel-group phase IV study Curr Med Res Opin, 2012 Oct, 28(10): 1617-34.
21. Waddell G. The Back Pain Revolution. 2nd ed. 2004. Elsevier Edinburgh. P.2 21-239.
22. Yakhno N, Guekht A, Skoromets A et al. Analgesic efficacy and safety of lornoxicam quick-release formulation compared with diclofenac potassium: randomised, double-blind trial in acute low back pain. Clin Drug Investig, 2006, 26(5): 267-277.
Читайте также:


