Эндопротезирование тазобедренного сустава в молодом возрасте
Под нашим наблюдением находилось 51 больной моложе 30 лет, которым выполнено первичное эндопротезирование тазобедренного сустава. Показаниями к операции были: диспластический коксартроз, врожденный вывих головки бедренной кости, асептический некроз головки бедренной кости, последствия травм головки и шейки бедренной кости больных. Клиническо - функциональные результаты лечения больных молодого возраста с патологией тазобедренного сустава в сроки от 1 года до 5 лет, которым выполнено первичное эндопротезирование показали, что отличный и хороший результат в указанные выше сроки отмечен у 89,7% больных, удовлетворительный у 10,3% больных. Неудовлетворительных результатов в раннем послеоперационном периоде и в срок до 5 лет не отмечено.
Under our supervision was 51 patients 30 years by which it is executed primary endoprothesis hyp a joint are younger. Indications to operation were: displastic cocsarthrosis , a congenital dislocation of a head of a femur, aseptic некроз heads of a femur, a consequence of traumas of a head and nec a femur of patients. Clinikal - functional results of treatment of patients of young age with a pathology hyp a joint in terms from 1 year till 5 years by which it is executed primary endopronhesis have shown, the excellent and good result in the terms specified above is noted at 89,7 % of patients, satisfactory at 10,3 % of patients. Unsatisfactory results in the early postoperative period and till 5 years it is noted.
Keywords: hip a joint, endoprothesis, young patients.
Изучить результаты эндопротезирования тазобедренного сустава у больных моложе 30 лет.
Под нашим наблюдением находилось 51 больной моложе 30 лет, которым выполнено первичное эндопротезирование тазобедренного сустава. Мужчин - 26, женщин - 25. Пациентов от 18 до 20 лет – 4 (7,8% от всех оперированных молодого возраста); от 21 до 25 лет – 14, соответственно 27,5%, и от 26 до 30 лет – 33 пациента (64,7%).
Показаниями к операции были: диспластический коксартроз - 22 больных, в т.ч. пациентов после устранения врожденного вывиха головки бедренной кости – 9, асептический некроз головки бедренной кости – 17, последствия травм головки и шейки бедренной кости – 12 больных. Из 22 пациентов с диспластическим коксартрозом, развившимся в связи с различной врожденной патологией тазобедренного сустава, 16 – ти в возрасте от 3 лет до 21 года было выполнено от одной до трех операций на тазобедренном суставе или проксимальном отделе бедренной кости. Это были различные виды корригирующих остеотомий бедренной кости, костей таза, операции на вертлужной впадине. Целью этих операций было уменьшение дефицита покрытия головки бедренной кости и уменьшение нагрузки на тазобедренный сустав в целом. В группе больных с диспластическим коксартрозом дисплазия вертлужной впадины имела место у 17 пациентов (60,7%), дисплазия проксимального отдела бедренной кости у 5 больных (17,9%) и в 7 случаях (21,4%) – дисплазия носила комбинированный характер.
Из 9 больных с врожденными вывихами головки бедренной кости бедренной кости пятеро в раннем детском возрасте перенесли операцию – открытое устранение вывиха, а четверым пациентам вывих вправлялся консервативными методами. При обследовании перед эндопротезированием тазобедренного сустава у пациентов с врожденным вывихом головки установлено, что у 6 – ти пациентов этой группы (66,7%) дефицит покрытия головки составил от 40 до 60%, а у 2 – х отмечался полный вывих головки.
Двенадцати пострадавшим с последствиями травм тазобедренного сустава выполнено тотальное эндопротезирование в срок от 6 мес. до 4 лет после травмы. Восьмерым больным этой группы выполнялись различные виды остеосинтеза, однако последний был несостоятельным. У них диагностированы ложные суставы, асептические некрозы головки бедренной кости и посттравматический коксартроз различной степени выраженности. Четверо пациентов получили сочетанные и множественные повреждения (в основном тяжелую нейротравму) и не были оперированы сразу в связи с тяжелым общим состоянием.
Семнадцать пациентов с асептическим некрозом головки бедренной кости были мужчины в возрасте от 22 до 30 лет. У 9 больных этой группы отмечены признаки вторичного коксартроза 1- 3 ст. (по Kelgren, 1956) Характерно, что у 11 пациентов этой группы (64,7%) имели отягощенный анамнез. Так, семь больных на протяжении длительного периода употребляли различные наркотические препараты, четверо из них были больны гепатитом B, а один ВИЧ – инфицирован. Еще трое молодых людей с асептическим некрозом головки бедренной кости во время службы в армии имели контакты с компонентами ракетных топлив (в частности - гептилом). Таким образом, у большинства пациентов этой группы заболевание, по - видимому, было связано с хроническим токсическим воздействием различных вредных веществ или же развилось на фоне хронических инфекционных процессов.
В качестве имплантов для эндопротезирования использовались тотальные эндопротезы тазобедренного сустава бесцесментной и гибридной фиксации. Эндопротезы фирмы Zimmer (США) использованы в 36 случаях, что составило 70,6% от всех оперированных, фирмы De Pue (США) в 8 случаях (15,7%), Seraver (Франция) – у 4 оперированных (7,8%), и ЭСИ (Россия) имплантированы у 3 пациентов (5,9%). Бесцементная фиксация компонентов суставов использовалась при 37 операциях (72,5%), гибридная – у 14 пациентов (27,5%). При дефектах стенок вертлужной впадины и иных проблемах, связанных с установкой вертлужного компонента, использовалась костная аутопластика крыши вертлужной впадины (2 операции), цементная пластика с каркасом из спонгиозных шурупов (2 операции) и укрепляющие кольца Мюллера использованы при 3-х операциях.
Анализу были подвергнуты данные клинико-рентгенологического обследования 39 пациентов, оперированных в срок от 1 года до 5 лет. В анализируемую группу вошли 21 женщина и 18 мужчин. По поводу диспластического коксартроза оперировано 18 пациента, с асептическим некрозом головки бедренной кости было 13 человек, последствиями травм головки и шейки бедренной кости – 8. Бесцементная фиксация имплантов использована в 29 случаях, гибридная - у 10 пациентов. Клиническая оценка результатов лечения проводилась по оценочной шкале Харриса (табл. 1) для тазобедренного сустава (Harris W.H., 1969).
Табл. 1
Результаты лечения больных после первичного эндопротезирования тазобедренного сустава по Харрису (абс. числа/%)

По мнению многих авторов, тотальное эндопротезирование тазобедренного сустава является одним из самых успешных и рентабельных хирургических вмешательств в медицине [1; 2]. Высокая эффективность и большая потребность в ортопедической помощи объясняет повсеместное постоянно увеличивающееся количество операций по замене тазобедренного сустава [3]. На современном этапе эффективность имплантации искусственного сустава определяется несколькими переменными: функциональный статус оперированных пациентов, оцениваемый с помощью специальных шкал; качество жизни, измеряемое на основе общепринятых опросников (SF 36, SF12, EQ5D и пр.), и специфический показатель функционирования эндопротеза – долгосрочная выживаемость. При этом оценка функционального статуса не позволяет в достаточной степени определить двигательную активность пациентов, которая оказывает ключевое влияние на длительность функционирования узла трения искусственного тазобедренного сустава и, как следствие, его выживаемость [2]. Если ранее считалось, что человек в среднем проходит в течение одного года около 1 миллиона шагов, то более поздние исследования показали, что при отсутствии болевого синдрома и средней степени двигательной активности пациент совершает около 1,9 миллиона шагов, а отдельные индивидуумы проходят в год более 10 миллионов шагов [4; 5]. Поэтому изучение двигательной активности в различных группах пациентов имеет существенное значение для прогнозирования результатов эндопротезирования ТБС и понимания эффективности различных типов искусственных суставов. Особенно важно проведение исследований по измерению двигательной активности в группе пациентов молодого возраста, поскольку они имеют большую предстоящую продолжительность жизни и пара трения установленных эндопротезов будет подвергаться значительно большим нагрузкам. Не существует однозначной позиции относительно того, до какого возраста считать пациентов молодыми. В доступных сериях наблюдений последних лет, представленных из пациентов с различной патологией, средний возраст колеблется в очень больших пределах – от 38 до 65 лет, но чаще называется цифра 50–55 лет [6], а в отдельных группах молодых пациентов составляет вообще 29–35 лет [6].
Цель исследования: оценить двигательную активность пациентов молодого возраста до операции эндопротезирования тазобедренного сустава и в разные периоды после замены сустава.
Вопросы. В данной работе мы хотели решить несколько вопросов. Каков уровень двигательной активности пациентов до и после операции? Насколько быстро пациенты достигают среднего уровня активности соответствующей возрастной группы? Как связаны показатели двигательной активности с функциональным исходом?
Материалы и методы
В период с января 2016 года по сентябрь 2017 года измерение двигательной активности было выполнено у 87 пациентов, подвергшихся односторонней операции эндопротезирования тазобедренного сустава, и 20 здоровых добровольцев без признаков остеоартрита (группа сравнения). Критерием включения для обеих групп являлся возраст от 18 до 50 лет. В основную группу включались пациенты с односторонним поражением тазобедренных суставов, в группу сравнения вошли добровольцы без очевидной патологии опорно-двигательной системы. Критериями исключения для обеих групп являлось отсутствие возможности проводить измерения уровня активности, индекс массы тела больше 35, тяжелые сопутствующие заболевания. Индекс массы тела должен был быть меньше 35, так как, по данным различной литературы, в которой авторы измеряли шаги с помощью шагомера, выявили закономерность, что при измерении шагов у пациентов с высоким индексом массы тела качество измерения может отличаться от более худых пациентов. Точность исследования при нормальных показателях составляет 98% [7].
Информация о пациентах включала: возраст, пол, клинический диагноз, индекс массы тела и оценку функции сустава с помощью опросников Harris Hip Score, Oxford Hip Score, WOMAC. Все операции выполнялись через прямой боковой доступ типа Хардинга, во всех случаях использовались эндопротезы бесцементной фиксации.
В основную группу вошли 54 женщины (62,1%) и 33 мужчины (37,9%), в группе сравнения женщин было меньше, 7 (35,0%), а мужчин больше, 13 (65,0%), но различия не были статистически значимыми, р=0,068. Средний возраст в основной группе составил 39,9 года (95% ДИ от 38,4 до 41,3), в группе сравнения 36,8 (95% ДИ от 33,1 до 40,6), р=0,158. В группе пациентов с идиопатическом остеоартрозом средний возраст был 46,46 (95%ДИ от 45,73 и до 47,18), в группе асептического некроза головки бедренной кости – 36,22 (95%ДИ от 33,98 и до 38,46), у пациентов с диспластическим остеоартрозом – 36,6 (95%ДИ от 34,59 и до 38,62) и в группе посттравматического поражения тазобедренного сустава 39,00 (95%ДИ от 34,27 и до 43,72).
Показанием к выполнению эндопротезирования у 26 пациентов (29,9%) послужило наличие терминальной стадии деформирующего остеоартроза, у 18 пациентов (20,7%) - наличие асептического некроза головки бедренной кости, у 28 пациентов (32,2%) – диспластический остеоартроз и в 15 случаях (17,2%) – посттравматическое поражение тазобедренного сустава.
Оценка двигательной активности пациентов выполнялась в течение 14 дней с помощью шагомеров (A&D Medical UW-101), поскольку в памяти шагомера записывается информация только за данный промежуток времени. Шагомеры калибровались с учетом размера шага и веса пациента. Информация о шагах собиралась в один климатический сезон, в одном регионе страны для исключения погодного фактора. Пациенты были проинструктированы измерять уровень своей активности в течение всего дня, т.е. во время ходьбы по улице и ходьбы дома. Пациенты обследовались не более чем за три недели до операции, затем через три и двенадцать месяцев после операции. Контрольная группа оценивалась единовременно в течение 2 недель. Информация, полученная от пациентов, содержала количество шагов и расстояние в течение дня, на протяжении 14 дней. Для оценки активности в течение года средние значения экстраполировались на весь период, т.е. среднее количество шагов в день умножалось на 365.
Статистический анализ выполнен в программном пакете SPSS 21.
Для количественных переменных рассчитывались средние показатели и 95% доверительные интервалы. Корреляционный анализ выполнялся с использованием коэффициентов Spearman и Pearson. Корреляция 0,6 и больше считалась сильной, от 0,6 до 0,4 - средней, 0,4 и меньше - не значимой.
Со всеми пациентами в течение года поддерживался контакт, заполнение опросников проводилось по телефону или во время контрольных осмотров врача.
Во всех случаях в исследуемой группе были получены хорошие и отличные результаты, осложнений отмечено не было. Удовлетворенность пациентов результатами операции: оцениваемая по 100-балльной VAS, составила в среднем 92,3 балла. Показатели шкалы Харриса улучшились с 32,0 (ДИ 95% 26,8-37,3) до 92,2 балла (ДИ 95% 91,4-95,1).
Улучшение состояния пациентов сопровождалось набором массы тела, несмотря на увеличение двигательной активности, индекс массы тела до операции составил в среднем 26,5 (95% ДИ от 26,0 до 26,9), но в течение 12 месяцев после операции увеличился на 16,2%, составив в среднем 30,8 (95% ДИ от 30,1 до 31,5). Индекс массы тела уменьшился только у 2 пациентов (2,3%), в остальных наблюдениях пациенты после операции набрали вес, при этом максимальное увеличение индекса массы тела составило 48,1% с 30,8 до 45,7.
Тем не менее в данной группе наблюдения не было пациентов, у которых двигательная активность после операции уменьшилась. Двигательная активность, оцениваемая по среднему количеству шагов, выросла в среднем на 23,7% в сравнении с дооперационными показателями: с 4,77 тысячи (95% ДИ от 4,51 до 5,03 тысячи) шагов в день до 5,9 тысячи шагов (95% ДИ от 5,6 до 6,2 тысячи). Средняя степень послеоперационной активности достигалась пациентами в срок от 38 до 102 дней (в среднем 67,4 дня).
При этом уровень активности до операции незначительно различался в этиологических группах пациентов. У пациентов с идиопатическим остеоартрозом количество шагов в день увеличилось с 4797,57 (95%ДИ от 4238,40 и до 5356,75) перед операцией до 6008,77 (95%ДИ от 5421,77 и до 6595,76) после, в группе асептического некроза головки бедренной кости – с 4837,33 (95%ДИ от 4115,91 и до 5558,75) до 5971,39 (95%ДИ от 5127,92 и до 6814,86), у пациентов с диспластическим остеоартрозом – с 4864,46 (95%ДИ от 4455,11 и до 5237,82) до 5978,53 (95%ДИ от 5537,23 и до 6419,84) и в группе посттравматического поражения тазобедренного сустава с 4501,33 (95%ДИ от 3984,92 и до 5017,74) до 5563,93 (95%ДИ от 4936,53 и до 6191,35) (рис. 1, 2).
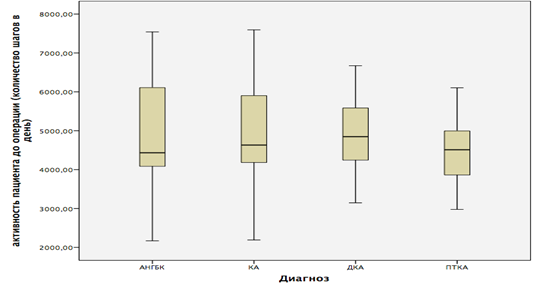
Рис. 1. Двигательная активность пациентов после операции в зависимости от этиологического диагноза. АНГБК – асептический некроз головки бедренной кости;
КА – коксартроз; ДКА – диспластический коксартроз; ПТКА – посттравматический коксартроз
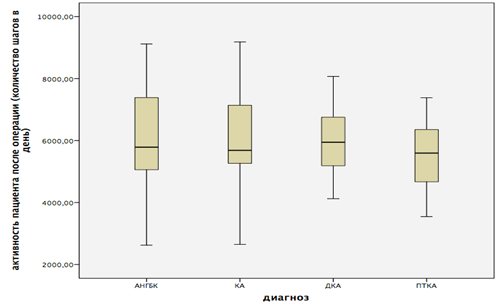
Рис. 2. Двигательная активность пациентов после операции в зависимости от этиологического диагноза. АНГБК – асептический некроз головки бедренной кости;
КА – коксартроз; ДКА – диспластический коксартроз; ПТКА – посттравматический коксартроз
Средний возраст в случае различных этиологических диагнозов незначительно отличался. Так, у пациентов с идиопатическим коксартрозом средний возраст составил 46,5 года (95%ДИ от 45,7 до 47,2). В группе пациентов с асептическим некрозом головки бедренной кости был наименьшим и составил 36,2 года (95%ДИ от 34,0 до 38,5). У пациентов с диспластическим коксартрозом возраст был чуть выше, чем в группе с асептическим некрозом головки бедренной кости, и составлял 36,6 года (95%ДИ от 34,6 до 38,6). В группе пациентов с посттравматическими изменениями тазобедренного сустава средний возраст составил 39,0 лет (95%ДИ от 34,3 до 43,7). В группе посттравматического поражения тазобедренного сустава наблюдалась самая низкая активность, связанная с тяжестью поражения, несмотря на средний возраст, но при этом после операции уровень активности также вырос до средних показателей здоровых пациентов.
Повышенная двигательная активность коррелировала с более высокими показателями опросников. Коэффициент корреляции Пирсона для шкалы Харриса составил R=0,671, p=0,01, а для шкалы Оксфорд – R=0,556, p=0,01. Шкала WOMAC показала наименее выраженную связь с двигательной активностью, коэффициент корреляции Пирсона составил R=0,382, p=0,01. Отмечалась устойчивая корреляция между предоперационным уровнем активности и послеоперационными показателями, коэффициент корреляции Пирсона составил R=0,9 (p=0,01); чем активнее пациенты были до операции, тем более высокие показатели активности они демонстрировали в послеоперационном периоде.
Индекс массы тела в контрольной группе составил 28,2 (95% ДИ от 25,3 до 32,9), р =0,101. Двигательная активность составила в среднем 5,9 тысячи шагов (95% ДИ от 5,3 до 6,4 тысячи), р=0,734.
Полноценная корректная оценка результатов эндопротезирования тазобедренного сустава – трудоемкая задача, которая может быть решена только в долгосрочных проспективных исследованиях. Тем не менее при эндопротезировании ТБС у пациентов молодого возраста необходимо, помимо выживаемости и функционального результата, в обязательном порядке анализировать двигательный режим и темпы износа узла трения искусственного сустава [8; 9], поскольку для понимания зависимости выживаемости эндопротезов от степени двигательной активности пациентов необходимо владеть информацией о реальной нагрузке, испытываемой эндопротезом. В нашем исследовании при среднем возрасте пациентов 39,9 года средний уровень двигательной активности увеличился на 23,7%, с 4,77 тысячи шагов в день до 5,9 тысячи. Лучшие показатели ежедневной активности коррелировали с более высокими показателями шкалы Харриса и Оксфорд, что подчеркивает важность этого параметра. Большинство пациентов молодого возраста в течение 1,5-2 месяцев достигают показателей, которые соответствуют среднему уровню активности здоровых людей, что, с одной стороны, свидетельствует о высокой эффективности операции по замене сустава. Однако, с другой стороны, если экстраполировать эти данные на среднегодовые показатели, получится цифра, превышающая 2 миллиона шагов в год, что существенно превышает расчетную нагрузку на трущиеся поверхности и в перспективе повышает вероятность развития остеолиза на фоне избыточного истирания узла трения. Соответственно в этой группе пациентов целесообразно использовать альтернативные пары трения, исключая пару трения металл-металл [10], обеспечивающие пониженный износ узла трения и способные потенциально повысить срок службы искусственного сустава.
Великолепные показатели износа, демонстрируемые поперечно связанным полиэтиленом в трибологических испытаниях и среднесрочных наблюдениях, позволяют докторам все чаще использовать пары трения диаметром более 32 мм, что обеспечивает близкую к нормальной биомеханику тазобедренного сустава [9; 10]. Однако клинические показатели, основанные на данных национальных регистров и метаанализов, свидетельствуют об ухудшении выживаемости при увеличении диаметра пары трения более 32 мм [11]. Исключение составляют только керамо-керамические пары трения, позволяющие увеличить диаметр без снижения выживаемости [12]. Однако другие проблемы, связанные с применением пары трения керамика-керамика, не позволяют увидеть разницы в выживаемости в первые 10-12 лет после эндопротезирования. Лишь в ежегодном отчете Австралийского регистра артропластики 2016 года на сроке в 15 лет накопленная частота ревизий у пациентов моложе 55-летнего возраста составила 6,6%, что является наименьшим показателем, зафиксированным в эти сроки [13]. Таким образом, требуется дальнейшее изучение выживаемости эндопротезов с различными парами трения в зависимости от степени двигательной активности пациентов.
Это высокотехнологичное оперативное удаление родного нежизнеспособного сустава с последующей имплантацией искусственного ТБС (эндопротеза). Во всем мире ежегодно выполняют до 500 тыс. подобных вмешательств людям с патологиями тазобедренного сустава, отзывы о лечении достаточно хорошие. Процент развития серьезных послеоперационных осложнений ничтожно мал – 1-2 %, что внушает большие надежды на успех.
Видео разрушения ТБС:
Ревизионная хирургия назначается в связи необходимостью замены изношенного протеза по окончании срока эксплуатации или вышедшего из строя устройства по причине возникших осложнений (инфекции, травм и пр.).
Показания
Если консервативное лечение уже не в силах улучшить качество жизни, хирургия является единственным способом возобновления нормальной амплитуды движений и ликвидации боли. Основные показания следующие:
- деформирующий артроз, или коксартроз (одна из самых частых причин дегенеративно-дистрофической природы);
- ревматоидного и любого другого системного генеза дегенеративно-дистрофические патологии с дислокацией в ТБ отделе;
- перелом шейки бедра (вторая по распространенности проблема, нуждающаяся зачастую в срочной установке эндопротеза);
- врожденная или приобретенная дисплазия (вывих) ТБС (преимущественно встречается первый тип аномалии);
- асептический некроз бедренной головки, то есть омертвение хряща вследствие локального нарушения кровообращения.
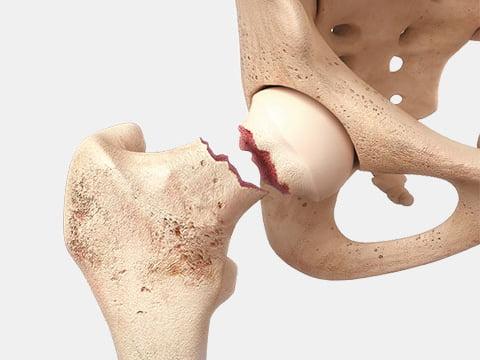
Один из видов перелома шейки бедра.
При переломах шейки перспективы на восстановление самые что ни на есть отличные, поскольку до травмы хромоты еще не было.

Пожилым людям такое лечение может существенно продлить жизнь за счет сохранения движения.
Еще недавно после переломов ТБС пациент был приковыван к постели, где он доживал максимум свой последний год. В травматологии, попросту не было еще способа установки искусственного сустава. Сегодня если своевременно поменять шейку сустава вместе с головкой бедра на долговечный имплантат, человек продолжает жить как и до травмы. Особенно актуальным такая хирургия является для пожилых людей, у которых срастание костей проблематично.
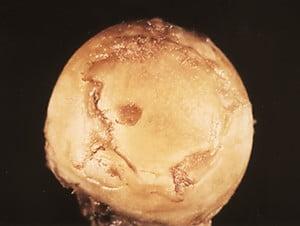
Поверхность головки ТБС на последней стадии артроза.
Процедура учитывает возрастное бессилие организма – агрессивным методам наркоза (общей анестезии) пожилого человека не подвергают, обезболивание может проводиться при помощи высокоэффективной и безопасной местной анестезии. После операции разрешается ранняя активизация пациента, при этом реабилитация проходит относительно легко и быстро.
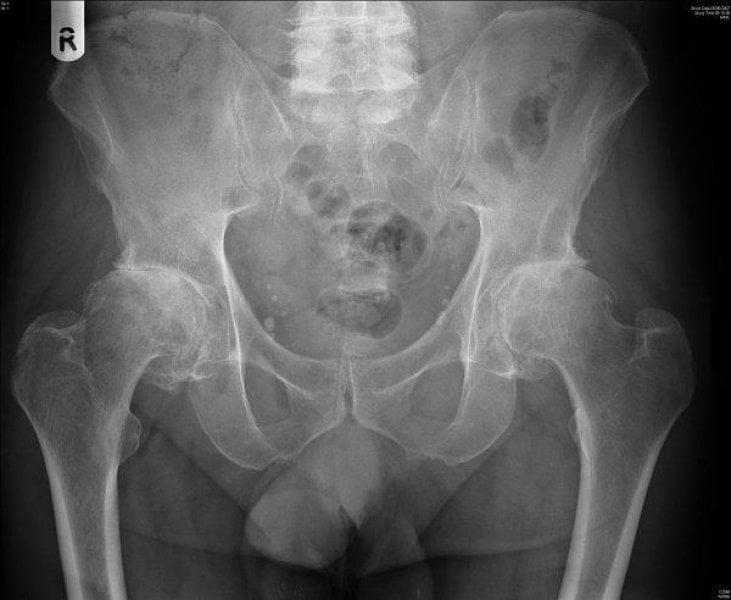
Двухсторонний коксартроз, обратите внимание на симметричное отсутствие суставной щели обоих суставов.
Отметим, жидкое протезирование не лечит суставы. Если кто-то все еще надеется на чудодейственное исцеление необратимых изменений посредством внутрисуставных инъекций, раскроем секрет, он попросту теряет деньги и время. Хрящ уже не восстановится, если имеется коксартроз 3 степени, и уколы здесь делать бессмысленно.
Противопоказания
Их не много, что дает возможность довольно широко применять методику, дарить пациентам свободу и легкость движений, причем даже людям преклонных лет:
- сердечный порок с критическим сбоем ритма сердца;
- тяжелой формы дыхательная и сердечно-сосудистая недостаточность;
- хронические заболевания в декомпенсированной фазе;
- сложно поддающийся контролю сахарный диабет;
- местные инфекционные и воспалительные процессы;
- общие инфекционно-воспалительные патологии в обострении;
- серьезные психические нарушения;
- ярко выраженный остеопороз костных тканей;
- венозный тромбоз конечностей;
- ожирение 3 степени (условное противопоказание);
- непереносимость материалов эндопротеза и используемых медикаментов.
Лучшие клиники эндопротезирования тазобедренного сустава, например, в Чехии, Германии, Израиле, принимают людей, которым было отказано в лечении в медучреждениях на территории своего государства.
Виды операций
В зависимости от характера поражений ТБС подбирается хирургическая техника. Если необходима полная замена, будет применен тотальный эндопротез; если обновление поверхности головки, тогда берется поверхностного вида имплантат; и т.д.
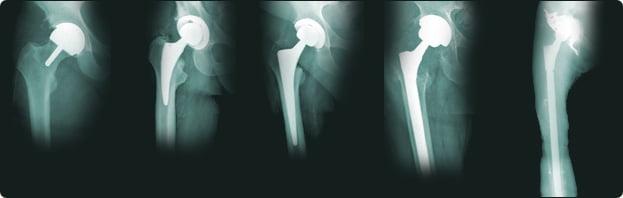
Разные виды, от частичного, до онкологического.
Хирургический подход может быть:
Малоинвазивный способ
В таком медицинском направлении, существует две хирургические техники выполнения артропластики:
Оперировать технически намного проще, если операционная рана будет большой. Поэтому ортопеды-травматологи утверждают, что классическая процедура на крупных суставах, все же, в неоспоримом приоритете.
Во многих клиниках практикуют малоинвазивный подход, используя почти в 2 раза меньший разрез, чем при традиционном вмешательстве. Однако и передовые хирурги с достаточным опытом все больше сходятся во мнении, что лучше лишний раз не рисковать, а использовать проверенную, традиционно устоявшуюся тактику, стандарт протезирования – создавать аккуратный разрез с прямого бокового доступа, длиной приблизительно в 13 см.
Согласно минимально инвазивному приему разрез равен примерно 7 см. Наиболее часто применяемые доступы, обеспечивающие менее травматичный с точки зрения физиологии подход, задне- и переднебоковые. Достоинствами миниинвазивного вида являются сохранность отводящих мышц, компактность операционной раны, ускоренный темп реабилитационного восстановления. Клинические исследования показывают, что интраоперационные кровопотери при щадящем вмешательстве незначительные, болевой синдром в постоперационную фазу менее выражен по сравнению со стандартной процедурой.
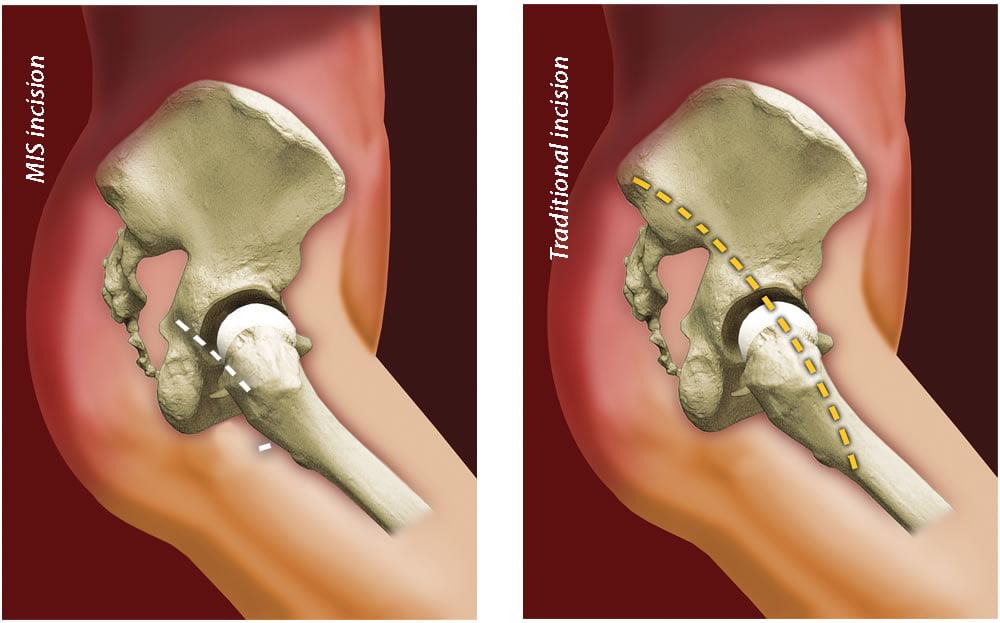
Наглядное сравнение размеров разрезов при классической(справа) и малоинвазивной(слева) методике.
Госпитализация
Всю необходимую информацию относительно подготовительных предоперационных мероприятий предоставляет лечащий доктор. Также на этой стадии хирург определяется с выбором эндопротеза и планирует каждый шаг, а анестезиолог подбирает подходящий вид анестезии на основании показателей здоровья пациента.
В клинике поступившего больного тщательно обследуют различные специалисты:
- осмотр у основного специалиста (ортопеда-травматолога);
- рентген, МРТ, УЗИ т/б сустава, при необходимости эндоскопическое обследование проблемного отдела;
- консультация узкопрофильных врачей (терапевт, кардиолог, иммунолог, анестезиолог, стоматолог, гастроэнтеролог и пр.);
- общий и биохимический анализ крови;
- коагулограмма (определяет работу системы гемостаза, в частности механизм и время свертываемости крови);
- тест на группу и резус-фактор крови;
- клинический анализ мочи;
- флюорография;
- электрокардиограмма.
Анестезия
Теперь осветим главные моменты, касающиеся наркоза, который применяется при замене двух тазобедренных суставов. По правилам допускается использование общей (полной эндотрахеальной), спинальной, эпидуральной анестезии или комбинацию двух последних видов.
К первому методу обращаются в крайне редких случаях, почти 90% операций выполняется либо под спинальным, либо под эпидуральным обезболиванием, оба подхода относятся к местному (регионарному) типу наркоза и не сопровождаются отключением сознания.
- Если вам будет показана спинальная анальгезия, тогда в субарахноидальное пространство позвоночника будет внедрена ультратонкая игла, через которую анестезиолог в спинномозговую жидкость произведет введение оптимальной дозы раствора-анестетика, за счет чего произойдет блокада передачи нервных импульсов.
Сам укол практически безболезненный.
- Если эпидурально, тогда наркоз будет подаваться через тонкий катетер в перидуральное пространство позвоночного столба. Такой прием приводит к полной потери болевой чувствительности в активной зоне оперирования.

Частичный наркоз лучше как для врача, так и для пациента.
Ход операции
Хирург самостоятельно определяет, по какой технологии производить замену, какой применить доступ и какую модель импланта устанавливать, исходя из конкретной клинической ситуации. А сейчас проведем краткое описание этапов хирургии.
- После действия анестезии и широкой антисептической обработки кожных покровов, коагулятором или скальпелем выполняется разрез по межвертельной линии до открытия сустава.
- Далее выполняется под правильным углом и уровнем пересечение бедренной кости в зоне шейки. Разверткой врач создает канал в подвергнувшемся остеотомии трубчатом элементе.
- Затем в созданный выпор вставляют клиновидную ножку, которая идеально должна совпадать с его параметрами, поэтому обработка данной кости должна пройти на безупречном уровне. На конусообразную верхушку ножки насаживается шаровидное тело имплантата.
- Сзади или спереди, в зависимости от примененного доступа, бедро смещают в сторону и приступают к подготовке вертлужной впадины. Используя долото и фрезы, специалист всецело удаляет гиалиновый хрящ с ее днища. Имплантат (чашу) вставляют в очищенное ложе. В него помещают полиэтиленовый вкладыш.
- Осуществляется вправление компонента бедра в чашку. После в рану ставится дренаж, рассеченные ткани ушиваются, на конечность накладывается повязка.
Принцип хирургии при всех видах оперативных вмешательств, о которых мы упомянули ранее, почти одинаков.
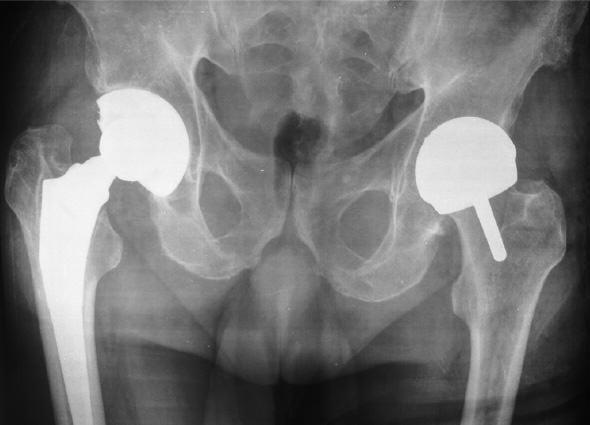
Интересный случай, двухсторонняя замена ТБС, но по разным технологиям. Слева тотальное протезирование, справа поверхностное.
Одновременное двустороннее эндопротезирование ТБС, рекомендуется в исключительно редких ситуациях, операционная травма будет больше, а, следовательно, и риск осложнений возрастет.
Виды фиксации сустава
В ортопедии и травматологии разработаны 3 способа фиксации, это:
- цементный;
- бесцементный;
- комбинированный.

Вертлужные компоненты импланта ТБС, розовая поверхность из керамики, белая из полиэтилена.
Бесцементная фиксация – это самый распространенный прием. Его принцип заключается в заколачивании деталей, у которых поверхность шероховатая, в подготовленные кости. Сразу, естественно, прочной связи с костями не свершится, имплантат должен хорошо обрасти соединительнотканными структурами, на что уйдет до 3 месяцев.
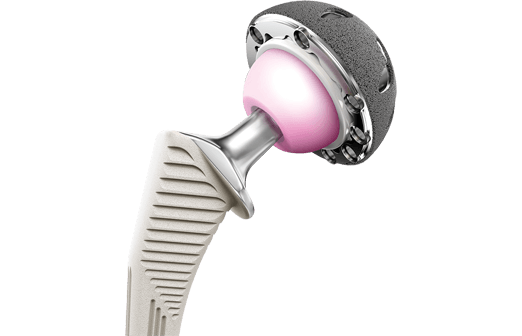
Комбинированное протезирование – это сочетание двух рассмотренных технологий единовременно в ходе одной операции. Подобной версии технология предназначена для тех, у кого обнаружена различная плотность кости бедра и таза. Когда какая-то из костей имеет хорошие показатели минеральной плотности, в то время как другая находится в неудовлетворительном состоянии.
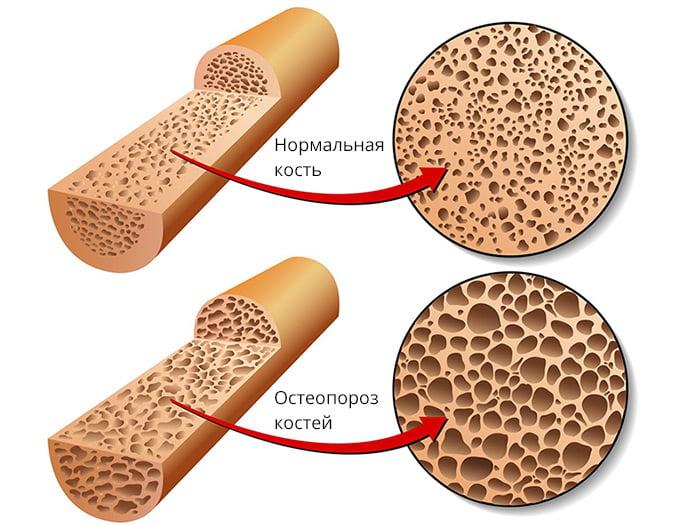
Остеопороз как видите делает кость рыхлее.
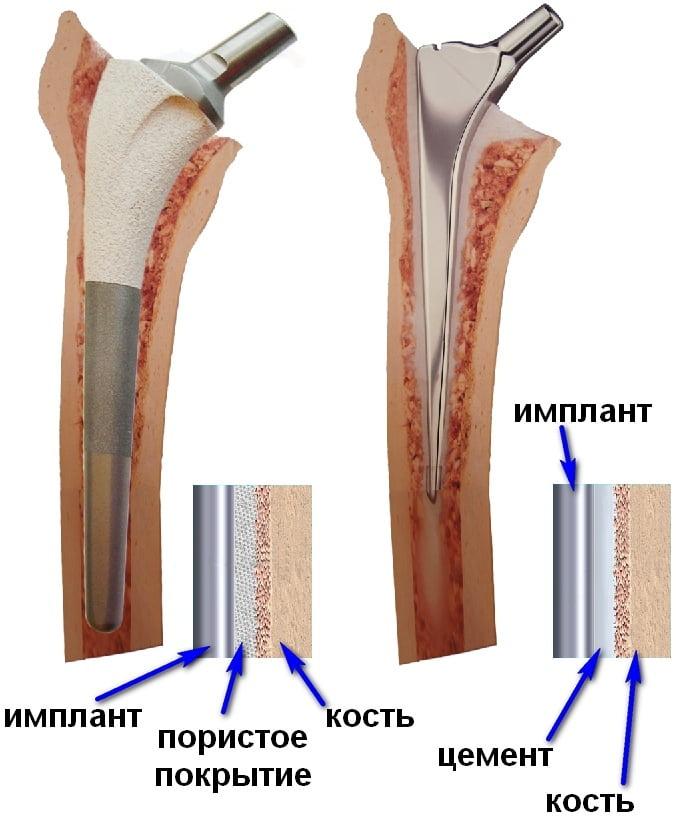
Именно состояние кости определяет какой тип фиксации будет использован.
Виды эндопротезов
Эндопротезная продукция, представлена следующими производителями:
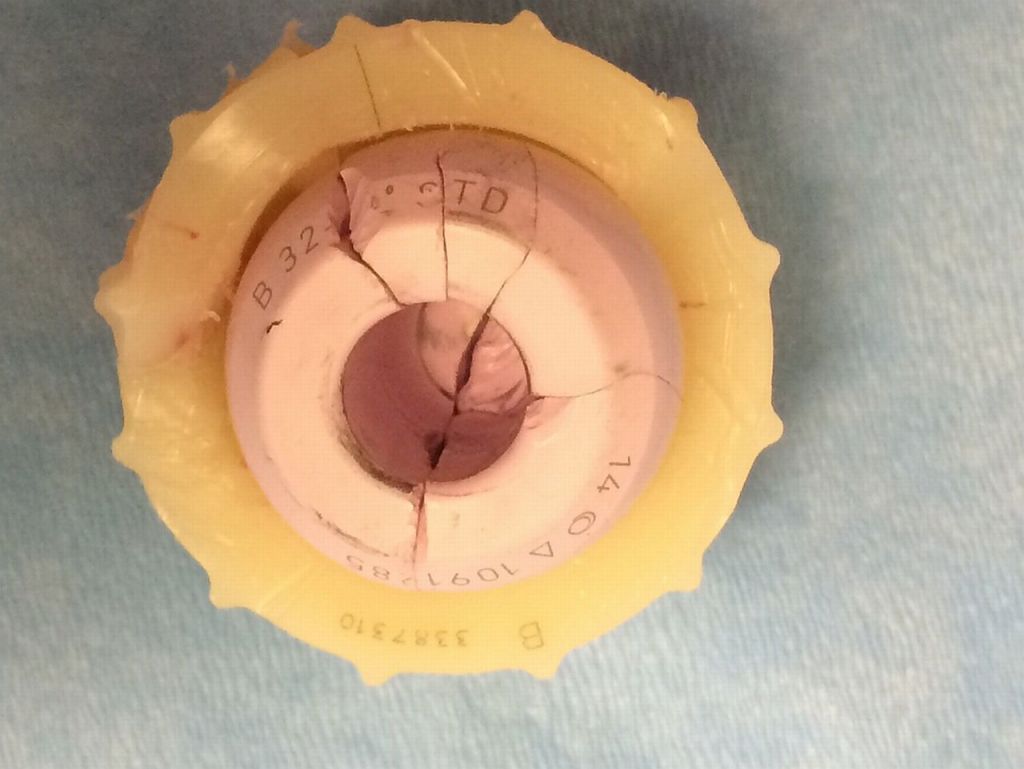
Керамика может треснуть, и если этому суждено случиться, то это в равной степени может произойти независимо от производителя импланта, потому что керамика всегда используется одной торговой марки.
Нельзя выделить из числа перечисленных брендов лучшего. Технологический подход, сборка, материалы, разнообразие типоразмеров, видовой ассортимент у всех одни и те же. Любой имплантат располагает самыми отменными техническими характеристиками. Поэтому отдавать свой приоритет какой-то определенной фирме попросту не имеет смысла. Высококачественные составляющие из диоксида циркония для всех моделей из керамики производит крупный концерн Ceramtech (США).

Линейка керамических компонентов.

Пара трения может быть разной: полностью металлической, керамической или в сочетании с полиэтиленом. Подбор узла трения определяется многими критериями: возрастом, весом, полом, физическим статусом, предполагаемым уровнем активности, заболеваниями в анамнезе и характером и тяжестью основной патологии. Больному может быть рекомендована любая из сочетающихся вариаций, фигурирующая в этом списке:
- металл-металл;
- металл-полиэтилен;
- керамика-керамика;
- керамика-полиэтилен.

Примеры полностью керамической пары трения.

В данном случае изображена комбинированная пара трения с полиэтиленом в качестве вертлужного компонента.
Объективно лучший вариант керамика-перекрестносвязанный полиэтилен. Это – современная комбинация, которая обеспечивает превосходную амортизацию и скольжение, отлично имитируя работу здорового сустава и гарантируя полную амплитуду движений.
Срок службы протеза
При корректно проведенной операции, грамотной реабилитации и строгом соблюдении правильного образа жизни, искусственный аналог тазобедренного сустава прослужит 20-30 лет. По возвращении домой необходимо не забывать об особенном режиме:
- чаще ходить, не допуская переутомления;
- ходить на костылях сколько сказал специалист, который наблюдает вас;
- продолжать заниматься лечебной гимнастикой, освоенной вами еще в медучреждении;
- следить за общим самочувствием и обращаться в больницу при любых недомоганиях, даже если они не связаны с протезированной ногой;
- следить за осанкой в момент сидения и в вертикальном положении;
- не перекрещивать ноги, кроме того, вы должны сидеть после эндопротезирования так, чтобы колени не находились на одном уровне с бедрами и, тем более, не превышали его;
- избегать интенсивных видов спорта, требующих совершения прыжков, поднятия тяжести, резких рывков телом и махов ногами.
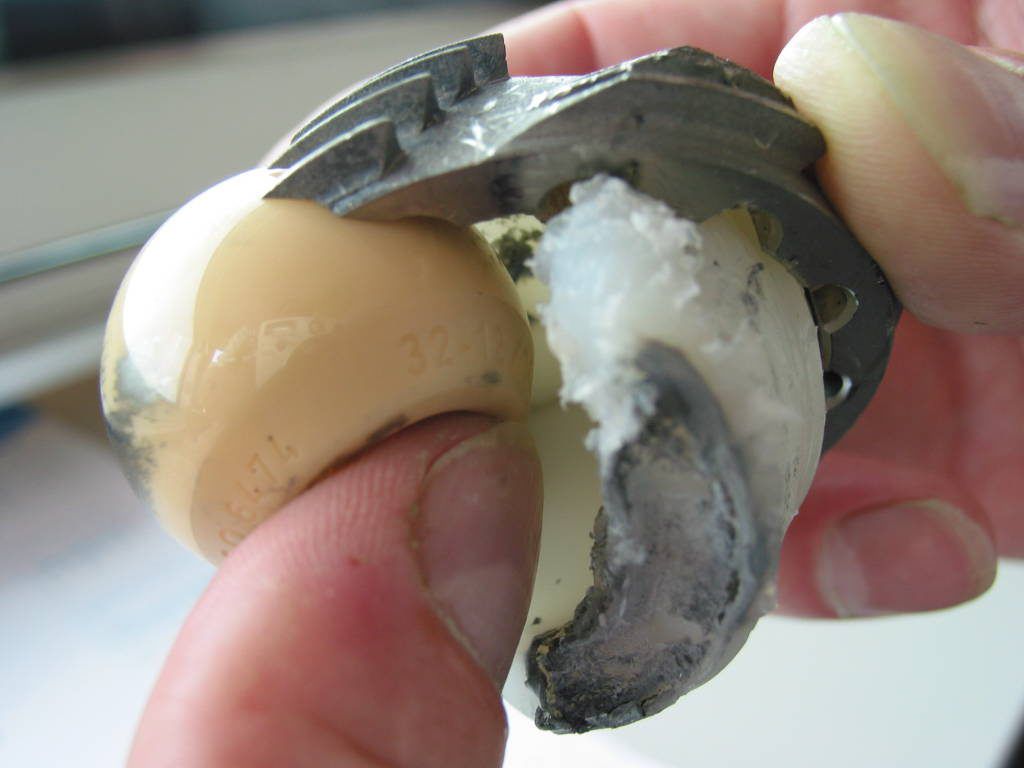
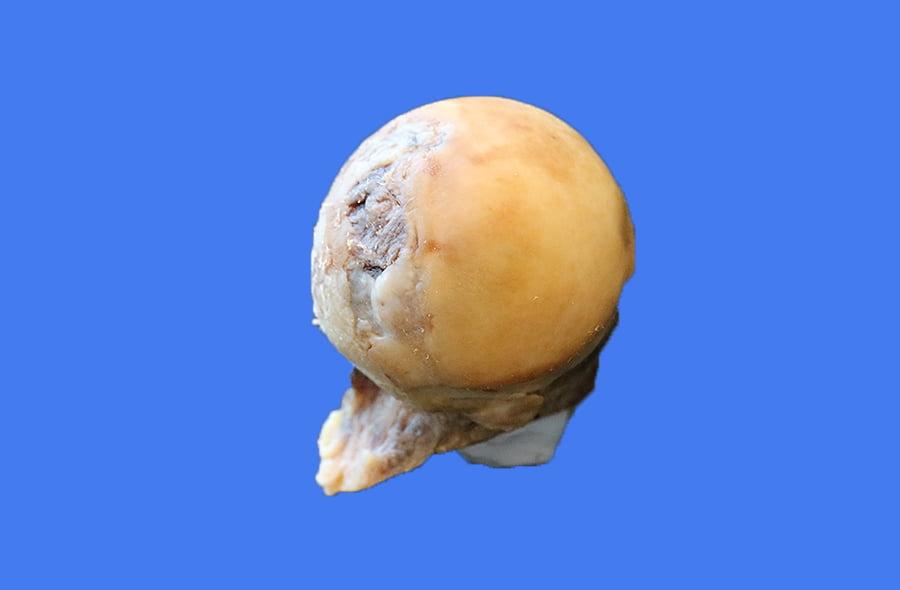
Такое лечение позволяет жить активно без боли, но перегибать палку не стоит, потому что может произойти такой износ импланта как на фото.
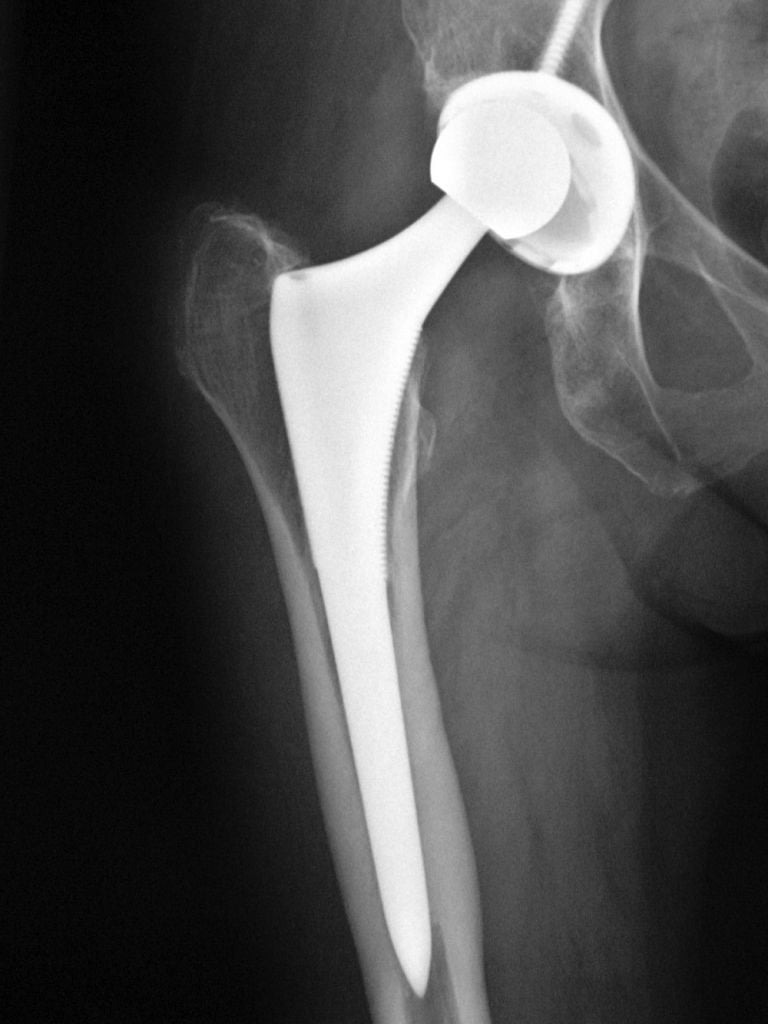
У слишком активных пациентов со временем может истончиться полиэтиленовый вкладыш, как это изображено на данном снимке.
Читайте также:


