Заболевания соединительной ткани нижних конечностей
Иммунные реакции сопровождаются воспалением, которое в норме является защитным процессом и стихает, когда отпадает необходимость в защите. Однако при аутоиммунных болезнях воспаление может стать хроническим и привести к повреждению нормальных тканей. Например, при ревматоидном артрите в результате хронического воспаления поражаются суставные хрящи. При этом страдают несколько суставов, так как антитела циркулируют с кровью по всему организму.
Воспаление может развиваться в соединительной ткани внутри и вокруг суставов, а также в других тканях организма. Обычно в воспалительный процесс вовлекаются и мышцы, а иногда и оболочки, которые окружают сердце (перикард), легкие (плевра) и даже мозг. Характер и тяжесть симптомов зависят от того, какие органы поражены.
Диагностика всех аутоиммунных болезней основывается на типичных симптомах, результатах общего осмотра и лабораторных анализов. Иногда бывают такие сочетания симптомов, что невозможно поставить диагноз конкретного заболевания соединительной ткани. В этих случаях диагностируется недифференцированное заболевание соединительной ткани или перекрестный синдром.
Болезни соединительной ткани часто сопровождаются анемией (снижением содержания эритроцитов в крови). При этом в анализах крови определяется увеличение скорости оседания эритроцитов (СОЭ). Увеличение этого показателя свидетельствует о наличии активного воспалительного процесса в организме, но не позволяет определить причину воспаления. Контролируя СОЭ, врач может определить, идет ли болезнь на убыль параллельно уменьшению симптомов.
При некоторых болезнях соединительной ткани в крови могут быть обнаружены необычные антитела. При наличии антител, специфических для какой-либо болезни, подтверждается диагноз соответствующей болезни. Например, антитела к двухспиральной ДНК выявляются почти исключительно при системной красной волчанке. Однако при большинстве болезней соединительной ткани антитела не специфичны. Например, у 70% больных ревматоидным артритом обнаруживаются антитела, называемые ревматоидным фактором, но у остальных больных их нет; кроме того, ревматоидный фактор может выявляться и при некоторых других заболеваниях. В таких случаях результаты лабораторного исследования хотя и помогают врачу в диагностике, но не позволяют поставить точный диагноз.
Когда болезнь поражает определенную ткань или орган, врач может сделать биопсию, то есть взять образец ткани из этого органа и исследовать ее под микроскопом. Результаты позволяют подтвердить диагноз и контролировать течение болезни.
Лечение зависит от вида болезни и степени ее тяжести. Лекарственная терапия назначается для уменьшения воспаления. Когда воспаление вызывает тяжелые симптомы или угрожает жизни, интенсивное лечение должно быть начато немедленно.
К лекарствам, уменьшающим воспаление, относятся нестероидные противовоспалительные средства (НПВС), например аспирин и ибупрофен, которые применяются при легких формах указанных заболеваний и внезапных обострениях. Эти препараты обладают также болеутоляющим действием. Некоторые НПВС можно приобрести без рецепта, но препараты, содержащие их в высоких дозировках, как правило необходимых при лечении аутоиммунных болезней, продаются по рецепту. Если лекарство принимается в средних дозах в течение недолгого времени, побочные эффекты (наиболее частый из них – расстройство желудка) чаще всего незначительны. Но бывают и тяжелые множественные побочные эффекты, особенно если лекарство принимается в высоких дозах или в течение длительного времени.
Кортикостероиды – синтетические препараты естественных гормонов; они обладают очень мощным противовоспалительным действием. Эти препараты назначаются внутрь или в инъекциях. Преднизолон – наиболее широко используемый кортикостероид – принимают внутрь. Низкие дозы кортикостероидов иногда приходится принимать в течение нескольких месяцев или лет даже после того, как воспаление подавлено более высокими дозами препаратов. По сравнению с НПВС кортикостероиды вызывают гораздо более тяжелые побочные эффекты – повышение уровня сахара в крови, увеличение риска инфекционных осложнений, остеопороз, задержку воды в организме и повреждение кожи. Во избежание этого врач обычно назначает минимально эффективную дозу, особенно для длительного лечения.
Иммунодепрессанты (препараты, подавляющие иммунитет), такие как метотрексат, азатиоприн и циклофосфамид, подавляют иммунную реакцию и тем самым уменьшают воспаление. Эти лекарства (некоторые из них используются также для лечения онкологических заболеваний) могут иметь опасные побочные эффекты. При длительном применении азатиоприна и циклофосфамида увеличивается риск развития отдельных видов злокачественных новообразований. Некоторые иммунодепрессанты негативно влияют на репродуктивную (детородную) функцию. Из-за подавления иммунитета самые обычные инфекции могут представлять угрозу для жизни. Поэтому наиболее мощные иммунодепрессанты, как правило, назначаются только в тяжелых случаях.
Системные заболевания соединительной ткани
Системные заболевания соединительной ткани, или диффузные заболевания соединительной ткани – группа заболеваний, характеризующихся системным типом воспаления различных органов и систем, сочетающимся с развитием аутоиммунных и иммунокомплексных процессов, а также избыточным фиброзообразованием.
Группа системных заболеваний соединительной ткани включает в себя следующие заболевания:
1) системная красная волчанка;
2) системная склеродермия;
3) диффузный фасциит;
4) дерматомиозит (полимиозит) идиопатический;
5) болезнь (синдром) Шегрена;
6) смешанное заболевание соединительной ткани (синдром Шарпа);
7) ревматическая полимиалгия;
8) рецидивирующий полихондрит;
9) рецидивирующий панникулит (болезнь Вебера – Крисчена).
Кроме того, в настоящее время к этой группе относят болезнь Бехчета, первичный антифосфолипидный синдром, а также системные васкулиты.
Системные заболевания соединительной ткани объединены между собой основным субстратом – соединительной тканью – и схожим патогенезом.
В настоящее время доказано, что при системных заболеваниях соединительной ткани происходят глубокие нарушения иммунного гомеостаза, выражающиеся в развитии аутоиммунных процессов, то есть реакций иммунной системы, сопровождающихся появлением антител или сенсибилизированных лимфоцитов, направленных против антигенов собственного организма (аутоантигенов).
Кроме близкого патогенеза, для всех системных заболеваний соединительной ткани являются характерными следующие черты:
1) мультифакториальный тип предрасположения с определенной ролью иммуногенетических факторов, связанных с шестой хромосомой;
2) единые морфологические изменения (дезорганизация соединительной ткани, фибриноидные изменения основного вещества соединительной ткани, генерализованное поражение сосудистого русла: васкулиты, лимфоидные и плазмоклеточные инфильтраты и др.);
3) схожесть отдельных клинических признаков, особенно в ранней стадии болезни (например, синдром Рейно);
4) системность, полиорганность поражения (суставы, кожа, мышцы, почки, серозные оболочки, сердце, легкие);
5) общие лабораторные показатели активности воспаления;
6) общие групповые и характерные для каждой болезни иммунологические маркеры;
7) близкие принципы лечения (противовоспалительные средства, иммуносупрессия, экстракорпоральные методы очищения и пульскортикостероидная терапия в кризовых ситуациях).
Этиология системных заболеваний соединительной ткани рассматривается с позиций мультифакторной концепции аутоиммунитета, согласно которой развитие этих болезней обусловлено взаимодействием инфекционных, генетических, эндокринных и внешнесредовых факторов (т. е. генетическая предрасположенность + внешнесредовые факторы, такие как стресс, инфекция, переохлаждение, инсоляция, травма, а также действие половых гормонов, в основном женских, беременность, аборты – системные заболевания соединительной ткани).
Чаще всего внешнесредовые факторы либо обостряют скрыто протекающую болезнь, либо являются, при наличии генетической предрасположенности, пусковыми моментами возникновения системных заболеваний соединительной ткани. До сих пор ведутся поиски конкретных инфекционных этиологических факторов, в первую очередь вирусных. Возможно, что происходит еще внутриутробное инфицирование, об этом свидетельствуют эксперименты на мышах.
В настоящее время накоплены косвенные данные о возможной роли хронической вирусной инфекции. Изучается роль пикорнавирусов при полимиозите, РНК-содержащих вирусов – при кори, краснухе, парагриппе, паротите, системной красной волчанке, а также ДНК-содержащих герпетических вирусов – Эпштейна – Барр цитомегаловируса, вируса простого герпеса.
Хронизация вирусной инфекции связана с определенными генетическими особенностями организма, что позволяет говорить о нередком семейно-генетическом характере системных заболеваний соединительной ткани. В семьях больных, по сравнению с семьями здоровых и с популяцией в целом, чаще наблюдаются различные системные заболевания соединительной ткани, особенно среди родственников первой степени родства (сестер и братьев), а также более частое поражение монозиготных близнецов, чем дизиготных.
Многочисленными исследованиями показана ассоциация между носительством определенных HLA-антигенов (которые размещаются на коротком плече шестой хромосомы) и развитием конкретного системного заболевания соединительной ткани.
Для развития системных заболеваний соединительной ткани наибольшее значение имеет носительство II класса HLA-D-генов, локализующихся на поверхности В-лимфоцитов, эпителиальных клеток, клеток костного мозга и др. Например, системная красная волчанка ассоциируется с DR3-антигеном гистосовместимости. При системной склеродермии отмечается накопление Al, В8, DR3-антигенов в сочетании с DR5-антигеном, а при первичном синдроме Шегрена – высокая связь с HLA-B8 и DR3.
Таким образом, механизм развития таких сложных и многоликих заболеваний, какими являются системные заболевания соединительной ткани, до конца не изучен. Однако практическое применение диагностических иммунологических маркеров заболевания и определение его активности позволит улучшить прогноз при этих заболеваниях.
Остановимся подробнее на некоторых наиболее значимых системных заболеваниях соединительной ткани.
Системная красная волчанка
Системная красная волчанка – это хроническое прогрессирующее полисиндромное заболевание преимущественно молодых женщин и девушек (соотношение больных женщин и мужчин 10: 1), которое развивается на фоне генетически обусловленного несовершенства иммунорегуляторных механизмов и ведет к неконтролируемому синтезу антител к собственным тканям организма с развитием аутоиммунного и иммунокомплексного хронического воспаления (В. А. Насонова, 1989 г.).
По своей сущности системная красная волчанка является хроническим системным аутоиммунным заболеванием соединительной ткани и сосудов, характеризующимся множественными поражениями различной локализации: кожи, суставов, сердца, почек, крови, легких, центральной нервной системы и других органов. При этом висцеральные поражения определяют течение и прогноз заболевания.
Распространенность системной красной волчанки увеличилась за последние годы с 17 до 48 человек на 100 тыс. населения. Вместе с тем улучшение диагностики, раннее распознавание доброкачественных вариантов течения со своевременным назначением адекватного лечения привели к удлинению продолжительности жизни больных и улучшению прогноза в целом.
Начало заболевания часто можно связать с длительным пребыванием на солнце в летний период, перепадами температуры при купании, введением сывороток, приемом некоторых лекарственных средств (в частности, периферических вазодилататоров из группы гидролазинов), стрессами, а также системная красная волчанка может начаться после родов, перенесенного аборта.
Подострое течение. Начало как бы исподволь, с общих симптомов, артралгий, рецидивирующих артритов, разнообразных неспецифических поражений кожи в виде дисковидной волчанки, фотодерматозов на лбу, шее, губах, ушах, верхней части груди. Отчетлива волнообразность течения. Развернутая картина болезни формируется через 2–3 года.
1) поражение сердца, чаще в виде бородавчатого эндокардита Либмана – Сакса с отложениями на митральном клапане;
2) часты миалгии, миозиты с атрофией мышц;
3) всегда присутствует синдром Рейно, довольно часто заканчивающийся ишемическим некрозом кончиков пальцев;
6) нефрит, который не достигает такой степени активности, как при остром течении;
7) радикулиты, невриты, плекситы;
8) упорные головные боли, утомляемость;
9) анемия, лейкопения, тромбоцитопения, гипергаммаглобулинемия.
Хроническое течение. Заболевание длительное время проявляется рецидивами различных синдромов: полиартрита, реже – полисерозита, синдромом дискоидной волчанки, синдромами Рейно, Верльгофа, эпилептиформным. На 5—10-м году болезни присоединяются другие органные поражения (преходящий очаговый нефрит, пневмонит).
В качестве начальных признаков заболевания следует отметить кожные изменения, лихорадку, исхудание, синдром Рейно, диарею. Больные жалуются на нервозность, плохой аппетит. Обычно, за исключением хронических олигосимптомных форм, заболевание прогрессирует достаточно быстро и развивается полная картина болезни.
При развернутой картине на фоне полисиндромности весьма часто начинает доминировать один из синдромов, что позволяет говорить о люпус-нефрите (наиболее часто встречающаяся форма), люпус-эндокардите, люпус-гепатите, люпус-пневмоните, нейролюпусе.
К поражениям кожных покровов относят капилляриты – мелкоотечную геморрагическую сыпь на подушечках пальцев рук, ногтевых ложах, ладонях. Встречается поражение слизистой оболочки твердого нёба, щек и губ в виде энантемы, иногда с изъязвлениями, стоматитом.
Довольно рано наблюдается выпадение волос, увеличивается ломкость волос, поэтому на этот признак следует обращать внимание.
Поражение серозных оболочек отмечается у подавляющего числа больных (90 %) в виде полисерозита. Наиболее часто встречаются плеврит и перикардит, реже – асцит. Выпоты необильные, с тенденцией к пролиферативным процессам, ведущим к облитерации плевральных полостей и перикарда. Поражение серозных оболочек кратковременно и обычно диагностируется ретроспективно по плевроперикардиальным спайкам или утолщению костальной, междолевой, медиастинальной плевры при рентгенологическом исследовании.
Поражение опорно-двигательного аппарата проявляет себя полиартритом, напоминающим ревматоидный артрит. Это наиболее часто встречающийся признак системной красной волчанки (у 80–90 % больных). Характерно преимущественно симметричное поражение мелких суставов кистей, лучезапястных, а также голеностопных суставов. При развернутой картине болезни определяется дефигурация суставов за счет периартикулярного отека, а в последующем – развитие деформаций мелких суставов. Суставной синдром (артрит или артралгии) сопровождается диффузными миалгиями, иногда тендовагинитами, бурситами.
Поражение сердечно-сосудистой системы встречается достаточно часто, примерно у трети больных. На различных этапах заболевания выявляют перикардиты с тенденцией к рецидивам и облитерации перикарда. Наиболее тяжелой формой поражения сердца является бородавчатый эндокардит Лимбана – Сакса с развитием вальвулитов митрального, аортального и трехстворчатого клапанов. При длительном течении процесса можно выявить признаки недостаточности соответствующего клапана. При системной красной волчанке достаточно часто встречается миокардит очагового (практически никогда не распознается) или диффузного характера.
В. А. Насонова обращает внимание на то, что поражения сердечно-сосудистой системы при системной красной волчанке имеют место чаще, чем это обычно удается распознать. Вследствие этого следует уделять внимание жалобам больных на боли в области сердца, сердцебиения, одышку и т. д. Больные системной красной волчанкой нуждаются в тщательном кардиологическом обследовании.
Поражение сосудов может проявляться в виде синдрома Рейно – расстройстве кровоснабжения кистей и (или) стоп, усиливающемся под воздействием холода или волнения, характеризующемся парестезиями, бледностью и (или) цианотичностью кожи II–V пальцев, их похолоданием.
Поражение легких. При системной красной волчанке наблюдаются изменения двоякого характера, как вследствие вторичной инфекции на фоне пониженной физиологической иммунологической реактивности организма, так и волчаночного васкулита легочных сосудов – люпус-пневмонита. Возможно также осложнение, возникающее как следствие люпус-пневмонита – вторичная банальная инфекция.
Если диагностика бактериальной пневмонии не представляет затруднений, то диагностика люпус-пневмонита иногда затруднительна вследствие ее мелкоочаговости с преимущественной локализацией в интерстиции. Люпус-пневмонит протекает либо остро, либо тянется месяцами; характеризуется малопродуктивным кашлем, нарастающей одышкой при скудных аускультативных данных и типичной рентгенологической картиной – сетчатым строением легочного рисунка и дисковидными ателектазами, преимущественно в средне-нижних долях легкого.
Поражение почек (волчаночный гломерулонефрит, люпус-нефрит). Часто является определяющим в исходе заболевания. Обычно он характерен для периода генерализации системной красной волчанки, однако иногда является и ранним признаком болезни. Варианты поражения почек различны. Очаговый нефрит, диффузный гломерулонефрит, нефротический синдром. Поэтому изменения характеризуются в зависимости от варианта либо скудным мочевым синдромом (протеинурией, цилиндрурией, гематурией), либо – чаще – отечно-гипертензивной формой с хронической почечной недостаточностью.
Поражение желудочно-кишечного тракта проявляется в основном субъективными признаками. При функциональном исследовании можно иногда обнаружить неопределенную болезненность в эпигастрии и в области проекции поджелудочной железы, а также признаки стоматита. В ряде случаев развивается гепатит – при обследовании отмечают увеличение печени, ее болезненность.
Поражение центральной и периферической нервной системы описывается всеми авторами, изучавшими системную красную волчанку. Характерно разнообразие синдромов: астено-вегетативный синдром, менингоэнцефалит, менингоэнцефаломиелит, полиневрит-радикулит. Поражения нервной системы возникают в основном за счет васкулитов. Иногда развиваются психозы – либо на фоне кортикостероидной терапии как ее осложнение, либо по причине ощущения безвыходности страдания. Может быть эпилептический синдром.
Синдром Верльгофа (аутоиммунная тромбоцитопения) проявляется высыпаниями в виде геморрагических пятен различной величины на коже конечностей, груди, живота, на слизистых оболочках, а также кровотечениями после незначительных травм.
Если определение варианта течения системной красной волчанки важно для оценки прогноза заболевания, то для определения тактики ведения больного необходимо уточнение степени активности патологического процесса.
Основные задачи комплексной патогенетической терапии:
1) подавление иммунного воспаления и иммунокомплексной патологии;
2) предупреждение осложнений иммуносупрессивной терапии;
3) лечение осложнений, возникающих в процессе проведения иммуносупрессивной терапии;
4) воздействие на отдельные, резко выраженные синдромы;
5) удаление из организма циркулирующих иммунных комплексов и антител.
Основным методом лечения системной красной волчанки является кортикостероидная терапия, которая остается средством выбора даже в начальных стадиях болезни и при минимальной активности процесса. Поэтому больные должны находиться на диспансерном учете с тем, чтобы при первых же признаках обострения заболевания врач своевременно мог назначить кортикостероиды. Доза глюкокортикостероидов зависит от степени активности патологического процесса.
При III степени активности – лечение в условиях специализированного или терапевтического стационара – пульстерапия глюкокортикостероидами, иммунодепрессанты. Пульстерапия: метипред – 1000 мг 3 дня подряд внутривенно капельно, одновременно глюкокортикостероиды per os – 40–60 мг в сутки до получения эффекта (снижение активности волчаночного процесса). Параллельно целесообразно делать плазмаферез 2–3—4 процедуры (с целью удаления ЦИК). В некоторых случаях можно проводить гемосорбцию.
Если нельзя использовать глюкокортикостероиды (непереносимость, резистентность), назначаются депрессанты в таблетках (метотрексат – 7,5 мг в неделю) или пульс-терапия: 20 мг/кг массы тела циклофосфамида 1 раз в месяц в течение 6 месяцев внутривенно с последующим плазмаферезом.
При уменьшении степени активности заболевания дозы глюкокортикостероидов снижают по 10 мг в неделю до 20 мг, а затем по 2,5 мг в месяц до поддерживающей дозы 5—10 мг в сутки. Никогда не отменять глюкокортикостероиды летом!
При II степени активности патологического процесса подавляющая доза преднизолона составляет 30–40 мг в сутки, а при I степени активности – 15–20 мг в сутки. Если через 24–48 ч состояние больного не улучшается, то первоначальную дозу увеличивают на 25–30 %, и если эффект наблюдается, то дозу оставляют без изменений. После достижения клиниколабораторного эффекта (снижение активности процесса), что обычно бывает после 2 месяцев кортикостероидной терапии, а при нефротическом синдроме или признаках поражения почек – спустя 3–6 месяцев, дозу преднизолона постепенно снижают до поддерживающей (5—10 мг), которую принимают годами.
Данный текст является ознакомительным фрагментом.
Дисплазия соединительной ткани – тяжелая патология, которая может развиться в любом сочленении. Несвоевременное лечение может стать причиной инвалидности. Поэтому при первых симптомах заболевания следует обратиться к врачу.
Что это такое
Соединительнотканная дисплазия – это заболевание, которому подвержены все органы и системы, в которых присутствует соединительная ткань. Заболевание генетически обусловлено, отличается широким спектром симптомов и вызывается нарушением выработки коллагена.
Так как наибольшее значение соединительная ткань играет в опорно-двигательном аппарате, большее число клинических признаков сосредоточено именно в этой сфере. За счет коллагена возможно сохранение форм, а эластин обеспечивает правильное сокращение и расслабление.
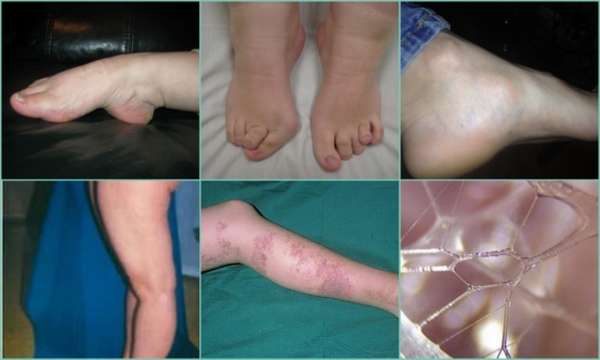
Дисплазия соединительной ткани является генетически предопределенной. Выявив болезнь, можно заранее предположить, как произойдет мутация. Из-за них возникают ненормальные структуры, которые неспособны выполнять стандартные нагрузки.
Классификация болезни
В МКБ-10 соединительнотканной дисплазии присвоен номер М35.7. Патология разделяется на две большие группы:
- Недифференцированная дисплазия,
- Дифференцированная дисплазия.
Недифференцированная форма встречается в 80% случаев. Проявляющиеся симптомы невозможно соотнести ни с каким существующим заболеванием. Признаки разрозненны, хотя по ним можно предположить наличие развивающейся патологии.
Дифференцированная дисплазия соединительной ткани имеет четко определенную форму наследования, характерный набор клинических симптомов и группу дефектов. Выделяют 4 основные формы:
- Синдром Марфана,
- Синдром вялой кожи,
- Синдром Эйлерса-Данло,
- Несовершенный остеогенез.
Для синдрома Марфана характерны следующие клинические особенности:
- Сколиозы,
- Отслоение сетчатки глаза,
- Чрезмерно высокий рост,
- Аномально длинные конечности,
- Голубые склеры глаз,
- Подвывихи хрусталика.
Наряду с этими симптомами дисплазии соединительной ткани, поражается сердце. Пациентам ставят диагноз пролапс митрального клапана, аневризму аорты и возможная последующая сердечная недостаточность.
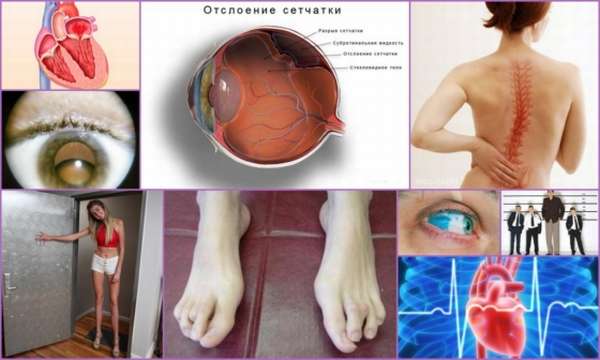
При синдроме вялой кожи соединительнотканная дисплазия выражается поражением волокон эластичности. Кожу легко растянуть, она способна образовывать свободные складки.
Для синдрома Эйлерса-Данло характерна аномальная подвижность суставов. Это приводит к частым вывихам, подвывихам и постоянным болям при движении.
При несовершенном остеогенезе в основе патологии лежит нарушение строения костной ткани. Ее плотность становится низкой, что приводит к особой хрупкости, частым переломам и медленному росту. У детей наблюдается неровная осанка.
Причины развития болезни
Причины развития дисплазии соединительной ткани связаны со следующими факторами:
- Наследование мутировавшего гена,
- Влияние внешних неблагоприятных факторов.
Аномалия развития может произойти на фоне нарушения белкового обмена и нехватки витаминно-минеральных соединений.
К внешним отрицательным факторам, способным повысить вероятность развития соединительнотканной дисплазии, относятся следующие:
- Наличие вредных привычек,
- Несбалансированное питание,
- Проживание на территории с плохой экологией,
- Перенесенный токсикоз во время беременности,
- Частые стрессовые ситуации,
- Тяжелая интоксикация в анамнезе,
- Нехватка магния в организме.
Все это способно увеличить риск развития соединительнотканной дисплазии. ДСТ чаще возникает из-за генетики, но при отсутствии патогенных факторов протекает легче.

Симптоматика заболевания
Определить соединительнотканную дисплазию можно по множеству характерных симптомов. Патология охватывает опорно-двигательную, сердечно-сосудистую, пищеварительную и другие системы.
Понимая, что такое дисплазия соединительной ткани, можно ожидать проявления следующих симптомов:
- Быстрая утомляемость,
- Слабость,
- Снижение работоспособности,
- Головные боли,
- Метеоризм,
- Боли в животе,
- Низкое давление,
- Частые патологии дыхательных путей,
- Низкий аппетит,
- Ухудшение самочувствия после небольших нагрузок.
У некоторых пациентов наблюдалась дисплазия мышечной ткани. Они чувствовали сильную слабость в мышцах.
Определить людей с дисплазией соединительной ткани можно по аномально большому росту или удлинении отдельных частей тела, по ненормальной хрупкости и болезненной худобе.
Дисплазия соединительной ткани у детей и взрослых может проявляться:
- Гипермобильностью,
- Контрактурой,
- Карликовостью,
- Хрупкостью.
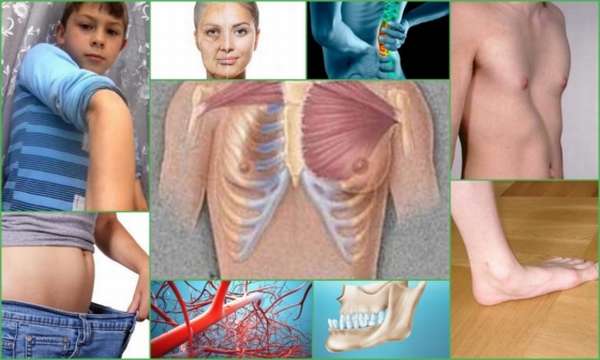
Внешние клинические симптомы включают:
- Снижение массы тела,
- Заболевания позвоночного столба,
- Изменение формы грудной клетки,
- Деформацию частей тела,
- Аномальную спосоность сгибать пальцы на 90 градусов в сторону запястья или выгибать локтевые суставы в обратную сторону,
- Отсутствие упругости кожи и ее повышенная растяжимость,
- Плоскостопие,
- Замедление и ускорение роста челюсти,
- Патологии сосудов.
Все эти нарушения свидетельствуют о наличии дисплазии соединительной ткани. У одного пациента может появиться несколько симптомов или целая группа. Все зависит от того, насколько сильно поразила патология и какого она типа.
Осложнения
Дисплазия соединительной ткани способна привести к следующим последствиям:
- Склонность к получению травм – вывихов, подвывихов и переломов,
- Системные патологии,
- Заболевания стопы, колена и бедренного сустава,
- Соматические патологии,
- Тяжелые сердечные заболевания,
- Психические расстройства,
- Патологии глаз.
Излечения от системной патологии не может гарантировать ни один врач, какие бы метод ни применялись. Однако грамотная терапия позволяет уменьшить опасность осложнений и повысить качество жизни пациента.
Диагностические меры
Диагностика дисплазии соединительной ткани проводится в медицинском учреждении. Вначале врач осматривает пациента, собирает информацию о генетической предрасположенности к данной патологии и ставит предположительный диагноз.
Для подтверждения заболевания необходимо будет пройти следующие исследования:
- УЗИ,
- МРТ,
- КТ,
- Электромиографию,
- Рентген костной ткани.
Поставить диагноз с помощью одного лишь метода невозможно. При подозрении на заболевание, может быть назначена генетическая экспертиза для выявления мутаций.
Чтобы определить, насколько сильно заболевание поразило внутренние органы, нужно посетить разных специалистов. Может потребоваться комплексное лечение нескольких систем одновременно.
Лечение
Лечение дисплазии соединительной ткани у взрослых пациентов проводится несколькими методами. Применяется медикаментозная и не медикаментозная терапия. Из-за разнообразия симптомов даже опытным врачам бывает сложно подобрать эффективные методики лечения и нужные препараты.
Медикаментозное лечение включает в себя заместительную терапию. Цель применения лекарственных средств – стимулировать выработку коллагена в организме. Это могут быть препараты следующих групп:
- Хондропротекторы (хондроитин и глюкозамин),
- Витамины (особенно группы Д),
- Комплексы микроэлементов,
- Препараты магния.
Терапия магнием – важная часть при борьбе с мышечной дисплазией. Этот микроэлемент выполняет множество функций и является незаменимым при поддержании следующих структур:
- Сердечная мышца,
- Дыхательные органы,
- Кровеносные сосуды.
Нехватка магния приводит к расстройствам в работе головного мозга. Пациенты сильно страдают от головокружения, головных болей и мигрени. Возможны судороги и нарушения ночного сна. Последствия мезенхимальной дисплазии можно снизить с помощью хорошо продуманной медикаментозной терапией.
Помимо приема лекарственных препаратов, назначенных врачом, при заболеваниях соединительной ткани важно заниматься укреплением мышц и костей другими методами. Только комплексный подход позволит сохранить нормальное качество жизни, несмотря на болезнь. Стоит рассмотреть несколько необходимых пациенту способов.
Все пациенты с врожденными патологиями соединительной ткани должны правильно составлять режим дня. Важно чередовать ночной отдых с разумной активностью в дневные часы. Чтобы выспаться, важно отводить не менее 8-9 часов.
При лечении детей следует обеспечить им полноценный дневной сон. Активный день всегда следует начинать с зарядки.

После консультации с лечащим врачом можно заняться спортом. Тренировки должны продолжаться всю жизнь. Важна регулярность.
Спорт не должен быть профессиональным, так как он будет способствовать частому получению травм, что при болезни соединительной ткани противопоказано. Щадящие спортивные тренировки позволят укреплять мышцы и сухожилия, не провоцируя развитие воспалительных и дистрофических процессов.
Следующие виды спорта рекомендованы при заболеваниях соединительной ткани:
- Плавание,
- Велосипед,
- Бадминтон,
- Ходьба по лестнице вверх,
- Частые прогулки пешком.
Регулярные дозированные занятия позволяют укрепить организм. Повышаются защитные силы, человек чувствует себя сильнее.
Массаж должен проводить медицинский работник. Курс процедур состоит из 20 сеансов. Особое внимание должно быть уделено спине, воротниковой зоне и суставам конечностей.
Рацион пациента должен быть богат следующей белковой пищей:
- Рыба,
- Мясо,
- Бобовые,
- Морепродукты.
Должен быть баланс между всеми важными витаминами и микроэлементами. Особенно нужно высокое содержание витамина С и Е.
Такое вмешательство проводится крайне редко при тяжелом течении патологии. Может быть проведено, если дисплазия вызвала нарушения, несущие опасность для жизни или наступление полной инвалидности.
Лечение назначает врач. Чем быстрее начать терапию, тем больше шансов на полное выздоровление. Поэтому важно при первых симптомах проконсультироваться со специалистом.
Читайте также:


