Признаки инфицирования эндопротеза коленного сустава

Увеличение средней продолжительности жизни, несомненно, положительная тенденция настоящего времени, но обратной стороной медали является не всегда высокое качество жизни, особенно в старшем возрасте. Одним из факторов, снижающих это качество, всё чаще становятся заболевания суставов. Боль и ограничение способности к движению при этих заболеваниях со временем значительно осложняют жизнь пациентам. Наиболее эффективным способом лечения в этих случаях считается хирургическое вмешательство. Для лечения пациентов с тяжелыми посттравматическими осложнениями и дегенеративными заболеваниями суставов оптимальным методом считается эндопротезирование. Однако, несмотря на то что после тотального эндопротезирования коленного сустава наблюдается значительное улучшение состояния пациента, существует риск осложнения в виде парапротезной инфекции, при котором увеличиваются сроки и стоимость лечения. Кроме того, инфекционное осложнение может привести к неблагоприятному исходу хирургического лечения. Согласно исследованиям, проведенным в ряде разных центров, после тотального эндопротезирования коленного сустава инфицирование происходило в 0,5-5% случаев 1.
I. Uçkay с соавт. выполнили ретроспективный анализ 6101 случая реэндопротезирования крупных суставов с 1996 по 2008 г. Из них 2099 случаев – после эндопротезирования коленного сустава. Всего было удалено 234 (11,15%) протеза коленного сустава, из них по поводу инфекции удалено 24 (1,14%) протеза. Полученные результаты позволили авторам сделать вывод, что парапротезная инфекция – редкое осложнение [4; 5].
Внедрение эндопротезирования в клиническую практику в России происходило постепенно, и первоначальные результаты не внушали оптимизма. По данным H.Н. Корнилова с соавт., частота инфекционных осложнений в некоторых лечебных учреждениях, где выполнялось лишь несколько эндопротезирований в год, достигала 17% [5; 6].
Волошин В.П. с соавт. проанализировали опыт лечения 66 пациентов с тотальным эндопротезированием крупных суставов. В 87,9% случаев (58 пациентов), в сроки от 1,5 до 3 лет после эндопротезирования, отмечалось развитие гнойной инфекции. Глубокое нагноение отмечено у 6 пациентов (9,1%). В итоге 10 пациентам было выполнено артродезирование коленного сустава аппаратом Илизарова [5; 7].
Т.А. Куляба с соавторами проанализировали результаты лечения 44 пациентов, у которых после первичного и ревизионного эндопротезирования коленного сустава развилось инфекционное воспаление. Происходило это в разные сроки, у 18 пациентов (40,1%) в раннем послеоперационном периоде, а у 26 (59,1%) в отдаленном, но так или иначе, купировать воспаление и сохранить эндопротез удалось только у 10 (22,7%) больных. В подавляющем большинстве случаев потребовалось провести двухэтапное хирургическое лечение, которое позволило купировать гнойный процесс в 89,3% случаев. Артродез был выполнен у 4 (9,1%) больных [5; 8].
Инфицирование может происходить через прямую или гематогенную передачу бактериальной флоры. Некоторыми примерами прямой передачи являются: несоблюдение условий стерильности в операционных, передача от инфицированного пациента, небрежность хирургов и обслуживающего персонала. Гематогенное инфицирование наблюдается после эпизода бактериемии. Например, стрептококковая инфекция может развиться после стоматологического вмешательства, стафилококковая – как следствие кожного инфекционного заболевания, энтерококковая и анаэробные инфекции – в результате желудочно-кишечных инфекционных заболеваний и инфекций мочеполовой системы [9].
Отек, боль и дисфункция коленного сустава возникают после эндопротезирования коленного сустава и усиливаются по мере прогрессирования инфекции. На фоне инфекции происходит перипротезный остеолиз, приводящий к нестабильности эндопротеза. У пациентов, не получающих своевременного лечения, может развиться сепсис и опасный для жизни септический шок [10].
На основе метаанализа, проведенного Cancienne J.M. с соавт., описаны исходы лечения 18 533 пациентов с ранними инфекционными осложнениями (в течение 1 года) после тотального эндопротезирования коленного сустава [11]. Среди них:
- 691 пациент (3,7%) умер в стационаре;
- 574 пациентам (3,1%) потребовалась ампутация конечности;
- 852 пациента (4,5%) перенесли артродез коленного сустава;
- 2683 пациентам (14,5%) проведена вторичная хирургическая обработка, без реимплантации;
- 13743 (74,1%) пациента прошли через двухэтапное реэндопротезирование коленного сустава, из них 11420 пациентам (61,6%) в течение 1 года проведено удаление спейсера и реимплантация, а 2323 пациентам (12,5%) оставлен спейсер.
Nodzo S.R. и соавторы, при проведении двухэтапного реэндопротезирования, разделили пациентов на три группы в зависимости от типа используемого спейсера [12]. В первой группе использовались преформованные артикулирующие спейсеры, во второй – спейсеры из цемента изготавливались интраоперационно. В третьей группе – в качестве спейсера использовали автоклавированный бедренный компонент удаленного эндопротеза. Признаки санации инфекционного процесса отметили в первой группе пациентов в 82,7% случаях, во второй группе – в 88,4%. Наименьшее количество положительных результатов отмечено в третьей группе – 79,4%. Таким образом, использование цементных спейсеров, изготовленных интраоперационно с использованием антибиотика по чувствительности флоры, приносит максимально положительный результат.
Цель исследования: провести анализ частоты, структуры и причин возникновения инфекционных осложнений при тотальном эндопротезировании и реэндопротезировании коленного сустава и определить оптимальную тактику лечения при этих осложнениях.
Материал и методы. В Новосибирском НИИТО за период с 2007 по 2016 год было проведено 12 245 операций первичного эндопротезирования коленного сустава. Инфекционные осложнения возникли у 470 (3,84%) человек. При этом эпифасциальная (поверхностная) инфекция была зафиксирована у 252 (2,06%) пациентов. В эту группу включены пациенты с некрозом послеоперационного шва и подкожной клетчатки, лигатурными свищами. В случае распространения процесса в пределах 5-6 см по ходу операционного шва, пациентам проводилась одномоментная санация и ушивание кожного дефекта. В случаях распространения процесса на весь шов, пациентам проводились этапные санационные перевязки до очищения стенок раны с последующим вторичным швом раны. Как результат применения такой методики лечения, у всех пациентов отмечался положительный результат.
Группу пациентов с субфасциальной (глубокой) инфекцией, развившейся в разные сроки, составили 218 пациентов (1,8%), что соответствует мировым тенденциям. По нашим убеждениям, в случае глубокой парапротезной инфекции, на фоне сформированной биопленки, эндопротез сохранять бесполезно, и он подлежит удалению. Однако дальнейшая тактика зависит от патологической флоры и других факторов. После удаления выполняется либо одномоментная имплантация нового эндопротеза, либо проведение этапного лечения с целью санации и последующего реэндопротезирования. В случае невозможности выполнения последующего этапа реэндопротезирования, в рассматриваемых случаях выполнялся артродез коленного сустава.
Бактериальное исследование пациентов с глубокой парапротезной инфекцией дало следующие результаты:
· у 172 (78,9%) пациентов была выделена грамположительная кокковая флора: у 113 пациентов – MSSA, у 33 – MSSE, у 8 пациентов – MRSA, и у 18 пациентов – MRSE;
· грамотрицательные палочки (Klebsiella, Pseudomonas, E.coli) были выделены у 33 пациентов (15,1%);
· грамположительные палочки (Korinebacterium, Propionobacter) – у 2 пациентов (0,9%);
· у 11 пациентов (5,0%) была выявлена смешанная флора.
При выборе тактики хирургического лечения больных с глубокой парапротезной инфекцией анализировались сроки возникновения инфекции, степень стабильности компонентов эндопротеза и степень вирулентности возбудителя. Также немаловажную роль в выборе тактики оперативного лечения играли сопутствующая патология и желания самого пациента.
Одномоментное реэндопротезирование после удаления эндопротеза выполнялось пациентам без выраженной сопутствующей патологии, в раннем послеоперационном периоде (до 6 мес.), при отсутствии признаков нестабильности эндопротеза и в случае чувствительности флоры к возможному проведению антибиотикотерапии. В ходе данного вида оперативного лечения выполняли удаление эндопротеза, патологических грануляций мягких тканей и имплантировали новый эндопротез с добавлением в цемент антибактериальных препаратов, подобранных по чувствительности к флоре. В последующем проводили адресную антибиотикотерапию в течение 6 недель.
Этим способом были пролечены 28 пациентов. В 26 случаях инфекция была купирована. У двух пациентов наблюдался рецидив, потребовавший проведения двухэтапного ревизионного вмешательства. Таким образом, выживаемость имплантата составила 93%.
Клинический пример 1. Больная К., 62 года. Выполнено первичное эндопротезирование КС по поводу левостороннего гонартроза III ст.
Через 3 месяца после проведения оперативного лечения развилось осложнение в виде глубокой парапротезной инфекции. По результатам бактериологического исследования выявлен патогенный микроорганизм – MSSA. Больной выполнено удаление эндопротеза и одномоментное реэндопротезирование коленного сустава.
На контрольных осмотрах через 1 год, 3 и 5 лет признаков рецидива инфекции не было.
В зависимости от степени сохранности связочного аппарата устанавливался артикулирующий либо неартикулирующий спейсер с добавлением антибиотика по чувствительности бактериальной флоры. После первого этапа пациенты получали антибиотикотерапию в течение 6-8 недель. Второй этап лечения – удаление цементного спейсера и реэндопротезирование коленного сустава, проводился по истечении 3-8 месяцев при условии нормализации клинических анализов и отсутствии положительных бактериологических исследований пунктата синовиальной жидкости.
Клинический пример 2. Больная Г., 62 года. Первичное эндопротезирование коленного сустава было проведено по поводу гонартроза III ст. Через 3 года после проведенной операции перенесла рожистое воспаление голени, осложнившееся глубокой парапротезной инфекцией. По результатам бактериологического исследования был выявлен патогенный микроорганизм – MRSA. Больной было выполнено удаление эндопротеза, санация и имплантация цементного артикулирующего спейсера (рис. 1).
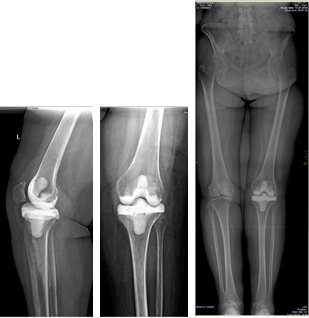
Рис. 1. Клинический пример 2. Рентгенограмма коленного сустава после
имплантации артикулирующего спейсера коленного сустава
Антибиотикотерапия поводилась в течение 6 недель. Через 6 месяцев, когда признаки инфекции были полностью купированы, больной выполнен второй этап оперативного лечения – удаление цементного спейсера и реэндопротезирование коленного сустава (рис. 2). На контрольных осмотрах через 1 и 3 года признаков рецидива инфекции не обнаружено.
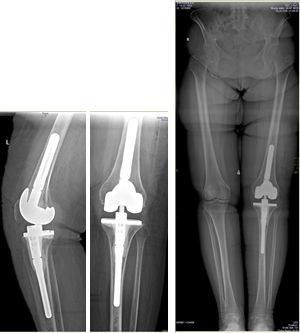
Рис. 2. Клинический пример 2. Рентгенограмма коленного сустава
после удаления спейсера и реэндопротезирования коленного сустава
За период наблюдения двухэтапное оперативное лечение было проведено 146 пациентам. У 124 пациентов признаки инфекции были купированы. Процедив отмечен у 22 пациентов. С целью купирования инфекционного процесса этим больным выполнялся артродез коленного сустава в аппарате внешней фиксации.
Первично артродез коленного сустава выполнялся пациентам с вирулентной флорой, на поддающейся антибиотикотерапии, с выраженной сопутствующей патологией, позволяющей оперировать пациента только по жизненным показаниям, и в случае желания пациента.
Клинический пример 3. Больная Л., 52 года. Первичное эндопротезирование коленного сустава было проведено по поводу вторичного артрозо-артрита коленного сустава III ст. на фоне ревматоидного полиартрита.
Через 6 месяцев после проведенного оперативного вмешательства у больной развилась глубокая парапротезная инфекция. Учитывая высокую активность основного заболевания, пациентка предпочла отказаться от дальнейших оперативных вмешательств, в связи с чем было выполнено удаление и артродез коленного сустава в аппарате внешней фиксации (рис. 3).
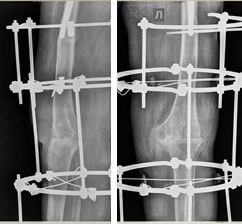
Рис. 3. Рентгенограмма коленного сустава после удаления эндопротеза и артродеза коленного сустава в аппарате внешней фиксации
По различным причинам артродез коленного сустава выполнялся в 66 случаях. В 54 случаях у пациентов сформировался костный анкилоз, и только в 12 случаях отмечалось формирование фиброзного анкилоза или неоартроза. Рецидива инфекции при выполнении артродеза коленного сустава зафиксировано не было.
Результаты. Таким образом, за 10 лет через отделение эндопротезирования коленного сустава Новосибирского НИИТО прошли 470 пациентов с парапротезной инфекцией. Эти пациенты получили следующее лечение:
- 252 (53,6%) пациентам с поверхностной инфекцией проведена вторичная хирургическая обработка, реимплантация эндопротеза не требовалась;
- 26 (5,5%) пациентам проведено одномоментное реэндопротезирование коленного сустава;
- 126 (26,8%) пациентов перенесли двухэтапное оперативное лечение;
- 66 (14,0%) пациентам по различным причинам выполнен артродез коленного сустава.
Ампутаций конечности и летальных исходов, вызванных инфекционным процессом, в отделении не отмечено.
Заключение. Инфекционные осложнения при первичном протезировании коленного сустава, невзирая на улучшение техники хирургического лечения и проводимой профилактики, остаются достаточно частыми и наиболее тяжелыми осложнениями. Как правило, они приводят к повторным оперативным вмешательствам, а зачастую и к инвалидизации пациентов. Обоснованный выбор хирургической тактики позволяет благополучно справиться с инфекционным осложнением и обеспечить пациенту приемлемое качество жизни.
Для продолжительности срока использования и функциональной характеристики суставов-имплантатов важны разные аспекты – из какого материала сделаны поверхности соприкасающихся искусственных компонентов, состояние костной ткани, активность пациента, его рост, вес, возраст, перенесенные операции на костях, хронические заболевания. Гнойно-воспалительные процессы возникают из-за внедрения микробов во время хирургической операции. Они могут попасть в рану аэрогенным путем (из воздуха), контактным (руками хирурга, инструментами), гематогенным (из очагов хронической инфекции).
- Материалы и продолжительность срока службы.
Одной из причин возникновения параинфекции является непереносимость компонентов искусственного сочленения. Организм иногда бурно реагирует на чужеродный агент. Перед операцией надо выявить персональную реакцию на конструкцию протеза, на все его компоненты. Чтобы увеличить прочность искусственных суставов, используемые материалы должны соответствовать самым высоким стандартам медицины. Неизбежный износ, возникающий в результате трения и истирания, должен быть как можно более низким. Кроме того, совместимость с телом и хорошее срастание коленного сустава с окружающими его костями должны быть максимально оптимальными, чтобы не было малейшего травмирования окружающей ткани. В этом случае вероятность инфицирования сводится к минимуму. Новая технология VERILAST (ВЕРИЛАСТ) объединяет два инновационных материала в уникальную пару трения: OXINIUM и высокосшитый полимерный материал. Результаты лабораторных исследований подтверждают, что эта комбинация является ключом к уменьшению износа при эндопротезировании и минимизирует риск инфицирования.
Традиционный полиэтилен был с 1968 года надежным компонентом, обеспечивающим легкое скольжение материалов друг по другу. Однако, наряду со своей высокой биосовместимостью, у этого материала есть недостаток, который и явился основной причиной для его ревизии: износ и - результирующая от этого - реакция тканей вплоть до асептического ослабления. Однако, с помощью новой технологии, которая дает возможность получить высокую степень сшивания полимеров посредством облучения, теперь создается стабильная сетчатая структура. Новая технология VERILAST считается устойчивой к окислению и демонстрирует улучшенную износостойкость.
- Сопутствующие болезни.
Риск послеоперационных осложнений особенно высок у лиц, страдающих определенными болезнями. Рассмотрим некоторые из них.
Ожирение - наличие патологического ожирения можно рассматривать в качестве фактора риска при эндопротезировании коленного сустава. В рамках метаболического синдрома оно может нести ответственность за более частое возникновение диабета типа II. Менископатии и возникающие дегенеративные заболевания коленного сустава в качестве прямых последствий ожирения, часто являются показаниями для имплантации протеза коленного сустава, что, в свою очередь, приводит к увеличению доли пациентов с ожирением с протезами коленного сустава.
- Сахарный диабет.
Сахарный диабет несет ответственность за нарушение процесса заживления ран; в качестве причин этого рассматриваются такие факторы, как замедленный синтез коллагена, оказание отрицательного влияния на фагоцитоз и замедленное прорастание капилляров в рубцовую ткань. Диабет же, в свою очередь, способствует возникновению раневых осложнений. Проксимальная мышечная слабость и диабетическая периферическая полинейропатия, в результате которых увеличивается частота возникновения и персистенция поражений кожи (таких, как например, нейротрофическая язва) приводят к увеличению риска возникновения инфицирования. Кроме того, у диабетиков увеличивается вероятность возникновения окклюзии периферических артерий. Таким образом, сахарный диабет следует рассматривать как фактор риска развития инфекции при выполнении имплантации протеза. Предоперационное оптимальное регулирование сахара в крови может свести к минимуму существующий риск. По данным некоторых исследований пациенты с диабетом имеют более плохое общее качество жизни после развития инфекции протеза коленного сустава по сравнению с контрольной группой пациентов, нестрадающих диабетом.
- Окклюзионное заболевание периферических артерий.
Болезнь также может способствовать нарушению процесса заживления ран, прежде всего, вследствие снижения перфузии в области раны. Поэтому, до проведения операции необходимо уточнить состояние периферических сосудов пациента и провести при необходимости ряд специальных обследований.
- Хронический полиартрит.
По данным некоторых исследований, при наличии у пациентов - в качестве предыдущего заболевания - хронического полиартрита, следует ожидать не только более частого возникновения инфекций, но и более плохих клинических результатов. У пациентов с хроническим полиартритом по сравнению с группой пациентов, не страдающих полиартритом, наблюдалось значительно меньшее количество случаев сохранения протезов и, в свою очередь, ампутации были чаще. Кроме того, число смертельных исходов было выше у пациентов, страдающих ревматизмом. Однако эти различия не были значительными
- Прием иммунодепрессантов.
У многих пациентов является ослабленной защита организма в результате приема различных иммунодепрессантов. Примерно 10% пациентов во время имплантации протеза коленного протеза приходилось регулярно принимать кортикостероиды. В результате, риск инфицирования у пациентов с артрозом значительно увеличивается, а некоторые авторы утверждают, что риск инфицирования даже утраивается. Кроме того, ревматики имеют более низкое качество костей, что может привести к проблемам фиксации эндопротеза, особенно в субхондральной области, что, в свою очередь, приводит к ревизиям и, следовательно, к повышенному риску инфицирования. Кстати, и длительная антибиотикотерапия перед операцией порой может спровоцировать появление инфекции, так как появляются резистентные формы возбудителей, и борьба с инфекцией в дальнейшей становится малоэффективной.
- Деформации верхних конечностей.
Деформации и дефекты верхних конечностей могут приводить к проблемам при послеоперационной мобилизации. Средний возраст этих пациентов при первичной имплантации протеза в среднем на 10 лет меньше, в результате чего протез должен оставаться функциональным в течение более длительного периода времени и, следовательно, вероятность возникновения поздних осложнений (таких как асептическое ослабление или инфекция протеза) является, соответственно, более высокой
- Предыдущие операции на колене.
Дополнительными факторами риска развития инфекции протеза является наличие у пациентов предыдущих инвазивных оперативных вмешательств на колене. Хирургические вмешательства или внутрисуставные пункции на соответствующем колене до проведения первичной операции по имплантации протеза коленного сустава приводят к меньшему количеству случаев сохранения первичного протеза и к большей частоте случаев ревизионного протезирования или выполнения артродезов, а также к более высокой смертности. Количество ранее выполненных оперативных вмешательств не играли никакой роли для клинических результатов.
- Нарушение предписания лечащего специалиста.
Реабилитационный период чрезвычайно важен для качественного восстановления. Необходимо тщательно соблюдать все рекомендации врача, добросовестно принимать лекарства, помнить о важности ЛФК, о щадящем режиме. Надо быть особо терпеливым и ответственным на этом не менее важном для сустава этапе.
- Халатное отношение к выбору клиники и врача.
Операции по эндопротезированию доведены до совершенства и изучены до малейших нюансов. Но эти знания есть только у опытных практикующих врачей, работающих в специализированных ортопедических центрах. Надо внимательно отнестись к выбору клиники, желательно предварительно посетить ее, услышать отзывы больных и поговорить с врачами, которым вы хотите довериться.
- Периоперационный риск.
Длительная операция способствует появлению инфекции, так, ее продолжительность более 3-х часов значительно увеличивает риск заражения тканей из-за их контакта с окружающей нестерильной средой. Периоперационный риск инфицирования может быть снижен путем предоперационной оптимизации некоторых из вышеуказанных факторов риска. Это включает в себя, как целенаправленное снижение веса пациентов, так и достижение в долгосрочной перспективе оптимальных показателей уровня глюкозы в крови у пациентов с диагностированным сахарным диабетом. Пациенты с хроническим полиартритом до начала лечения должны быть проинформированы о возможности получения более плохих конечных результатов.
У пациентов с ранней инфекцией более часто достигалось сохранение первичного протеза и относительно более часто было успешное использование ревизионных протезов.
Напротив, при поздних инфекциях было выполнено больше артродезов и при этом было зафиксировано больше случаев смертельного исхода. Частота случаев ампутации была примерно одинаковой в обеих группах. Представленные различия являются незначительными.
Прогноз при парапротезной инфекции достаточно благоприятный, но сохранить функциональность сустава иногда не получается, поэтому инфекционные риски, имеющие место при эндопротезировании, являются большой проблемой в медицине и для социума. Необходимо тщательно подойти к профилактике осложнений эндопротезирования. Она будет заключаться в определенных действиях до госпитализации, во время самого вмешательства и в реабилитационном периоде. Поэтому чрезвычайно важно найти специализированную клинику и опытного квалифицированного врача. Большое значение играет положительный настрой самого пациента и желание активно участвовать в процессе выздоровления. Особенно важна подготовка пациента перед операцией, а затем его настойчивость и добросовестность на этапе восстановлениявосстановления.
Цель: Осложнения при эндопротезировании коленного сустава – изучение и анализ.
Материалы и методы: проанализированы результаты лечения 885 больных, перенесших эндопротезирование коленного сустава в период с 2003 по 2013 годы. Женщин было 684 (77,29%), мужчин – 201 (22,71%). Возрастной диапазон – от 19 до 82 лет, средний возраст – 61,68 лет.
Результаты: в ближайшем и отдаленном послеоперационном периоде у 10 пациентов (1,13%) были зафиксированы осложнения: 1 (0,11%) – стойкая контрактура, 3 (0,34%) глубокое нагноение, 1 (0,11%) – асептическая нестабильность, 2 (0,23%) – стойкая артралгия, 3 (0,34%) нефатальная ТЭЛА. Венозные тромбоэмболические осложнения зафиксированы у 87 (9,83%) больных, геморрагические осложнения – у 18 (2,03%) пациентов.
Выводы: в ходе проведенного лечения пациентов удалось получить в течение первого года хорошие анатомические, рентгенологические и функциональные результаты у 96,38% пациентов.

Алабут Анна Владимировна
Алабут Анна Владимировна Заведующая отделением травматологии и ортопедии клиники РостГМУ, кандидат медицинских наук, доцент кафедры травматологии и ортопедии

Сикилинда Владимир Данилович
Сикилинда Владимир Данилович, Профессор, Доктор медицинских наук, Заведующий кафедрой травматологии и ортопедии Ростовского государственного медицинского университета, Вице-президент Всероссийской Ассоциации травматологов-ортопедов ЮФО
Несмотря на внедрение новых технологий, осложнения при эндопротезировании коленного сустава и неудовлетворительные результаты встречаются достаточно часто и составляют 3,3–13,2%. Частота развития инфекции области хирургического вмешательства при первичном эндопротезировании коленного сустава составляет от 0,5 до 3,5%, а при повторных операциях достигает от 3,2% и 5,6% [1, 2]. Частота таких осложнений как параартикулярная боль, асептическая нестабильность, контрактура может достигать 3-12% [3]. Частота тромбоза глубоких вен после эндопротезирования коленного сустава колеблется от 41 до 88 %, проксимальный тромбоз регистрируется у 5-22% больных, тромбоэмболия легочной артерии без тромбопрофилактики встречается у 1,5-10% пациентов, фатальные случаи ТЭЛА регистрируются у 0,1-1,7% пациентов [4, 5].
В 1982 году Mc Elwaine J.P. впервые сообщил о 7 случаях стрессовых переломов проксимального отдела бедренной кости через 3-16 месяцев после тотального эндопротезирования коленного сустава в группе из 500 прооперированных больных. В последующем, публикации по поводу стрессовых переломов стали носить регулярный характер [6, 7, 8]. По мнению авторов, стрессовые переломы полиэтиологичны. Имеет значение локальный и системный остеопороз, диагностируемый у пациентов, стероидная терапия, увеличение мышечной активности и давления не шейку бедренной кости у пациентов, ограничивающих подвижность до операции из-за резких болей. Имеет значение техника операции, когда при установке бедренного компонента ударные усилия передаются на шейку и приводят к микропереломам. При расширении двигательной активности переломы становятся завершенными.
Целью исследования явился анализ осложнений тотального эндопротезирования коленного сустава.
Материалы и методы анализирования осложнений.
Проанализированы результаты лечения 885 больных, перенесших эндопротезирование коленного сустава отделении травматологии и ортопедии ЮОМЦ, травматолого-ортопедическом отделении клиники РостГМУ и базах кафедры травматологии и ортопедии РостГМУ в период с 2003 по 2013 годы. Женщин было 684 (77,29%), мужчин – 201 (22,71%). Возрастной диапазон – от 19 до 82 лет, средний возраст – 61,68 лет.
В структуре больных преобладали пациенты с первичным – 665 (75,14%) и посттравматическим 160 (18,08%) артрозом III-IV стадии (по Kellgren I., LawrenceI., 1957), на втором месте пациенты с ревматоидным артритом – 48 (5,43%) человек, реже эндопротезирование требовалось по поводу хронического остеомиелита – 4 (0,45%), доброкачественных и злокачественных опухолей – 8 (0,90%) больных.
С целью профилактики и выявления венозных тромбоэмболических осложнений через 7-10 дней после оперативного вмешательства больным выполняли триплексное исследование вен нижних конечностей. Диагностика остеопороза осуществлялась на основании оценки факторов риска остеопороза, остеоденситометрического исследования.
Рентгенологическую оценку результатов эндопротезирования коленного сустава выполняли по шкале E.C. Ewald (1989) в модификации О.А.Кудинова с соавторами (2005). Рентгенограмму выполняли в прямой и боковой проекции от тазобедренного до голеностопного сустава с центрацией на коленный сустав.
Осложнения при эндопротезировании коленного сустава: результаты и обсуждение.
В ближайшем и отдаленном послеоперационном периоде у 10 пациентов (1,13%) были зафиксированы следующие осложнения при эндопротезировании коленного сустава, таблица. 1.
Характер осложнений после эндопротезирования коленного сустава
У одной пациентки в послеоперационном периоде развилась стойкая контрактура правого коленного сустава.
Клинический пример. Пациентка Г., 57 лет, история болезни № 5587 была госпитализирована в отделение по поводу посттравматического гонартроза правого коленного сустава 3 клинико-рентгенологической стадии по Косинской, сросшегося перелома наружного мыщелка правой большеберцовой кости в условиях кортикального металлоостосинтеза двумя винтами, асептического некроза наружного мыщелка, стойкой смешанной контрактуры правого коленного сустава. Пациентке было выполнено удаление металлоконструкции, тотальное эндопротезирование правого коленного сустава. Объем движений после операций 90°, сгибание 90°, разгибание 180°. Через 4 месяца после операции больная обратилась с жалобами на ограничение движений в правом коленном суставе сгибание 100°, разгибание 165°, амплитуда 65°. Пациентке была выполнена редрессация правого коленного сустава, восстановлен объем движений 90°. В связи с несоблюдением рекомендаций в реабилитационном периоде пациентке не удалось сохранить оптимальный объем движений. При контрольном осмотре через 7 лет у больной признаков нестабильности эндопротеза нет. Объем движений в коленном суставе 70°, разгибание 170°, сгибание 100°. Пациентка оценивает объем движений как достаточный, от предложенного хирургического лечения отказалась. На рисунке 1 представлены рентгенограммы больной после операции. Через 7 лет после эндопротезирования коленного сустава определяется выраженная оссификация параартикулярных тканей.
У трех больных была зафиксирована глубокая инфекция. У одного больного развилась параэндопротезная острая послеоперационная инфекция по Coventry-Fitzgerald. У второго больного экзогенная острая послеоперационная инфекция. У третьего больного поздняя хроническая инфекция. У всех пациентов санация послеоперационной раны и попытки сохранить эндопротез оказались безуспешными, было выполнено удаление металлоконструкции.
Клинический пример. Больной К., 68 лет, история болезни №001792, №008995, №010533, №012564, №013448, №014097, №018967, №023756, №038616, №039490 был прооперирован по поводу двухстороннего гонартроза 3 клинико-рентгенологической стадии по Косинской. Пациенту было выполнено тотальное эндопротезирование левого коленного сустава. Через 2 месяца после операции выходя из машины, пациент ударился оперированным коленным суставов о дверь. После удара сформировалась гематома. В результате позднего обращения в лечебное учреждение через 3 недели после травмы произошло нагноение гематомы. Пациенту было выполнено активное дренирование нагноившейся гематомы с использованием приточно-промывных систем. В посеве из раны был выделен S. aureus. В связи с неэффективностью антибактериальной терапии и санационных мероприятий через 6 месяцев после эндопротезирования было выполнено удаление эндопротеза, артродез левого коленного сустава в условиях аппарата внешней фиксации. Приточно-промывная система функционировала в течение 3 недель. После трехкратного отрицательного посева промывных вод из раны приточно-промывная система была удалена. Через 6 месяцев был демонтирован аппарат внешней фиксации. В течение 2 лет после купирования инфекции рецидивов воспаления не было. В связи с этим в ноябре 2012 года больному выполнено ревизионное эндопротезирование левого коленного сустава эндопротезом Мати. Через 4,5 месяцев после ревизионного эндопротезирования коленного сустава у пациента сохраняется дефицит активного разгибания 10 градусов за счет слабости четырехглавой мышцы бедра, пассивное разгибание полное. Активное сгибание 95 градусов, пассивное – 85 градусов. Пациент продолжает реабилитационное лечение.
У одной пациентки 72 лет на фоне прогрессирование остеопороза произошел лизис кости вокруг большеберцового компонента, в результате чего развилась асептическая нестабильность эндопротеза. Больной было выполнено ревизионное эндопротезирование.
У двух пациентов наблюдалась стойкая артралгия коленного сустава без признаков асептического расшатывания и конфликта надколенника. Обоим пациентам была выполнена ревизия полости коленного сустава с релизом тканей, в одном случае посредством артротомии, во втором – артроскопически.
У 1 пациентки 68 лет, через 10 месяцев после эндопротезирования коленного сустава на фоне постменопаузального остеопороза произошел перелом проксимального отдела бедренной кости на стороне операции.
Венозные тромбоэмболические осложнения. У 12 (1,36%) пациентов выявлены флотирующие тромбы в берцово-подколенном сегменте, у 7 (0,79%) произошел тромбоз бедренной вены. Всем пациентам потребовалась экстренная операция. Были выполнены тромбэктомия, пликация поверхностной бедренной вены. Тромбоэмболия мелких ветвей легочной артерии развилась у трех (0,34%) больных в первые шести суток после операции. Своевременная интенсивная терапия позволила избежать фатальных осложнений. У 24 (2,71%) больных клинически значимый тромбоз глубоких вен развился в течение первого месяца после операции и потребовал госпитализации. Неэмболоопасный бессимптомный тромбоз глубоких вен голени диагностирован у 41 (4,63%) больных как случайная находка при контрольном ультразвуковом исследовании через 2,5-3 месяца после операции.
Все пациенты получали антикоагулянтную терапию согласно отраслевому стандарту. На фоне антикоагулянтной терапии у 18 (2,03%) пациентов развились геморрагические осложнения. У трех пациентов (0,34%) были диагностированы большие кровотечения из желудочно-кишечного тракта.
У 15 (1,69%) пациентов развились малые кровотечения: у одного (0,11%) – из геморроидальных узлов, у 4 (0,45%) – маточные кровотечения, у 7 (0,79%) – носовое кровотечение, у трех (0,34%) пациентов развился гемартроз. У 1 пациента на фоне длительной антикоагулянтной терапии после эндопротезирования и по поводу хронической сердечной недостаточности развился рецидивирующий гемартроз, потребовавший артроскопической абляции (рис. 2).
Рис. 2. Гематома и гемартроз у пациента после эндопротезирования коленного сустава на фоне длительной антикоагулянтной терапии
Осложнения при эндопротезировании коленного сустава требуют тщательной корректировки.
Прогнозирование, медикаментозная и немедикаментозная профилактика инфекционных осложнений в области хирургического вмешательства позволили получить минимальное количество 3 (0,34%) гнойно-септического осложнения.
Комплексная диагностика медикаментозная профилактика снижения минеральной плотности костной ткани и лечение остеопороза позволили снизить риски развития ранней нестабильности эндопротеза у пациентов перенесших артропластику.
Адекватная по дозам и длительности специфическая и неспецифическая профилактика венозных тромбоэмболических осложнений, использование современных таблетированных антикоагулянтов позволили уменьшить риски развития тромбозов. Выполнение контрольного ультразвукового исследования вен нижних конечностей больным через 5-7 дней после операции эндопротезирования помогли избежать фатальных тромбоэмболий легочной артерии.
Продуманная комплексная терапия имеющихся у пациента коморбидных состояний позволила уменьшить количество осложнений, связанных с обострением сопутствующих заболеваний. Выбор хирургической тактики позволил снизить травматичность оперативного вмешательства, получить хорошие анатомические, рентгенологические и функциональные результаты у 96,38% пациентов.
Читайте также:


