Подагра и отек легких
Отек при подагре возникает довольно часто. Припухлость в области сустава свидетельствует о наличии воспаления. Отек необходимо устранять, так как при отсутствии своевременных мер возможно начало деформационных изменений в структурах суставных сочленений.
- Почему при подагре отекают суставы?
- Как снять отечность?
- Мочегонные средства
- Криотерапия
- Народная медицина
- Профилактика отеков
Почему при подагре отекают суставы?

Отечность в области сустава один из симптомов подагры
Припухлость в области сустава является характерным симптомом подагрического заболевания.
Отечность обуславливается нарушенным обменом веществ, так как почки не выводят в полном объеме мочевую кислоту и ее соли. Вследствие этого ураты кристаллизуются и откладываются в хрящевой ткани. В большинстве случаев отечность возникает в суставах ног, реже подагра поражает сочленения рук и спины.
К появлению отечности наиболее склонны мужчины, у них отеки в области суставов возникают в 20 раз чаще, чем у женщин.
Подагра практически всегда сопровождается развитием отека в области пораженного сустава. Кожа в этой области краснеет, повышается местная температура. Способствует появлению отека неправильное питание, частое употребление острой и соленой пищи. Отеки преимущественно возникают в вечернее время, они могут не сходить достаточно долгое время.
Без своевременных мер отек увеличивается в размерах и доставляет дискомфортные и болевые ощущения. Выраженная отечность способна полностью блокировать двигательную функцию сустава.
Как снять отечность?
Многие пациенты интересуется, как устранить отечность при подагре. Для этого широко используются медикаментозные препараты, криотерапия и народные рецепты. Кроме этого, для устранения отечности необходимо соблюдать следующие правила:
- Обеспечить опухшей конечности полный покой, избегать резких движений. По возможности рекомендован постельный режим.
- При незначительном отеке выполнять лечебную зарядку, которая поможет нормализовать движения в суставе и устранить скованность. Физическая активность не должны быть чрезмерной, при появлении болевых ощущений зарядкой заниматься запрещается.
- При наличии избыточного веса необходимо похудеть, так как лишний вес оказывает колоссальную нагрузку на суставы.
- Придерживаться диетического питания, отказаться от соленой и острой пищи, употреблять большое количество свежих овощей.
- Полностью отказаться от алкогольных и газированных напитков.
- Употреблять не менее, но и не более 2 литров чистой воды ежедневно. Пациентам, имеющим проблемы в деятельности почек, запрещается пить много воды.

Лёд поможет снять опухлость суставов
При резком образовании отека на пораженном суставе рекомендуется приложить лед, это помогает снизить болевые ощущения и способствует уменьшению отечности. Стоит учитывать, что такая мера является экстренной, кроме нее, необходимо соответствующее лечение.
Снятие отека при подагре проводится с помощью мочегонных препаратов. Диуретические медикаменты увеличивают количество жидкости, которая выводится вместе с мочой из организма. Существует несколько типов мочегонных препаратов:
- петлевые,
- калийсберегающие,
- тиазидные.
Внимание! Подбирать мочегонные медикаментозные препараты при подагре может только врач, учитывая степень поражения суставов и сопутствующие заболевания пациента. Бесконтрольный прием диуретиков способствует значительному ухудшению течения заболевания и развитию осложнений.
Самое распространенное мочегонное средство для снятия отеков при подагре – Фуросемид. Он обладает мощным действием, способствует быстрому выведению из организма застоявшейся жидкости, также он часто используется при различных нарушениях в деятельности сердечно-сосудистой системы. Более легкими диуретиками являются Гидрохлортиазид и Трифас. Они обладают меньшим списком противопоказаний по сравнению с Фуросемидом.
При подагрическом поражении суставов мочегонные препараты назначают совместно с другими медикаментами. Монотерапия диуретиками приводит к стремительному повышению уровня мочевой кислоты в организме, что значительно усугубляет течение патологического процесса.
Данная процедура имеет несколько показаний, в их числе и устранение отечности. Методика холодового воздействия позволяет убирать припухлости локально, не оказывая воздействия на организм в целом.
Процедура направлена на ускорение местного кровообращения, устранение покраснений и отеков. Метод подразумевает местное воздействие, поэтому является относительно безопасным. Действующими веществами выступают жидкий азот и кислород. Именно под их воздействием устраняется опухоль.
Уже после первой процедуры пациент испытывает значительное облегчение, которое проявляется снятием болевых и дискомфортных ощущений, а также улучшением двигательной функции сустава. Для достижения наилучшего результата требуется курс процедур.

Криотерапия жидким азотом помогает снять воспаление сустава
Под воздействием криотерапии ускоряются процессы регенерации, и удается купировать воспаление сустава. Лечение холодом позволяет достичь хороших результатов за короткий промежуток времени, его недостатком является относительно высокая стоимость. Одна процедура в среднем обойдется в 700-1000 рублей.
Народные методики широко используются в лечении многих заболеваний, в том числе их применяют для снятия отека при подагре. Наиболее распространены следующие способы:
- Соленые ванны с настоем ромашки. Потребуется 100 г сухих цветков ромашки и 10 л воды. Ромашку заливают горячей водой, после чего необходимо настаивать в течении 20 минут. Затем настой нужно охладить и добавить в него 200 г поваренной соли, все тщательно перемешать. Полученный раствор используется для ванночек, которые помогают быстро устранить припухлость сустава.
- Настойка сирени. Потребуется медицинский спирт и цветки сирени. Для получения настойки нужно заполнить полулитровую банку наполовину цветами, затем залить их спиртом. Настаивать необходимо в течение месяца в темном месте. Употреблять внутрь по 30 капель до 3 раз в сутки. Также полученная настойка применяется в качестве средства для растираний и компрессов.
Народные рецепты могут использоваться только в качестве дополнительных мер, они не заменяют медикаментозного лечения отеков при подагре.
Профилактика отеков

Сбалансированное питание при подагре нормализует обмен веществ
При подагре конечности отекают достаточно часто. Чтобы избежать этого, необходимо соблюдать следующие правила:
- придерживаться сбалансированного рациона питания, исключить острую и жареную пищу. Отдавать предпочтение свежим овощам и фруктам, кисломолочным продуктам.
- Полностью отказаться от вредных привычек. Алкоголь способствует застою жидкости в организме, а также повышает уровень мочевой кислоты.
- Принимать сбалансированные витаминно-минеральные комплексы. Перед их употреблением рекомендуется проконсультироваться с врачом.
- Уделять время физической активности, например, пешим прогулкам на свежем воздухе.
- Пораженные конечности запрещается перегружать. При малейшем чувстве усталости необходимо обеспечить себе состояние покоя минимум на полчаса.
- При наличии лишнего веса желательно от него избавиться. Избыточный вес оказывает дополнительную нагрузку на суставы и увеличивает вероятность развития отеков.
Соблюдение перечисленных правил поможет минимизировать риск появления отеков на суставах при подагре, а также улучшит самочувствие пациента.
Общие сведения
Отек легких — это клинический синдром, в основе которого избыточная транссудация жидкости из венул/капилляров в интерстициальную легочную ткань, а затем — в альвеолы и сопровождающийся выраженным нарушением газообмена в легких с развитием гипоксии различных тканей, ацидоза, угнетением функций ЦНС. Код отек легких по МКБ-10: J81. Этот клинический синдром может быть осложнением различных кардиологических, пульмонологических урологических, гинекологических, неврологических, гастроэнтерологических заболеваний.
В клинической практике чаще встречается кардиогенный отек легких, являющийся осложнением ОСН. В большинстве случаев кардиогенный отек развивается при ИБС, ХСН, острых нарушений сердечного ритма, патологии клапанов при которых развиваются застойные явления в легких. В пожилом возрасте преобладает ИБС, а в молодом — превалируют пороки сердца, дилатационная кардиомиопатия, миокардиты.
Относится к жизнеугрожающим осложнениям, требующим принятия неотложных мер. Промедление с оказанием врачебной помощи при отеке легких, приводит к летальному исходу.
В основе развития патологического процесса — повышение давления (постепенное/резкое) в малом круге кровообращения. При этом, важнейшее значение имеет непосредственно скорость развития патологического процесса, поскольку вероятность возникновения кардиогенного отека значительно выше при остро возникших нарушениях, так как в таких ситуациях компенсаторные механизмы не срабатывают (не успевают купировать/уменьшить их последствия). В случаях более постепенного развития процесса недостаточности кровообращения и нарастаниях клинических проявлений последствия чаще не столь драматические.
Некардиогенный отек легких развивается как при прямом повреждении легких (ингаляция токсинов/токсичных газов, аспирация содержимого ЖКТ, воды, крови, ожоги, пневмонии), так и при внелегочных заболеваниях (шок, тяжелая политравма, сепсис, массивная кровопотеря, панкреатит/панкреонекроз, гемотрансфузия, уремия) встречается значительно реже. Еще одним синдромом, проявляющимся некардиогенным отеком легких и острой дыхательной недостаточностью является ОРДС — острый первичный/вторичный респираторный дистресс-синдром (синоним мокрое легкое, шоковое легкое). Развитие этого типа отека обусловлено преимущественно нарушением функции/структуры альвеолокапиллярной мембраны.
Согласно современным представлениям о первичном ОРДС повреждающий фактор оказывает влияние непосредственно на альвеолоциты, сурфактант, приводящих к повреждению эпителия альвеол и нарушению целостность альвеолокапиллярной мембраны в результате чего происходит трансфузия жидкой составляющей крови в альвеолярные пространства. При вторичном ОРДС в основе лежит внелегочный фактор, формирующийся на фоне синдрома воспалительной реакции в организме (сепсис, бактериемия). Отек такого типа (шоковое легкое) не подчиняется законам транспорта жидкости и не зависит от уровня гидростатического давления.
Его особенностью является резкое снижение вентиляции/оксигенации организма, вызывающее застой в легких, кислородную недостаточность тканей головного мозга и сердца с быстрым развитием состояний, угрожающих жизни. При неадекватной/несвоевременно оказанной помощи летальность достигает 65-80%.
Патогенез
Патогенез отека легких определяется его типом (кардиогенный/некардиогенный). Соответственно различают гидростатический и мембраногенный механизм развития отека.
Основным этиологическим фактором являются заболевания сердечно-сосудистой системы, при которых происходит повышение внутри капиллярного гидростатического давления. При достижении давления 15 мм рт. ст. происходит трансфузия плазмы крови в интерстиций в объеме, который превышает физиологическую возможность удаления её путем лимфооттока. При росте давления до 20 мм рт. ст. и выше жидкость поступает на поверхность альвеол. Механизм развития отека этого типа основан на законе Франка-Старлинга, описывающего закономерности обмена жидких сред в тканях легких. В рамках статьи нет возможности расшифровки каждого из действующих факторов формулы. Выделим лишь основные последовательно сменяющиеся взаимосвязанные этапы патологического процесса:
- Повышение гидростатического давления в малом круге кровообращения, способствующее повышению давления в легочной артерии и затем внутри капилляров легких.
- Повышение фильтрации жидкости из лёгочных сосудов непосредственно в ткань.
- Образование избыточного отрицательного давления в интерстициальном пространстве легких и развитие интерстициального отека.
- Декомпенсация оттока жидкости через лимфопути.
- Развитие альвеолярного отека (наблюдается развернутая клиника отека легких).
- Сокращение площади газообмена и дезорганизация механизма газообмена между наружной воздушной средой и кровью.
- Состояние гипоксии, которое, в свою очередь, провоцирует продуцирование гормонов стресса, катехоламинов, что приводит к еще большему нарастанию артериального давления и снижению проницаемости сосудов, дополнительно увеличивая нагрузку на левый желудочек сердца, формируя тем самым порочный круг.
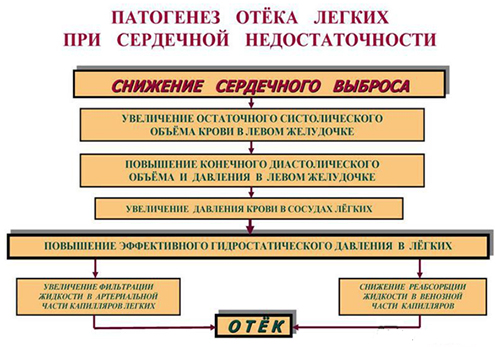
На рисунке схематически представлен патогенез отека легких кардиогенного типа
Его развитие обусловлено первичным повышением проницаемости и нарушением функции альвеолярно-капиллярной мембраны, что вызвано повреждением эпителия альвеол и эндотелия капилляров. Повышение проницательности происходит под воздействием токсичных кислородных радикалов, протеиназ, простагландинов, лейкотриенов, гистамина, образующихся или освобождающихся в ткани под воздействием на нее различного рода раздражителей.
Повышение проницаемости легочных капилляров быстро приводит к появлению большого количества отечной жидкости, в которой содержится много белка. При этом, изменения проницаемости альвеолярной и капиллярной части барьера происходит не одночастно. Вначале повышается проницаемость эндотелиального слоя, что приводит к пропотеванию сосудистой жидкости в интерстиций, где она временно накапливается (интерстициальный отек легких). При этом, интерстициальный отек частично компенсируется за счет ускорения лимфооттока. В большинстве случаев эта приспособительная реакция является недостаточной, и постепенно отечная жидкость проникает через поверхность деструктивно измененных клеток альвеол в их полость, заполняя весь объем.
Развивается альвеолярный отек легких. Выключение из процесса газообмена части альвеол компенсируется растяжением (эмфиземой) еще оставшихся неповрежденных альвеол, что приводит к сдавливанию лимфатических сосудов и капилляров легких. Альвеолярный отек развивается при заполнении альвеол жидкостью и характеризуется появлением выраженных нарушений со стороны дыхательной системы, развитием артериальной гипоксемии/гиперкапнии.
На этом фоне изменяется микроциркуляция/повышается вязкость крови (развитие ДВС-синдрома). Нарушается реактивность сосудов и тонус мышечной ткани бронхов, снижается активность сурфактанта, что приводит к развитию микроателектаз. Нарастает гиповентиляция альвеол, приводящая к несоответствию между перфузией и вентиляцией, изменению диффузии углекислого газа/кислорода и снижению снабжения тканей кислородом с развитием гипоксии и метаболического ацидоза.
Мембраногенный отёк лёгких развивается при воздействии различных типов повреждающих факторов, одним из которых являются токсиканты различного генеза, на примере которых более подробно рассмотрим патогенез токсического отека.
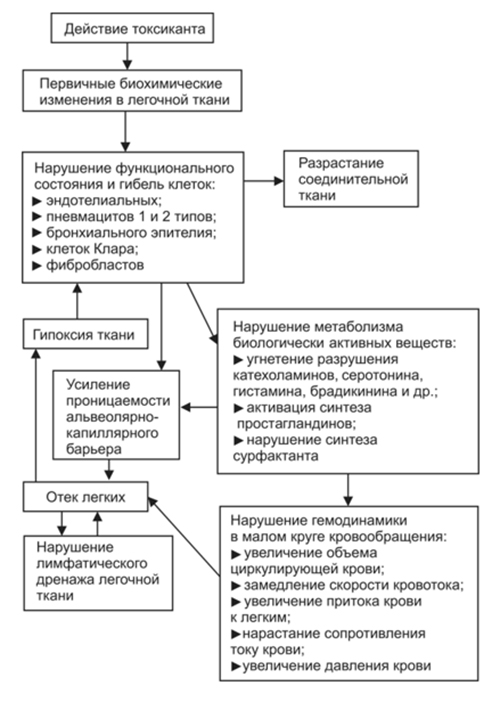
На рисунке схематически представлен патогенез токсического отека легких
Токсический отек легких. Патогенез отека легких такого типа обусловлен воздействием токсикантов непосредственно на клетки альвеолярно-капиллярного барьера с нарушением их функции. Токсический отек имеет различные механизмы повреждения клеток легких, но развивающиеся за этим патологические процессы достаточно схожи. При повреждении/гибели клеток происходит усиление проницаемости барьера и резкому к усилению процессов выработки в легочной ткани биологически активных веществ (гистамина, норадреналина, ангиотензина, ацетилхолина, серотонина, простагландинов) что способствует дальнейшему повышению проницаемости/нарушению функции альвеолярно-капиллярного барьера и развитию нарушений гемодинамики в легких (уменьшается скорость кровотока, растет давление в малом круге кровообращения). По мере прогрессирования отека респираторные и терминальные бронхиолы заполняет жидкость, а под действием турбулентности, возникающей при движении воздуха, образуется пена в дыхательных путях.
Отек легких смешанного типа. В основе развития сочетание механизмов отека обоих типов.
Классификация
Единой общепринятой классификации отека легких нет. Общепризнанным является разделение отека легких на кардиогенный и некардиогенный.
Кардиогенный отек легких в свою очередь разделяют по нескольким признакам.
По наличию/отсутствию в анамнезе ХСН:
- Впервые возникший (без наличия в анамнезе ХСН).
- Декомпенсированный (острая декомпенсация ХСН).
По причине возникновения:
- Левожелудочковая недостаточность (аритмии; острый коронарный синдром; миокардит/перикардит/эндокардит; дисфункции клапанов — митральная недостаточность, аортальный стеноз и др.).
- Увеличение внутрисосудистого объема (почечная недостаточность, объемная перегрузка).
- Легочная венозная обструкция (стеноз митрального клапана).
Некардиогенный отек разделяют на:
- Первичный — связанный с наличием повреждающего фактора непосредственно в легочной ткани.
- Вторичный — развивающегося при наличии внелегочного фактора и выраженном системном воспалении.
По течению выделяют:
- Молниеносный отек – бурное развитие на протяжении нескольких минут, летальный исход.
- Острый отек – быстро нарастает (на протяжении до 4-х часов). Развивается преимущественно при инфаркте миокарда, анафилаксии, черепно-мозговых травмах. Даже при своевременно проведенных реанимационных мероприятиях высокий риск летального исхода.
- Подострый отек – характеризуется волнообразным течением с постепенным нарастанием симптоматики и ее стиханием. Наблюдается чаще при эндогенной интоксикации организма различного генеза (печеночной недостаточности, сепсисе, уремии).
- Затяжной отек – период развития от 12 часов до 1-3 суток. Часто протекает стерто, с невыраженной симптоматикой без характерных клинических признаков. Встречается чаще при хронических заболеваниях легких, ХСН.
Причины отека легкого
Основной причиной отека легкого при болезни сердца (кардиогенного отека) является увеличение гидростатического давления в капиллярной системе легочной артерии. Наиболее частой причиной, от чего бывает отек является застойная сердечная, чаще левожелудочковая недостаточность, обусловленная снижением сократительной возможности миокарда, перегрузкой объемом/давлением или патологией клапанов сердца. Нарастающий дисбаланс артериального/венозного кровенаполнения, развитие в малом кругу кровообращения выраженного венозного застоя является неблагоприятным прогностическим признаком. Венозный застой в легких что это такое? Это нарушение гемодинамики малого круга кровообращения, характеризующийся переполнением венозного участка кровеносного русла кровью, обусловленное расстройствами сердечной деятельности.
Причинами развития некардиогенного отека легких могут быть: ингаляция токсических субстанций, тяжелая травма грудной клетки, острые вирусные заболевания легких (пневмонии), сепсис, аспирационный синдром, радиационное повреждение легких, переливание крови, панкреонекроз, политравма, кровопотеря.
Симптомы отека легких
Относится к той группе состояний, диагностировать которую можно практически уже на расстоянии, поскольку симптомы отека легких у взрослых относятся к весьма характерным: выраженная одышка, преимущественно инспираторная, значительно реже — смешанная; ортопноэ (одышка в положении лежа); кашель с выделением мокроты; число дыханий превышает 30/мин.; холодный обильный пот; цианоз кожных покровов/слизистых; наличие в легких хрипов; тахикардия (ритм галопа), аускультативно — акцент 2 тона над легочной артерией.
Признаки отека легких у человека определяются патогенетическими процессами. Условно клинически выделяют несколько стадий:
- Диспноэтическая. Проявляется сухими хрипами, диспноэ, что связано с началом отека преимущественно интерстициальной легочной ткани, единичные влажные хрипы.
- Стадия ортопноэ. Характерно нарастание влажных хрипов, которых превалируют над сухими хрипами.
- Стадия развернутой клиники. Выраженное ортопноэ, хрипы отчетливо слышны на расстоянии.
- Тяжелая стадия. Множество разнокалиберных хрипов, выделение пены, обильный холодный пот, прогрессирующий диффузный цианоз.
В практике чрезвычайно важно различать интерстициальную и альвеолярную стадию развития отека. Интерстициальному отеку легких соответствует клиническая симптоматика сердечной астмы, что обусловлено резким ухудшением обмена кислородом и углекислотой между кровью и воздухом альвеол, способствующее повышению сосудистого и бронхиального сопротивления.
Приступ сердечной астмы, как правило, развивается в ночной период времени. Больной просыпается от сильного ощущения недостатка воздуха, вынужденно принимает положение сидя, пытается открыть окно, появляется страх смерти, возбуждение, на вопросы не отвечает, сосредоточившись на борьбе за воздух.
Продолжительность приступа сердечной астмы варьирует от 5-10 минут до 1-3 часов. При аускультации— сухие хрипы, в нижних отделах легких ослабленное дыхание. В случаях хронической сердечной недостаточности, митрального стеноза, сопровождаемых гиперволемией малого круга кровообращения для диагностики интерстициального отека большее значение имеет рентгенологическое обследование. На рентгенограмме отмечаются характерные признаки — усиление легочного рисунка, который особенно выражен в прикорневых зонах, что обусловлено наличием лимфатических пространств и отечной инфильтрации перибронхиальной/периваскулярной и межуточной ткани; наличие линии Керли и субплеррального отека.
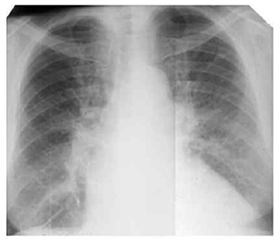
Рентген-снимок. Интерстициальной отек
Далее жидкость из интерстиция поступает в альвеолы, что вызывает альвеолярный отек легких со спаданием альвеол, разрушением сурфактанта, затоплением альвеол транссудатом. На этой стадии может происходить образование стойкой белковой пены, которая перекрывает просвет бронхов/бронхиол, что приводит к гипоксемии и гипоксии.
Острый альвеолярный отек легких относится к более тяжелой форме проявления левожелудочковой недостаточности. Переход интерстициального отека к альвеолярному зачастую происходит достаточно быстро – на протяжении нескольких минут. Бурно протекающий альвеолярный отек чаще развивается в дебюте инфаркта миокарда или на высоте гипертонического криза.
Характерным является громко клокочущее дыхание с выделением белой или из-за примеси эритроцитов розовой пены. На этом фоне резко нарушается оксигенация крови и присутствует высокий риск асфиксии. Как правило, развернутая клиническая симптоматика альвеолярного отека является ярко выраженной и не вызывает затруднений с постановкой диагноза. Дополнительным характерным признаком является появление значительного количества влажных разнокалиберных хрипов, иногда присутствуют и сухие хрипы. Альвеолярный отек, как и сердечная астма, наблюдается преимущественно в ночное время. Приступ может быть как кратковременным, который проходит самостоятельно, так и длительным, продолжающимся несколько часов. В случаях сильного пенообразования может быстро наступить смерть от асфиксии, буквально на протяжении 5-10 минут после появления первых клинических проявлений.
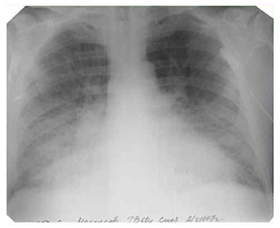
Рентген-снимок. Альвеолярный отек легких.
При альвеолярном отеке легких типичная рентгенологическая картина обусловливается пропитыванием транссудатом симметрично в обоих легких с локализацией отека преимущественно в базальных и прикорневых отделах.
Лабораторные данные клинического значения не имеют и сводятся преимущественно к резким изменениям в газовом составе (гипоксемия) и кислотно-щелочном состоянии крови (метаболический ацидоз). На ЭКГ — тахикардия, повышение/деформация амплитуды зубца Р, снижения сегмента ST.
При застойной сердечной недостаточности, обусловленной снижением сократительной возможности левого желудочка отек чаще развивается при нарушениях сердечного ритма/повышении АД, приводящих к снижению минутного объема крови.
Анализы и диагностика
Диагностическими критериями являются жалобы на резкое ощущение нехватки воздуха, сухой/влажный кашель, позже выделение пенистой мокроты; наличие в анамнезе различных заболеваний сердца (ХСН, ИБС, кардиомиопатии, АГ) или некардинальных причин.
Физикальное обследование: к основным признакам острой левожелудочковой недостаточности относятся пароксизмальная ночная одышка, ортопноэ, двусторонние легочные хрипы, влажные холодные конечности, головокружение, спутанность сознания, олигурия, низкое пульсовое давление.
Вероятные признаки наличия ОСН: тахикардия (ЧСС> 120 уд./мин.)/брадикардия (ЧСС 25/мин. с вовлечением в дыхательный процесс вспомогательных мышц.
Лабораторные критерии постановки диагноза кардиогенного отека легких:
- Низкая сатурация кислорода (при пульсоксиметрии SaO2 45 мм.рт.ст. в артериальной крови).
- Дыхательная недостаточность гиперкапнического типа.
- Метаболический ацидоз.
- Рентгенография легких – признаки легочного застоя.
- ЭКГ – наличие нарушений проводимости, пароксизмальных нарушений ритма и ОКС, признаки структурного поражения сердца.
- Пульсоксиметрия — сатурации кислорода 25 в мин) проводится неинвазивная вентиляция легких специальными аппаратами в режиме CPAP/BiPAP.
Медикаментозное лечение проводится в зависимости от показателей артериального давления. Именно уровень АД у больных с ОСН имеет наибольшее значение в выборе лечебных препаратов при неотложных мероприятиях.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
- Код по МКБ-10
- Эпидемиология
- Причины
- Патогенез
- Симптомы
- Где болит?
- Стадии
- Диагностика
- Как обследовать?
- Какие анализы необходимы?
- Дифференциальная диагностика
- Лечение
- К кому обратиться?
- Лекарства
- Профилактика
- Прогноз
Подагра - системное заболевание, при котором в различных тканях откладываются кристаллы моноурата натрия и у лиц с гиперурикемией развивается воспаление, обусловленное внешнесредовыми и/или генетическими факторами.

[1], [2], [3], [4], [5]
Код по МКБ-10
Эпидемиология
По экспертным оценкам, подагрой страдает не менее 1-3% взрослого населения. Заболеваемость подагрой составляет в различных популяциях от 5 до 50 на 1000 мужчин и 1 9на 1000 женщин. Число новых случаев в год - 1-3 на 1000 у мужчин и 0.2 на 1000 у женщин, соотношение мужчин и женщин составляет 7:1. Пик заболеваемости отмечают в 40-50 лет у мужчин. 60 лет и старше - у женщин.
Причины подагры
Стойкая гиперурикемия (повышенный сывороточный уровень мочевой кислоты) - облигатный фактор риска развития подагры. Ранее гиперурикемией считали уровень мочевой кислоты выше 420 мкмоль/л, основываясь на точке супернасыщения сыворотки уратами, при которой начинают образовываться кристаллы моноурата натрия. Европейская лига по борьбе с ревматизмом рекомендует считать гиперурикемией уровень мочевой кислоты выше 60 мкмоль/л (6 мг/дл), что основано им результатах исследований, продемонстрировавших 4-кратное повышение риска развития подагры у мужчин и 17-кратное у женщин при превышении указанного уровня сывороточной мочевой кислоты.
Причины гиперурикемии: ожирение, артериальная гипертензия, приём лекарственных препаратов, генетические дефекты, приводящие к гиперпродукции уратов, другие сопутствующие болезни, приём алкоголя.

[6], [7], [8], [9], [10], [11]
Патогенез
Сильная интенсивность боли при подагре объясняется локальным синтезом чрезвычайно широкого спектра медиаторов, участвующих в сенситизация боле пых ноцицепторов, к которым относят простагландины, брадикинин, а также субстанцию Р. Напомним, что субстанция Р высвобождается из немиелинизированных нервных волокон и приводит к вазодилатации, экстравазации плазменных белков, высобождению простагландинов и цитокинов.
Среди многочисленных клеток, участвующих в развитии подагрического воспалении, особую роль придают нейтрофилам, выраженная инфильтрация которыми сини анальной ткани рассматривается как характерный признак подагрического артрита.
Установлено, что активация нейтрофилов кристаллами уратов приводит к высвобождению широкого спектра провоспалительных медиаторов: лейкотриенов, ИЛ-1, ИЛ-8, лизосомальных ферментов супероксидных кислородных радикалов, которые играют важную роль и повреждении тканей. Кроме того, активацией нейтрофилов при подагрическом артрите сопровождается активацией фосфолипаз А2 и D, мобилизацией внутриклеточного кальция, формированием инозитол-1,4,5-трифосфата и усилением фосфорилирования протеинкиназы. Взаимодействие между кристаллами уратов и нейтрофилами человека осуществляется через Fcy-рецепторы IIIВ (CD16) и CD11b/CD18.
Определённое значение может иметь и эндотелин-1 - эндотелиальный пептид, одним из многочисленных эффектов которого является регуляция миграции нейтрофилов. Имеются данные, что введение лабораторным животным рецепторных антагонистов эндотелина подавляет поступление нейтрофилов в перитонеальную полость, индуцированное внутрибрюшинным введением кристаллов уратов.
Для расшифровки молекулярных механизмов, лежащих в основе подагрического воспаления, активно изучаются сигнальные молекулы, принимающие участие в реализации ответа нейтрофилов на кристаллы уратов. Установлено, что в основе активации нейтрофилов кристаллы уратов участвуют тирозинкиназы Syk, Lyn и Hсk. Кроме того, идентифицировано несколько тирозин-фосфорилированных субстратов: р38 внеклеточная сигнальная киназа 1/2 , паксилин, Сb1 и SAM68. Напомним, что тирозинкиназа Syk участвует в регуляции фагоцитоза и активации нейтрофилов в ответ на кристаллы уратов. Syk-SH2 подавляет синтез лейкотриенов и активацию митогенактивированной протеинкиназы/фосфолипазы.
Другой потенциальный механизм связывают с активацией оси гипоталамус- гипофиз-надпочечник, проявляющейся в синтезе меланокортинов (адренокортикотропного гормона, меланоцитстимулирующего гормона), которые, в свою очередь, проявляют мощную противовоспалительную активность.
Имеются данные о том, что кристаллы уратов индуцируют синтез не только провоспалительных, но и ряда противовоспалительных медиаторов. К ним относятся рецепторные антагонисты ИЛ-1 и ИЛ-10, которые обладают способностью подпилить воспаление, индуцированное кристаллами уратов, а также трансформирующий фактор роста b. Особое внимание привлечено к трансформирующему фактору роста b, который обнаруживается и синовиальной жидкости у пациенток г подагрическим артритом и обладает способностью подавлять микрокристаллическое воспаление у лабораторных животных.
Ещё один уникальный механизм, определяющий своеобразное течение подагрического артрита, заключается в том, что кристаллы уратов обладают способностью быстро и селективно индуцировать экспрессию активированных рецепторов пролифератора пероксисом у (peroxisome proliferator-activated receptor у - PPAR-y). PPAR - члены суперсемейства ядерных гормональных рецепторов, которые действуют как лигандзависимые факторы транскрипции. Долгое время считалось, что РРАR-y экспрессируются главным образом в клетках жировой ткани (адиноциты) и участвуют в регуляции метаболизма липидов и глюкозы. Однако в настоящее время установлено, что PPAR экспрессируются в очень многих клетках, включай моноциты и макрофаги. По современным представлениям, фундаментальное значение PPAR заключается в отрицательной регуляции воспалительного ответа.
Таким образом, в основе развития подагрического воспаления лежит сложное взаимодействие различных типов клеток, приводящее к нарушению баланса между синтезом провоспалительных и противовоспалительных медиаторов.

[12], [13], [14], [15], [16], [17], [18], [19], [20], [21], [22], [23], [24]
Симптомы подагры
При отсутствии антигиперурикемической терапии более чем у половины боль пых повторный приступ развивается в течение первого года. В дальнейшем наблюдают учащение атак, сокращение продолжительности бессимптомного периода, затяжное течение артрита. Несмотря на проводимую противовоспалительную терапию, в патологический процесс вовлекаются новые суставы, поражения при обретают олиго- и полиартикулярный характер.

[25]
Образование депозитов кристаллов моноурата натрия в виде тофусов характерный признак болезни, наблюдаемый при подагре практически во всех органах и тканях. Развитие видимых тофусов, чаще подкожных или внутрикожных, в области пальцев кистей и стоп, коленных суставов, на локтях и ушных раковинах свойственно хронической стадии подагры. Иногда отмечают изъязвление кожи над тофусами со спонтанным выделением содержимого в виде пастообразной белой массы.
Пефролитиаз при подагре также относят к одной из тофусных форм, поскольку компоненты камней – ураты.
Тофусы могут появляться и в самой ранней стадии болезни подагры, что зависит от выраженности гиперурикемии и скорости кристаллообразования. Часто это наблюдается при хронической почечной недостаточности: у женщин пожилого возраста, принимающих диуретики; при некоторых формах ювенильной подагры, миелопролиферативных заболеваниях и посттрансплантанионной (циклоспориновой) подагре. Обычно наличие тофусов любой локализации сочетается с хроническим подагрическим артритом, при котором отсутствует бессимптомный период, а поражение суставов носит олиго- или полиартикулярный характер.

[26], [27], [28]
Читайте также:


