Эндопротезирование коленного сустава с костной аутопластикой

КЛИНИЧЕСКАЯ ОЦЕНКА ПРИМЕНЕНИЯ КОСТНОЙ И ЦЕМЕНТНОЙ ПЛАСТИК ДЕФЕКТОВ МЫЩЕЛКОВ ТИБИАЛЬНОГО ПЛАТО ПРИ ЭНДОПРОТЕЗИРОВАНИИ КОЛЕННОГО СУСТАВА
М.Ж. Азизов1, А.П. Алимов2, А.М. Азизов3
1 доктор медицинских наук, профессор, директор,
2 кандидат медицинских наук, старший научный сотрудник,
3 младший научный сотрудник
Научно-исследовательский институт травматологии и ортопедии МЗ Республики Узбекистан (Ташкент), Узбекистан
При дефектах мыщелков тибиального плато наиболее часто применяется аутокостная пластика или полное цементирование зоны дефекта, при этом нет определенной ясности в каких случаях приемлем тот или иной метод восполнения при тотальном эндопротезировании коленного сустава.
Целью настоящего исследования является изучение исходов оперативного лечения больных с дефектами мыщелков тибиального плато после эндопротезирования коленного сустава.
У 34 больных с дефектами мыщелков большеберцовой кости было произведено эндопротезирование коленного сустава; с аутокостной пластикой у- 15 и цементным заполнением у-19. Клиническое обследование больных проводилось по оценочной шкале для коленного сустава Bristol Knee Score.
На месте остеоимпакции имелось сращении аутокости с плато большеберцовой кости, а в зоне остеосклероза наблюдали явления лизиса со смещением бедренного компонента в передне-заднем и боковом направлениях до 2,0 мм, большеберцового компонента в переднезаднем направлении также до 2,0 мм над зоной цементной мантии.
При эндопротезировании коленного сустава с дефектами мыщелков тибиального плато возможно применение обоих видов замещения, у лиц пожилого возраста предпочтительнее цементное замещение, в более в молодом возрасте костная аутопластика.
Ключевые слова: дефекты тибиального плато, цементная и костная пластика, эндопротезирование коленного сустава.
Наличие дефектов мыщелков пораженного сустава представляют особые сложности при тотальном эндопротезировании коленного сустава.
При значительных некрозах и дефектах мыщелков коленного сустава А.В. Каземирский и соавтор. [1] с целью создания надежной опоры большеберцовых компонентов предложили следующее в тактических решениях:
- резекцию проксимального отдела большеберцовой кости на уровне дна дефекта;
- заполнение дефекта костным цементом;
- костная аутопластика;
- армирование цемента в зоне дефекта;
- смещение большеберцового компонента в сторону непораженного мыщелка от дефекта;
- металлические тибиальные модульные блоки [1].
Дефекты мыщелков большеберцовой кости приводят к осевым деформациям коленного сустава. Выравнивание варусного угла деформации с устранением дефекта внутреннего мыщелка большеберцовой кости возможно с применением резецированных костных пластин тибиального плато и фиксацией спонгиозными винтами, затем проводится имплантация эндопротеза. При длительном сроке наблюдения отмечаются положительные функциональные исходы без резорбции костного трансплантата [4].
Несложный и эффективный метод реконструкции костного дефекта медиального края тибиального плато аутокостью с фиксацией винтом способствует восстановлению механической оси и стабильности в коленном суставе при эндопротезировании, но с осторожностью необходимо применять при склерозе тибиального плато, так как могут быть осложнения в виде латерального смещения компонента эндопротеза с увеличением линии суставной щели и разламывание костного трансплантата [5].
Экспериментальное ремоделирование биомеханического стресса при поверхностном и полном цементировании компонентов эндопротеза коленного сустава в сравнении выявляет положительные стороны полного цементирования, так как тибиальное плато более резистентной к стрессовой нагрузке при большей толщине цементного слоя, чем при поверхностном, когда происходит резорбция окружающей костной ткани, способствующая асептической нестабильности [3].
Эндопротезирование коленного сустава при наличии значительных некротических дефектов мыщелков большеберцовой кости требует их коррекции для обеспечения полноценной фиксации компонентов. Применение костного трансплантата позволяет выполнить экономную резекцию суставных поверхностей мыщелков, значительно уменьшить количество костного цемента, используемого при трансплантации эндопротеза, обеспечить надежную опору для компонентов эндопротеза [1].
При дефектах мыщелков тибиального плато наиболее часто применяется аутокостная пластика или полное цементирование зоны дефекта, при этом нет определенной ясности в каких случаях приемлем тот или иной метод восполнения при тотальном эндопротезировании коленного сустава. В клинике выработана тактика, при которой замещение дефектов мыщелков проводится в зависимости от размера и глубины недостающей зоны мыщелка.
Целью настоящего исследования является изучение исходов оперативного лечения больных с дефектами мыщелков тибиального плато после эндопротезирования коленного сустава.
МАТЕРИАЛ И МЕТОДЫ
В отделении взрослой ортопедии клиники НИИТО МЗ РУз у 34 больных (19 женщин, 15 мужчин; средний возраст 67 лет) с дефектами мыщелков большеберцовой кости было произведено эндопротезирование коленного сустава; с аутокостной пластикой у- 15 и цементным заполнением у-19.
Оперативное вмешательство проводилось стандартным образом. Парапателярным доступом вскрывался сустав, удалялись патологически измененные ткани. После проксимальной резекции большеберцового плато, если определялся значительный дефект, то для аутокостной пластики во время фигурной остеотомии дистального отдела бедренной кости из межмыщелковой зоны выкраивался аутотрансплантат, который после придания формы соответствующей ложу дефекта был имплантирован и фиксирован винтом, после чего проводилось эндопротезирование сустава с цементной фиксацией.
Всем больным до и после оперативного вмешательства были проведены клинико-рентгенологические, лабораторные и инструментальные методы исследования (денситометрия, допплерография). Клиническое обследование больных проводилось по оценочной шкале для коленного сустава Bristol Knee Score (по J.MacKinnon и соавт., 1988).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЯ
Данные клинического обследования больных через 6 месяцев после операции, проводимое по оценочной шкале для коленного сустава Bristol Knee Score, в зависимости от вида замещения дефекта были распределены следующим образом. При аутокостной пластики у 9 больных был отмечен хороший исход (от 36 до 40 баллов), удовлетворительный результат (30-35 баллов) был получен у 6 больных. При цементном замещении у 10 больных был отмечен хороший исход, удовлетворительный был получен у 9 больных, неудовлетворительных результатов мы не отмечали.
При наблюдении за всеми больными через 1 год после операции клинические результаты были оценены как хорошие и удовлетворительные. Выраженный мышечный дисбаланс имелся у одного больного, который проявлялся дискомфортом в суставе. После принятия физиотерапевтических процедур и комплекса упражнений для укрепления и расслабления мышечных групп, данное чувство уменьшилось. На рентгенограмме определялся остеосклероз вокруг цементной мантии эндопротеза. На месте остеоимпакции имелось сращении аутокости с плато большеберцовой кости у больных более молодого возраста (от 50 до 58 лет), а в зоне остеосклероза наблюдали явления лизиса со смещением бедренного компонента в переднезаднем и боковом направлениях до 2,0 мм, большеберцового компонента в переднезаднем направлении также до 2,0 мм над зоной цементной мантии у лиц старшей возрастной категории (от 64 до 76 лет).
Денситометрические показатели позволили выявить остеопению в периферических сегментах скелета. Доплерографическое исследование - снижение кровотока по венам обоих голеней.
В качестве иллюстраций приводим случаи успешного тотального эндопротезирования коленных суставов.

Рис. 1 (а, б). Фотоснимки больной АХ. 52 года до и после лечения

Рис. 2. Фотоснимки коленного сустава больной А.Х. 52 года во время операции

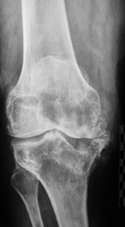
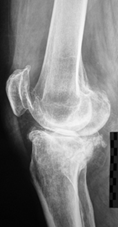
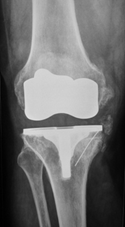
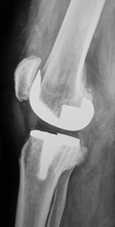
Рис. 3 (а, б). Рентгенограммы правого коленного сустава больной АХ. 52 года до и после лечения

Рис. 4. Рентгенограммы левого коленного сустава больного М.Р. 56 лет до лечения

Рис. 5 (а, б). Фотоснимки коленного сустава больного М.Р. 56 лет во время операции

Рис. 6 (а, б). Рентгенограммы левого коленного сустава больного М.Р. 56 после лечения
По мнению Liu J, несложный и эффективный метод реконструкции костного дефекта медиального края тибиального плато аутокостью с фиксацией винтом способствует восстановлению механической оси и стабильности в коленном суставе при эндопротезировании. Эту методику с осторожностью необходимо применять при склерозе тибиального плато, так как могут быть осложнения в виде латерального смещения компонента эндопротеза с увеличением линии суставной щели и разламыванием костного трансплантата [5].
Мы применили данную методику у одного больного с внутренним дефектом мыщелка большеберцовой кости и отметили консолидирование аутотрансплантата

Рис. 7 (а, б). МСКТ картина и интраоперационный фотоснимок больного А.Н. 46 лет

Рис. 8 (а, б). Интраоперационные снимки фиксации костного аутотрансплантата больного А.Н. 46 лет

При эндопротезировании коленного сустава с дефектами мыщелков тибиального плато возможно применение обоих видов замещения, у лиц пожилого возраста предпочтительнее цементное замещение, в более в молодом возрасте костная аутопластика.
Цементное замещение незначительных дефектных зон мыщелков обеспечивают достаточную стабильную фиксацию имплантата.
Остеоимпакция аутокостью из резецированных пластин большеберцового плато приводило к её сращению с плато большеберцовой кости, а в зоне остеосклероза происходил лизис костной ткани вокруг цементной мантии тотального эндопротеза коленного сустава.
Материал поступил в редакцию 20.10.15.
CLINICAL EVALUATION OF USING AUTOLOGOUS BONE GRAFTING AND CEMENTED FILLING OF CONDYLE DEFECT OF THE TIBIAL PLATEAU AT TOTAL KNEE ARTHROPLASTY
M.Zh. Azizov1, A.P. Alimov2, A.M. Azizov3
1 Doctor of Medicine, Professor, Head,
2 Candidate of Medicine, Senior Researcher,
3 Junior Researcher
Abstract. At condyle defect of the tibial plateau, autologous bone grafting or full cemented filling of the defect is mostly used, herewith no determined clarity in what events one or another method of the filling at total knee arthroplasty is acceptable.
The aim of this research is studying outcomes of operative treatment ofpatients with tibial condyle defect after total knee arthroplasty.
Methods. 34 patients with tibial condyle defect had total knee arthroplasty; 15 with autologous bone grafting and 19 with cement filling. The Clinical examination sick was conducted scale for knee joint Bristol Knee Score.
Results. On osteoimpaction place hadjoining of the tibial plateau, but in osteosclerosis area observed the osteolysis offset of the hip component in front-back and lateral directions to 2,0 mms, tibial component in front-back direction also to 2,0 mms above of the cement mantle.
Conclusion. At total knee arthroplasty with tibial condyle defect, using both types is possible, cement filling is preferable at elderly patients, autologous bone grafting - at younger patients.
Keywords: condyle defect of the tibial plateau, autologous bone grafting and full cemented filling, total knee arthroplasty.
В структуре дегенеративно-дистрофических заболеваний суставов деформирующий остеоартроз коленного сустава встречается у 54,7-69,7% пациентов, при этом поздние стадии заболевания составляют до 75% [2; 4; 5]. Нарушение биомеханической оси нижней конечности на декомпенсированных стадиях заболевания встречается в 64% случаев. В структуре заболеваний коленного сустава некроз мыщелков бедренной и большеберцовой кости занимает от 8 до 22% [1;6; 7]. Терминальная стадия аваскулярного некроза мыщелков большеберцовой кости характеризуется формированием остеонекротических дефектов и потерей костной массы мыщелка, что в 15–20% случаев приводит к выраженной деформации коленного сустава [3]. Для лечения декомпенсированной стадии гонартроза методом выбора является тотальное эндопротезирование коленного сустава с замещением костного дефекта. Костная аутопластика для замещения дефектов мыщелков большеберцовой кости используется хирургами значительно реже в сравнении с другими способами, что обусловлено не только трудным техническим исполнением данного метода, но и отсутствием единых методических рекомендаций как по способам получения аутокости для формирования аутотроансплантатов, так и по способам их фиксации.
Изучить ближайшие и отдаленные результаты лечения больных гонартрозом декомпенсированной стадии методом тотального эндопротезирования коленного сустава с замещением дефектов мыщелков большеберцовой кости модульными аутотрансплантатами.
Материал и методы исследования
Среди пациентов, поступивших на лечение, лиц женского пола было 43 (78,18%), мужского – 12 (21,82%). Возраст больных составил от 38 до 76 лет. Средний возраст соответствовал 63±0,5 года. Клинико-рентгенологическую стадию заболевания устанавливали по классификации Н.С. Косинской (1961). Односторонний гонартроз III ст. был диагностирован у 31 (56,36%) пациента, двусторонний II-III ст. – у 24 (43,64%). В 55 случаях определялся дефект мыщелков большеберцовой кости, из них в пяти (9%) случаях – двусторонний. При поступлении всем пациентам проводилось клиническое, лабораторное и инструментальное обследование. По шкалам Josef & Kaufman и KOOS выполняли балльную оценку функции коленного сустава, способности пациентов к самообслуживанию, выполнению ежедневной бытовой деятельности и физической активности. Полученные результаты сравнивали.
При анализе дооперационных рентгенограмм коленных суставов в 60 случаях определялся дефект мыщелка большеберцовой кости, медиального – в 59 случаях, латерального – в одном. В пяти (8%) случаях определялся дефект внутренних мыщелков большеберцовой кости с двух сторон. Оценку зоны дефекта мыщелков большеберцовой кости выполняли по рентгенограммам пораженного коленного сустава в передне-задней и боковой проекциях. Исследовали высоту и ширину дефектов в сагиттальной и фронтальной плоскостях. Степень поражения мыщелка (С) – процентное отношение ширины дефекта во фронтальной плоскости (dF) к ширине непораженного мыщелка во фронтальной плоскости (DF), рассчитывали по формуле: С = dF / DF × 100%. Значение высоты дефекта во фронтальной плоскости у больных в исследуемой группе было от 14 до 36 мм, в среднем 26±0,5 мм. Степень поражения мыщелка у больных в исследуемой группе варьировала от 62,2 до 100% и в среднем составила 83,5%.
При оценке вида и значения деформации коленных суставов в 58 (96,6%) случаях бедренно-большеберцовый угол имел варусное отклонение. Его значение варьировало от 135 до 175° и в среднем составило 161±2°. Вальгусное отклонение бедренно-большеберцового угла до 160° наблюдалось в одном (1,6%) случае. В одном случае бедренно-большеберцовый угол имел нормальное значение с вальгусным отклонением до 175°.
Техника оперативного вмешательства и послеоперационное ведение пациентов
В качестве анестезиологического пособия во всех случаях применяли спиномозговую анестезию с катетеризацией эпидурального пространства. Во всех случаях на верхнюю треть бедра накладывали манжету пневможгута. После обработки кожи раствором антисептика и драпировки стерильным бельем на операционное поле наклеивали хирургическую пленку. Выполняли продольный срединный разрез кожи в области коленного сустава до 20 см с учетом имеющейся деформации. Медиальным парапателлярным доступом выполняли артротомию коленного сустава. Тщательно выполняли артролиз и мобилизацию мыщелков бедренной и большеберцовой костей. Проводили визуальную оценку дефекта пораженного мыщелка, измеряли его глубину и приблизительную площадь для выбора способа получения аутокости для формирования трансплантата. Обработку суставных концов бедренной и большеберцовой костей выполняли с применением приемов, позволяющих уменьшить время операции и избежать трудоемких манипуляций. Аутокость получали в процессе резекции суставных концов бедренной и большеберцовой костей с применением способов, целью которых являлось получение максимального объема аутокости с требуемыми качественными характеристиками, уже подготовленную для формирования аутотрансплантата требуемой высоты и формы. После окончательной обработки тибиального плато выполняли моделирующую резекцию кости в области дефекта пораженного мыщелка с максимальным сохранением костной массы мыщелка, что обеспечивает условия для надежной фиксации аутотрансплантата и его сращения со стенками и дном ложа трансплантата. Из ранее полученной аутокости по разработанной методике формировали аутотрансплантат необходимой высоты и формы, добиваясь полной конгруэнтности его граней со стенками и дном ложа трансплантата. Для фиксации аутотрансплантатов использовали оригинальные фиксаторы в виде скоб с П-образным профилем, изготовленные в процессе оперативного вмешательства путем двукратного сгибания спицы из нержавеющей стали Ø 1 мм. Длина полок и зубьев скоб, а также количество фиксаторов были индивидуальными в каждом случае и зависели от высоты и площади остаточного дефекта мыщелка после выполнения моделирующей резекции. В дальнейшем приступали к цементированию и окончательной установке компонентов эндопротеза. В течение времени, необходимого для полимеризации костного цемента, конечность удерживали в положении разгибания в коленном суставе 180°. При этом осуществляли умеренную компрессию по оси конечности для лучшей интеграции цемента в костные трабекулы. Одновременно выполняли формирование суставной поверхности надколенника и производили денервацию по его периметру. Расслабляли клапан манжеты пневможгута и выполняли тщательный гемостаз, после чего устанавливали полиэтиленовый суставной вкладыш. Осуществляли вправление голени. Между этапами операции регулярно осуществляли промывание полости сустава изотоническим раствором хлорида натрия общим объемом около 1500 мл. В полость сустава вводили от одной до двух дренажных трубок. Реинфузатор устанавливали по показаниям. В положении разгибания в коленном суставе сухожильное растяжение надколенника в области его верхнего полюса сводили цапкой, определяли функцию коленного сустава. Допустимыми значениями функции коленного сустава считали: сгибание – 90°, разгибание – 180°. Рану ушивали послойно в положении сгибания в коленном суставе 120–130°. Накладывали повязки. Для профилактики тромбоэмболических осложнений выполняли эластическую компрессию обеих нижних конечностей сразу после наложения повязок. Выполняли контрольные рентгенограммы коленного сустава в двух проекциях. Со вторых – третьих суток активизировали всех пациентов, обучали ходьбе при помощи двух костылей. ЛФК оперированного сустава на сгибание и разгибание в щадящем режиме назначали с третьего дня после операции. Контрольную рентгенографию оперированного сустава выполняли после снятия швов. Рекомендовали ходьбу при помощи двух костылей с дозированной нагрузкой на оперированную конечность в течение 1,5-2 месяцев после операции, с постепенным переходом к полной. Пациентам, имевшим двустороннее поражение, рекомендовали ходьбу при помощи двух костылей и использование подбивки под обувь для коррекции разности длины конечностей в течение всего периода реабилитации до выполнения оперативного вмешательства на втором коленном суставе. Контрольные осмотры проводили через 3, 6 и 12 месяцев после операции, в последующем – ежегодно.
В оставшейся группе ближайшие результаты лечения были изучены у всех пациентов. Отдаленные результаты изучены у 33 (55%) пациентов, из них: более 12 месяцев после операции – у 13, более двух лет – у 18 (32,7%), более трех лет – у двух (3,6%) пациентов.
Амплитуда движений в коленном суставе до оперативного лечения в среднем составила 78±2° (n=60). В раннем послеоперационном периоде её среднее значение составило 92±2° (n=58). В сроки от 1 до 3 лет среднее значение амплитуды движений составило 108±2° (n=33). В шести случаях (10,3%) на сроках более 12 месяцев после операции наблюдался рецидив сгибательной контрактуры оперированного сустава в среднем до 7°, что связывали с недостаточным объемом функциональной реабилитации пациентов по месту жительства. При оценке результатов лечения по шкале KOOS на дооперационном этапе результаты были неудовлетворительными в 15 (25%) случаях, в 33 – удовлетворительными, в 12 (20%) – хорошими. Через один год после лечения были получены отличные результаты в 13 (24%) случаях, хорошие – в 44. В сроки наблюдения до трех лет отличные результаты наблюдались в 35 (62%) случаях, хорошие в 23. В срок наблюдения более трех лет у всех пациентов результаты были отличными. При балльной оценке результатов по шкале Joseph & Kaufman на дооперационном этапе результаты были неудовлетворительными в 6 (9%) случаях, в 54 – удовлетворительными. Среднее значение составило 37,8 балла (n=60). Через один год после лечения были получены отличные результаты в 52 (90%) случаях, хорошие – в 6 (10%). В сроки наблюдения до трех лет и более - отличные результаты наблюдались во всех случаях наблюдения.
Рентгенограммы правого коленного сустава до и после лечения
Диагноз: правосторонний посттравматический гонартроз III ст. Дефект медиального мыщелка правой большеберцовой кости, глубина 20 мм.
Выполнено эндопротезирование коленного сустава с аутопластикой дефекта медиального мыщелка большеберцовой кости. Аутотрансплантат получен из межмыщелкового опила бедренной кости, высота 12 мм. Фиксация двумя скобами с П-образным профилем.
1. Применение костной аутопластики для замещения дефектов мыщелков большеберцовой кости при первичном эндопротезировании коленного сустава:
– является эффективным методом реабилитации больных гонартрозом декомпенсированной стадии, осложненным формированием дефектов мыщелков большеберцовой кости;
– дает возможность восстановить форму и утраченный объем костной ткани пораженного мыщелка, и тем самым создать условия для надежной стабильной фиксации большеберцового компонента эндопротеза, увеличить прогнозируемые сроки его выживаемости, обеспечить более благоприятные условия для возможных ревизионных вмешательств;
– позволяет обеспечить максимальное сохранение костной ткани пораженного мыщелка в сравнении другими способами компенсации дефектов;
– существенно снижает стоимость оперативного лечения в сравнении с применением для замещения дефектов мыщелков модульных блоков, компенсаторов высоты проксимального отдела большеберцовой кости, систем ревизионного эндопротезирования, дополнительного объема костного цемента;
– дает возможность достичь удовлетворительной фронтальной стабильности сустава с суставным вкладышем минимальной высоты.
2. Разработанный алгоритм позволяет уменьшить продолжительность операции и количество трудоемких энергозатратных манипуляций.
3. Разработанные способы моделирующей резекции мыщелка в области дефекта при формировании ложа трансплантата, способы получения аутокости и формирования трансплантатов, способы улучшения внутрикостной микроциркуляции увеличивают вероятность консолидации и полной перестройки аутотрансплантатов.
4. Разработанные способы получения аутокости при резекции суставных концов бедренной и большеберцовой костей дают возможность получить аутокость с требуемыми качественными характеристиками без значимого увеличения продолжительности оперативного вмешательства и выполнения энергозатратных манипуляций.
5. Оригинальные фиксаторы обеспечивают стабильную фиксацию аутотрансплантатов и создают достаточную компрессию.
6. Два случая ранней нестабильности большеберцового компонента эндопротеза в ближайшие сроки изучения, вероятно, были обусловлены выраженной степенью остеопороза проксимального отдела большеберцовой кости. При этом в одном случае аутопластика дефекта мыщелка большеберцовой кости была состоятельной, а плотность кости в области замещенного дефекта существенно превосходила плотность кости контрлатеральной части плато большеберцовой кости. В обоих случаях наблюдалось хорошее кровонаполнение костных трабекул в области замещенного дефекта.
7. Предложенные способы получения аутокости, способ моделирующей резекции в области дефекта мыщелков, способы формирования аутотрансплантатов и оригинальные фиксаторы являются альтернативными и обеспечивают оптимизацию лечения данной категории пациентов методом тотального эндопротезирования коленного сустава. Полученный высокий реабилитационный потенциал лечения больных свидетельствует о необходимости более широкого внедрения разработанных предложений в клиническую практику.
Pецензенты:
ISSN: 1819-1495
E-ISSN: 2541-867X

Д.А. Марков
ФГБОУ ВО СГМУ им. В.И. Разумовского Минздрава России, г. Саратов
Россия
к.м.н., доцент кафедры травматологии и ортопедии
К.П. Зверева
ФГБОУ ВО СГМУ им. В.И. Разумовского Минздрава России, г. Саратов
Россия
ассистент кафедры травматологии и ортопедии
В.Н. Белоногов
ФГБОУ ВО СГМУ им. В.И. Разумовского Минздрава России, г. Саратов
Россия
к.м.н., ассистент кафедры травматологии и ортопедии
А.Ю. Трошкин
ФГБОУ ВО СГМУ им. В.И. Разумовского Минздрава России, г. Саратов
Россия
ординатор кафедры травматологии и ортопедии
№ 1 - 2020

Марков Д.А., Зверева К.П., Белоногов В.Н., Бычков А.Е., Трошкин А.Ю.
Саратовский государственный медицинский университет им. В.И. Разумовского,
Саратовская городская клиническая больница № 9,
г. Саратов, Россия
КОСТНАЯ АУТОПЛАСТИКА КРЫШИ ВЕРТЛУЖНОЙ ВПАДИНЫ ПРИ ТОТАЛЬНОМ ЭНДОПРОТЕЗИРОВАНИИ У ПАЦИЕНТОВ С ДИСПЛАСТИЧЕСКИМ КОКСАРТРОЗОМ
Ключевые слова: диспластический коксартроз; тотальное эндопротезирование; костная аутопластика
В настоящее время диспластический коксартроз в структуре дегенеративно-дистрофических заболеваний тазобедренного сустава прочно занимает второе место 1. Встречаемость патологии по различным данным колеблется от 25 % до 77 % [1, 4]. Эпидемиологическая составляющая представлена молодыми пациентами женского пола в возрасте от 30 до 40 лет [1, 2, 5]. Инвалидизация и снижение трудоспособности регистрируются в 11,5 % и 70 % случаев соответственно [1, 2]. На настоящий момент основным методом лечения патологии признается тотальное эндопротезирование, позволяющее в кратчайшие сроки избавить пациентов от выраженного болевого синдрома и улучшить их социальную адаптацию [6, 7]. Однако имеющиеся дефекты задне-верхнего и передне-верхнего краев вертлужной впадины при диспластическом коксартрозе в случае тяжелой степени дисплазии не только значительно утяжеляют вмешательство, но и способствуют ухудшению хирургических результатов и увеличению числа послеоперационных осложнений [3, 7, 8]. Наиболее перспективным вариантом обеспечения полного покрытия ацетабулярного компонента, по мнению большинства авторов, является способ импакционной костной пластики с фиксацией аутотрансплантата из опила головки бедренной кости в надацетабулярной области 9.
Цель исследования – провести анализ результатов тотального эндопротезирования тазобедренного сустава с применением костной аутопластики крыши вертлужной впадины у пациентов с диспластическим коксартрозом 1 и 2 типов по Hartofilakidis.
МАТЕРИАЛЫ И МЕТОДЫ
Техника оперативного вмешательства
В положении пациента на здоровом боку под спинно-мозговой анестезией после трехкратной обработки операционного поля выполняли передне-боковой доступ к тазобедренному суставу по Уотсон-Джонсону. Рассечение кожи, подкожно-жировой клетчатки и широкой фасции бедра осуществляли по классической методике. Отсечение сухожилия средней ягодичной мышцы выполняли в безопасной зоне, отступив на 2-3 смот места его прикрепления к большому вертелу, для возможности последующего восстановления отводящего механизма. Производили продольное рассечение капсулы сустава и вывихивание головки бедренной кости. Опил головки бедра осуществляли на уровне основания шейки. Расстановкой 4 ретракторов Хомана по окружности обеспечивали адекватный доступ к вертлужной впадине. Из опила головки бедренной кости при помощи осцилляторной пилы формировали спонгиозный аутотрансплантат трапециевидной формы (рис. 1).
Рисунок 1. Аутотрансплантат, приготовленный из опила бедренной кости
Вертлужную впадину очищали от рубцовых тканей. При помощи распатора удаляли склерозированные участки в области крыши до кровоточащей костной ткани. На подготовленное ложе укладывали сформированный аутотрансплантат и фиксировали его при помощи 2-3 спонгиозных винтов (рис. 2).
Рисунок 2. Аутотрансплантат, установленный в область крыши вертлужной впадины
Рисунок 3. Установленный ацетабулярный компонент
Вскрыв костно-мозговой канал бедренной кости окончатым долотом и осуществив его разработку рашпилями до необходимого размера, производили установку феморального компонента с углом антеверсии в пределах 10-20°. На примерочной головке выполняли проверку сустава на стабильность и определение объема движений. Производили установку металлической головки и вправление, после чего осуществляли послойное ушивание раны.
Характеристика установленных компонентов эндопротеза в зависимости от фирмы-производителя представлена в таблице 1.
Таблица 1. Характеристика установленных компонентов
Читайте также:


