Могут быть доброкачественной опухоли ребер
Рёбра представляют собой дугообразные кости, соединенные с позвоночником и грудиной, и выполняющие в теле человека такую функцию, как защита жизненно важных органов человека от внешних воздействий.
Рак рёбер – это редкое, но тяжёлое злокачественное образование, характерное в основном для детей и мужчин. Женщины подвержены болезни реже. Рак рёбер опасен тем, что расположение этих костей способствует быстрому распространению метастазов на близлежащие органы – сердце и лёгкие. А отсутствие симптомов на ранних стадиях уменьшает шансы на своевременное обнаружение болезни и удачное лечение.
Грудная клетка состоит из 24 рёбер, соединённых грудиной спереди и позвоночником сзади. В любом может появиться злокачественное образование. Хотя рак рёбер – редкое заболевание и по статистике не превышает 10% от общего числа заболеваний костной ткани, для самого больного это становится настоящим испытанием. В первую очередь, наличие опухоли даёт о себе знать уже на поздних стадиях. А во-вторых, даже при удачном лечении нет гарантии, что рецидива не произойдёт.
Симптомы
Первая стадия воспаления характеризуется отсутствием симптомов. Проявление болезни случается уже на 2-3 стадии развития раковых клеток. Этот факт затрудняет своевременную диагностику, что способствует быстрому распространению образования по органам из-за отсутствия лечения на ранних этапах развития болезни.
Первый признак присутствия злокачественного образования – боль в области груди. Нарастание болевых ощущений напрямую зависит от роста опухоли. Боль становится ощутима по мере роста новообразования и чаще выражается в вечернее и ночное время суток. Ночью больному становится больно дышать. Последние стадии болезни характеризуются сильными болями, которые не способны устранить даже сильнодействующие препараты.

Одновременно с появлением боли у больного проявляется кратковременное повышение температуры. Но так как боль носит тупой характер, а повышение температуры краткосрочное, то многие не связывают вместе эти два симптома.
При росте опухоли на наружной стороне при пальпации обнаруживается костный, рыхлый или твёрдый нарост в области ребра, покрытый тонкой кожей. Часто кожа на месте опухоли приобретает сосудистый рисунок, начинает лосниться.
Постепенно у больного ухудшается общее состояние. Отсутствие аппетита приводит к потере веса. Быстрая утомляемость сопровождается снижением трудоспособности. Снижение гемоглобина приводит к анемии.
Распространение метастазов на вегетативную нервную систему сопровождается нервными расстройствами. Учащаются нервные срывы, раздражительность, тревожность, постоянное чувство страха, депрессия.
Симптомы зависят от вида опухоли и вовлечённости в заболевание конкретного органа.
Виды заболевания
Рак рёбер подразумевает ряд разновидностей. Классификация заболевания зависит от вида тканей, затронутых воспалением.
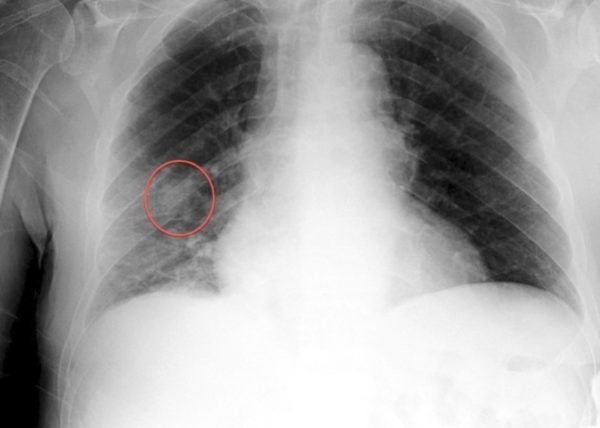
Новообразование затрагивает костные ткани. Опасна тем, что на ранних этапах болезнь не проявляется. Симптомы отсутствуют. Тупая боль появляется, когда новообразование начинает разрастаться. Рост и возникновение новых раковых клеток характеризуется усилением болевых ощущений, в том числе и при дыхании, а также периодическим повышением температуры тела. Остесаркома может развиваться как наружу, так и внутрь. Наружную остеосаркому легко обнаружить путём пальпации. О наличии внутренней опухоли человек может узнать только после появления болевых ощущений при увеличении новообразования.
Новообразованием затрагивается хрящевая ткань костей. Для этого вида саркомы характерны припухлости, отёки на месте образования раковых клеток. Признаки наличия хондросаркомы легко обнаружить, так как они появляются уже на средних стадиях остеосаркомы, когда за основной болезнью уже ведётся наблюдение.
Указанный вид рака затрагивает связки и сухожилия грудной клетки. Внешние признаки болезни проявляют себя в виде припухлости синевато-коричневого оттенка. Отличается от остальных видов рака рёбер болезненными ощущениями во время пальпации. Фибросаркома быстро разрастается, образуя метастазы.
Редкая разновидность заболевания. Развитие болезни начинается с сосудов и быстро образует метастазы.
Факторы риска
Онкология – заболевание, которое не щадит никого. Возраст и пол равнозначны. Раку рёбер больше остальных подвержены мужчины и дети до 15 лет.
Причины возникновения
Причины появления новообразования:
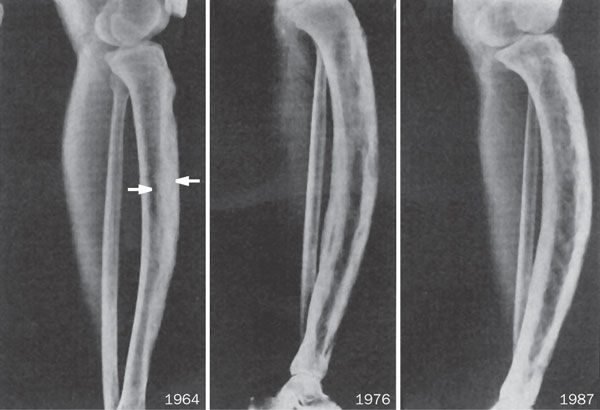
- Заболевание костей. К примеру, болезнь Педжета либо фиброзная дисплазия.
- Канцерогенные вещества. Попадая в организм человека, эти химические элементы способны вызвать в ДНК необратимые изменения, способствующие образованию раковых клеток.
- Наследственность. Прямой зависимости возникновения раковых клеток у человека по причине того, что у ближайших родственников выявлен рак, медицина не доказала. Но статистика показывает, что если одному из родителей поставлен диагноз рак рёбер, как правило, риск возникновения болезни у детей таких родителей достаточно высок.
- Радиация. К сожалению, необходимое лечение одного очага заболевания может стать причиной возникновения нового. Лучевая терапия, применимая однажды для блокирования раковых клеток, часто влияет на развитие другой раковой опухоли даже спустя годы после облучения.
- Отклонения в генетическом коде. Учёными доказана прямая связь между нарушениями в определённых хромосомах и увеличением риска развития злокачественных опухолей у человека. А вот по каким причинам происходит патология в хромосомах, учёные до сих пор не выявили. Есть предположение, что данные сбои в генетике происходят ещё во внутриутробном развитии. Ребёнок становится невинной жертвой страшной болезни уже во время своего формирования.
- Снижение иммунитета. На появление раковых клеток в организме может повлиять наличие других заболеваний, связанных со снижением иммунитета. К примеру, СПИД или сифилис.
- Возраст. Учёные обнаружили, что возникновение рака у детей напрямую связанно с их активным ростом в подростковом периоде.
Диагностика рака рёбер
Диагностировать злокачественное новообразование в костях тяжело, так как первые симптомы появляются не сразу. А возникающая периодически боль в груди часто воспринимается как боль после травмы либо невралгия.
Основные методы диагностирования наличия опухоли:
- рентген;
- компьютерная томография;
- позитронно-эмиссионная томография;
- биопсия.
Предоставляет точное описание опухоли. На рентгене отображается размер, структура, распространение новообразования. При этом конкретный вид рака выглядит на рентгене по-разному. Рентгенограмму назначают на первых этапах диагностики.
Второй этап исследования – компьютерная томография. Помогает выявить плотность образования, степень распространённости и метастазирования злокачественного образования.
Диагностика РС помогает выявить количество очагов, их распространение и метастатическое поражение затронутых опухолью костей.
Важный заключительный этап исследования перед назначением лечения. Биопсия помогает в определении вида новообразования. После этого врач назначает лечение, исходя из совокупности результатов.
Лечение
Лечение рака костей грудной клетки включает удаление опухоли путём хирургического вмешательства и дальнейшего проведения химио- и лучевой терапии. Проведение повторной, послеоперационной химиотерапии обязательно при обнаружении воспаления на поздних стадиях, большой локализации опухоли и объёмном метастазировании близлежащих органов. Повторное проведение терапии направлено на уменьшение размеров очага и купирование образования.
Хирургические методы лечения считаются приоритетными для предотвращения возможного дальнейшего распространения новообразования. Хирургам редко приходится встречаться с данным видом злокачественной опухоли. Проводят такие операции только опытные врачи. Удаляться может как одна поражённая кость, так и при необходимости несколько рёбер вместе с грудиной.
Рак рёбер – злокачественный вид опухоли, поражающий грудной каркас. После удаления поражённых рёбер и грудины хирургическим путём проводится операция по восстановлению грудной клетки. После операции удалённые части исследуют. Если края резекции не задеты раковыми клетками это означает, что операция принесла положительный результат, и очаг воспаления удален полностью.
Лучевая терапия назначается единственно при наличии запущенной стадии рака для облегчения общего состояния пациента, поскольку эффективна не при всех видах опухоли. Облучение назначают при наличии саркомы Юинга.
Прогнозы
При болезни рака рёбер высока вероятность появления новых очагов новообразования. По статистике 30-40% прооперированных подвержены повторению рецидивов. Усложняют ситуацию симптомы, которые проявляются уже на поздних стадиях рака. Успешное лечение этой болезни не гарантирует отсутствие рецидива.
Метастазы часто сопровождают злокачественную опухоль костей, что усугубляет положение. Как показывает статистика, повторное возникновение воспалений часто приводит к летальному исходу.
Остеома ребра характеризуется разрастанием костной ткани в результате внутренней опухоли. Изменение костной структуры происходит внутри кости, патогенез обусловлен нарушением клеточной регенерации. Заболевание встречается в 15% всех заболеваний скелета. Остеомы чаще диагностируют у детей раннего возраста и у молодых людей до 25 лет. Распространённость среди детей объясняется постоянным ростом костной ткани и интенсивным формированием скелета.
Остеома ребра — что это такое?

Остеома — доброкачественное новообразование, развивающееся внутри кости. Локализация в рёберной дуге относится к частым клиническим ситуациям, редко проявляет себя выраженной симптоматикой. Размер растущей опухоли совпадает с размером кости, завершается при заполнении полости.
Существует два типа внутрикостных остеом:
- Солитарные, ограниченные или одиночные;
- Множественные.
Последние могут заполнить всю костную ткань и значительно изменить форму рёберной дуги.
Заболевание нередко сочетается с другой патологией – синдромом Гарднера, который в свою очередь сочетается полипозом кишечника (симптом полипов кишечника вот тут), неоплазией кожных покровов, соединительной и костной ткани. Клетки малигнизируют крайне редко. Остеома ребра код по МКБ-10 — D16.7 — остеома ребер, грудины и ключицы.
Существует два основных типа остеомы рёберных дуг:
- Гиперпластические — причиной становится разрастание костной ткани (остеомы и остеоидные остеомы);
- Гетеропластические — развитие обусловлено делением соединительной ткани (остеофиты).
Структура остеомы не отличается от здоровой целостной ткани.
При обнаружении рёберной остеомы важно учитывать степень плотности новообразований:
- Твёрдые опухоли — пластины расположены скученно, однако костномозговой ткани и канальцев мало;
- Губчатые или пористые — новообразование в разрезе имеет пористую структуру, между костными канальцами пролегает обильный сосудистый компонент, соединительная и мягкая ткани с выраженными остеогенными свойствами;
- Мозговидные — крупные полости с обильным костномозговым компонентом.
Опухоли способны формироваться на любом участке рёберных дуг, а патологический процесс может быть односторонним или двусторонним.
По результатам снимка выделяют два типа реберной остеомы:
- Компактные. Выпячивание в дужках отсутствует, опухоль сосредоточена внутри кости. Компактные остеомы имеют форму шара правильной формы. На снимке определяется как тень без явной структуры, имеет место небольшое утолщение ребра.
- Губчатая. Опухоль крупных размеров, кость утолщена, имеет холмообразную форму в очаге присутствия. На снимке определяется участок округлой формы, который отграничен внутренними тканями рёберных дуг.
Классификация позволяет начать адекватное лечение, составить правильный прогноз на выздоровление и тактику дальнейшего ведения пациента.
Причины возникновения

Патогенез заболевания до конца не выяснен. Частой причиной считают наследственную предрасположенность, врождённые патологии развития тканей и особенности созревания костей.
Способствовать возникновению болезни могут следующие факторы:
- ревматоидный артрит;
- подагра;
- сифилис на поздних стадиях.
В группе риска мальчики и юноши до 20 лет. Наследственный фактор составляет почти 55%.
Врождённые рёберные остеомы развиваются в результате патологии развития тканей мезенхимы — эмбриональных зачатков мягкой, соединительной и костной тканей.
Симптомы
Часто заболевание обнаруживают случайно по причине отсутствия выраженной симптоматики. На ранних этапах даже множественных остеом опухоль не провоцирует расширения кости, появления бугорков и изменения рельефа рёберной дуги.
Первые признаки появляются только после увеличения остеомы в размере.
Характерными симптомами считают:
- болезненные ощущения;
- межрёберная невралгия (из-за компрессии нервных корешков);
- внешняя припухлость кожи в области поражения.
Во время первичного осмотра пациента врачи нередко первоначально подозревают миозит или плеврит легких.
По мере прогрессии заболевания могут появляться и внешние признаки:
- припухлость,
- покраснение кожных покровов,
- повышение местной температуры.
Частой локализацией рёберной остеомы считается область сочленения ребра с хрящом или шейкой дуги.
Диагностические мероприятия

Остеома является областью исследования травматологии и хирургии. Диагностика рёберной остеомы заключается в дифференциации патологий внутренних органов, расположенных вблизи рёбер, а это лёгкие, позвоночник, желудок и сердце.
Первоначально назначают следующие исследования:
- анализ крови на воспаление, уровень щелочной фосфатазы, кальция;
- рентген грудной клетки, флюорограмма;
- изучение костной ткани с применением контрастного вещества;
- МРТ или КТ-исследование;
- биопсия тканей (проводится после ампутации или удаления поражённого очага).
По результатам проведённых исследований определяют тип опухоли — остеоидная или простая. При остеоидной форме наблюдается значительное разрастание клеток, которые отвечают за рост кости. Такой тип опухоли соотносят с одним из видов хронического остеомиелита (воспаления костной ткани).
При недостаточности исследований прибегают к дополнительным методам диагностики:
- дооперационная биопсия лапароскопическим методом,
- ангиография,
- ультразвуковое исследование,
- радиоизотопное изучение тканей.
При появлении сильных болей в рёбрах и при обнаружении неких структурных изменений важно отделить остеому от:
- патологического вывиха,
- остеомиелита,
- сепсиса,
- контрактуры и ограничения подвижности,
- гнойного артрита.
Тактика лечения
При отсутствии симптомов врачи придерживаются выжидательной тактики. Возможно до конца жизни опухоль никак себя не проявит и хирургическое лечение не потребуется.
Основными показаниями к вмешательству по поводу остеомы ребра являются:
- боли при вдохе;
- усиление болезненности при подвижности, смене положения тела.
Прямым показанием является значительное ухудшение качества жизни больного при диагностированной опухоли рёберной дуги. После проведённого вмешательства рецидивы исключены.
Подготовка к удалению заключается в тщательном сборе данных различных диагностических исследований. Учитывая необходимость общего наркоза, важно изучить аллергологический анамнез на лекарственные препараты во избежание жизнеугрожающих осложнений.
Накануне операции выполняют такие рекомендации:
- последний приём пищи не позднее 18.00 предшествующего вечера;
- последнее питьё не позднее, чем за 2 часа до операции.
Обязательно проводят общеклинические исследования (ЭКГ, ЭХОКГ при наличии проблем с сердцем, флюорограмма, анализ крови и мочи). Дополнительно могут потребоваться консультации невропатолога, кардиолога, эндокринолога.
Если пациент напуган или сильно напряжён, врачи вводят седативные препараты для купирования чрезмерного возбуждения (например, раствор морфина).

Операция по удалению рёберной опухоли проводится несколькими методами:
- Хирургическое иссечение — извлечение опухоли инструментами в пределах здоровых тканей;
- Кюретаж — выскабливание опухоли и очищение ядра от патологических включений;
- Полное или частичное удаление ребра.
Сначала хирург осуществляет надрез в области предполагаемой опухоли, изучает состояние кости. При поражении значительного объёма костной ткани принимают решение о резекции или удалении единицы рёберной дуги вместе с повреждёнными кровеносными сосудами. После купируют кровотечение и наглухо ушивают раневую поверхность.
Кюретаж проводится редко из-за риска повреждения здоровых тканей. Радикальную хирургию выполняют наряду с малоинвазивными методами воздействия на опухоли.
Малоинвазивный метод, позволяющий удалить опухоль небольшого объёма при осложнённом онкологическом анамнезе. Техника называется радиочастотное излучение с компьютерно-томографическим наведением. В момент манипуляции требуется местный наркоз. Ядро опухоли обнаруживается при помощи компьютерной томографии, после чего внутрь вводят высокочастотный радиодатчик. Опухоль нагревают до 90 градусов и уничтожают.
Эта методика защищает ткани от инфицирования, исключает повреждение здоровых тканей. Основной недостаток — вероятность оставления незначительной части остеомы и рецидивы в отдаленном будущем.
После любого объёма оперативного вмешательства пациент наблюдается в стационарных условиях. Рёберные дуги фиксируются специальным корсетом для обеспечения неподвижности и восстановления кровообращения.
Во избежание послеоперационного инфицирования рекомендуется назначение следующих медикаментозных препаратов:
- антибиотики широкого спектра действия (Супракс, Цефтриаксон, Сумамед);
- спазмолитики и обезболивающие препараты для инъекционного или перорального введения (Но-шпа, Дротаверин, Ибупрофен);
- местные обезболивающие средства (Капсикам, Финалгон).
Одновременно проводят регулярные перевязки раневой поверхности, соблюдают постельный охранительный режим.
Спустя 5-7 суток пациента выписывают для домашнего наблюдения. Дома рекомендуется исключать физические нагрузки. Пища должна быть обогащена витаминами, белком и кальцием для наилучшего восстановления организма.
После окончательной выписки больного ставят на учёт к травматологу и хирургу, которых важно посещать не менее 2 раз в год для контроля над восстановлением тканей ребра.
Многие родители паникуют, заметив папилломы на шее у ребёнка. Мы рекомендуем не делать поспешных выводов и обратиться за консультацией к специалистам, а начать следует с педиатра.
Можно ли прижигать папилломы чистотелом узнайте здесь. Обратите внимание, что перед использованием средства в домашних условиях необходимо выяснить тип вируса.
Нередко боли в области рёбер вводят в панику людей, так как вызывают ассоциации с сердечными проблемами.
Межрёберная невралгия или серьёзный повод бежать к врачу, попробуем разобраться:
Прогноз
Остеомы с локализацией в рёберных дугах редко ухудшают качество жизни человека, не трансформируются в онкологические новообразования. Осложнения возникают только при множественном распространении, сочетанности с другими патологиями костной ткани, а также при компрессии нервных корешков. Прогноз при заболевании благоприятный, зависит от своевременного адекватного лечения. Обычно остеома рёберной кости хорошо поддаётся лечению, не рецидивирует, не несёт прямой угрозы для жизни и здоровья пациента.
О методах лечения остеомы нижней челюсти читайте в этой нашей статье.
Записаться на приём к врачу вы можете непосредственно на нашем ресурсе.
Опухоли и диспластические процессы ребер и грудины встречаются сравнительно часто. В связи с особенно важной функцией грудной стенки в дыхании правильная диагностика и лечение ее заболеваний приобретают особое значение. Однако, несмотря на большое число работ, освещающих некоторые аспекты этой проблемы, обобщающих работ нет или проводимые исследования также посвящены отдельным разделам.
Наш опыт основан на лечении 147 больных с опухолями и диспластическими процессами ребер и 49 больных с опухолями и диспластическими процессами грудины.
Среди оперированных нами больных, у которых поражение ребер было основным очагом заболевания, некоторым пациентам со злокачественными опухолями выполняли только трепанобиопсию.
Злокачественные опухоли ребер обнаружены у 48 больных, из них остеогенная саркома — у 17, полиморфно-клеточная — у 1, фибросаркома — у 2, ретикулосаркома — у 6, паростальная саркома — у 1 и хондросаркома — у 21 больного.
Доброкачественные опухоли ребер выявлены у 31 больного, в том числе: остеоид-остеома — у 2, гигантоклеточная опухоль — у 5, хондрома — у 10, хондробластома — у 1, хондромиксоидная фиброма — у 1, липома ребер — у 2, фиброма — у 6, гемангиома — у 2 и неврогенные доброкачественные опухоли — у 2 больных.
Диспластические процессы ребер обнаружены у 75 больных, из них фиброзная дисплазия — у 23, экзостозная дисплазия — у 37, болезнь Педжета — у 2, эозинофильная гранулема — у 1, спонтанное рассасывание — у 5, ангиодисплазия — у 7 больных.
Наблюдения хирургов свидетельствуют, что опухоли грудины в основном злокачественные (85 %), половина опухолей ребер — доброкачественные.
В клинике братьев Мейо под наблюдением находились 2000 больных с опухолями костей, из них 44 — с опухолями грудины. Нидерландский центр опухолей костей сообщил о 80 больных с опухолями грудной стенки из 1402 пациентов, у которых выявлены опухоли костей. C.C.M.L. сообщил о 16 больных с опухолями грудины, оперированных с 1964 по 1980 г., что составило I % по отношению к общему числу 12 868 операций.
Эмбриологические данные. Развитие грудины у человеческого эмбриона начинается на 6-й неделе с появления спереди двух лентовидных скоплений мезенхимальных клеток, которые в течение 8-й недели сходятся к средней линии, срастаются, начиная с головного конца, приобретая предхрящевое строение. В это же время от позвонков к грудине растут реберные хрящи. На 9-й неделе они достигают грудины, которая устанавливается по средней линии. На 10— 12-й неделе грудина вторично разделяется на ряд сегментов, но уже в горизонтальной плоскости. Эти участки, называемые sternebrae, имеют уже хрящевое строение и обычно один или два центра обызвествления. По мнению Б.М.Пэттен, эти центры окостенения сливаются между собой только с наступлением половой зрелости.
Однако следует помнить, что не всегда происходит сращение первичных закладок грудины по продольной оси, и тогда наблюдаются разной величины продольные дефекты грудины, сопровождающиеся изменениями кожи, органов средостения, бывает припаяна сердечная сорочка и т.д. Возможны также несращения закладок грудины, когда их делят в горизонтальной плоскости — sternebrae. В этих случаях развивается так называемая сегментированная грудина, что можно зафиксировать на уровне 1-го и 2-го сегмента, реже — III и IV тела грудины.
У людей с сегментированной грудиной иногда возникают упорные болевые ощущения, и, как показывают данные различных авторов, диагноз не всегда легко поставить [Patersons М., 1904; Hartmann W.H., 1938; Zimmer Е., 1938; Paul U., 1971].
Как показывают клинические наблюдения, опухолевое поле грудины никогда не возникает на основе лентовидных скоплений мезенхимальных клеток, из слияния которых и формируется грудина на всем ее протяжении.
Опухоли — чаще всего это хондросаркомы (более 85 % первичных опухолей грудины) — не развиваются одновременно в рукоятке и теле грудины, возникают на месте вторичных сегментов грудины, разделяющихся в горизонтальной плоскости (sternebrae) и имеющих хрящевое строение и центры оссификации. Таким образом, особенности эмбрионального развития грудины откладывают определенный отпечаток на формирование первичных опухолей грудины.
Злокачественные и доброкачественные опухоли, а также метастазы различной локализации рака, диспластические процессы поражают ребра, особенно часто при экзостозной дисплазии зон роста.
Больной должен быть квалифицированно обследован (клиническое, рентгенологическое, лабораторные и биохимические исследования, компьютерная томография, пункционная или трепанобиопсия). Данные морфологической верификации патологического процесса — необходимая составная часть диагностических процедур.
Нормальная функция грудной стенки играет большую роль в жизни человека. В некоторых работах указывается, что грудная стенка сравнительно редко поражается опухолями, но это далеко не так: ребра, мягкие ткани грудной стенки, включая молочную железу у женщин, грудина часто поражаются диспластическими опухолеподобными процессами, доброкачественными опухолями, первично-злокачественными опухолями и метастазами рака других органов. Особенно если к этому добавить, что грудная стенка иногда поражается опухолями, исходящими из легких и органов средостения.
Эти больные, как показали наши наблюдения, обращаются к хирургам, онкологам, травматологам-ортопедам. Поскольку очень важны правильный диагноз, адекватный объем оперативного вмешательства и полноценное пластическое закрытие дефекта грудной стенки, образовавшегося после операции, то становится ясным, что возникает много сложных вопросов при выборе метода лечения. Знакомство с литературой последних десятилетий свидетельствует о том, что наибольшее число работ опубликовано в журналах грудной и сердечно-сосудистой хирургии.
В 1878 г. Holden описал случай частичной резекции грудины по поводу саркомы. В 1881 г. Speicher собрал в литературе описание 28 больных с опухолями грудной стенки (лишь немногие из них были оперированы), а в 1898 г. F.W.Parham (Новый Орлеан) — 78 больных с опухолями костей при резекции грудной стенки: 26 больным была проведена экстраплевральная и 52 — интраплевральная резекция, в том числе было 2 собственных наблюдения.
По сообщению Hedblom, к 1910 г. были опубликованы данные о 188 больных с опухолями грудной стенки и грудины, из которых только незначительная часть была оперирована. Так, в клинике братьев Мейо наблюдали 25 больных, но ни один не был прооперирован. Иссечения опухолей грудной стенки, сопровождающиеся пневмотораксом, заставляли хирургов воздерживаться от проведения этих операций.
А.С.Токмаков в 1930 г. указал, что, по отчетам Пермской губернской больницы, с 1843 по 1921 г. не было выполнено ни одной операции по поводу опухоли грудной клетки. Это было время, когда сердце, легкие и мозг считались органами, которых не должен касаться нож хирурга.
Количество оперативных вмешательств было незначительным, поскольку хирурги часто не могли успешно бороться с опасными для жизни больного последствиями пневмоторакса и плевропульмонального шока.
О возникновении пневмоторакса в момент операции на грудной стенке написано большое число научных работ во всех странах. Ф.М.Плоткин, описавший в 1946 г. 4 больных, оперированных им по поводу злокачественных опухолей грудной клетки, основное внимание уделял плевропульмональному шоку и взглядам двух школ хирургов.
Хирурги французской хирургической школы (Pierre Bazy, Delageniere, Pierre Duval и др.) считали, что односторонний пневмоторакс не представляет опасности для жизни больного, а хирурги немецкой школы (Sauerbruch, Bauer) считали, что пневмоторакс опасен, — применяли аппараты, устраняющие разность давления.
Больных с опухолями грудной стенки оперировали многие отечественные хирурги: С.М.Федоров, Н.Н.Петров, Л.Г.Стуккей, Дерюжинский, К.Н.Черепнин (1926), В.Н.Перин (1930), Мельников, Брегадзе (1955), Т.А.Алиева (1958), Ярцев и Кадыров (I960) и др.
Появление интубационного наркоза устранило страх перед возникновением пневмоторакса во время операции, даже двустороннего. И действительно, последние 45 лет количество операций по поводу опухолей грудины и грудной стенки значительно возросло, однако осталась не менее важная проблема — создание каркасности грудной стенки на заключительном этапе операции.
Вопросам хирургического лечения опухолей грудной стенки были посвящены работы Н.И.Березинговского (1923), который оперировал 3 больных с опухолями ребер; Ф.М.Плоткина (1946). Гесс-де Кольва (1931) сообщил, что в русской литературе были опубликованы данные о 52 больных, из них с опухолями грудины — 9 больных, прооперировано 30 человек, 3 пациента умерли. З.И.Карташов (1949) описал больную, оперированную по поводу хондросаркомы грудины, — дефект был закрыт правой молочной железой. По данным отечественной литературы, на 816 опухолей грудной стенки было 35 опухолей грудины, т.е. не больше 5 %. D.C.Dahlin у 3987 больных с опухолями костей (клиника Мейо, стационарный и консультативный материал) наблюдал 26 больных с опухолью грудины: с доброкачественной гигантоклеточной опухолью (1) и со злокачественными (28): с миеломой (8), ретикулосаркомой (6), первичной хондросаркомой (7), остеогенной саркомой (6), саркомой Юинга (1 больной).
В период с 1964 по 1980 г. на 12 868 вмешательств было проведено только 16 операций по поводу опухоли грудины, т.е. приблизительно 0,01 %.
A.Ochsner и др. (1966) из Нового Орлеана сообщил о 134 больных с опухолями костей грудной клетки, из них 48 были доброкачественными, 36 — злокачественными и 50 — метастатическими. Авторы наблюдали 7 больных с поражением грудины: 3-е хондросаркомой, 1 — с болезнью Ходжкина, 1 — с эозинофильной гранулемой, 1-е метастазами рака молочной железы и 1 больного с поражением почки. В ключице чаще встречались метастатические опухоли (6 больных), гемангиомы (2), эозинофильные гранулемы (2), аневризмальная киста кости (1 больной). В том же году J.P.Dineen и R.S.Boltax сообщили о 17 больных с опухолями костей грудной клетки, наблюдавшихся за 12 лет. F.Alonso-Lei и F.A.de Linera (1971) произвели успешную операцию тотального удаления грудины по поводу громадных размеров хондромиксоидной фибромы (ее масса 4500 г), которая росла 9 лет и располагалась кнаружи от грудины. Замещение дефекта было выполнено акриловой резиной.
R.C.Marcow сначала проводит криохирургию, а затем хирургическое удаление больших опухолей грудной стенки; дефекты замещает пластинками из метилметакрилата либо танталовой сетки или marlex (изготовитель Devol Corporation, Cranston Rhode Island).
H.Masuda, H.Jamamoto (1973) описали 64-летнюю больную с метастазом рака щитовидной железы в грудину; сначала они резецировали тело грудины и через 9 мес — рукоятку; таким образом была полностью удалена грудина и осуществлена пластика аутокостью. Б.А.Берков (1959) дважды обвивает ребра лигатурой и потом их стягивает. A.G.Noediz, Stolf и др. (1976) для закрытия дефектов грудной стенки и диафрагмы применяют аллогенную твердую мозговую оболочку, консервированную в глицерине.
Вопрос о закрытии дефекта грудной стенки очень важен. При плохом замещении дефекта ткани грудной стенки совершают парадоксальные движения, что отрицательно отражается на функции органов грудной клетки, дыхании и кровообращении. Это хорошо известно хирургам, поэтому они избегали больших резекций грудной стенки и старались делать их как можно меньшими, что приводило к продолженному росту опухоли или рецидивам.
Ряд авторов высказывался против закрытия дефекта грудной стенки при помощи различных эндопротезов, потому что последние как инородные тела отторгаются и становятся подвижными при дыхании, в связи с чем их приходится удалять. Вот почему мы придаем большое значение методике пластики дефекта, которую мы разработали и рекомендуем, так как у нас не было ни одного случая неудачи. Однако нам известен случай, когда хирург воспользовался рекомендуемым нами эндопротезом из фторопласта, но закрепил его, не использовав нашу методику, эндопротез сместился и больной к концу суток умер.
Известны также случаи, когда к дефекту грудины подшивали перикард. В 1947 г. Griswald заместил дефект грудины танталовой пластинкой, Rebond в 1964 г. — нейлоновой тканью, Leroux в 1964 г. — акриловой резиной.
К.Н.Черепнин в 1926 г. описал больного, которому по поводу саркомы он резецировал рукоятку грудины вместе с прилежащими отделами ключиц. Дефект закрыт большими грудными мышцами, сухожилия которых были отсечены от плечевых костей и перемещены навстречу друг другу.
H.Brodin и K.Linden (1959) после удаления всей грудины заместили ее костным аутотрансплантатом, взятым из крыла подвздошной кости, фиксировав верхний отдел дефекта к ключицам и первым ребрам. Нижнюю часть дефекта они заместили лоскутами кожи, подшитыми к хрящевым отделам ребер, однако затем натяжение кожи уменьшилось и нижняя часть дефекта грудины была замещена, по их оценке, неудовлетворительно. Подобные сообщения принадлежат А.Е.Вапе (1963), который закрыл дефект marlex mesh.
Ph.Dartevelle, Ph.Levasseur, A.Pogas-Miranda и др. (1981) сообщили, что в Marie Lannelougne Surgical Clinic (1964—1980) наблюдали 16 больных с опухолями костей: у 1 — фиброзная дисплазия, у 5 — метастазы рака, у 10 — первичные опухоли, из них у 5 — хондромы и хондросаркомы, у 2 — остеогенная саркома, у 2 — плазмоцитомы и у 1 — болезнь Ходжкина. Прооперировано 10 больных, из них 3 умерли в послеоперационном периоде и еще 1 от множественных метастазов хондросаркомы. Хорошая реконструкция грудной стенки была достигнута с помощью marlex mesh, а затем metacrylate prosthesis.
По мнению многих хирургов, marlex mesh является более подходящим материалом. Рядом негативных свойств обладают эндопротезы из кости, нержавеющей стали, метилметакрилата и других материалов. Многие авторы использовали сетчатую ткань high density polyethylene produced as a monofilament mesh by the Phillips Petroleum Company, которая достаточно прочна на растяжение, чтобы удерживать грудную стенку в необходимом положении. Если она пришита с натяжением, то получается полуригидная структура, которая не фрагментируется и, имея крупные ячейки, хорошо прорастает фиброзной тканью. Она совершенно инертна и не вызывает нежелательной реакции ткани больного, устойчива к инфекции. Пришитая к краям дефекта, она не требует дополнительной наружной фиксации. Однако другие авторы поверх нее применяют протезы.
F.Alonso-Lei и F.A.de Linera (1971) из Испании пишут, что Graham и сотр. использовали marlex mesh с хорошим результатом. Этот материал из цельных полиэтиленовых нитей устойчив к инфекции, хорошо подшивается к краям дефекта, но он несовершенен, так как в послеоперационном периоде не избавляет больного от парадоксальных движений грудной клетки. В.Т. Le Roux (1964) из Эдинбурга применил акриловую резину, чтобы достичь ригидности грудной стенки. F.Paris, E.Blasco и др. (1980) описали 6 больных с опухолями грудины: 3 с хондросаркомами, 1 с плазмоцитомой и 2 с метастазами рака молочной железы. При тотальном удалении грудины они использовали силиконовую сетчатую ткань, на ребра накладывали 2 титановые пластинки и проводили пластику метилметакрилатовой пластинкой. P.R.Baffi, M.S.Didolkar, V.Bakamjian (1977) сообщили о больших реконструктивных операциях при опухолях грудины, ожогах мягких тканей после облучения или при использовании больших филатовских стеблей. О сложностях диагностики писал J.Pirschel (1981).
K.Kawamura (1974) считал, что большими материалами располагали Bisgard и Vieta. По данным G.Spay, P.Toure (1976), они удалили гигантскую хондросаркому массой 5 кг, которая росла кнаружи и имела ножку. Размер резецированного участка грудины был небольшим, он был закрыт протезом из силикона.
C.Newton-Peabody (1971) резецировал тело грудины по поводу хондросаркомы, заместив ее marlex mesh и мышечно-фасциальными лоскутами, а P.G.Arnold, P.C.Pairolero (1978) — рукоятку грудины по поводу хондросаркомы, заместив ее левым ребром и левой большой грудной мышцей, отсеченной от плечевой кости.
H.Eschapasse, A.Bonafe, H.Taobane, A.Brut, C.Manelfe, описавшие в 1972 и 1977 гг. свой опыт удаления опухолей грудины и использования для восстановления грудной стенки протеза из акриловой резины, в 1981 г. пишут о целесообразности эмболизации через наружные и внутренние грудные артерии с обеих сторон опухолевых сосудов перед удалением гиперваскулязованных опухолей — метастазов рака щитовидной железы, гипернефромы, когда нередко ощущается пульсация опухоли. Они предостерегают от применения эмболизации без тщательно разработанной схемы и методики, поскольку известны случаи тяжелых неврологических расстройств (нижних парапарезов и параплегии), если эмболизацию и даже ангиографию проводят на уровне D4—D8 позвонков.
С.Т.Зацепин
Костная патология взрослых
Читайте также:



