Заживление костной ткани вокруг имплантата называется
-
Вход Регистрация
- Главная →
- Новости и статьи по стоматологии →
- Имплантология →
- Остеоконденсация: биологическое обоснование и клиническое применение
Остеоциты и мезенхимальные клетки кости (МКК) играют ключевую роль в процессе костного ремоделирования. По своей функции остеоциты являются клетками, которые являются чувствительными к механическим стимулам, и которые принимают участие в формировании костной ткани наряду с остеобластами и остеокластами. При этом остеобласты развиваются из мезенхимальных клеток и отвечают за синтез костного матрикса, а остеокласты дифференцируют из многоядерных клеток моноцитарно-макрофагальной линии. Мезенхимальные, или как еще их называют выстилающие клетки костной ткани отвечают за формирование костной ткани на новых костных поверхностях, и характеризуются плоскостной внешней архитектурой.

Нагрузка и резорбция костной ткани
Ремоделирование кости вокруг дентальных имплантатов
После установки дентальных имплантатов вскоре вокруг них начинает развиваться имунно-воспалительная реакция, предусматривающая реализацию ангиогенных и остеогенных процессов. Элементы данной реакции зависят от характеристик поверхности самого имплантатов (топографии, химической составляющей и структуры материала), которые могут способствовать или же ингибировать адсорбцию соответствующих белков. Тромбин и фибриноген, адсорбируясь на поверхности внутрикостной опоры, играют ключевую роль в достижении гомеостаза периимплантатной области, после чего выделение соответствующих цитокинов и факторов роста стимулирует депозицию коллагенового матрикса вокруг слоя титана оксида, находящегося на поверхности винта. Все это в конце концов приводит к формированию новой костной ткани (обычно происходит на протяжении 5 дней). В течение 8-12 недель пластинчатая кость инициирует развитие такого феномена как биологическая стабильность, что также именуется остеоинтеграцией.
Впоследствии, как и в случае естественного зубного ряда, имплантаты подвергаются ремоделированию мягких и твердых тканей с формированием параметра биологической ширины на уровне 3,5 мм. Многие исследования при этом указывают на то, что наличие микрозазора между двумя компонентами имплантологической системы провоцирует более выраженную потерю костной ткани. Интерфейс соединения между абатментом и имплантатом характеризуется наличием микропространства в диапазоне от 10 до 50 микрон, что приводит к развитию эффекта помпы. Под действием последнего интерфейс соединения контаминируется жидкостью полости рта, содержащей как грамположительные, так и грамотрицательные бактерии. Именно из-за этого внутреннее соединение в структуре имплантологической системы является более предпочтительным, чем внешнее. Кроме того, особый интерес представляет собой принцип переключения платформ, который позволяет корригировать параметры биологической ширины.
Значительное количество исследований было посвящено аспектам оптимизации дизайна имплантата для улучшения его стабильности и/или качества остеоинтеграции, а также для минимизации уровня потери маргинальной костной ткани. Однако при этом совсем мало внимания уделялось возможностям оптимизации самой области имплантации в процессе выполнения остеотомии. В данной статье мы рассмотрим аспекты влияния исходной плотности костной ткани на первичную стабильность имплантата, а также хирургические концепции приема остеоконденсации как метода, позволяющего улучшить первичную стабильность имплантата путем уплотнения доступной аутогенной костной ткани.
Влияние исходного качества кости на параметры остеоинтеграции и торка имплантата
Таким образом, можно резюмировать, что дефицит первичной стабильности имплантата в целом может компрометировать процесс остеоинтеграции, однако слишком высокие показатели ТИ негативно влияют на поддержку необходимого уровня периимплантатной костной ткани. Не менее важным фактором, который влияет на исход установки имплантата, является исходная плотность альвеолярной кости и ее связь с показателями первичной стабильности. В своих ранних работах Misch классифицировал все возможные варианты альвеолярного костного гребня на 4 типа. Согласно этой классификации, более плотная костная ткань локализируется в переднем участке нижней челюсти, в то время как наиболее пористая – в дистальных участках верхней челюсти. Логично, что чем больший слой кортикальной кости, тем более сильную поддержку имплантата она обеспечивает, что, в свою очередь, позволяет достичь более высоких показателей первичной стабильности. Однако, кортикальная составляющая кости также характеризуется и меньшим уровнем васкуляризации, что, в свою очередь, снижает ее ангиогенный потенциал и снижает возможности для миграции остеогенных клеток в область имплантации. В конечном счете, все это может привести к более выраженной потере уровня костной ткани в периимплантатной области.
Simons и соавторы провели исследование, в котором изучили влияние исходного соотношения кортикальной и губчатой костной ткани на характер потери кости в периимплантатной области. Они обнаружили, что при наличии 50-60% губчатой кости удаётся минимизировать раннюю редукцию уровня периимплантатного костного гребня до 0,6-0,7 мм, в то же время превалирование кортикальной кости в области имплантации провоцирует убыль уровня окружающего костного гребня до 1,5 мм. По этой причине при выраженно толстом слое кортикальной кости исходные параметры ТИ все же лучше минимизировать. Также для того, чтобы свести показатели редукции костного гребня к минимальным, авторы рекомендуют проводить конденсацию участка остеотомии при наличии толстой кортикальной пластинки, таким образом, обеспечивая редукцию исходных параметров торка.
Таким образом, можно резюмировать, что кортикальная кость характеризуется наличием определенных недостатков по сравнению с трабекулярной, что выражается в ограниченном кровоснабжении и сниженном количестве присутствующих остеопрогениторных клеток. Кроме того, кортикальная кость также характеризуется повышенной чувствительностью к высоким напряжениям, иными словами – она является более механически чувствительной. Исходя из этого, становиться понятным почему апоптоз остеоцитов более часто регистрируется именно в области кортикального слоя в случаях микроразрушений кости и действия на нее высоких функциональных напряжений. Понимая влияние данных факторов, врач должен учитывать исходное состояние качества костной ткани в области остеотомии, для того чтобы обеспечить профилактику потенциально возможных имплантат-ассоциированных осложнений.
Немедленная имплантация с достижением высоких и низких показателей торка
Ряд клинических исследований долгое время изучали гипотезу о том, что более высокие показатели первичной стабильности ассоциированы с лучшими параметрами остеоинтеграции. В случаях немедленной имплантации достижение высоких параметров торка, превышающих 32 Нсм, является обязательным. При этом показатели торка, превышающие 50 Нсм при немедленной установке имплантатов, провоцировали более выраженную потерю костного гребня, особенно с вестибулярной стороны, а также развитие рецессий в области имплантации. При экстремально высоком торке (более 70 Нсм) потеря окружающей костной ткани была клинически выраженной и часто негативно влияла на конечный исход реабилитации. С другой стороны, слишком низкие показатели торка также были связаны с повышением частоты неудач после установки внутрикостных титановых опор. Таким образом, полученные результаты указывают на наличие прямой связи между исходными показателями торка и уровнем потери периимплантатной костной ткани.
Процедура конденсации костной ткани с помощью остеотомической техники, позволяющая улучшить первичную стабильность имплантатов и костное заживление в области вмешательства, была впервые описана Summers уже около 20 лет назад. Büchter и Stavropoulos, однако, отметили, что к данной технике следует относится с огромной осторожностью, поскольку данный подход при неадекватном использовании может привести к развитию микропереломов в структуре костной ткани, окружающей имплантат. На протяжении многих лет исследователи старались сгруппировать все возможные варианты реализации техники остеоконденсации в определенные практические рекомендации. Так, например, появилась концепция установки имплантата более широкого диаметра, чем последнее используемое остеотомическое сверло, что позволяет повысить исходные показатели торка. В подобных случаях врачам удаётся добиться адекватной вторичной стабильности и плотного контакта имплантата с окружающей костью, хотя сам процесс заживления кости происходил более медленно, учитывая развитие очагов микронекроза. Другие исследователи показали, что установка имплантатов с торком равным 0, позволяет добиться таких же успешных отдаленных результатов через 4 месяца, как и при установке имплантатов с торком в 30 Нсм или 70 Нсм. Учитывая разнообразность, полученных в ходе разных исследований данных, можно только резюмировать, что роль высоких показателей ТИ на уровень резорбции костной ткани в периимплантатной области остается не до конца изученной.
Остеоконденсация
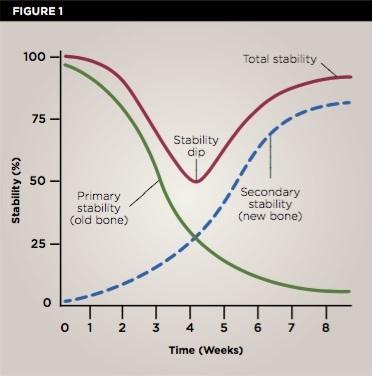
Биомеханическая стабильность имплантатов обычно зависит от нескольких факторов. Во-первых, от макро- и микродизайна самих интраоссальных конструкций, а также от качества и количества костной ткани в области вмешательства – все эти факторы непосредственно влияют на первичную стабильность имплантатов (фото 1).
Фото 1. Классическая диаграмма графиков стабильности имплантатов. Самые высокие показатели первичной стабильности регистрируются на первой неделе после установки имплантатов, далее на 4 неделе отмечается снижение стабильности, после чего начинает развиваться механизм вторичной стабильности. Многие клиницисты стараются оптимизировать показатели стабильности в особенно критический период 4 недель за счет модификации протоколов установки имплантатов, их поверхностей, изменения макро- и микродизайна.
Протоколы, направленные на повышение параметров первичной стабильности имплантатов, предусматривают возможную реализацию следующих принципов:
Костная ткань человека характеризуется способностью поглощать энергию, то есть она является гибкой, но при этом она также может изменять свою форму в процессе деформации без сколов или переломов. Также кость может противостоять компрессии, несколько расширяясь под ее действием и удлиняясь во время напряжения.
Фото 2. В определенных случаях процедура классической остеотомии может привести к потере костной ткани в периимплантатной области, что чревато дальнейшим обнажением витков интраоссальной опоры.
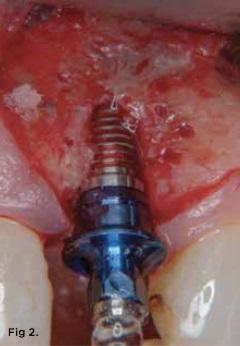
Фото 3. В определенных случаях процедура классической остеотомии может привести к потере костной ткани в периимплантатной области, что чревато дальнейшим обнажением витков интраоссальной опоры.
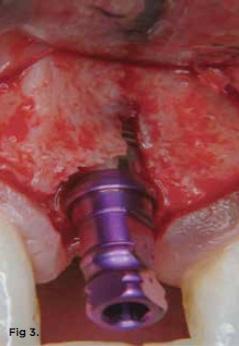
Фото 4. В определенных случаях процедура классической остеотомии может привести к потере костной ткани в периимплантатной области, что чревато дальнейшим обнажением витков интраоссальной опоры.
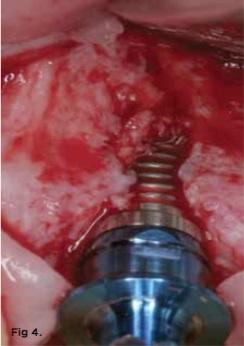
Сверла для остеоконденсации также оснащены датчиком реального времени, который показывает, стоит ли хирургу увеличить или ослабить усилие в зависимости от исходной плотности костной ткани. Ввиду своего движения против часовой стрелки, боры для остеоконденсации не режут, а наоборот – уплотняют кость со скоростью движения 800-1200 оборотов в минуту (фото 5). Логично, что для того, чтобы не перегреть кость, врач должен обеспечить надлежащий уровень ирригации. Движения боров против часовой стрелки индуцируют развитие компрессионных волн во внешнем направлении, а поскольку бор окружен костной тканью – то именно в ее структуре. Это и называется уплотнение аутографта, или остеоконденсация. Грубо говоря, ошурки костной ткани перераспределяются по канавкам бора и вдавливаются в трабекулярные стенки имплантологического ложа. Таким образом повышается плотность костной ткани в периферических участках остеотомии.
Фото 5. Бор для проведения остеоконденсации, который, в отличие от классических сверл, не режет костную ткань, но уплотняет ее во внешнем направлении. Данные инструменты позволяют провести пластическую деформацию костной ткани, не провоцируя ее экскавацию.

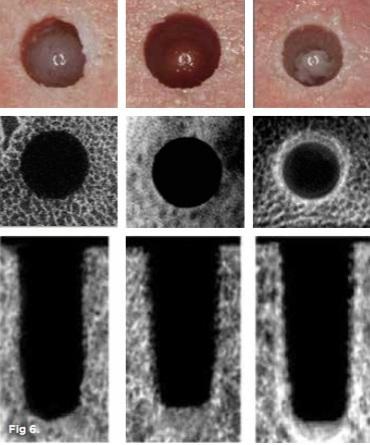
Trisi и коллеги, изучая методики остеоконденсации на животных моделях, установили, что последняя позволяет добиться повышения параметров контакта имплантата с окружающей костью даже при установке титановых опор в участки с низким качеством кости. Таким образом, по мнению авторов, удается повысить стабильность имплантатов, снижая параметры их микродвижений. Huwais и Meyer также сообщили, что уплотнение аутографта в периферических участках остеотомии позволяет добиться лучшей первичной стабильности имплантата (фото 6). При этом авторы указали на то, что для реализации данного подхода требуется наличие достаточного объема костной ткани определённого исходного уровня плотности (фото 6).
Фото 6. Результаты доклинических исследований. В верхнем ряду: вид участков стандартной остеотомии, экстракционного препарирования и остеоконденсации. В нижнем ряду: результаты микрокомпьютерной томографии, на которых можно увидеть, как отличается качество костной ткани по периферии имплантологического ложа во всех трех случаях.
При этом исследователям не удалось зарегистрировать каких-то значительных повышений в температуре при реализации остеокондесанции, которые могли бы спровоцировать ятрогенную травму костной ткани. Наоборот, полученные результаты свидетельствуют об оптимизации процесса костного заживления за счет наличия своей же кости по периферии остеотомии, но только лучшего качества.
Таким образом, предварительно проведенные исследования на животных позволили резюмировать несколько ключевых моментов остеоконденсации. Данная процедура позволяет увеличить минеральную плотность костной ткани в периферических участках остеотомии, таким образом, повышая первичную стабильность имплантатов и параметры их торка при установке. С точки зрения клинической безопасности, манипуляция остеоконденсации также приемлема в качестве процедуры классической остеотомии при условии адекватного контроля скорости сверла и обеспечения надлежащей ирригации. Уплотнение имплантационного ложа позволяет распределить имеющуюся костную ткань во всех направлениях с повышением параметров ее качества на всю глубину, особенно в области дна лунки. Все это повышает качество контакта костной ткани с поверхностью имплантата в среднем в три раза по сравнению с обычной процедурой препарирования области вмешательства.
Выводы
Остеоконденсация позволяет сохранить необходимый объем костной ткани за счет двух подходов: посредством компрессии губчатой кости в ходе ее вязкоупругой и пластической деформации, а также за счет уплотнения частиц аутографта по всей длине и глубине остеотомии. Разные подходы к конденсации аутотрансплантата используются врачами на протяжении уже более 20 лет в разных отраслях медицины (например, в ортопедической хирургии для улучшения стабильности протеза при замене тазобедренного сустава). Концепция остеоконденсации отличается от принципов классической остеотомии тем, что она не предполагает удаления кости, а наоборот обеспечивает улучшение параметров качества кости за счет ее перераспределения по периферии имплантологического ложа.
Авторы: Michael A. Pikos, DDS; and Richard J. Miron, DDS, PhD
Костная ткань постоянно ремоделируется, что означает, что кость постоянно саморазрушается и самовосстанавливается; следовательно, поверхность имплантата должна иметь определенную топографию, содержащую поры и комплексные 3D характеристики, чтобы обеспечить спайку кости с поверхностью имплантата [2]. Это обеспечивает интеграцию имплантата с костью.
Ниже приводится краткое описание процесса заживления пери-имплантатной кости:
Для достижения надлежащего заживления, имплантат должен быть надежно прикреплен к принимающей кости, обеспечивая формирование костной ткани и не должен быть слишком подвижным [4,5]. Так же, как и в случае перелома, когда подвижность сломанной кости может замедлить процесс заживления 8, оссео-интеграция ингибируется, если имплантат должным образом не закреплен на кости [9]. Должен быть соблюден тонкий баланс при размещении имплантата, поскольку, для правильного формирования кости после имплантации, наличие определенного пространства между имплантатом и принимающей костью является все же необходимым [10,11].
Процесс имплантации начинается с хирургической процедуры, которая приводит к кровотечению из мягких тканей, окружающих кость, и образованию гематомы. Контакт крови и стороннего предмета – имплантата – влечет за собой множество биологических процессов, таких как воспаление, коагуляция и формирование тканей, которые подвержены влиянию химического состава и топографии поверхности имплантата [12]. В рамках данного процесса образуется монослой белков, таких как фибронектин и витронектин, которые способны прикрепляться к поверхности имплантата и взаимодействовать с ней, если топография и химический состав имплантата способствуют этому [13,14]. Данное взаимодействие между имплантатом и белком формирует основу для оссео-интеграции и оссификации (формированию костной массы), и имеет решающее значение для правильного заживления раны и, в конечном счете, успешной имплантации.
Первым шагом на пути к заживлению является коагуляция (свёртывание) крови в области вокруг имплантата, которая контролируется тромбоцитами [15]. Тромбоциты это маленькие клетки, которые активируются при появлении посторонних объектов, повреждении тканей или при получении сигналов от других клеток. При активации тромбоциты секретируют различные молекулы, которые взаимодействуют с факторами коагуляции и начинают процесс коагуляции [16] и ускоряют адгезию рецепторов, которые препятствуют взаимодействую тромбоцитов с имплантатом [17]. Результатом этого процесса является формирование тромба [18], который способствует созданию условий для остеокондукции (прироста костных клеток) [19]. Множество цитокинов, факторов роста и хемоаттрактантов, содержащихся в тромбе, стимулирует клеточную миграцию и адгезию 20.
Топография поверхности, как было упомянуто ранее, является одним из ключевых факторов успеха на начальной стадии формирования кости после имплантации. Исследования показали, что шероховатые поверхности имплантатов с нано- и микро-топографией способствуют большему уровню активации клеток, чем гладкие поверхности [23]. Принимая во внимание важность образования сгустка как для миграции клеток к месту имплантации и, так и для воспалительного и коагуляционного процессов, легко понять, почему топография и химия поверхности и химия имеют большое влияние на успех лечения[24,25].
Воспалительная реакция начинается непосредственно сразу после активации тромбоцитов и начала процесса коагуляции [16]. Приток иммунных клеток к области трансплантации способствует высвобождению цитокинов [26]. Цитокины стимулируют воспаление, и вносят свой вклад в формирование костной массы, способствуя притоку или созреванию костных клеток [27]. Наряду с цитокинами, секретируется семейство других факторов, называемых факторами роста ткани β (TGF-β); эти факторы способствуют формированию новой костной ткани, заживлению трещин и ран имплантации 31.
Костные клетки, как и все клетки в организме, нуждаются в постоянном притоке крови; следовательно, ангиогенез (формирование новых кровеносных сосудов) имеет решающее значение для процесса имплантации, секреция ангиогенных факторов, таких как VEGF, стимулирует рост новых кровеносных сосудов 34.
Результатом воспалительного и ангиогенного процессов является приток и активация костных клеток, тем самым создаются условия для формирования новой костной массы в области имплантации.
Сигнальные микромолекулы, секретируемые в области образовавшейся раны, способствуют притоку мезенхимальных клеток, которые дифференцируются в строительные костные клетки (остеобласты) и начинают секретировать матрикс [37,38]. Матрикс служит в качестве цемента и создает условия для минерализации 39,что способствует формированию слоя кальцификации на поверхности имплантата. Этот слой растет и расширяется, и обеспечивает формирование новых костных тканей в зоне вокруг имплантата и окружающих мягких тканей [42]. Растущая кость также обеспечивает дополнительную поддержку для имплантата [43]. После заживления раны первичный костный слой, сформировавшийся на поверхности имплантата, отмирает и абсорбируется, и имплантат фиксируется путем спайки зрелой кости и поверхности имплантата. В случае если поверхность имплантата обладает многомерной сложной топографией, интеграция кости с поверхностью протекает легче, в отличие от гладких поверхностей, где кость просто растет вокруг имплантата [44]. В случае успешного лечения, процесс формирования кости заканчивается прочной фиксацией имплантата на принимающей кости.
Подводя итог, имплантация запускает ряд процессов, начиная с образования гематомы, секреции различных факторов, активации тромбоцитов и образования тромба. После чего начинается приток иммунных клеток, которые индуцируют воспалительные процесс. В дальнейшем запускается процесс ангиогенеза, кровеносные сосуды формируются в области имплантации, костные клетки созревают и начинают строительство новой костной ткани. В результате чего формируется первичный костный слой на поверхности имплантата, который впоследствии заменяется зрелой костной тканью. После успешного завершения этого процесса имплантат надежно зафиксирован на принимающей кости и функционирует как ее естественное продолжение.

Достаточно часто в ходе подготовки к имплантации зубов пациенты встречаются с распространенной проблемой – это недостачное количество костной ткани или ее атрофия. В такой ситуации требуется искать другие методы решения проблемы, или же врач назначает процедуру по наращиванию костной ткани.
Как это происходит, каковы отзывы о процедуре и особенности, вы и узнаете ниже.
Что делать при малом объеме костной ткани?
Если сокращается объем ткани на верхней челюсти, то при имплантации зубов есть высокий риск повреждения гайморовой пазухи. Импланты по длине превышают кость, все это может увеличить риск разрыва гайморовой пазухи и происходит ее инфицирование. Вследствие чего появляется хронический насморк или гайморит.
Проблемы с верхней челюстью могут решаться таким образом:
- проводится имплантация зубов без наращивания ткани;
- выполняется операция по синус-лифтингу;
- при атрофии костной ткани нижней челюсти врач часто сталкивается с тем, что нижнечелюстной нерв расположен слишком близко, а его повреждение может привести к потере языковой чувствительности целиком или полностью, нижней части лица и проблемам с произношением или глотанием.
А чтобы выполнить наращивание костной ткани нижней челюсти, делается следующее:
- в передний отдел челюсти вживляют имплант, но это наращивание возможно только при присутствии полной челюстной адентии и используется с целью фиксации протеза;
- имплант устанавливается по соседству с нервом;
- меняется положение нерва;
- выполняется имплантация зубов с наращиваем ткани на нижней челюсти.
Назначение костной пластики

Чтобы вживить титановую конструкцию, ткань должна иметь достаточную ширину и высоту. Именно от этого зависит устойчивость положения импланта и длительность его использования.
Если пациент решил выполнять имплантацию зубов без необходимости наращивания кости, то здесь обязательным условием является то, что ткань по высоте должна составлять максимум миллиметров в высоту.
Показанием к процедуре наращивания кости является небольшое количество ткани. При этом недостаточность в каждом отдельном случае просчитывается индивидуально. Например:
- если проводится имплантация в переднем челюстном отделе и планируется последующая фиксация съемных протезов, то проведение костной пластики не требуется;
- при необходимости проведения несъемного протезирования, а костной ткани при этом недостаточно, то в данном случае требуется наращивание костей.
Данная пластика – это необходимая мера еще и по причине того, что некомпенсированная костная атрофия приводит к таким последствиям:
- патологическое смещение зубов, которое может привести к их шатанию и выпадению;
- мимика, артикуляция и речь искажаются;
- нарушается функция жевания, что провоцирует проблемы с пищеварительными органами;
- контур лица искажаются, появляются морщины и западают губы.
Поэтому костная пластика при атрофических изменениях костной ткани – это жизненная необходимость.
Методы наращивания костной ткани
Благодаря современным технологиям по восстановлению костной ткани можно проводить имплантацию на любом участке кости независимо от того, в каком она состоянии. Сейчас есть такие методы наращивания, как:
- костная регенерация;
- пластика;
- синус-лифтинг;
- пересадка костных блоков.
Костная регенерация направленного типа

При проведении данной процедуры выполняется подсадка костной ткани в виде мембраны, имеющую высокую степень бисовместимости и помогает образовать костную ткань. Мембрану делают на основе коллагенового волокна, она может рассасываться и не рассасываться. А после того как мембрана вживляется, раненую поверхность зашивают. И только после образования костной ткани, проводится имплантация.
После того как удаляется зуб, на его месте остается большая лунка. А когда ставят имплант, с целью его лучшего закрепления в костной ткани, иногда врачи используют костную ткань.
Костная пластика и ее применение
А вот костная пластика практикуется несколько реже. Кость наращивается посредством трансплантата следующим образом:
- костная ткань подсаживается, ее берут с области нижней челюсти (в районе подбородка) или верхней за зубами мудрости;
- фрагмент костной ткани после вживления фиксируют с помощью титановых винтов;
- примерно через полгода винты убирают и проводится процедура по имплантации.
- Сама процедура проводится таким образом:
- десна разрезается;
- специальными инструментами костная ткань расщепляется и раздвигается;
- в полученную полость погружают остеопластический материал;
- трансплантат фиксируют с помощью титановых винтов;
- промежуточные дефекты заполняют костнопластической крошкой;
- накладывается мембрана, а десна ушивается.
Что такое синус-лифтинг?
Это понятие подразумевает увеличение объема, поднимая при этом гайморову пазуху. Такая методика наращивания ткани зубов используется в таких случаях:
![]()
при отсутствии патологических явлений в месте выполнения процедуры;- если кость присутствует в объеме, который соответствует требованиям для проведения процедуры, которая нужна с целью первоначальной фиксации внутрикостных имплантатов;
- когда нет риска осложнений при оперативном вмешательстве.
- Данную операцию не назначают тогда, когда у пациента есть как минимум одно противопоказание. В их числе такие;
- большое количество перегородок в гайморовых пазухах;
- хронический насморк;
- синусит;
- полип;
- плохое состояние костной ткани;
- если в анамнезе присутствует операция на гайморовы пазухи;
- если пациент много курит.
Синус-лифтинг подразделяется на открытый и закрытый.
Операция открытого типа достаточно сложная, и ее назначают при сильной недостаточности костной ткани по бокам верхних челюстей. Она выполняется так:
- проделывается маленькое отверстие снаружи стенки пазухи, чтобы не была задета слизистая оболочка;
- слизистую оболочку приподнимают на требуемую высоту;
- полученное свободное пространство заполняется специальным материалом для наращивания;
- частично ткань и слизистая оболочка, отслоенная до этого, возвращается обратно и зашивается.
Спустя некоторое время формируется нужный объем кости, затем выполняется имплантация.
Такая операция используется при имплантации, когда не бывает достаточно всего 1-2 мм костной ткани по высоте. Она включает такие этапы:
![]()
препарируется костное ложе для имплантата – по длине формируют отверстие, до гайморовой пазухи не доходит около 1-2 мм;- с помощью инструментов посредством легкого простукивания выполняется смещение оставшегося костного фрагмента вглубь пазухи, таким образом вверх поднимается надкостнично-слизистый лоскут;
- через полученное отверстие вглубь ложа вводится материал, потом устанавливается и сам имплантат.
Преимущества такого способа наращивания таковы:
- можно восстановить объем ткани;
- с помощью закрытого типа операции можно нарастить костную ткань с минимум травм;
- можно получить новые зубы, которые полноценно заменяют настоящие.
Но если операция была проведена неудачно, то, согласно отзывам, могут встречаться такие последствия:
- носовая пазуха повреждается, это в будущем провоцирует появление хронического насморка;
- конструкция западает вглубь гайморовой пазухи, поэтому ее потребуется удалить;
- может развиться воспаление в пазухе.
А период после операции и реабилитация больного может проходить очень долго. Пациенту в течение определенного времени нужно будет соблюдать ряд требований, например, не кашлять и не чихать, поэтому имплантат или искусственная кость могут выпасть.
После проведения операции не рекомендуется:
- есть твердое, горячее или холодное;
- ходить в сауну или баню;
- выполнять тяжелые физические нагрузки;
- нырять;
- пить жидкость через трубочку;
- пользоваться авиатранспортом.
Что используют при наращивании
Чтобы восстановить утраченный объем костной ткани применяют специальный трансплантат. С этой целью применяются такие материалы:
![]()
аутотрансплантат (ткань самого пациента) – у него берется участок ткани из челюстного подбородочного участка, челюстные выросты, бугры ребра, верхней челюсти или подвздошной кости. Настоящая кость приживается быстрее и успешнее всего;- аллотрансплантат (донорская ткань) – донором при наращивании выступает другой человек, чаще всего недавно умерший. Перед тем как установить материал, кость обрабатывают, чтобы не допустить осложнения. Заживление происходит медленно, поскольку отсутствуют жизнеспособные клетки;
- ксенотрансплантат –применяется ткань животного. Она более доступная, нежели человеческая. Замещение материала и рассасывание костной тканью происходит крайне медленно;
- аллопласт – искусственный материал, например, гидрооксиаппатит и его производные материалы (биокерамика и другое).
Отзывы о процедуре
А сейчас давайте прочтем отзывы реальных пациентов о том, как у них при имплантации зубов проходила процедура наращивания кости.
Решила установить на нижнюю челюсть два импланта. Костной ткани практически нет, поскольку настоящие зубы я давно потеряла, ведь мне уже за 60. Перед имплантацией зубов врач мне предложил пересадить костные блоки. После процедуры остались отеки и синяки, они ушли примерно через неделю. Дискомфорта особого не ощущалось. Имплантаты вместо зубов после приживления кости мне поставили примерно через 2 месяца. А еще через время сделали протезирование с применением временных коронок на зубы.
Я недавно рожала и после родов потеряла два зуба, которые находились на нижней челюсти. Проведенная томография показала, что мой объем костной ткани не позволит врачам поставить мне искусственные зубы нужного размера. Если они по диаметру слишком малы, то нужна остеопластика. Иногда при этом одновременно требуется вживление имплантатов. После процедуры какое-то время было неприятно, были отеки и синюшность в нижней челюсти. Импланты на месте зубов прижились через пару месяцев, врач поставил формирователь десен. Совсем скоро слепки сняли и поставили коронки.
Нужно было поставить искусственные зубы и пришлось обращаться к врачу. Там выяснилось, что я нуждаюсь в костной пластике. На верхней челюсти делается синус-лифтинг, а на нижней наращивается кость. Дискомфорт продолжался примерно 10 дней после выполнения процедуры, были отеки и синяки на лице, я пила таблетки против болей. Но уже после установки имплантатов и протезирования все утряслось.
Далеко не во всех случаях можно просто поставить имплантаты вместо потерянных зубов. Если есть проблемы, то требуется предварительно нарастить костную ткань. Как происходит эта операция, мы и рассказали в этом материале.
Читайте также:





