Замещение мышечной ткани хрящевой
Группа соединительных тканей объединяет собственно соединительные ткани (РВСТ и ПВСТ), соединительные ткани со специальными свойствами (ретикулярная, жировая, слизистая, пигментная), скелетные соединительные ткани (хрящевая и костная). Также к соединительным тканям относится жидкая подвижная кровь, строение которой мы изучим в разделе "Кровеносная система".
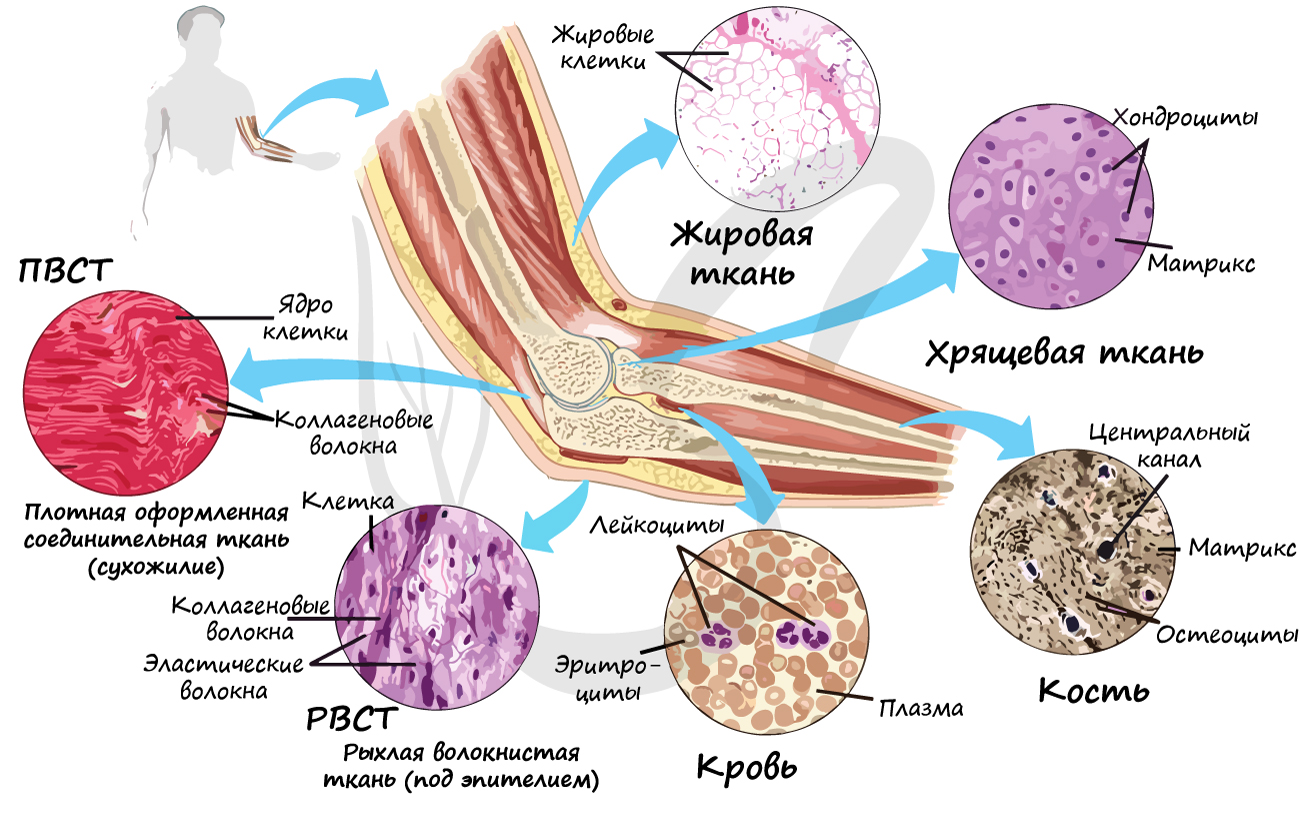
Что же общего между жидкой подвижной кровью и плотной неподвижной костью? Общим оказываются два основополагающих признака соединительных тканей:
- Хорошо развито межклеточное вещество
- Наличие разнообразных клеток
Рыхлая волокнистая соединительная ткань (РВСТ) содержит клетки разной формы: фибробласты (юные), фиброциты (зрелые). РВСТ содержится во всех внутренних органах, она располагается по ходу прохождения кровеносных, лимфатических сосудов и нервов, образует соединительнотканные прослойки.
Обратите внимание на название клеток: фибробласты, фиброциты - эти слова происходят от (лат. fibra — волокно). В соединительных тканях имеются три основных типа волокон:
- Коллагеновые - обеспечивают механическую прочность
- Эластические - обуславливают гибкость тканей
- Ретикулярные - образуют ретикулярные сети, служащие основой многих органов (печень, костный мозг)

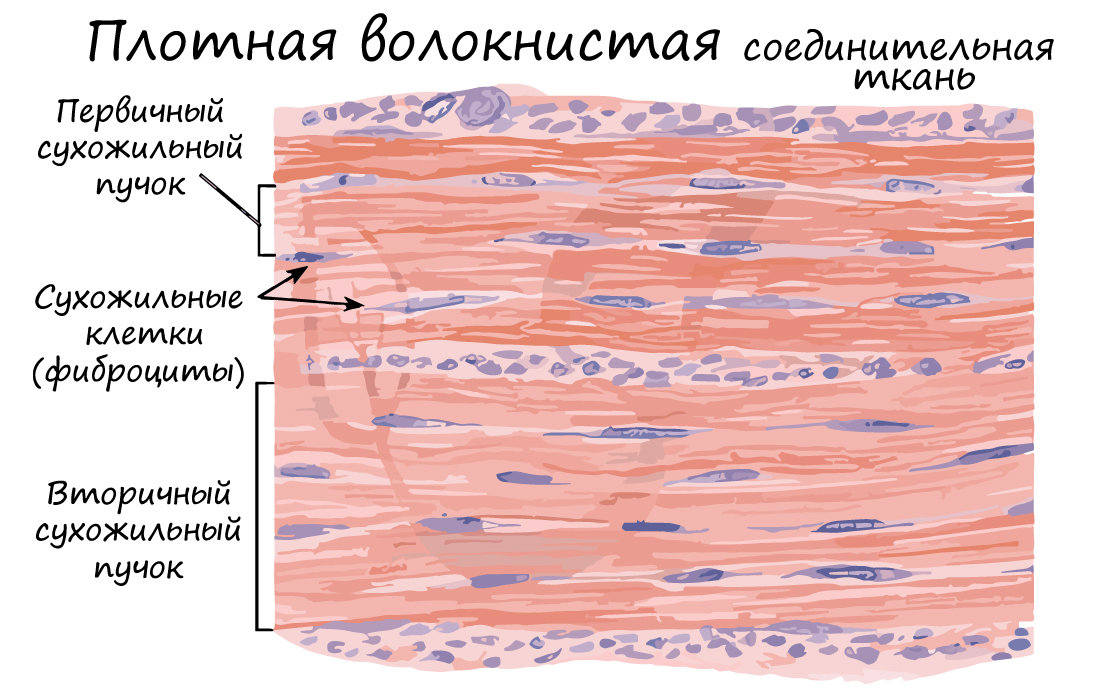
Плотная волокнистая соединительная ткань (ПВСТ) отличается преобладанием волокон над клетками. ПВСТ участвует в образовании сухожилий, связок, формирует оболочки внутренних органов.
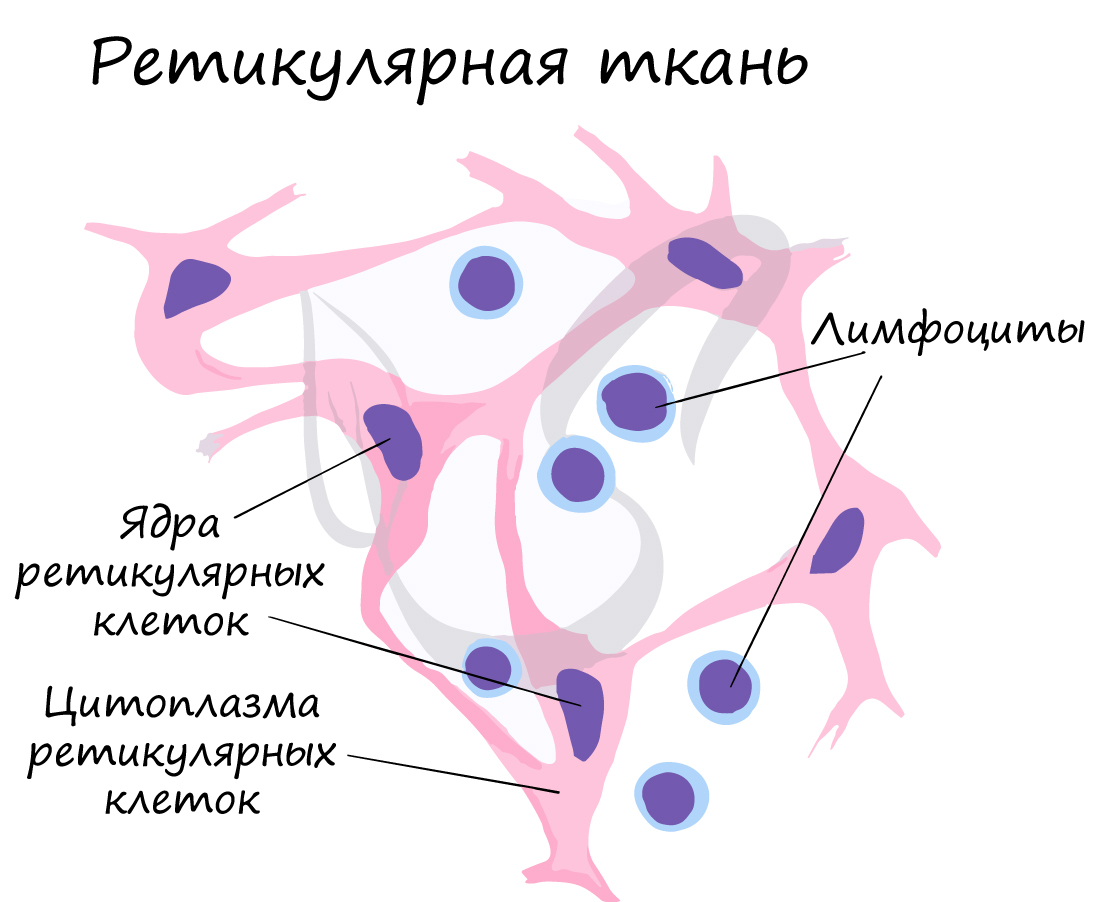
Ретикулярная ткань (от лат. reticulum - сетка) образует строму (опорную структуру) кроветворных и иммунных органов. Здесь зарождаются все клетки кровеносной и иммунной систем.
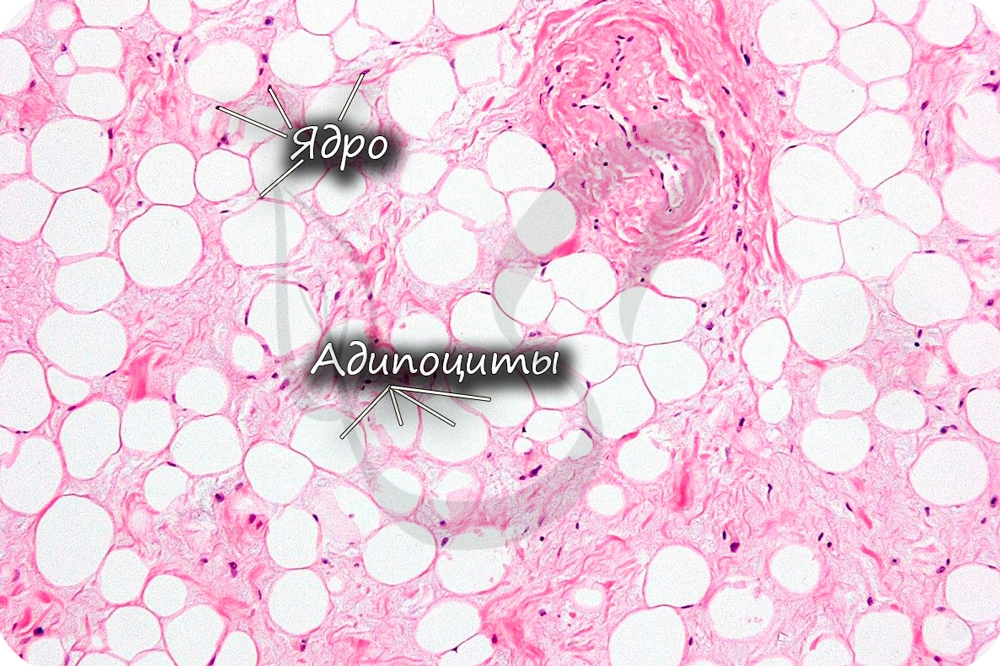
Жировая ткань состоит из скопления жировых клеток (адипоцитов). Создает резерв питательных веществ, образует подкожный жировой слой и капсулу почек. Кроме того, жировая ткань выполняет защитную (механическую) функцию, предупреждая повреждения внутренних органов, и участвует в терморегуляции.
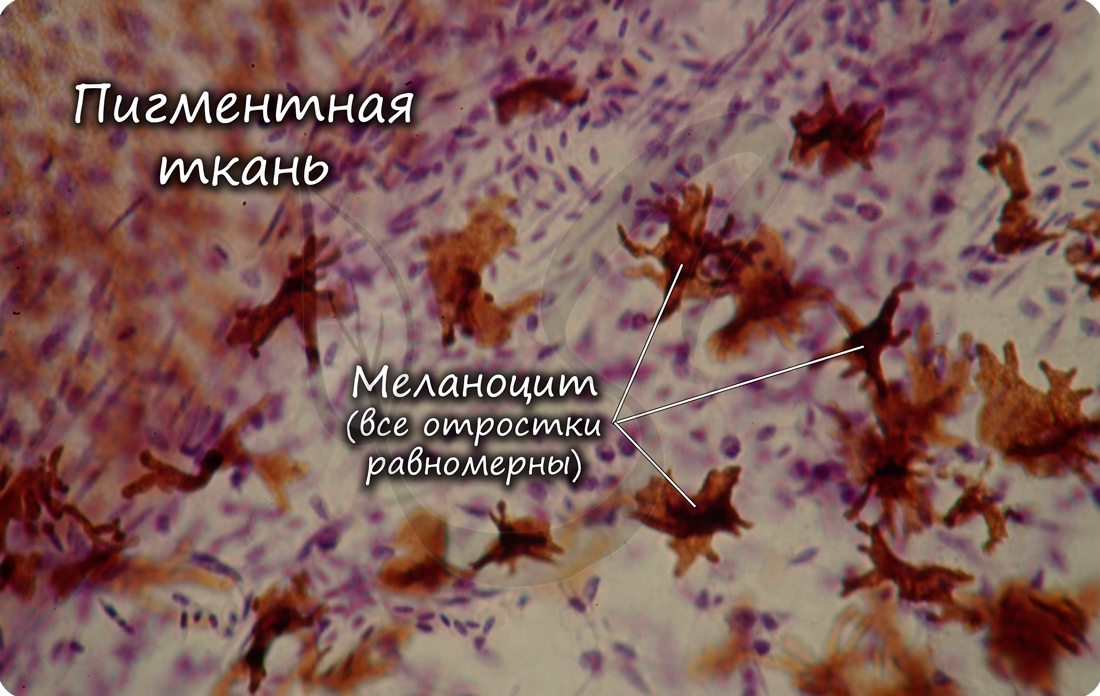
Слизистая (студенистая) ткань встречается в норме только в составе пупочного канатика зародыша, ее относят к эмбриональным тканям.
К скелетным тканям относятся хрящевая и костная ткани, которые выполняют защитную, механическую и опорную функции, принимают активное участие в минеральном обмене.
Хрящевая ткань состоит из молодых клеток - хондробластов, зрелых - хондроцитов (от греч. chondros - хрящ). Межклеточное вещество упругое, содержит много воды, особенно в молодом возрасте. С течением времени воды в хряще становится меньше и его функция постепенно нарушается.
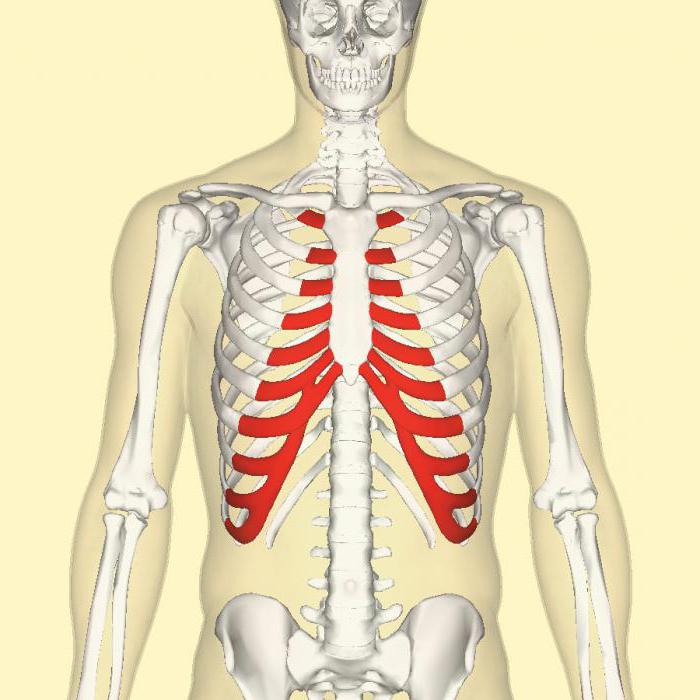
Хрящевая ткань образует межпозвоночные диски, хрящевые части ребер, входит в состав органов дыхательной системы. В хрящевой ткани, как и в эпителии, отсутствуют кровеносные сосуды, благодаря чему хрящи отлично приживаются после пересадки. Питание хряща происходит диффузно.
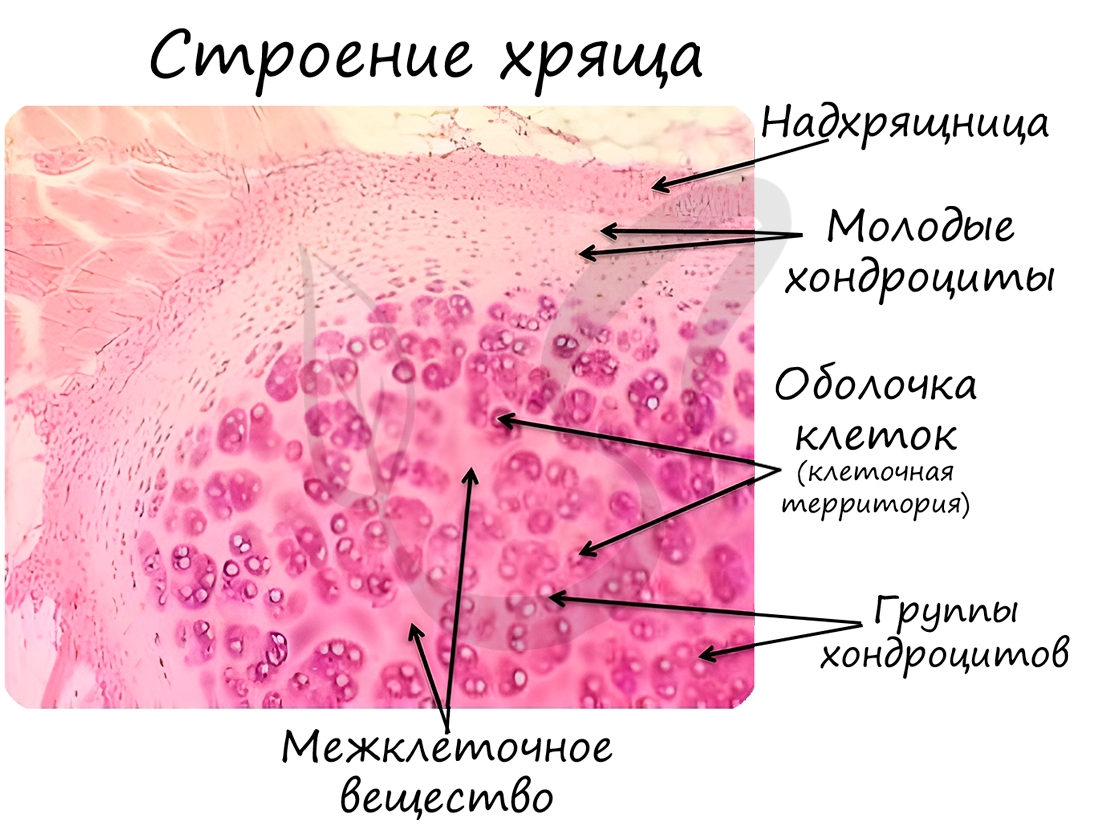
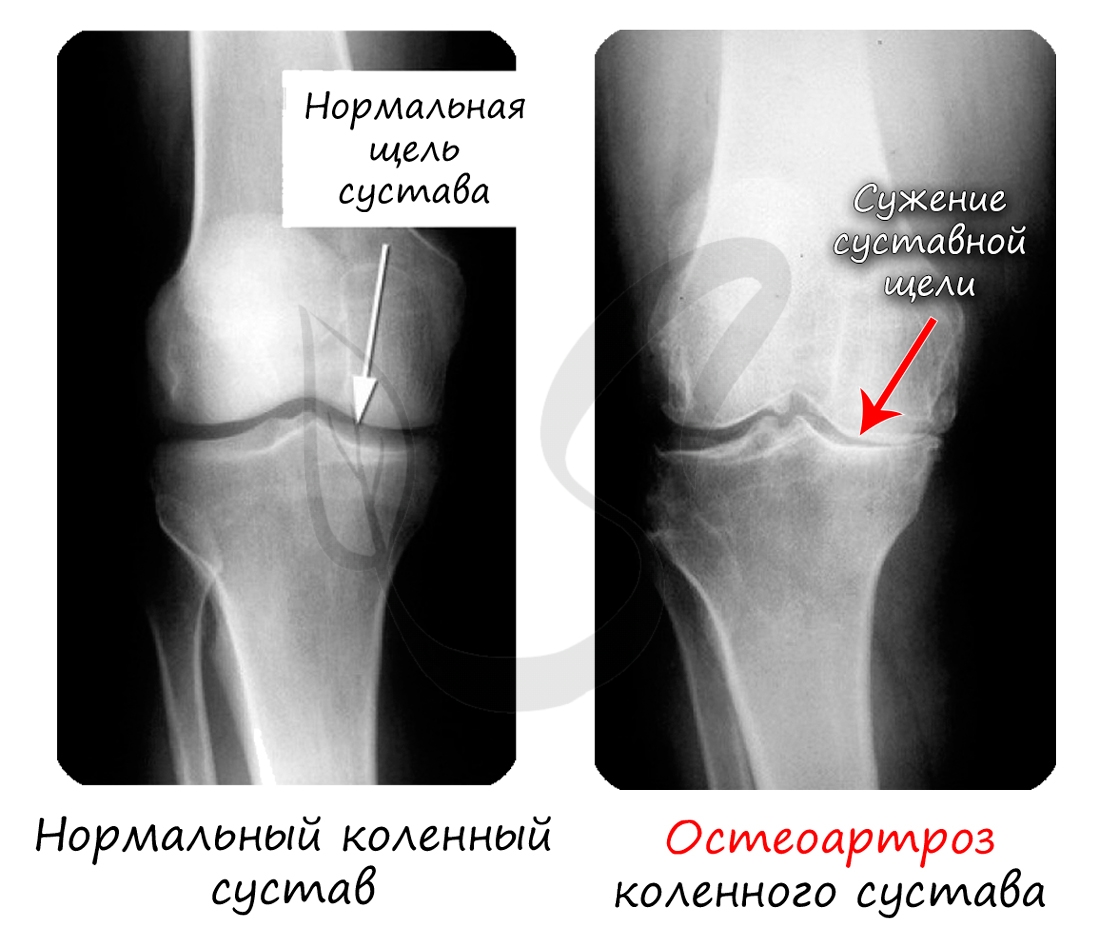
Хрящевая ткань выстилает поверхность костей в месте образования суставов. При нарушении в ней обменных процессов хрящевая ткань начинает заменяться костной, что сопровождается скованностью и болезненностью движений, возникает артроз.
Костная ткань состоит из клеток и хорошо развитого межклеточного вещества, пропитанного минеральными солями (составляют около 70%), преобладающим из которых является фосфат кальция Ca3(PO4)2.
В костной ткани активно идет обмен веществ, интенсивно поглощается кислород. Кости - это вовсе не что-то безжизненное, в них постоянно появляются новые и отмирают старые клетки. В кости можно обнаружить следующие типы клеток:
- Остеобласты - молодые клетки
- Остеоциты - зрелые клетки (от греч. osteon — кость и греч. cytos — клетка)
- Остеокласты - отвечают за обновление кости, разрушают старые клетки

Кость состоит из компактного и губчатого вещества. Компактное вещество значительно тяжелее и плотнее губчатого, обеспечивает основополагающие функции кости: защитную, поддерживающую. В компактном веществе запасаются химические элементы. Губчатое вещество содержит орган кроветворение - красный мозг.
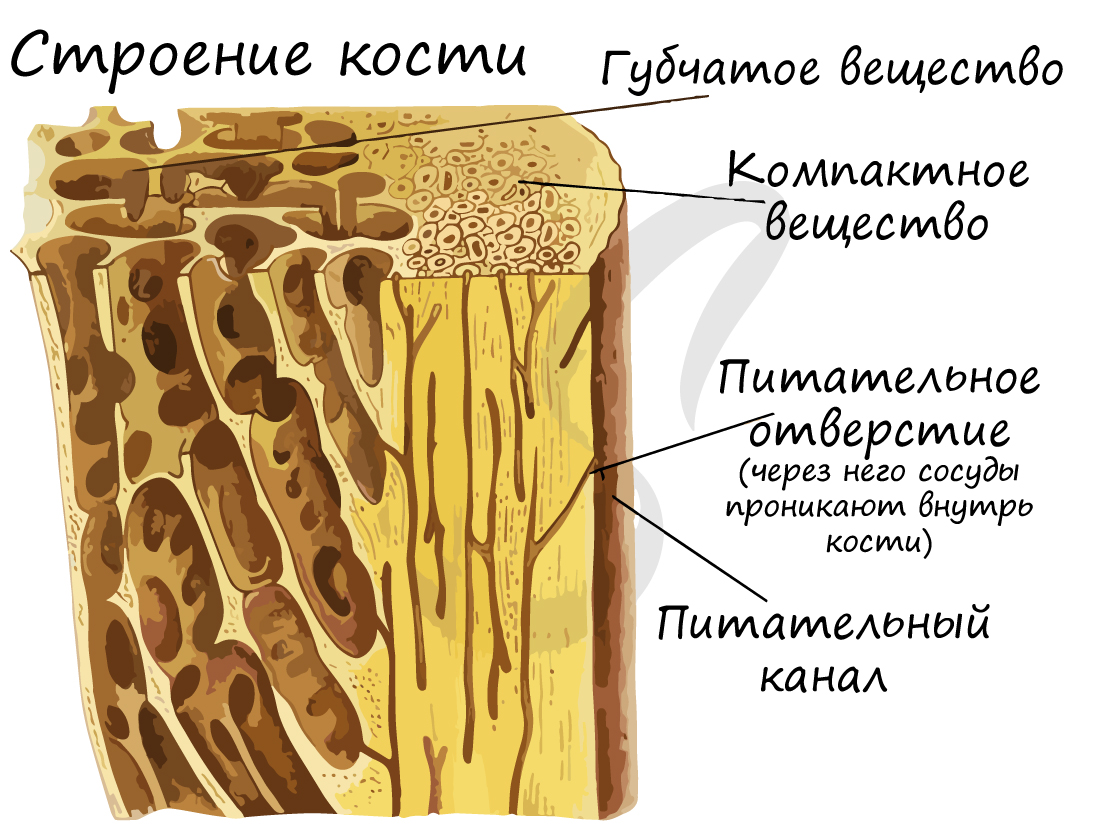
Структурной единицей компактного вещества является остеон (Гаверсова система). В Гаверсовом канале, расположенном в центре остеона, проходят кровеносные сосуды - источник питания для костной ткани. По краям канала лежат юные клетки, остеобласты, и стволовые клетки. Вокруг канала лежат соединенные друг с другом остеоциты, образующие пластинки.
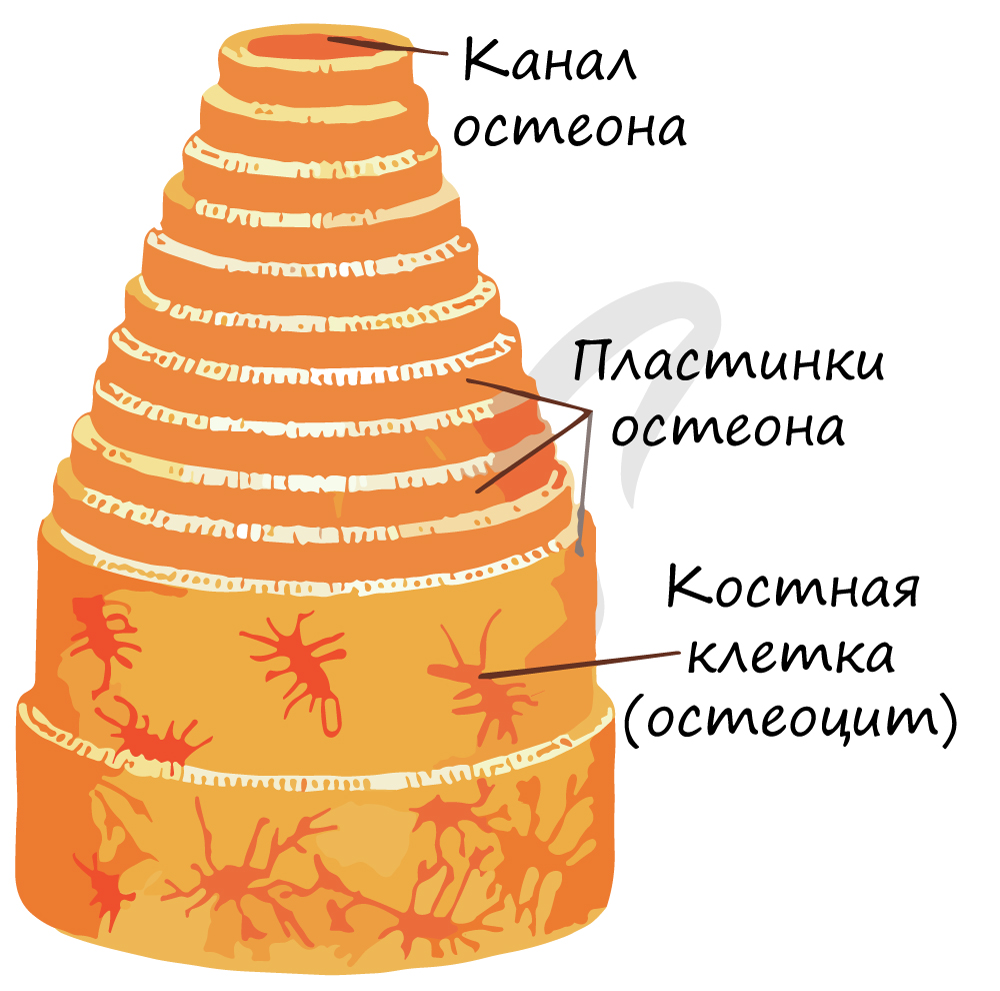
Кость состоит из двух компонентов:
-
Минеральный
Межклеточное вещество костной ткани содержит коллагеновые волокна, которые пропитаны минеральными солями, главным образом - фосфатом кальция Ca3(PO4)2, за счет чего костная ткань выполняет опорную функцию и способна выдерживать значительные нагрузки.
С возрастом доля минерального компонента увеличивается, и кость становится более ломкой и хрупкой, возникает склонность к переломам. Истончение костной ткани называется остеопороз (от греч. osteon - кость + греч. poros - пора).
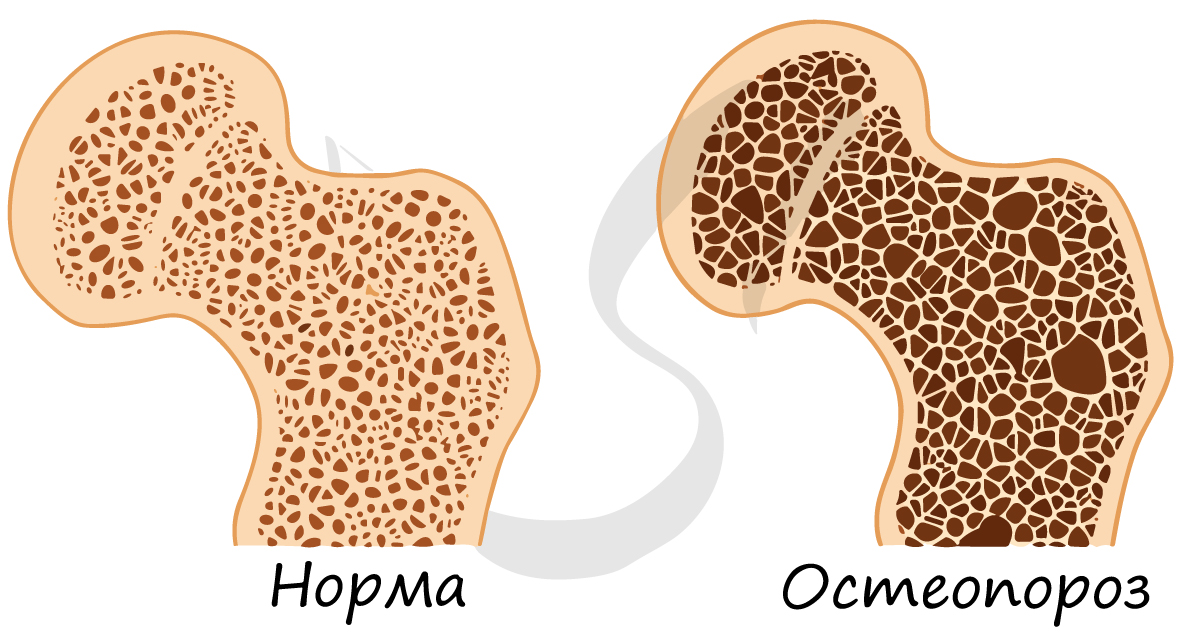
Органический компонент представлен белками и жирами (липидами). За счет данного компонента обеспечивается еще одно важное свойство кости - эластичность. Если провести химический опыт и удалить из кости все соли (мацерация кости), то она станет настолько гибкой, что ее можно завязать в узел.

Органический компонент превалирует в костях новорожденных. Их кости очень эластичные. Постепенно минеральные соли накапливаются, и кости становятся твердыми, способными выдержать значительные физические нагрузки.
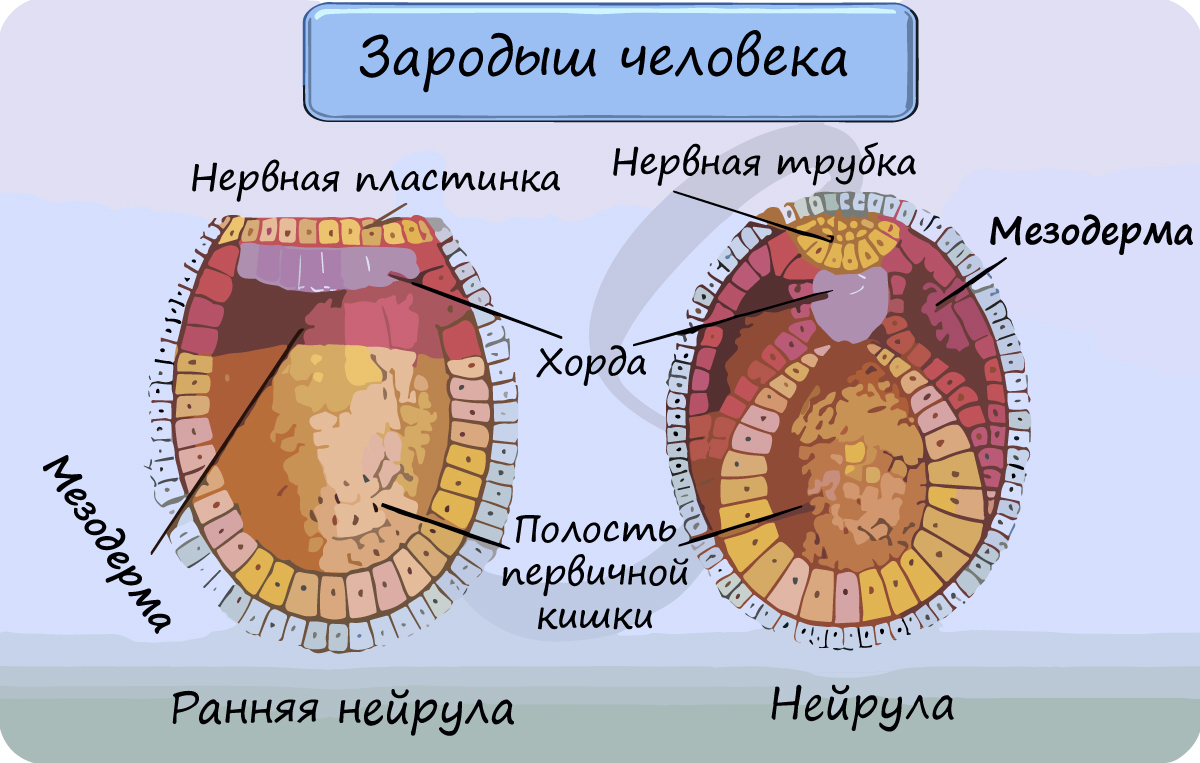
Соединительные ткани развиваются из мезодермы - среднего зародышевого листка.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Регенерация хрящевой ткани возможна лишь в очень незначительных пределах, и в настоящее время ученые и медики активно работают над этой проблемой. Сейчас пациентам с патологиями хряща могут предложить такие методы лечения, как туннелизация, хондропластика, артропластика и микрофрактурирование. К последним разработкам относится замещение разрушенных участков хряща собственными хондроцитами. Если ведущиеся сегодня разработки окажутся успешными, то в будущем количество операций эндопротезирования суставов может значительно сократиться.
Вырастить хрящевую ткань отдельно от организма, а затем трансплантировать ее – это достаточно дорогое мероприятие. Такого рода проблемами занимается генная и тканевая инженерия. Кстати, пересадка хряща сегодня благодаря артроскопии возможна без значительной травматизации сустава и окружающих тканей.
Традиционное хирургическое лечение
Еще до недавнего времени работоспособность возвращали с помощью лаважа (промывание) и более продуктивного дебридмента (санация и обработка) поверхности сустава. Как только артроскопы внедрили в широкую хирургическую практику, эти два метода активно помогали избавляться от свободных тел и других патологических тканей внутри коленных, локтевых и других суставов. Эти процедуры были весьма эффективны, улучшения после их применения отмечали примерно 2/3 пациентов; однако через три года многие из прооперированных пациентов начинали жаловаться на прежние проблемы. Некоторые болезни с помощью дебридмента и лаважа лечить вообще невозможно (например, остеохондроз с полным обнажением кости).
Позднее поврежденную патологическими процессами хрящевую ткань предложили замещать фибрином. Для этого оставшуюся хрящевую ткань счищали, затем следовала туннелизация и микрофрактурирование костной ткани. Кость сверлили артроскопическим буром, пока не появлялось петехиальное кровотечение. Таких отверстий делалось множество. Из них на поверхность выходил костный мозг, из которого формировался фиброзный сгусток. Ту же операцию проводили и другим образом, рассверливая кость микроперфоратором до появления микропереломов. В итоге поверхность кости покрывал волокнистый хрящ либо фиброзная ткань.
Недостатком данного метода является тот факт, что фиброзная ткань не была такой же прочной, как гиалиновый хрящ, поэтому она быстро изнашивалась. Кроме этого, у многих больных сохранялись болевые ощущения. Приемлемые результаты наблюдались преимущественно у молодых больных, которые постоянно занимались разработкой коленного сустава.
Биологические методы, которые задействуют собственные ресурсы организма
С начала 90-ых годов XX столетия специалисты стали пересаживать в коленный сустав хрящ из реберной области. Трансплантат фиксировался фибриновым клеем. Контрольные тесты через год показали, что дефект закрывался почти полностью, больные переставали жаловаться на дискомфорт. Но долговременные исследования позволили установить, что такой пересаженный хрящ может подвергаться энхондральной оссификации.
Взятие трансплантата из районов с интактным хрящом. В этом случае хрящевая ткань бралась из мыщелка бедренной кости. Такая методика хорошо зарекомендовала себя в тех случаях, когда размер трансплантата не превышал 2 сантиметров. Но долговременных исследований результатов такого рода операций не проводилось.
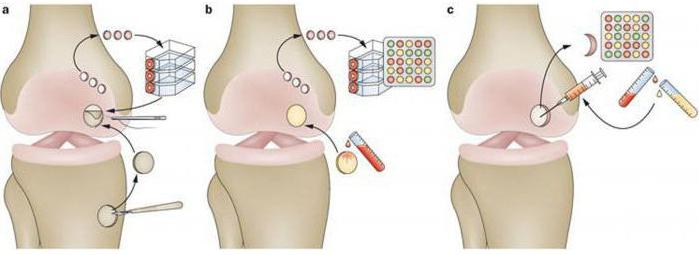
Трансплантация собственных хондроцитов. Этот метод придумали еще в конце 80-х годов, он применяется только на коленном суставе. Нужно изъять неповрежденный хрящ из мыщелка бедра, количество биоптата невелико: всего 200 - 300 миллиграммов. Затем полученная ткань в течение двух или трех недель культивируется в специальных лабораторных условиях. Спустя это время количество хондроцитов вырастает в 10 -12 раз. Чтобы пересадить их в проблемную область, потребуется повторная артротомия. Перед этим хрящевой дефект следует подготовить, то есть убрать все лишнее и обнажить субхондральную кость.
Затем из области голени изымается небольшой фрагмент большеберцовой кости, и эту надкостницу пришивают к поврежденному хрящу. Шов закрывается фибриновым клеем, в нем остается лишь небольшое отверстие, куда вставят катетер. По нему вводят хондроциты в район дефекта, после чего катетер изымают и отверстие заливают фибриновым клеем.
Все наши кости в процессе эмбрионального (зародышевого) развития образуются из хрящей. У взрослого человека они составляют не более 2% массы тела. Кости растут благодаря диафизарному хрящу, удлиняются они до тех пор, пока не закрываются так называемые зоны роста1. Однако некоторые из них увеличиваются в течение всей жизни человека. Установлено, что постоянно растут, хотя и малыми темпами, нижняя челюсть, нос, ушные раковины, ступни ног и кисти рук.
Наиболее часто, спортсмены покидают спорт из-за травм суставно-связочного аппарата. Его слабое место — хрящ. Проблемы с позвоночником также обусловлены в основном патологией межпозвоночных хрящей.
Можно сказать, что в спортивной травматологии лечение хрящей является заботой № 1. При этом некоторые авторы считают, что восстанавливаются они не более чем на 50%, ставя, таким образом, под сомнение возможность полного восстановления спортивной работоспособности. Попробуем более подробно рассмотреть, что же такое хрящ и определить пределы и методы его регенерации.
Хрящевая ткань — одна из разновидностей соединительной ткани, которая выполняет в организме опорные функции. Непременным атрибутом хряща, за исключением суставного, является надхрящница, обеспечивающая его питание и рост. В суставах хрящ обнажен и контактирует непосредственно с внутренней средой сустава — синовиальной жидкостью. Она выполняет роль своеобразной смазки между трущимися поверхностями суставов, покрытых гладким глиаиновым хрящом. Хрящи костей и позвоночника постоянно испытывают как статическую, так и динамическую нагрузки. Хрящи носа, гортани, бронхов, фиброзных треугольников в сердце осуществляют также и опорную функцию.
Структура хряща позволяет ему испытывать обратимую деформацию и в то же время сохранять способность к обмену веществ и размножению. Главные его компоненты — хрящевые клетки (хендроциты) и внеклеточный матрикс, состоящий из волокон и основного вещества. Причем, большую часть массы хряща составляет именно межклеточное вещество.
В зависимости от преобладания коллагеновых, эластических волокон или основного вещества различают гиалиновый, эластический и волокнистый хрящ.
Особенностью хряща, по сравнению с другими видами тканей в организме является то, что в нем мало клеток и они окружены большим количеством межклеточного пространства — матрикса. Хрящ так плохо восстанавливается после повреждений именно потому, что в нем очень мало клеток, способных размножаться и основная часть репарации (восстановления) идет за счет внеклеточного матрикса. В эластическом хряще (гортани, носа, ушной раковины) содержится много эластина (из него, например, на 30% состоит ухо человека ).
Биомеханические свойства хрящей делают их высокоспецифическими и по существу уникальными компонентами опорно-двигательного аппарата.
Они:
а) принимают на себя действие внешних механических сил сжатия и растяжения; распределяют эти силы равномерно, поглощают и рассеивают их, переводя аксиально направленные силы в тангенциальные (в суставах конечностей, позвоночника и т.д.);
б) образуют устойчивые к износу поверхности сочленений скелета, участвуют в формировании смазочного аппарата в синовиальных суставах;
в) являются местом прикрепления и опорой для мягких тканей и мышц; образуют полости в местах контакта с внешней средой (хрящи носа, ушей, органов дыхания).
Считается, что хрящевой матрикс состоит из 3-х основных компонентов:
1) волокнистый коллагеновый каркас, который образует трехмерную сеть переплетений;
2) молекулы протеогликанов, которые заполняют петли волокнистого каркаса;
3) вода, свободно перемещающаяся между переплетениями каркаса и молекулами протеогликанов.
У суставного хряща нет кровеносных сосудов. Он питается диффузно, поглощая питательные вещества из синовиальной жидкости.
В чем причина низкой метаболической активности хряща? Только в одном — в малом количестве клеток (1-10%) в единице объема ткани. В пересчете на чистую клеточную массу уровень метаболизма хондроцитов ничуть не меньше, чем у других клеток организма. Особенно низким метаболизмом отличаются суставные хрящи и пульподные ядра межпозвонковых дисков. Именно эти структуры отличаются самым малым количеством хондроцитов (1% от общей массы хряща) и именно они хуже всех других восстанавливаются после повреждений.
Окислительные процессы в хряще протекают в основном анаэробным (бескислородным) путем. Так, например, хондроциты пульпозных ядер межпозвоновых дисков на 99% питаются анаэробно и лишь на 1% аэробно. В среднем же кислородные окисление в хрящевой ткани как минимум в 50 раз менее интенсивно, чем в обычных тканях организма. Анаэробный характер окисления в хондроцитах — это защитно-приспособительная реакция, сложившаяся в процессе эволюции. И это неудивительно, если учесть, что хрящ не имеет (глаиновый, фиброзный) или почти не имеет (эластический) кровоснабжения. Если начать введение кислорода в пространство, пограничное с хрящом, то диффузия в хрящ О2 не только не улучшает его трофику, но, наоборот, резко ухудшает ее.
Насколько низка метаболическая активность хряща, можно понять из следующего сравнения. Белковый состав печени полностью обновляется за 4(!) дня. Коллаген хрящей обновляется всего лишь на 50% за 10(!) лет. Поэтому становится понятным, что любая травма хрящевой ткани практически неизлечима, если только не принять специальных мер, направленных на увеличение числа хондроцитов, которые сформируют новый матрикс.
Регенерация хрящевой ткани как физиологическая, так и репаративная (восстановительная) напрямую зависит от гормонального фона и модулирующего действия тех или иных гормонов. Так, например, глюкокортикоидные гормоны угнетают анаболические реакции в хондроцитах, ингибируют синтез коллагена и протеогликанов, вызывают дефицит глауроновой кислоты в синовиальной жидкости и в матриксе. И это угнетающее действие глюкокортикоидов более выражено, если оно сочетается со сдавлением (компрессией) хряща. В принципе, в этом нет ничего удивительного, если учесть, что глюкокортикоиды подавляют гликолиз — анаэробное окисление глюкозы в хряще. Регенерация без энергетического обеспечения становится попросту невозможной. Инсулин стимулирует синтез коллагена в матриксе хрящевой ткани, однако эта стимуляция невелика и носит опосредованный характер.
Самым сильным фактором, стимулирующим как физиологический, так и репаративный синтез в хрящевой ткани является соматотропный гормон. Сродство хрящей к соматотропному гормону отсутствует как таковое. Однако под действием соматотропного гормона в печени образуется инсулиноподобный фактор роста (ИРФ-1), который и обладает собственно анаболическим действием на все ткани, включая хрящевую. Сам по себе гормон роста способен оказывать анаболическое действие на клетки лишь в том случае, если его концентрация в 2000 раз превышает физиологическую. Такое возможно только в пробирке и полностью исключается в реальной жизни. Применяя соматотропин с репаративной целью необходимо помнить, что его влияние на синтез ИРФ-1 возможно лишь в условиях нормальной работы печени, при отсутствии серьезных заболеваний, иначе ИРФ-1 просто не будет синтезироваться и введение соматотропина не даст никакого результата. Способность соматомедина усиливать регенерацию хрящевой ткани в 100 раз превышает эффект от введения в организм инсулина и тестостерона. ИРФ-1 — это единственный фактор, вызывающий деление (размножение) хондроцитов. Другие анаболические факторы организма (а их довольно много) такой способностью не обладают.
Тестостерон — основной андроген организма умеренно стимулирует биосинтетические процессы в хрящах, а эстрогены — женские половые гормоны, наоборот, тормозят ее.
Анаболические стероиды обладают способностью вызывать регенерацию хряща в намного большей степени, нежели чистый тестостерон и это неудивительно, если учесть, что они обладают анаболическим действием в несколько раз превышающим анаболическое действие тестостерона.
Интересно, что матрикс — порождение хондроцитов — живет своей самостоятельной жизнью. Он способен модулировать действие различных гормонов на хондроциты, ослабляя, либо усиливая их действие. Воздействуя на матрикс, можно изменить состояние хондроцитов как в лучшую, так и в худшую сторону. Удаление части матрикса вызывает немедленную интенсификацию биосинтеза недостающих в нем макромолекул. Более того, одновременно усиливается пролиферация (разрастание) хондроцитов. Количественные изменения в матриксе способны вызвать их качественные изменения.
Длительное ограничение движений в суставе (гипсовая иммобилизация и др.) приводит к уменьшению массы хрящей. Причина на удивление проста: в неподвижном суставе отсутствует перемешивание синовиальной жидкости. При этом диффузия молекул в хрящевую ткань замедляется и питание хондроцитов ухудшается. Недостаток прямой компрессивной нагрузки (на сжатие) так же приводит к ухудшению питания хондроцитов. Хрящу нужна хотя бы минимальная компрессионная нагрузка для поддержания нормальной трофики. Чрезмерная нагрузка на растяжение в эксперименте вызывает перерождение хряща с развитием грубых фиброзных волокон.
Очень сложное влияние на состояние внутрисуставных хрящей оказывает синовиальная оболочка. Она может как усиливать анаболизм хрящевой ткани, так и усиливать ее катаболизм. Удаление синовиальной оболочки резко ухудшает трофику хрящей, которая восстанавливается лишь после ее отрастания.
Хондроциты способны и к ауторегуляции. Они синтезируют специальные факторы роста, стимулирующие разрастание соседних хондроцитов. Пока их структура полностью не расшифрована. Известно лишь то, что они имеют полипептидную природу.
Если в шейном отделе позвоночника негативные явления развиваются с подросткового возраста, то в поясничном отделе, где нагрузка на единицу поперечного сечения намного ниже — начиная с 25-30 лет. В целом они носят такой же морфологический характер, как и в шейном отделе, но отличаются клиническими (медицинскими) признаками. В шейном отделе позвоночника сквозь поперечные отростки шейных позвонков проходят крупные артерии, питающие все основание мозга и его стволовую часть, где находится жизненно важные центры (дыхания, кровообращения и т.д.). С развитием шейного остеохондроза происходит постепенное незаметное сдавливание этих артерий с развитием недостаточности мозгового кровообращения. При этом практически не бывает (или они бывают очень редко) никаких болевых признаков процесса. В поясничном отделе позвоночника картина несколько иная. Из этого отдела выходят нервные корешки, несущие чувствительные волокна от нижних конечностей и двигательные волокна к мышцам ног. Поясничный остеохондроз прежде всего проявляется различными болевыми симптомами, нарушением чувствительности и двигательной сферы. При этом никаких жизненно важных функций организма он не нарушает. Шейный остеохондроз никакими болевыми признаками себя не обнаруживает и особых неудобств не доставляет, однако может привести к серьезным нарушениям мозгового кровообращения, вплоть до инсультов с развитием параличей.
Возрастные изменения эластических хрящей не носят фатального характера. Они выражаются в основном в оссификации — накоплении кальция и не приводят ко сколько-нибудь заметному нарушению функций.
В глиаминовых хрящах суставов уже начиная с 30-летнего возраста обнаруживается фибриляция — разволокнение хрящевой поверхности. При микроскопическом исследовании на поверхности хряща обнаруживаются разломы и расщепления. Расщепление хряща происходит как вертикальном, так и в горизонтальном направлении. При этом местами встречаются скопление клеток хрящевой ткани как ответная реакция организма на разрушение хряща. Иногда отмечается возрастное увеличение (!) толщины суставных хрящей как ответное действие на действия механических (тренировка) факторов. Возрастную эволюцию хрящей коленного сустава многие исследователи отмечают начиная уже с 40-летнего возраста. Наиболее существенное изменение, отмечаемое при старении хряща — это уменьшение содержания воды, что автоматически приводит к снижению его прочности.
Потенциальные возможности регенерации хряща достаточно велики. Он может регенерировать за счет собственного потенциала (размножение хондроцитов и рост матрикса) и, что не менее важно, за счет других видов соединительной ткани, которые имеют общее с ним происхождение. Примыкающие к хрящу ткани обладают способностью к переориентации своих клеток и превращению их в хрящеподобную ткань, которая неплохо справляется со своими функциями. Возьмем для примера самый частый вид повреждений — повреждение внутрисуставного хряща.
При поверхностных повреждениях можно добиться полного восстановления хряща применяя сильнодействующие фармакологические средства. За последние 40 лет экспериментальных и клинических работ свою высокую эффективность доказал лишь один единственный препарат — соматотропный гормон (СТГ). Он стимулирует рост хрящевой ткани в 100 раз сильнее, чем введение тестостерона и инсулина. Еще больший эффект оказывает комбинированное введение СТГ и тиреокальцитонина — особого рода гормона щитовидной железы, который усиливает репарацию как костной, так и хрящевой ткани. Исключительная эффективность действия СТГ на репарацию хряща обусловлено тем, что он стимулирует непосредственно деление хондроцитов. Используя СТГ теоретически можно довести количество хондроцитов до любого нужного количества. Они, в свою очередь, восстанавливают матрикс до необходимого объема, синтезируя все его компоненты, начиная с коллагеновых волокон и кончая протеогликанами. Недостатком СТГ является то, что его нельзя применять местно, вводя непосредственно в зону поражения хрящевой ткани, поскольку действует он опосредованно. СТГ вызывает образование в печени инсулиноподобного фактора роста (ИРФ-1) который и оказывает сильнейший анаболический эффект. Парентеральное (инъекционное) его введение вызывает рост не только поврежденных хрящей, но и нормальных тоже, а это нежелательно, ведь в организме существуют кости, в которых хрящевые зоны роста не закрываются на протяжении всей жизни. Длительное введение больших доз СТГ в сформировавшийся организм может вызвать диспропорции скелета. Хотя следует отметить, что на пораженный хрящ он действует сильнее, и явных деформаций скелета при лечении СТГ в научной литературе не встречается.
В последние годы синтезирована лекарственная формы ИРФ-1, которую все шире применяют инъекционно вместо соматотропина. Поскольку ИРФ-1 действует непосредственно на ткани (в т.ч. и на хрящевую), то возникает заманчивая перспектива использовать его для местного введения (электрофорез, ультразвук и т.д.). Такое применение ИРФ-1 позволило бы локализовать его действие местом пораженного хряща и исключить действие на здоровые хрящи организма.
Неплохое действие на восстановление хряща и окружающего его соединительной ткани оказывают анаболические стероиды (АС). По эффективности они стоят на втором месте после ИРФ-1 и соматотропного гормона, хотя непосредственно деления хондроцитов они не вызывают. Анаболические стероиды, однако, ускоряют физиологическую регенерацию и потенцируют анаболическое действие инсулина и других эндогенных анаболических факторов, блокируют действие катаболических гормонов (глюкокортикоидов). Практическое применение АС в хирургической и травматологической практике доказало их высокую эффективность. Очень жаль, что до сих пор не разработаны лекарственные формы АС для локального применения. Это позволило бы создавать высокие концентрации лекарственного вещества именно в месте повреждения и предотвращать системные (на уровне всего организма) побочные действия. К сожалению, исследования в данной сфере никем не финансируются из-за причисления АС к допинговым средствам в спорте.
Некоторые исследователи в области молекулярной биологии представили очень убедительный материал, доказывающий, что стимуляторы (2-адренергических рецепторов способны симулировать анаболические эффекты соматомединов и, в частности, по отношению к хрящевой ткани. Механизм такого действия не вполне ясен. Не исключено, что просто повышается чувствительность печени к эндогенному соматотропному гормону и возрастает синтез в печени ИРФ-1. Одним из наиболее сильных избирательных стимуляторов (2-адренергических рецепторов является кленбутерол. Этот препарат не обладает гормональными эффектами и, в то же время, оказывает хорошее анаболическое действие. Подобно ИРФ-1 он стимулирует рост хрящевой ткани и может с успехом применяться в посттравматическом восстановительном периоде. Препаратов, стимулирующих (2-адренорецепторы много, но особо хотелось бы отметить такое старое и проверенное средство как адреналин. Адреналин — гормон мозгового вещества надпочечников даже при длительном курсовом применении не вызывает привыкания. В больших дозах адреналин воздействует в основном на а-адренорецепторы. Происходит сужение сосудов кожи, повышение артериального давления, подъем уровня сахара в крови. Малые дозы адреналина не затрагивают а-адренорецепторов, стимулируют (2-адренорецепторы. Расширяются сосуды мышц, снижаются уровень сахара в крови и артериальное давление. Развивается общее анаболическое действие и, в особенности по отношению к хрящевой ткани. Ежедневное введение малых (именно малых!) доз адреналина хорошо зарекомендовало себя как средство, способствующее регенерации.
Некоторые витамины в больших фармакологических дозировках способны существенно увеличить выброс в кровь эндогенного соматотропина. Пальму первенства здесь держит никотиновая кислота (витамин РР). Внутривенное введение сравнительно небольших доз никотиновой кислоты способно увеличить базальную секрецию СТГ в 2-3 раза. Увеличивает секрецию гормона роста витамин К, только применять его необходимо в умеренных дозах, чтобы не повысить чрезмерно свертываемость крови.
1 Прекращение роста большинства костей в длину могут служить признаком того, что уже возможно лечение, например, анаболическими стероидами, которые приводят к преждевременному закрытию ростовой зоны хряща, если ростовые зоны узе закрыты, (что явствует из рентгеновского снимка лучевой кости молодого человека), то уже отсутствует опасность слишком быстро закрыть зоны роста применения стероиды, а значит, их применение можно начинать.
Костная и хрящевая ткани составляют человеческий скелет. На эти ткани возложена опорная функция, вместе с этим они защищают внутренние органы, системы органов от неблагоприятных факторов. Для нормального функционирования человеческого организма необходимо, чтобы все заложенные природой хрящи были на анатомически верных местах, чтобы ткани были прочными и регенерирующими по мере необходимости. В противном случае человек сталкивается со множеством неприятных заболеваний, понижающих уровень жизни, а то и вовсе лишающих возможности передвигаться самостоятельно.
Особенности ткани
Ткань, как и любые другие структурные элементы организма, сформирована из специальных клеток. Клетки хрящевой ткани в науке именуются дифферонами. Это понятие сложное, включает в себя несколько разновидностей клеток: стволовые, полустволовые, объединенные в рамках анатомии в группу малоспециализированных, – этой категории присуща способность к активному делению. Также выделяют хондробласты, то есть такие клетки, которые могут делиться, но вместе с тем способны продуцировать межклеточные соединения. Наконец, есть клетки, чья основная задача – создание промежуточного вещества. Их специализированное наименование – хондроциты. В составе этих клеток есть не только волокна хрящевой ткани, функции которых – обеспечение устойчивости, но также основное вещество, именуемое учеными аморфным. Это соединение способно связывать воду, благодаря чему хрящевая ткань стойко сопротивляется нагрузкам на сжатие. Если все клетки сустава здоровы, он будет упругим, прочным.
В науке выделяют три вида хрящевой ткани. Для деления на группы анализируют особенности межклеточного соединительного компонента. Принято говорить о следующих категориях:
- эластичная;
- гиалиновая;
- волокнистая.
А если подробнее?
Как известно из анатомии, все виды хрящевой ткани имеют свои характерные особенности. Так, эластичная ткань отличается спецификой строения межклеточного вещества – для него характерна довольно высокая концентрация коллагеновых волокон. Вместе с тем такая ткань богата аморфным веществом. В то же время в этой ткани наблюдается высокий процент эластичных волокон, которые и дали ей название. Функции хрящевой ткани эластичного типа связаны с этой особенностью: обеспечение упругости, гибкости, стойкого сопротивления внешнему влиянию. Что может рассказать еще интересного анатомия? Где находится хрящевая ткань этого типа? Обычно – в тех органах, которые от природы предусмотрены сгибающимися. Например, из эластичной хрящевой ткани состоят гортанные хрящи, нос и раковины ушей, центр бронхов.
Волокнистая ткань: некоторые особенности
В той точке, из которой начинается гиалиновый хрящ, заканчивается волокнистая соединительная ткань. Обычно эта ткань находится в дисках между позвонками, а также в местах соединения костей, где подвижность не важна. Особенности строения хрящевой ткани этого типа прямо связаны со спецификой ее расположения. Сухожилия, связки в точке контакта с хрящевой тканью провоцируют активно развитую систему коллагеновых волокон. Особенность такой ткани – наличие хрящевых клеток (вместо фибробластов). Эти клетки формируют изогенные группы.
Что еще нужно знать
Курс анатомии человека позволяет четко уяснить себе, для чего нужна хрящевая ткань: для обеспечения подвижности при сохранении упругости, стабильности, безопасности. Эти ткани плотные и позволяют гарантировать механическую защиту. Современная анатомия как наука характеризуется обилием терминов, в том числе дополняющих и взаимно заменяющих друг друга. Так, если речь о стекловидной хрящевой ткани позвоночника, то предполагается, что говорят о гиалиновой. Именно эта ткань формирует концы косточек, составляющих реберную клетку. Из нее же созданы и некоторые элементы дыхательной системы.
Функции хрящевой ткани из категории соединительнотканной – соединение ткани и гиалинового стекловидного хряща, имеющего совершенно другую структуру. А вот сетчатая хрящевая ткань обеспечивает нормальное функционирование надгортанника, системы слуха, гортани.
Зачем нужна хрящевая ткань?
Природа ничего не создает просто так. Все ткани, клетки, органы имеют довольно обширную функциональность (а некоторые задачи и по сей день скрыты от ученых). Как известно из анатомии уже сегодня, функции хрящевой ткани включают в себя гарантию надёжности соединения элементов, обеспечивающих человеку возможность двигаться. В частности, костные элементы позвоночника между собой связаны именно хрящевой тканью.
Как удалось установить в ходе исследований, посвященных аспектам питания хрящевой ткани, она принимает активное участие в углеводном обмене. Это объясняет некоторые особенности регенерации. Отмечается, что в детском возрасте восстановление хрящевой ткани возможно на 100 %, а вот по прошествии лет эта способность теряется. Если взрослый человек сталкивается с повреждением хрящевой ткани, он может рассчитывать только на частичное восстановление подвижности. В то же время восстановление хрящевой ткани – это одна из задач, привлекающих внимание передовых умов медицины нашего времени, поэтому предполагается, что удастся найти эффективное фармацевтическое решение этой проблемы в ближайшее время.
Проблемы с суставами: есть варианты
В настоящее время медицина может предложить несколько методик восстановления поврежденных по разным причинам органов и тканей. Если сустав получил механическую травму либо некое заболевание спровоцировало разрушение биологического материала, в большинстве случаев наиболее эффективным решением проблемы становится протезирование. А вот уколы для хрящевой ткани помогут, когда ситуация зашла еще не столь далеко, дегенеративные процессы начались, но обратимы (хотя бы частично). Как правило, прибегают к средствам, в составе которых есть глюкозамин, сульфат натрия.
Разбираясь, как восстановить хрящевую ткань на начальных этапах заболевания, обычно прибегают к физическим упражнениям, строго следя за уровнем нагрузки. Хороший эффект показывает терапия с использованием блокирующих воспаление препаратов. Как правило, большинству больных назначают лекарственные медикаменты, богатые кальцием в форме, легко усвояемой организмом.
Хрящевая соединительная ткань: откуда берутся проблемы?
В большей части случаев заболевания провоцируются полученными ранее травмами или инфицированием сустава. Иногда дегенерация хрящевой соединительной ткани провоцируется приходящимися на нее длительный временной промежуток повышенными нагрузками. В ряде случаев проблемы связаны с генетическими предпосылками. Свою роль может сыграть переохлаждение тканей организма.
Особенности строения
Как видно из анатомии, гиалиновый хрящ, другие хрящевые ткани, а также костные объединены в категорию скелетных. На латинском языке эта группа тканей получила наименование textus cartilaginus. До 80 % этой ткани – это вода, от четырех до семи процентов – соли, а остальной объем – органические компоненты (до 15 %). Сухая часть хрящевой ткани на половину или больше (до 70 %) сформирована из коллагена. Матрикс, производимый клетками ткани, представляет собой комплексное вещество, включающее в себя гиалуроновую кислоту, гликозаминогликаны, протеогликаны.
Клетки ткани: некоторые особенности
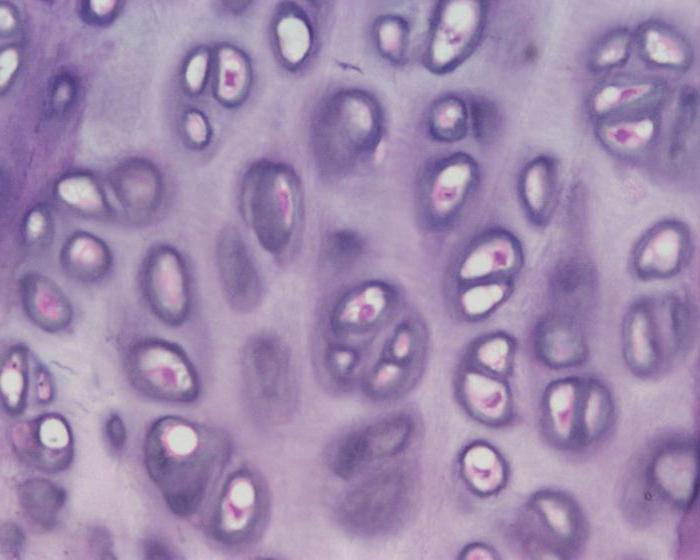
Как удалось выяснить учёным, хондробласты представляют собой такие молодые клетки, которые обычно имеют неправильную вытянутую форму. Такая клетка в процессе жизнедеятельности генерирует протеогликаны, эластин, другие незаменимые для нормального функционирования сустава компоненты. Цитолемма такой клетки – микроворсинки, представленные в огромном количестве. В цитоплазме содержится в обилии РНК. Такой клетке свойственна эндоплазматическая сеть высокого уровня развития, представленная как в незернистой форме, так и в зернистой. В цитоплазме хондробластов также присутствуют гликогеновые гранулы, комплекс Гольджи, лизосомы. Обычно в ядре такой клетки одно или два ядра. Образование содержит большое количество хроматина.
Отличительная особенность хондроцитов – крупный размер, поскольку эти клетки уже зрелые. Для них характерна круглая форма, овальная, полигональная. Большинство хондроцитов оснащены отростками, органеллами. Обычно такие клетки занимают лакуны, а вокруг них располагается межклеточное соединительное вещество. Когда лакуна содержит одну клетку, ее классифицируют как первичную. Преимущественно наблюдают изогенные группы, состоящие из пары или тройки клеток. Это позволяет говорить о вторичной лакуне. Стенка такого формирования имеет два слоя: снаружи она создана из волокон коллагена, а изнутри выстлана протеогликановыми агрегатами, взаимодействующими с хрящевым гликокаликсом.
Биологические особенности ткани
Если рассматривать процесс формирования костей в человеческом организме, можно заметить, что на первичном этапе большая их часть состоит из гиалинового хряща. Со временем происходит преобразование суставной ткани в костную.
Что еще особенного?
А вот волокнистый хрящ очень прочен, так как состоит из толстых волокон. Для его клеток характерна вытянутая форма, ядро в виде палочки и цитоплазма, образующая небольшой ободок. Такой хрящ обычно создает фиброзные кольца, свойственные позвоночнику, мениски, диски внутри суставов. Хрящ покрывает некоторые суставы.
Если рассматривать эластичную хрящевую ткань, можно заметить, что она довольно гибкая, так как матрикс богат не только коллагеном, но и эластичными волокнами. Для этой ткани характерны округлые клетки, заключенные в лакуны.
Хрящ и хрящевая ткань
Эти два термина, несмотря на свою схожесть, нельзя путать. Хрящевая ткань является разновидностью соединительных биологических тканей, хрящ же представляет собой анатомический орган. В его структуре есть не только хрящевая ткань, но также присутствует надхрящница, покрывающая ткани органа снаружи. При этом надхрящница не закрывает суставную поверхность. Этот элемент хряща сформирован соединительной тканью, состоящей из волокон.
Надхрящница состоит из двух слоев: фиброзного, покрывающего ее снаружи, и камбиального, которым орган выстлан внутри. Второй также известен как ростковый. Внутренний слой представляет собой скопление малодифференцированных клеток. К таковым относят хондробласты в неактивной стадии, прехондробласты. Из этих клеток сначала формируются хондробласты, затем они прогрессируют до хондроцитов. А вот фиброзный слой отличается развитой кровеносной сетью, представленной обилием сосудов. Надхрящница – это одновременно и защитный слой, и хранилище материала для регенеративных процессов, и ткань, благодаря которой реализуется трофика хрящевой ткани, в структуре которой сосудов нет. А вот если рассматривать гиалиновый хрящ, то в нем основные задачи по трофике ложатся на синовиальную жидкость, а не только лишь на сосуды. Очень важную роль играет система кровоснабжения костной ткани.
Как это работает?
Основа для формирования хряща, хрящевой ткани – мезенхима. Процесс роста ткани в науке именуют хондрогистогенезом. Мезенхимные клетки в точках, где природой предусмотрено наличие хрящевой ткани, размножаются, делятся, разрастаются, округляются. Это приводит к клеточному скоплению, называемому очагом. Наука обычно именует такие места хондрогенными островками. По мере продвижения процесса вперед происходит дифференциация на хондробласты, благодаря чему становится реальным продуцирование фибриллярных белков, попадающих в среду между живыми клетками. Это приводит к формированию первого типа хондроцитов, способных не только производить специализированные белки, но и ряд других незаменимых для нормальной деятельности органов соединения.
По мере развития хрящевой ткани хондроциты дифференцируются, что приводит к формированию второго и третьего типа клеток этой ткани. На этом же этапе появляются лакуны. Мезенхима, расположенная вокруг хрящевого островка, становится источником клеток для создания надхрящницы.
Особенности роста ткани

По мере старения организма в целом, хрящевой ткани в частности, намечаются дегенеративные процессы. Наиболее склонны к таковым гиалиновые хрящи. Люди пожилого возраста зачастую сталкиваются с болями, спровоцированным солевыми отслоениями в глубоких хрящевых слоях. Чаще накапливаются соединения кальция, что приводит к омелению ткани. Сосуды прорастают в пораженную область, хрящевая ткань постепенно трансформируется в костную. В медицине этот процесс именуют оссификацией. А вот эластичные ткани таким изменениям не повреждены, они не костенеют, хотя и теряют эластичность по прошествии лет.
Хрящевая ткань: проблемы дегенерации
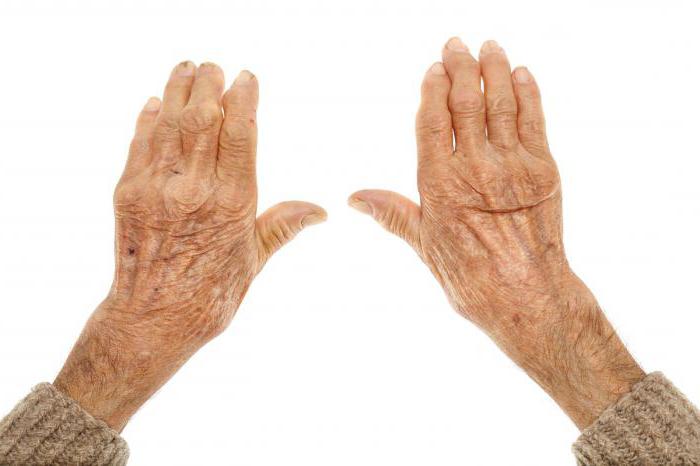
Так сложилось, что с точки зрения человеческого здоровья хрящевая ткань – одна из наиболее уязвимых, и от заболеваний, связанных с суставами, страдают почти все люди пожилого возраста, а зачастую и более молодое поколение. Причин тому много: это и экология, и неправильный образ жизни, и некорректное питание. Конечно же, очень часто мы получаем травмы, сталкиваемся с инфекциями или воспалениями. Разовая проблема – травма или болезнь – проходит, но в старшем возрасте возвращается отголосками – суставными болями.
Хрящ довольно чувствителен ко многим заболеваниям. Проблемы с опорно-двигательной системой возникают, если человек столкнулся с грыжей, дисплазией, артрозом, артритом. Некоторые страдают от недостаточности природного синтеза коллагена. С возрастом хондроциты дегенерируют, и хрящевая ткань от этого сильно страдает. Во многих случаях наилучший терапевтический эффект дает оперативное вмешательство, когда пострадавший сустав меняют на имплантат, но такое решение не всегда применимо. Если есть вероятность восстановления природной хрящевой ткани, не нужно пренебрегать этим шансом.
Суставные болезни: как проявляются?
Большинство страдающих от таких патологий могут точнее любого прогноза предсказать перемену погоды: пораженные заболеванием суставы отзываются на малейшие смены в окружающем пространстве мучительной, тянущей болью. Если больной страдает от поражения суставов, ему нельзя резко двигаться, так как ткани реагируют на это резкой, сильной болью. Как только похожие симптомы начали появляться, нужно сразу же записаться на прием к врачу. Гораздо проще вылечить заболевание или блокировать его развитие, если начать борьбу на ранней стадии. Промедление приводит к тому, что регенерация становится совершенно невозможной.
Для восстановления нормальной функциональности хрящевой ткани было разработано довольно много препаратов. Преимущественно они относятся к категории нестероидных и созданы для блокирования воспаления. Также выпускаются обезболивающие средства – таблетки, уколы. Наконец, в последнее время широкое распространение получили специальные хондропротекторы.
Как лечить?
Наиболее эффективные средства против дегенеративных процессов в хрящевой ткани влияют на клеточном уровне. Они блокируют воспалительные процессы, защищают от негативного влияния хондроциты, а также прекращают дегенеративную активность различных агрессивных соединений, атакующих хрящевую ткань. Если удалось эффективно блокировать воспаление, следующим шагом терапии обычно является восстановление межклеточного соединения. Для этого применяют хондропротекторы.
Было разработано несколько средств этой группы – они построены на разных активных компонентах, а значит, различаются механизмом воздействия на человеческий организм. Для всех средств этой группы характерна эффективность только при приеме длительным курсом, позволяющим достигнуть действительно хороших результатов. Особенное распространение получили препараты, изготовленные на хондроитине сульфата. Это глюкозамин, который участвует в процессе формирования хрящевых белков и позволяет восстановить структуру ткани. За счет поставки вещества из внешнего источника во все виды хрящевой ткани активизируется процесс производства коллагена, гиалиновой кислоты, и хрящ самостоятельно восстанавливается. При правильном использовании медикаментов можно довольно быстро восстановить подвижность сустава и избавиться от боли.

Еще один хороший вариант – средства, содержащие другие глюкозамины. Они восстанавливают ткань от разного рода повреждений. Под влиянием активного компонента обмен веществ в хрящевых тканях сустава нормализуется. Также в последнее время применяют препараты животного происхождения, то есть изготовленные из биологического материала, полученного у животных. Чаще всего это ткани телят, водных существ. Хорошие результаты показывает терапия с применением мукополисахаридов и построенных на них медицинских препаратах.
Читайте также:


