Смачивание мениск краевой угол
Сма́чивание — это поверхностное явление, заключающееся во взаимодействии жидкости с поверхностью твёрдого тела или другой жидкости.
Смачивание зависит от соотношения между силами сцепления молекул жидкости с молекулами (или атомами) смачиваемого тела (адгезия) и силами взаимного сцепления молекул жидкости (когезия).
Если жидкость контактирует с твёрдым телом, то существуют две возможности:
2. молекулы жидкости притягиваются друг к другу слабее, чем к молекулам твёрдого тела. В результате жидкость стремится прижаться к поверхности, расплывается по ней. Так ведёт себя ртуть на цинковой пластине, вода на чистом стекле или дереве. В этом случае говорят, что жидкость смачивает поверхность.
Степень смачивания характеризуется углом смачивания. Угол смачивания (или краевой угол смачивания) это угол, образованный касательными плоскостями к межфазным поверхностям, ограничивающим смачивающую жидкость, а вершина угла лежит на линии раздела трёх фаз: твердого тела, жидкости и газа. Угол смачивания находится по следующей формуле,
38. Капиллярные явления: поднятие жидкости в капилляре, изменение давления насыщенного пара жидкости над искривленной поверхностью.
Капиллярные явления, поверхностные явления на границе жидкости с др. средой, связанные с искривлением ее поверхности. Искривление поверхности жидкости на границе с газовой фазой происходит в результате действияповерхностного натяжения жидкости, которое стремится сократить поверхность раздела и придать ограниченному объему жидкости форму шара. Поскольку шар обладает минимальной поверхностью при данном объеме, такая форма отвечает минимуму поверхностной энергии жидкости, т.е. ее устойчивому равновесному состоянию. В случае достаточно больших масс жидкости действие поверхностного натяжения компенсируется силой тяжести, поэтому маловязкая жидкость быстро принимает форму сосуда, в который она налита, а ее своб. поверхность представляется практически плоской.
В отсутствие силы тяжести или в случае очень малых масс жидкость всегда принимает сферическую форму (капля), кривизна поверхности которой определяет мн. свойства вещества. Поэтому капиллярные явления ярко выражены и играют существенную роль в условиях невесомости, при дроблении жидкости в газовой среде (или распылении газа в жидкости) и образовании систем, состоящих из многих капель или пузырьков (эмульсий, аэрозолей,пен), призарождении новой фазы капель жидкости при конденсации паров. пузырьков пара при вскипании, зародышейкристаллизации. При контакте жидкости с конденсированными телами (другой жидкостью или твердым телом) искривление поверхности раздела происходит в результате действия межфазного натяжения.
В случае смачивания, например, при соприкосновении жидкости с твердой стенкой сосуда, силы притяжения, действующие между молекулами твердого тела и жидкости, заставляют ее подниматься по стенке сосуда, вследствие чего примыкающий к стенке участок поверхности жидкости принимает вогнутую форму. В узких каналах, например, цилиндрических капиллярах, образуется вогнутый мениск - полностью искривленная поверхность жидкости (рис. 1).
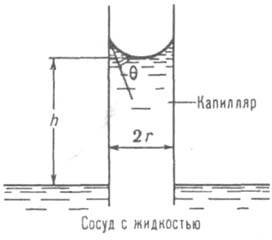
Рис. 1. Капиллярное поднятие на высоту h жидкости, смачивающей стенки капилляра радиуса r; q - краевой угол смачивания.
Высота на которую может подняться жидкость вычисляется по формуле
Капиллярное давление. Так как силы поверхностного (межфазного) натяжения направлены по касательной к поверхности жидкости, искривление последней ведет к появлению составляющей, направленной внутрь объема жидкости. В результате возникает капиллярное давление, величина которого p связана со средним радиусом кривизны поверхности r0 уравнением Лапласа:
где p1 и p2- давления в жидкости 1 и соседней фазе 2 (газе или жидкости), s12 - поверхностное (межфазное) натяжение.
Если поверхность жидкости вогнута (r0 0) знак p изменяется на обратный. Отрицательное капиллярное давление, возникающее в случае смачивания жидкостью стенок капилляра, приводит к тому, что жидкость будет всасываться в капилляр до тех пор, пока вес столба жидкости высотой h не уравновесит перепад давления p.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Поверхностное натяжение растворов отличается от поверхностного натяжения чистых жидкостей. Например, для воды сахар повышает поверхностное натяжение, а поваренная соль (и другие электролиты) – его понижают. Вещества, которые в самой малой концентрации значительно снижают поверхностное натяжение, называются поверхностно-активными.
Поверхностно-активными, как правило, являются вещества, способные адсорбироваться на поверхности жидкости, образуя мономолекулярный слой, в котором действуют молекулярные силы, отличные от чистой жидкости. Адсорбционные силы, вытесняющие молекулы поверхностно-активного вещества на поверхность растворителя противодействуют силам, втягивающим молекулы растворителя в глубину жидкости, которые и создают поверхностное натяжение. Поэтому последнее значительно снижается.
Поверхностно-активные вещества не только широко применяются в различных производствах в качестве моющих средств, эмульгаторов, пенообразователей и т.п., но и имеют большое значение в биологических процессах, особенно на клеточном и молекулярном уровнях, где процессы происходят на границе раздела различных сред. Поверхностно-активные вещества содержатся как в соках растений, так и во многих жидких средах животных организмов.
Смачивание и несмачивание. Мениски
Молекулярные силы притяжения действуют не только между молекулами жидкости, но и между молекулами жидкости и твердого тела, которое с ней соприкасается.
Если силы притяжения молекул жидкости к молекулам твердого тела больше, чем между молекулами самой жидкости, то прилежащие к твердому телу частицы жидкости пристают (прилипают) к его поверхности. Это явление называется смачиванием, а жидкость – смачивающей. Поверхность твердого тела в этом случае называется гидрофильной.
Кривизна поверхности жидкости характеризуется углом между касательными к поверхностям жидкости и твердого тела, построенным внутри жидкости. Угол называется краевым углом жидкости. Для смачивающей жидкости краевой угол острый, он изменяется в пределах 0/2. Если =0, то смачивание полное (идеальное), в остальных случаях – неполное. Капля смачивающей жидкости на горизонтальной поверхности твердого тела растекается (рис. 4а) и при полном смачивании покрывает ее тонким мономолекулярным слоем.


Рис. 4. Явление смачивания (а) и несмачивания (б) жидкостью твердого тела
Если силы притяжения между молекулами жидкости и твердого тела меньше, чем между молекулами жидкости, то жидкость называется несмачивающей, а поверхность твердого тела – гидрофобной.
В этом случае молекулы жидкости не прилипают к поверхности твердого тела, а краевой угол тупой (/2). При = – полная несмачиваемость. Капля несмачивающей жидкости на горизонтальной поверхности имеет форму приплюснутой сферы. Одна и та же жидкость смачивает одни тела и не смачивает другие. Например, вода смачивает стекло и не смачивает жиры. Ртуть не смачивает стекло, но смачивает чистую поверхность железа. Почва, древесина и кора, обезжиренные волокна льна, пеньки, шерсти смачиваются водой, жиры и смолы – водными растворами щелочей и др.
Криволинейные поверхности, которые имеют смачивающие и несмачивающие жидкости в узких круглых трубках, называются менисками. При смачивании мениск вогнутый, при несмачивании – выпуклый.
Под криволинейной поверхностью мениска сила поверхностного натяжения, стремящаяся сократить эту поверхность, создает давление Δрм дополнительное к давлению р, действующему снаружи на жидкость (рис. 5а). Это давление зависит от коэффициента поверхностного натяжения и кривизны поверхности. При выпуклом мениске оно направлено внутрь жидкости и складывается с внешним давлением р. Давление в жидкости рж = р + Δрм.
При вогнутом мениске это давление направлено наружу (рис. 5б) и вычитается из внешнего давления Р на жидкость: рж = р – Δрм.

Рис. 5. Виды менисков, формирование менискового давления
(а – несмачивающая жидкость, б – смачивающая жидкость)
Величина дополнительного давления при полном смачивании и мениске в виде полусферы радиуса rм определяется как отношение силы поверхностного натяжения, действующей по периметру основания полусферы к его площади:

;

;

;

.

–формула Лапласа.
Автор работы: Пользователь скрыл имя, 13 Декабря 2011 в 15:29, курсовая работа
Актуальность в теме капиллярные явления заключается в том, что эти явления очень распространены. И если внимательно посмотреть, то можно их увидеть, даже невооруженным глазом. Просто мы не знаем, что эти явления называются капиллярными.
Введение………………………………………………………………………… 3
Глава 1. Теоретические основы капиллярного поднятия жидкости
1.1. Поверхностное натяжение σ жидкостей………………………… 6
1.2. Краевой угол смачивания. Мениск……………………………… 11
1.3. Смачивание. Несмачивание……………………………………… 13
1.4. Капиллярные явления……………………………………………. 19
1.5. Силы, возникающие на кривой поверхности жидкости……….. 22
Глава 2. Капиллярное поднятие жидкости……………………………….. 27
2.1. Жидкость. Капиллярное поднятие в узкой трубке. Формула Жюрена………………………………………………………………………….. 28
2.2. Уравнение Кельвина………………………………………………. 31
Глава 3. Общие вопросы методики преподавания физики
3.1. Методика преподавания физики, как педагогическая наука……… 32
3.2. Методы исследования, применяемые в методике преподавания физики…………………………………………………………………………… 34
3.3. Структура и содержание курса физики……………………………. 35
3.4. Проблемное обучение физики……………………………………….. 38
Глава 4. Изучение капиллярных явлений жидкостей в школе………… 40
Глава 5. Опыт с капиллярным поднятием жидкости……………………. 43
Заключение…………………………………………………………………….. 48
Список использованной литературы………………………………………. 49
Курсовая Айнаш 2009.doc
Fx = 2σlx = ∆Us . (5)
При перемещении перемычки на рис.3 площадь свободной поверхности жидкости возрастает на ∆S = 2lx, так как пленка имеет две свободные поверхности. Поскольку рассматриваемое медленное изменение поверхности, при котором в каждый момент имеется равновесие сил, является обратимым, то поверхностную энергию можно считать потенциальной [2].
Если, изменение поверхности S осуществляется при постоянной температуре, т.е. изотермически (и обратимо), то, потребная для этого работа равна изменению свободной энергии F поверхности
Рис. 3. Силы поверхностного натяжения.
Если изменение поверхности жидкости произвести адиабатно, то ее температура изменится, например, увеличение поверхности приведет к ее охлаждению. Значит, избыточная потенциальная энергия поверхности жидкости, о которой говорилось выше, является свободной энергией поверхности и, следовательно,
т.е. коэффициент поверхностного натяжения жидкости можно определить как свободную энергию единицы площади этой поверхности (см. формулу 3).
Теперь ясно, в чем заключаются указанные выше особые условия, в которых находится поверхность жидкости. Они заключаются в том, что поверхность жидкости обладает избыточной по сравнению с остальной массой жидкости потенциальной (свободной) энергией.
Посмотрим, к чему это приводит.
Известно, что всякая система при равновесии находится в том из возможных для нее состояний, при котором ее энергия имеет минимальное значение. Применительно к рассматриваемому случаю это означает, что жидкость в равновесии должна иметь минимально возможную поверхность. Это в свою очередь означает, что должны существовать силы, препятствующие увеличению поверхности жидкости, т.е. стремящиеся сократить эту поверхность. Очевидно, что эти силы должны быть направлены вдоль самой поверхности, по касательной к ней.
Жидкость ведет себя так, как будто по касательной к ее поверхности действуют силы, сокращающие (стягивающие) эту поверхность. Эти силы называются силами поверхностного натяжения [3].
В живых организмах поверхностное натяжение клетки – один из факторов, определяющих форму целой клетки и её частей. У клеток, лишённых прочной мембранной структуры (большинство клеток животных, некоторые простейшие, сферопласты бактерий), поверхностное натяжение в основном определяет конфигурацию (клетки, находящиеся во взвешенном в жидкости состоянии, приобретают форму, близкую к сферической). Форма клетки, прикрепленной к какому-либо субстрату или к др. клеткам, зависит преимущественно от др. факторов – цитоскелета, образуемого микротрубочками, контактных структур и т.д. Полагают, что локальные изменения поверхностное натяжение существенны в таких явлениях, как фагоцитоз , пиноцитоз , гаструляция . Определение поверхностное натяжение клетки – сложная экспериментальная задача; обычно поверхностное натяжение клетки не превышает несколько дин/см (10 -3 Н/м) [3].
1.2. Краевой угол смачивания. Мениск
Существование краевого угла приводит к тому, что вблизи стенок сосуда наблюдается искривление поверхности жидкости. В узкой трубке или в узком зазоре между двумя стенками искривленной оказывается вся поверхность. Если жидкость смачивает стенки, поверхность имеет вогнутую форму (рис. 4, б), если не смачивает – выпуклую (рис. 4, а). Такого рода изогнутые поверхности жидкости называются менисками.
Мениск – форма поверхности жидкости вблизи стенки сосуда. Мениск зависит от того, смачивает или не смачивает жидкость стенки сосуда.
Для характеристики мениска вводится краевой угол q между смоченной поверхностью стенки и мениском в точках их пересечения. Если q p /2 (рис. 5, а), то жидкость считается не смачивающей стенку, если q > p /2, то жидкость смачивает стенку (рис. 5, б). Кривая поверхность жидкости называется мениском.
Рис. 5, а, Поверхность смачивающей Рис. 5, б, Поверхность несмачивающей жидкости у стенки сосуда жидкости у стенки сосуда
Q - краевой угол. Q - краевой угол
Посмотрев на поверхность смачивающей и несмачивающей жидкостей у стенки сосуда, мы увидим, что поверхность смачивающей жидкости имеет вогнутую форму. Она приподнята у стенок (рис. 4, б), а у несмачивающей — выпуклая, опущенная у стенок сосуда (рис. 4, а). Кривая поверхность жидкости называется мениском.
Рис. 6. Мениски смачивающей жидкости а, б, в,
и несмачивающей жидкости г, д, е .
Появление мениска связано с тем, что молекула жидкости взаимодействуют друг с другом и с частицами твердого тела. Форма мениска обусловливается молекулярными силами. Молекула жидкости, а находится на границе жидкости и стенки сосуда (рис. 6, б, д). Проведем вокруг нее сферу молекулярного действия. Половина сферы приходится на твердое тело, четверть — на жидкость и четверть — на пар. Молекулы твердого тела, заключенные в полусфере, будут действовать на молекулу, а с равнодействующей силой f1, направленной внутрь стенки сосуда, перпендикулярной к ней. Молекулы жидкости, заключенные в нижней четверти сферы, действуют на молекулу, с силой f2 направленной внутрь жидкости под углом 45° к поверхности. Пренебрегая притяжением молекул пара и силой тяжести, действующей на молекулы, найдем по правилу параллелограмма равнодействующую сил F1 и F2. Для смачивающей жидкости равнодействующая F направлена внутрь твердого тела, так как f1 > F2 (рис. 6, в), для несмачивающей жидкости — внутрь жидкости, так как F2 > F1 (рис. 6, е). Молекула, а находится в равновесии только в том случае, если результирующая сила
направлена перпендикулярно к поверхности жидкости (при этом мы пренебрегаем силой тяжести молекулы а, которая пренебрежимо мало по сравнению с силами F1 и F2). Иначе молекула, а перемещалось бы вдоль этой поверхности.
1.3. Смачивание. Несмачивание
Пусть, как показано на рисунке 7, капля жидкости 2 помещена на поверхности другой жидкости, более легкой, (например, масло на воде). Вес капли заставляет ее несколько углубиться в жидкость 1, образуя чечевицу.
Заметим, однако, что далеко не всегда капли одной жидкости на поверхности другой образуют чечевицу. Так, например, бензин и керосин на поверхности воды образуют не чечевицу, а тонкие пленки с цветными радужными пятнами.
Рассмотрим, при каких условиях образуется чечевица, и при каких - тонкая пленка.
Из рисунка 7 видно, что в рассматриваемом случае друг с другом граничат следующие среды:
жидкость 1 граничит с жидкостью 2;
жидкости 1 и 2 граничат со средой 3;
среда 3 — это смесь паров жидкостей 1 и 2 с воздухом, если опыт проводится на воздухе. Впрочем, присутствие газообразной среды существенной роли не играет.
Границей соприкосновения трех сред является окружность, ограничивающая чечевицу. На элемент длины dl этой окружности действуют три силы поверхностного натяжения:
F — сила на границе между жидкостями 1 и 2;
Каждая из них направлена по касательной к поверхности соприкосновения соответствующих двух сред; s 12 , s 13 и s 23—соответствующие коэффициенты поверхностного натяжения (практически можно считать, что s 13 = s 1 и s 23= s 2 поскольку газообразная среда мало влияет на поверхностную энергию жидкостей).
Условием равновесия является обращение в нуль равнодействующих всех сил, действующих на элемент dl:
Возведя оба равенства в квадрат и сложив их, получим
Обозначив q 1+ q 2 = q, , получим
Углы q 1 и q 2, т.е. углы между касательными к поверхностям капли жидкости 2 и поверхностью жидкости 1, с которой она соприкасается, называются краевыми углами [3].
Угол q между касательными поверхности жидкости и поверхности твердого тела называется краевым углом [11].
Физически это означает, что сила F13 по величине больше равнодействующей сил F12+ F23, т.е.
Из рисунка 7 видно, что результирующая сила в этом случае направлена так, что она растягивает каплю.
На границе жидкость — твердое тело уже нельзя не считаться с силами притяжения между молекулами жидкости и молекулами твердого тела. Более того, в ряде случаев сила притяжения между молекулами жидкости и твердого тела оказывается больше силы притяжения между молекулами самой жидкости. В этом случае про жидкость говорят, что она смачивает твердое тело. Если силы притяжения между молекулами жидкости больше сил притяжения молекул твердого тела и молекул жидкости, то такая жидкость называется несмачивающей.
Так, стекло смачивается водой, но не смачивается ртутью. Значит, сила притяжения между молекулами воды и молекулами стекла больше силы притяжения молекул воды. В случае ртути и стекла силы притяжения между молекулами ртути и стекла малы по сравнению с силами притяжения между молекулами ртути.
Это подтверждает следующий опыт. Подвесим на чашке весов с укороченным подвесом чистую стеклянную пластинку и подведем под нее снизу сосуд с водой. Соприкасаясь с водой, пластинка смачивается и удерживается ею. Чтобы оторвать пластинку от воды, надо на другую чашку весов положить небольшой груз (рис. 7.14, а).

Нижняя часть оторвавшейся пластинки оказывается покрытой водой (рис. 7.14, б). Это доказывает, что разрыв произошел не между поверхностями пластинки и воды, а между слоями воды. Следовательно, сила притяжения молекул стекла и молекул воды больше силы притяжения молекул воды друг к другу.
Если мы приведем ту же стеклянную пластинку в соприкосновение не с водой, а со ртутью, то при этом нижняя часть пластинки останется чистой (рис. 7.14, в). Это означает, что взаимодействие между молекулами ртути сильнее, чем взаимодействие между молекулами стекла и ртути. Здесь можно привести аналогию с растягиваемой цепью, которая рвется там, где у нее самое слабое звено.
Отличить смачивающую жидкость от несмачивающей очень просто. Для этого достаточно нанести каплю жидкости на поверхность твердого тела. Если жидкость смачивает тело, то капля растекается по поверхности, несмачивающая жидкость не растекается (рис, 7.15).

Форма поверхности жидкости в том месте, где она соприкасается с твердой стенкой и газом, зависит от того, смачивает или не смачивает жидкость стенки сосуда. Если жидкость является смачивающей, то угол Θ между касательной к поверхности жидкости и твердым телом на общей границе трех сред, отсчитываемый внутрь жидкости (краевой угол), острый (рис. 7.16, а). В том случае, когда жидкость не смачивает твердое тело, краевой угол Θ тупой (рис. 7.16, б). В случае полного смачивания Θ = 0°, а полного несмачивания — Θ = 180°.

Только удаленная от стенок сосуда часть поверхности жидкости горизонтальна. Сближая противоположные стенки (беря более узкий сосуд), мы будем сокращать горизонтальную часть свободной поверхности жидкости (рис. 7.17, а, б), пока наконец она не исчезнет совсем (рис. 7.17, в). Поверхность жидкости становится изогнутой. Изогнутая поверхность жидкости называется мениском (от греческого слова menisos — лунный серп).

В узких трубках смачивающие жидкости имеют вогнутый мениск (см. рис. 7.17, в), несмачивающие — выпуклый (рис. 7.18).

В узких трубках при полном смачивании (или несмачивании) мениск жидкости представляет собой полусферу, радиус которой равен радиусу г канала трубки. Если смачивание (или несмачивание) неполное, то мениск жидкости в узких трубках также принимают за часть сферы, радиус которой R связан с радиусом трубки соотношением r = R cos Θ (рис. 7.19).

Смачивание имеет важное значение в промышленности и быту. Хорошее смачивание необходимо при крашении и стирке, обработке фотографических материалов, нанесении лакокрасочных покрытий и др.
Моющие свойства мыла и синтетических порошков объясняются тем, что мыльный раствор имеет меньшее поверхностное натяжение, чем вода. Большое поверхностное натяжение воды мешает ей проникать в промежутки между волокнами ткани и в мелкие поры.
Склеивание деревянных, кожаных, резиновых и других материалов также пример использования свойства смачивания. Пайка тоже связана со свойствами смачивания и несмачивания. Чтобы расплавленный припой (например, сплав олова со свинцом) хорошо растекался по поверхностям спаиваемых металлических предметов и прилипал к ним, надо эти поверхности тщательно очищать от жира, пыли, оксидов. Оловянным припоем хорошо можно паять детали из меди, латуни. Но алюминий не смачивается оловянным припоем. Для пайки алюминиевых изделий применяют специальный припой, состоящий из алюминия и кремния.
Важный пример применения явления смачивания и несмачивания — флотационный процесс обогащения руд. Для этой цели руду измельчают так, что кусочки ценной породы теряют связь с ненужной примесью. Затем полученный порошок взбалтывают в воде, в которую добавляют маслообразные вещества. Масло обволакивает (смачивает) ценную породу, но не пристает к примесям (не смачивает их). В полученную взвесь вдувают воздух. Пузырьки воздуха прилипают к несмачивающимся водой (вследствие покрытия масляной пленкой) кусочкам ценной породы. Это происходит потому, что тонкий слой воды между пузырьками воздуха и масляной пленкой, обволакивающей ценную породу, стремясь уменьшить свою поверхность, обнажает поверхность масляной пленки (подобно тому как вода на жирной поверхности собирается в капли, обнажая эту поверхность). Крупицы ценной породы вместе с прилипшими к ним пузырьками воздуха под действием архимедовой силы поднимаются вверх, в то время как ненужные примеси оседают на дно (рис. 7.20).

Вода смачивает поверхности одних твердых тел (прилипает к ним) и не смачивает поверхности других. Эти свойства воды определяют множество полезных и просто любопытных явлений.
Разделы: Физика
Класс: 10
Цели урока:
- продолжить изучение темы смачивание, капиллярные явления;
- объяснить формулы по определению смачивания и капиллярным явлениям;
- продолжить формирование естественнонаучных представлений по изучаемой теме;
- создавать условия для формирования познавательного интереса, активности учащихся;
- способствовать развитию конвергентного мышления;
- формирование коммуникативного общения.
Оборудование: интерактивный комплекс SMART Board Notebook, на каждом столе лежит “Сборник по физике” Г. Н. Степановой.
Метод ведения урока: беседа с использованием интерактивного комплекса SMART Board Notebook.
План урока:
- Оргмомент
- Проверка знаний, их актуализация (методом фронтального опроса)
- Изучение нового материала (каркасом нового материала является презентация)
- Закрепление
- Рефлексия
Ход урока
Смачивание. Капиллярные явления
Рассмотрим вопрос смачивания и несмачивания жидкостями твёрдых тел. Жидкость, которая растекается тонкой плёнкой по данному телу, смачивает поверхность. Жидкость, которая не растекается по поверхности твёрдого тела, а собирается в каплю, не смачивает данное тело. Вода смачивает чистое стекло, но не смачивает парафин. Ртуть не смачивает стекло, но смачивает алюминий.
Объяснить явление несложно: если силы притяжения между молекулами жидкости и твёрдого тела больше, чем между молекулами жидкости, то возникает смачивание. Если силы притяжения между молекулами жидкости больше, чем между молекулами жидкости и твёрдого тела, то возникает несмачивание.
Смачивание - явление, возникающее вследствие взаимодействия молекул жидкости с молекулами твердых тел и приводящее к искривлению поверхности жидкости на границе с твердым телом.
Смачивание бывает двух видов:
1. Иммерсионное (вся поверхность твёрдого тела контактирует с жидкостью)
2. Контактное (состоит из 3х фаз - твердая, жидкая, газообразная)
Смачивание зависит от соотношения между силами сцепления молекул жидкости с молекулами (или атомами) смачиваемого тела (адгезия) и силами взаимного сцепления молекул жидкости (когезия).
Степень смачивания характеризуется углом смачивания. Угол смачивания (или краевой угол смачивания) это угол, образованный касательными плоскостями к межфазным поверхностям, ограничивающим смачивающую жидкость, а вершина угла лежит на линии раздела трёх фаз. Измеряется методом лежащей капли. Надёжных методов, дающих высокую степень воспроизводимости, пока не разработано. Предложен весовой метод определения степени смачивания, но он пока не стандартизован.
Измерение степени смачивания весьма важно во многих отраслях промышленности ( лакокрасочная, фармацевтическая, косметическая и т.д.). К примеру, на лобовые стёкла автомобилей наносят особые покрытия, которые должны быть устойчивы против разных видов загрязнений. Состав и физические свойства покрытия стёкол и контактных линз можно сделать оптимальным по результатам измерения контактного угла.
К примеру, популярный метод увеличения добычи нефти при помощи закачки воды в пласт исходит из того, что вода заполняет поры и выдавливает нефть. В случае мелких пор и чистой воды это далеко не так, поэтому приходится добавлять специальные ПАВ. Оценку смачиваемости горных пород при добавлении различных по составу растворов можно измерить различными приборами.
Капиллярные явления
Попробуем получить формулу для расчёта h. Результирующая сила поверхностного натяжения Fн должна уравновешиваться силой тяжести Fт столба жидкости в капилляре:
Капиллярные явления можно наблюдать не только в трубках, но и в узких щелях. Если опустить в воду две стеклянные пластины так, чтобы между ними образовалась узкая щель, то вода между пластинами поднимется, и тем выше, чем ближе они расположены. Капиллярные явления играют большую роль в природе и технике. Множество мельчайших капилляров имеется в растениях. В деревьях по капиллярам влага из почвы поднимается до вершин деревьев, где через листья испаряется в атмосферу. В почве имеются капилляры, которые тем уже, чем плотнее почва. Вода по этим капиллярам поднимается до поверхности и быстро испаряется, а земля становится сухой. Ранняя весенняя вспашка земли разрушает капилляры, т. е. сохраняет подпочвенную влагу и увеличивает урожай.
Роль в жизни человека
В технике капиллярные явления имеют огромное значение, например, в процессах сушки капиллярно-пористых тел и т. п. Большое значение капиллярные явления имеют в строительном деле. Например, чтобы кирпичная стена не сырела, между фундаментом дома и стеной делают прокладку из вещества, в котором нет капилляров. В бумажной промышленности приходится учитывать капиллярность при изготовлении различных сортов бумаги. Например, при изготовлении писчей бумаги ее пропитывают специальным составом, закупоривающим капилляры. В быту капиллярные явления используют в фитилях, в промокательной бумаге, в перьях для подачи чернил и т. п.
Роль в природе
Роль поверхностных явлений в природе разнообразна. Например, поверхностная плёнка воды является для многих организмов опорой при движении. Такая форма движения встречается у мелких насекомых и паукообразных. Наиболее известны водомерки, опирающиеся на воду только конечными члениками широко расставленных лапок. Лапка, покрытая воскообразным налётом, не смачивается водой, поверхностный слой воды прогибается под давлением лапки, образуя небольшое углубление. Подобным образом перемещаются береговые пауки некоторых видов, но их лапки располагаются не параллельно поверхности воды, как у водомерок, а под прямым углом к ней. Некоторые животные, обитающие в воде, но не имеющие жабер, подвешиваются снизу к поверхностной плёнке воды с помощью не смачивающихся щетинок, окружающих их органы дыхания. Этим приёмом “пользуются” личинки комаров (в том числе и малярийных).
Перья и пух водоплавающих птиц всегда обильно смазаны жировыми выделениями особых желёз, что объясняет их непромокаемость. Толстый слой воздуха, заключённый между перьями утки и не вытесняемый оттуда водой, не только защищает утку от потери тепла, но и чрезвычайно увеличивает запас плавучести, действуя подобно спасательному поясу.
Воскообразный налёт на листьях препятствует заливанию так называемых устьиц, которое могло бы привести к нарушению правильного дыхания растений. Наличием того же воскового налёта объясняется водонепроницаемость соломенной кровли, стога сена и т.д. Большинство растительных и животных тканей пронизано громадным числом капиллярных сосудов. Именно в капиллярах происходят основные процессы, связанные с дыханием и питанием организма, вся сложнейшая химия жизни тесно связана с диффузионными явлениями. Стволы деревьев, ветви и стебли растений пронизаны огромным числом капиллярных трубочек, по которым питательные вещества поднимаются до самых верхних листочков. Корневая система растений оканчивается тончайшими нитями-капиллярами. И сама почва, источник питания для корня, может быть представлена как совокупность капиллярных трубочек, по которым в зависимости от структуры и обработки быстрее или медленнее поднимается к поверхности вода с растворёнными в ней веществами. Высота подъёма жидкости в капиллярах тем больше, чем меньше его диаметр. Отсюда ясно, что для сохранения влаги надо почву перекапывать, а для осушения – утрамбовывать.
Читайте также:


