Ревматизм на нервной почве
Ревматические болезни относятся к группе заболеваний, которые характеризуются развитием аутоиммунных процессов против антигенов почти всех органов и тканей организма, что сочетается с образованием аутоантител с органонеспецифическими с
Ревматические болезни относятся к группе заболеваний, которые характеризуются развитием аутоиммунных процессов против антигенов почти всех органов и тканей организма, что сочетается с образованием аутоантител с органонеспецифическими свойствами.
Аутоиммунные процессы осуществляют информационный обмен между нейроэндокринной и иммунной системами, при этом главную роль играют аутоантитела к гормонам, медиаторам и их рецепторам. Продемонстрирован синтез нейропептидов в иммунокомпетентных клетках, а в клетках нейроэндокринной системы доказана возможность синтеза лимфокинов и монокинов.
Функционирование клеток и сигнальная информация обеспечиваются медиаторами и нейротрансмиттерами в обеих системах, между нервной и иммунной системой происходит взаимообмен информацией с помощью цитокинов, стероидов и нейропептидов [1, 2].
Таким образом, доказана общность и взаимосвязь нервной и иммунной систем, сходство между их структурами и функциями и развитие нового направления современной иммунологии — нейроиммунологии [3, 4]. Широкий диапазон неврологических синдромов при аутоиммунных системных заболеваниях позволяет рассматривать их как модельные системы для изучения патогенетической роли иммунных механизмов поражения центральной и периферической нервной системы [5].
Потенциальными мишенями для аутоиммунной агрессии могут быть различные антигены нервной ткани, включая миелин, в том числе ассоциированный с гликопротеином, и его основной белок, ганглиозиды, белок ядер нейрональных клеток и другие [6]. Так, мишеневидные антигены при нейролюпусе представлены антигенами нейрональной ткани, рибосомальным Р-белком, рДНК, малым ядерным рибонуклеопротеидом, а также анионными фосфолипидами при антифосфолипидном синдроме, что обуславливает широкий спектр неврологической симптоматики при данной патологии [7, 8].
По данным различных авторов, частота поражений нервной системы при ревматических заболеваниях (РЗ) колеблется от 40% до 70% и выше, если учитывать психические синдромы и головную боль. Неврологические синдромы включены в классификационные критерии системных васкулитов, опубликованные Американской коллегией ревматологии в 1990 году, в диагностические критерии и критерии активности системной красной волчанки (СКВ), а также в ряд других диагностических критериев, в частности узелкового полиартериита у детей. Неврологические нарушения при РЗ требуют проведения дифференциальной диагностики и назначения адекватного лечения совместно ревматологом и неврологом.
При СКВ в диагностические критерии неврологических поражений включены судороги или психозы. Поражение ЦНС обусловлено в основном сосудистой патологией, к которой относят васкулопатию, тромбозы, истинные васкулиты, инфаркты и геморрагии [7]. В цереброспинальной жидкости обнаруживаются антинейрональные антитела, определяется повышение уровня белка, увеличение клеточного состава. Описаны разные виды судорожных припадков: большие, малые, по типу височной эпилепсии, а также гиперкинезы. При ЦНС-люпусе имеет место головная боль типа мигрени, устойчивая к анальгетикам, но отвечающая на лечение глюкокортикостероидами. Параличи черепных нервов обычно сопровождаются офтальмоплегией, мозжечковыми и пирамидными симптомами и нистагмом. Имеют место зрительные нарушения, преходящие нарушения мозгового кровообращения. Острый поперечный миелит встречается редко и имеет неблагоприятный прогноз. Психические синдромы разнообразны и характеризуются аффективными, органическими мозговыми или шизофреноподобными проявлениями [9, 10].
В рамках СКВ был описан и антифосфолипидный синдром. Этот синдром включает: рецидивирующие артериальные или венозные тромбозы, привычное невынашивание беременности и тромбоцитопению и дополнительные признаки: сетчатое ливедо, неврологические проявления: хорею, эпилепсию, мигренеподобную головную боль, нарушения мозгового кровообращения и деменцию вследствие множественных инфарктов, хронические язвы голеней, Кумбс-положительную гемолитическую анемию, клапанные поражения сердца и серологические маркеры — антифосфолипидные антитела, к которым относятся антикардиолипиновые антитела IgG и IgM и волчаночный антикоагулянт [11].
При системной склеродермии (ССД) неврологический синдром представлен в основном полиневритическими проявлениями, связанными с сосудистыми изменениями и фиброзными процессами в соединительной ткани. Для узелкового полиартериита характерны множественные мононевриты, для гранулематоза Вегенера — асимметричная полинейропатия, для неспецифического аортоартериита — дисциркуляторная энцефалопатия и нарушения мозгового кровообращения.
Собственные данные включали обследование 229 больных различными формами РЗ, среди которых 110 больных страдали системными заболеваниями соединительной ткани: 88 больных СКВ, 22 — ССД и 119 больных — системными васкулитами: облитерирующий тромбангиит (ОТ) — 21, узелковый полиартериит (УП) — 27, неспецифический аортоартериит — (НАА) — 32, геморрагический васкулит (ГВ) — 15 и гранулематоз Вегенера (ГрВ) — 2, другие формы — 22. Проведено детальное неврологическое исследование, ультразвуковая транскраниальная допплерография сосудов мозга, реоэнцефалография, компьютерная (КТ) и магнитно-резонансная томография (МРТ) головного мозга, электроэнцефалография, исследование иммунного статуса.
У большинства больных заболевания дебютировали кожным (50,6%), суставно-мышечным (35,4%) и сосудистым (27,1%) синдромом. Органные поражения в дебюте регистрировались с частотой 7%, синдром артериальной гипертензии — у 5,2%, лихорадка — у 7,0%, гематологические нарушения — 7,9%. Неврологические расстройства в дебюте заболевания отмечены у 12,2% и проявлялись моно- и полиневропатией и синдромом энцефаломиелополирадикулоневрита (ЭМПРН). Поражение периферической нервной системы в дебюте заболевания было особенно характерно для УП и наблюдалось у 30% больных. Основными синдромами дебюта со стороны ЦНС был цефалгический (10,5%) и вестибулярный (6,3%), чаще они наблюдались при НАА. Вовлечение ЦНС имело место у 96 (41,9%) больных, являясь наиболее выраженным при СКВ, НАА, УП.
Цереброваскулярная патология была доминирующей в клинической картине болезни у 34,7% больных, а иногда разнообразные симптомы поражения ЦНС развивались задолго до появления полисиндромной картины заболевания. Основные клинические проявления цереброваскулярной патологии включали: цефалгический (82%), астенический (76%), вестибулярно-атактический (80%), пирамидный (74%) синдромы, синдром вегетативно-сосудистой недостаточности (69%), диссомнический (79%) и базально-оболочечный (37%), гипопоталамической дисфункции (34,7%).
Описанная неврологическая симптоматика часто сочеталась с симптомами сосудистой недостаточности головного мозга, которые объединялись синдромом дисциркуляторной энцефалопатии 1 (11%), 2 (26,4%) или 3 (8%) степени. У 7,8% больных имели место преходящие нарушения мозгового кровообращения.
Гипоталамическая дисфункция у больных РЗ проявлялась полиморфными нейроэндокринными расстройствами, нарушением терморегуляции, преимущественно по типу пароксизмальной центральной гипертермии, инсомнией, патологией психоэмоциональной сферы.
Установлено достоверное преобладание у больных пирамидной недостаточности слева (41%). Преобладание пирамидной недостаточности справа регистрировалось реже (23,7%). Дистонические феномены в форме вестибулярно-мозжечковой установки кисти и диссоциированная мышечная гипотония в ногах также были более выражены слева. Полученные данные свидетельствуют о преобладающем поражении пирамидной и сенсорной систем, а также неспецифических структур правого полушария, которое тесно связано с гипоталамической областью и обеспечивает адаптацию организма к воздействующим факторам внешней среды. Обнаруженная функциональная асимметрия свидетельствует о срыве адаптационных механизмов нервной системы и указывает на роль дисфункции правополушарно-гипоталамической системы.
При использовании методов МРТ и/или КТ было выявлено изменение желудочковой системы в виде ее расширения или деформации и/или расширения субарахноидального пространства, а также очаговые поражения различных структур головного мозга, атрофия вещества мозга и краниовертебральные аномалии. Признаки наружной, внутренней или сочетанной гидроцефалии отмечались при всех нозологических формах. Очаговые изменения вещества мозга включали гиперденситивные зоны, гиподенситивные зоны с отеком или без него, единичные или множественные.
При исследовании сосудистой системы и мозгового кровообращения достоверно наблюдалось повышение тонуса сосудов, гипертонический и дисциркуляторный тип кровообращения по данным реоэнцефалографии (РЭГ) и увеличение линейной скорости кровотока по средней мозговой артерии. Больные с вовлечением ЦНС отличались по электроэнцефалографии: им были свойственны диффузные патологические изменения, наличие дезорганизации альфа-ритма, дизритмий и пароксизмальной активности.
Корреляционный анализ цереброваскулярной патологии и результатов инструментальных исследований сосудов головного мозга показал, что при всех нозологических формах у пациентов имело место нарушение венозной гемоциркуляции. В последующем происходило сужение церебральных артерий, ликвородинамические нарушения с формированием внутричерепной гипертензии, нарушением системы микроциркуляции в головном мозге. Очаговые поражения головного мозга отличались локализацией процесса в зависимости от нозологической формы. В табл. представлены основные неврологические проявления РЗ.
Среди больных РЗ цереброваскулиты (ЦВ) имели место у 28,3% больных. Диагноз ЦВ ставился при обнаружении очаговой неврологической симптоматики, изменений на глазном дне, снижения зрения, наличии признаков нарушения мозгового кровообращения, а также по результатам КТ и ядерно-магнитно-резонансной томографии (ЯМРТ), при которых выявлялись наружная и внутренняя гидроцефалия, очаговые изменения в коре и субкортикальном веществе. При этом с течением времени число очагов любой локализации в головном мозге нарастало. При магнитно-резонансном ангиографическом (МРА) исследовании отмечались множественные сегментарные неровности сосудистой стенки, циркулярные или эксцентричные стенозы и дилятация мелких и средних интракраниальных артерий с формированием аневризм, нарушения кровотока. Выявленное снижение интенсивности МРА-сигнала на фоне повышения активности ревматического процесса свидетельствовало о наличии ЦВ.
Иммунологическими маркерами ЦВ считали антитела к нативной ДНК, IgG-антитела к кардиолипину (аКЛ) и IgM аКЛ, антинейтрофильные цитоплазматические антитела (АНЦА), в меньшей степени — РФ и волчаночный антикоагулянт (ВА). Имели место клинико-иммунологические корреляции с неврологическими проявлениями.
Изолированный (первичный) ЦВ характеризовался обнаружением симптомов вовлечения ЦНС и такими признаками, как головная боль, судороги, менингеальный синдром, острая прогрессирующая энцефалопатия без признаков экстракраниального или системного васкулита, психические синдромы, деменция, прогрессирующее снижение интеллекта, инсульты, нарушения зрения, нистагм. Чаще перивентрикулярные очаги выявлялись в первый год заболевания.
Ряд больных обращались на консультацию к окулисту в связи с ухудшением зрения, вплоть до амавроза, наличием увеита, ишемического неврита. Ангиопатия сетчатки имела место у 41% этих больных, флебопатия — у 14%, ретиноваскулит — у 6%, ангиоспазм — у 13%, ангиосклероз — у 18%.
Полиневритический синдром встречался у подавляющего большинства больных (96,7%) в виде сенсорной, чувствительно-двигательной полиневропатии или в сочетании с поражениями ЦНС, с синдромом ЭПН и ЭМПРН. При ССД, ОТ и ГВ преобладали формы в виде чувствительной или чувствительно-двигательной полиневропатии, а при СКВ и НАА — формы с сочетанным поражением периферической НС (ПНС) и ЦНС — синдромы ЭПН и ЭМПРН. При ОТ и НАА отмечалась отчетливая диссоциация степени выраженности полиневропатии по оси тела, причем при ОТ симптоматика была более отчетливой в ногах, при НАА — в руках. В целом асимметричная полиневропатия имела место у 19,2% больных, достигая максимума при УП (59,3%).
Патология НС при РЗ нередко определяет прогноз, клиническую картину заболевания и качество жизни больных, а также требует обязательного сочетанного применения базисной противовоспалительной терапии, ангио- и нейропротекторов. К группе нейропротекторов относят Актовегин, Инстенон. Используются препараты, улучшающие мозговое кровообращение, — Винпоцетин, Кавинтон, метаболические средства с антигипоксантным действием — Ноотропил, Пирацетам, Церебролизин, по показаниям седативные и противосудорожные средства, антидепрессанты.
При РЗ терапия включает глюкокортикостероиды, иммуносупрессанты, иммуноглобулин, плазмаферез, иммуномодуляторы, дезагреганты, нестероидные противовоспалительные препараты и симптоматические средства.
Лечение состоит из нескольких этапов: быстрое подавление иммунного ответа в дебюте заболевания и при его обострениях (индукция ремиссии); длительная поддерживающая терапия иммуносупрессантами, в дозах, достаточных для достижения клинической и лабораторной ремиссии заболевания; определение степени повреждения органов или систем организма и их коррекция, проведение последующих реабилитационных мероприятий.
Первый этап включает эффективное подавление иммунного воспаления на ранних стадиях болезни и предполагает использование глюкокортикостероидов, иммуносупрессантов цитостатического действия типа Циклофосфана и антиметаболитного действия типа Метотрексата, цитокинсупрессивного препарата Циклоспорина А, внутривенного иммуноглобулина, назначение повторных курсов пульс-терапии метилпреднизолоном и Циклофосфаном, в сочетании с экстракорпоральными методами лечения.
При острых церебральных нарушениях при высокой активности СКВ используется схема пульс-терапии с введением Метипреда 1 г внутривенно 1 раз в день в течение 3 дней и с добавлением 800 мг Циклофосфана во 2-й день. При хроническом течении СКВ суточная доза преднизолона составляла 15–20 мг с последующим постепенным снижением, Циклофосфан применяется внутримышечно в дозе 400 мг в неделю до 1600–2000 мг на курс, затем по 200 мг в неделю в течение года и более. Апробируются препараты мофетила микофенолат и лефлуномид.
При патологии органа зрения назначают нестероидные противовоспалительные препараты в виде инъекций диклофенака, а затем пероральные препараты этой группы, дезагреганты, при наличии признаков воспалительной активности добавляют умеренные дозы глюкокортикостероидов, а при резком снижении зрения и выраженных признаках активности используют пульс-терапию.
Проводится определение наиболее эффективных и менее токсичных схем применения иммуносупрессивных препаратов, путей их введения, и включение в комплексное лечение больных препаратов, улучшающих микроциркуляцию и/или влияющих на реологические свойства крови (Гепарин, Фраксипарин, Трентал, Ралофект, Тиклид).
В ряде случаев назначают препараты типа Реаферона, а при наличии инфицированных язв, некрозов кожи или конечностей применяют антибиотики. Ввиду многообразия нозологических форм на выбор лекарственных средств в дебюте заболевания оказывает влияние распространенность патологического процесса и наличие интеркуррентной инфекции. Показано назначение ангиопротекторов и посиндромная терапия.
Учитывая высокий удельный вес неврологической патологии, больные РЗ должны проходить комплексное клинико-инструментальное неврологическое исследование уже на ранней стадии патологического процесса. Постановка диагноза РЗ и комплексная терапия глюкокортикостероидами и иммуносупрессантами способствуют коррекции нарушений ЦНС и ПНС.
Стрессы не проходят бесследно для организма. Суставы тоже страдают от такого воздействия. Изменения в работе нервной системы под влиянием шока нарушают осанку человека, вызывают гипертонус и спазм в мышцах, нарушают циркуляцию крови. Это отзывается болевым синдромом в теле и развитием остеохондроза, артроза или артрита. Лечение индивидуально и комплексно. Медицинские препараты устраняют только симптомы заболеваний, но без борьбы со стрессом они не избавляют от недуга.

Может ли болеть сустав на нервной почве?
Появления болевого синдрома в опорно-двигательном аппарате развивается по разным причинам. При неврозе самым вероятным недугом, который может развиться, является остеохондроз. Определить первопричину появления боли в коленях, шее, позвоночниках, локтях фактически невозможно. Но медики утверждают, что вполне вероятно чувствовать боль в мышцах при неврозе. Каждый 3-й житель планеты с артрозом получает этот недуг от воздействия стрессового фактора.
Артрит, ревматизм, хондроз, артроз и другие суставные недуги могут быть спровоцированными или усиленными стрессом, особенно при сильном шоке или длительном нервном перенапряжении. Нередко болят ноги, руки, спина после пережитого морального потрясения.
Механизм развития боли на нервной почве
При депрессии или психоэмоциональном перенапряжении увеличивается давление на корешки нервных волокон в суставных тканях. Из-за стресса нарушается кровообращение, и сустав начинает болеть. Если речь идет об осанке, то физиологически человек сжимается при ощущении стресса. Мышцы шеи и поясницы начинают характерно сокращаться вызывая сколиоз. Смещение позвоночных дисков и деформация скелета от нервов провоцирует остеохондроз. Все это вызывает спазмирование мышечных и хрящевых тканей, из-за чего могут болеть колени, локти, шейный отдел.
Иммунитет на нервной почве снижается, а риск попадания и развития инфекции в организме увеличивается. Таким образом может развиться артрит. Длительная депрессия вызывает усиленную выработку кортикостероидных гормонов, большое количество которых понижает концентрацию гиалуроновой кислоты. Суставы не получают необходимой смазки, уменьшается их эластичность, функциональность, усиливается трение, что провоцирует воспалительные процессы и боли в мышцах. При ВСД (веготососудистой дистонии) характерно развитие гипертонуса и спазма мышц, которые зажимают суставы, провоцируя их деформацию.
Какие болезни могут развиваться?
Нервные стрессы склонны вызывать:
- хондроз;
- остеохондроз;
- артроз;
- артрит;
- коксартроз;
- ревматизм;
- сколиоз.
Боли в суставах не возникают без причины. Они являются предвестниками или сигналами о развитии заболевания опорно-двигательной системы. Изменения в осанке, нарушения кровообращения, гормональный дисбаланс негативно воздействуют на общее состояния здоровья. Психологические сбои провоцируют частые головные боли, быструю утомляемость, ломоту и зажимы в теле.
Особенности лечения
Симптомы заболевания устраняются с помощью медицинских препаратов, массажей или средств народной медицины. Но вылечить болящие суставы на нервной почве может только искоренение причины развития. Главным помощником в борьбе против стресса является спорт. Лечебная физкультура, гимнастика, йога, упражнения, одобренные доктором, помогут не только укрепить осанку и восстановить двигательные функции, но и переключить нервную систему от стресса. Немаловажным фактором в лечении является правильный режим сна, питание и отказ от вредных привычек, которыми люди заглушают нервозность (алкоголь, табак, жирная пища). Нужно чаще гулять на свежем воздухе, заняться медитацией, а в особо сложных случаях обратиться за помощью к психологу.
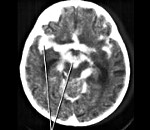
Нейроревматизм — ревматический процесс в тканях центральной и периферической нервной системы. Проявляется симптоматикой энцефалита, менингита, миелита, арахноидита, радикулита, неврита. Ведущая клиническая форма — малая хорея. Нейроревматизм диагностируется неврологом и ревматологом с учётом данных лабораторных исследований, электроэнцефалографии, КТ/МРТ церебральных структур, исследования ликвора. Лечение включает терапию ревматизма, противоотёчные средства, психотропные, противоэпилептические, антигиперкинетические препараты.

- Причины нейроревматизма
- Патогенез
- Классификация
- Симптомы нейроревматизма
- Осложнения
- Диагностика
- Лечение нейроревматизма
- Прогноз и профилактика
- Цены на лечение
Общие сведения

Причины нейроревматизма
Этиологическим фактором возникновения ревматизма выступает инфекционный процесс, обусловленный β-гемолитическим стрептококком (ангина, острый пиелонефрит, фарингит). В своей структуре возбудитель имеет антигены, сходные с отдельными элементами соединительной ткани организма человека. В отдельных случаях выработка антител к стрептококку сопровождается сбоем в работе иммунной системы, приводящим к продуцированию аутоантител к компонентам собственной соединительной ткани. Развивается аутоиммунное воспаление с вовлечением стенок сосудов, сердечных клапанов, внутрисуставных и околосуставных тканей, нервных структур.
Ревматизм возникает у 0,3-3% переболевших стрептококковой инфекцией. Предрасполагающими факторами выступают:
- Молодой возраст — пик заболеваемости приходится на период 7-15 лет.
- Дисфункция иммунной системы с наклонностью к аутоиммунным процессам.
- Отягощённая наследственность — наличие ревматизма у ближайших родственников
- Женский пол — женщины заболевают в 3 раза чаще мужчин.
Патогенез
Нейроревматизм с поражением периферической НС связан с продукцией антител к соединительнотканным элементам спинальных корешков и нервных стволов. Ревматическое поражение ЦНС обусловлено церебральным васкулитом, воспалительными изменениями мозговых тканей. Васкулит характеризуется утолщением сосудистых стенок, периваскулярным отёком, диапедезными кровоизлияниями, микротромбированием. Поражение сосудов приводит к затруднению венозного оттока, ишемии тканей мозга. Одновременно наблюдаются воспалительные изменения в мозговых оболочках (утолщение, повышенное кровенаполнение, геморрагии), подкорковых структурах (глиоз, дегенеративные процессы), мозговом веществе, диэнцефальной области. Особенности клинической картины зависят от преимущественного вовлечения того или иного отдела головного мозга. В подавляющем числе случаев нейроревматизм протекает с поражением подкорковых узлов (полосатого тела, хвостатого ядра), клинически проявляющемся симптомами малой хореи.
Классификация
Классифицирование ревматических поражений НС основано на их клиникоморфологических особенностях. Иногда наблюдаются комбинации различных вариантов нейроревматизма с преобладанием одного из компонентов. В соответствии с классификацией выделяют две формы заболевания – с поражением периферической и центральной нервной системы.
Нейроревматизм с поражением ЦНС:
- Энцефалит — диффузное мелкоочаговое воспаление церебральных тканей сочетается с участками размягчения. При преимущественной локализации процесса в полосатом теле развивается самая часто встречающаяся форма нейроревматизма — малая хорея. Преимущественное поражение диэнцефальной области обуславливает возникновение ревматического диэнцефалита.
- Менингит — ревматическое воспаление церебральных оболочек.
- Арахноидит — воспалительные изменения подпаутинной оболочки с образованием спаек, арахноидальных кист.
- Миелит — воспалительные процессы в веществе спинного мозга.
- Эпилептиформный синдром — развивающиеся на фоне ревматизма приступы эпилепсии.
Нейроревматизм с поражением периферической НС:
- Радикулит — аутоиммунное воспаление в области спинномозгового корешка. Может носить множественный характер.
- Неврит — воспаление ствола одного (мононеврит) или нескольких (полиневрит) периферических нервов.
Симптомы нейроревматизма
Клинические проявления полиморфны, зависят от формы патологии. Возникают преимущественно после перенесённой атаки ревматизма. При латентном течении ревматического процесса нейроревматизм может выступать дебютом заболевания.
Ревматический энцефалит манифестирует психоэмоциональными симптомами: раздражительностью, плаксивостью, обидчивостью. Из общемозговых проявлений на первый план выходит головная боль. Затем присоединяются гиперкинезы, которые могут носить характер тиков, хореи, миоклоний, торсионной дистонии. В классическом варианте заболевание характеризуется симптоматикой малой хореи: быстрым хореическим гиперкинезом в мышцах конечностей, мимической мускулатуре с мышечной дистонией, психическими нарушениями, вегетативными симптомами, дискоординацией. Диэнцефалит протекает с гипертермическим синдромом, полидипсией, артериальной гипертензией, гипергидрозом, расстройством ритма сон/бодрствование, нарушениями эмоциональной сферы (страхами, ипохондрией, истерией).
Ревматический менингит проявляется выраженной головной болью, повышенной восприимчивостью к внешним раздражителям, менингеальным синдромом. Арахноидит сопровождается нарушением оттока цереброспинальной жидкости, повышением интракраниального давления с распирающей головной болью, тошнотой, чувством давления на глазные яблоки, зрительными нарушениями, мозжечковой атаксией. Клиника миелита зависит от места поражения спинного мозга, включает центральные и периферические парезы, расстройства чувствительности, нарушения тазовых функций.
Эпилептиформный синдром отличается атипичностью эпилептических пароксизмов, преобладанием малых приступов (абсансов, акинетических пароксизмов). Характерны изменения психики (возбуждение, сумеречное состояние сознания, галлюцинаторный синдром), автоматизмы. В отличие от истинной эпилепсии некоторые пациенты способны чувствовать приближающийся приступ, что позволяет им избежать внезапных падений, травм. Эпилептические эпизоды редки, возникают раз в 2-3 месяца, учащение наблюдается на фоне ухудшения соматического состояния.
Нейроревматизм с поражением спинальных корешков манифестирует корешковым синдромом. Отмечаются боли в позвоночнике и по ходу корешка, выпадения чувствительности, слабость мышечных групп, иннервацию которых обеспечивает поражённый спинномозговой нерв. Вовлечение в ревматический процесс периферического нерва проявляется болью, парестезиями, онемением, мышечной слабостью и гипотонусом. Указанные симптомы локализуются в зоне иннервации поражённого ревматизмом нерва, при множественном характере процесса охватывают несколько областей.
Осложнения
В тяжёлых случаях нейроревматизм осложняется отёком головного мозга. Воспаление при энцефалите, менингоэнцефалите, энцефаломиелите сопровождается экссудативным процессом, приводящим к отёку и набуханию мозгового вещества. Ведущий симптом — прогрессирующее расстройство сознания, приводящее к коме. Без оказания срочной медицинской помощи происходит сдавление церебрального ствола с расположенными в нём витальными центрами, отвечающими за регуляцию дыхания и сердечно-сосудистой деятельности. Возникает парадоксальное дыхание, резкая гипотензия, нарушения сердечного ритма. Возможен летальный исход.
Диагностика
Полиморфизм симптоматики делает нейроревматизм сложным в диагностическом плане заболеванием. Постановка диагноза упрощается при указании в анамнезе на наличие у пациента ревматизма. Диагностические мероприятия включают:
- Осмотр невролога. В 90% случаев нейроревматизм сопровождается нарушениями произвольных движений, рефлекторной сферы, тонуса мышц. Могут отмечаться сенсорные расстройства, признаки вегетативной дисфункции, психические изменения. При невритах и радикулитах определяются болевые точки, зоны гипестезии.
- Люмбальную пункцию. У половины пациентов отмечается повышенное давление ликвора. Исследование цереброспинальной жидкости (ликвора) не обнаруживает явных отклонений, что позволяет исключить острую нейроинфекцию.
- Электроэнцефалографию. Выявляет диффузные изменения в виде дезорганизации ритма, понижения/повышения амплитуды альфа-ритма. Если нейроревматизм протекает с эпилептиформным синдромом, отмечается повышенная эпилептическая активность.
- МРТ/КТ головного мозга. Могут не выявлять патологических изменений, позволяют исключить объёмные образования (кисты, абсцессы, церебральные опухоли). Более информативна МРТ головного мозга с контрастированием, визуализирующая воспалительные очаги по накоплению контраста.
- Консультацию ревматолога. Необходима для диагностики ревматического процесса, его стадии, степени активности. Включает оценку состояния сердца.
- Лабораторную диагностику ревматизма. Проводится клинический анализ крови, определение в крови ревматоидного фактора, С-реактивного белка, АСЛ-О, антистрептокиназы, баночная проба.
В зависимости от клинической формы нейроревматизм приходится дифференцировать от бактериального менингита, клещевого энцефалита, инфекционного миелита, опухолевых процессов в ЦНС, хореи Гентингтона, идиопатической эпилепсии.
Лечение нейроревматизма
Терапия осуществляется преимущественно в стационаре. Пациенту показан постельный режим с большим количеством сна. Рекомендована богатая белками и витаминами пища с ограничением потребляемой жидкости, соли. Основу медикаментозного лечения составляет противоревматическая терапия, на фоне которой проводятся мероприятия по купированию возникшей неврологической симптоматики, психических нарушений. Фармакотерапия включает:
- Антиревматическое лечение: нестероидные противовоспалительные, глюкокортикостероиды, антибактериальные препараты (бициллин). Назначения зависят от активности и стадии ревматизма.
- Дегидратационная терапия. Проводится мочегонными (ацетазоламидом, фуросемидом). Направлена на снижение интракраниального давления, профилактику отёка мозга.
- Купирование гиперкинезов при малой хорее осуществляется хлорпромазином, при других гиперкинезах — бензодиазепинами, холинолитиками. Препарат и доза подбираются индивидуально.
- Витаминотерапию: витамины группы В, аскорбиновую кислоту, рутин.
- Психотропные препараты: нейролептики (галоперидол), транквилизаторы (диазепам), антидепрессанты (амитриптилин), седативные. Показаны при психических нарушениях.
- Антиконвульсанты: препараты вальпроевой кислоты, карбамазепин, фенобарбитал, клоназепам. Назначаются при эпилептиформном синдроме.
Прогноз и профилактика
Исход зависит от своевременности и успешности лечения основного заболевания — ревматизма. На фоне терапии продолжительность малой хореи обычно варьирует в пределах 1-3 мес. При ангине, ОРВИ, беременности возможны рецидивы. Отсутствие специфического лечения чревато усугублением поражений ЦНС, имеет неблагоприятный прогноз. К мерам, способным предупредить нейроревматизм, относятся ранее выявление и корректное лечение первичных форм ревматизма, проведение медикаментозной профилактики рецидивов. В целях вторичной профилактики пациент должен наблюдаться у ревматолога.
Читайте также:


