Реактивный синовит клинические рекомендации
Общие сведения
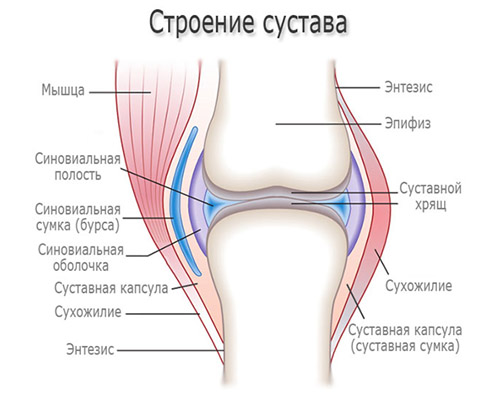
Среди различных проявлений заболеваний суставов одно из ведущих мест занимает синовит, представляющий собой очаговое воспаление синовиальной оболочки, выстилающей внутреннюю поверхность суставов. Синовиальная оболочка вырабатывает синовиальную жидкость, необходимую для нормального функционирования сустава. В ней расположены кровеносные сосуды, обеспечивающие питание хрящевой ткани и обмен веществ в суставе, и нервные окончания.
Характерные клинические проявления заболевания обусловлены воспалительным процессом в синовиальной оболочки и изменением ее структуры и функции (утолщением, снижением растяжимости, продуцированием большого количества экссудата (воспалительной жидкости), которая, скапливаясь в суставной полости, вызывает отек в суставную полость и увеличение размеров (деформацию) сустава.
Именно воспалительный процесс в синовиальной оболочке — это движущая сила прогрессирования деструктивно-дегенеративного процесса в суставах. Синовит, по сути, является предиктором (прогностическим параметром) повреждения хряща. Возникает преимущественно в крупных суставах (синовит коленного сустава и синовит тазобедренного сустава), однако встречается и в относительно мелких суставах (синовит плечевого сустава, голеностопного). Код синовита коленного сустава по МКБ-10: M65. Синовит коленного/тазобедренного сустава встречаются относительно чаще других в силу больших нагрузок на них и более частой травматизации, а также из-за обильного лимфо/кровоснабжения, что способствует заносу с током крови/лимфы различных повреждающих факторов (инфекционные агенты, антитела, иммунные комплексы).
Как правило, синовит развивается в одном суставе, а вовлечение в процесс одновременно нескольких суставов — относительно редкое явление. Синовит может протекать как в острой, так и хронической форме. Острый синовит чаще развивается вследствие травматизации суставов и синовиальной оболочки или на фоне попадания инфекционного агента в полость сустава в результате травм или заноса инфекции из других очагов воспаления в организме гематогенным и лимфогенным путем. Достаточно часто встречается и реактивный синовит. Как правило, реактивный синовит развивается после перенесенных аллергических и инфекционных заболеваниях, при которых образуются антитела или иммунные комплексы, которые и являются факторами, повреждающими синовиальную оболочку.
Хронический синовит чаще развивается как осложнение при отсутствии/несвоевременном лечении/недолеченном остром процессе после травм. В ряде случаев хронический синовит может развиваться и при постоянном присутствии повреждающих факторов в организме (нарушение обмена веществ, ревматизм, аутоиммунные реакции). Как правило, хронически протекающее заболевание — это заболевание с умеренно выраженной симптоматикой (умеренный синовит) с периодическими обострениями воспалительного процесса. Достаточно часто встречаемым является реактивный синовит. Как правило, реактивный синовит развивается после перенесенных аллергических и инфекционных заболеваниях, при которых образуются антитела или иммунные комплексы, которые и являются факторами, повреждающими синовиальную оболочку.
Нередко в воспалительный процесс вовлекаются сухожилия и его синовиальные оболочки, вызывая теносиновит. Наиболее часто – встречается теносиновит плечевого сустава при котором в патологический процесс вовлекаются ткани вращательной манжеты (сухожилия в области плечевого сустава), теносиновит сухожилия длинной головки двуглавой мышцы плеча — с вовлечением в процесс сухожилия длинной головки двуглавой мышцы плеча, лучевого/локтевого сгибателей кисти, ахиллово сухожилие, сухожилия мышц подколенной ямки, сухожилия короткого разгибателя кисти/отводящей мышцы большого пальца, которые имеют одно фиброзное влагалище.
Провоцирующими факторами теносиновитов являются: растяжение/непривычно чрезмерные нагрузки, однократные тяжелые травмы или частые незначительные микротравмы. Особенно часто страдает сухожилия головки бицепса у спортсменов при высоких резких нагрузках. Кроме того, теносиновит сухожилия длинной головки бицепса часто развивается в пожилом возрасте, когда кровоснабжение сухожилий уменьшается и любая неоднократно повторяющаяся микротравма может вызывать возникновению дегенеративных изменений в сухожилиях.
Под маской воспаления суставных тканей могут протекать и опухоли суставов, как доброкачественные (синовиалома, фиброэндотелиома), так и злокачественные, в частности, злокачественная опухоль синовиома (синовиальная саркома — МКБ–10: С49), дебют которой часто аналогичен клинической симптоматике синовита. Опухоль может развиваться из синовиальной оболочки суставов и околосуставных тканей (сухожилий, фасций), часто повторно рецидивирует, быстро даёт метастазы, распространяющиеся лимфогенным и гематогенным путем. Синовиальная саркома растёт кнаружи от сустава, распространяется вдоль сухожилий и быстро прорастает в окружающие мышцы. Опухоль плотной консистенции, имеет форму узла. Поражаются преимущественно суставы нижних конечностей (коленный, суставы стопы). Наиболее часто встречается синовиома стопы. Прогноз неблагоприятный.
Еще одной формой синовита является виллонодулярный синовит. Однако, по существу, виллонодулярный синовит — это заболевание не воспалительного генеза, а является новообразованием (доброкачественной опухолью) синовиальной сумки, сухожильных влагалищ и сухожилий, которая проявляется несколько другой симптоматикой и требует иного подхода к ее лечению.
Патогенез
Очевидно, что в процесс развития синовита вовлечены инфекционные агенты и механизм иммунного ответа на их воздействие. При этом, в основе развития иммунокомплексного синовита лежит чрезмерная иммунная реакция макроорганизма на антигены инфекционных агентов, находящихся вне сустава с постепенным формированием иммунных комплексов, откладывающихся в синовиальной оболочке.
Значительная роль в поддержании патологического процесса отводится воспалению и выработке провоспалительных цитокинов, что способствует высвобождению медиаторов воспаления, повреждающих коллагено-эластический слой синовиальной оболочки с развитием реактивного синовита. В свою очередь воспаленная синовиальная оболочка выделяет биологические медиаторы воспаления, что поддерживает синовит и способствует деструкции хрящевой ткани, продукты распада которой являются антигенами и в свою очередь индуцируют образование аутоантител и усиление локального воспалительного процесса. То есть, формируется замкнутый круг воспалительной реакции.
Как следствие, страдает процесс образования эндогенной гиалуроновой кислоты и синовиальной жидкости. На фоне присутствия медиаторов воспаления повышается проницаемость сосудов, что приводит к увеличению трансфузии плазмы в синовиальную жидкость сустава, вызывая нарушения в структуре синовиальной оболочки (утолщение, снижение эластических свойств) и ее функции (продуцирование синовиальной жидкости).
Классификация
В основу классификации синовита положены несколько различных факторов, в соответствии с которыми выделяют несколько видов синовита.
- Септический синовит – инфекционный агент попадает в сустав с током крови/лимфы или контактным путем при проникающих ранах.
- Асептический (преимущественно травматический синовит), вызванный механическими повреждениями (разрыв связок, ушибы, переломы), нарушениями структуры сустава при артритах, артрозах, нарушениями обмена веществ, аутоиммунными и эндокринными заболеваниями.
- Аллергический синовит – развивается под действием аллергических агентов.
- Реактивный — повреждающими факторами синовиальной оболочки являются аутоантитела/иммунные комплексы.
По течению заболевания: острый и хронический.
По локализации: синовит тазобедренного, коленного, голеностопного, плечевого, лучезапястного, локтевого сустава.
По типу поражения: первичный и вторичный.
По характеру экссудата: серозный, гнойный, серозно-фиброзный, геморрагический.
Причины
Синовит является полиэтиологическим заболеванием. К основным причинам его развития относятся:
- Травматические повреждения сустава различной степени (ушибы, подвывихи, вывихи, разрывы связок/менисков, переломы), что приводит к травматизации синовиальной оболочки и скоплению в коленном суставе экссудата.
- Инфекции. Инфекционный агент может попадать в сустав как в результате нарушения целостности сустава (проникающие раны, открытые переломы, операционные вмешательства), так и путем заноса через кровь/лимфу из других очагов воспаления в организме. При этом в качестве инфекционного агента могут выступать пневмококк, стафилококк, гонококк, стрептококк, микобактериями туберкулеза, спирохет, и другими.
- Дегенеративно-дистрофические изменения в хрящевой ткани, которые вызваны различными системными заболеваниям (ревматизм), возрастными изменениями, погрешностями в питании.
- Иммунная реакция. Инициатором заболевания является иммунная система человека. Повреждающими факторами синовиальной оболочки являются аутоантитела/иммунные комплексы.
- Поражения мышечно-связочного аппарата, способствующие повышению нагрузки на сустав, следствием чего являются микротравмы суставной сумки.
- Нарушения метаболизма (подагра), при которой образуются в тканях сустава скопления кристаллоподобных солей, вызывающих интенсивное воспаление.
- Гемофилия. Появление мелких кровоизлияний из сосудов, питающих сустав, может вызвать скопления выпота и развития воспалительного процесса синовиальной оболочки.
К факторам, способствующим развитию синовита, относятся: избыточный, увеличивающий нагрузку на суставной аппарат, частые инфекционные заболевания, чрезмерные физические нагрузки.
Симптомы синовита
Симптоматика синовита определяется интенсивностью патологического процесса и степенью поражения синовиальной оболочки. Симптомы синовита коленного сустава и симптомы синовита тазобедренного сустава в целом идентичны.
Синовит коленного и тазобедренного сустава
С более выраженной симптоматикой протекает острый гнойный синовит. Состояние пациента быстро ухудшается, возникают и нарастают признаки острой интоксикации: резкая слабость, повышение температуры, озноб. Болевой синдром резко выражен, сустав увеличен в объеме, отечен, кожа над ним гиперемирована. Движения болезненны, реже развивается регионарный лимфаденит.
Анализы и диагностика
Постановка диагноза синовита базируется на жалобах пациента, визуальном осмотре/пальпация сустава и лабораторных/инструментальных методах обследования, включающих:
- Общий анализ крови (СОЭ, лейкоцитоз).
- Рентгенографию.
- УЗИ.
При необходимости назначается компьютерная или магнитно-резонансная томография, артроскопия, диагностическая пункция. Дополнительно — аллергические пробы, биопсия синовиальной оболочки.
Проводится дифференциальная диагностика с артритом, деформирующим остеоартрозом, тендинитом, теносиновитом.
Лечение синовитa
Лечение синовита, независимо от локализации проводится по аналогичным принципам. Поэтому, рассматривать отдельно лечение синовитa коленного сустава или лечение синовита тазобедренного сустава не имеет смысла, также, как и рассматривать отдельно лечение синовита крупных и более мелких суставов, например, лечение синовита голеностопного сустава.
При асептическом синовите и большом количестве выпота проводится тугое бинтование пораженного сустава, иммобилизация конечности и придание ей возвышенного положения. При большом количестве экссудата или его гнойном содержимом проводится лечебная пункция полости сустава, а при необходимости — проточно-аспирационное промывание сустава раствором антибиотиков.
Основой лечения синовита служит противовоспалительная терапия, что позволяет не только купировать болевой синдром, но и устранить другую симптоматику, присущую воспалению — гипертермию сустава, припухлость, а также улучшить суставную функцию за счет подавления продуцирования провоспалительных цитокинов в суставных структурах и снижения активности процессов катаболизма.
Основным критерием выбора кроме эффективности, служит профиль желудочно-кишечной безопасности (желудочно-кишечной токсичности). Если болевой синдром слабо выражен, могут назначаться мази/гели из группы НПВС, которые наносят на кожу сустава на протяжении 7-10 дней 2-3 раза в сутки (Диклофенакол, Финалгель, Фастум гель и др.).
Из глюкокортикостероидов назначается Преднизолон, Дексаметазон длительностью на 5-10 дней.
При синовите коленного/тазобедренного сустава возможны внутрисуставные введения ГК, однако для этой цели предпочтительно использовать более сильнодействующие препараты (Дексаметазон) или ГК пролонгированного действия (Дипроспан). При синовите голеностопного сустава и мелких суставов стопы/кисти можно назначать аппликации Дексаметазона с Димексидом.
Болевой синдром при ограничении движений в суставе зачастую усиливается за счет рефлекторного мышечного спазма в местах прикрепления мышцы к кости сустава, что приводит к формированию мышечно-суставного блока. С целью уменьшения спастического мышечного компонента рекомендуется назначать миорелаксанты центрального действия, которые подавляют синаптическую передачу сигнала и снижают чрезмерный тонус мышц на уровне межнейронных связей (Тизанидин). Для этой цели также можно назначать и комбинированный препарат Нимид форте (Нимисулид+Тизанидин) на протяжении 10-15 дней.
Также, болевой синдром при длительно текущем синовите может усиливаться за счет невропатического компонента, что обусловлено усилением чувствительности центральных ноцицепторов из-за длительного присутствия воспалительных реакций в суставе. Для подавленяе гиперактивности центров боли в ЦНС могут назначаться Ньюропентин или Габапентин, которые эффективно купируют нейропатическую боль.
Лечение хронического синовита с наличием выраженной инфильтрации синовиальной оболочки и постоянного/часто рецидивирующего выпота предусматривает кроме указанных выше препаратов применение ингибиторов протеолитических ферментов внутрь сустава – Гордокс, Трасилол. Длительно текущий хронический синовит требует регулярного приема специализированного витаминно-минерального комплекса и БАДов, позитивно действующих на все суставные ткани (Сустанорм, Артривит, Кальцемин, Коллаген Ультра).
Лечение теносиновита базируется на аналогичных принципах — при остром процессе (иммобилизация, НПВС, при тяжелом течении — введение глюкокортикоидов в сухожильное влагалище). В период стихания воспаления для профилактики быстро формирующих контрактур плечевого сустава — щадящие упражнения на увеличение объема движений. При хроническом процессе — тепловые процедуры, симптоматическая терапия.
Лечение синовита самостоятельно в домашних условиях народными средствами проводить не рекомендуется, поскольку отсутствие/несвоевременное адекватное лечение может привести к осложнениям и хронизации патологического процесса. Необходима обязательная консультация врача, а уже назначенное лечение можно проводить по возможности амбулаторно в домашних условиях.
![]()
Реактивный артрит, возникающий после воздействия определенной желудочно-кишечной и мочеполовой инфекции. Классическую триаду постинфекционного артрита, не гонококкового уретрита и конъюнктивита описывают часто, однако наблюдается она в незначительном количестве случаев и не требует установления диагноза.
Реактивный артрит принадлежит к семейным спондилоартропатиям, которые имеют схожие клинические, радиографические и лабораторные характеристики, включая воспаление позвоночника и связь с HLA-антигеном В 27. К этой группе заболеваний относят псориатический артрит, анкилозирующий спондилоартрит, артрит, связанный с воспалением кишечника, и не дифференцированной спондилоартропатией.
Бактерии, связанные с реактивным артритом (ReA), как правило, являются причиной венерического заболевания и инфекционной дизентерии. Это грамнегативные организмы с липополисахаридным компонентом в пределах их клеточной стенки; и бактерии, и бактериальные компоненты были выявлены в синовиальной ткани.
Наиболее распространенными бактериальными видами являются виды Chlamydia, Salmonella, Campylobacter, Shigella и Yersinia, хотя реактивный артрит описан после многих других бактериальных инфекций. Виды Chlamydia традиционно считают наиболее распространенными видами, вызывающими реактивный артрит.
Как C. trachomatis, так и C. pneumoniae, являются известными триггерами. Однако C. trachomatis является более частым возбудителем инфекции. В одном исследовании C. trachomatis была обнаружена у 50% пациентов с урогенитальными инфекциями, у которых развился реактивный артрит. Обсервационное исследование предполагает, что хламидии также являются обычным этиологическим возбудителем не дифференцированного спондилоартрита. Поэтому, можно говорить о том, что настоящее влияние хламидий как этиологических возбудителей инфекционного артрита не было должным образом распознано.
Campylobacter jejuni вероятно является самой распространенной причиной развития реактивного артрита после дизентерии в США. Уровень атак реактивного артрита, вызванного Campylobacter, отличается в разных исследованиях и колеблется в пределах 1–7%. Генотип HLA-B27 не был заявлен как способствующий риску возникновения реактивного артрита после инфекции, вызванной Campylobacter.
Salmonella enteritidis является одной из наиболее частых кишечных инфекций в США, приблизительно у 6–30% пациентов с острой инфекцией, вызванной Salmonella, развивается реактивный артрит.
Бактериальные антигены Salmonella были выявлены в синовиальной жидкости пациентов с реактивным артритом, вызванным Salmonella. Бактериальная ДНК микроорганизмов Shigella может быть обнаружена в синовиальной ткани пациентов с реактивным артритом. Исследование, выполненное в Финляндии в 2005 году показало, что общая частота развития заболевания составила 7%. Данные о 2-х вспышках инфекции, вызванной Yersinia, возникших в 1998 году, показали, что у 12% инфицированных людей в дальнейшем развился реактивный артрит; в ходе недавнего исследования с участием 37 взрослых было выявлено, что фактический показатель заболеваемости может быть выше (22%). Бактериальные антигены Yersinia были выявлены в синовиальной ткани, и в одном исследовании предположили, что такие синовиальные бактерии могут быть метаболически активными.
В синовиальной ткани пациентов с реактивным артритом были выявлены разные бактериальные ДНК известных инфекционных возбудителей. Бактериальные нуклеиновые кислоты были выявлены у людей с соответствующим поражением методом ПЦР. Рибосомальные РНК, как Chlamydia trachomatis, так и C. pneumoniae, были выявлены в синовиальной ткани пациентов с реактивным артритом, вызванным хламидиями; благодаря этому было доказано наличие этих микроорганизмов в суставах.
Кроме того, ДНК энтеробактерий были выявлены в синовиальной ткани пациентов с пост-дизентерийным реактивным артритом. Хотя постоянно присутствующие синовиальные патогены были зафиксированы как в случаях пост-хламидийного реактивного артрита, так и реактивного артрита, который развился после перенесенной кишечной инфекции, истинная связь между ними остается непонятной.
Однако данные, полученные в ходе исследования мышей с реактивным артритом, показали, что у мышей, чувствительных к SKG, развиваются периферический синовит, сакроилеит, спондилит, энтерит и псориазная сыпь через 5 недель после возникновения вагинальной инфекции, вызванной C. muridarum. Именно хламидиоз вызвал реактивный артрит, связанный с ФНО-альфа, зависящий от активной инфекции. Тяжесть реактивного артрита коррелирует с бактериальной составляющей и сниженным уровнем бактериального клиренса.
Продукты бактериального распада находят в синовиальной ткани пациентов с реактивным артритом, который развился после перенесенной кишечной инфекции; однако, хламидии, которые находятся в синовиальной ткани, постоянно существуют в метаболически активном состоянии. Хотя эта хламидийная инфекция является хронической, бактерии пребывают в аберрантном состоянии, поэтому такие внутриклеточные организмы не могут определяться.
В синовиальной ткани пациентов с реактивным артритом не были выявлены персистирующие активные микроорганизмы, которые остались после кишечной инфекции, за исключением, возможно, микроорганизмов Yersinia. В хронической стадии происходит смена экспрессии гена. Экспрессия гена наружной мембраны (omp 1), используемого в делении клеток, снижается в отношении персистирующих организмов Chlamydia по сравнению с бактериями в продуктивной стадии. Дальнейшие результаты стимуляции синтеза белков теплового шока (HSP)-60 C. trachomatis и C. pneumoniae важны для поддержания персистирующего состояния.
Также было показано, что у пациентов с реактивным артритом наблюдается пониженная бактерицидная активность моноцитов после воздействия Chlamydia. Виды Chlamydia имеют несколько способов уклонения от иммунного ответа хозяина. Было выявлено, что антиген HLA-B27 класса 1 гистосовместимости играет важную роль в патофизиологии спондилоартропатии. В соответствии с эпидемиологическими исследованиями реактивного артрита, его распространенность чаще всего колеблется в пределах от 30% до 50%.
Точная генетическая роль HLA-B27 не выяснена до конца, однако, его определение не обязательно для постановки диагноза. Было описано несколько возможных патогенных механизмов. Они включают молекулярную мимикрию, представляя артритогенный бактериальный материал для Т-клеток, вызывая аутоиммунные реакции, стимулируя бактерии к изменению собственной толерантности к B27 антигену ,и изменяя защитную реакцию организма хозяина в связи с повышенной инвазией микробов в кишечник и облегчая персистенцию Chlamydia.
Специфического теста для диагностики реактивного артрита (ReA) не существует. Однако, существует целый ряд тестов для подтверждения подозрения в отношении данного заболевания у людей с клиническими симптомами, указывающими на воспалительный артрит, возникший после перенесенного венерического заболевания или дизентерии.
Ревматические пробы острой фазы, такие как СОЭ (оседание эритроцитов) или С- реактивный белок (СРБ), часто повышены, но имеют тенденцию возвращаться к норме, если заболевание становится хроническим. Тесты на ревматоидный фактор, в случае ревматоидного артрита, и антинуклеарные антитела, которые выявляют при многих аутоиммунных состояниях, как правило, отрицательные. Хотя распространенность HLA-B27 в предыдущих исследованиях колебалась в пределах от 0% до 80%, в большинстве исследований реактивного артрита сообщали о распространенности HLA-B27 в пределах от 30% до 50%.
Ген не является специфическим или необходимым для диагностики реактивного артрита, но его присутствие в клиническом контексте улучшает точность диагноза.
Идентификация обычных возбудителей, вызывающих инфекцию, помогает установить диагноз. Бактериологическое исследование выделений из мочеполового канала и посев кала помогают в диагностике на этапе появления инфекции, однако результаты таких бактериологических исследований обычно отрицательные после начала артрита. Тем не менее, эти исследования легко выполнять и они должны проводиться после начала артрита.
Обычные бактериологические исследования синовиальной жидкости должны проводиться для исключения гонореи или других инфекционных процессов. Анализ кристаллов синовиальной жидкости также необходимо выполнять для исключения подагры или другого вида кристаллиндуцированного артрита.
ПЦР анализ бактериальных компонентов синовиальной ткани или жидкости полезен для подтверждения диагноза, но не практичен. При развитии артрита необходимо провести ПЦР анализ мочи, однако, результат также часто отрицательный на этой стадии.
Тесты амплификации нуклеиновых кислот показаны мужчинам или женщинам с бессимптомным течением заболевания, у которых подозревают реактивный артрит, приобретенный в результате полового акта.
Существует возможность проведения серологических исследований известных патогенных бактериальных возбудителей, однако, трудно доказать причинно-следственную связь; поэтому эти исследования, как правило, не рекомендуют.
Рентгенологическое исследование осевого скелета должно проводиться пациентам с подозрением на хронический реактивный артрит. При рентгенографии периферических суставов можно увидеть некоторые признаки реактивного артрита, они являются менее специфичными для этого заболевания.
На ранней стадии заболевания не существует специфических рентгенологических признаков, за исключением отека мягких тканей. При хронической форме заболевания сужение суставной щели и эрозии могут наблюдаться в небольших суставах рук и ног. Обычная рентгенограмма осевого скелета показывает асимметричный сакроилеит у трети пациентов с хроническим реактивным артритом.
В случае развития хронического артрита может проявляться энтезит в форме мягкого надкостного остеогенеза в области сухожилий и в месте прикрепления связок. Как правило, наблюдают окостенения в области ахиллова сухожилия и большие шпоры на пятках. Не маргинальные синдесмофиты можно наблюдать в области поясницы и в грудном отделе позвоночника, как результат хронического энтезита параспинальных связок.
МРТ может быть более чувствительным при выявлении раннего сакроилеита, но контрольные исследования не проводились. МРТ-исследование крестцово-подвздошных суставов может быть полезным, в частности, для пациентов с подозрением на реактивный артрит, который сопровождается болью в пояснице или ягодицах. В ходе МРТ могут быть обнаружены не только эрозивные изменения или анкилоз крестцово-подвздошных суставов, но также изменения в костном мозге вокруг крестцово- подвздошных суставов, что указывает на активную форму сакроилеита.
Как и при лечении синдромов воспалительного артрита, лечение направлено на симптоматическое облегчение и предупреждение или угнетение дальнейшего поражения суставов. Традиционные средства лечения включают нестероидные противовоспалительные препараты (НПВП), кортикостероиды и противоревматические препараты (DMARD).
НПВП часто используют в качестве терапии первой линии. Доказано, что нет таких НПВП, действие которых лучше, чем других. Кажется, что НПВП имеют умеренный эффект в лечении клинических симптомов как аксиальной, так и периферической артралгии. Однако, ни в одном из перспективных исследований не была проанализирована их эффективность в лечении реактивного артрита. Несмотря на это, большой клинический опыт показывает, что они эффективны. Их назначают на раннем этапе заболевания для улучшения функционального состояния суставов. Согласно мнению экспертов, в первую очередь следуют применять индометацин или напроксен. Применение НПВП ограничивается их токсическим действием на почки и печень, сопровождающимся осложнениями в виде желудочно-кишечного кровотечения.
В отличие от НПВП кортикостероиды имеют ограниченное действие на аксиальные симптомы и являются более эффективными в лечении реактивного артрита периферических суставов. Кортикостероиды можно назначать в том случае, если пациенты не отвечают на лечение НПВП или на этапе обострения заболевания. Внутрисуставные инъекции при моноартикулярной и олигоартикулярной форме заболевания могут обеспечить кратковременное облегчение, но в случае полиартрита может понадобиться применение системных кортикостероидов. Системные кортикостероиды могут быть эффективными для лечения проявлений со стороны глаз, таких как ирит. Кортикостероиды местного действия могут применяться для лечения поражений кожи, таких как кольцевидный баланит и бленноррагическая кератодермия.
Считают, что БМПАП являются препаратами второй линии или препаратами на случай, если применение НПВП оказалось неэффективным, или когда необходим более радикальный подход к лечению с целью предупреждения рентгенографической деструкции суставов. Единственным БМПАП, который прошел официальную апробацию в рамках контрольного двойного слепого исследования, является сульфасалазин. В этом исследовании группа пациентов, которые получали 2 г сульфасалазина ежедневно, показали определенно улучшение по сравнению с группой плацебо. Если препарат не эффективен на протяжении 3-4 месяцев, его применение нужно отменить.
Данные, которые указывали бы на то, что длительное применение антибиотиков имеет какой-либо терапевтический эффект в лечении реактивного артрита, возникшего после перенесенной кишечной инфекции, отсутствуют.
Спорный характер носят данные относительно длительного лечения антибиотиками реактивного артрита, вызванного перенесенным хламидиозом. Важно помнить, что существует острый и хронический реактивный артрит. Большинство исследований проведены среди пациентов с острым реактивным артритом, вызванным хламидиями. Так как это состояние часто улучшается само по себе, может быть трудно доказать, что длительное лечение антибиотиками может быть эффективным в периоде обострения болезни. По сравнению с группой плацебо в ходе исследования было выявлено отсутствие положительной динамики от объединения офлоксацина и рокситромицина при лечении пациентов или с острым реактивным артритом, вызванным перенесенной дизентерийной инфекцией, или с реактивным артритом, вызванным мочеполовой инфекцией.
Большинство данных указывают на то, что такой метод лечения не работает, за исключением одного исследования, которое предполагает эффективность метода. Для лечения хронического реактивного артрита, вызванного перенесенным хламидиозом, в рамках исследования использовался комбинированный противомикробный подход, который показал положительные результаты.
Проведенный мета-анализ показал гетерогенные результаты, которые предполагают, что потенциальная эффективность антибиотиков в лечении реактивного артрита остается не ясной.
Читайте также:


