Пункция костного мозга при миеломной болезни
Число лейкоцитов, вариабильное, нормальное или повышенное. В развитых стадиях болезни можно наблюдать лейкопении, отягощаемые и применяемыми цитостатическими лечениями. Лейкоцитарная формула, обычно нехарактерная, может показывать иногда повышенное число плазмоцитарных элементов, подобных клеткам в костном мозге.
Число тромбоцитов нормальное или умеренно пониженное.
Исследование костного мозга при множественной миеломе имеет важнейшее значение для постановки диагноза. Костная пункция производится обычно в грудную кость или в подвздошный гребень, но ее можно производить и в другие затронутые кости: позвонки, пяточную кость, ключицу. Иногда проникание в кость происходит очень легко, костная ткань давая ощущение особой хрупкости.
В цитоплазме миеломатозных клеток можно встретить гиалиновые шарики (тела Russel), многочисленные вакуоли, придающие клетке вид ежевики (клетки Mott), или хрустальные азурофильные включения иногда подобные телам Auer при миелобластической лейкемии (протеиновые кристаллы) (цветная вклейка III).
С цитохимической точки зрения, цитоплазма миеломатозных клеток является пероксидазо-отрицательной и окрашивается метахроматически с метиловой зеленью. Гиалиновые шарики (тела Russel) обычно PAS-положительные.
Миеломатозные клетки преставляют множество нуклеоцитоплазматических асинхронизмов созревания. Согласно Bernier и Graham, степень этих асинхронизмов пропорциональна клиническому распространению заболевания.

Исследования при помощи электронного микроскопа показали наличие определенных аномалий на уровне клеточных органитов, аномалии тем более явные, чем менее дифференцирована миеломатозная клетка. Митохондрии численно увеличены и имеют патологические аспекты: удлиненные, кольцевидные, иногда с чертами миелиновой дегенерации; аппарат Гольджи везикулярнио трансформирован, центриоли имеют гигантский удлиненный вид, а число рибозомов может возрастать (Bessis). Наиболее интересный аспект представляет эргастоплазмический аппарат. В большинстве случаев он расширен и имеет везикулярный вид.
Содержимое эргастоплазмических везикул состоит из протеина и имеет твердую консистенцию, принимая аспект тел Russel, либо в растворимой форме, flaming cells или тезауроцотив (Paraskevas и сотр.), либо в кристаллизованной форме.
Протеиновые кристаллы бирефрингентные с периодичностью около 110 A (Bessis). В других случаях эргатоплазмический аппарат менее развит и представлен несколькими пластинками, а редко бывает плохо развитым, подобным лимфоидной клетке. На уровне ядра появляются аномалийные, гипертрофированные нуклеоли, а также и множество интрануклеарных вакуолей (Smetena и сотр.). Некоторые авторы описали наличие в ядре вирусных телец, в 15% случаев (Sorensen), тельца, которые Bessis нашел лишь в одном из 12 изученных им случаев.
Иммунохимические и иммунофлюоресцентные исследования, с разными специфическими антисыворотками (IgG, IgA, IgM, IgD IgE, ламбда, каппа) показали наличие Ig в цитоплазме миеломатозных клеток. Они локализированы в особенности на уровне эргастоплазмического аппарата и рибозомов. Делались попытки установить связь между морфологическим аспектом клеток и типом секретированного Ig. Полученные до настоящего времени результаты неубедительны. Paraskevas и сотр. утверждают, что пламенистые клетки секретируют IgA.
Цитогенетическое исследование множественной миеломы показало существование разных форм анейплоидии, но которые наблюдаются не во всех случаях. Кроме этого кыло описано и присутствие различных хромозомов маркеров. Вследствие внедрения метода бандирования, Liang и Rowley нашли хромозом 14р+ у 3 больных с множественной миеломой и 1 больного с плазмоцитарной лейкемией, из 22 изученных больных. Этот хромозом 14q+ был найден и при других лимфомах типа Б, а также, изредка, и при лимфомах non-Б. Следует отметить, что Croce и сотрудники установили, что структуральные гены для тяжелых цепей Ig локализированы у человека на хромозоме 14.
Исследование протеинового обмена при множественной миеломе. Расстройства протеинового метаболизма составляют характерный аспект множественной миеломы. Злокачественно модифицированные плазмоциты сохраняют и усиливают способность синтетизировать цельные Ig или только определенные составные части глобулиновой молекулы.
В сыворотке большинства больных, общее количество протеинов повышено, достигая 23 г/100 мл. Среднее количество сывороточных протеинов у больных с миеломой равняется 9 г/100 мл. Этот рост происходит за счет глобулинов, точнее Ig. При электрофорезе на бумаге или в агаре наблюдается появление узкой и высокой полосы, с заметным сокращением остальных дуг. Это является изображением количественного роста гомогенного населения глобулинов. Пик находится обычно в зоне миграции у-глобулинов или b-глобулинов. Аномалийный протеин, находящийся в сыворотке больных с миеломой, получил название парапротеина, миеломатозного глобулина (М-глобулин) или компонента М.
В рамках множественной миеломы может происходить:
1) избыточный синтез, однако уравновешенный, цепей Н и L, с образованием цельных Ig;
2) неуравновешенный синтез, с избытком цепей L и образованием цельных Ig, параллельно с повышенным количеством свободных цепей L и
3) синтез лишь цепей L.
В настоящее время миеломы делятся по типу секретируемого Ig: миеломы IgG наиболее частые, встречающиеся в 60% случаев; миеломы IgA, в 20—25% случаев; IgD, в 2,1% случаев; и ограниченное число миелом IgE. Среди случаев множественной миеломы, 20% — с цепями L (миеломы Бенс-Джонса), причем некоторые без патологического протеина в сыворотке, так как он элиминируется через мочу. Очень малый процент заболеваний (1%) не представляет изменений протеинового метаболизма (несекретирующие миеломы).
В рамках миелом IgG, наблюдается следующее распределение на субклассы (Schur): yG1 60—82%; yG2 10—18%; yG3 6—15%; yG4 1—8%. Сравнивая эти цифры с относительными концентрациями в нормальной сыворотке (гл. 7) можно утверждать, что моноклональные Ig типа yGl и yG3 встречаются чаще по сравнению с yG2.
Характерной чертой миеломатозного Ig является его гомогенность: узкая зона электрофоретической миграции, индивидуальная антигенная специфичность и цепь L только одного типа (ламбда или каппа). При миеломах IgG и IgA преобладают случаи с цепями каппа (2/3 случаев) (Hobbs и Corbet); при миеломах IgD, цепи ламбда преобладают в 90% случаев, в то время как при миеломах Бенс-Джонса, цепи ламбда присутствуют приблизительно в 45% случаев (Jancelewicz и сотр.). До сих пор не удалось выявить физико-химические или иммунохимические различия между миеломатозными протеинами и соответствующими им нормальными Ig.
Было доказано, что миеломатозные Ig обладают способностью связываться с другими веществами, следовательно действовать как антитела. Такая антителовая деятельность отмечалась по отношению к бактериальным соединениям (стрептолизин 0 или спрептококковая гиалу-ронидаза), к гематиям, к некоторым сывороточным протеинам, а также и к гаптенам (динитрофенол, 5-ацетоурацил, пуриновые и пиримидиновые нуклеотиды) (Osterland и сотр.). Способность миеломатозного протеина связываться с гематиями или сывороточными протеинами порождает определенные симптомы, как например агглютинация гематий в виде монетных столбиков, явления повышенной кровоточивости и пр.
У больных с миеломой, количественный рост характерного миеломатозного Ig сопровождается сокращением производства других типов глобулинов.
Значительная диспротеинемия в крови больных с множественной миеломой оказывает влияние на все пробы коллоидальной лабильности.
Реакция оседания эритроцитов в большинстве случаев бывает очень ускоренной, достигая 100 мм в час. При миеломах Бенс-Джонса, РОЭ показывает более низкие цифры, иногда даже в нормальных пределах.

Реакции на формол-гелифицирование, сульфат кадмия, Вельтмана — положительные. Реакция Sia (помутнение сыворотки в дистилированной воде) — слабо или умеренно положительная.
В редких случаях отмечалось наличие сывороточных криоглобулинов с появлением синдрома Рейно на холоде и наблюдалось также наличие пироглобулинов.
Тесты на коагуляцию модифицированы у некоторых больных. Патологические протеины в сыворотке могут интерферировать с различными фазами коагуляции, как например в трансформация фибриногена в фибрин, во взаимодействии с факторами II, V и VII. Функции тромбоцитов могут быть также модифицированными.
Анализ мочи показывает наличие протеина Бенс-Джонса в 40—50% случаев, когда он детерминируется путем нагревания и в 61% случаев, когда он выявляется путем иммуноэлектрофореза. Он представлен выведением легких цепей. Протеин Бенс-Джонса преципитирует в моче нагретой до 50—60°, создавая беловатое облако, которое перерастворяется при кипячении. В случае ассоциированной альбуминурии, перерастворение является неполным и иногда оказывается неполным и без альбуминурии. В такой ситуации мочу можно сделать прозрачной путем добавления нескольких капель 5%-й уксусной кислоты. Физикохимическое исследование альбумина Бенс-Джонса показало, что он состоит из легких цепей, димеризованных дисульфидными связями. Постоянно легкая цепь в моче идентична с легкой цепью сывороточного миеломатозного протеина.
В мочевом осадке могут появляться цилиндры, гематии, а в случаях почечного калкулеза появляются кристаллы фосфатов, уратов, а также гематии и лейкоциты.
Гиперкальцемия встречается часто при множественной мизломе (20—53% случаев), достигая 12—16 мг/100 мл сыворотки. Этот рост связан в первую очередь с процессами костной деструкции, но и с гиперпаратиреоидизмом, как вторичное явление почечной недостаточности. Гиперкальцемия при множественной миеломе не сопровождается ростом фосфора в крови, а щелочные сывороточные фосфатазы находятся в нормальных пределах, что представляет ценные данные для дифференциальной диагностики по отношению к первичному гиперпаратиреоидизму.
Сывороточная мочевая кислота бывает часто повышена, а в случаях, осложняющихся почечной недостаточностью, наблюдается рост креатинина и непротеинового азота.
Патологоанатомическое исследование при множественной миеломе. Наиболее явные изменения встречаются на уровне скелета, особенно в черепных костях, позвонках, ключицах, ребрах, грудной кости, лопатке, тазовых костях. Длинные кости затронуты в меньшей мере. На срезе, кость оказывается мягкой, а нормальная ткань заменяется красноватой или серо-красноватой туморальной тканью. Иногда опухоль переходит за периост, инфильтрируя смежные участки.
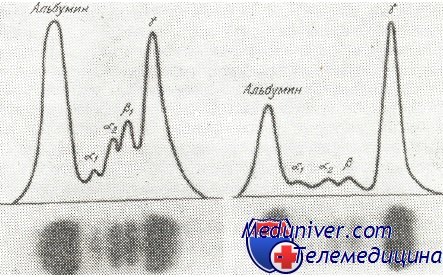
Изображения электрофореза нормальной сыворотки человека (слева) и сыворотки больного с множественной миеломой (справа). При миеломе констатируется наличие большого количества гаммагпобулина (высокая и узкая волна), с сокращением альбуминов и остальных глобулинов
Микроскопически, туморальная ткань состоит из пролиферации злокачественных плазмоцитоидных клеток, описанных при исследовании костного мозга. На срезе остеокласты и остеобласты немодифицированы.
В редких случаях внекостных миелом можно обнаруживать плазмоцитарные опухоли в различных органах, причем характерные особенности пролиферированных клеток подобны тем, которые наблюдаются при костных опухолях.
При множественной миеломе почка бывает часто затронута. Наиболее важные поражения встречаются на уровне канальцев. Дистальные канальцы расширены, с уплощенным эпителием и просветами заполненными эозинофильными и полихроматофильными цилиндрами. На периферии этих цилиндров встречаются многоядерные синцитин эпителиальных клеток. Цилиндры состоят из цельного миеломатозного Ig или из цепей L (протеин Бенс-Джонса). На электронном микроскопе, эти цилиндры имеют фибрилярную, амилоидную структуру (Abrahams и сотр.). Не удалось установить несомненную связь между наличием амилоида и протеинурией Бенс-Джонса. Несмотря на это, Glenner и сотр. показали in vitro образование амилоидных волокон путем протеолитической дигестии человеческого протеина Бенс-Джонса. Возможно, что подобный процесс происходит и на уровне почечных канальцев (Zlotnick).
В тубулярных эпителиальных клетках часто встречаются отложения кальция. Также на уровне почечных канальцев было отмечено наличие кристаллов, находящихся как в просвете, так и в эпителии. Их химическая структура не была установлена.
Почечные гломерулы бывают реже затронутыми при множественной миеломе. Отмечается утолщение базальной мембраны и мезангиомы, которое выступает с особенной ясностью на электронном микроскопе. Встречается также и гипертрофия эндотелиальных и эпителиальных клеток. В развитых фазах болезни появляются гиалиноз и склероз. Иногда в гломерулах можно найти отложения амилоида, что приводит к его гомогенизации.
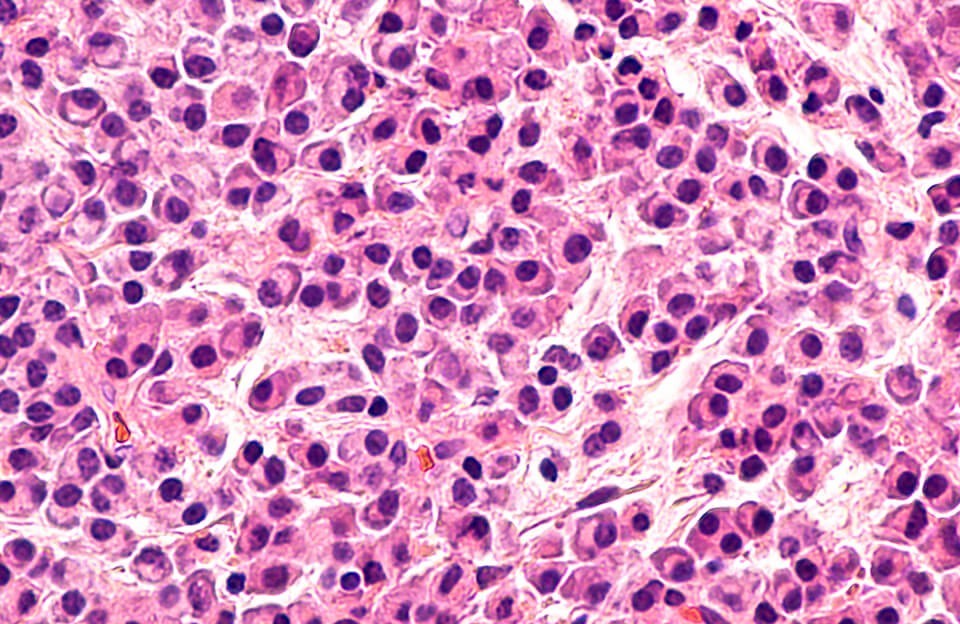
Что такое миеломная болезнь?
Это опухолевое заболевание, возникающее из плазматических клеток крови (подтип лейкоцитов, т.е. белых кровяных телец). У здорового человека эти клетки участвуют в процессах иммунной защиты, вырабатывая антитела. При миеломной болезни (ее еще называют миеломой) в костном мозге и в костях накапливаются измененные плазматические клетки, что нарушает образование нормальных клеток крови и структуру костной ткани. Иногда можно услышать о миеломе костей, миеломной болезни позвоночника, почек или крови, но это не совсем верные названия. Миеломная болезнь уже подразумевает поражение кроветворной системы и костей.
Классификация миеломной болезни
Болезнь неоднородна, можно выделить следующие варианты:
моноклональная гаммапатия неясного генеза - это группа заболеваний, при которых избыточное количество В-лимфоцитов (это клетки крови, которые участвуют в иммунных реакциях) одного вида (клона) вырабатывают аномальные иммуноглобулины разных классов, которые накапливаются в разных органах и нарушают их работу (очень часто страдают почки).
лимфоплазмацитарная лимфома (или неходжкинская лимфома), при которой очень большое количество синтезирующихся иммуноглобулинов класса М повреждает печень, селезенку, лимфоузлы.
плазмацитома бывает двух видов: изолированная (поражает только костный мозг и кости) и экстрамедуллярная (накопление плазматических клеток происходит в мягких тканях, например, в миндалинах или носовых пазухах). Изолированная плазмацитома костей в некоторых случаях переходит во множественную миелому, но не всегда.
Множественная миелома составляет до 90% всех случаев заболевания и обычно затрагивает несколько органов.
асимптоматическую (тлеющую, бессимптомную миелому)
миелому с анемией, поражением почек или костей, т.е. с симптомами.
Код миеломы по МКБ-10: С90.
Стадии миеломной болезни
Стадии определяют в зависимости от количества в сыворотке крови бета-2 микроглобулина и альбумина.
1 стадия миеломы: уровень бета-2 микроглобулина менее 3,5 мг/л, а уровень альбумина равен 3,5 г/дл или более.
2 стадия миеломы: бета-2 микроглобулин колеблется между 3,5 мг/л и 5, 5 мг/л или же уровень альбумина ниже 3,5, тогда как бета-2 микроглобулин ниже 3,5.
3 стадия миеломы: уровень бета-2 микроглобулина в сыворотке составляет более 5,5 мг/л.
Причины и патогенез миеломной болезни
Причины миеломы неизвестна. Есть ряд факторов, повышающих риск заболеть:
Возраст. До 40 лет миеломной болезнью почти не болеют, после 70 лет риск развития заболевания значительно повышен
Мужчины болеют чаще женщин
У людей с черным цветом кожи риск миеломы в два раза выше, чем у европейцев или азиатов
Имеющаяся моноклональная гаммапатия. У 1 из 100 человек гаммапатия трансформируется в множественную миелому
Семейная история заболевания миеломой или гаммапатией
Патология иммунитета (ВИЧ или применение лекарств, подавляющих иммунитет)
Воздействие радиации, пестицидов, удобрений
Костный мозг в обычных условиях вырабатывает строго определенное количество В-лимфоцитов и плазматических клеток. При миеломной болезни их выработка выходит из-под контроля, костный мозг заполняется аномальными плазматическими клетками, а образование нормальных лейкоцитов и эритроцитов снижается. При этом вместо антител, полезных в борьбе с инфекциями, такие клетки производят белки, способные повреждать почки.
Симптомы и признаки миеломной болезни
Признаки, которые помогут заподозрить миелому:
Боль в костях, особенно в ребрах и позвоночнике
Патологические переломы костей
Частые, повторяющиеся случаи инфекционных заболеваний
Выраженная общая слабость, постоянная усталость
Кровотечения из десен или носовые, у женщин - обильные менструации
Головная боль, головокружение
Тошнота и рвота
Диагностика миеломной болезни
Поставить диагноз бывает сложно, так как при миеломной болезни нет какой-то явной опухоли, которую можно заметить, а иногда заболевание вообще протекает без каких-либо симптомов.
Диагностикой миеломной болезни обычно занимается врач-гематолог. Во время расспроса врач выявляет основные симптомы заболевания у данного пациента, выясняет, нет ли кровотечений, боли в костях, частых простуд. Затем проводят дополнительные исследования, необходимые для точной постановки диагноза и определения стадии болезни.
Клинический анализ крови при миеломе часто указывает на увеличение вязкости крови и повышение скорости оседания эритроцитов (СОЭ). Нередко снижено количество тромбоцитов и эритроцитов, гемоглобина.
В результатах анализа крови на электролиты часто повышен уровень кальция; по данным биохимического анализа увеличено количество общего белка, определяются маркеры нарушения функции почек - высокие цифры мочевины, креатинина.
Анализ крови на парапротеин проводят для оценки типа и количества аномальных антител (парапротеинов).
В моче часто определяют патологический белок (белок Бенс-Джонса), который представляет собой моноклональные легкие цепи иммуноглобулинов.
На рентгенограмме костей (черепа, позвоночника, бедренных и тазовых костей) видны характерные для миеломы повреждения.
Пункция костного мозга - самый точный способ диагностики. Тонкой иглой берут кусочек костного мозга, обычно прокол делают в области грудины или кости таза. Затем полученный изучают под микроскопом в лаборатории на предмет перерожденных плазматических клеток и проводят цитогенетическое исследование для выявления изменений в хромосомах.
Компьютерная томография, магнитно-резонансная томография, ПЭТ-сканирование позволяют выявить участки повреждения в них.
Способы лечения миеломной болезни
В настоящее время используют разные методы лечения, прежде всего лекарственную терапию, при которой препараты применяют в разных комбинациях.
Таргетная терапия с использованием лекарства (бортезомиб, карфилзомиб (не зарегистрирован в России), которые за счет влияния на синтез белков вызывают гибель плазматических клеток.
Терапия биологическими препаратами, такие как талидомид, леналидомид, помалидомид, стимулируют собственную иммунную систему бороться с опухолевыми клетками.
Химиотерапия циклофосфаном и мелфаланом, которые тормозят рост и приводят к гибели быстрорастущих клеток опухоли.
Кортикостероидная терапия (дополнительное лечение, которое усиливает эффект основных препаратов).
Бисфосфонаты (памидронат, золендроновая кислота) назначают для повышения плотности костной ткани.
Обезболивающие, в том числе наркотические анальгетики, применяют при сильных болях (очень частая жалоба при миеломной болезни), для облегчения состояния пациента применяют хирургические методы и лучевая терапия.
Хирургическое лечение требуется, например, для фиксации позвонков с помощью пластин или других приспособлений, так как происходит разрушение костной ткани, в том числе позвоночника.
После проведения химиотерапии часто проводят пересадку костного мозга, при этом наиболее эффективной и безопасной является аутологичная трансплантация стволовых клеток костного мозга, Для осуществления этой процедуры проводят забор стволовых клеток красного костного мозга. затем назначают химиотерапию (как правило, высокими дозами противоопухолевых препаратов), которая уничтожает раковые клетки. После окончания полного курса лечения делают операцию по пересадке забранных ранее образцов, и в результате начинают расти нормальные клетки красного костного мозга.
Некоторые формы заболевания (прежде всего “тлеющая” меланома) не требуют срочного и активного лечения. Химиотерапия вызывает тяжелые побочные эффекты и в некоторых случаях - осложнения, а эффекты на течение болезни и прогноз при бессимптомной “тлеющей” миеломной болезни сомнителен. В таких случаях проводят регулярное обследование и при первых признаках обострения процесса начинают лечение. План контрольных исследований и регулярность их проведения врач устанавливает индивидуально для каждого пациента, и очень важно соблюдать эти сроки и все рекомендации врача.
Осложнения миеломной болезни
Сильные боли в костях, требующие назначения эффективных обезболивающих средств
Почечная недостаточность с необходимостью гемодиализа
Частые инфекционные заболевания, в т.ч. воспаление легких (пневмонии)
Истончение костей с переломами (патологические переломы)
Анемия, требующая переливания крови
Прогноз при миеломной болезни
При “тлеющей” миеломе заболевание может не прогрессировать десятки лет, но необходимо регулярное наблюдение у врача, чтобы вовремя заметить признаки активизации процесса, при этом появление очагов разрушения костей или увеличение в костном мозге количества плазматических клеток выше 60% говорит об обострении заболевания (и ухудшении прогноза).
Выживаемость при миеломе зависит от возраста и общего состояния здоровья. В настоящее время в целом прогноз стал оптимистичнее, чем еще 10 лет назад: 77 из 100 больных миеломой человек будут жить как минимум год, 47 из 100 - как минимум 5 лет, 33 из 100 - как минимум 10 лет.
Причины смерти при миеломной болезни
Чаще всего к смерти приводят инфекционные осложнения (например, пневмония), а также фатальные кровотечения (связанные с низким количеством тромбоцитов в крови и нарушениями свертываемости), переломы костей, тяжелая почечная недостаточность, тромбоэмболия легочной артерии.
Питание при миеломной болезни
Рацион при миеломе должен быть разнообразным, содержать достаточное количество овощей и фруктов. Рекомендуют уменьшить потребление сладостей, консервов и готовых полуфабрикатов. Специальной диеты можно не придерживаться, но так как миеломе часто сопутствует анемия, то желательно регулярно есть продукты, богатые железом (постное красное мясо, сладкий перец, изюм, брюссельская капуста, брокколи, манго, папайя, гуава).
В одном из исследований было продемонстрировано, что употребление куркумы предупреждает резистентность к химиотерапии. Исследования на мышах показали, что куркумин может замедлять рост раковых клеток. Также добавление в пищу куркумы во время химиотерапии может несколько облегчить тошноту и рвоту.
Все изменения в диете нужно согласовывать с лечащим врачом, особенно во время химиотерапии.

Миелома — злокачественная опухоль, подавляющая нормальное кроветворение, разрушающая кости и вырабатывающая патологические белки, повреждающие внутренние органы. Когда говорят о миеломе крови или костей, или позвоночника, или костного мозга, то имеют ввиду одно заболевание с разнообразными проявлениями.
Относящееся к гемобластозам или онкогематологическим процессам, то есть злокачественным болезням крови и лимфатической ткани заболевание имеет много названий: множественная миелома, миеломная болезнь и генерализованная плазмоцитома, плазмоцитарная миелома.
- Причина миеломы
- Что происходит при миеломе?
- Диагностика миеломной болезни
- Когда диагноз миеломы не вызывает сомнений
- Симптомы миеломы
- Лечение миеломной болезни у молодых
- Лечение миеломы у пожилых
- Прогноз при миеломной болезни
Причина миеломы
Миелома состоит из изменённых плазматических клеток. В нормальном костном мозге плазматические клетки рождаются из В-лимфоцитов, но число их ограничено всего 5%, большее количество — уже патология.
Определённой ясности с первопричиной развития плазматической опухоли нет, в инициации процесса подозревают плохую наследственность и склонность к аллергии против собственных тканей, радиацию и работу с токсичными веществами, под подозрение попал и вирус герпеса 8 типа.

Миеломная болезнь поражает трёх из 100 тысяч россиян, как правило, пожилых — преимущественно на седьмом десятке жизни, у молодых до 40 лет заболевание встречается очень редко.
Среди страдающих заболеваниями крови и лимфатической ткани плазмоцитому имеет 10-13%, но из всех существующих в природе злокачественных процессов на больных плазмоклеточной опухолью приходится не более одного процента.
Что происходит при миеломе?
По какой-то причине в костном мозге появляются ненормальные клетки, размножаясь, они нарушают нормальное кроветворение, что проявляется анемией. Недостаток эритроцитов сказывается на работе всех органов, но особенно сильно на легочной ткани и головном мозге, что проявляется недостаточностью их функций.
Функция нормальных плазматических клеток — выработка антител-иммуноглобулинов для защиты от болезнетворных агентов. Миеломные плазмоциты тоже вырабатывают иммуноглобулины, но дефектные парапротеины, не способные к иммунной защите.
В костях миеломные клетки стимулируют остеокласты, вызывая остеолизис — разъедание кости. Из разрушенной кости кальций выходит в плазму, накапливаясь, приводит к гиперкальциемии — тяжёлому состоянию, требующему принятия срочных мер.
Диагностика миеломной болезни
Диагноз устанавливается по анализам крови, где находят парапротеины и определяют их суммарную и видовую концентрацию. Парапротеины обозначают как иммуноглобулины — IgA, IgG и IgМ. Плазмоциты вырабатывают иммуноглобулины по собственному усмотрению и в разном количестве, по их изменению продукции патологических белков впоследствии оценивают эффективность лечения и активность заболевания.
Степень агрессивности плазматических клеток выясняют при микроскопии костного мозга, его получают из грудины при стернальной пункции или при биопсии тазовой кости. Особенно актуально исследование при невысокой продукции парапротеинов или при изменении характера течения болезни.

Часто заболевание случайно обнаруживается во время обычной рентгенографии органов грудной клетки по литическим дефектам ребер. На первом этапе необходимо выявить все деструктивные изменения в костях, чтобы в дальнейшем следить за процессом и результатами терапии, что позволяет высокочувствительная низкодозная КТ всего скелета.
При МРТ изучается состояние плоских костей — черепа и таза, что обязательно при тлеющей и солитарном варианте опухоли. МРТ помогает оценить не только дефекты кости, но и наличие опухолевой инфильтрации мягких тканей, вовлечение в процесс спинного мозга.
Обязательно проводится анализ на кариотип для выявления генетических аномалий, влияющих на прогноз в отношении жизни больного и эффективность лечения.
Когда диагноз миеломы не вызывает сомнений
Характерные особенности клеток определяют течение процесса от медленной и практически доброкачественной гаммапатии или тлеющей миеломы до стремительного плазмоклеточного лейкоза.
Не всегда изначально удаётся классифицировать заболевание, что усложняет выбор оптимальной терапии. В 2014 году международный консенсус определил критерии, облегчающие постановку точного диагноза и отделяющие один вариант опухолевого процесса от других.
В первую очередь, в костном мозге определяют процент плазматических клеток, так при симптоматической миеломной болезни их должно быть более 10%, а 60% говорит о высокой агрессивности опухоли.
- М-протеин в крови, то есть IgA или IgG;
- легкие цепи иммуноглобулинов;
- в моче белок Бенс-Джонса;
- очаги в костях скелета.
При недостаточности специфических критериев диагностике помогают неспецифические, но часто встречающиеся последствия деятельности плазмоцитов и парапротеинов на органы-мишени:
- повышение уровня кальция крови в результате массивного разрушения костей;
- снижение гемоглобина при опухолевом замещении костного мозга;
- повышение креатинина крови — маркёра почечной недостаточности.
Симптомы миеломы
Замечено, что каждый пул плазматических клеток производит иммуноглобулины с персональными особенностями и по своему графику, отчего клинические проявления очень своеобразны и глубоко индивидуальны. Нет двух одинаковых больных, тем более невозможно найти двух похожих пациентов по диагностическим критериям. Тем не менее, выделяют несколько типов заболевания.
По количеству поражений опухоль может быть генерализованной или множественной и солитарной — с единственным очагом.
По течению различают вялотекущую или тлеющую, она же индолетная, и симптоматическую плазмоцитому, протекающую с явными клиническими проявлениями.

Основное проявление симптоматической миеломы — боли в костях вследствие их разрушения, которые появляются не сразу и часто даже не в первый год заболевания. Болевой синдром возникает при вовлечении в опухолевый процесс надкостницы, пронизанной нервными окончаниями. При медленно текущем процессе до выявления опухоли может пройти несколько лет, поскольку ничего кроме эпизодов слабости у пациента не возникает.
В развёрнутой стадии с множественными поражениями на первый план выходят в разных комбинациях и с индивидуальной интенсивностью переломы в местах деструкции костей и проявления почечной недостаточности, или амилоидоз органов.
Лечение миеломной болезни у молодых
Вялотекущий вариант миеломной болезни не всегда требует лечения, поскольку не угрожает жизни, а терапия совсем не безвредна. В данном случае наблюдение за течением процесса более выгодно пациенту, нежели токсичная химиотерапия. Регулярные обследования позволяют вовремя диагностировать активизацию процесса.
Симптоматическая миелома разделяется по стадиям от I до III по уровню в крови специфического микроглобулина и альбумина, стратегия при стадии I и II-III различается только используемыми препаратами и их комбинациями.
При любой стадии основное и определяющее тактику — состояние пациента и его возраст. Так сохранным больным до 65-летнего возраста и без тяжёлых хронических болезней предлагается агрессивная химиотерапия высокими дозами с пересадкой собственных стволовых клеток крови, по-научному, аутологичной трансплантацией.
Физически сохранные пациенты от 65 до 70-летия тоже могут претендовать на высокодозную химиотерапию, но уже не комбинацией лекарств, а единственным препаратом — мелфаланом.
До начала высокодозной химиотерапии проводится несколько курсов полихимиотерапии обычными дозами, затем специальным препаратом стимулируется выработка костным мозгом собственных стволовых клеток, которые собираются и консервируются. Затем пациент получает очень высокие дозы цитостатиков, в результате чего гибнут все клетки крови — опухолевые и нормальные. Нормальные, заблаговременно законсервированные кровяные элементы и вводят пациенту.
Лечение миеломы у пожилых
Пациенты старше 65 лет и помоложе, но с сопутствующими болезнями, влияющими на общее состояние и активность, тоже на первом этапе проходят цикловую химиотерапию, в том числе с использованием таргетных препаратов. Результат лечения оценивается по анализам крови и костного мозга, где определяют концентрацию специфических для заболевания белков и процент опухолевых клеток.
На результате лечения отражается не только возраст, но и наличие нескольких хронических болезней, астенизация, подразумевающая физическое ослабление с похуданием или без оного.
В последние годы спектр химиопрепаратов существенно расширился за счёт таргетных средств, продемонстрировавших хороший непосредственный результат и увеличение продолжительности жизни участников исследований.
Поражения скелета подлежат длительной терапии бисфосфонатами, уменьшающими болевой синдром, предотвращающими переломы и гиперкальциемию. На отдельные опухолевые очаги воздействуют ионизирующим излучением, обязательна лучевая терапия при угрозе сдавления спинного мозга и поражении шейного отдела позвоночника.

Прогноз при миеломной болезни
Кроме возраста пациента и его физического состояния на прогнозе миеломы и продолжительности жизни отражается чувствительность опухоли к лекарственному лечению и биологические характеристики плазматических клеток, в частности генетические аномалии с делецией участков хромосом и амплификацией — удвоением генов.
Читайте также:


