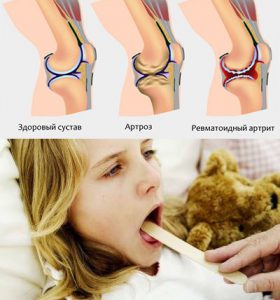
Поствакцинальные артриты у детей
Поствакцинальными называются изменения, происходящие в организме после проведения профилактической вакцинации и являющиеся физиологическими реакциями. Они не оставляют последствий для здоровья и характеризуются непродолжительностью (от нескольких часов до недель).

Поствакцинальные реакции могут быть:
- местные – затрагивают только место введения препарата (например, покраснение, болезненность и отек);
- общие – влияют на весь организм (например, повышение температуры тела).
Одной из общих поствакцинальных реакций может быть артрит.
Все поствакцинальные реакции могут быть:
- слабыми;
- средними;
- сильными.
О силе местных реакций судят по степени выраженности изменений в месте инъекции. Общие поствакцинальные реакции в основном оцениваются по степени повышения температуры тела.
В настоящее время средние и сильные реакции на введение вакцин отмечаются редко. Это связано с высоким качеством современных вакцин. Если у ребенка отмечалась сильная поствакцинальная реакция на введение какого-либо препарата, то повторное введение того же средства противопоказано.
По клиническим проявлениям поствакцинальный артрит похож на реактивный, а по своей морфологической характеристике он является иммунным синовитом.
Поствакцинальный артрит могут вызывать любые вакцины: 
- против краснухи;
- против кори;
- БЦЖ;
- АКДС;
- против ветряной оспы;
- против вирусных гепатитов (В и А);
- против эпидемического паротита;
- другие.
Особенности течения поствакцинальных артритов зависят от типа используемых вакцин.
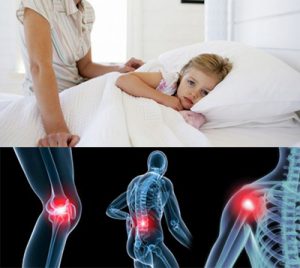
В большинстве случаев поствакцинальный артрит у детей возникает после введения вакцины краснухи, реже – свинки, ветряной оспы или коклюша. У взрослых это осложнение чаще появляется после вакцинации от туберкулеза (вакцина БЦЖ).
Если пациент недавно перенес реактивный артрит или болезнь Рейтера вызванные шигеллой или сальмонеллой, и вводится вакцина против этих возбудителей, то существует риск рецидива воспаления.
Механизм возникновения поствакцинальных реакций связан с тем, что введение любой вакцины вызывает физиологичные изменения в организме: активизация клеток иммунной системы, образование защитных антител и другие реакции. Иногда эти процессы могут сопровождаться клиническими симптомами.
Причины возникновения поствакцинального артрита связывают с индивидуальными особенностями организма, патологией иммунной системы. Доказан повышенный риск возникновения этого состояния у людей, имеющих антиген HLA-B27.
Симптомы поствакцинального артрита у детей
Типичные проявления поствакцинального артрита следующие:
Редко воспаление суставов может сочетаться с симптомами васкулита или аллергической реакции (покраснение, зуд, отечность в месте введения вакцины). Иногда поствакцинальный артрит возникает вместе с патологическими признаками, схожими с проявлениями болезни Рейтера. Однако инфицирования хламидиями или другими микроорганизмами не наблюдается.

Возможно возникновение артралгии без внешних изменений суставов.
Как правило, течение поствакцинального артрита доброкачественное. Проявления заболевания обычно проходят полностью, возможно даже спонтанно за 10-14 дней. Но при следующем плановом введении вакцины симптомы артрита могут вернуться с большей интенсивностью. Если поражение сустава не исчезает или даже усиливается, значит, скорее всего, это не поствакцинальный, а какой-либо другой артрит.
В редких случаях возможно тяжелое течение поствакцинального артрита с хронизацией процесса. Как правило, такой вариант возникает после введения вакцины против краснухи (моно- или в составе других препаратов). Этот артрит является уже не поствакцинальной реакцией, а побочным эффектом от введения вакцины.
Из-за того, что проявления патологии возникают отсрочено, через несколько недель после вакцинации, и быстро исчезают, многие родители не догадываются об их связи со сделанной прививкой.
Существуют особенности течения артрита, в зависимости от введенной вакцины и места введения. Так, у взрослых больных описаны характерные проявления артрита, после введения БЦЖ для лечения онкологической патологии мочевого пузыря. При этом у женщин при внутримышечном введении вакцины возможно возникновение симметричного артрита мелких суставов, напоминающего ревматоидный, который сопровождается утренней скованностью. А у мужчин при введении препарата в виде инстилляций в мочевой пузырь возможно возникновение асимметричного моноартрита с поражением суставов нижних конечностей и крестцово-подвздошных сочленений.
Специфических методов определения поствакцинального артрита не существует.
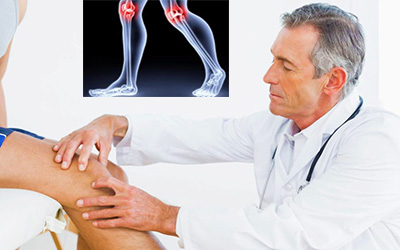
Основные мероприятия направлены на исключение более тяжелых вариантов артрита – ревматоидного, ревматического, инфекционного и других. Для этого необходимо обратиться к врачу сразу после появления симптомов заболевания.
Помогают в постановке диагноза сведения о проведенной профилактической вакцинации в течение последнего месяца. Поэтому родителям следует знать, какой препарат вводился ребенку и когда. Если побочные эффекты во время использования каких-либо медикаментов или аллергические реакции возникали ранее, необходимо сообщить специалисту их характер и то, какими лекарственными средствами эти симптомы купировались.
План обследования включает:
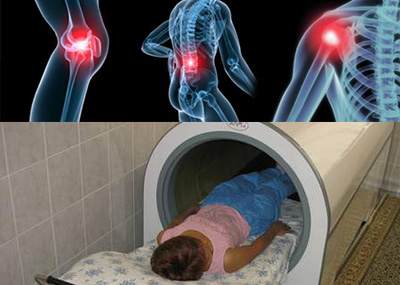
- Лабораторные исследования:
- Инструментальные исследования: рентгенография пораженных суставов для исключения деструктивных и других изменений. Могут также использоваться УЗИ сустава, КТ и МРТ, диагностическая пункция.
Лабораторные исследования включают в себя:
- общий и биохимический анализы крови для исключения воспалительных и инфекционных изменений;
- специальные исследования: определение ревматоидного фактора, антинуклеарных антител, циркулирующих иммунных комплексов, иммуноглобулинов различных классов, антигенов HLA.
Лечение поствакцинального артрита
В случае истинного поствакцинального артрита, симптомы заболевания проходят даже при отсутствии терапии. Однако для наблюдения и проведения диагностических ме 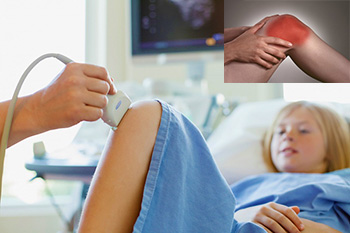
роприятий ребенок должен находиться в стационаре.
Применяются следующие методы лечения:
- Медикаментозные средства:
- нестероидные противовоспалительные препараты – для уменьшения проявлений воспаления, боли;
- симптоматические средства – обезболивающие, противоаллергические и другие препараты.
- Курс физиотерапевтических процедур – показан после стихания воспалительного процесса.
- Лечебная физкультура – проводится при остаточных проявлениях заболевания для восстановления полного объема движений в суставах.
Прогноз заболевания благоприятный. Через 10-14 дней симптомы полностью исчезают, не оставляя после себя никаких патологических изменений.
Специфических мер профилактики поствакцинального артрита не существует. Однако после возникновения подобного побочного эффекта от введения препарата, многие родители начинают бояться проведения профилактической вакцинации. Совсем отказываться от прививок не стоит, ведь они направлены на защиту организма от серьезных инфекционных заболеваний. Но чтобы предотвратить возможные побочные эффекты в будущем, введение вакцин следует проводить по индивидуальному графику под контролем врача-иммунолога.
Современные препараты обладают низкой вероятностью развития побочных эффектов после введения. Перед введением вакцины квалифицированный специалист расскажет, на какие возможные реакции следует обращать внимание.
Также необходимо придерживаться следующих правил:
- Не следует делать прививки сразу после перенесенных инфекционных и других заболеваний, аллергических реакций, отдыха в других климатических зонах, стрессовых ситуаций (например, первый поход в школу или детский сад). Все эти факторы увеличивают риск возникновения поствакцинального артрита.
- С особой настороженностью при проведении профилактической вакцинации следует относиться к детям, страдающим аллергическими реакциями, патологией иммунной системы, имеющим отягощенную наследственность (носители антигена HLA-B27).
- Необходимо наблюдать за ребенком после проведения прививки, избегать стресса и чрезмерных физических нагрузок.
- Детям, страдающим аллергическими реакциями, следует за несколько дней до и после вакцинации соблюдать гипоаллергенную диету. Маленьким детям в этот период не следует вводить новые блюда прикорма.
- Хотя бы несколько дней после прививания не следует посещать организованный коллектив (детский сад, школу), поликлиники, стационары и места скопления большого количества людей, чтобы предотвратить возможные инфекционные заболевания.
Как лечить ребенка, заболевшего артритом?
Мы привыкли считать артрит проблемой бабушек и у дедушек, но, к сожалению, дошколята тоже нередко сталкиваются с этим противным заболеванием. Правда, возникающие у малышей проблемы с суставами вылечить значительно легче, главное — не запускать процесс!
В общем и целом
Артрит — это воспаление сустава и, прежде всего, его синовиальной оболочки, то есть "пленки", выстилающей изнутри всю суставную полость. Статистика свидетельствует: из 100 тысяч дошкольников этой болезнью страдают Процент не то чтобы очень высокий, но и незначительным его не назовешь. Ситуация усугубляется еще и тем, что артрит не всегда удается правильно диагностировать, ведь эта болячка умеет приобретать самые разнообразные формы.
Какие они бывают?
Реактивный артрит. Возникает как осложнение после перенесенных кишечных или мочеполовых инфекций.
Вирусные артриты. Эта разновидность болезни провоцируется вирусными инфекциями — краснухой, гепатитом В, парвовирусными и энтеровирусными инфекциями и эпидемическим паротитом.
Постстрептококковый артрит (раньше его называли ревматизмом). Вызывается артстрептококковой инфекцией.
Поствакцинальный артрит. Как понятно из названия, "ноги" здесь растут из неудачно сделанной прививки.
Ювенильный ревматоидный артрит. Аутоиммунное воспаление, при котором организм начинает как бы "переваривать" собственные ткани.
Существуют также инфекционные артриты, при которых микроб "забирается" непосредственно в сустав и вызывает там гнойное воспаление, артрит после перенесенной травмы, туберкулезный артрит и множество других вариантов. В этой статье мы рассмотрим формы болезни, наиболее распространенные среди детей.
Важно. Если вы подозреваете у ребенка артрит, немедленно ведите его к педиатру. Врач назначит анализы и по их результатам решит, нужно малышу ложиться в больницу или родители могут лечить его дома.
Реактивный артрит
Отличительная особенность этой формы артрита — стерильность: несмотря на то что ребенок недавно переболел, в пострадавшем суставе нет вредных микроорганизмов. Правда, радоваться этому обстоятельству не стоит: клеточная стенка болезнетворного микроба активизирует лимфоциты, а те, в свою очередь, выделяют большое количество антител, с помощью которых образуются так называемые иммунные комплексы. Вот эти-то комплексы и вызывают воспаление. К счастью, такая цепочка выстраивается не всегда, а только в случае совпадения двух факторов: ребенок подхватывает где-то инфекцию (сальмонеллез, дизентерия, иерсиниоз, псевдотуберкулез, хламидиоз) и одновременно у него обнаруживается генетическая предрасположенность к заболеваниям суставов. В этом случае через недели после выздоровления суставы внезапно начинают болеть: руки, ноги или, скажем, пальцы отекают, краснеют и становятся непослушными. Для реактивных артритов характерна несимметричность: страдают, например, не обе коленки сразу, а одна (допустим, слева) и голеностоп (справа). Еще одна особенность заболевания — небольшое количество очагов: от одного до четырех. Классический пример реактивного артрита — синдром Рейтера, который проявляется воспалением суставов (артрит), слизистой глаз (конъюнктивит) и уретры (уретрит). На ощупь "болевые точки" заметно горячее других, а кожа над ними может покраснеть и даже покрыться сухими, шелушащимися бляшками (они впоследствии проходят самостоятельно). Поставить диагноз не так легко, как кажется. Если артрит начался через месяц после перенесенной кишечной инфекции, то родители могут и не вспомнить о ней в беседе с доктором. Именно поэтому изрядная часть анализов, назначаемых при реактивном артрите, направлена на поиск возможной "заразы".
Итак, что назначит врач, подозревающий у ребенка именно это заболевание?
- Общие анализы крови и мочи. При реактивных артритах в них наблюдаются воспалительные изменения.
- Специальные анализы крови (из вены) для определения перенесенных кишечных или мочеполовых инфекций.
- Биохимический анализ крови. Необходим для исключения других заболеваний, при которых проявления артрита сочетаются с поражением печени или почек. Кроме того, по результатам этого исследования можно узнать, не было ли у ребенка "стрептококка".
- Анализ крови для исключения аутоиммунных заболеваний суставов (из вены).
- Анализ мочи и кала на наличие болезнетворных микробов.
Кроме того, при необходимости врач может попросить вас сделать мазок из носа и зева и отправить пациента на УЗИ и/или рентген воспаленных суставов.
А еще ребенка обязательно должен осмотреть офтальмолог: как правило, сопутствующий артриту конъюнктивит проходит бесследно, но у некоторых малышей может начаться увеит (воспаление сосудистой оболочки глаза), требующий немедленного медицинского вмешательства.
Лечение реактивного артрита включает в себя.
Покой. Необходимо создать такие условия, при которых малышу не придется напрягать пораженные суставы.
Нестероидные противовоспалительные средства. Врач назначает ибупрофен, диклофенак, индометацин или нимесулид — эти препараты возвращают суставам подвижность, а также уменьшают воспаление и боль.
Антибиотики. Их прописывают строго в определенных случаях: при рецидивирующем или хроническом реактивном артрите, при хламидийной природе заболевания, при выявлении кишечной инфекции или при обнаружении хронического источника инфекции в носоглотке.
Гормональные препараты. Такие средства используются исключительно при тяжелых артритах, против которых бессильны нестероидные лекарства.
Физиотерапия. На стадии затихания воспаления и в период восстановления малыша активно используются фонофорез, магнито- и парафинолечение и лечебная физкультура.
Важно. Как правило, на фоне лечения облегчение наступает через а через дней малыш чувствует себя здоровым. И тут у уже успокоившихся родителей возникает вопрос: "Это точно больше не повторится?!" К сожалению, рецидивы реактивного артрита случаются, поэтому следить за состоянием здоровья ребенка нужно очень внимательно. Важно оперативно реагировать на все очаги "долгоиграющей" инфекции, например на хронический тонзиллит или кариес. Определить генетическую предрасположенность к артритам довольно просто: если родители карапуза или его бабушки с дедушками страдают "суставными" болями, значит, и у наследника могут возникнуть подобные проблемы.
Вирусные артриты
Мы уже говорили о том, что такая форма болезни возникает на фоне вирусных заболеваний, а именно:
- краснухи (с появлением сыпи или за несколько дней до этого симметрично опухают и начинают болеть, колени, запястья, голеностопы и суставы рук);
- парвовирусной инфекции (в разгар заболевания начинают опухать пальцы и запястья);
- аденовирусной инфекции (через дней после появления "простудных" симптомов развивается симметричный артрит коленных суставов, запястий и голеностопов);
- гриппа и других вирусных респираторных инфекций (на фоне повышения температуры могут появиться кратковременная припухлость и летучие боли в суставах);
- энтеровирусной инфекции (суставы начинают болеть на фоне повышения температуры и возможного нарушения стула);
- эпидемического паротита, т.е. свинки (артрит появляется спустя недели после исчезновения симптомов заболевания и поражает крупные суставы). Большинство вирусных артритов, как правило, проходят самостоятельно — через а для облегчения боли врачи обычно используют нестероидные противовоспалительные средства.
Постстрептококковый артрит
Стрептококки группы А вызывают острый тонзиллит (ангину) и/или фарингит. Если вовремя не начать лечение антибиотиками, иммунная система может принять болезнетворные микроорганизмы за собственные клетки организма — научившись уничтожать стрептококки, она точно так же начинает бороться с сердцем и суставами. В результате через недели после перенесенной инфекции возникает артрит, затрагивающий преимущественно колени, локти, запястья и голеностоп, при этом воспаление быстро "перескакивает" с одного сустава на другой. Диагностировать постстрептококковый артрит помогает анализ крови, выявляющий резкое увеличение количества специфических противострептококковых антител.
Важно. В случае постстрептококкового артрита ребенком должен заниматься кардиоревматолог! Готовьтесь к длительному лечению с курсами антибиотиков.
Поствакцинальные артриты
Как правило, такой артрит вызывается прививкой против краснухи (комплексной или "моно"). Реже воспаление возникает после вакцинирования от свинки, коклюша или ветряной оспы. Признаки артрита появляются через недели после укола, но через пять дней они бесследно проходят.
Ювенильный и ревматоидный артрит
Тяжелое системное заболевание, затрагивающее не только суставы, но и внутренние органы, чаще всего встречается у девочек Такой артрит может начинаться остро (повышение температуры и сильные боли) или постепенно — без жара, с медленным нарастанием отека и чувствительности. По утрам ребенок чувствует скованность в движениях, которая обычно проходит к вечеру, но возвращается на следующий день. Еще одна особенность болезни — симметричное поражение суставов. Нередко воспаляются и оболочки глаза — это выявляется при офтальмологическом осмотре. При ювенильном ревматоидном артрите врач назначает ребенку гормональные, нестероидные противовоспалительные препараты и — обязательно — иммуносупрессивные средства.
Одной из актуальных проблем современной педиатрии является диагностика и лечение воспалительных заболеваний суставов. Наиболее распространен среди ревматических заболеваний детского возраста реактивный артрит (РеА), который встречается
Одной из актуальных проблем современной педиатрии является диагностика и лечение воспалительных заболеваний суставов. Наиболее распространен среди ревматических заболеваний детского возраста реактивный артрит (РеА), который встречается у 86,9 на 100 000 детского населения [1].
В настоящее время к РеА относят воспалительные негнойные заболевания суставов, развивающиеся вследствие иммунных нарушений, после кишечной или урогенитальной инфекции. В преобладающем большинстве случаев РеА ассоциируется с острой или персистирующей кишечной инфекцией, вызываемой энтеробактериями (Yersinia enterocolitica, Yersinia pseudotuberculosis, Salmonella enteritidis, Salmonella typhimurium, Shigella flexneri, Shigella sonnei, Shigella Newcastle, Campylobacter jejuni), и с острой или персистирующей урогенитальной инфекцией, вызываемой Chlamydia trachomatis. Инфекции респираторного тракта, связанные с Mycoplasma pneumoniae, и особенно Chlamydophila pneumonia, также могут служить причинами развития РеА. Имеются также данные о связи РеА с кишечной инфекцией, вызванной Clostridium difficile и некоторыми паразитарными инфекциями.
РеА, ассоциированный с кишечной инфекцией и инфекцией, вызванной Chlamydia trachomatis, развивается преимущественно у генетически предрасположенных лиц (носителей HLA-B27) и относится к группе серонегативных спондилоартритов [2, 3, 6]. Было обнаружено, что антитела к ряду микроорганизмов перекрестно реагируют с HLA-B27. Это объясняется феноменом молекулярной мимикрии, согласно которой белки клеточной стенки ряда кишечных бактерий и хламидий имеют структурное сходство с отдельными участками молекулы HLA-B27. Предполагается, что перекрестно реагирующие антитела способны оказывать повреждающее действие на собственные клетки организма, которые в наибольшей степени экспрессируют молекулы HLA-B27. Но при этом считают, что такое перекрестное реагирование может препятствовать осуществлению адекватного иммунного ответа, способствуя персистированию и хронизации инфекции. Имеются данные, что у носителей НLA-B27 после перенесенной кишечной и урогенитальной инфекции РеА развивается в 50 раз чаще, чем у лиц, не имеющих этого антигена гистосовместимости.
Диагноз РеА ставится в соответствии со следующими диагностическими критериями, принятыми на III Международном совещании по РеА в Берлине в 1996 г. [7].
– Олигоартрит (поражение до 4 суставов).
– Преимущественное поражение суставов ног.
– Время возникновения: за 2–4 нед до развития артрита.
Лабораторное подтверждение инфекции:
– Необязательно, но желательно при наличии клинических проявлений инфекции.
– Обязательно, при отсутствии явных клинических проявлений инфекции.
Критерии исключения — установленная причина развития моно- или олигоартрита:
Вместе с тем в реальной практике термин РеА ошибочно используется ревматологами гораздо шире и включает артриты после перенесенной вирусной инфекции, поствакцинальные артриты, постстрептококковый артрит и некоторые другие.
В настоящее время одной из наиболее распространенных причин развития РеА является хламидийная инфекция.
В структуре РеА хламидийные артриты составляют до 80% [8, 9, 10]. Это связано с пандемией хламидиоза в мире, особенностями путей передачи хламидийной инфекции, цикла развития хламидий и реакции на терапию. Восприимчивость к хламидиям всеобщая, существует множество путей передачи инфекции в том числе и контактно-бытовой путь (в отношении Chlamydia pneumonia). Триггерная роль кишечной инфекции в развитии РеА также остается актуальной.
Классическим проявлением РеА является болезнь Рейтера или уретро-окуло-синовиальный синдром, впервые описанный Бенджамином Броди, а затем Гансом Рейтером, под именем которого синдром и вошел в медицину. Болезнь Рейтера в настоящее время рассматривается как особая форма РеА и характеризуется классической триадой клинических симптомов: уретрит, конъюнктивит, артрит. При наличии кератодермии говорят о тетраде болезни Рейтера. Синдром Рейтера чаще всего начинается с симптомов поражения урогенитального тракта через 2–4 нед после перенесенной инфекции или предполагаемого заражения хламидиями или бактериями кишечной группы. При синдроме Рейтера триггерными инфекционными факторами чаще всего являются Chlamydia trachomatis, Shigella flexneri 2а, либо их сочетание.
Болезнь Рейтера, ассоциированная с хламидийной инфекцией, характеризуется менее выраженной остротой клинической картины [8, 10]. Поражение урогенитального тракта характеризуется стертостью клинической картины. У мальчиков могут развиваться баланит, инфицированные синехии, фимоз. У девочек поражение урогенитального тракта может ограничиваться вульвитом, вульвовагинитом, лейкоцитурией и/или микрогематурией, а также клиникой цистита. Поражение урогенитального тракта может на несколько месяцев опережать развитие суставного синдрома.
Поражение глаз характеризуется развитием конъюнктивита: чаще катарального, невыраженного, непродолжительного, но склонного к рецидивированию. У 1/3 больных может развиться острый иридоциклит, угрожающий слепотой. Поражение глаз также может на несколько месяцев или лет опережать развитие суставного синдрома.
Экссудативный артрит (моно- или олигоартрит) при болезни Рейтера хламидийной этиологии может протекать без боли, скованности, выраженного нарушения функции, но с большим количеством синовиальной жидкости и непрерывно рецидивируя. Поражение суставов при этом характеризуется длительным отсутствием деструктивных изменений, несмотря на рецидивирующий синовит.
Нередко РеА протекает без отчетливых внесуставных проявлений, относящихся к симптомокомплексу синдрома Рейтера (конъюнктивит, уретрит, кератодермия). В таких случаях ведущим является суставной синдром, который также характеризуется преимущественным поражением суставов нижних конечностей, асимметричного характера. Несмотря на отсутствие внесуставных проявлений у этих детей также имеется высокий риск развития ювенильного спондилоартрита. Наличие характерного суставного синдрома, сопровождающегося выраженной экссудацией и связанного с перенесенной кишечной или урогенитальной инфекцией или с наличием серологических маркеров кишечной или урогенитальной инфекции, позволяет с большой долей вероятности отнести заболевание к разряду реактивных артритов.
Диагностика РеА основывается на клинико-анамнестических данных, включающих наличие характерного суставного синдрома, связанного с инфекционным процессом. В связи с тем, что инфекция, предшествующая развитию РеА, не всегда бывает ярко выражена, в процессе диагностики особую значимость приобретают данные дополнительных лабораторных исследований. Для постановки точного диагноза необходимо выделение возбудителя, вызвавшего инфекцию, и/или обнаружение в сыворотке крови высоких титров антител к нему. Для идентификации триггерных инфекций используют различные микробиологические, иммунологические и молекулярно-биологические методы. Этиологическая диагностика включает следующее.
1.1. Выявление антигена хламидий в эпителиальных клетках, полученных в результате соскобов из уретры и конъюнктивы, а также в синовиальной жидкости (прямой иммунофлюоресцентный анализ и др.).
1.2. Выявление антител к антигенам хламидий в сыворотке крови и в синовиальной жидкости (реакция связывания комплемента, прямая и непрямая иммунофлюоресценция):
- острая фаза хламидиоза или обострение хронического процесса — наличие иммуноглобулин (Ig) M в течение первых 5 дней, IgA — в течение 10 дней, IgG — через 2–3 нед;
- реинфекция или реактивация первичной хламидийной инфекции — повышение уровня IgG, определяются IgA, могут быть единичные IgM;
- хроническое течение хламидиоза — наличие постоянных титров IgG и IgA;
- бессимптомное течение хламидиоза, персистенция возбудителя — низкие титры IgA;
- перенесенная хламидийная инфекция — низкий титр IgG.
1.3. Выявление антител к бактериям кишечной группы в сыворотке крови (при помощи реакции прямой гемагглютинации и реакции связывания комплемента).
Наиболее доказательным является выделение триггерных микроорганизмов классическими микробиологическими методами (посевы кала, перенос соскоба с эпителия уретры и/или конъюнктивы на культуру клеток). Чаще удается выделить хламидии из урогенитального тракта, значительно реже — энтеробактерии из кала.
Трудности диагностики РеА часто обусловлены стертым субклиническим течением первичного инфекционного процесса. Артрит развивается чаще при нетяжелых формах кишечной или урогенитальной инфекций, и к моменту развития артрита признаки триггерной инфекции в большинстве случаев проходят. Кроме того, в условиях нарушенного иммунного ответа возможно развитие хронических персистирующих форм инфекции. Поэтому в дебюте суставного синдрома необходимо в первую очередь исключить скрытую кишечную и хламидийную инфекции. Кроме того, диагностику РеА затрудняет сочетание предшествовавших инфекционных процессов различной локализации. Установлено также, что поражение кишечника и мочевыводящих путей может быть как первичным по отношению к РеА, так и развиваться одновременно с ним и даже позже, что нередко затрудняет определение причинно-следственных связей.
Дифференциальный диагноз РеА от других видов ювенильных артритов часто бывает затруднен. Наиболее распространенной патологией, требующей дифференциальной диагностики с РеА, являются инфекционные артриты, заболевания, связанные с инфекцией, сопровождающиеся артритами, а также ортопедическая патология и разные формы ювенильного идиопатического артрита.
Вирусный артрит. В настоящее время известно, что около 30 вирусов могут вызывать развитие острого артрита. К ним относятся: вирусы краснухи, парвовирус, аденовирус, вирус гепатита В, вирусы герпеса различных типов, вирус паротита, энтеровирусы, Коксаки-вирусы и др. Диагностика основана на связи с вирусной инфекцией или проведенной вакцинацией. Клиническая картина чаще представлена артралгиями, чем артритами. Клинические симптомы наблюдаются в течение 1–2 нед и исчезают без остаточных явлений.
Диагностические критерии постстрептококкового артрита включают:
- появление артрита на фоне или спустя 1–2 нед после перенесенной носоглоточной инфекции (стрептококковой этиологии);
- одновременное вовлечение в процесс преимущественно средних и крупных суставов;
- возможную торпидность суставного синдрома к действию нестероидных противовоспалительных препаратов (НПВП), нерезкие сдвиги в лабораторных показателях;
- наличие повышенных титров постстрептококковых антител;
- выявление хронических очагов инфекции в носоглотке (хронический тонзиллит, фарингит, гайморит).
Клещевой боррелиоз (болезнь Лайма). Диагностика боррелиоза основана на данных анамнеза: пребывание пациента в эндемичной зоне, наличие в анамнезе факта укуса клеща, а также характерную клиническую картину. Подтверждают диагноз серологическими методами, которые выявляют антитела к Borrelia burgdorferi.
Диагноз септического артрита ставится на основании клинической картины инфекционного процесса, определения характера синовиальной жидкости, результатов посева синовиальной жидкости на флору с определением чувствительности к антибиотикам, а также рентгенологических данных (в случае развития остеомиелита).
Клиническая картина туберкулезного артрита представлена общими симптомами туберкулезной инфекции: интоксикацией, субфебрильной температурой, вегетативными нарушениями и локальными симптомами — боли в суставах, преимущественно в ночное время, явления артрита. Для подтверждения диагноза необходимы рентгенологические данные, анализ синовиальной жидкости, биопсия синовиальной оболочки.
Ювенильный спондилоартрит. Данное заболевание является возможным исходом хронического течения РеА у предрасположенных лиц (HLA-B27 носителей). Суставной синдром так же, как и при РеА, представлен асимметричным моно- или олигоартритом с преимущественным поражением суставов ног. Кардинальными признаками, позволяющими поставить диагноз ювенильного спондилоартрита, являются рентгенологические данные, свидетельствующие о наличии сакроилеита (одно- или двустороннего).
Выделяют три вида терапии: этиотропную, патогенетическую, симптоматическую.
Этиотропное лечение РеА, ассоциированного с хламидийной инфекцией. Поскольку хламидии являются внутриклеточными паразитами, то выбор антибактериальных препаратов ограничивается только теми, которые способны накапливаться внутриклеточно. К таким препаратам относятся макролиды, тетрациклины и фторхинолоны. Однако тетрациклины и фторхинолоны достаточно токсичны, их применение ограничено в детской практике. В связи с этим для лечения хламидийного артрита у детей используются макролиды. Азитромицин — для детей в первый день приема доза препарата составляет 10 мг/кг, а в последующие 5–7 дней — 5 мг/кг в один прием. Лучший эффект достигается при использовании антибиотика в течение 7–10 дней. Рокситромицин — для детей суточная доза составляет 5–8 мг/кг массы тела. Джозамицин (вильпрафен) суточная доза препарата составляет 30–50 мг/кг массы тела, разделенные на три приема. Кларитромицин используется у детей старше 6 мес — 15 мг/кг/сут в 2 приема, спирамицин — детям массой более 20 кг из расчета 1,5 млн МЕ/10 кг массы тела в сутки. Кратность приема — 2–3 раза.
У подростков возможно применение тетрациклинов и фторхинолоновых препаратов.
В отношении РеА, связанных с кишечной инфекцией, однозначных рекомендаций по антибактериальной терапии не существует. Наличие антител к бактериям кишечной группы и особенно бактериологическое подтверждение кишечной инфекции является основанием для назначения антибиотиков. Используются аминогликозиды — амикацин в/м или в/в — до 15 мг/кг/сут в одно-два введения, 7 сут, гентамицин в/м или в/в 5–7 мг/кг/сут в два введения, 7 сут, фторхинолоновые препараты (для детей старше 12 лет).
Патогенетическая терапия. Монотерапия антибиотиками оказывает недостаточный эффект при затяжном и хроническом течении РеА, неадекватности иммунного ответа. Целесообразно для лечения хронического хламидийного артрита использовать различные иммуномодулирующие средства (тактивин, ликопид, полиоксидоний) в сочетании с антибиотиками.
Наиболее эффективной, по результатам многолетних контролируемых исследований, оказалась схема с использованием ликопида [8, 10, 13].
Схема комбинированной терапии ликопидом и антибиотиками у больных с хроническим течением РеА, ассоциированного с хламидийной инфекцией, следующая.
- Ликопид применяется в виде сублингвальных таблеток. Детям до 5 лет целесообразно назначать ликопид по 1 мг 3 раза в день, дети старше 5 лет — ликопид по 2 мг 3 раза в день. Курс лечения составляет 24 дня.
- На 7-й день приема ликопида назначается антибиотик. Возможно использование любого антибиотика, обладающего противохламидийной активностью. Так как необходимо перекрыть 2–3 жизненных цикла хламидий, курс лечения антибиотиком должен составлять не менее 7–10 дней.
- После завершения курса антибактериальной терапии дети продолжают получать ликопид до 24 дня.
Использование иммуномодуляторов противопоказано при трансформации РеА в спондилоартрит, высокой иммунологической активности.
Симптоматическая терапия. С целью лечения суставного синдрома при РеА применяют НПВП. Диклофенак внутрь 2–3 мг/кг/день в 2–3 приема или напроксен внутрь 15–20 мг/кг/день в 2 приема или ибупрофен внутрь 35–40 мг/кг в 2–4 приема или нимесулид внутрь 5 мг/кг в 2–3 приема или мелоксикам внутрь 0,3–0,5 мг/кг в 1 прием.
Глюкокортикостероиды как наиболее мощные противовоспалительные средства используются в период обострения суставного синдрома. Их применение ограничивается преимущественно внутрисуставным способом введения. При необходимости можно воспользоваться коротким курсом пульс-терапии метилпреднизолоном, который предполагает быстрое (в течение 30–60 мин) внутривенное введение больших доз метилпреднизолона (5–15 мг/кг в течение 3 дней).
При тяжелом и торпидном течении заболевания, появлении признаков спондилоартрита, высокой клинической и лабораторной, в том числе иммунологической, активности возможно применение иммуносупрессивных препаратов. Наиболее часто используется сульфасалазин (в дозе 30–40 мг/кг массы в сутки), реже метотрексат ( в дозе 10 мг/м 2 в неделю).
У большинства детей РеА заканчивается полным выздоровлением. У части больных эпизоды РеА рецидивируют и в дальнейшем появляются признаки спондилоартрита, особенно у HLA-B27 позитивных больных. Мерами профилактики являются своевременное выявление хламидийной инфекции у ребенка и членов его семьи, адекватная терапия урогенитальной инфекции.
Е. С. Жолобова, доктор медицинских наук, профессор
Е. Г. Чистякова, кандидат медицинских наук, доцент
Д. В. Дагбаева
ММА им. И. М. Сеченова, Москва
Читайте также:


