Подагрический артрит национальные рекомендации
Рассмотрены подходы к лечению подагры в соответствии с современными рекомендациями. Уделено внимание и немедикаментозным методам профилактики, представлены рекомендации по диетотерапии при подагре.
Approaches to gout therapy were considered according to modern guidelines. Attention was also paid to non-drug methods of prevention, guidelines on dietary treatment in gout were presented.
Подагра является наиболее частой причиной артрита [1], что обусловлено отложением кристаллов моноурата натрия (МУН) в суставах и мягких тканях. Для формирования кристаллов МУН необходима персистирующая гиперурикемия. При повышении сывороточного уровня мочевой кислоты (МК) происходит насыщение тканей МУН, что создает условия для его кристаллизации и, соответственно, манифестации подагры [2]. Порог насыщения МК составляет около 7 мг/дл (420 мкмоль/л), хотя для пациентов с подагрой рекомендуется достигать сывороточный уровень МК менее 6 мг/дл (360 мкмоль/л), поскольку такой уровень МК приводит к более быстрому уменьшению кристаллических отложений МУН [3–6].
Достигнутые в настоящее время успехи в понимании основных механизмов развития хронической гиперурикемии и подагры позволили пересмотреть многие положения, лежащие в основе диагностики и лечения заболевания. Между тем, несмотря на успехи в понимании патофизиологии подагры и доступность эффективных методов лечения, подагра остается плохо контролируемым заболеванием во всех странах [7, 8]. Пожалуй, самой распространенной проблемой является низкая приверженность пациентов к снижению сывороточного уровня МК, что главным образом связано с недостаточным пониманием цели терапии подагры и врачами, и пациентами. Целесообразно объяснить пациентам цель лечения [9–11], которая заключается в растворении имеющихся отложений кристаллов МУН путем снижения сывороточного уровня МК ниже точки насыщения сыворотки уратами и купировании приступов артрита, если таковые возникают. Следует также поддерживать сывороточный уровень МК ниже порога насыщения, чтобы избежать образования новых кристаллов.
Целью настоящей статьи было предоставить практический обзор существующих подходов к управлению заболеванием в четырех аспектах: немедикаментозные методы профилактики и лечения гиперурикемии; купирование острого приступа артрита; уратснижающая терапия, направленная на профилактику приступов артрита и образование тофусов; профилактика приступов артрита при инициации уратснижающей терапии.
Лечение подагры в соответствии с современными рекомендациями направлено на улучшение исходов заболевания. Эффективность лечебно-профилактических вмешательств при подагре зависит от четкого следования предложенной в них концепции лечения [4, 12, 13].
Немедикаментозные методы профилактики, нацеленные на модификацию факторов образа жизни, связанных с риском развития гиперурикемии, предусматривают индивидуальное или групповое профилактическое консультирование по актуальным вопросам диетотерапии, контролю массы тела при ожирении, достижению целевых уровней артериального давления, коррекции нарушений углеводного и липидного обмена.
Ожирение является ведущим фактором риска подагры, особенно у мужчин, соответственно, контроль массы тела оказывает существенное влияние на частоту приступов подагры [14]. Снижение веса за счет ограничения общей калорийности пищи и потребления углеводов благотворно влияет на уровни сывороточного урата у пациентов с подагрой [15, 16].
Следует отметить, что в настоящее время пересмотрены некоторые принципиальные позиции по диетотерапии при подагре. Так, рекомендация по жесткому ограничению в пищевом рационе пуринсодержащих продуктов распространяется только на животные производные (мясо, морепродукты), поскольку именно такая мера способствует снижению сывороточного уровня мочевой кислоты. При этом богатая пуринами растительная пища не оказывает существенного влияния на урикемию [4, 17]. Показано, что потребление обезжиренных молочных продуктов [18, 19], растительных масел и овощей ассоциируется с уменьшением риска гиперурикемии и приступов подагры [4, 12]. Витамин С увеличивает почечную экскрецию мочевой кислоты, поэтому его можно использовать в качестве дополнительной меры при терапии подагры [20, 21]. Безопасным в отношении сывороточного уровня МК и риска развития подагры считается потребление небольшого количества сухого вина [20, 22]. При этом потребление пива, в т. ч. безалкогольного, крепких спиртных напитков, а также подслащенных безалкогольных напитков с высоким содержанием фруктозы должно быть ограничено максимально [20, 23–25].
Несмотря на то, что основная масса клинических исследований затрагивают оценку эффективности диетотерапии в аспекте профилактики риска развития подагры, а не управления частотой приступов артрита у лиц с верифицированным диагнозом, рекомендации по модификации образа жизни должны даваться всем пациентам с подагрой, в т. ч. получающим медикаментозную терапию.
В современных рекомендациях в качестве препаратов первой линии противовоспалительной терапии рассматриваются нестероидные противовоспалительные средства (НПВС), колхицин и глюкокортикостероиды (ГК) [4, 12, 13]. Сравнительно недавний систематический обзор показал, что НПВС (в том числе селективные ингибиторы ЦОГ-2), ГК (перорально и внутримышечно), колхицин и ингибитор ИЛ-1β (канакинумаб) являются эффективными методами лечения острых приступов [26]. Целесообразность персонифицированного выбора режима терапии обусловлена и индивидуальными особенностями больного, и гетерогенностью собственно подагрического процесса, протекающего с вовлечением многих органов и систем организма, что существенно модифицирует фармакодинамику препаратов, приводя к кумуляции нежелательных эффектов.
Терапия НПВС занимает лидирующие позиции в лечении как острого приступа, так и хронического подагрического артрита. Считается, чем раньше назначен препарат, тем быстрее может быть достигнут анальгетический эффект. НПВС следует использовать в максимальных суточных дозах, которые могут быть уменьшены по мере ослабления симптоматики. Выбор конкретного НПВС во многом зависит от личных предпочтений. И селективные ингибиторы ЦОГ-2, и традиционные НПВС эффективны при лечении острых приступов подагрического артрита. Недавний систематический обзор, объединяющий результаты шести рандомизированных клинических исследований (851 пациент), продемонстрировал одинаковый эффект эторикоксиба (120 мг в сутки), индометацина и диклофенака при остром артрите, с лучшей у эторикоксиба переносимостью со стороны желудочно-кишечного тракта [27]. Другой селективный ингибитор ЦОГ-2 — целекоксиб также обнаружил сопоставимый с индометацином эффект в отношении умеренной и выраженной боли у пациентов с острым подагрическим артритом [28]. Еще в одном систематическом обзоре был сделан вывод о том, что НПВС и селективные ингибиторы ЦОГ-2 обнаруживают эквивалентные преимущества в плане уменьшения боли, отечности и улучшения общего самочувствия, однако традиционные НПВС отличаются большей частотой отмены из-за нежелательных явлений [29].
Колхицин — алкалоид, получаемый из растения безвременника осеннего (Colchicum autumnae), используется для лечения острой подагры на протяжении многих десятилетий. Клинические исследования и ежедневная рутинная практика демонстрируют высокую частоту побочных эффектов при применении колхицина, которые, вероятно, можно объяснить назначением в прошлые годы более высоких доз препарата, чем рекомендованы в настоящее время. По крайней мере, большое многоцентровое исследование пациентов с подагрой и сохраненной функцией почек убедительно показало сопоставимую эффективность двух режимов терапии острого подагрического артрита: низкодозового (1,8 мг колхицина в сутки: 1,2 мг сразу и 0,6 мг через час) и высокодозового (4,8 мг колхицина в сутки: 1,2 мг сразу и по 0,6 мг каждый час; 6 раз), с существенно меньшей частотой побочных эффектов со стороны желудочно-кишечного тракта в группе с низкой дозой. Причем эффективность низких доз колхицина была эквивалентна высоким в том случае, если колхицин в низких дозах назначался в течение первых 12 часов после начала острого приступа артрита [30]. Клиническая практика показывает, что колхицин оказывается гораздо менее эффективным, если его назначают после 12–24 часов от начала приступа. Соответственно, более позднее назначение может потребовать больших доз препарата, что практически всегда заканчивается развитием нежелательных лекарственных реакций.
Согласно современным национальным рекомендациям для купирования острой атаки артрита целесообразным считается назначение у большинства пациентов низких доз колхицина (1,5 мг в первые сутки (1 мг сразу и через 1 час еще 0,5 мг) и по 1 мг со следующего дня) [13].
Назначение ГК для купирования острого приступа подагры возможно в виде внутрисуставных (после удаления синовиальной жидкости), внутримышечных инъекций или внутрь.
Пероральный прием преднизолона в суточной дозе 30–35 мг/сут демонстрирует высокую эффективность [31, 32] и рекомендуется группами Американского колледжа ревматологов (American College of Rheumatology, ACR) и Европейской антиревматической лиги (European League Against Rheumatism, EULAR) в качестве терапии первой линии при лечении острого приступа подагры [12, 33]. При этом стартовая доза преднизолона 30–35 мг/сут назначается на несколько (3–6) дней с последующей быстрой (в течение 1 недели) полной отменой.
Внутримышечное введение ГК может быть применено в случаях полиартикулярного поражения суставов [34]. Внутрисуставные инъекции стероидов оказываются очень эффективными и рекомендуются как ACR, так и EULAR при моно- или полиартикулярном поражении суставов, несмотря на отсутствие рандомизированных клинических исследований [12, 33].
Однако важно отметить, что, вопреки бытующему мнению, прием преднизолона не эффективнее НПВС. Так, сравнение двух режимов терапии (преднизолон 35 мг/сут и напроксен 1000 мг/сут) у пациентов с острым подагрическим артритом показало отсутствие различий в динамике интенсивности боли при сопоставимой частоте нежелательных эффектов [35]. Кроме того, ГК не безопаснее НПВС, поскольку способны усугубить течение артериальной гипертонии и сахарного диабета [36]. В исследовании [37] частота побочных эффектов даже на однократное внутрисуставное введение ГК (бетаметазон 7 мг) оказалась чрезвычайно высокой: у 73% пациентов обнаружилось клинически значимое повышение уровня систолического артериального давления, у 23% — гликемия натощак, у 13% — ЭКГ-признаки ишемии миокарда.
При наличии абсолютных противопоказаний и/или неэффективности НПВС, колхицина и ГК, а также отсутствии текущей инфекции, с целью купирования острого артрита возможно применение моноклональных антител к ИЛ-1 (канакинумаб) [12].
Уратснижающая терапия, основной целью которой является предупреждение образования и растворение имеющихся кристаллов МУН, возможна посредством достижения уровня МК ниже точки супернасыщения сыворотки уратами (
М. И. Шупина 1 , кандидат медицинских наук
Г. И. Нечаева, доктор медицинских наук, профессор
Е. Н. Логинова, кандидат медицинских наук
ФГБОУ ВО ОмГМУ МЗ РФ, Омск
Версия: Клинические рекомендации РФ (Россия) 2013-2017
Общая информация
Общероссийская общественная организация Ассоциация ревматологов России
Федеральные клинические рекомендации "Подагра"
Клинические рекомендации "Подагра" прошли общественную экспертизу, согласованны и утверждены 17 декабря 2013 г., на заседании Пленума правления АРР, проведенного совместно с профильной комиссией МЗ РФ по специальности "ревматология". (Президент АРР, академик РАН - Е.Л.Насонов)
Общая характеристика болезни
Основные клинические проявления подагры: рецидивирующие атаки острого артрита, накопление кристаллов уратов в тканях с образованием тофусов, нефролитиаз, подагрическая нефропатия.
В развитии подагры выделяют 3 стадии:
- острый подагрический артрит
- периоды между приступами подагрического артрита (межприступная подагра)
- хроническая тофусная подагра.


Классификация
Для диагностики подагрического артрита в 1975 году Американской Ассоциацией Ревматологов (ААР) были рекомендованы предварительные классификационные критерии, одобренные ВОЗ в 2002 году.
Классификационные критерии острого подагрического артрита
А. Наличие характерных кристаллов мочевой кислоты в суставной жидкости
Б. Наличие тофусов, содержание кристаллов мочевой кислоты, в которых подтверждено химически или поляризационной микроскопией
В. Наличие 6 из 12 ниже перечисленных признаков:
1. Более одной атаки острого артрита в анамнезе
2. Воспаление сустава достигает максимума в 1-й день болезни
3. Моноартрит
4. Гиперемия кожи над пораженным суставом
5. Припухание и боль в первом плюснефаланговом суставе
6. Одностороннее поражение первого плюснефалангового сустава
7. Одностороннее поражение суставов стопы
8. Подозрение на тофусы
9. Гиперурикемия
10. Асимметричный отек суставов
11. Субкортикальные кисты без эрозий (рентгенография)
12. Отрицательные результаты при посеве синовиальной жидкости
Диагностика
Демонстрация кристаллов моноурата натрия (МУН) в синовиальной жидкости или в содержимом тофуса позволяет поставить определенный диагноз подагры (уровень доказательности IIb). Специфичность метода поляризационной микроскопии для демонстрации кристаллов крайне высока.
Основным клиническим проявлением, который позволяет заподозрить подагру является острый артрит. Острая атака с быстрым развитием выраженной боли и воспаления, которые достигают максимума в течение 6-12 часов, особенно сопровождающиеся эритемой, высоко подозрительны в отношении микрокристаллического воспаления, хотя не специфичны для подагры (уровень доказательности IIb).
Рутинный поиск кристаллов рекомендуется в любой синовиальной жидкости, полученной из воспаленного сустава у больных с отсутствием определенного диагноза (уровень доказательности IV).
Пунктировать суставы в диагностических целях можно и в межприступный период. Идентификация кристаллов МУН из невоспаленного сустава обеспечивает определенный диагноз в межприступном периоде (уровень доказательности IIb).
Подагра и сепсис могут сосуществовать, поэтому при подозрении на септический артрит окраска по грамму и исследования культуры синовиальной жидкости должны выполняться даже в случае идентификации кристаллов МУН (уровень доказательности IIb). Гораздо чаще септического артрита развиваются нагноения мягких тканей в области вскрывшихся подкожных тофусов.
Несмотря на то, что ГУ является наиболее важным фактором риска подагры, сывороточный уровень МК не является фактором исключения или подтверждения подагры: многие люди с ГУ не развивают подагры, а во время острой атаки сывороточный уровень МК может быть нормальным (уровень доказательности Ib).
Почечная экскреция мочевой кислоты должна определяться у некоторых больных подагрой, имеющих семейную историю подагры с ранним началом, начало подагры ранее 25 лет, с анамнезом МКБ (уровень доказательности IIb).
Рентгенологическое исследование суставов помогает в проведении дифференциального диагноза и может демонстрировать типичные признаки хронической подагры, но бесполезно в ранней диагностике подагры (уровень доказательности IIb). Формирование внутрикостных тофусов часто происходит одновременно с подкожными тофусами, в связи с чем, рентгенологическое исследование используется для определения тяжести тофусного поражения. В действительности, при остром подагрическом артрите, рентгенологические изменения не всегда могут быть полезны для постановки диагноза подагры. Тем не менее, в ряде ситуаций выполнение рентгенограмм вполне оправдано для проведения дифференциального диагноза с травмами и т.д.
Факторы риска подагры и сопутствующие болезни должны выявляться, включая признаки метаболического синдрома (ожирение, гипергликемия, гиперлипидемия, гипертензия) (уровень доказательности Ia или Ib для отдельных факторов).
Лечение
Лечение подагры
Общие рекомендации
1. Оптимальное лечение подагры требует комбинации нефармакологических и фармакологических подходов (уровень доказательности Ib) и должно учитывать:
а) специфические факторы риска (уровень мочевой кислоты, количество предшествующих атак, рентгенография) (уровень доказательности IIb)
б) стадию болезни (асимптоматическая гиперурикемия, острый/интермиттирующий артрит, межприступный период, хроническая тофусная подагра) (уровень доказательности Ib)
в) общие факторы риска (возраст, пол, ожирение, гиперурикемические препараты, сопутствующие, полипрагмазия) (уровень доказательности Ib).
2. Обучение больного правильному образу жизни (уменьшение веса тела при ожирении, диета, уменьшение приема алкоголя, особенно пива) - ключевой аспект лечения. Ограничение в пищевом рационе богатых пуринами продуктов животного происхождения и снижение массы тела способствует снижению сывороточного уровня мочевой кислоты (уровень доказательности IIb), а алкоголь, особенно пиво, является независимым фактором риска для подагры (уровень доказательности III).
3. Гиперлипидемия, гипертензия, гипергликемия, ожирение и курение должны выявляться в каждом случае, т.к. являются важными компонентами при ведении больного с подагрой (уровень доказательности Ib).
Лечение острого приступа подагрического артрита
1. НПВП и колхицин могут быть эффективны в терапии острого приступа артрита (уровень доказательности Ib) и являются первой линией терапии. Данные о сравнительной эффективности НПВП и колхицина отсутствуют и при отсутствии противопоказаний, следует считать рациональным назначение НПВП.
2. Высокие дозы колхицина приводят к побочным эффектам, а низкие дозы (например 0,5 мг 3 раза в день) могут быть достаточны у ряда пациентов (уровень Ib).
3. Удаление синовиальной жидкости (уровень доказательности IV) и введение внутрисуставно длительно действующих глюкокортикоидов (уровень доказательности IIb) может быть эффективным и безопасным лечением острого приступа артрита.
4. При наличии противопоказании и/или неэффективности НПВП, колхицина и глюкокортикоидов для купирования острого приступа возможно применение препаратов, блокирующих интерлейкин-1 (уровень доказательности Ib).
Антигиперурикемическая терапия.
1. Антигиперурикемическая терапия показана больным с персистирующей гиперурикемией и острыми атаками, артропатией, тофусами или рентгенологическими изменениями. Проведение антигиперурикемической терапии показано в указанных случаях при неэффективности нефармакологических методов лечения. Решение о подобной терапии должно быть принято индивидуально, учитывать баланс между пользой и потенциальными рисками и согласовано с больным (уровень доказательности IV).
2. Целью антигиперурикемической терапии является предупреждение образование и растворение имеющихся кристаллов моноурата натрия, это достигается поддержанием уровня МК ниже точки супернасыщения сыворотки уратами (
Информация
- Федеральные клинические рекомендации по ревматологии 2013 г. с дополнениями от 2016 г.
Методология
Методы, использованные для сбора/селекции доказательств: поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств:
доказательной базой для рекомендаций является глубина публикаций вошедших в Кохрановскую библиотеку, базы данных EMBASE и MEDLINE. Глубина поиска составляла 20 лет.
Методы, использованные для оценки качества и глубины доказательств:
· Консенсус экспертов
· Оценка значимости в соответствии с рейтиноговой схемой
Рейтиноговая схема для оценки силы рекомендаций
| Сила | Описание |
| Ia | Мета-анализ рандомизированных контролируемых исследований |
| Ib | Рандомизированное контролируемое исследование |
| IIa | Контролируемое исследование без рандомизации |
| IIb | Квази-экспериментальное исследование |
| III | Неэкспериментальные описательные исследования, таких как сравнительные, корреляционные и исследования случай-контроль |
| IV | Сообщения или мнения экспертных комитетов или клинический опыт |
Описание метода валидизации рекомендаций
Данные рекомендации в проектной версии были рецензированы независимыми экспертами с целью их адаптации для врачей ревматологов и врачей первичного звена.
Комментарии, полученные от экспертов систематизировались и обсуждались членами рабочей группы, внесенные изменения регистрировались для каждого пункта рекомендаций.
Рабочая группа
Для окончательной редакции и контроля качества предложенных рекомендаций они были повторно проанализированы членами рабочей группы, которые пришли к заключении, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок сведен к минимуму.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.

Читайте в новом номере
В последние несколько десятилетий отмечается рост заболеваемости подагрой. Несмотря на активное развитие новых направлений диагностики данного заболевания, постановка этого диагноза вызывает трудности. Возможно, это связано с недостаточной оснащенностью медучреждений в регионах необходимым оборудованием (поляризационный микроскоп, ультразвуковая диагностика поражения суставов, двухэнергетическая компьютерная томография) и/или наличием подготовленных специалистов. В этих случаях важным является разработка клинических критериев с более высокими показателями чувствительности и специфичности, позволяющих диагностировать подагру. В 2015 г. Европейской антиревматической лигой (EULAR) и Американским колледжем ревматологов (ACR) предприняты попытки разработать такие критерии, а в 2016 г. различными медицинскими сообществами (Американским колледжем врачей (ACP) и EULAR) выработаны стратегии ведения таких пациентов в клинической практике. Кроме того, в 2016 г. в Российской Федерации зарегистрированы новые препараты для лечения подагры (колхицин, фебуксостат). Важным является внедрение алгоритма этих рекомендаций в работу врачей, к которым обращаются пациенты с подагрой: ревматологов, травматологов, хирургов, терапевтов, врачей общей практики. На примере реального клинического случая в статье разбираются алгоритм постановки диагноза, стратегические направления лечения этих пациентов, принципы выбора лекарственных препаратов, роль нимесулида в терапии пациентов с подагрой.
Ключевые слова: подагра, подагрический артрит, критерии диагностики, принципы терапии, нимесулид.
Для цитирования: Якупова С.П. Алгоритм ведения пациентов с подагрой в свете современных рекомендаций. РМЖ. Медицинское обозрение. 2017;1:53-56.
Algorithm for gouty patients management in light of modern guidelines
Yakupova S.P.
Kazan State Medical University
In the past few decades, there has been an increase in the gout incidence rate. Despite the active development of new directions in the diagnosis of this disease, the formulation of this diagnosis is difficult. Perhaps this is due to insufficient equipment in the regions (polarizing microscope, ultrasound diagnosis of joints lesion, dual energy computed tomography) and / or trained specialists. In these cases, it is important to develop clinical criteria with higher sensitivity and specificity indicators that allow diagnosing gout. In 2015, the European Anti-Rheumatic League (EULAR) and the American College of Rheumatology (ACR) have attempted to develop such criteria, and in 2016 various medical communities (American College of Physicians (ACP) and EULAR) have developed strategies for managing such patients in clinical practice. In addition, in 2016 new drugs for the treatment of gout (colchicine, febuksostat) were registered in the Russian Federation. It is important to implement the algorithm of these guidelines in the work of doctors, who treat patients with gout, - rheumatologists, traumatologists, surgeons, therapists, general practitioners. On an example of a real clinical case, the article deals with the algorithm of diagnosis, the strategic directions of treatment of these patients, the principles of drug choice, the role of nimesulide in the therapy of gouty patients.
Key words: gout, gouty arthritis, diagnostic criteria, principles of therapy, nimesulide.
For citation: Yakupova S.P. Algorithm for gouty patients management in light of modern guidelines // RMJ. MEDICAL REVIEW. 2017. № 1. P. 53–56.
В статье приведен алгоритм ведения пациентов с подагрой в свете современных клинических рекомендаций. На примере реального клинического случая разбираются алгоритм постановки диагноза, стратегические направления лечения пациентов, принципы выбора лекарственных препаратов, роль нимесулида в терапии пациентов с подагрой.
Только для зарегистрированных пользователей
1. 2014 Федеральные клинические рекомендации "Подагра" (Ассоциация ревматологов России).
Симптомы и признаки
Основные клинические проявления подагры: рецидивирующие атаки острого артрита, накопление кристаллов уратов в тканях с образованием тофусов, нефролитиаз, подагрическая нефропатия.
В развитии подагры выделяют 3 стадии:
- острый подагрический артрит
- периоды между приступами подагрического артрита (межприступная подагра)
- хроническая тофусная подагра.
Демонстрация кристаллов моноурата натрия (МУН) в синовиальной жидкости или в содержимом тофуса позволяет поставить определенный диагноз подагры. Специфичность метода поляризационной микроскопии для демонстрации кристаллов крайне высока.
Основным клиническим проявлением, который позволяет заподозрить подагру является острый артрит. Острая атака с быстрым развитием выраженной боли и воспаления, которые достигают максимума в течение 6-12 часов, особенно сопровождающиеся эритемой, высоко подозрительны в отношении микрокристаллического воспаления, хотя не специфичны для подагры.
Рутинный поиск кристаллов рекомендуется в любой синовиальной жидкости, полученной из воспаленного сустава у больных с отсутствием определенного диагноза.
Пунктировать суставы в диагностических целях можно и в межприступный период. Идентификация кристаллов МУН из невоспаленного сустава обеспечивает определенный диагноз в межприступном периоде.
Подагра и сепсис могут сосуществовать, поэтому при подозрении на септический артрит окраска по грамму и исследования культуры синовиальной жидкости должны выполняться даже в случае идентификации кристаллов МУН. Гораздо чаще септического артрита развиваются нагноения мягких тканей в области вскрывшихся подкожных тофусов.
Несмотря на то, что ГУ является наиболее важным фактором риска подагры, сывороточный уровень МК не является фактором исключения или подтверждения подагры: многие люди с ГУ не развивают подагры, а во время острой атаки сывороточный уровень МК может быть нормальным.
Почечная экскреция мочевой кислоты должна определяться у некоторых больных подагрой, имеющих семейную историю подагры с ранним началом, начало подагры ранее 25 лет, с анамнезом МКБ.
Рентгенологическое исследование суставов помогает в проведении дифференциального диагноза и может демонстрировать типичные признаки хронической подагры, но бесполезно в ранней диагностике подагры (уровень доказательности IIb). Формирование внутрикостных тофусов часто происходит одновременно с подкожными тофусами, в связи с чем, рентгенологическое исследование используется для определения тяжести тофусного поражения. В действительности, при остром подагрическом артрите, рентгенологические изменения не всегда могут быть полезны для постановки диагноза подагры. Тем не менее, в ряде ситуаций выполнение рентгенограмм вполне оправдано для проведения дифференциального диагноза с травмами и т.д.
Факторы риска подагры и сопутствующие болезни должны выявляться, включая признаки метаболического синдрома (ожирение, гипергликемия, гиперлипидемия, гипертензия).
Критерии для постановки диагноза
Для диагностики подагрического артрита в 1975 году Американской Ассоциацией Ревматологов (ААР) были рекомендованы предварительные классификационные критерии, одобренные ВОЗ в 2002 году.
Наличие характерных кристаллов мочевой кислоты в суставной жидкости
Наличие тофусов, содержание кристаллов мочевой кислоты, в которых подтверждено химически или поляризационной микроскопией
Наличие 6 из 12 ниже перечисленных признаков:
- Более одной атаки острого артрита в анамнезе
- Воспаление сустава достигает максимума в 1-й день болезни
- Моноартрит
- Гиперемия кожи над пораженным суставом
- Припухание и боль в первом плюснефаланговом суставе
- Одностороннее поражение первого плюснефалангового сустава
- Одностороннее поражение суставов стопы
- Подозрение на тофусы
- Гиперурикемия
- Асимметричный отек суставов
- Субкортикальные кисты без эрозий (рентгенография)
- Отрицательные результаты при посеве синовиальной жидкости
В своей практике любой врач–ревматолог периодически обращается к неким официальным правилам, предписывающим ему то или иное действие. Они касаются выбора методов диагностики, базисной и симптоматической помощи, продолжительности стационарного пребывания или амбулаторной терапии. Таким образом, клинические рекомендации по лечению подагры охватывают все аспекты борьбы с недугом, а значит, должны соответствовать изменениям, происходящим в фармацевтике и стандартах первичной медико-санитарной помощи.

Что такое клинические рекомендации?
Клинические рекомендации — это законодательно утвержденные протоколы лечения больных, которые вместе с правилами оказания медицинской помощи и порядком информирования пациентов являются основой профессиональной деятельности врача и позволяют оценить качество оказанных услуг. На это прямо указывают статьи Федерального закона №323-ФЗ от 21.11.2011.
Существующие сегодня стандарты помощи больным, страдающим от подагры, носят преимущественно международный или национальный характер, хотя ничто не мешает создавать подобные руководства местного значения или даже уровня конкретной лечебной организации.
По-видимому, дело здесь не столько в нежелании специалистов брать на себя ответственность, сколько в опасении остаться без необходимого содействия, поскольку поддержкой национальных руководств занимаются специально созданные организации.
Для России наиболее актуальными является стандарты федерального значения, разработанные ассоциацией ревматологов под руководством член-корреспондента РАМН Е.Л. Насонова. Ну а поскольку за последнее время назрела явная необходимость пересмотра некоторых ключевых позиций, в 2017 году были опубликованы обновленные клинические рекомендации.
Переработанные и дополненные протоколы лечения призваны упростить деятельность медиков, обеспечить их необходимой информацией о новых препаратах и методах терапии. Кроме того, ценность медицинских стандартов заключается в четкой проработке действий врача в сложной ситуации и подведении знаний к единому знаменателю: общая терминология — одинаковые подходы к диагностике и лечению пациента — улучшение прогнозов даже самого запущенного недуга.
Основные пункты по ведению больных подагрой
Согласно последним клиническим рекомендациям 2017 года, протокол ведения пациентов регламентирует виды, объемы и качество медицинской помощи больным подагрой. В отличие от правил терапии, которые могут быть разработаны местным лечебным учреждением или некоммерческой организацией медицинского направления, протокол создается под руководством государства.
Федеральные рекомендации предназначены для всех медиков, без учета местных проблем и нюансов
Основные направления ведения больных, указанные в документе, носят общий характер и содержат описание болезни, принципы диагностики и требования к процессу оказания медицинской помощи при подагре. При этом не учитываются материально-техническое оснащение местных клиник и стационаров, эпидемиологическая или демографическая ситуация, сложившаяся в регионе либо городе.
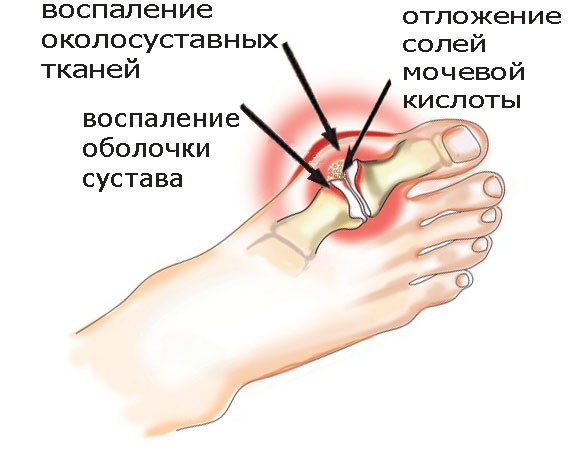
Подагра — системное расстройство пуринового обмена, для которого типично отложение мочекислых солей в суставах или близлежащих тканях и возникающее в связи с этим воспаление.
Обнаружения гиперурикемии недостаточно для постановки диагноза, так как только 10–12% имеющих избыток моноурата натрия страдают подагрой. По МКБ 10 системное нарушение классифицируется как воспалительные полиартропатии и находится под кодом М.10.
По современным медицинским данным, этиология недуга очень разнообразна. Помимо нарушения обмена веществ и ухудшения работы почек, спровоцировать подагру может неправильное питание, злоупотребление спиртным, лишний вес или наличие хронических недомоганий.
В ревматологии принято выделять три стадии недуга:
- острая подагра;
- межприступная подагра;
- тофусная подагра.
Знание современных методов борьбы с каждой из этих форм болезни поможет эффективно управлять недугом, отсрочивая очередной приступ на долгие годы.
Для облегчения диагностики Американской Ассоциацией Ревматологов были предложены классификационные критерии, которые сегодня широко используются на практике российскими врачами:
- В анамнезе пациента уже были приступы острого артрита.
- Максимум страданий наблюдается в первый день атаки.
- Заболевание одного сустава.
- Гиперемия кожи над областью поражения.
- Воспаление плюснефалангового сочленения на большом пальце ноги.
- Появление тофусов.
- Моноартикулярный характер скопления уратов в зоне первого плюснефалангового соединения.
- Односторонний отек сустава.
- Гиперурикемия.
- Асимметричность воспаления элементов стопы.
- На рентгенограмме видна киста в субкортикальном слое.
- Суставная жидкость не содержит следов патогенной микрофлоры.
В правильности диагноза можно не сомневаться, если присутствуют 6 из 12 перечисленных выше признаков, при этом наблюдается нарастание тофусов и наличие кристаллов урата в синовии.
Успешная борьба с подагрой должна включать применение медикаментозных и немедикаментозных методов, а также учитывать стадию недуга, возраст и пол пациента, наличие хронических патологий и специфических факторов риска.
Медицинская помощь при остром приступе основана на следующих принципах:
- Колхицин и НПВС являются препаратами выбора при подагрической атаке;
- хорошим способом устранения боли может быть удаление синовия и внутрисуставное введение глюкокортикостероидов;
- при неэффективности описанных мер возможно назначение медикаментов, блокирующих медиатор воспаления Interleukin-1.
Ключевым аспектом терапии является обучение пациента правильному образу жизни — соблюдению диеты, уменьшению массы тела, отказу от спиртного. При ведении больных подагрой следует учитывать наличие гипергликемии, стойкой гипертензии, повышение уровня липидов в крови.
Антигиперурикемическая помощь показана людям с костными деформациями, тофусами, артропатией, частыми атаками и гиперурикемией. Решение о подобном методе терапии принимается совместно с больным, при этом учитывается соотношение между пользой и возможными рисками.
Целью противоподагрической терапии является уменьшение синтеза и ускорение экскреции уже имеющихся уратов.
Основным медикаментом долгосрочного применения при подагре считается Аллопуринол. Его назначают в исходно низкой дозировке с постепенным увеличением порции. При существовании почечных патологий средство применяют с осторожностью.
Сульфинпиразон и Пробенецид могут использоваться как альтернатива Аллопуринолу у людей со здоровыми почками, но нежелательны пациентам с мочекаменной болезнью. Бензбромарон допустим к применению при умеренном нарушении функций почек, но может быть токсичным для печени.
Применение диуретиков больным подагрическим артритом запрещено, если лекарства не назначаются по жизненным показаниям. В качестве альтернативы допустимо использовать гипотензивные средства.
Смягченный узикозурический эффект имеют Лозартан и Фенофибрат, что позволяет назначать их пациентам, с трудом переносящим Аллопуринол. Клиническая эффективность такой методики пока не определена. О народных способах лечения в стандартах не упоминается.
Какие изменения внесены в клинические рекомендации по подагре
Ввиду появления новых медикаментов и способов терапии в 2017 году были пересмотрены существующие российские и международные клинические рекомендации по лечению подагры. Что же в них изменилось?
Были обновлены пункты по использованию НПВС для купирования острого приступа — сейчас медикаменты могут применяться как сами по себе, так и в дополнение к Колхицину. Интересной новацией в лечении подагрических атак стало включение в общую схему терапии таблеток Преднизолона.
Еще один способ избавления от болей, отраженный в новом документе — введение кортикостероидов. Российские национальные стандарты, в отличие от международных, предусматривают возможность внутримышечных уколов гормона.
В европейских протоколах лечения рекомендуется широко использовать блокаторы ИЛ-1(Канакинумаб, Анакинру) как дополнение или альтернативу другим методам борьбы с подагрой. В российском варианте рекомендаций разрешено назначать только Канакинумаб.
По сравнению с прошлой версией стандартов изменился подход к подбору продуктов питания, рекомендованных больным. Новый вариант рациона нашел отражение в издании американских коллег.
Для многих пациентов приятным моментом стала реабилитация кофе, которое раньше строго запрещалось. Оказалось, что напиток не только не повышает опасность гиперурикемии, а, наоборот, снижает риск развития подагры.
Важные новшества коснулись и времени назначения базисной терапии недуга. Если по прошлым рекомендациям антигиперурикемическое лечение начинали только после 2 острых атак в год, да еще при наличии тофусов и стойкой гиперурикемии, то сегодня российские и европейские эксперты рекомендуют как можно более раннее начало уратснижающей терапии.
Подагра — это один из немногих хронических недугов, которое теоретически можно излечить. Действительно, восстановление нормального уровня моноурата натрия в крови должно привести к постепенному расщеплению кристаллов и исчезновению симптомов заболевания. Однако на практике все сложнее. Поэтому нет сомнений, что новые клинические рекомендации по лечению подагрического артрита станут прекрасным руководством как для начинающих, так и опытных врачей-практиков.
Читайте также:


