Остеоартроз и патофизиология его
Деформирующий остеоартроз -- это дегенеративно-дистрофическое заболевание суставов с первичной дегенерацией суставного хряща, с последующими изменениями суставной поверхности и развитием краевых остеофитов, что ведёт к деформации суставов.
Деформирующий остеоартроз является наиболее распространённым заболеванием суставов. Среди всех пациентов с заболеваниями суставов более двух трети составляют именно больные деформирующим остеоартрозом.
Остеоартрозом страдает 5-10% населения и его обнаруживают у половины людей старше 60 лет. Средний возраст заболевших -- 40-50 лет. Особой разницы между полами нет, за исключением эрозивного остеоартроза дистальных и проксимальных межфаланговых суставов, который в 10 раз чаще встречается у женщин.
Если в двух словах, то причина развития деформирующего остеоартроза кроется в несоответствии между механической нагрузкой на сустав и возможностями хряща сопротивляться этой нагрузке. В итоге возникает дегенерация и деструкция суставного хряща.
Факторы, способствующие развитию остеоартроза:
Хроническая микротравматизация хряща и перегрузка суставов:
Активные занятия спортом или особенности труда с перегрузкой отдельных групп мышц и суставов (например, повреждение плечевого сустава у дальнобойщиков или проектировщиков).
Невропатии (например, при сахарном диабете). Нормальное функционирование сустава зависит от тонуса околосуставных мышц. Нарушение проприоцептивной импульсации приводит к снижению мышечного тонуса, в результате увеличиваются нагрузки на сустав, и возникает деформирующий остеоартроз.
Ожирение. Деформирующий остеоартроз коленных суставов имеет наибольшую корреляцию с лишним весом.
Врождённые или приобретённые дефекты опорно-двигательного аппарата:
Дисплазия (в основном это дисплазия тазобедренного сустава) -- плохое развитие суставных поверхностей, отсутствие правильной опоры, нарушение микроциркуляции, подвывихи, дистрофические изменения хряща.
Травмы и хирургические вмешательства на суставах (например, удаление мениска).
Воспаление -- артриты. Единственный инфекционный артрит, который не даёт деструкции -- гонорейный артрит.
Нарушения метаболизма: подагра, охроноз (при охронозе в отличие от болезни Бехтерева нет сакроилеита), гемохроматоз, болезнь Уилсона. Вторичная подагра -- развивается после 40 лет, накапливается кальций в хрящах и бывают вторичные воспалительные вспышки. При хондроматозе суставов и вторичной подагре хондропротекторы противопоказаны (хондрокальциноз).
Возраст и наследственность:
Возраст (возрастные изменения хряща) и менопауза.
Генетические факторы: мутация гена коллагена типа II (синдром Стиклера), наследственная патология костей и суставов, этническая принадлежность (негры).
Наследственная предрасположенность (узелки Гебердена встречаются в 2 раза чаще у матерей и в 3 раза чаще у сестёр больного остеоартрозом).
Деформирующей остеоартроз -- это необратимый процесс. Прогрессирование болезни зависит от исходной трофики суставной ткани, нарушений регионарного кровотока, реологии и выраженности капиллярной недостаточности (это один из ведущих факторов, потому что хрящ не имеет своих сосудов! Он питается из кости и из синовиальной жидкости).
В настоящее время считается, что деформирующий остеоартроз поражает все структуры сустава. Причём, по данным сцинтиграфии, изменениям в хряще предшествуют нарушения субхондральной кости.
В основе остеартроза лежат количественные и качественные изменения протеогликанов (основного действующего вещества хряща) и повреждение хондроцитов. Протеогликаны обладают антигенными свойствами, следовательно, могут служить источником аутоиммунных реакций (этот раздел патогенеза плохо изучен).
Клиническая картина деформирующего остеоартроза
Нередко боли усиливаются под влиянием метеорологических факторов, в частности, при понижении температуры воздуха, изменении барометрического давления. Обычно боль в суставе носит диффузный характер. Однако иногда в дебюте деформирующего артроза наблюдается лишь ограниченное поражение периартикулярных тканей в области одного из суставов с локальной болью и участком пальпаторно выявляемой болезненности в области синовиальной сумки, месте прикрепления связок и (или) сухожилий. При вовлечении в процесс сухожилия боль в суставе наиболее выражена во время активных движений. В ряде случаев появлению болей в суставах в течение определенного времени предшествует хруст в них при движениях.
Тазобедренный сустав -- наиболее частая локализация деформирующего остеоартроза, причем у трети больных отмечается двустороннее поражение суставов.
Коленный сустав -- вторая по частоте локализация деформирующего остеоартроза.
Примерно у 20% больных первичным деформирующим остеоартрозом встречаются практически патогномоничные для данного заболевания и своеобразные по своим клиническим проявлениям дегенеративно-дистрофические изменения межфаланговых суставов кистей (узелковый остеоартроз).
У некоторых больных первичный деформирующий остеоартроз протекает с множественным, нередко симметричным, поражением суставов, в том числе межфаланговых суставов кистей с образованием узелков Гебердена и Бушара. Считается, что такой генерализованный остеоартроз (семейный полиостеоартроз, болезнь Келлгрена) обусловлен распространенной хондропатией и снижением резистентности хряща, по-видимому, вследствие наследственной неполноценности синтетической функции хондроцитов. Поражение суставов при генерализованном остеоартрозе нередко сочетается с энтезопатиями, а также с остеохондрозом и спондилезом позвоночника. В то же время лучезапястные суставы в отличие от ревматоидного артрита редко вовлекаются в патологический процесс.
При вторичном деформирующем остеоартрозе дегенеративно-дистрофические изменения хряща возникают только в тех суставах, на которые действует первичный этиологический фактор. Так, вторичный коксартроз развивается при врожденной неполноценности вертлужной впадины, недостаточно покрывающей головку бедра, а также при деформации головки бедренной кости в результате остеохондропатии (болезнь Кальве--Легга--Пертеса), выраженного остеонекроза, хронического артрита и других патологических процессов, нарушающих конгруэнтность суставных поверхностей. Причинами вторичного гонартроза могут быть гипермобильность коленных суставов, дефекты их развития (варусная или вальгусная деформация), последствия внутрисуставного перелома, хондрокальциноз и др. При этом вторичный деформирующий остеоартроз может развиваться в более молодом возрасте, но клиническая картина его в основном сходна с таковой при первичной форме заболевания.
Диагностика деформирующего остеоартроза
При типичной клинической картине и характерных рентгенологических изменениях диагноз деформирующего остеоартроза обычно не вызывает затруднений. В план дифференциального диагноза при этом включают метаболические, эндокринные, нейрогенные и другие заболевания, приводящие к дегенеративно-дистрофическому поражению суставного хряща и обусловливающему развитие так называемого симптоматического остеоартроза. При наличии полиостеоартроза следует учитывать, что он может быть осложнением полиартикулярных форм подагры или хондрокальциноза, а также проявлением болезни Кашина--Бека, охронозной артропатии, акромегалии. Важно также помнить, что у больного деформирующим остеоартрозом возможно развитие любого вида артрита, который может ошибочно приниматься за вторичный синовит.
Уже было отмечено, что при вторичном синовите дистальных межфаланговых суставов кистей, обусловленном узелками Гебердена, в ряде случаев возникает необходимость в дифференциальном диагнозе с псориатическим артритом, а при воспалительных изменениях проксимальных межфаланговых суставов кистей, связанных с узелками Бушара, -- с ревматоидным артритом. Помимо этого вторичный синовит отдельных межфаланговых суставов кистей, развившийся на фоне узелков Гебердена и Бушара, иногда приходится дифференцировать с тофусной подагрой. Необходимо также принимать во внимание, что узелки Гебердена и Бушара могут служить лишь фоном для развития различных ревматических воспалительных заболеваний, встречающихся в пожилом возрасте, в том числе паранеопластического артрита.
Дополнительные сложности возникают при моноартикулярном характере деформирующего остеоартроза. Как уже указывалось, деформирующий остеоартроз I плюснефалангового сустава, осложненный острым бурситом, иногда напоминает подагру. Если поражен крупный сустав, следует рассматривать возможность других невоспалительных артропатий, а при затяжном вторичном синовите -- туберкулезного, грибкового и других хронических инфекционных и паразитарных артритов. В таких случаях иногда приходится прибегать к специальным методам рентгенологического исследования пораженного сустава (томография, контрастная артрография, артропневмография, ангиография), а также к артроскопии с прицельной биопсией и последующим гистологическим и бактериологическим исследованием биоптатов. Для диагностики некоторых инфекционных артритов немаловажное значение имеет также исследование синовиального выпота с применением серологического, бактериоскопического и культурального методов.
Лечение деформирующего остеоартроза
Лечение деформирующего остеоартроза должно быть комплексным и направлено на устранение факторов, способствовавших развитию заболевания, предотвращение прогрессирующей дегенерации суставного хряща, уменьшение болевых ощущений, ликвидацию явлений вторичного синовита и улучшение функции сустава. Важное значение имеет разгрузка пораженных суставов, особенно коленного и тазобедренного. С этой целью больной должен избегать длительной ходьбы, частых подъемов и спусков по лестнице, ношения тяжестей, продолжительного стояния в одной и той же позе, ходьбу и часто повторяющиеся движения целесообразно чередовать с 5--10-минутным отдыхом. Необходимо добиваться снижения массы тела больных, страдающих ожирением, а при вторичной форме заболевания показаны коррекция нарушений статики, ортопедическое пособие (например, ношение обуви со специальными стельками при плоскостопии). В некоторых случаях бывает необходимо сменить профессию, прекратить спортивные занятия. При существенном нарушении функции суставов нижних конечностей рекомендуется при ходьбе пользоваться тростью, которую больной должен держать в руке, противоположной пораженному суставу. В тяжелых случаях следует ходить на костылях.
С целью устранения неполноценности суставного хряща и предотвращения прогрессирования в нем дегенеративных изменений применяют хондропро-тективные препараты, в частности пептидный комплекс гликозаминогликанов, приготовленный из экстракта хряща и костной ткани телят, Cu-Zn-супероксид-дисмутаза из бычьей печени, полисульфатированный гликозаминогликан, хондроитинсульфат, D-гликозаминхлорид и др. Терапевтический эффект хондропротекторов основан на снижении активности лизосомальных ферментов, увеличении количества хондроцитов, стимуляции в них синтеза РНК и выработки протеогликанов, создании предпосылок для формирования устойчивого хряща, улучшении состояния субхондральной кости. Конкретные механизмы действия отдельных препаратов могут различаться. При развитии значительной деформации суставов с резким ограничением их подвижности хондропротекторы не назначают.
Широкое распространение при лечении деформирующего остеоартроза получили физиотерапевтические методы, например, назначаемые при отсутствии вторичного синовита местные тепловые процедуры: высокочастотная электротерапия, аппликации парафина, озокерита, нафталана. Некоторые авторы рекомендуют аппликации на суставы 50% раствора диметилсульфоксида. Важное значение имеет регулярное санаторно-курортное лечение с применением лечебной грязи и бальнеотерапии (общие сероводородные и радоновые ванны).
При вторичном синовите назначают нестероидные противовоспалительные препараты в небольших дозах и на срок не более 1--2 недель. У больных с повышенным риском развития язвенной болезни показано применение селективного ингибитора циклооксигеназы 2-го типа мелоксикама (Мовалиса). К достоинствам препарата относятся высокая противовоспалительная активность, низкий риск развития пептических язв и других побочных эффектов, отсутствие отрицательного влияния на гиалиновый хрящ. Целесообразно применение так называемой ступенчатой терапии, при которой Мовалис назначают сначала внутримышечно по 15 мг (1,5 мл) в/м в течение 5--6 дней, а затем переходят на длительный прием препарата перорально по 15 мг 1 раз в сутки. В случае медленно рассасывающегося суставного выпота проводят его эвакуацию. Местно применяют ультрафиолетовое облучение в эритемных дозах, ультразвук. При сопутствующем вовлечении периартикулярных мягких тканей показаны обкалывание анестетиками участков локальной болезненности, электрофорез с новокаином и анальгином, втирание мазей с нестероидными противовоспалительными препаратами и отвлекающими средствами. Вторичный синовит тазобедренного и коленного сустава служит показанием к значительному снижению двигательной активности вплоть до постельного режима.
Для улучшения функции пораженных суставов больным деформирующим остеоартрозом показана систематическая лечебная гимнастика, направленная на укрепление соответствующих мышц. Инструктор лечебной физкультуры должен обучить больного необходимым упражнениям, чтобы он мог выполнять их в домашних условиях. При этом необходимо придерживаться определенных правил. Так, больной не должен пытаться выполнять упражнения, превозмогая возникающую боль в суставах. Объем движений следует увеличивать постепенно и очень осторожно, не допуская, чтобы они были слишком интенсивными, способными травмировать пораженные суставы. Желательно проводить лечебную гимнастику лежа и сидя, а также в бассейне. Можно применять упражнения со статической нагрузкой. Кроме того, показана механотерапия (кинезотерапия) на специальных тренажерах, способствующая укреплению связочно-мышечного аппарата.
Быстро прогрессирующий деформирующий остеоартроз тазобедренного и коленного суставов со значительными и необратимыми анатомическими изменениями, приводящими к инвалидизации больного, может потребовать артропластики или эндопротезирования.
Остеоартроз — хроническое невоспалительное заболевание суставов неизвестной этиологии, характеризующееся прогрессирующей дегенерацией суставного хряща, структурными изменениями субхондральной кости и сопутствующим реактивным синовитом
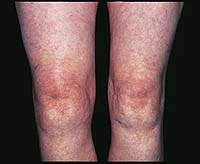 |
| Рисунок 1. Синовит (припухлость, гиперемия, локальное повышение температуры) правого коленного сустава при ОА |
При прогрессировании ОА в результате происходящих дегенеративных процессов хрящ размягчается, разрыхляется. В нем появляются трещины, простирающиеся до кости.
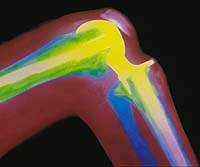 |
| Рисунок 2. Эндопротез коленного сустава. Рентгенограмма |
Особая роль в патогенезе ОА отводится синовиту, морфологически характеризующемуся умеренно выраженными пролиферативными и экссудативными реакциями (гиперплазией синовиальной оболочки и ее мононуклеарной инфильтрацией), наиболее выраженными в местах прикрепления синовии к хрящу с последующим исходом в склероз и липоматоз. В субхондральной кости выявляются микропереломы, утолщение костных трабекул и остеофитоз. Экссудативно-пролиферативные реакции как в субхондральной кости, так и в синовиальной оболочке протекают на фоне нарушений региональной гемодинамики и микроциркуляции с развитием тканевой гипоксии. В последующем прогрессирование болезни принимает, по сути, необратимый характер.
Боль, деформация и тугоподвижность сустава являются основными клиническими проявлениями ОА.
Боль в суставе — наиболее частый и выраженный симптом при ОА, носит неоднородный характер. Причинами ее могут быть деструктивные процессы в хрящевых и субхондральных структурах, нарушения микроциркуляции, особенно при затруднении венозного кровотока в спонгиозной части кости, фиброз капсулы сустава, воспалительный процесс в мягких околосуставных тканях, спазм близлежащих мышц и реактивный синовит.
В целом для заболевания характерен механический ритм болей — возникновение боли под влиянием дневной физической нагрузки и стихание за период ночного отдыха, что связано со снижением амортизационных способностей хряща и костных подхрящевых структур к нагрузкам. При этом происходит прогибание костных балок в сторону спонгиозной кости.
Возможны непрерывные тупые ночные боли, связанные с венозным стазом в субхондральной спонгиозной части кости и повышением внутрикостного давления.
Рефлекторный спазм близлежащих мышц, а также развитие реактивного синовита вызывают постоянные боли.
Реактивный синовит и воспалительный отек параартикулярных тканей усугубляют клиническую картину. При наличии синовита, помимо боли в суставе как при движении, так и в покое, характерны утреннняя скованность, припухлость сустава, локальное повышение кожной температуры. С прогрессированием заболевания рецидивы синовита учащаются.
Обычно ОА развивается медленно и начинается как моноартикулярное заболевание, но через некоторое время в патологический процесс включаются и другие суставы, чаще всего те, которые компенсаторно брали на себя повышенную механическую нагрузку, чтобы разгрузить первоначально заболевший сустав.
Клинически значимыми и инвалидизирующими формами ОА являются гонартроз и коксартроз. Клиническая картина ОА определяется конкретным суставом и группой суставов, вовлеченных в патологический процесс.
Среди неинвазивных методов диагностики гонартроза ведущее место по информативности занимает ультразвуковое двумерное сканирование коленных суставов, которое используют для объективизации и детализации характеристики вторичного синовита, являющегося прогностически неблагоприятным фактором, усугубляющим процессы дегенерации хряща. Наряду с диагностикой наличия синовиальной жидкости можно определить ее характер, особенно над bursa suprapatellaris и появлением жидкости над мыщелками бедренной кости, толщину и характер синовиальной оболочки; при этом ее утолщение при 0,4 см и более, а также контуры суставных поверхностей с учетом однородности контуров хряща на мыщелках бедренной кости и толщину хряща принимают за патологию. Ультразвуковое исследование суставов позволяет также уточнить характер и степень воспалительного процесса для выработки адекватного лечения.
Артроскопия в артрологии для диагностики воспалительных и дегенеративных заболеваний суставов, к сожалению, применяется недостаточно широко и, более того, не выявляет качественных отличий от воспаления синовии при других артритах. Существенно расширяет диагностические возможности артроскопии использование прицельной биопсии, а визуальный контроль позволяет получить фрагмент синовиальной ткани или хряща, наиболее адекватно отражающих развивающийся в суставе патологический процесс, но при этом данная процедура редко показывает распространенность патологического процесса. Артроскопия используется и с лечебной целью — с целью промывания полоски коленного сустава, при которой удаляется хрящевой детрит, а также фрагменты мениска, утолщенной и воспалительной синовии; выполняется аброзивная артропластика при гонартрозе. При коксартрозе ультразвуковое исследование отмечает, наряду с наличием и характером синовиальной жидкости, эхоуплотнение капсулы синовиальной оболочки, хрящевой губы, остеофиты. Однако следует сказать, что как ультразвуковые, так и эндоскопические признаки не могут считаться специфическими при гонартрозе и коксартрозе, поскольку они встречаются и при других заболеваниях суставов, как воспалительного, так и дегенеративного характера.
Основными целями терапии ОА являются: замедление прогрессирования дегенерации хряща и максимально возможное сохранение функции сустава. Терапевтическая тактика при ОА состоит из трех компонентов:
- механическая разгрузка пораженных суставов;
- купирование синовита;
- предотвращение прогрессирования заболевания.
Задачи, которые ставятся при составлении комплекса лечебных мероприятий, можно решать с учетом следующей шкалы приоритетов: болевой синдром, синовит, нарушение трофики суставов и местного кровотока, гипотрофия и гипотония мышц, контрактура.
Режим. Механическая разгрузка сустава является определяющим фактором как в уменьшении болевого синдрома, так и в лечении ОА в целом. Сюда входят рекомендации по исключению длительного пребывания в фиксированной позе, долгого стояния на ногах, длительной ходьбы, повторяющихся стереотипных движений, переноса больших тяжестей, ведущих к механической перегрузке определенных зон суставов. В далеко зашедших стадиях заболевания пациенту полезно ходить с тростью, костылями. При выраженных болях в фазу обострения может быть назначен полупостельный режим.
Диета. Четких патогенетических рекомендаций по диете ОА на настоящий момент не существует. Важным условием в лечении ОА коленных суставов является снижение избыточной массы тела. В последнее время рекомендуются пищевые добавки (глюкозамин, хондроитин и др.), но эффективность их требует клинических подтверждений.
В терапии ОА наиболее часто применяются обезболивающие препараты, нестероидные противовоспалительные препараты (НПВП) и средства с хондропротективными свойствами.
В терапии ОА, который сопровождается болевым и воспалительным синдромами, широко применяются НПВП. В настоящее время известно около 100 НПВП различных классов, но поиск новых лекарственных средств этой группы продолжается. Это связано с потребностью в медикаменте, имеющем оптимальное соотношение обезболивающего и противовоспалительного действия и характеризующемся высокой степенью безопасности. В этом плане большой интерес представляет появившийся на российском рынке препарат ксефокам.
Ксефокам — новый НПВП класса оксикамов.
Подобно другим НПВП, ксефокам обладает обезболивающей и противовоспалительной активностью, связанной с подавлением синтеза простагландинов посредством ингибирования циклооксигеназы (ЦОГ).
Так как большинство НПВП подавляют, как правило, и ЦОГ-1 и ЦОГ-2, то развитие гастропатий, а также нарушение функции почек и агрегации тромбоцитов являются запрограммированным фармакологическим эффектом этих препаратов.
Существует достоверная связь между приемом НПВП и развитием патологии верхних отделов ЖКТ: геморрагий, эрозий, язв в желудке (гастропатий), а также эзофагопатий и дуоденопатий, что проявляется болями или чувством тяжести в эпигастральной области, тошнотой, иногда рвотой, изжогой, дисфагией, метеоризмом, диареей и др. Возможно бессимптомное течение гастропатий, в связи с чем увеличивается риск развития таких серьезных осложнений, как кровотечение и перфорация, нередко ведущих к летальному исходу. Кроме того, длительный прием НПВП вызывает энтеропатии и колонопатии с последующим развитием железодефицитной анемии и гипоальбуминемии.
К образованию эрозий и язв приводит подавление НПВП синтеза простагландинов слизистой ЖКТ, что вызывает:
- уменьшение секреции слизистого геля;
- снижение секреции бикарбонатов;
- ухудшение кровотока в слизистой ЖКТ.
Высокий риск возникновения язв ЖКТ отмечается при продолжительной терапии НПВП, но максимален в первый месяц приема препарата. Снижение риска в дальнейшем объясняется, по-видимому, адаптационными механизмами, благодаря которым гастродуоденальная слизистая приобретает способность противостоять повреждающему действию НПВП.
Полагают, что при приеме НПВП нарушается репарация хряща и субхондральной кости за счет угнетения синтеза простагландинов, в частности в зонах микропереломов, с образованием очагов деструкции и кист. При этом, купируя болевой синдром и явления синовита, НПВП не задерживают дегенеративно-дистрофических изменений в суставных тканях пациента.
Установлено, что селективное ингибирование ЦОГ-2 оказывает незначительный эффект при острой боли. В то же время при острой боли концентрация ЦОГ-1 увеличивается в три-четыре раза, поэтому для анальгетического эффекта может иметь значение ингибирование именно этого изофермента. Таким образом, оптимальным сочетанием анальгетического и противовоспалительного эффекта обладают препараты, ингибирующие как ЦОГ-1, так и ЦОГ-2. Ксефокам является наиболее мощным ингибитором обоих изоферментов. Эта способность ксефокама в 100-200 раз превышает таковую у эталонных НПВП, например у диклофенака и пироксикама. При этом соотношение ингибиторной активности ксефокама в отношении ЦОГ-1 и ЦОГ-2 (мера селективности) занимает срединное положение по сравнению с аналогичными показателями других НПВП, что и обеспечивает баланс анальгетической и противовоспалительной активности ксефокама.
Ксефокам угнетает высвобождение свободных радикалов кислорода из активированных лейкоцитов, что усиливает его анальгетическую и противовоспалительную активность.
Обезболивающий эффект ксефокама отчасти связан с его влиянием на центральную нервную систему. Это подтверждается тем, что внутривенное введение лорноксикама (ксефокама) больным с болями в пояснице повышало уровень эндогенных морфинов при одновременном улучшении состояния. Активация системы нейропептидных опиоидов может быть одним из путей реализации анальгетического эффекта ксефокама. По анальгетическому эффекту ксефокам приравнивается к 20 мг морфина, при этом он не оказывает опиатоподобного действия на ЦНС и не вызывает лекарственной зависимости.
Исследования показали, что в терапевтических дозах ксефокам стимулирует синтез протеогликанов, предотвращая дегенерацию суставного хряща. Эта важная особенность ксефокама делает его препаратом выбора при ОА, поскольку известно, что многие НПВП, напротив, отрицательно влияют на хрящ.
Ксефокам практически весь (на 99%) связывается с белками плазмы, тем не менее он активно проникает в суставные полости, где длительное время (10-12 часов) сохраняется в достаточной терапевтической концентрации — даже когда в плазме его концентрация снижается. Это позволяет принимать препарат всего лишь два раза в день. Благодаря короткому периоду полувыведения из плазмы крови (примерно 4 часа) прием ксефокама сопровождается меньшей выраженностью побочных эффектов, так как в период между введениями доз возможно восстановление протекторных физиологических уровней простагландинов, необходимых для защиты слизистой желудка и поддержания нормального кровотока в почках.
Ксефокам полностью метаболизируется в печени, при этом одна треть его неактивных метаболитов выводится почками, а две трети — печенью и кишечником. Такой двойной путь экскреции снижает нагрузку на данные органы и улучшает переносимость ксефокама. После многократного введения ксефокама не наблюдается его кумуляция в плазме, что снижает риск побочных эффектов по сравнению с НПВП, имеющими более длительный период полувыведения. Фармакокинетика ксефокама примерно одинакова у пожилых людей и лиц молодого или зрелого возраста, поэтому не требуется какой-либо коррекции дозы препарата у пожилых.
Клинические испытания подтвердили высокую эффективность и хорошую переносимость ксефокама у больных ОА. В результате месячного приема лекарства в суточной дозе 16 мг уменьшались боль, длительность утренней скованности, улучшалась функция суставов.
К средствам, модифицирующим течение ОА, относятся препараты, в основе действия которых лежат:
- активация анаболических процессов в матриксе хряща
- подавление активности лизосомальных ферментов
- стимуляция синтетических функций хондроцитов.
Традиционно для лечения ОА использовались парентеральные гликозаминогликаны, однако в последнее время предпочтение отдается пероральным препаратам, а именно глюкозаминсульфату и хондроитинсульфату.
При некупируемом реактивном синовите показана пункция сустава, удаление синовиальной жидкости и внутрисуставное введение глюкокортикоидов, которые ингибируют синтез интерлейкина-1 и фактора некроза опухоли-α, участвующих в воспалении и деградации хряща. Широко используются при этом гидрокортизон, метипред, кеналог и дипроспан. Последние препараты характеризуются более выраженным и пролонгированным лечебным действием. Вместе с глюкокортикоидами возможно введение анестетиков (новокаина, лидокаина), действие которых при этом потенцируется. Введение ингибиторов медиаторов воспаления — контрикала (трасилола) или гордокса — благотворно влияет на метаболизм хряща.
В настоящее время рассматривается вопрос о широком внедрении в практику для подавления локального воспаления внутрисуставного введения ксефокама.
Широко применяемые для восстановительного лечения ОА физиотерапевтические методы уменьшают болевой синдром, а также воспалительные процессы и мышечный спазм, улучшают микроциркуляцию, благоприятно воздействуют на метаболические процессы в тканях сустава. При этом используются ультрафиолетовое облучение, электрические токи, переменные магнитные поля, электрофорез и фонофорез лекарственных средств на суставы. При пролиферативных явлениях, вазотрофических расстройствах и контрактурах показаны тепловые процедуры, включая аппликации парафина, озокерита, иловой и торфяной грязи. При отсутствии синовита эффективны морские, радоновые, сульфидные, бишофитные и йодобромные ванны. Для укрепления мышц рекомендуется применение электромиостимуляции.
При выполнении лечебного массажа больным ОА следует избегать механического раздражения суставной капсулы, обращая особое внимание на работу с прилегающими к суставу мышцами. Тогда снижается болевой мышечный спазм, повышается тонус ослабленных групп мышц, усиливается трофика пораженных суставов и улучшаются функциональные способности больного.
При выраженном длительном болевом синдроме, не купируемом традиционными средствами, а также при значительных нарушениях функции сустава применяется хирургическое лечение чаще всего на коленных и тазобедренных суставах. Кардинальной операцией является эндопротезирование сустава. Хорошо зарекомендовали себя эндопротезы, в которых узел скольжения состоит из пары металл–полиэтилен.
Важную роль в профилактике ОА играет выявление и своевременная ортопедическая коррекция врожденных аномалий: вывиха бедра, варусной и вальгусной установки голеней, плоскостопия и др. В профессиональной деятельности необходимо исключить длительные статические и стереотипные механические перегрузки суставов. Существенным условием профилактики ОА коленных суставов является нормализация избыточной массы тела.
Читайте также:


