Об этиологии и патогенезе артроза



- Главная
- Новые материалы
- Популярное
- Поиск
- Карта сайта
- Связь с нами
Этиология и патогенез первичных артрозов полностью не выяснены. Среди этиологических факторов, способствующих развитию местных проявлений болезни, первое место занимает статическая нагрузка, превышающая функциональные возможности сустава, и механическая микротравматизация. С возрастом наступают изменения сосудов синовиальной оболочки. Важная роль отводится также некоторым эндокринным расстройствам, особенно увеличению активности соматотропного гормона гипофиза, снижению функции щитовидной и половых желёз и др. При ожирении происходит не только увеличение механической нагрузки на суставы нижних конечностей, но и отмечается общее воздействие метаболических нарушений на функцию опорно-двигательного аппарата. Кроме того, не исключается значение инфекционных, аллергических и токсических факторов. Отмечена определённая роль патологии вен голени в развитии артроза коленных суставов. Имеются также данные, указывающие на роль наследственности в этиологии артроза.
В свете современных представлений патологический процесс в суставах при артрозе развивается следующим образом. В результате длительной повышенной и даже нормальной нагрузки на суставы при одновременных изменениях в сосудах синовиальной оболочки и ухудшении условий питания хряща разрушаются лизосомы клеток хряща и активизируются протеолитические энзимы, которые вызывают деполемиризацию протеино-полисахаридных комплексов. Такая активация лизосомальных энзимов вызывает гибель клеток, особенно в поверхностном слое хряща, вследствие чего хрящ теряет свою эластичность, на его поверхности образуются небольшие трещины, начинается усиленная пенеретрация ферментов синовиальной оболочки, особенно гиалуронидазы, катепсинов, плазминогена и др., в хрящ.
При старении хряща в нём доминирует анаэробный гликолиз, в результате чего увеличивается содержание лактата и уменьшается рН. Это увеличивается активность указанных ферментов, т.к. оптимальное их действие бывает в кислой среде, и деградация компонентов межклеточного вещества хряща ещё больше усугубляется.
В ответ на увеличенную деполимеризацию протеино-полисахаридных
Комплексов и уменьшение компонентов хряща наступает пролиферизация хондроцитов и усиление синтеза хондроитинсульфата. Таким образом, дистрофия хряща постепенно прогрессирует, поверхностный слой его приобретает клочковидную структуру. Кроме того, при артрозе изменяются синовиальной жидкости, которая является хорошим смазочным средством особенно за счёт гиалуроновой кислоты. Это тоже способствует развитию артроза.
Синовиальная оболочка, богатая соединительными элементами, кровеносными и лимфатическими сосудами, нервами, тоже принимает в развитии артроза, особенно при появлении реактивных воспалительных реакций. При электронно-микроскопическом изучении синовиальной оболочки выделено два типа клеток: тип А тип В. Клетка типа А является преимущественно абсорбтивными и имеют способность фагоцитировать, а клетки типа В основном вырабатывают комплексы гиалуроновой кислоты и протеинов. При артрозе активность этих клеток вначале усиливается, а по мере прогрессирования процесса ослабевает. Причины, вызывающие пуск этого механизма, неизвестны. Полагают, что может иметь значение генетическая предрасположенность, обусловленная дефектом в синтезе полисахаридов и ферментов хряща.
В этиологии и патогенезе вторичных артрозов главную роль играют травмы, нарушающие целость или конгруэнтность (соответствие) суставных поверхностей.
Другими причинами вторичных артрозов являются врождённые дисплазии и приобретённые нарушения статики, перенесённые артриты, заболевания эпифизов костей, заболевания обмена веществ (напр., подагра, охроноз, болезнь Кашина – Бека), эндокринные заболевания (гипотериоз, сахарный диабет и др.).
Врождённые и приобретённые дефекты хряща и других элементов костно-суставного аппарата в сочетании с продолжающейся или даже увеличивающейся нагрузкой на суставы могут через определённый период времени привести развитию артроза. Учитывая то обстоятельство, что травмы и микротравматизация, аномалии статики (варусное или вальгусное положение бёдер, голеней и стоп, плоскостопие, врождённый вывих или дисплазия бедра, кифоз, лордоз, сколиоз и др.), перенесённые болезни костей (асептические некрозы) и суставов (артриты) и некоторые другие состояния весьма часто являются причиной развития артроза, Хаккенброх (M. Hackenbroch, 1968) предложил называть их преартрозами и принимать профилактические меры для предупреждения артроза.
Деформирующий артроз (остеоартроз, ранее — остеоартрит, дегенеративный артрит или гипертрофический артрит) —дегенеративное заболевание с поражением суставного хряща, вовлечением субхондрального слоя кости, синовиальной оболочки.
Филогенетически деформирующий артроз выявляется, начиная от рептилий и амфибий, затем и у всех видов млекопитающих, за исключением тех, кто проводит большую часть жизни вниз головой, таких как летучие мыши и ленивцы.
Патогенез атроза
Как утверждает авторитетный сайт про артроз, несмотря на имеющуюся прямую взаимосвязь между возрастом и частотой деформирующего артроза, артроз не является просто результатом старения организма, механического износа сустава или хронически текущего воспаления. Для него характерна последовательная смена цепочки событий в хондроцитах и внеклеточном матриксе, приводящая к нарушению структуры и функции хряща, и сопровождающаяся неполноценными репаративными реакциями хрящевой ткани, ремоделированнем костной ткани. Вырабатывая соответствующие ферменты, хондроциты контролируют ремоделирование матрикса. Внеклеточный матрикс, в свою очередь, состоит из каркаса упорядоченных макромолекул и связанных с ними молекул воды. Это определяет свойства ткани — прочность и эластичность. Вода составляет до 80% от веса нативного суставного хряща.
Стадии артроза
Большинство механизмов, ответственных за прогрессирование дегенерации суставного хряща при первичном деформирующем артрозе, до сих пор остаются неизвестными. Однако патологический процесс условно может делиться на три перекрывающиеся стадии:
- альтерация межклеточного матрикса;
- репаративный ответ хондроцитов;
- срыв компенсаторных реакций
На первой стадии , макроскопически представленной фибрилляцией поверхностных слоев суставного хряща или всего лишь некоторым размягчением хряща, в результате повреждения макромолекулярной структуры матрикса возрастает содержание связанных молекул воды. Повреждение макромолекулярной структуры заключается в уменьшении агрегации протеогликанов, концентрации гликозаминогликанов и длины их цепочек, изменении состава и соотношения минорных коллагенов в волокнах и соответственно в деградации коллагеновых волокон. Таким образом, из-за увеличения проницаемости матрикса для молекул и уменьшения его прочности снижается резистентность гиалинового хряща к обычной механической нагрузке — как известно, первыми поражаются самые нагружаемые отделы сустава.
Вторая стадия начинается, когда хондроциты распознают повреждение ткани, нарушение осмолярности, плотности и напряжения электрического заряда и начинают продуцировать медиаторы (цитокины), стимулирующие очень быстрый клеточный ответ, состоящий из пролиферации хондроцитов и усиления как их анаболической, так и катаболической активности, т. е интенсифицируются процессы как синтеза, так и деградации матрикса. Основными ферментами, вызывающими деградацию матрикса, являются металлопротеиназы. На этой стадии репаративные процессы могут в течение многих лет компенсировать продолжающуюся дегенерацию хряща и, по мнению отдельных авторов, у некоторых пациентов происходит временная стабилизация патологического процесса. Макроскопически площадь разволокнения увеличивается, хрящ становится шероховатым, трещины углубляются.
Если повреждающий фактор не устранен, то со временем происходит срыв репаративных реакций и десинхронизация анаболических и катаболических процессов — начинается третья стадия патологического процесса, характеризующаяся резким снижением активности хондроцитов и их смертью. Трещины постепенно достигают уровня субхондральной кости.
Изменения субхондральной кости, сопровождающие дегенерацию хряща, заключаются в склерозировании (образуются новые плотные костные слон), появлении кистоподобных костных полостей, содержащих миксоидную, фиброзную или хрящеподобную ткань, к формировании фиброзных, хрящевых и костных выступов (остеофитов), которые располагаются по периферии сустава и вдоль прикрепления капсулы. Ремоделированне костной ткани приводит к деформации, укорочению вовлеченной конечности и нестабильности сустава.
Вторичные изменения происходят и в синовиальной оболочке. Уменьшение использования сустава, уменьшение амплитуды движений ведет к атрофии мышц. В итоге возникают туго- подвижность и слабость.
Остеоартроз (OA) является наиболее частым заболеванием суставов. На его долю приходится 60-70 % всех ревматических болезней. Клинические проявления остеоартроза встречаются почти у 20 % населения земного шара. Проблема остеоартроза чрезвычайно актуальна и для России. Так, из 13 млн зарегистрированных в 2001 г. по поводу ревматических заболеваний пациентов 16 % (примерно 1 млн 800 тыс.) страдали остеоартрозом. Хотя заболевание не приводит к смертельному исходу, оно является одной из основных причин преждевременной инвалидности, потери трудоспособности и значительно ухудшает качество жизни больных.
Отдельные случаи остеоартроза встречаются уже в возрасте 16-25 лет, однако с возрастом частота заболевания увеличивается. У лиц старше 50 лет остеоартроз встречается в 50 % случаев, а в возрасте 70 лет и более - у 80-90 % обследуемых. Женщины болеют OA почти в 2 раза чаще мужчин. Однако в возрасте старше 70 лет распространенность остеоартроза практически одинакова у лиц обоего пола.
Этиология остеоартроза.
Истинная причина остеоартроза до настоящего времени остается невыясненной. По современным представлениям остеоартроз является мультифакториальным заболеванием. В развитии дегенеративных изменений суставного хряща принимают участие сразу несколько факторов, среди которых можно выделить два основных - чрезмерную механическую и функциональную перегрузку хряща и снижение его резистентности к обычной физиологической нагрузке. Таким образом, основной предполагаемой причиной развития остеоартроза является несоответствие между механической нагрузкой, падающей на суставную поверхность хряща, и его возможностями выдерживать эту нагрузку, в результате чего развивается дегенерация и деструкция хряща.
Факторы риска развития остеоартроза:
- наследственная предрасположенность;
- избыточная масса тела;
- профессиональные, спортивные или бытовые перегрузки;
- травмы;
- возраст больных старше 50 лет;
- другие заболевания суставов.
Рядом исследователей показано, что частота остеоартроза дистальных межфаланговых суставов кистей ( узелки Гебердена ) встречаются в 2 раза чаще у матерей и в 3 раза чаще у сестер больного остеоартрозом. В семьях больных остеоартрозом заболевание встречается в 2 раза чаще, чем в общей популяции, причем риск развития остеоартроза у лиц с врожденными дефектами опорно-двигательного аппарата повышается в 7,7 раза. У пациентов с избыточной массой тела достоверно чаще встречается остеоартроз коленных суставов.
Патогенез остеоартроза.
Вследствие воздействия различных этиологических факторов возникают нарушения обмена и синтетической активности хондроцитов, а также физико-химические повреждения матрикса суставного хряща.
Установлено, что при остеоартрозе в основе нарушения метаболизма хряща лежат нарушения обмена протеогликанов(ПГн) - основного вещества хряща: уменьшение и качественные их изменения, нарушающие стабильность структуры коллагеновой сети.
В норме в суставном хряще уравновешены процессы его синтеза (анаболизм) и деградации (катаболизм). При формировании остеоартроза обычно наблюдается недостаточное образование или усиленный катаболизм компонентов хрящевой ткани.
Характерным признаком деструкции хряща при остеоартрозе является потеря матриксом гликозамингликанов - хондроитинсульфата, кератансульфата, гиалуроновой кислоты поверхностной, промежуточной и глубокой зонами хряща. Кроме того, отмечается уменьшение молекул ПГн, которые становятся способными к выходу из матрикса хряща.
В ранней стадии остеоартроза протеогликаны (измененные, мелкие) способны поглощать воду, но не способны прочно ее удерживать. Избыточная вода поглощается коллагеном, который набухает и разволокняется, что ведет к снижению резистентности хряща. В дальнейшем происходит дегидратация хряща, дезорганизация и разрыв коллагеновых волокон.
При повреждении хондроцитов наблюдается выработка ими не свойственных нормальной хрящевой ткани коллагена и ПГн (короткий коллаген, не образующий фибрилл, и низкомолекулярные мелкие ПГн), неспособных формировать агрегаты с гиалуроновой кислотой, что приводит к потере биохимических свойств матрикса хряща.
Определенную роль в патогенезе остеоартроза играет воспаление. Причина воспаления при остеоартрозе остается неясной: роль макромолекул-детритов хряща и кальцийсодержащих кристаллов является спорной. Механизмом, посредством которого воспаление может участвовать в деградации хряща, является выработка провоспалительных цитокинов (ИЛ-1β, ИЛ-6, ФНО-α и др.), которые, в свою очередь, высвобождают ферменты, повреждающие коллаген (коллагеназу, эластазу, пептидазу) и протеогликаны (металлопротеиназу, стромелизин, катепсин), а также выработка простагландинов и активаторов плазминогена. Это играет важную роль в моделировании воспаления и восприятии боли. Некоторые продукты воспаления, такие как брадикинин и гистамин, способны сами стимулировать первичные афферентные нервные волокна, в то время как простагландины, лейкотриены и ИЛ-1β и ИЛ-6 могут повышать чувствительность этих волокон к различным экзогенным раздражителям.
Однажды начавшееся высвобождение биологически активных веществ способствует поддержанию воспаления в тканях сустава при остеоартрозе, в результате происходит последующее повреждение синовиальной оболочки сустава с развитием реактивного синовита и повышением продукции провоспалительных цитокинов.
Освобождающиеся протеогликаны, продукты распада хондроцитов и коллагена, являясь антигенами, могут индуцировать образование аутоантител с формированием локального воспалительного процесса.
Суммируя приведенные данные, можно представить схему патогенеза остеоартроза в следующем виде.

Патогенез остеоартроза
Наиболее ранние изменения состоят в обеднении матрикса поверхностного слоя хряща протеогликанами, что сопровождается его гипергидратацией. Одновременно наблюдаются некроз некоторых хондроцитов, дезорганизация и уплотнение фибрилл коллагена. В дальнейшем происходит разволокнение (дефибрилляция) поверхностного слоя хряща. В более глубоких его слоях наряду с некрозом хондроцитов развиваются реактивные изменения - гиперплазия и пролиферация хондроцитов с увеличением их синтетической функции - повышением синтеза протеогликанов. Хрящ из прочного, эластичного, гладкого становится шероховатым на поверхности, менее прочным и эластичным. Эти изменения предшествуют деструкции хряща и развиваются в зоне наибольшей нагрузки.
В развернутой стадии остеоартроза гистологически определяются вертикальные трещины хряща, вплоть до субхондральной кости, более выраженное уменьшение протеогликанов и хондроцитов в поверхностных и глубоких слоях хряща. Хрящ истончается, местами обызвествляется. Растрескивание хряща приводит к изъязвлению с обнажением подлежащей кости и отделением фрагментов, которые поступают в полость сустава. В суставной полости эти фрагменты подвергаются фагоцитозу лейкоцитами с высвобождением медиаторов воспаления, лизосомальных ферментов, что клинически проявляется синовитом сустава и развитием иммунологических реакций на продукты распада, однако эти реакции носят местный характер.
Структурно-метаболическая неполноценность суставного хряща приводит к нарушению конгруэнтности суставных поверхностей, что приводит к локальной перегрузке суставов в местах наибольших изменений и нагрузки.
Костные суставные поверхности в результате поражения хрящевой ткани испытывают повышенные нагрузки. В результате возникают микропереломы костных трабекул с образованием округлых дефектов - кист и повреждением сосудов, приводящим к внутрикостной гипертензии. Также обнаруживаются субхондральный остеосклероз и краевые костные разрастания - остеофиты, что обеспечивает увеличение площади соприкосновения суставных поверхностей и уменьшение давления на суставной хрящ и подлежащую кость, но вызывает деформацию сустава. Это приводит к усилению болевого синдрома вследствие давления на околосуставные мягкие ткани.
Аналогичные изменения наблюдаются при вторичных артрозах, но при них изменения хряща имеют более диффузный характер, хотя явления вторичного реактивного синовита выражены слабее.
Выделяют остеоартроз первичный (идиопатический) и вторичный (вследствие дисплазий, артритов, травм, статических нарушений, гипермобильности и др.).
Остеоартроз — хроническое невоспалительное заболевание суставов неизвестной этиологии, характеризующееся прогрессирующей дегенерацией суставного хряща, структурными изменениями субхондральной кости и сопутствующим реактивным синовитом
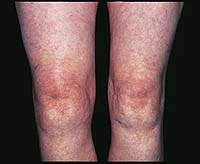 |
| Рисунок 1. Синовит (припухлость, гиперемия, локальное повышение температуры) правого коленного сустава при ОА |
При прогрессировании ОА в результате происходящих дегенеративных процессов хрящ размягчается, разрыхляется. В нем появляются трещины, простирающиеся до кости.
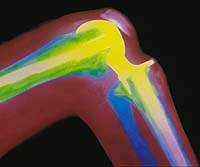 |
| Рисунок 2. Эндопротез коленного сустава. Рентгенограмма |
Особая роль в патогенезе ОА отводится синовиту, морфологически характеризующемуся умеренно выраженными пролиферативными и экссудативными реакциями (гиперплазией синовиальной оболочки и ее мононуклеарной инфильтрацией), наиболее выраженными в местах прикрепления синовии к хрящу с последующим исходом в склероз и липоматоз. В субхондральной кости выявляются микропереломы, утолщение костных трабекул и остеофитоз. Экссудативно-пролиферативные реакции как в субхондральной кости, так и в синовиальной оболочке протекают на фоне нарушений региональной гемодинамики и микроциркуляции с развитием тканевой гипоксии. В последующем прогрессирование болезни принимает, по сути, необратимый характер.
Боль, деформация и тугоподвижность сустава являются основными клиническими проявлениями ОА.
Боль в суставе — наиболее частый и выраженный симптом при ОА, носит неоднородный характер. Причинами ее могут быть деструктивные процессы в хрящевых и субхондральных структурах, нарушения микроциркуляции, особенно при затруднении венозного кровотока в спонгиозной части кости, фиброз капсулы сустава, воспалительный процесс в мягких околосуставных тканях, спазм близлежащих мышц и реактивный синовит.
В целом для заболевания характерен механический ритм болей — возникновение боли под влиянием дневной физической нагрузки и стихание за период ночного отдыха, что связано со снижением амортизационных способностей хряща и костных подхрящевых структур к нагрузкам. При этом происходит прогибание костных балок в сторону спонгиозной кости.
Возможны непрерывные тупые ночные боли, связанные с венозным стазом в субхондральной спонгиозной части кости и повышением внутрикостного давления.
Рефлекторный спазм близлежащих мышц, а также развитие реактивного синовита вызывают постоянные боли.
Реактивный синовит и воспалительный отек параартикулярных тканей усугубляют клиническую картину. При наличии синовита, помимо боли в суставе как при движении, так и в покое, характерны утреннняя скованность, припухлость сустава, локальное повышение кожной температуры. С прогрессированием заболевания рецидивы синовита учащаются.
Обычно ОА развивается медленно и начинается как моноартикулярное заболевание, но через некоторое время в патологический процесс включаются и другие суставы, чаще всего те, которые компенсаторно брали на себя повышенную механическую нагрузку, чтобы разгрузить первоначально заболевший сустав.
Клинически значимыми и инвалидизирующими формами ОА являются гонартроз и коксартроз. Клиническая картина ОА определяется конкретным суставом и группой суставов, вовлеченных в патологический процесс.
Среди неинвазивных методов диагностики гонартроза ведущее место по информативности занимает ультразвуковое двумерное сканирование коленных суставов, которое используют для объективизации и детализации характеристики вторичного синовита, являющегося прогностически неблагоприятным фактором, усугубляющим процессы дегенерации хряща. Наряду с диагностикой наличия синовиальной жидкости можно определить ее характер, особенно над bursa suprapatellaris и появлением жидкости над мыщелками бедренной кости, толщину и характер синовиальной оболочки; при этом ее утолщение при 0,4 см и более, а также контуры суставных поверхностей с учетом однородности контуров хряща на мыщелках бедренной кости и толщину хряща принимают за патологию. Ультразвуковое исследование суставов позволяет также уточнить характер и степень воспалительного процесса для выработки адекватного лечения.
Артроскопия в артрологии для диагностики воспалительных и дегенеративных заболеваний суставов, к сожалению, применяется недостаточно широко и, более того, не выявляет качественных отличий от воспаления синовии при других артритах. Существенно расширяет диагностические возможности артроскопии использование прицельной биопсии, а визуальный контроль позволяет получить фрагмент синовиальной ткани или хряща, наиболее адекватно отражающих развивающийся в суставе патологический процесс, но при этом данная процедура редко показывает распространенность патологического процесса. Артроскопия используется и с лечебной целью — с целью промывания полоски коленного сустава, при которой удаляется хрящевой детрит, а также фрагменты мениска, утолщенной и воспалительной синовии; выполняется аброзивная артропластика при гонартрозе. При коксартрозе ультразвуковое исследование отмечает, наряду с наличием и характером синовиальной жидкости, эхоуплотнение капсулы синовиальной оболочки, хрящевой губы, остеофиты. Однако следует сказать, что как ультразвуковые, так и эндоскопические признаки не могут считаться специфическими при гонартрозе и коксартрозе, поскольку они встречаются и при других заболеваниях суставов, как воспалительного, так и дегенеративного характера.
Основными целями терапии ОА являются: замедление прогрессирования дегенерации хряща и максимально возможное сохранение функции сустава. Терапевтическая тактика при ОА состоит из трех компонентов:
- механическая разгрузка пораженных суставов;
- купирование синовита;
- предотвращение прогрессирования заболевания.
Задачи, которые ставятся при составлении комплекса лечебных мероприятий, можно решать с учетом следующей шкалы приоритетов: болевой синдром, синовит, нарушение трофики суставов и местного кровотока, гипотрофия и гипотония мышц, контрактура.
Режим. Механическая разгрузка сустава является определяющим фактором как в уменьшении болевого синдрома, так и в лечении ОА в целом. Сюда входят рекомендации по исключению длительного пребывания в фиксированной позе, долгого стояния на ногах, длительной ходьбы, повторяющихся стереотипных движений, переноса больших тяжестей, ведущих к механической перегрузке определенных зон суставов. В далеко зашедших стадиях заболевания пациенту полезно ходить с тростью, костылями. При выраженных болях в фазу обострения может быть назначен полупостельный режим.
Диета. Четких патогенетических рекомендаций по диете ОА на настоящий момент не существует. Важным условием в лечении ОА коленных суставов является снижение избыточной массы тела. В последнее время рекомендуются пищевые добавки (глюкозамин, хондроитин и др.), но эффективность их требует клинических подтверждений.
В терапии ОА наиболее часто применяются обезболивающие препараты, нестероидные противовоспалительные препараты (НПВП) и средства с хондропротективными свойствами.
В терапии ОА, который сопровождается болевым и воспалительным синдромами, широко применяются НПВП. В настоящее время известно около 100 НПВП различных классов, но поиск новых лекарственных средств этой группы продолжается. Это связано с потребностью в медикаменте, имеющем оптимальное соотношение обезболивающего и противовоспалительного действия и характеризующемся высокой степенью безопасности. В этом плане большой интерес представляет появившийся на российском рынке препарат ксефокам.
Ксефокам — новый НПВП класса оксикамов.
Подобно другим НПВП, ксефокам обладает обезболивающей и противовоспалительной активностью, связанной с подавлением синтеза простагландинов посредством ингибирования циклооксигеназы (ЦОГ).
Так как большинство НПВП подавляют, как правило, и ЦОГ-1 и ЦОГ-2, то развитие гастропатий, а также нарушение функции почек и агрегации тромбоцитов являются запрограммированным фармакологическим эффектом этих препаратов.
Существует достоверная связь между приемом НПВП и развитием патологии верхних отделов ЖКТ: геморрагий, эрозий, язв в желудке (гастропатий), а также эзофагопатий и дуоденопатий, что проявляется болями или чувством тяжести в эпигастральной области, тошнотой, иногда рвотой, изжогой, дисфагией, метеоризмом, диареей и др. Возможно бессимптомное течение гастропатий, в связи с чем увеличивается риск развития таких серьезных осложнений, как кровотечение и перфорация, нередко ведущих к летальному исходу. Кроме того, длительный прием НПВП вызывает энтеропатии и колонопатии с последующим развитием железодефицитной анемии и гипоальбуминемии.
К образованию эрозий и язв приводит подавление НПВП синтеза простагландинов слизистой ЖКТ, что вызывает:
- уменьшение секреции слизистого геля;
- снижение секреции бикарбонатов;
- ухудшение кровотока в слизистой ЖКТ.
Высокий риск возникновения язв ЖКТ отмечается при продолжительной терапии НПВП, но максимален в первый месяц приема препарата. Снижение риска в дальнейшем объясняется, по-видимому, адаптационными механизмами, благодаря которым гастродуоденальная слизистая приобретает способность противостоять повреждающему действию НПВП.
Полагают, что при приеме НПВП нарушается репарация хряща и субхондральной кости за счет угнетения синтеза простагландинов, в частности в зонах микропереломов, с образованием очагов деструкции и кист. При этом, купируя болевой синдром и явления синовита, НПВП не задерживают дегенеративно-дистрофических изменений в суставных тканях пациента.
Установлено, что селективное ингибирование ЦОГ-2 оказывает незначительный эффект при острой боли. В то же время при острой боли концентрация ЦОГ-1 увеличивается в три-четыре раза, поэтому для анальгетического эффекта может иметь значение ингибирование именно этого изофермента. Таким образом, оптимальным сочетанием анальгетического и противовоспалительного эффекта обладают препараты, ингибирующие как ЦОГ-1, так и ЦОГ-2. Ксефокам является наиболее мощным ингибитором обоих изоферментов. Эта способность ксефокама в 100-200 раз превышает таковую у эталонных НПВП, например у диклофенака и пироксикама. При этом соотношение ингибиторной активности ксефокама в отношении ЦОГ-1 и ЦОГ-2 (мера селективности) занимает срединное положение по сравнению с аналогичными показателями других НПВП, что и обеспечивает баланс анальгетической и противовоспалительной активности ксефокама.
Ксефокам угнетает высвобождение свободных радикалов кислорода из активированных лейкоцитов, что усиливает его анальгетическую и противовоспалительную активность.
Обезболивающий эффект ксефокама отчасти связан с его влиянием на центральную нервную систему. Это подтверждается тем, что внутривенное введение лорноксикама (ксефокама) больным с болями в пояснице повышало уровень эндогенных морфинов при одновременном улучшении состояния. Активация системы нейропептидных опиоидов может быть одним из путей реализации анальгетического эффекта ксефокама. По анальгетическому эффекту ксефокам приравнивается к 20 мг морфина, при этом он не оказывает опиатоподобного действия на ЦНС и не вызывает лекарственной зависимости.
Исследования показали, что в терапевтических дозах ксефокам стимулирует синтез протеогликанов, предотвращая дегенерацию суставного хряща. Эта важная особенность ксефокама делает его препаратом выбора при ОА, поскольку известно, что многие НПВП, напротив, отрицательно влияют на хрящ.
Ксефокам практически весь (на 99%) связывается с белками плазмы, тем не менее он активно проникает в суставные полости, где длительное время (10-12 часов) сохраняется в достаточной терапевтической концентрации — даже когда в плазме его концентрация снижается. Это позволяет принимать препарат всего лишь два раза в день. Благодаря короткому периоду полувыведения из плазмы крови (примерно 4 часа) прием ксефокама сопровождается меньшей выраженностью побочных эффектов, так как в период между введениями доз возможно восстановление протекторных физиологических уровней простагландинов, необходимых для защиты слизистой желудка и поддержания нормального кровотока в почках.
Ксефокам полностью метаболизируется в печени, при этом одна треть его неактивных метаболитов выводится почками, а две трети — печенью и кишечником. Такой двойной путь экскреции снижает нагрузку на данные органы и улучшает переносимость ксефокама. После многократного введения ксефокама не наблюдается его кумуляция в плазме, что снижает риск побочных эффектов по сравнению с НПВП, имеющими более длительный период полувыведения. Фармакокинетика ксефокама примерно одинакова у пожилых людей и лиц молодого или зрелого возраста, поэтому не требуется какой-либо коррекции дозы препарата у пожилых.
Клинические испытания подтвердили высокую эффективность и хорошую переносимость ксефокама у больных ОА. В результате месячного приема лекарства в суточной дозе 16 мг уменьшались боль, длительность утренней скованности, улучшалась функция суставов.
К средствам, модифицирующим течение ОА, относятся препараты, в основе действия которых лежат:
- активация анаболических процессов в матриксе хряща
- подавление активности лизосомальных ферментов
- стимуляция синтетических функций хондроцитов.
Традиционно для лечения ОА использовались парентеральные гликозаминогликаны, однако в последнее время предпочтение отдается пероральным препаратам, а именно глюкозаминсульфату и хондроитинсульфату.
При некупируемом реактивном синовите показана пункция сустава, удаление синовиальной жидкости и внутрисуставное введение глюкокортикоидов, которые ингибируют синтез интерлейкина-1 и фактора некроза опухоли-α, участвующих в воспалении и деградации хряща. Широко используются при этом гидрокортизон, метипред, кеналог и дипроспан. Последние препараты характеризуются более выраженным и пролонгированным лечебным действием. Вместе с глюкокортикоидами возможно введение анестетиков (новокаина, лидокаина), действие которых при этом потенцируется. Введение ингибиторов медиаторов воспаления — контрикала (трасилола) или гордокса — благотворно влияет на метаболизм хряща.
В настоящее время рассматривается вопрос о широком внедрении в практику для подавления локального воспаления внутрисуставного введения ксефокама.
Широко применяемые для восстановительного лечения ОА физиотерапевтические методы уменьшают болевой синдром, а также воспалительные процессы и мышечный спазм, улучшают микроциркуляцию, благоприятно воздействуют на метаболические процессы в тканях сустава. При этом используются ультрафиолетовое облучение, электрические токи, переменные магнитные поля, электрофорез и фонофорез лекарственных средств на суставы. При пролиферативных явлениях, вазотрофических расстройствах и контрактурах показаны тепловые процедуры, включая аппликации парафина, озокерита, иловой и торфяной грязи. При отсутствии синовита эффективны морские, радоновые, сульфидные, бишофитные и йодобромные ванны. Для укрепления мышц рекомендуется применение электромиостимуляции.
При выполнении лечебного массажа больным ОА следует избегать механического раздражения суставной капсулы, обращая особое внимание на работу с прилегающими к суставу мышцами. Тогда снижается болевой мышечный спазм, повышается тонус ослабленных групп мышц, усиливается трофика пораженных суставов и улучшаются функциональные способности больного.
При выраженном длительном болевом синдроме, не купируемом традиционными средствами, а также при значительных нарушениях функции сустава применяется хирургическое лечение чаще всего на коленных и тазобедренных суставах. Кардинальной операцией является эндопротезирование сустава. Хорошо зарекомендовали себя эндопротезы, в которых узел скольжения состоит из пары металл–полиэтилен.
Важную роль в профилактике ОА играет выявление и своевременная ортопедическая коррекция врожденных аномалий: вывиха бедра, варусной и вальгусной установки голеней, плоскостопия и др. В профессиональной деятельности необходимо исключить длительные статические и стереотипные механические перегрузки суставов. Существенным условием профилактики ОА коленных суставов является нормализация избыточной массы тела.
Читайте также:


