Метастазы в вертлужную впадину

Какие злокачественные заболевания осложняются
метастазами в костях

Какие кости поражаются при раке
Принципиально возможно развитие метастаза в любой кости скелета, но чаще всего опухолевые клетки задерживаются в костях с лучшим кровоснабжением, где всегда есть достаточное питание для продолжения неуправляемого деления. Очень редко метастазы образуются в мелких косточках кисти и стопы, но часты в обильно пронизанных сосудистой сетью костях таза, позвонках и ребрах, нередко поражают кости черепа, за исключением лицевого скелета. Наибольшую опасность для пациента несёт опухолевое поражение позвонков и трубчатых костей конечностей, когда в месте деструкции при обычной нагрузке случается перелом, лишающий возможности двигаться, а при патологическом переломе шейного позвонка высока вероятность паралича из-за сдавления спинного мозга отломками разрушенной опухолью кости.




Какими бывают метастазы в костях
Раковые клетки разрушают ткань кости, вызывая её деструкцию, которая может проявляться как разрежением костной ткани с образованием бескостных участков, так и увеличением патологической, гораздо менее прочной и чётко структурированной костной массы.
По распространённости выделяют:
- множественные – более десятка вовлечённых в процесс костей, но также обозначается и обширное метастатическое поражение только одной кости;
- единичные – до десяти очагов или не более десятка патологически изменённых костей;
- солитарный – единственный очаг.
Диагностика метастазов в костях

Динамическое наблюдение за течением метастазирования и оценка результатов лечения должны осуществляться одним способом, на одном аппарате и, желательно, одним и тем же специалистом. Если до начала терапии не удалось выполнить МРТ, а было сделано только КТ, то и оценивать итоги терапии надо по КТ
Клинические проявления метастазов в кости
Неблагоприятное осложнение опухолевого поражение кости – патологический перелом в месте деструкции:
- Часто переломы позвонков без существенного смещения происходят незаметно для больного и выявляются при рентгенологическом обследовании.
- Шейные позвонки при переломе могут защемить спинной мозг, вызывая разнообразные нарушения двигательной активности.
- Не остаются незамеченными для пациента переломы конечностей, особенно бедра или плеча, сопровождающиеся усилением боли в месте деструкции и нарушением движений.
- Переломы ребер могут проявиться клиникой межреберной невралгии.
- Кости таза преимущественно ломаются в области лона или вертлужной впадины, как правило, боли невысокой интенсивности, но существенно изменяется походка.
Химиотерапия при метастазах в костях

Преимущественно при костных поражениях используют лекарственный метод – химиотерапию или гормонотерапию, для минимизации возможных осложнений в виде переломов и повышения концентрации кальция в крови дополнительно вводят бисфосфонаты. Бисфосфонаты помогают уменьшить болевой синдром.
Химиотерапия проводится длительно, частые контрольные обследования нецелесообразны, поскольку костная ткань на месте уничтоженной опухоли растет очень медленно. Практически всегда при химиотерапии достигается хороший обезболивающий эффект. При интенсивном болевом синдроме зону деструкции можно облучить, в обязательном порядке лучевой терапии подлежит метастазирование в шейные позвонки, что снижает вероятность перелома.
Операция при метастазах в костях


Хирургическое лечение при метастазировании в скелет преследует одну из двух целей:
- Радикальная операция - полное удаление раковых очагов;
- Паллиативная операция -восстановление функции кости после перелома.
Радикальное лечение возможно при отсутствии первичного рака и одиночном метастатическом поражении скелета. После стабилизации роста солитарного – единственного костного метастаза, с помощью курсов химиотерапии, ставится вопрос об оперативном лечении. Как правило, таким способом лечат поражения конечностей.
Сегодня есть возможность заменить протезом пораженные кости верхних и нижних конечностей, но чаще к операции прибегают при патологическом переломе, когда из-за обширной опухолевой деструкции маловероятно восстановление костной целостности. Операция сложная, требующая плановой подготовки, в том числе и нескольких предварительных курсов химиотерапии и долгого лекарственного лечения после операции.

Такие вмешательства выполняются специальной бригадой, владеющей навыками онкологов и травматологов-ортопедов, в специальной операционной, оснащенной рентгеновским оборудованием, но лучше – КТ-установкой. Опухоль разрушает не только кость, но и прорастает в окружающие мягкие ткани – мышцы, сухожилия и суставы, очень важно для будущего восстановления удалить всё поражённое раком, поэтому во время оперативного вмешательства возникает необходимость уточнения объективной реальности с помощью высокоточной КТ.
В лечении костных метастазов нашел свое место и хирургический метод.
В течение всего времени его использования не прекращаются дебаты — оправдано ли применение достаточно травматичного метода у заведомо бесперспективных больных?
Отвечая на поставленный вопрос, все большее и большее количество профессионалов склоняются в пользу возможности применения оперативного метода в лечении костных метастазов у части больных раком молочной железы.
Теоретически существует опасность, что хирургическое вмешательство может способствовать распространению опухолевых клеток в здоровые участки кости, способствуя тем самым генерализации процесса. Однако на практике это предположение так и не было доказано, особенно в тех случаях, когда операция дополнялась лучевой терапией (Galasko, 1991).
Более того, нет подтверждения того, что последствия хирургического вмешательства и общей анестезии могут влиять на плохой прогноз у этих больных. Наоборот, как было показано в работе Bouma et al. (1983), патологические переломы ассоциируются с повышенным риском развития легочных метастазов, а профилактическая стабилизация угрожающих переломов снижает этот риск.
Хирургическое лечение костных метастазов
Цели хирургического лечения костных метастазов — уменьшение боли, ликвидация состояния паралича, профилактика и лечение патологических переломов. В итоге все это сказывается на качестве и продолжительности жизни пациентов (Махсон А.Н. и соавт., 1994, 2000; Maurer et al., 1995; Tateishi et al., 1997; Dominkus et al., 1998).
Так, средняя продолжительность жизни больных раком молочной железы с патологическими переломами после оперативного вмешательства составляет 12,7 мес. (Parrish and Murray, 1970; Perez et al., 1972). Еще более оптимистичные результаты продемонстрировал в своих работах Harrington (1972, 1975).
Из тех больных, которые находились до перелома на амбулаторном лечении, 94% восстановили после операции способность ходить, у 85% больных было зарегистрировано значительное ослабление боли. Средняя продолжительность жизни при этом составила 19,8 месяцев.
Оперативное лечение костных метастазов обычно проводится в случае прогнозируемой продолжительности жизни пациента не менее 6 месяцев. Но в последнее время, вследствие совершенствования оперативной техники и появления новых имплантационных материалов, агрессивные оперативные вмешательства проводятся более широко, когда предполагаемый срок жизни может исчисляться 2-3 мес., и направлены, в первую очередь, на улучшение качества жизни пациентов (Tateishi, 1996; Shulte et al., 1998).
Состояние этих отрезков должно быть адекватным, чтобы поддерживать металлическую конструкцию. К сожалению, у многих больных качество кости, в виду распространенности процесса, не позволяет выполнить стандартные методики внутренней фиксации.
Оперативное вмешательство при костных метастазов может быть направлено на лечение как угрожающих, так и развившихся патологических переломов.
Литические очаги деструкции в бедренных костях, размер которых превышает 2,5 см, при условии поражения коркового слоя, в высшей степени подвержены переломам (Beals et al., 1971). В группу риска входят также больные с литическими очагами, поражающими трубчатые кости в диаметре более, чем на 50%; и пациенты с непрекращающейся болью после лучевой терапии.
Операцией выбора при угрозе патологического перелома является внутренняя стабилизация, причем вид хирургического вмешательства зависит от локализации пораженного участка. Если возможно, то более предпочтительно использовать интрамедуллярный остеосинтез.
Очень важно, чтобы внутренняя стабилизация поврежденного участка выдерживала необходимую нагрузку при ходьбе, включая давление массы тела на конечность. В случае, когда внутримозговой штифт не может обеспечить этого, стабилизацию конструкции необходимо подкрепить использованием метилметакрилового цемента.
Пластичность акрилового цементирующего вещества до полимеризации делает возможным полное заполнение полости с неровными границами, которая образуется при выскабливании очага, усиливая при этом стандартную металлическую фиксацию.
После полимеризации метилметакрила восстанавливается целостность кости, причем сочетание материалов позволяет добиться свойств конструкции, напоминающих бетон повышенной прочности (Harrington, 1972, 1975; Van Geffen et al., 1997; Krol and Gusta, 1998). Подобная тактика позволяет больному восстановить осанку в течение нескольких дней после операции с минимальным риском возникновения патологического перелома.
Наиболее часто при раке молочной железы патологические переломы возникают в бедренной кости (66%), затем в плечевой кости (28,4%), в голени и предплечье — 3,2%, ключице — 1,3%, на долю всех остальных костей приходится 1,2% (Galasko, 1991).
Патологические трансцервикальные переломы бедренной кости не срастаются вне зависимости от метода ортопедического лечения и степени смещения (Galasko, 1974). В случае локализации очага деструкции в проксимальном отрезке бедренной кости, артропластика, по мнению большинства хирургов, является операцией выбора (Galasko, 1991; Tateishi et al., 1997; Sabo and Bernd, 1998; Wedin et al., 1999).
Причем вид операции зависит от степени распространенности опухоли. Если метастатический очаг отсутствует в вертлужной впадине, то все что требуется — это выполнить гемиартропластику. При данной операции производят широкое иссечение опухоли с последующей фиксацией протеза головки бедренной кости с помощью метилметакрилового цемента.
Если же вертлужная впадина поражена, то показана полная замена сустава. При этом опухоль выскабливается из вертлужной впадины, а поврежденный участок заполняется метилметакрилом. В случаях более распространенного поражения вертлужной впадины может потребоваться восстановление костей таза (Harrington, 1981).
При патологическом переломе диафиза бедренной или берцовой костей операцией выбора является сегментарная резекция кости с последующим внутримозговым остеосинтезом и восполнением дефицита костной ткани керамическими конструкциями или метиметакриловым цементом (Tateishi et al., 1997; Sabo and Bemd, 1998).
Как показали результаты работы Gainor and Buchert (1983), внутренняя фиксация улучшает результаты сращения патологических переломов на 23% по сравнению с фиксацией конечности с помощью шины. Если резекция кости по каким-либо причинам затруднена, то возможно проведение кюретажа опухоли с заполнением образованной полости метилметакрилом и с последующей фиксацией с помощью экстрамедуллярных пластин (Galasko, 1991).
При патологическом переломе плечевых костей внутренняя фиксация также имеет предпочтение, т.к. дает пациенту большую подвижность. Больной раньше начинает пользоваться конечностью и быстрее освобождается от боли.
Вместе с тем, при этой локализации преимущества оперативного лечения по сравнению с консервативной терапией не так очевидны, как в случае с патологическим переломом нижней конечности (Galasko, 1980).
McCormack et al. (1985) подтвердили, что иммобилизация конечности с помощью функционального фиксирующего устройства более предпочтительна только в том случае, если предполагаемая продолжительность жизни не превышает 3 месяцев, во всех остальных ситуациях внутренняя фиксация является методом выбора, что обеспечивает уменьшение боли, восстановление функции верхней конечности и помогает избежать повторного перелома.
Переломы проксимальных отделов плечевых костей могут потребовать выполнения замещающей артропластики. Показания к артропластике в данном случае отличаются от таковых при трансцервикальных переломах бедренной кости.
Замещение плечевых суставов показано только в том случае, если отломки кости нельзя стабилизировать с помощью остеосинтеза из-за локализации очага или распространенности процесса, в то время как замещение тазобедренных суставов необходимо выполнять всегда, т.к. патологические переломы шейки бедра не срастаются вне зависимости от метода лечения.
Большинство патологических переломов плечевых, лучевых и локтевых костей можно лечить с помощью интрамедуллярного остеосинтеза. Переломы в области метафизов могут потребовать фиксации с помощью экстрамедуллярных пластинок. Там, где это необходимо, имплантат может быть дополнительно фиксирован метилметакрилом.
Основная неудача при ортопедических операциях по поводу патологических переломов связана с нестабильностью металлических конструкций. В работе Wedin et al. (1999) говорится о том, что из 162 операций по поводу патологических переломов неудовлетворительный результат зарегистрирован у 14% больных после остеосинтеза и только у 2% — после артропластики.
Махсон А.Н. и соавт. (2000) доложили о результатах хирургического лечения костных метастазов у 43 больных раком молочной железы. Чаще всего проводили резекцию суставного конца кости с эндопротезированием (19 наблюдений), реже выполняли металлосинтез.
Показания к хирургическому лечению
Показаниями к хирургическому лечению метастаза в длинные трубчатые кости являлись: солитарный метастаз и множественные метастазы при наличии патологического перелома или угрозе его возникновения. У 22 (51,2%) больных удалось провести повторные курсы лекарственного и гормонального лечения.
При солитарных метастазах в скелет три года прожили 90,9% больных, при множественных — 39,9% пациенток (р
В настоящее время онкологи исходят из концепции, что только раннее выявление злокачественной опухоли и ее адекватное лечение обеспечивают стойкий и длительный клинический эффект. Практика онкологической службы показала, что только диспансерный метод, являющийся достижением отечественного здравоохран.
Общеизвестно, что дистантное распространение по лимфатическим и кровеносным сосудам (метастазирование) — это высшее выражение автономности опухоли, главный отличительный признак злокачественного процесса и наиболее частая причина смерти больных. Способность к метастазированию позволяет опухо.
Морфологическое исследование опухоли играет ведущую роль в определении прогноза и выборе оптимальной тактики лечения онкологического больного. Патоморфолог информирует клинициста о характере опухопи (доброкачественная или злокачественная), ее гистологической принадлежности, степени дифференц.
Цитологический метод, основанный на микроскопическом изучении и оценке клеточного материала, полученного различным способом из патологического очага, является ветвью онкоморфологии. Цель цитологического исследования — установить правильный диагноз злокачественных опухолей любой локализации и в любой.
Химиотерапия обычно применяется как метод лечения первично-распространенных форм, рецидивов и метастазов злокачественных опухолей. Наряду с этим она может проводиться в дополнение к локальному лечению опухоли (удаление, облучение) вне зависимости от его радикальности. Подобная химиотерапия, .
Хирургический метод лечения злокачественных опухолей остается доминирующим, хотя его отдаленные результаты можно считать удовлетворительными лишь в I-II стадии заболевания, а в остальных — операция рассматривается как обязательный компонент специального лечения. Совершенствование хирургической техни.
Тазобедренный сустав — одно из крупных соединений костей в теле человека, обеспечивающих опору и движение. Образуют его вертлужная впадина и головка бедренной кости. Рассмотрим анатомию вертлужной впадины тазовой кости, а также ее возможные травмы.
Костные и хрящевые структуры таза
Что это такое — вертлужная впадина? Это анатомическое углубление полусферической формы, состоящее из частей седалищной, лобковой и подвздошной костей. У впадины выделяют следующие анатомические структуры:
- передняя стенка,
- задняя стенка,
- передняя колонна,
- задняя колонна,
- дно,
- крыша вертлужной впадины (свод).
Костные колонны обеспечивают прочность. Они соединяются между собой в области свода (крыши). В образовании также имеется вертлужная губа, благодаря которой впадина становится несколько глубже. В самом центре она соединяется с головкой тазобедренной кости.
Полулунная область вертлужной впадины покрыта хрящом, остальную часть выстилает синовиальная оболочка, продуцирующая суставную жидкость. 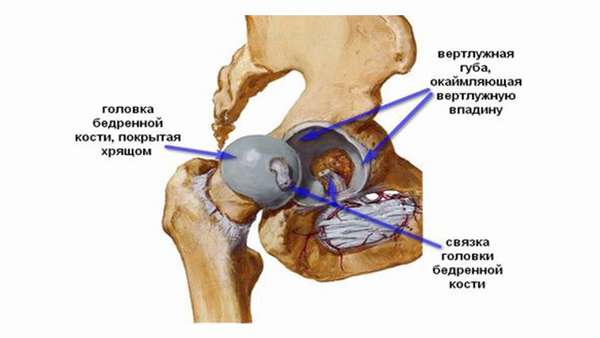
Связочный аппарат
Тазобедренный сустав защищает фиброзная сумка. Она образована поперечными и продольными волокнами соединительной ткани. Стабильность крепления головки бедренной кости к костям таза обеспечивают мышцы и связки.
Выделяют пять пар крупных связок:
- подвздошно-бедренная,
- лобково-бедренная,
- седалищно-бедренная,
- круговая,
- связки головки бедренной кости.
Благодаря большому количеству связок обеспечивается стабильность сустава, снижается риск повреждений при ходьбе и беге. Движения обеспечивают передняя и задняя группа мышц бедра.
Что делать, когда болит нога от бедра до стопы.
Как лечить эпифизеолиз головки бедренной кости.
Функции вертлужной впадины
Вертлужная впадина и головка бедренной кости выполняют важную функцию в опорно-двигательном аппарате. На них приходится большая часть нагрузки при движении и обеспечении опоры.
Благодаря сложному строению в тазобедренном суставе осуществляются следующие движения:
- сгибание и разгибание,
- отведение и приведение,
- ротация (вращение).
Связки и суставная капсула ограничивают амплитуду движений, чтобы не допустить переразгибания ноги и вывихов.
Возможные болезни, травмы и их последствия
Патологические процессы, происходящие в тазобедренном суставе, заключаются, с одной стороны, в изменениях свойств хряща, а с другой — в механических нарушениях. Рассмотрим болезни, связанные с тазовой костью.
Внимание! Каждая из патологий имеет свои клинические особенности и осложнения, поэтому требуется грамотный врачебный подход к диагностике и лечению.
Часто травмы тазовых костей наблюдаются при ДТП, падении человека. Переломы разделяют на простые и сложные. Пострадавший после перелома испытывает сильную боль, не может шевелить поврежденной ногой. Также отмечаются укорочение и патологический поворот нижней конечности.
Диагноз устанавливается на основе рентгена и компьютерной томографии. На фото хорошо видны место и характер перелома, наличие осколков. 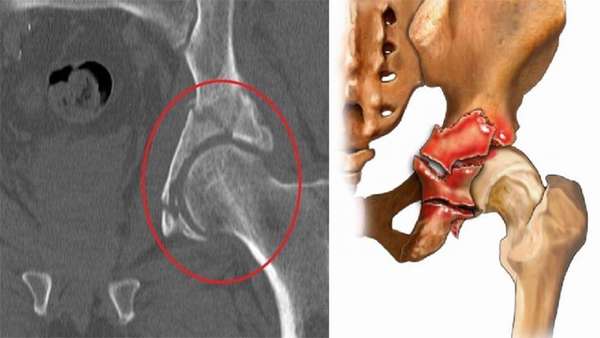
Внимание! Перелом вертлужной впадины требует немедленной госпитализации. Первая помощь — обеспечить горизонтальное положение и покой пострадавшему, дать обезболивающее, дождаться приезда скорой помощи.
Для лечения подобных состояний необходимы проведение скелетного вытяжения и хирургическое вмешательство. Травмы вертлужной впадины могут привести к частичной или полной потере подвижности, постоянной хромоте, укорочению конечности, развитию коксартроза.
При чрезмерной нагрузке на сустав, неудобной постановке ног при беге, прыжках и других движениях отмечаются такие состояния, как подвывих и вывих бедра. При этом происходит смещение головки бедренной кости, что приводит к заклиниванию всего сочленения и невозможности совершения в нем движений.
Протрузия вертлужной впадины — это продавливание ее дна головкой бедренной кости в полость таза. Протрузия может возникнуть в результате рахита, коксартроза, при остеопорозе престарелых. В результате трения костей хрящевая ткань разрушается, формируется артроз.
У подростков продавливание лечат с помощью физиотерапии, вытяжения и лечебной гимнастики, у взрослых проводят операции — артропластику, резекцию головки или шейки бедренной кости, остеотомию, эндопротезирование.
Синдром бедренно-вертлужного соударения (импинджмент-синдром) — одна из аномалий тазобедренного сустава. При ней происходит соударение части бедренной кости и края вертлужной впадины во время движения.
Если на шейке бедренной кости возникает бугорок, или если край вертлужной впадины и ее губы будет неровным, утолщенным, то именно эти бугорки или утолщения будут соударяться при движениях в суставе. При этом возникнет порочный круг: ударяющиеся образования при движении будут воспаляться, отекать, становиться еще больше в размере и еще сильнее соударяться. Лечение проводят оперативным путем.
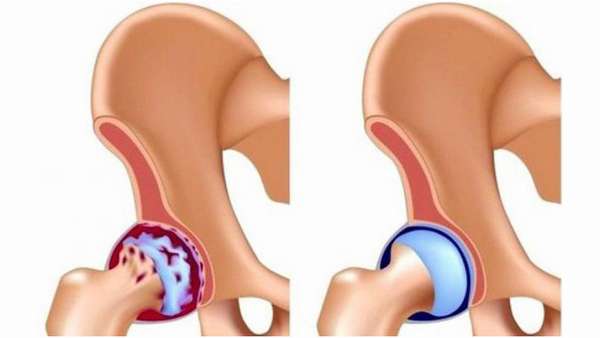
Коксартроз — это дегенеративно-дистрофическое заболевание. Первичный коксартроз появляется на фоне перегрузок тазобедренных суставов, особенно часто он поражает людей с лишним весом. Вторичная форма нередко развивается на фоне дисплазии тазобедренного сустава, частых вывихах бедра.
Эти состояния приводят к разрушению хрящевой ткани. Трение кости о кость вызывает асептическое (неинфекционное) воспаление. Вначале появляются боли в тазобедренном суставе при ходьбе, затем хруст, хромота и ограничение движений. При неэффективности консервативной терапии проводят операцию по эндопротезированию.
Меры профилактики повреждений вертлужной впадины
Для того, чтобы избежать повреждений, врачи советуют придерживаться следующих рекомендаций:
- избегать резких движений ногами, особенно при занятиях динамическими и контактными видами спорта: футбол, баскетбол и др.,
- при занятиях спортом всегда следует выполнять динамическую разминку, позволяющую подготовить суставы к последующим физическим упражнениям,
- нагрузка должна быть адекватной для уровня физической подготовки человека,
- при наличии сопутствующих болезней опорно-двигательного аппарата и внутренних органов важно придерживаться советов и рекомендаций лечащего врача.
Заключение
Вертлужная впадина — важная анатомическая структура, необходимая для формирования и функционирования тазобедренного сочленения. При различных травматических и нетравматических заболеваниях симптомы патологии легко выявляются при внешнем осмотре больного и на фото рентгена.
Любые болезни, связанные с вертлужной впадиной, должен лечить только врач. Самолечение недопустимо, так как оно может привести к прогрессированию патологии и развитию осложнений.

- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
В случае онкологического заболевания в одном из парных органов, его удаление часто позволяет сохранить пациенту жизнь без ущерба для ее качества. Так, например, рак почки эффективно лечится ее удалением, при этом функциональная нагрузка перераспределяется на здоровую почку. Однако в случае с парными конечностями все не так однозначно — ампутация ноги ведет к значительной инвалидизации, депрессии и снижению качества жизни пациента. Для решения данных проблем около 60 лет назад начали применять онкологическое эндопротезирование — замена пораженных опухолью костей и суставов на искусственные конструкции. Клинический случай из моего фоторепортажа наглядно иллюстрирует тактику лечения пациента с учетом перечисленных приоритетов.

Описание клинического случая
В 2007 году у мужчины была удалена почка по поводу онкологического заболевания. Однако через 10 лет были обнаружены метастазы в легких и левой бедренной кости. С помощью иммунотерапии удалось уменьшить очаги в легких, однако опухоль бедренной кости привела к ее патологическому перелому. На снимке видно густое сосудистое сплетение опухоли, которая прорасла в кость и стала причиной патологического перелома шейки бедра:

Сложность операции обуславливалась тем, что удаление метастазов рака почки сопряжено с крупными кровопотерями. Такая опухоль активно выделяет сосудистый фактор роста и очень обильно кровоснабжается. Интраоперационную кровопотерю корректируют переливанием эритроцитарной массы, а эта процедура, в свою очередь, может осложнять клубочковую фильтрацию почек. Поэтому у возрастного пациента с одной почкой выполнять операцию подобного объема очень опасно — высок риск потерять единственную почку. Именно поэтому ему отказали в ведущих медицинских центрах Украины, РФ и Германии. Однако решительно настроенный мужчина все-таки нашел эксперта в лечении пациентов с такой сложной патологией — члена Восточно-европейской группы по изучению Сарком (EESG) — Петра Сергеева, хирурга-онколога клиники Медицина 24/7.
Этап организации доступа
Пациент уложен на правый бок, операционный доступ организуется с внешней стороны левого бедра. Длинна разреза — от проекции тазобедренного сустава до середины бедра. Вид сзади:

После рассечения кожи и жировой клетчатки хирург разрезает мышцы таким образом, чтобы минимизировать травматичность. От этого будет зависеть скорость последующей реабилитации.

Мышцы обильно кровоснабжаются, поэтому часто приходится работать электрокоагулятором:

К удаляемой части бедренной кости крепится несколько крупных мышц, а также сосуды и нервы. Их отделение занимает значительное время операции. На снимке показан момент отсечения связок ягодичных мышц, вид спереди:

Скелетипрована надкостница, бедренная кость готова к резекции.

Этап резекции части бедренной кости с опухолью
Хирургическая электрическая пила-дрель для обработки костей:

Процесс занимает меньше минуты.

В месте распила хирург берет образцы костного мозга и направляет в лабораторию, чтобы убедиться, что оставшаяся часть бедренной кости не содержит опухолевых клеток.

Резецированные связки и фрагмент бедренной кости удаляется вместе с опухолью без вскрытия оболочки кости. На фотографии показаны суставные поверхности тазобедренного сустава:

Хирург объясняет, что удаление большого объема мягких тканей вокруг опухоли снижает риск рецидива злокачественного заболевания.


Этап эндопротезирования
Первые эндопротезы изготавливались заранее под индивидуальный заказ, что не позволяло хирургам пересмотреть планируемый размер резекции кости в ходе операции. Кроме того, необходимо было ждать изготовления изделия не менее 2-х месяцев, что не всегда приемлемо в онкологии. Современные модульные эндопротезы позволяют хирургу прямо во время операции собрать конструкцию с индивидуальными размерами, учитывающими конституцию пациента и особенности клинического случая. Металлические компоненты эндопротеза состоят из сплавов титана, алюминия и никеля, что обеспечивает высокую прочность, низкий вес конструкции, а также инертность в отношении биологических тканей.

Перед установкой эндопротеза костномозговой канал высверливается для удаления костного мозга.

Затем путем многократной обработки костномозговому каналу придается форма шестиугольника — как и у ножки эндопротеза. Такая форма увеличивает площадь контакта ножки эндопротеза с твердыми тканями и обеспечивает более надежную фиксацию.

Специальной насадкой на торце кости формируется фаска для плотного прилегания эндопротеза и равномерного распределения нагрузки:

Перед установкой эндопротеза проводится примерка с использованием набора временных компонентов разных размеров:

Временные элементы конструкции установлены для проведения примерки:

Пациента укладывают на спину, хирург оценивает симметрию и длину ног:

После примерки устанавливаются компоненты эндопротеза с нужными размерами. С учетом удовлетворительного состояния кости хирург принял решение об установке ножки эндопротеза с бесцементной фиксацией. Сначала в костномозговой канал устанавливается ножка эндопротеза. Она имеет матовое напыление гидроксиапатита, чтобы окружающие ткани лучше вросли и зафиксировали эндопротез:

Ножка устанавливается при помощи молотка:

Внешняя часть ножки эндопротеза с креплением:

К ножке фиксируется основной модуль:

К периметру вертлужной впадины тазовой кости пришивается синтетическая муфта-чулок, которая будет служить основой для формирования новой суставной сумки вокруг эндопротеза.

Затем на место удаленной головки бедренной кости в вертлужную впадину тазовой кости устанавливается вкладыш с головкой эндопротеза. Золотистый цвет головке придает напыление нитрида титана — гипоаллергенный и износостойкий материал:

Весь эндопротез укрыт муфтой:

Ранее отсеченные от удаленного фрагмента бедренной кости мышцы подшиваются к муфте. В процессе реабилитации соединительные ткани прорастут в волокна муфты, тем самым образовав прочный связочный аппарат, с помощью которого мышцы смогут вновь управлять конечностью.

Устанавливается дренаж для отведения экссудата лимфы и крови, а также для промывания операционной раны антисептиками с целью профилактики инфекционных осложнений.

Края кожи ушиваются с помощью хирургического степлера за 30 секунд:

После операции выполняется контрольный снимок эндопротеза в 2-х проекциях:

А пациенту давайте все вместе пожелаем сил и терпения, которые понадобятся ему для длительной реабилитации!
Через неделю после операции:
Читайте также:






