Лечение мышечной дистонии баклофеном
Основными препаратами, используемыми для снижения мышечного тонуса, являются миорелаксанты. Рассмотрены вопросы выбора терапии с использованием антиспастических препаратов в зависимости от заболевания, выраженности мышечной спастичности, побочных эффектов
Myorelaxants are the basic preparations used for reduction in the muscular tone. Issues of selection of therapy by anti-spastic preparations depending on the disease, manifestation of muscular spasticity, side effects and special features of the preparation effect are considered.
Основными препаратами, используемыми для снижения мышечного тонуса, являются миорелаксанты. По механизму действия различают миорелаксанты центрального действия (влияют на синаптическую передачу возбуждения в центральной нервной системе) и периферического действия (угнетают прямую возбудимость поперечно-полосатых мышц). При применении миорелаксантов могут возникать достаточно значимые побочные действия, которые при выборе препарата надо тщательно оценивать [1, 2].
При выборе антиспастических препаратов учитывают в основном их способность тормозить полисинаптические рефлексы (уменьшение спастики), оказывая при этом наименьшее влияние на моносинаптические рефлексы (сила мышц). Антиспастический препарат должен уменьшать мышечную спастичность при минимальном снижении мышечной силы [3, 4].
Медикаментозная терапия основана на использовании таблетированных и инъекционных форм. Применяемые внутрь антиспастические средства, уменьшая мышечный тонус, могут улучшить двигательные функции, облегчить уход за обездвиженным пациентом, снять болезненные мышечные спазмы, усилить действие лечебной физкультуры, предупредить развитие контрактур [5]. При легкой степени спастичности применение миорелаксантов может привести к значительному положительному эффекту, однако при выраженной спастичности могут потребоваться большие дозы миорелаксантов, применение которых нередко вызывает нежелательные побочные эффекты. Лечение миорелаксантами начинают с минимальной дозы, затем ее медленно повышают для достижения эффекта [6].
К миoрелаксантам центрального действия, наиболее часто используемым в России для лечения спастического мышечного гипертонуса, относятся баклофен, тизанидин, толперизон, диазепам [7, 8].
Баклофен (Баклосан, Лиорезал) оказывает антиспастическое действие преимущественно на спинальном уровне. Препарат представляет аналог гамма-аминомасляной кислоты (ГАМК), который связывается с пресинаптическими ГАМК-рецепторами, приводя к уменьшению выделения возбуждающих аминокислот (глутамата, аспартата) и подавлению моно- и полисинаптической активности на спинальном уровне, что и вызывает снижение спастичности. Препарат проявляет также умеренное центральное анальгезирующее действие. Баклофен используется при спинальном и церебральном спастическом мышечном гипертонусе различного генеза. Начальная доза составляет 5–15 мг/сут (в один или три приема), затем дозу увеличивают на 5 мг каждый день до получения желаемого эффекта. Препарат принимают во время еды. Максимальная доза баклофена для взрослых составляет 60–75 мг/сут. Побочные эффекты чаще проявляются седацией, сонливостью, снижением концентрации внимания, головокружением и часто ослабевают в процессе лечения. Возможно возникновение тошноты, запоров и диареи, артериальной гипертонии, усиление атаксии, появление парестезий. Требуется осторожность при лечении больных пожилого возраста, пациентов, перенесших инсульт, пациентов с язвенной болезнью желудка и двенадцатиперстной кишки. Баклофен противопоказан при эпилепсии, наличии судорог в анамнезе [9, 10].
При выраженной спастичности, когда обычное пероральное применение антиспастических препаратов не эффективно, показано интратекальное введение баклофена, которое впервые было предложено в 1984 г. R. Penn. Для достижения необходимой концентрации препарата в спинномозговой жидкости необходимо принимать довольно значительные дозы баклофена, что может привести к нарушениям сознания, сонливости, слабости. В связи с этим были разработаны системы, при помощи которых баклофен доставляется непосредственно в подоболочечное пространство спинного мозга при помощи подоболочечной баклофеновой насосной системы. При этом клинического эффекта добиваются гораздо меньшими дозами баклофена, чем при использовании таблетированных форм [11, 12].
Данная система состоит из резервуара, где содержится баклофен или аналогичный препарат, насоса (помпы), при помощи которого препарат дозированно подается в подоболочечное пространство спинного мозга через люмбальный катетер и блока питания. Из резервуара баклофен поступает непосредственно в спинномозговую жидкость, а его дозировка контролируется специальным радиотелеметрическим устройством. Количество поступающего в спинномозговую жидкость лекарственного препарата можно изменять в зависимости от клинической картины. Добавление баклофена в резервуар производится через 2–3 месяца при помощи чрезкожной пункции [13].
Использование баклофеновой помпы улучшает скорость и качество ходьбы больных с нефиксированными рефлекторными контрактурами, обусловленными высокой спастичностью мышц-синергистов и дисбалансом мышц-антагонистов. Имеющийся 15-летний клинический опыт применения баклофена интратекально у больных, перенесших инсульт, свидетельствует о высокой эффективности этого метода в уменьшении не только степени спастичности, но и болевых синдромов и дистонических расстройств. Отмечено положительное влияние баклофеновой помпы на качество жизни больных, перенесших инсульт [14].
Тизанидин (Сирдалуд) — миорелаксант центрального действия, агонист альфа-2-адренергических рецепторов. Препарат снижает спастичность вследствие подавления полисинаптических рефлексов на уровне спинного мозга, что может быть вызвано угнетением высвобождения возбуждающих аминокислот L-глутамата и L-аспартата и активацией глицина, снижающего возбудимость интернейронов спинного мозга. Тизанидин обладает также умеренным центральным анальгетическим действием. Препарат эффективен при церебральной и спинальной спастичности, а также при болезненных мышечных спазмах. Начальная доза препарата составляет 2–6 мг/сут в один или три приема, при индивидуальном подборе увеличение дозы происходит на 3–4 день на 2 мг. При пероральном приеме действие препарата проявляется через 30–45 минут, максимальный эффект наступает в течение 1–2 часов. Средняя терапевтическая доза составляет 12–24 мг/сут, максимальная доза — 36 мг/сут. В качестве побочных эффектов могут возникнуть сонливость, сухость во рту, головокружение и снижение артериального давления, что ограничивает использование препарата при постинсультной спастичности. Антиспастический эффект тизанидина сопоставим с эффектом баклофена, однако тизанидин при адекватном подборе дозировки лучше переносится, т. к. не вызывает общей мышечной слабости и не усиливает мышечную слабость в парализованной конечности [15, 16].
Толперизон (Мидокалм) — антиспастический препарат центрального действия, угнетает каудальную часть ретикулярной формации и обладает Н-холинолитическими свойствами. Толперизон снижает активность спинальных нейронов, участвующих в формировании спастичности, путем ограничения потока натрия через мембрану нервных клеток. Наиболее часто используется по 300–450 мг/сут в два или три приема. Снижение мышечного тонуса при назначении толперизона иногда сопровождается сосудорасширяющим действием, что следует учитывать при назначении больным с тенденцией к артериальной гипотонии. Также препарат может вызывать или усиливать у больных недержание мочи [17].
Основным побочным эффектом баклофена, тизанидина и толперизона является быстрое наступление мышечной слабости, причем в каждом случае врач должен находить баланс между снижением тонуса и усилением слабости. Кривая баланса между снижением спастического тонуса и усилением мышечной слабости у больных на фоне увеличения дозы Мидокалма, Сирдалуда или Баклофена показывает, что наиболее быстрое усиление слабости происходит при приеме Баклофена, а самый мягкий препарат, позволяющий эффективно подобрать индивидуальную дозировку, — Мидокалм. Во всех случаях, учитывая наличие узкого терапевтического окна, курс лечения начинают с небольшой дозы препарата, постепенно наращивая ее до достижения отчетливого антиспастического эффекта, но не до появления слабости [18, 19].
Диазепам (Реаланиум, Релиум, Сибазон) является миорелаксантом, поскольку обладает способностью стимулировать уменьшенное пресинаптическое торможение на спинальном уровне. Он не имеет прямых ГАМК-ергических свойств, увеличивает концентрацию ацетилхолина в мозге и тормозит обратный захват норадреналина и дофамина в синапсах. Это приводит к усилению пресинаптического торможения и проявляется снижением сопротивляемости растяжению, увеличением диапазона движений. Диазепам также обладает способностью уменьшать болевой синдром, вызываемый спазмом мышц. Наряду со снижением мышечного тонуса, развиваются заторможенность, головокружение, нарушение внимания и координации ввиду токсического действия на центральную нервную систему. Это значительно ограничивает применение диазепама в качестве миорелаксанта. Используется он, в основном, для лечения спастичности спинального происхождения при необходимости кратковременного снижения мышечного тонуса. Для лечения спастичности назначают в дозе 5 мг однократно или по 2 мг 2 раза в день. Максимальная суточная доза может составлять 60 мг. При больших дозах могут отмечаться расстройства сознания, преходящая дисфункция печени и изменения крови. Продолжительность лечения ограничена из-за возможного развития лекарственной зависимости [20].
Клоназепам является производным бензодиазепина. Клоназепам оказывает успокаивающее, центральное миорелаксирующее, анксиолитическое действие. Миорелаксирующий эффект достигается за счет усиления ингибирующего действия ГАМК на передачу нервных импульсов, стимуляции бензодиазепиновых рецепторов, расположенных в аллостерическом центре постсинаптических ГАМК-рецепторов восходящей активирующей ретикулярной формации ствола головного мозга и вставочных нейронов боковых рогов спинного мозга, а также уменьшения возбудимости подкорковых структур головного мозга и торможения полисинаптических спинальных рефлексов.
Быстрое наступление сонливости, головокружения и привыкания ограничивает применение этого препарата. Для снижения проявления возможных побочных реакций, достигать терапевтической дозы необходимо путем медленного титрования в течение двух недель. Для приема внутрь взрослым рекомендуется начальная доза не более 1 мг/сут. Поддерживающая доза — 4–8 мг/сут. Возможно назначение небольших доз в сочетании с другими миорелаксантами. Клоназепам эффективен при пароксизмальных повышениях мышечного тонуса. Противопоказан при острых заболеваниях печени, почек, миастении [21].
Дикалия клоразепат (Транксен) — аналог бензодиазепина, трансформируется в главный метаболит диазепама, обладает большей активностью и длительностью антиспастического действия, чем диазепам. Отмечен его хороший эффект при лечении в виде уменьшения фазических рефлексов на растяжение, обладает незначительным седативным эффектом. Первоначальная доза составляет 5 мг 4 раза в сутки, затем уменьшается до 5 мг 2 раза в сутки [22].
Дантролен — производное имидазолина, действует вне центральной нервной системы, преимущественно на уровне мышечных волокон. Механизм действия дантролена — блокирование высвобождения кальция из саркоплазматического ретикулума, что ведет к снижению степени сократимости скелетных мышц, редукции мышечного тонуса и фазических рефлексов, увеличению диапазона пассивных движений. Важным преимуществом дантролена по отношению к другим миорелаксантам является его доказанная эффективность в отношении спастичности не только спинального, но и церебрального генеза. Начальная доза — 25 мг/сут, при переносимости дозу увеличивают в течение 4 недель до 400 мг/сут. Побочные эффекты — сонливость, головокружение, тошнота, диарея, снижение скорости клубочковой фильтрации. Серьезную опасность, особенно у пожилых пациентов в дозе более 200 мг/сут, представляет гепатотоксическое действие, поэтому в период лечения надо регулярно следить за функцией печени. Элиминация дантролена на 50% осуществляется за счет печеночного метаболизма, в связи с этим он противопоказан при заболеваниях печени. Осторожность следует соблюдать и при тяжелых сердечных или легочных заболеваниях.
Катапресан — применяется в основном при спинальных повреждениях, действует на альфа-2-агонисты головного мозга, обладает пресинаптическим торможением. Из побочных эффектов отмечаются снижение артериального давления и депрессия. Первоночальная доза — 0,05 мг 2 раза в день, максимальная — 0,1 мг 4 раза в день.
Темазепам — взаимодействует с бензодиазепиновыми рецепторами аллостерического центра постсинаптических ГАМК-рецепторов, расположенных в лимбической системе, восходящей активирующей ретикулярной формации, гиппокампе, вставочных нейронах боковых рогов спинного мозга. В результате открываются каналы для входящих токов ионов хлора и таким образом потенцируется действие эндогенного тормозного медиатора — ГАМК. Рекомендуемая доза — 10 мг 3 раза в день. Эффективно его сочетание с баклофеном [23, 24].
Основные лекарственные средства, используемые для лечения спастического мышечного гипертонуса, представлены в табл.
Таким образом, выбор препарата определяется основным заболеванием, выраженностью мышечной спастичности, а также побочными эффектами и особенностями действия конкретного препарата.
Так, например, тизанидин и баклофен в большей степени действуют на тонус мышц-разгибателей, поэтому в случаях наличия значительного гипертонуса мышц-сгибателей руки, легкой спастичности мышц ноги их прием не показан, поскольку легкое повышение тонуса мышц-разгибателей ноги компенсирует мышечную слабость в ноге и стабилизирует походку больного. В таком случае средством выбора являются методы физического воздействия на мышцы верхней конечности.
При лечении церебральной спастичности наиболее часто применяют Сирдалуд, а при спинальной спастичности — Сирдалуд и Баклофен. Важным преимуществом перед другими миорелаксантами обладает Мидокалм, который не оказывает седативного эффекта и имеет благоприятный спектр переносимости, поэтому является препаратом выбора для лечения в амбулаторных условиях и для лечения пожилого контингента пациентов.
Допустима комбинация нескольких средств, что позволяет эффективно снижать тонус на меньших дозах каждого из препаратов. Сочетание препаратов с разными точками приложения, начиная от центров в головном мозге и до мышц, может привести к суммированию терапевтического эффекта.
Эффективность пероральных антиспастических препаратов снижается при их длительном использовании, часто возникает необходимость возрастающего повышения дозировок для поддержания начального клинического эффекта, что сопровождается увеличением частоты и тяжести побочных реакций [25–27].
В ситуации, когда спастичность носит локальный характер и системный эффект пероральных миорелаксантов нежелателен, предпочтительны локальные методы воздействия, одним из которых является локальное введение ботулотоксина [28, 29].
Литература
А. А. Королев, кандидат медицинских наук
- Все
- А
- Б
- В
- Г
- Д
- И
- К
- Л
- М
- Н
- О
- П
- Р
- С
- Т
- Ф
- Х
- Ц
- Э
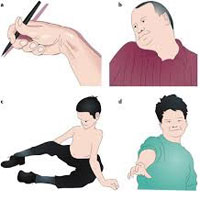
Симптомы дистонии
Мышечная дистония может быть в различных частях тела. Ранние симптомы могут включать в себя ухудшение почерка после написания нескольких строк, судороги в ногах или скованность в мышцах ног, могут возникать неожиданно как "гром среди ясного неба" или возникать после бега или ходьбы на некоторое расстояние. Возможно непроизвольное скручивание шеи, особенно после нагрузки или стресса. Иногда возникает непроизвольное частое моргание глаз, что может приводить к функциональной слепоте. Другие возможные симптомы это тремор и нарушения речи. Начальные симптомы могут быть очень незначительными и могут быть заметны только после длительных нагрузок, стресса или усталости. Со временем симптомы могут стать более явными и стойкими, но, иногда, они могут не прогрессировать.
У некоторых пациентов, симптомы дистонии появляются в детстве, в возрастном промежутке от 5 до 16 лет, чаще всего, в конечностях (ноге или в руке). При генерализованной дистонии дистонические движения могут быстро прогрессировать и вовлекать все конечности и туловище, но скорость прогрессирования обычно заметно замедляется после завершения пубертатного возраста.
У других пациентов, симптомы появляются в конце подросткового или раннего взрослого возраста. В таких случаях, дистония нередко начинается в верхних частях тела, а симптоматика прогрессирует медленно. Дистония, которая начинается в зрелом возрасте, чаще всего, остается фокальной или сегментарной дистонией.
Прогрессирование дистонии проходит несколько стадий. Первоначально дистонические движения преходящие и появляются только во время произвольных движений или стресса. В дальнейшем, у пациентов могут возникать дистонические ненормальные позы и движения во время ходьбы и, в конечном счете, даже в состоянии покоя. Дистонические движения могут со временем привести к стойким физическим дефектам, так как возникают укорочения сухожилий.
При вторичных дистониях вследствие травмы или инсульта у пациентов отмечаются аномальные движения только с одной стороны тела, которые могут появиться сразу после травмы головного мозга (инсульта) или через некоторое время после. Симптомы обычно не прогрессируют и не охватывают другие части тела.
Классификация дистоний
Одна из классификаций дистонии подразделяет их в зависимости от частей тела, вовлеченных в это состояние:
- Генерализованная дистония охватывает большую часть тела или все тело.
- Фокальная дистония локализуется в определенной части тела.
- Мультифокальная дистония включает в себя два или более участка тела.
- Сегментарная дистония влияет на два или более соседних части тела.
- Гемидистония охватывает одну сторону тела
Некоторые типы дистонии выделяются как отдельные синдромы:
Торсионная дистония, которая ранее называлась мышечная деформирующая дистония является редкой формой дистонии, имеет генетическую детерминированность, обычно начинается в детстве и неуклонно прогрессирует. Торсионная дистония приводит к выраженным физическим дефектам и нередко к тяжелой инвалидизации. Исследования генетиков выявили причину этой формы дистонии (у многих пациентов имелись мутации в гене под названием DYT1). Было также отмечено, что этот ген ассоциирован не только с генерализованной дистонией, но и с некоторыми формами фокальной дистонии. Тем не менее, есть данные, что большинство дистоний не связаны с этим дефектом гена и имеют неизвестную причину.
Цервикальная дистония или спастическая кривошея, является наиболее распространенной фокальной дистонией. При спастической кривошее страдают мышцы, контролирующие положение головы, в результате чего, происходит скручивание и поворот головы в одну сторону. Кроме того, голова может быть наклонена вперед или назад. Спастическая кривошея может возникнуть в любом возрасте, хотя большинство людей дебютные симптомы отмечают в среднем возрасте. Спастическая кривошея начинается медленно и, постепенно прогрессируя, останавливается на одном уровне. У 10 - 20 процентов пациентов со спастической кривошеей возникает ремиссия, но, к сожалению, ремиссия не бывает стойкой.
Блефароспазм, второй из наиболее распространенных видов фокальной дистонии - это непроизвольное, насильственное закрытие век. Первые симптомы могут быть в виде неконтролируемого мигания. На начальном этапе может быть вовлечен только один глаз, но в итоге происходит вовлечение мышц обоих глаз. Спазмы могут приводить к полному закрытию век, в результате чего, возникает функциональная слепота, хотя сами глаза и зрение в норме.
Краниальная дистония это термин, используемый для описания дистонии, которая влияет на мышцы головы, лица и шеи. Оромандибулярная дистония затрагивает мышцы челюсти, губ и языка. Челюсть, может выдвигаться вперед, опускаться или закрываться и возможны нарушения глотания и речи. Спастические дисфония поражает мышцы гортани, которые контролируют речь, что может вызвать нарушения речи, дыхания или хриплость голоса. Синдром Мейга является сочетанием блефароспазма и оромандибулярной дистонии и иногда спастической дисфонии.Спастическая кривошея также иногда классифицируется, как краниальная дистония.
Писчий спазм - это дистония, которая затрагивает мышцы кисти, а иногда и предплечья, и возникает только во время письма. Подобные координационные дистонии также называется судорогами машинистки и судорогами музыканта.
Допа - зависимая дистония (ДЗД), одной из которых является дистония Segawa, достаточно хорошо поддается лечению препаратами этой группы (леводопа), которые обычно используются для лечения болезни Паркинсона.
Как правило, ДЗД начинается в детстве или в подростковом возрасте, с прогрессирующим ухудшением процесса ходьбы, а в некоторых случаях и наличием спастичности. При дистонии Segawa, симптомы могут колебаться в течение дня от относительной мобильности утром, с постепенным ухудшением в дневное и вечернее время, а также после физических упражнений. Диагноз ДЗД может быть не выставлен своевременно, так как эта форма дистонии по проявлениям напоминает по симптоматике церебральный паралич. Кроме того, существуют формы дистонии, которые могут иметь четкую генетическую причину: DYT1 дистония является редкой формой доминантно наследуемой генарализованной дистонии, которая может быть вызваны мутацией в гене DYT1. Эта форма дистонии обычно начинается в детстве, сначала влияет на конечности, и неуклонно прогрессирует, часто вызывая инвалидизацию. Поскольку эффекты мутации гена проявляются не всегда, у некоторых людей с наличием мутации этого гена может не быть проявлений дистонии.
В последнее время исследователи выявили еще одну генетическую причину дистонии связанную связано с мутациями в гене DYT6. Дистония вызванная мутацией в гене DYT6 часто проявляется как черепно-лицевая дистония, цервикальная дистонии или дистония руки.
Многие другие гены, которые вызывают дистонические синдромы, были идентифицированы в последние годы. Некоторые важные генетические причины дистонии включают мутации в следующих генах: DYT3, который вызывает дистонию, связанную с паркинсонизмом; DYT5 (GTP циклогидролазы 1), который связан с допа - зависимой дистонией (болезнь Segawa); DYT6, связанный с несколькими клинические проявления дистонии; DYT11 - вызывает дистонию, связанную с миоклонусами, DYT12 - вызывает быстрое развитие дистонии, связанной с паркинсонизмом.
Механизм развития дистонии
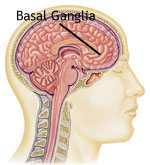
Ученые считают, что дистонии возникают в результате нарушений функционирования в области мозга, которая называется базальные ганглии, где происходит обработка информации от импульсов, которые поступают в мозг при сокращениях мышц. Ученые предполагают, что происходит нарушение выработки организмом определенной группы химических веществ (нейротрансмиттеров), которые позволяют клеткам мозга взаимодействовать друг с другом. Некоторые из этих нейротрансмиттеров включают:
- GABA (гамма-аминомасляная кислота), ингибирующее вещество, которое помогает мозгу контролировать мышцы.
- Допамин, химическое вещество, которое оказывает тормозящее влияние мозга на двигательную активность.
- Ацетилхолин, химическое вещество активирующего действия, которое помогает регулировать действие дофамина в головном мозге. В организме ацетилхолин выделяется в нервные окончания и вызывает сокращение мышц.
- Норадреналин и серотонин, ингибирующие вещества, которые помогают мозгу регулировать действие ацетилхолина.
Приобретенные дистонии, которые также называются вторичные дистонии, являются результатом влияния экзогенных факторов или заболеваний, приводящих к повреждению базальных ганглиев. Родовая травма (в частности, из-за гипоксии мозга), некоторые инфекции, реакция на некоторые лекарства, тяжелые металлы или отравления окисью углерода, травмы, или инсульт могут привести к появлению дистонических симптомов. Дистонии также могут быть симптомами других заболеваний, некоторые из которых могут быть наследственными.
Около 50% случаев дистонии не имеют никакой связи с заболеваниями или травмами и называются первичной или идиопатической дистонией.
Некоторые случаи первичной дистонии могут иметь различные типы наследственных паттернов.
Лечение
В настоящее время не существует медикаментов, которые могут предотвратить развитие дистонии или замедлить прогрессирование. Однако существует несколько вариантов лечения, которые могут облегчить некоторые симптомы дистонии, поэтому врачи могут подобрать каждому пациенту определенную тактику лечения, основанную на конкретных симптомах.
- Ботулинотерапия. Инъекции ботулинического токсина часто являются наиболее эффективным средством для лечения фокальной дистонии. Инъекции небольших количеств этого химического вещества в пораженные мышц предотвращает мышечные сокращения и может обеспечить временное улучшение аномальных поз и движений, которые характерны для дистонии. Вначале эти инъекции использовались для лечения блефароспазма, но в настоящее время широко используются для лечения других основных дистоний. Ботулинический токсин уменьшает мышечные спазмы, блокируя высвобождение нейромедиатора ацетилхолина, который вызывает сокращение мышцы. Эффект обычно начинает проявляться через несколько дней после инъекции и может длиться в течение нескольких месяцев, прежде чем появляется необходимость повторной инъекции.
- Медикаментозное лечение. Несколько классов лекарственных средств, которые оказывают влияние на различные нейромедиаторы могут быть эффективными для лечения различных форм дистонии. Эти препараты включают:
- Антихолинергические средства - блокируют действие нейротрансмиттера ацетилхолина. Медикаменты этой группы включают тригексифенидил и бензтропин. Иногда эти лекарства могут вызывать побочные действия, такие как сонливость или нарушения памяти, особенно при использовании высоких доз и у пожилых людей. Эти побочные действия могут ограничивать их положительный эффект. Другие побочные эффекты, такие как сухость во рту и запор,обычно можно корректировать с помощью изменения диеты или других лекарственных препаратов.
- ГАМК-эргические препараты, регулирующие нейротрансмиттер ГАМК. Эти препараты включают бензодиазепины, такие как диазепам, лоразепам, клоназепам и баклофен. Сонливость является их общим побочным эффектом.
- Допаминергические препараты действуют на систему дофамина и нейротрансмиттера допамина, который участвует в контроле работы мышц. Некоторые пациентам хороший эффект дает применение препаратов, которые блокируют действие допамина, таких как тетрабеназин. Побочные эффекты (например, увеличение веса и непроизвольные и повторяющиеся движения мышц) могут ограничить использование этих препаратов. Dopa- зависимая дистония (ДЗД) является специфической формой дистонии, которая чаще всего встречается у детей, и достаточно неплохо лечится леводопой.
- Глубокая стимуляция мозга может быть рекомендована некоторым пациентам с дистонией, особенно когда лекарства не достаточно снижают симптоматику или побочные эффекты лекарств достаточно выраженные. При ГСМ проводится имплантация небольших электродов (подключенных к генератору импульсов) в конкретные отделы головного мозга, которые контролируют движение. Контролируемые электрические импульсы направляются точно в области мозга, которые формирует дистонические симптомы, и таким образом блокируют патологическую импульсацию этих отделов.
- ЛФК. Программы упражнений являются дополнением к другим методам лечения.
Хирургические методы лечения в некоторых случаях могут быть рекомендованы отдельным пациентам, когда лекарства оказываются не эффективны или побочные эффекты являются слишком серьезными. В отдельных случаях при выраженной генерализованной дистонии проводится хирургическая деструкция части таламуса, глубокой структуры мозга контролирующей движения. Нарушение речи является основным риском такой процедуры, так как таламус располагается около структур головного мозга, контролирующих речь. Хирургическая денервация мышц иногда помогает при фокальной дистонии, в том числе при блефароспазме, спазматической дисфонии и кривошее. Но результаты таких денерваций не очень обнадеживающие в долгосрочной перспективе.
Использование материалов допускается при указании активной гиперссылки на постоянную страницу статьи.
Дистония — это общий медицинский термин, объединяющий ряд двигательных расстройств, вызывающих мышечные спазмы и сокращения, или же судороги.
Судороги и спазмы могут быть либо замедленными, либо приходящими и уходящими, то есть периодическими. Кроме того, пациентам с дистонией причиняет неудобства положение тела — конечности и голова подвергаются тремору, позы болезненны и неестественны для здорового человека. Тремор является симптомом лишь определенного типа дистонии, этот симптом несвойственен всем подтипам заболевания.
Дистония относится к неврологическим заболеваниям (вызванным проблемами с мозгом и нервной системой). Однако в большинстве случаев функции мозга, такие как интеллект, память, речь и другие – остаются неизменными.
Типы мышечных дистоний
Дистония может воздействовать только на одну мышцу или группу мышц.
Существует пять основных типов дистонии:
- Фокусная.
Затрагивает только одну мышцу или часть тела, например, руки или глаза. К такому типу относится блефароспазм — аномальное подергивание одного века или обоих век, цервикальный спазм, писчий спазм или спазм мышц руки, отвечающих за правильное удерживание ручки или карандаша. В целом, если спазм и судорога охватывает один определенный участок, этот тип дистонии называется фокусной.
- Цервикальная.
- Сегментная.
Относится к двум и более областям тела. Например, шее и ноге, двум ногам, двум рукам и т.д.
- Черепная.
Задействованы мышцы нижней челюсти, языка, подбородка. Вызывает затруднения в процессе глотания пищи, воды, слюны. Может влиять на тембр голоса, общую способность говорить.
- Мультифокальная.
Охвачены два или более участка тела, причем не обязательно связанные между собой.
- Обобщенная.
Локализуется следующим образом: мышцы позвоночника и минимум две конечности или какие-либо два участка тела. Мышцы ног не всегда поражены.
- Гемидистония.
Поражение одной половины тела.
- Медикаментозная.
Может вызывать различные типы дистоний, например, фокусную или мультифокальную. Хорошо поддается лечению. Были зафиксированы случаи, при которых медикаментозная дистония самопроизвольно исчезала за несколько дней при отмене лекарства, вызывающего мышечные спазмы.
- Семейная, несемейная.
Наследственный тип дистонии называется семейным, может наследоваться любой тип из описанных выше. Несемейная означает, что даже при полностью здоровых близких родственниках заболевание проявляется либо с рождения, либо в более поздний период. Причинами такого проявления могут быть различные состояния и синдромы.
- Идиопатическая.
Развивается без очевидных причин, спонтанно.
Различают также классификацию дистонии по типу конечностей или частей тела, которые они поражает.
Примерно 90% случаев всех проявленных дистоний — это цервикальная дистония, затрагивающая мышцы шеи или блефароспазм (веки). Оба подтипа в действительности являются подтипами фокальной дистонии, развиваются в более зрелом возрасте, а не в раннем детстве, и могут поддаваться лечению при своевременной диагностике и комплексном терапевтическом подходе.
Причины дистонии мышц, диагностика
В большинстве случаев мышечная дистония не имеет конкретной причины. Дистония — следствие нарушений работы базальных ганглиев мозга. Эта область мозга отвечает за инициирование сокращения мышц. Основная проблема при данном состоянии — это нарушение сообщения нервных импульсов с мышцами.
Приобретенная дистония всегда является следствием повреждения базальных ганглиев.
Кроме того, причины дистонии могут быть следующими:
- травма мозга;
- инсульт;
- опухоль мозга;
- кислородное голодание;
- инфекционное заболевание (энцефалит, менингит инфекционного характера);
- реакция на медикаменты;
- отравление свинцом;
- токсический эффект монооксида углерода.
Если идентифицируемой причины дистонии нет, она называется первичной.
Вторичная мышечная дистония развивается как симптом основного заболевания или последствие травмы. Общие причины вторичной дистонии это:
- черепно-мозговая травма;
- энцефалит;
- болезнь Паркинсона;
- инсульт;
- менингит.
Тип заболевания определяют по области спастичности. Запущенные состояния диагностируются исходя из внешних признаков, без дополнительных диагностических манипуляций. Для точной диагностики необходимы:
- анализ крови;
- анализ мочи;
- МРТ;
- генетическая экспертиза;
- физический осмотр.
Симптомы дистонии, факторы риска
Симптомы дистонии варьируются в зависимости от типа заболевания и возраста, в котором оно развивается. При раннем начале симптомы проявляются в детстве или подростковом возрасте. Обычно первыми страдают ноги и руки, либо мышцы верхней части тела.
Типы мышц, которые чаще всего поражаются при дистонии:
- мышцы шеи;
- мышцы ног и рук;
- мышцы спины.
Дистония, начинающаяся во взрослом возрасте, поражает шею, руки или голову.
Симптомы ранней мышечной дистонии:
Практически все типы мышечной дистонии схожи по своим симптомам и проявляются интенсивнее при стрессе, плохом самочувствии, усталости, заболеваниях, не связанных с мышцами.
Факторы риска или факторы, из-за которых мышечная дистония усиливается, это:
- стресс;
- бессонница;
- усталость;
- эмоциональная перегрузка;
- большое количество новой информации;
- инфекционные заболевания;
- неврологические нарушения;
- употребление алкоголя;
- употребление кофе и продуктов с кофеином;
- употребление психоактивных веществ;
- наркотическое опьянение.
Методы лечения дистонии мышц, прогноз
Лечение дистонии определяется типом заболевания и точной клинической картиной. Однако существует четыре основных метода лечения, применяемых практически при всех типах:
- ботулинический токсин; широко используется для лечения неврологических состояний, к которым относятся аномальные сокращения мышц, токсин вводится прямо в пораженные мышцы, чтобы временно ослабить или уменьшить спазмы;
- лекарственные препараты; например, антихолинергические препараты, баклофен и миорелаксанты;
- физиотерапия; специальные программы упражнений для улучшения мышечного тонуса и положения тела в пространстве, а также для предотвращения мышечной слабости;
- хирургическое лечение; применяется в том случае, когда другие методы лечения не оказывают ожидаемого эффекта. При таком лечении нервы, контролирующие мышцы, подвергаются селективной периферической денервации.
Еще один метод лечения — временное имплантирование электродов в головной мозг с устройством, похожим на кардиостимулятор (метод глубокой стимуляции мозга).
Препараты, уменьшающие проявления дистонии:
- Леводопа;
- Проциклидина гидрохлорид;
- Диазепам;
- Лоразепам;
- Клоназепам;
- Баклофен.
Прогноз
Дистония — непредсказуемое заболевание. Она имеет тенденцию медленно прогрессировать, и тяжесть симптомов у пациента зависит как от индивидуальных причин, общего состояния здоровья, степени прогресса и общих факторов. Фокальная дистония прогрессирует медленно в течение примерно 5 лет, а затем наступает резкое ухудшение состояния здоровья.
Иногда состояние больного спонтанно улучшается, а симптомы практически или полностью исчезают. Это состояние называется полной ремиссией, происходит оно примерно у 5-10% пациентов. Общая ремиссия свойственна людям с вторичной дистонией, появившейся как следствие приема лекарственных препаратов или стресса, травмы или других факторов. При болезни Паркинсона, например, симптомы высокого мышечного тонуса сохраняются до конца жизни.
Читайте также:


