Изменения синовиальной оболочки при ревматоидном артрите
Аннотация научной статьи по клинической медицине, автор научной работы — Комарова Е.Б.
В синовиальной оболочке (СО) на разных стадиях ревматоидного артрита (РА) могут преобладать экссудативные или пролиферативные процессы, сопровождающиеся деструкцией сустава. Особенности изменений СО следует учитывать при ранней диагностике РА и разработке комплексной терапии заболевания. Цель исследования изучить изменения СО при артроскопии у больных с различной длительностью РА и разным уровнем антител к циклическому цитруллинированному пептиду (АЦЦП) в крови. Материал и методы. Артроскопия была выполнена 37 пациентам с РА, использовался артроскоп (Karl Storz GmbH, Германия) диаметром 2,4 мм с углом 30°. У 17 больных продолжительность РА была артроскопии преобладает гиперемия СО с усиленным сосудистым рисунком (р 2 лет преобладает ворсинчатая гиперплазия с образованием булавовидных ворсин (р 60 Ед/мл ассоциировались с преобладанием воспалительной гиперплазии (р научных работ по клинической медицине , автор научной работы — Комарова Е.Б.
Synovial membrane changes in patients with rheumatoid arthritis revealed during arthroscopy
Изменения синовиальной оболочки у больных ревматоидным артритом при артроскопии
Lugansk State Medical University, Lugansk 1g, 50 Years of Lugansk Defense Quarter, Lugansk 91045
Контакты: Елена Борисовна Комарова; elbelcom@ua.fm
Elena Komarova; elbelcom@ua.fm
В синовиальной оболочке (СО) на разных стадиях ревматоидного артрита (РА) могут преобладать экссуда-тивные или пролиферативные процессы, сопровождающиеся деструкцией сустава. Особенности изменений СО следует учитывать при ранней диагностике РА и разработке комплексной терапии заболевания. Цель исследования — изучить изменения СО при артроскопии у больных с различной длительностью РА и разным уровнем антител к циклическому цитруллинированному пептиду (АЦЦП) в крови. Материал и методы. Артроскопия была выполнена 37 пациентам с РА, использовался артроскоп (Karl Storz GmbH, Германия) диаметром 2,4 мм с углом 30°. У 17 больных продолжительность РА была 2 лет преобладает ворсинчатая гиперплазия с образованием булавовидных ворсин (р 60 Ед/мл ассоциировались с преобладанием воспалительной гиперплазии (р 2 years. The increase in anti-CCP by >60 U/ml was associated with a predominance of inflammatory hyperplasia (p Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
0 - отсутствует Сосуды четкие, тонкие, просматриваются
1 - незначительная Сосуды четкие, тонкие, акцент яркого рисунка
2 - умеренная Сосуды четкие, яркие, ровные
и изогнутые, местами с лакунами
3 - выраженная Контуры сосудов нечеткие,
рисунок сливается, много лакун
4 - резко выраженная Контуры сосудов плохо просматриваются,
много лакун, густой красный цвет, местами цианоз Атрофические изменения СО
0 - нет Синовиальная ткань нежно-розового цвета
1 - незначительные Сосудистый рисунок незначительный,
но просматривается без пробелов
2 - умеренные Слабая васкуляризация, аваскулярные
очаги желтоватого и беловатого цвета
3 - выраженные Аваскулярные поля
4 - резко выраженные Желтая или белая аваскулярная вялая ткань
Тип гиперплазии СО
0 - нет Поверхность оболочки лишена ворсин
1 - ворсинчатая Поверхность оболочки полностью
2 - смешанная Ворсинчатая и безворсинчатая гиперплазия
в одном отделе сустава
3 - комбинированная Выросты гиперплазированной оболочки
покрыты ворсинами Паннус
1 - слабо выраженый Нежная грануляционная ткань в области
периферических отделов мениска
2 - умеренный Расширяется на мениски
и поверхность суставного хряща
3 - выраженный Поглощает мениски
4 - массивный Расширяется на плато большеберцовой кости
1 - мелкие пластины
2 - массивные сгустки
Цель исследования — изучить особенности СО коленного сустава при артроскопии у больных с различной длительностью РА и разным уровнем АЦЦП в крови.
Материал и методы
В исследование были включены 37 пациентов с РА; верификация диагноза согласно критериям Американской коллегии ревматологов/Европейской антиревматической лиги (АСR/EULAR) 2010 г. Среди обследованных преобладали женщины (84%), средний возраст составлял 41,3+11,4 года. У 17 (46%) пациентов продолжительность РА была 2 лет преобладает ворсинчатая гиперплазия СО с образованием булавовидных ворсин (рис. 3).
При АЦЦП >60 ед/мл отмечались достоверно более выраженные воспалительная гиперплазия (р 60 ед/мл (р 2 лет (п=20)
Воспалительная гиперплазия СО 2 [1; 3] 2 [1; 4] 0,85
Гиперемия и выраженный 3 [1; 4] 2 [1; 3] 0,014
сосудистый рисунок СО
Ворсинчатая гиперплазия СО 2 [1; 3] 3 [2; 3] 0,042
Атрофические изменения СО 1 [1; 2] 2 [1; 3] 0,062
Наличие паннуса 2 [1; 3] 2 [1; 4] 0,16
Наличие фибрина 1 [0; 2] 1 [0;1] 0,035
Существуют методологические и классификационные подходы к оценке состояния внутрисуставного хряща при артроскопии у больных ос-теоартритом на разных стадиях, но без оценки СО [10]. Шведскими учеными был разработан артроскопи-ческий счет изменения СО при сино-витах коленного сустава, который включал оценку гипертрофии, васку-ляризации и гиперемии в баллах (0 — изменений нет, 4 — максимальные изменения) [4], однако это не отражало полную картину воспалительно-про-лиферативных процессов в СО. В нашем исследовании были использованы критерии для оценки как воспали-тельно-экссудативных, так и проли-феративных процессов в СО при арт-роскопии у больных РА.
Ангиогенез является важным этапом патогенеза РА на ранних стадиях, обеспечивая миграцию иммуновос-палительных клеток в СО, снабжение питательными веществами и кислородом пролиферирующей ткани. Увеличенная площадь эндотелиальной поверхности также создает огромный потенциал для продукции цитокинов, молекул адгезии и факторов роста, что способствует развитию пролиферативно-деструктивных процессов в СО с формированием костно-хрящевых эрозий [11, 12]. В нашем исследовании у больных ранним РА преобладали процессы воспалительной гиперемии и васкуляриза-ции СО, а также накопление фибрина, тогда как у больных с длительным течением РА превалирует гиперплазия СО. Ряд авторов подчеркивают, что именно в начале РА в СО интенсивно протекают процессы ангиогенеза и вос-
Рис. 1. Гиперемия и выраженный сосудистый рисунок СО коленного сустава у пациента с РА длительностью 10 мес
Рис. 2. Массивные сгустки фибрина у пациента с длительностью РА >5 лет
Рис. 3. Гиперплазия СО с булавовидными ворсинами у пациента с РА длительностью 3 года
Рис. 4. Наличие паннуса в коленном суставе у высокопозитивного по АЦЦП больного РА
Таблица 3 Изменения СО суставов
в зависимости от уровня АЦЦП в крови, Ме [25-й; 75-й перцентили]
Признак 60 ед/мл р
Воспалительная гиперплазия СО 2 [1; 3] 3 [1; 4] 0,01
Гиперемия и выраженный 2 [1; 3] 3 [1; 4] 0,04
сосудистый рисунок СО
Ворсинчатая гиперплазия СО 2 [1; 3] 2 [1; 3] 0,22
Атрофические изменения СО 1 [1; 3] 2 [1; 3] 0,07
Наличие паннуса 2 [1; 3] 3 [1; 4] 0,006
Наличие фибрина 1 [0; 1] 1 [1; 2] 0,055
паления, а на более поздних стадиях превалируют проли-феративные процессы [13, 14].
В нашем исследовании при АЦЦП >60 ед/мл в СО отмечались более выраженные воспалительные процессы, ангиогенез и формирование паннуса, чем при меньших значениях этого показателя, что может быть связано с более агрессивным течением РА у данной категории больных с быстрым развитием костно-хрящевой деструкции [15]. Полученные данные подтверждают и другие авторы, наблюдавшие более тяжелое течение РА, раннее развитие деструкции в суставах и быстрое прогрессирование заболевания у высокопозитивных по АЦЦП больных [9, 16, 17].
Дальнейшее детальное исследование СО может способствовать разработке дифференцированного подхода к комплексному лечению РА в зависимости от длительности заболевания и тяжести течения. Артроскопия также может быть использована для оценки влияния терапии на процессы ангиогенеза и пролиферации СО у больных РА.
1. Dhaouadi T, Sfar I, Abelmoula L, et al. Role of immune system, apoptosis and angiogenesis in pathogenesis of rheumatoid arthritis and joint destruction, a systematic review. Tunis Med. 2007;85(12):991-8.
2. Hitchon CA, El-Gabalawy HS. The synovium in rheumatoid arthritis. Open Rheumatol J. 2011;5:107-14.
3. Лялина ВВ, Шехтер АБ. Артроскопия и морфология синови-тов. Москва: Наука; 2007. 108 с. [Ljalina VV, Shehter AB. Artroskopiya i morfologiya sinovitov [Arthroscopy and morphology of sinovitis]. Moscow: Nauka; 2007. 108 p.].
4. Klint E, Catrina AI, Matt P, et al. Evaluation of arthroscopy and macroscopic scoring. Arthr Res Ther. 2009;11:R81.
5. Carl HD, Swoboda B. Effectiveness of arthroscopic synovectomy in rheumatoid arthritis. Rheumatology. 2008;67(6):485-90.
6. Capitanescu B, Simionescu C, Margaritescu C, et al. Clinical and morphological aspects of sinovitis in early rheumatoid arthritis. Curr Health Sci J. 2011;37(1):17-20.
7. Vordenba umen S, Sewerin P, Lo gters T, et al. Inflammation and vascularisation markers of arthroscopically-guided finger joint synovial biospies reflect global disease activity in rheumatoid arthritis. Clin Exp Rheumatol. 2014 Jan-Feb;32(1):117-20.
8. Machold KP. Very recent onset rheumatoid arthritis: clinical and serological patient characteristics associated with radiographic progression over the first years of disease. Rheumatology (Oxford). 2007;46:342-9. doi: 10.1093/rheumatology/kel237
9. Algergawy SA, Abd El-Sabour M, Osman AS, et al. Early diagnostic and prognostic values of anti-cyclic citrullinated peptide antibody and cartilage oligomeric matrix protein in rheumatoid arthritis. Egypt J Immunol. 2013;20(2):11-20.
10. Лучихина ЛВ, Каратеев ДЕ. Новые подходы к ранней диагностике артроза и перспективы его патогенетической терапии. Современная ревматология. 2014;8(4):33-8 [Luchikhina LV, Karateev DE. New approaches to early diagnosis of arthrosis and prospects for its pathogenetic therapy. Sovremennaya Revmatologiya = Modern Rheumatology Journal. 2014;8(4):33-8 (In Russ.)].
1. У пациентов с длительностью РА до 2 лет преобладает гиперемия СО с усиленным сосудистым рисунком и наличием фибрина.
2. У пациентов с длительностью РА >2 лет преобладает ворсинчатая гиперплазия СО.
3. Для высокопозитивных по АЦЦП больных РА характерны воспалительная гиперплазия СО, гиперемия с выраженным сосудистым рисунком и наличие паннуса.
Исследование не имело спонсорской поддержки. Автор несет полную ответственность за предоставление окончательной версии рукописи в печать.
Декларация о финансовых и других взаимоотношениях
Окончательная версия рукописи была одобрена автором. Автор не получал гонорар за исследование.
11. Paleolog EM. The vasculature in rheumatoid arthritis: cause or consequence? Int J Exp Pathol. 2009;90(3):249-61.
12. Marrelli A, Cipriani P, Liakouli V, et al. Angiogenesis in rheumatoid arthritis: a disease specific process or a common response to chronic inflammation? Autoimmun Rev. 2011;10(10):595-8.
13. Clavel G, Bessis N, Lemeiter D, et al. Angiogenesis markers (VEGF, soluble receptor of VEGF and angiopoietin-1) in very early arthritis and their association with inflammation and joint destruction. Clin Immunol. 2007;124(2):158-64. doi: 10.1016/j.clim.2007.04.014
14. Раденска-Лоповок СГ. Ревматические заболевания. Морфологическая диагностика: Руководство для врачей. Москва: Практическая медицина; 2014. С. 13 [Radenska-Lopovok SG. Revmaticheskie zabolevaniya. Morfologicheskaya diagnostika: Rukovodstvo dlya vrachey [Rheumatic diseases. Morphological diagnostics: A guide for doctors]. Moscow: Prakticheskaya Meditsina; 2014. Р.13].
15. Van Oosterhout M, Bajema I, Levarht EW, et al. Differences in synovial tissue infiltrates between anti-cyclic citrullinated peptide-positive rheumatoid arthritis and anti-cyclic citrullinated peptide-negative rheumatoid arthritis. Arthritis Rheum. 2008 Jan;58(1):53-60. doi: 10.1002/art.23148
16. Boyesen P, Hoff M, Odegard S, et al. Antibodies to cyclic citrulli-nated protein and erythrocyte sedimentation rate predict hand bone loss in patients with rheumatoid arthritis of short duration:
a longitudinal study. Arthritis Res Ther. 2009;11(4):R103. doi: 10.1186/ar2749
17. Демидова НВ. Взаимосвязь иммуногенетических и иммунологических маркеров и их влияние на активность заболевания и рентгенологическое прогрессирование у больных ранним ревматоидным артритом. Научно-практическая ревматология. 2009;47(3):12-7 [Demidova NV. Relationship of immuno-genetic and immunologic markers and their influence on disease activity and radiological progression in patients with early rheumatoid arthritis. Nauchno-Prakticheskaya Revmatologiya = Rheumatology Science and Practice. 2009;47(3):12-7 (In Russ.)]. doi: 10.14412/1995-4484-2009-1307
Ревматоидный артрит – хроническая патология, обусловленная системным типом воспаления соединительной ткани различных органов. При заболевании иммунная система человека принимает собственные здоровые клетки за чужеродного агента и начинает им противоборствовать. Размножение аутоиммунных антител приводит к прогрессирующему разрушению околосуставных и суставных структур, фиброзным образованиям. Патологические изменения затрагивают суставы и синовиальные сумки (полости, заполненные эластичной смазкой в местах трения тканей о костные выступы).

Патогенез ревматоидного артрита
Что конкретно служит толчком к развитию ревматоидного артрита до сих пор точно не установлено. Косвенные данные указывают на несколько факторов, в научной среде именуемых ревматологической триадой:
Воздействие внутренних и внешних раздражителей. Приверженцы этой версии толчком, способным спровоцировать патологические отклонения считают:

Признаки проявления патологии
Первые симптомы ревматоидного артрита обнаруживаются неожиданно. По утрам появляется скованность движений, припухлость в местах пястно-фаланговых и лучезапястных суставов. Хорошо заметен отек в области выпирающих косточек указательного и среднего пальца руки. Поражению подвергаются мелкие суставы ног, стоп, голени, локтевые подвижные соединения. Отличительная особенность заболевания – симметричные патологические изменения органов с обеих сторон тела.
Воспалительные процессы сопровождаются болевыми ощущения. Интенсивность которых нарастает с 4 часов утра и идет на убыль во второй половине дня. К вечеру боль уходит, а ночью возвращается снова. Круговорот повторяется изо дня в день. Клиническая картина дополняется повышенной температурой (от 37º до 38º), слабостью, потерей аппетита, уменьшением массы тела. Отмечается сухость и истончение кожного покрова, ломкость ногтевых пластинок.
При отсутствии своевременного лечения ревматоидный артрит переходит в хроническую форму. Сустав деформируется, синовиальная оболочка разрастается, проникает в хрящ. Формируются ревматоидные узлы – подкожные или надкостные образования из некротической ткани. Новообразования могут самовольно исчезать и появляться вновь. Мышечные волокна теряют тонус, атрофируются.

Болевой синдром, носящий в начале заболевания непостоянный характер, усугубляется, переходит в острую форму. Страдания не оставляют больного на протяжении 24 часов. Патологический процесс захватывает новые области. Распространяется на крупные суставы, колени, плечи, позвоночные сочленения. Места воспалений на голени сопровождаются покраснением, образованием язвочек. В результате анкилозирования (сращение сочленяющих костей из-за костного, хрящевого, фиброзного образования) пораженный сустав становится тугоподвижным, либо полностью утрачивает подвижность.
Особое внимание стоит обратить на ревматоидное поражение сочленений колена. Заболевание способствует скоплению большого количества жидкости в суставной капсуле (киста Бейкера). Есть опасность разрыва кисты и распространение ее содержимого в мягкие ткани. В этом случае самолечение категорически недопустимо. Только терапевтические мероприятия, назначенные опытным специалистом, смогут приостановить активную выработку опасной жидкости. А если разрыв произошел, минимизировать нарушение жизнедеятельности организма и вернуть утраченное здоровье.
Иногда заболевание характеризуется неспецифичным течением. Отмечается боль в глазах, неприятные ощущение при глубоком вздохе.
Осложнения ревматоидного артрита
Разрушение костных и хрящевых тканей, связок приводит к нарушению обменных процессов в организме, уменьшению кровоснабжения отдельных участков тела. Прогрессирующее течение патологии чревато необратимыми последствиями. Ревматоидный артрит, кроме суставов способен вовлечь в патологическое состояние другие органы биологической системы:
Патология обуславливается рядом нарушений в периферической нервной системе. Наблюдаются некоторые изменения в психике больных: эмоциональная нестабильность, склонность к плаксивости, повышенная чувствительность, депрессии.
Спровоцировать обострение ревматоидного артрита могут: переохлаждение, физическая нагрузка, гормональный сбой, травмы, эмоциональное перенапряжение, инфекционное заболевание, неблагоприятное экологическое окружение.

Стадии протекания заболевания
Ревматоидный артрит имеет несколько форм клинических проявлений:
По уровню расстройства опорно-двигательных функций дифференцируют три стадии ревматоидного артрита:
Клинико-морфологические изменения, происходящие во второй и третьей стадии заболевания, приводят к инвалидности.
Диагностические мероприятия
Чтобы не допустить перехода заболевания в кризисную фазу, обратиться к специалисту необходимо при первых подозрениях. Оптимальный вариант для консультации – осмотр врача-артролога. Это медицинский работник хирургического профиля, занимающийся качественной диагностикой, лечением и профилактикой суставов и околосуставных тканей. Если посетить узкого специалиста нереально, следует прибегнуть к помощи ревматолога, либо терапевта.
Диагностирование ревматоидного артрита затрудняет неспецифичность его симптомов. В активной фазе выявить заболевание не составляет труда. Для исследования используют следующие методы диагностики.

Общий анализ крови. На наличие ревматоидного артрита указывает: низкий уровень гемоглобина, повышенная СОЭ (чем больше показатель, тем активнее патология). Содержание эозинофилов в лейкоцитах выше нормы.
Биохимический анализ крови. При остром течении болезни в сыворотке отмечается повышение фибриногена, сиаловых кислот, гаптоглобина, С-реактивного белка.
Анализ синовиальной жидкости. При исследовании выявляются: изменение цвета и прозрачности; снижение вязкости и гемолитической активности комплекса белков; умеренный лейкоцитоз с преобладанием нейтрофилов.
Анализ крови на наличие ревматоидного фактора. Действие неустановленного патогенного агента приводит к структурным изменениям лимфоцитов В, ответственных за формирование антител lg. Поврежденные лимфоциты распознаются организмом, как чужеродные и провоцируют выработку иммунных комплексов.
Тест на антитела к циклическому цитруллинированному пептиду (АЦЦП). Аминокислота цитруллинин синтезируется при воспалении. Белковые клетки, содержащие кислоту, иммунитет принимает за агрессора и формирует антитела.
Артроскопия. Исследование поврежденного сустава с помощью артроскопа (маленькой видеокамеры). Позволяет точно определить степень повреждений, необходимость хирургического вмешательства, взять материал для биопсии.
Рентгенограмма суставов. На ранних этапах неинформативна. По мере прогрессирования патологии выявляет истончение хрящей, сужение межсуставных щелей, остеопороз, разрушение суставов, формирование анкилоз.
Сцинтиграфия. Оценивает степень накопления радиоактивного вещества костной тканью, точно определяет вид артрита.
МРТ. Наиболее достоверная диагностика ревматоидного артрита на ранней стадии. Процедура дает возможность визуализировать разрастание костной ткани, структурные изменения хряща, утолщение синовиальной оболочки, выпот сустава в полость, субхондральные кист ы .
Ультразвуковое исследование. Метод применяется при подозрении на вовлечение в процесс внутренних органов.
Диагноз устанавливается по совокупности всех клинических и лабораторных данных, после исключения других причин воспаления.

Методики терапевтического и оперативного лечения
Основные цели лечения ревматоидного артрита: купирование острой фазы заболевания, приостановление прогрессирования структурных изменений, поддерживающая терапия.
Терапевтические мероприятия начинают с назначения противовоспалительных препаратов из группы НПВП. Предпочтение отдается быстро всасывающимся и быстро выводящимся из организма средствам. При отсутствии результата препарат последовательно заменяют.
В активной стадии течение ревматоидного артрита удается приостановить, используя комплексный лечебный курс. К нестероидным средствам добавляют:
Препараты базисной терапии . Наиболее часто применяют метотрексат, плаквенил, сульфасалазин, препараты золота, D-пенициллинамид. При их своевременном назначении удается предотвратить деструкцию суставов, уменьшить и отдалить внесуставные проявления, снизить дозу гормонов и НПВС. Соответственно уменьшается риск инвалидности, сохраняется форма и подвижность суставов.
Биологические препараты. Их назначение – уменьшить концентрацию одного из важнейших в патогенезе вещества – фактора некроза опухоли (ФНО), направление очень перспективное, позволяет добиться ремиссии даже при тяжелом течении, устойчивом к другим видам терапии. Следует только учитывать, что при применении таких лекарств возрастает риск активации неактивного (латентного) туберкулеза.
Введение лекарственных препаратов при терапии ревматоидного артрита может быть энтеральным (через желудочно-кишечный тракт), парентеральным и внутрисуставным. В полость сустава чаще всего вводят стероидные гормональные вещества короткого и продленного действия, такой метод применяется для местного лечения крупных суставов.
Для снятия нагрузки и предотвращения смещения деформированных суставов используются ортопедические средства.
Миновав острый период, к медикаментозному лечению подключают:

Учитывая состояние больного и его возможности, физиотерапевт составляет комплекс упражнений лечебной физкультуры, позволяющий сохранить и восстановить функциональные способности суставов. Предлагаем применить комплекс упражнений для коленных суставов .
Если классические препараты и процедуры не справляются, болезнь продолжает свое разрушительное действие проводится эндопротезирование. Замена сустава протезом, идентичным по форме и структуре поврежденному, выполняющему все функции. Синовэктомия – полное или частичное иссечение синовиальной оболочки.
На поздних стадиях ревматоидного артрита выполняется артродезирование. В ходе процедуры сустав обездвиживают, помогая снять боль и вернуть опороспособность.
Поддерживающая терапия во время ремиссии
Положительное действие на больных ревматоидным артритом оказывает санаторно-курортное лечение. Множество здравниц с полезными ресурсами готовы гостеприимно распахнуть свои двери. Оказать необходимую помощь для полного восстановления после перенесенной патологии. Рекомендуемые процедуры:
Предписаний, гарантирующих стопроцентное излечение или предупреждение обострений, не существует. Но некоторые меры смогут уменьшить риск перехода заболевания в активную фазу. Санаторно-курортное лечение разрешается только во время стойкой ремиссии.
Первоочередная задача – проследить, что вызывает обострение. Максимально снизить влияние провоцирующих факторов.

Избегать стрессовых ситуаций. Стабилизировать эмоциональное состояние помогут навыки аутотренинга.
Не перегружать организм тяжелой работой, требующей полной отдачи сил. Следует помнить, что хорошо работает тот, кто хорошо отдыхает.
Специалисты рекомендуют спортивную ходьбу, плавание, езду на велосипеде.
Народное лечение
Полностью заменить официальную медицину народными методами нельзя. Но продлить ремиссию, повысить сопротивляемость организма в домашних условиях возможно. Средства, используемые народом, включают в себя рецепты, опробованные веками. Вернуть утраченное здоровье помогут: травяные настои; домашние мази и компрессы; сборы для регулирования обмена веществ.
При лечении народными средствами помните:
В большинстве случаев домашнее лечение основывается на самом лучшем лекарстве – вере в излечение.
Пищевые предпочтения
Отдельное внимание уделяется характеру и качеству пищи. Рацион при ревматоидном артрите строится с учетом протекания заболевания, принимаемых лекарственных препаратов, сбоя в работе внутренних органов.
В остром периоде патология провоцирует нарушение обменных процессов. Это предпосылка к снижению калорийности и уменьшению количества белков и углеводов в пище. Животные жиры заменяются растительными. Количество жидкости, употребляемой в сутки ограничивается до 1 литра. Полностью исключаются блюда с повышенным содержанием соли, холестерина, канцерогенов, острых специй. Распространяется запрет на алкоголь, табак, газированные напитки. Рацион максимально обогащается витаминами, микро и макрокомпонентами. Приветствуется дробное питание. Термическая обработка пищевых ингредиентов проводится путем варки, тушения, парообразования.
При ликвидации острых симптомов увеличивается количество употребляемых белков, углеводов, жидкости.

Прогнозы
Патология коварна. В 75% случаях наступает потеря трудоспособности. Разные группы инвалидности люди, подверженные ревматоидному артриту, получают в течение 5 лет после дебюта заболевания. Инфекционные осложнения, кровотечение и прободение органов пищеварения, инсульт, инфаркт, почечная и печеночная недостаточность провоцируют летальный исход в 20% случаев.
При постоянном наблюдении специалиста и отсутствии рецидивов значимый прогресс наблюдается в течении 2 – 6 лет от начала болезни.
Отличия ревматоидного артрита от полиартрита
Артрит насчитывает несколько десятков разновидностей с характерными особенностями. Отличительные признаки полиартрита:
Ревматоидный артрит представляет собой системное иммуновоспалительное заболевание соединительной ткани, проявляющееся хроническим эрозивно-деструктивным полиартритом с преимущественно симметричным поражением суставов кистей и стоп и сопровождающееся у бо
Ревматоидный артрит представляет собой системное иммуновоспалительное заболевание соединительной ткани, проявляющееся хроническим эрозивно-деструктивным полиартритом с преимущественно симметричным поражением суставов кистей и стоп и сопровождающееся у большинства больных образованием особого вида аутоантител (ревматоидный фактор). Женщины болеют в 3–4 раза чаще мужчин, причем заболевание у них начинается обычно в возрасте 35–45 лет.
Болезненные, тугоподвижные суставы не только мешают выполнять самые простые повседневные движения, но и значительно нарушают ритм нормальной жизни.
Ревматоидный полиартрит — тяжелое системное заболевание, которое проявляется прогрессирующим воспалительным синовитом, симметрично поражающим периферические суставы конечностей.
В соответствии с рекомендациями Американской ревматологической ассоциации (1987) при диагностике ревматоидного артрита целесообразно придерживаться следующих критериев:
- утренняя скованность суставов или вблизи суставов длительностью не менее 1 ч до ее полного исчезновения;
- опухание мягких тканей (артрит) трех суставов или более, наблюдаемое врачом (т. е. в период осмотра или в анамнезе под наблюдением врача);
- опухание (артрит) проксимальных межфаланговых, пястно-фаланговых или запястных суставов;
- симметричное опухание (артрит) как минимум в одной паре суставов;
- ревматоидные узелки;
- наличие ревматоидного фактора;
- обнаружение при рентгенологическом исследовании эрозий и (или) периартикулярного остеопороза в суставах кистей и стоп.
При длительно текущем заболевании деформируются пораженные суставы. Помимо суставов, при ревматоидном полиартрите нарушаются околосуставные структуры (связки, сухожилия и др.), развиваются ревматоидный васкулит (поражение мелких сосудов), остеопороз, происходит поражение внутренних органов.
В пользу иммунопатологического/аутоиммунного характера воспалительного процесса при ревматоидном артрите свидетельствует обнаружение у большинства больных в сыворотке крови и синовиальном выпоте из пораженных суставов аутоантител — ревматоидного фактора.
Большое значение в развитии ревматоидного артрита имеет генетическая предрасположенность. Это подтверждается выраженной семейной агрегацией заболевания, наличием у части больных ревматоидным артритом антигенов II класса главного комплекса гистосовместимости HLA DR4 и Dw4 (с носительством которых связывают тяжелое течение артрита и быстрое прогрессирование эрозивных изменений суставов). Рассматривается роль наследственных или приобретенных нарушений Т-супрессорной регуляции иммунных реакций, недостаточной функции моноцитарно-макрофагальной системы. Пусковую роль в развитии ревматоидного артрита могут играть: хронические очаги инфекции, гормональная перестройка организма, пищевая аллергия, предшествующие травмы суставов, длительное воздействие влажного холода и физическое перенапряжение.
При хроническом воспалении у края суставного хряща в месте прикрепления к эпифизам суставной капсулы происходит разрушение и замещение паннусом участков субхондральной костной ткани с образованием эрозий. Иногда разрастающиеся грануляции проникают через субхондральную замыкательную пластинку в костную ткань. Продукты костно-хрящевой деструкции, в свою очередь, оказывают раздражающее воздействие на синовиальную оболочку, что способствует поддержанию в ней воспалительного процесса. Одновременно возникают воспалительные изменения в капсуле сустава, связках, синовиальной выстилке сухожилий и синовиальных сумках с последующим их склерозированием, приводящему к стойкому ограничению подвижности пораженных суставов, подвывихам и контрактурам. Иногда наблюдается некроз и разрыв сухожилий, синовиальных сумок. Нередко отмечается развитие вторичного остеоартроза.
Воспалительный процесс при ревматоидном артрите характеризуется неуклонным прогрессированием, темпы которого зависят от активности воспалительного процесса. Даже в периоды клинической ремиссии в синовиальной оболочке сохраняются признаки воспаления. Постепенно паннус разрушает хрящ на значительной поверхности эпифиза, а замещающая его грануляционная ткань соединяет между собой противоположные суставные поверхности и в последующем трансформируется вначале в фиброзную, а затем в костную ткань, что приводит к образованию соответственно фиброзного и костного анкилоза, обусловливающего полную неподвижность пораженных суставов.
При рентгенологическом исследовании суставов отмечается асимметричность эрозивных изменений с частым и ранним анкилозированием суставов запястий.
Течение серонегативного ревматоидного артрита менее тяжелое, в прогностическом плане более благоприятное, чем при серопозитивной форме заболевания: слабее выражены деструктивные (эрозивные) изменения и функциональные нарушения суставов, реже наблюдаются ульнарная девиация пальцев кистей, контрактуры и анкилоз (за исключением анкилоза суставов запястья). Вместе с тем серонегативный ревматоидный артрит хуже, чем серопозитивный, поддается терапии базисными и иммуносупрессивными препаратами. Чаще развивается вторичный амилоидоз.
При лечении ревматоидного артрита используются НПВП, в тяжелых случаях применяются глюкокортикостероиды, иммуносупрессоры, с целью профилактики остеопороза обычно назначают комбинацию препаратов кальция и витамина D.
Несмотря на все успехи фармакологии, ревматоидный артрит до настоящего времени остается тяжелым заболеванием с неблагоприятным прогнозом.
Приведем пример из личного опыта ведения больной с ревматоидным артритом, представляющим, по мнению автора, научный интерес.
Больная В., возраст — 71 год, обратилась к неврологу в августе 2006 г. с жалобами на боли в суставах кистей, коленных суставах, в пояснице. Боль в суставах беспокоила днем и ночью, обычно была выраженной, нередко мигрирующей, обусловливала ограничение всех активных и пассивных движений в пораженных суставах. Артралгия зачастую сочеталась с выраженной миалгией, оссалгией, болями в сухожилиях. Из анамнеза: проявления полиостеоартроза в течение 15 лет, дебют суставного синдрома воспалительного характера в июне 2002 г. (отек и воспаление в области суставов, фебрильная лихорадка, подтвержденная лабораторно активность воспалительного процесса). Амбулаторно (сначала периодически, в последние 3 года постоянно) получала НПВП (ибупрофен, индометацин, диклофенак, ацеклофенак). С 2004 г. регулярно принимала кальций D3 (1 г кальция в сутки).
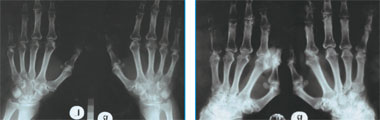 |
| Рис. 1. Рентгенограмма кистей больной В. 2003 г.: проявления полиостеоартроза, явных эрозий нет. Рис. 2. Рентгенограмма кистей больной В. 2006 г.: множественные кисты и эрозии, отрицательная динамика с 2003 г. |
Стационарно проходила лечение в городском ревматологическом центре г. Санкт-Петербурга (апрель 2003 г., июнь–июль 2006 г.) с диагнозом: ревматоидный артрит, серопозитивный, с системными проявлениями (субфебрилитет, амиотрофия, миалгии), активность 2-й степени, функциональная недостаточность суставов 1–2-й степени. Сопутствующая патология: ишемическая болезнь сердца, стенокардия II ФК. Гипертоническая болезнь 3-й степени, ОНМК (декабрь 2002 г.). Хронический бронхит вне обострения. Диффузный зоб второй стадии. Эутиреоз. Полиостеоартроз. Желчно-каменная болезнь.
С 2003 г. постоянно получает метотрексат в дозировке 2,5 мг 2 раза в неделю. Несмотря на проводимое лечение, суставной болевой синдром нарастал, учащались обострения, ухудшалось состояние костей (остеопороз, эрозии). Показательна рентгенография кистей (рис. 1–2).
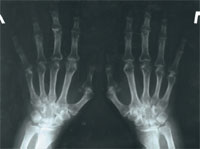 |
| Рис. 3. Рентгенограмма кистей больной В. 2007 г.: проявления полиостеоартроза, положительная динамика с 2006 г. |
С августа 2006 г. на фоне лечения метотрексатом неврологом был дополнительно назначен Структум в дозировке 500 мг 2 раза в день. Больная ориентирована врачом на длительный, до полугода, прием препарата. Некоторое уменьшение интенсивности (непрекращающегося в течение 2 последних месяцев) болевого синдрома наступило через 3 нед. Эпизоды обострений ревматоидного артрита были в течение 4 мес. К концу 5-го месяца комбинированной терапии (метотрексат + Структум) болевой синдром значительно снизился, уменьшилась утренняя скованность, спала отечность лучезапястных и коленных суставов.
В феврале 2007 г. была сделана рентгенография кистей (рис. 3). Результат сравнения с предыдущими рентгенографиями оказался более чем положительным (уменьшились эрозии костей). Прием структума продлен на 3 мес. По состоянию на май 2007 г. обострений суставного синдрома не наблюдалось в течение 4 мес, сохранялась небольшая отечность на лучезапястных (больше слева) и коленных суставах. С целью коррекции противоревматической терапии (снижение дозы метотрексата) больной рекомендована консультация в городском ревмоцентре.
И. Н. Бабурин
СПбНИПНИ им. В. М. Бехтерева, Санкт-Петербург
Читайте также:


