Инфантильная артериальная кальцификация сердца плода
Первое описание пренатальной диагностики инфантильной артериальной кальцификации в 1990 г. принадлежит R. Spear и соавт. В опубликованном ими наблюдении была обнаружена не только кальцификация аорты, но и самого сердца. В последующие годы было опубликовано еще несколько случаев пренатальной ультразвуковой диагностики ИАК, но во всех наблюдениях диагноз был установлен только во второй половине беременности.
В опубликованном нами наблюдении ИАК была заподозрена уже в 13 нед. При оценке сердца плода была обнаружена гиперэхогенная во всех отделах межжелудочковая перегородка. Ее эхогенность была настолько высокой, что она была сравнима с эхогенностью костей плода. При этом размеры желудочков и предсердий были практически одинаковыми, так же как и диаметры главных артерии. Нарушений кровотока через атриовентрикулярные клапаны и клапаны главных артерий не было зарегистрировано не было. Сочетанных пороков не обнаружено. Полученные данные не укладывались ни в одну из описанных нозологических форм, диагностированных в ранние сроки беременности.
Наиболее вероятный предположительный диагноз, высказанный консультативно, сводился к ИАК, но она обычно сопровождается изменением аорты, а в представленных цифровых материалах аорта была не изменена. На основании полученных данных и их обсуждения было решено провести контрольное обследование в динамике. В 16 нед беременности отмечено выраженное превалирование диаметра легочной артерии над аортой, что свидетельствовало о формировании ее гипоплазии. В 20 нед беременности на фоне сохраняющейся гиперэхогенной межжелудочковои перегородки зарегистрировано выраженное повышение эхогенности стенок аорты, диаметр которой был даже меньше диаметра верхней полой вены. Соответственно было обнаружено превалирование размеров правого желудочка над левым. Таким образом, в 20 нед беременности были зарегистрированы характерные изменения аорты, что дало основание установить диагноз ИАК.
Учитывая неблагоприятый прогноз, беременность прервана в 23 нед по медицинским показаниям. При микроскопическом исследовании было обнаружено, что эндокард в области перегородки и левых отделов сердца резко утолщен (в 10-15 раз) за счет разрастания эластических волокон и в меньшей степени коллагеновых, располагающихся параллельными слоями. Внутренняя оболочка аорты утолщена за счет разрастания эластических волокон и очагов петрификации.
Аномалия Уля - редкая врожденная патология, проявляющаяся выраженной гипоплазией или почти полным отсутствием миокарда одного из желудочков сердца. В основном при данной аномалии поражается миокард правого желудочка. Чаще всего гипоплазия бывает диффузной, хотя возможна очаговая форма. Трикуспидальный клапан может быть нормальным или дисплазированным. В некоторых случаях отмечаетя стеноз или атрезия легочного клапана. Аномалия Уля обычно диагностируется на секции и составляет 0,1% от числа всех ВПС.
В ходе пренатального ультразвукового исследования, в первую очередь обращает на себя внимание выраженная кардиомегалия за счет дилатации пораженного желудочка. Миокард желудочка едва различим, а сократительная способность минимальна. Нередко поэтому при аномалии Уля регистрируются признаки застойной сердечной недостаточности (перикардиальный, плевральный выпоты, асцит).
Впервые о пренатальной ультразвуковой диагностике аномалии Уля в 24 нед беременности сообщили G. Wager и соавт. Е.П. Затикян и соавт. удалось диагностировать этот порок сердца пренатально в 23-24 нед беременности. В представленном ими наблюдении при ультразвуковом исследовании плода наряду с выраженной дилатацией полости левого желудочка отмечалось выраженное истончение миокарда его задней стенки (1 мм). При этом также констатировано практически полное отсутствие сокращения миокарда левого желудочка в различные фазы сердечного цикла. В плевральной полости определялось небольшое количество свободной жидкости. Отмечена также умеренно выраженная брадикардия - 110 уд/мин. Показатель ударного объема сердца оказался сниженным и составил 70% от средних нормативных величин.
С. Benson и соавт. сообщают о случае, в котором аномалия Уля, обнаруженная в 18-19 нед беременности, была расценена как аномалия Эбштейна и только при патологоанатомическом исследовании был установлен правильный диагноз. Авторы указывают на существенные трудности, возникающие при дифференциальной диагностике аномалии Уля с аномалией Эбштейна в начале II триместра беременности, так как оба этих порока сопровождаются выраженной кардиомегалией за счет правых отделов сердца. По мнению R. Oberhoffer и соавт., ключом к правильной пренатальной диагностике аномалии Уля является визуализация нормального (несмещенного) трикуспидального клапана на фоне дилатированного правого предсердия и истонченного миокарда правого желудочка.
Предметы
Аннотация
Мы сообщаем об очень редком случае изолированной множественной кальцификации легочной артерии с тяжелым двусторонним стенозом периферической легочной артерии, диагностированным внутриутробно . Несмотря на лечение бисфосфонатом в течение 6 месяцев, систолическое давление в правом желудочке постоянно повышалось и превышало давление в левом желудочке. После успешной двусторонней легочной артериопластики в возрасте 13 месяцев у пациента наблюдалось снижение систолического давления в правом желудочке с нормальной конфигурацией межжелудочковой перегородки. Это первый отчет о случаях кальцификации изолированной легочной артерии без кальцификации других артерий, подтвержденной неконтрастной компьютерной томографией живого пациента.
Вступление
Кальцификация легочной артерии (ПА) является необычной у детей, встречается только в сочетании с тяжелым заболеванием, лежащим в основе клапанов, или в связи с синдромом переливания от двух к двум (TTTS), перфузией артериального тона с двойной артериальной гипертензией (TRAP), 1 или идиопатической артериальной кальцификацией младенчества. Мы сообщаем об очень редком случае изолированной множественной кальцификации легочной артерии с тяжелым двусторонним стенозом периферической легочной артерии, диагностированным внутриутробно.
случай
Младенца мужского пола перевели в детскую больницу Сеульского национального университета через 5 дней после рождения из-за кальцификации основного ПА, выявленной при эхокардиографии плода.
Его родители не были родственниками. Его матери было старше 35 лет, но, за исключением возраста, риска для плода не было, и она регулярно наблюдалась. Ей была выполнена эхокардиограмма плода в гестационном возрасте 27 + 3 недели из-за полигидрамниоза и стеноза ПА в акушерской сонографии. Эхокардиография плода продемонстрировала яркую эхогенную стенку основного ПА и слегка увеличенный поток бифуркации ПА (около 1, 0 м с -1 ). За исключением аномальных сердечных обнаружений при акушерском сонографическом обследовании, не было никаких ненормальных лабораторных данных. Он не показал задержки внутриутробного развития.
Он был доставлен в гестационном возрасте 38 + 4 недели через кесарево сечение без каких-либо перинатальных проблем. 1- и 5-минутный балл по шкале Апгар составил 8 и 9 баллов, а его вес при рождении составил 2, 89 кг (от 10 до 50 процентилей). При физикальном осмотре у пациентки выявлен систолический шум II степени на левой верхней части грудины. Жизненные показатели были стабильными. Компьютерная томография (КТ) сердца выявила тяжелый двусторонний периферический легочный стеноз. Диаметр проксимального правого PA (RPA) составлял 3, 9 мм, а диаметр грудной части RPA составлял 1, 4-2, 0 мм. Диаметр проксимального левого PA (LPA) составлял 3, 5 мм, а диаметр грудной части LPA составлял 2, 0-2, 2 мм. Неконтрастная КТ сердца показала кальцификацию в боковых стенках обоих ПА, от основного ПА до правого и левого отделов хилар (рис. 1), хотя количество кальцификации в ПА, наблюдаемое на КТ, было не очень впечатляющим. Мы проверили серию изображений, чтобы обнаружить кальцификацию других артерий. Инфантография, сонография головного мозга и живота, а также неконтрастное КТ изображение от шеи до обеих ног не выявили другой тени кальцификации, кроме поражений в ПА. Эхокардиография выявила умеренный градиент давления между правым желудочком (RV) и PA-ответвлениями, градиент пиковых давлений на RPA и LPA составил 36 мм рт. Лабораторные данные, включая уровни общего сывороточного и ионизированного кальция, фосфата, щелочной фосфатазы, мочевины в крови, креатинина, 25 (OH) витамина D и 1, 25 (OH) 2 витамина D, были в пределах нормы, за исключением уровня гормона околощитовидной железы что составило менее 5 пг мл -1 (нормальный диапазон: от 10 до 65 пг мл -1 ). Результат теста флуоресцентной гибридизации in situ (FISH) для синдрома Уильямса был отрицательным. Поскольку у пациента не было никаких симптомов и значительных проблем с гемодинамикой, изначально мы наблюдали за пациентом без лечения.

Начальная неконтрастная компьютерная томография (КТ). Неконтрастная КТ грудной клетки показала кальцификацию сосудистой стенки (кружки) от основной легочной артерии (ПА) ( а ) до правой и левой частей голени ПА. ( b, левый PA; c, правый PA).
Изображение в полном размере
Последующая эхокардиограмма, полученная в возрасте 5 месяцев, показала, что градиент давления на грудном LPA увеличился до 81 мм ртутного столба, а внутриглазный RPA составил 59, 9 мм ртутного столба. Однако у пациента не было респираторных или сердечно-сосудистых симптомов, и его жизненные показатели были стабильными.
Изучив литературу по успешному лечению бисфосфонатом для генерализованной кальцификации артерий у детей раннего возраста (GACI), 2 мы решили назначить бисфосфонат вместо проведения срочной легочной артериопластики. Когда пациенту было 6 месяцев, мы назначали памидронат динатрия в дозе 0, 25 мг / кг в день в течение 3 последовательных дней каждые 6 недель (половина дозы назначалась при остеопорозе). После 24 недель (4 цикла) лечения мы пересмотрели лабораторные показатели. КТ сердца показала, что диаметры правой верхней ПА, правой нижней ПА и верхней части LPA составляли 2, 1 и 2 мм соответственно; это подразумевало, что не произошло никаких изменений в диаметрах хиларных частей любого из PA (Рисунки 2a и b). Последующая эхокардиограмма показала, что предполагаемое систолическое давление RV было приблизительно 120 мм рт.ст., которое было больше, чем систолическое давление левого желудочка (LV) (систолическое артериальное давление было 93 мм рт.ст.), и LV казалось сжатым (рис. 2c).

Компьютерная томография (КТ) и эхокардиограмма после четырех циклов лечения бисфосфонатом. КТ сердца левой легочной артерии (PA) ( a ) и правой PA ( b ) выявили стеноз икроножных участков (круги) и постстенотическую дилатацию (стрелки). Эхокардиограмма показала расширенный и гипертрофированный правый желудочек (RV) и сдавленный левый желудочек (LV) ( c, стрелка).
Изображение в полном размере
Поэтому мы выполнили двустороннюю легочную артериопластику от ворот до ворот с помощью искусственного пластыря трансплантата в возрасте 13 месяцев (рис. 3а); эта процедура была выполнена без осложнений. После операции отношение RV к аорте составило всего 0, 4. Послеоперационная КТ сердца выявила облегчение стеноза в LPA и правой нижней части PA (Рисунки 3c и d). Эхокардиограмма, выполненная через 6 месяцев после операции, показала снижение давления RV с нормализованной конфигурацией перегородки без значительного градиента давления на периферическом ПА (Рисунок 3b).

Схематическое изображение двусторонней легочной артериопластики и послеоперационной эхокардиограммы и компьютерной томографии сердца (КТ). Схематическое изображение двусторонней патологии артериопластики легочной артерии ( а ). Послеоперационная КТ сердца выявила облегчение стеноза (круги) в левой легочной артерии (ПА) ( в ) и в правой ПА ( г ). Межжелудочковая перегородочная конфигурация ( б, белая стрелка) нормализовалась после операции.
Изображение в полном размере
Через 13 месяцев после операции у пациента не было респираторных или сердечно-сосудистых симптомов. Его рост был приемлемым (масса тела, от 10 до 25 процентилей в возрасте 26 месяцев), и он достиг нормальных этапов развития.
обсуждение
ПА кальцификация необычна у детей. В некоторых исследованиях сообщалось о кальцификации PA, связанной с TRAP, 1 TTTS, 3, 4, 5 GACI 6, 7, 8, 9, 10, 11, 12 и внутриутробной гиперкальциемией (возможный случай синдрома Вильямса). 13 Насколько нам известно, ни одно исследование не сообщало об изолированной кальцификации ПА, доказанной на сегодняшний день неконтрастной КТ у живого пациента.
Кальцификация сосудов у новорожденных может возникнуть в результате дистрофических, метастатических или идиопатических процессов. 3 Оскорбление или повреждение плода может привести к некрозу, кровоизлиянию или фиброзу, предшествующему дистрофической кальцификации. 1 Артериальная кальцификация, вызванная атеросклерозом или внутрисосудистым устройством у взрослых, является примером дистрофической кальцификации. Метастатическая артериальная кальцификация может быть результатом почечной недостаточности, гипервитаминоза D или гиперпаратиреоза. 14 Третья категория — идиопатическая артериальная кальцификация у младенцев, также известная как GACI или идиопатическая инфантильная артериальная кальцификация, которая является аутосомно-рецессивным заболеванием, связанным с геном ENPP1 . 10, 12 Это клинически смертельно вследствие обширной кальцификации артерий. 10, 12 GACI встречается крайне редко; по состоянию на 2009 год в мировой литературе было зарегистрировано около 170 случаев. 2 Однако есть некоторые случаи, такие как кальцификация артерий вследствие ТТТС, которые не попадают ни в одну из этих трех категорий. 3
Настоящее дело не вписывается ни в одну из вышеупомянутых трех категорий. Пациент не имел признаков инсульта или травмы плода, а также статуса заболевания, вызывающего метастатическую кальцификацию артерий. Кроме того, у пациента были кальцификации только в легочных артериях, и у него не было семейной истории артериальной кальцификации.
Мы не проводили биопсию периферической артерии. Идиопатическая инфантильная артериальная кальцификация обычно включает артерии среднего или большого размера. 12 Биопсия средних или крупных артерий не является общепринятой в данной ситуации, кроме как во время операции или после смерти. 10, 12 Поэтому мы сделали КТ всего тела, кроме мозга, чтобы подтвердить кальцификацию других артерий. И КТ изображение показало, что не было кальцификации в закрытой области, кроме поражения в PA.
Это первый отчет о случаях кальцификации изолированного ПА без кальцификации других артерий, подтвержденной неконтрастной КТ живого пациента. Данный случай может быть уникальным типом кальцификации артерий или одним из редких и легких типов идиопатической инфантильной артериальной кальцификации.
В этом случае, в отличие от клинического испытания бисфосфоната при GACI, 2 инфузия бисфосфоната была недостаточной. Мы могли использовать бисфосфонат только в течение короткого времени, потому что гипертония RV усугубилась. Мы не могли оценить эффект от более длительного использования этого лечения. Во-вторых, поскольку нет единого мнения относительно дозы лечения бисфосфонатом для кальцификации PA или для GACI, 2, 10 мы использовали динатрий памидронат в половине дозы, используемой для остеопороза (0, 25 мг / кг в день в течение 3 дней каждые 6 недель), Это может быть меньше, чем эффективная доза.
Было очень трудно определить сроки хирургического лечения, потому что у пациента не было определенных сердечных симптомов или признаков. Мы приняли решение об обратной реконструкции стены RV после успешного снижения нагрузки под давлением. RV гипертония резко улучшилась после двусторонней легочной артериопластики с пластырем трансплантата, включая разрез и резекцию самой стенозированной области. Если бы мы выполнили легочную артериопластику сразу после рождения или в раннем детстве, у нас могло бы не быть достаточного снижения давления RV.
Мы сделали биопсию при стенозе легочной артериальной стенки в основном ПА во время операции, после исследования бифосфоната. Патологическая находка выявила стенку сосудов с микоидной дегенерацией (клинически стеноз ПА). Этот результат может быть эффект бисфосфоната. Поскольку рентгенологических данных о кальцификации было достаточно для постановки диагноза, мы не проводили дополнительную биопсию.
Тщательный мониторинг сердечных симптомов и признаков и частая визуализация сердца для обнаружения изменений гемодинамики были очень полезны в нашем решении о проведении хирургической коррекции. Мы проведем обследование пациента на предмет повторного стеноза на месте операции.
В заключение мы сообщаем о первом случае изолированной множественной кальцификации PA с тяжелым двусторонним периферическим легочным стенозом, диагностированным внутриутробно ; это состояние было успешно вылечено хирургической легочной артериопластикой без значительной заболеваемости.
| Обобщенная артериальной кальцификации младенчестве | |
|---|---|
| Синонимы | Идиопатическая инфантильная артериальная кальцификация (ИИАЦ), артериальная кальциноз младенчества, идиопатический кальциноз артерий младенчества (IACI), окклюзионная инфантильная артериальная кальцификация, окклюзионная инфантильная артериопатия |
| Специальность | медицинская генетика |
Обобщенная артериальная кальцификация младенчества ( GACI ) является крайне редко, как правило , со смертельным исходом генетического нарушения, вызванные мутациями в ENPP1 гене у 75% испытуемых. Состояние поражает младенцев в течение первых 6 месяцев жизни. Это состояние наследуется как аутосомно - рецессивный рисунком. Она характеризуется обобщенной кальцификацией артериальной внутренней упругой пластинки, что приводит к разрыву пластинки и окклюзионных изменений в белочном интиме с стенозом и снижением эластичности стенки сосуда. Большинство дети умирают от сосудисто-окклюзионных заболеваний, особенно из коронарных артерий .
содержание
- 1 Признаки и симптомы
- 2 Причина
- 3 Диагностика
- 4 Профилактика
- 5 Лечение
- 6 Прогноз
- 7 Смотрите также
- 8 Ссылки
- 9 Внешние ссылки
Признаки и симптомы
Клиническая картина варьирует. Первые симптомы обычно возникают при рождении , но могут иметь место в течение первых 6 месяцев жизни или в утробе матери .
- Снижение активности плода
- Беременности с дородовой диагностики водянки плода ,
- многоводие
- Низкий биофизический профиль
- Заметное цианоз
- водянка
- Тяжелая гипертензия
- Нет или замирание импульсов
- Отказ от корма
- Тахипноэ
- рвота
- вздутие живота
- Общая артериальная жесткость
- Сердечная недостаточность (наиболее частая клиническая находка)
- Штамм модель
причина

Результаты болезни от инактивирующей мутации в экто-нуклеотиде пирофосфатаз / фосфодиэстераза-1 ENPP1 гене, что приводит к снижению неорганического пирофосфата (PPI), мощный ингибитор осаждения кальция в стенке сосуда. Эта мутация позволяет нерегулируемое отложение кальция в мышечных артериях. Эти симптомы вызваны кальцификации крупных и средних артерий, в том числе аорты, коронарных артерий и почечных артерий. Большинство больных умирают от 6 месяцев из - за сердечной недостаточности. В последнее время , гомозиготные или сложные гетерозиготные мутации гена для ENPP1 были представлены как причинных для расстройства. ENPP1 регулирует внеклеточный неорганический пирофосфат (PPI), главный inhibiter внеклеточной матрицы кальцификации.
диагностика
Обобщенные инфантильный артериальной кальцификации всегда следует учитывать у младенцев и детей , представляющих с гипертонией, сердечной недостаточности или внезапной смерти. Обычная рентгенография , сонография и МРТ может помочь в диагностике. Постнатальный серой шкалы и цвета Доплера эхокардиографии и эхографические обследования позволили неинвазивной диагностики, оценка степени тяжести, а также мониторинга прогрессирования. Контрастное МР - ангиография с задержкой дыхания и сердечной стробирования техники может провести оценку степени заболевания.
- Dilated и гипертрофированные желудочки
- Экстрамедуллярные кроветворения печени
- Гипертрофия миокарда
- Яркий и гипер-отражательный миокарда
- Околосуставных обызвествления в запястьях, уши, плечи, лодыжки и бедра
- Сердце обычно выглядит структурно нормальным
- Кардиомегалия и легочное полнокровие
- Диффузный артериальной кальцификации с участием аорты, сонных, церебральный, почек, мезентериальных и сердечных артерий
- Эхо-плотные кольца аорты , восходящая аорта , поперечная арка, нисходящая аорта, главная легочная артерия и коронарные артерии необычно.
- УЗИ брюшной полости может выявить гепатомегалия , асцит , почечную эхогенность и рассеянным артериальной кальцификации , связанные с аортой , общей подвздошной , селезеночной и почечных артерий , а также перитонеального кальцификации , связанные с висцеральной брюшины , покрывающий печень и кишечник
- Мозг УЗИ может показать расширенные боковые желудочки, слаборазвитый мозолистое тело и лейкомаляцию
- Эхокардиография может выявить структурно нормальное сердце, нормальную функцию желудочков, однако мягкий концентрической гипертрофии желудочков и несколько внутрисердечной , а также сосудистые кальцификации
- Идиопатические артериальные кальцификации младенчества следует заподозрить при наличии гиперэхогенности стенок сосудов, что свидетельствует о многоводии или прошлой историей ранней неонатальной смертности.
- ДНК-тестирование может идентифицировать одну из мутаций, ответственных за состояние
Рубрика МКБ-10: Q28.8
Содержание
- 1 Определение и общие сведения
- 2 Этиология и патогенез
- 3 Клинические проявления
- 4 Другие уточненные врожденные аномалии системы кровообращения: Диагностика
- 5 Дифференциальный диагноз
- 6 Другие уточненные врожденные аномалии системы кровообращения: Лечение
- 7 Профилактика
- 8 Прочее
- 9 Источники (ссылки)
- 10 Дополнительная литература (рекомендуемая)
- 11 Действующие вещества
PHACE синдром
Синонимы: синдром Паскуаля-Кастровехо тип 2, синдром PHACES
PHACE синдром - это аббревиатура, используется для описания синдрома, характеризующегося сочетанием пороков развития задней черепной ямки мозга (Posterior), большой лицевой гемангиомы (Haemangioma), анатомических аномалий мозговых артерий (Arteries), коарктации аорты и других кардиальных дефектов (Cardiac), а также аномалий формирования органа зрения (Eye). Иногда также присутствуют аномалии грудины (Sternum) - в этих случаях синдром называют PHACES синдром. Недавно были добавлены два дополнительных признака к клинической картине синдрома PHACE: стеноз сосудов основания черепа и участки продольного растяжения внутренней сонной артерии.
Синдром PHACE является редким, менее чем о 100 случаях заболевания было сообщено в литературе до сих пор, патология гораздо чаще встречается у женщин, чем у мужчин (8:1).
Наследование Х-сцепленное, доминантное
Этиология синдрома неизвестна.
PHACE синдром обнаруживается у новорожденных и младенцев. Полный спектр клинической картины синдрома PHACE встречается крайне редко. Пороки развития задней черепной ямки включают гипоплазию мозжечка, арахноидные кисты, корковую дисгенезиию и пороки развития Денди-Уокера. Капиллярные гемангиомы имеют те же морфологические, клинические и эволюционные характеристики, что и спорадические доброкачественные гемангиомы. Внутричерепные и субарахноидальное повреждения могут происходить одновременно с внутричерепными поражениями, развивающимися таким же образом, как и челюстно-лицевые или цервикальные гемангиомы. Два типа артериальных аномалий были описаны для синдрома PHACE: сохранение эмбриональных артерий и недоразвитие сонной или позвоночной артерии. Эти анатомические изменения позволяют сохранять нормальную мозговую функцию, но ограничивают возможности для коллатерального кровообращения в случае дополнительной окклюлизии или стеноза. Офтальмологические аномалии включают глаукому, колобому, микрофтальм, криптофталмию и гипоплазию зрительного нерва. В большинстве случаев сосудистые поражения являются уни- и гомолатеральными, что свидетельствует о том, что синдром PHACE относится к группе цереброфациальных синдромов с вовлечением нескольких смежных сегментов нервного гребня. Аномалии грудины, возникающие в результате дефекта развития внутренних органов, являются редкими и включают образование расщелины грудины и/или пороки развития надпупочного шва. Прогрессирующий стеноз внутримозговых артерий (как правило, односторонний) локализуется в передних или задних отделах внутренней сонной артерии. Они являются результатом концентрической пролиферации сосудистой стенки, которая вызывает постепенное уменьшение просвета сосуда. Утолщение сосудистой стенки также отвечает за развитие удлинения внутренних сегментов сонной артерии. Неврологическая симптоматика разнообразна, в зависимости от размера и локализации окклюзированного сосуда. Другие проявления патологии, такие как головные боли или задержка психомоторного развития - также могут быть следствием ишемии.
Диагноз может быть подтвержден с помощью КТ, МРТ и сердечно-легочных исследований, реже выполняется ангиография. Ранняя диагностика и своевременное лечение уменьшает уменьшает тяжесть развития осложнений.
В зависимости от объема и локализации очагов поражения используют медикаментозное или хирургическое лечение капиллярных гемангиом. Аспирин часто рекомендуется для предотвращения ишемии и для улучшения церебральной реваскуляризации. Хирургическое вмешательство, часто используемое у пациентов с болезнью Мойя-Мойя, может также предложены для лечения синдрома PHACE.
Прогноз зависит от тяжести церебральных и артериальных дефектов.
Генерализованная артериальная кальцификация у младенцев
Синонимы: идиопатическая инфантильная артериальная кальцификация, идиопатическая облитерирующая артериопатия, инфантильный артериосклероз, окклюзионная инфантильная артериопатия
Определение и общие сведения
Идиопатическая артериальная кальцификация у младенцев - редкое состояние, характеризующееся обширной кальцификацией и стенозом крупных и средних артерий.
Описано больше 100 случаев заболевания, большинство в европейской популяции. Генерализованная артериальная кальцификация чаще всего встречается у младенцев в возрасте менее шести месяцев. Предполагается аутосомно-рецессивное наследование.
Этиология и патогенез
Этиология до конца не понятна. Есть свидетельства наличия семейных кластеров. Недавно были обнаружены мутации, которые инактивировали эктонуклеотидную пирофосфатазу/фосфодиэстеразу 1.
Клинические проявления
Выраженная системная гипертензия, кардиомиопатия и застойная сердечная недостаточность являются частыми осложнениями инфантильного артериосклероза. Сопутствующие аномалии встречаются редко и включают в себя неспецифические пороки сердца, гидронефроз, поликистоз почек, трисомию 17 и 18. Патологически состояние характеризуется осаждением кальция вдоль внутренней эластичной мембраны артерий, сопровождающееся фиброзным утолщением интимы, которое вызывает сужение просвета сосуда. Поражение артерий распространено повсеместно, но сужение просвета артерий неизменно приводит к окклюзии коронарной артерии и ишемии миокарда.
Диагностика
Клинический диагноз инфантильного артериосклероза основан на рентгенологических исследованиях, в том числе ангиографии или КТ сканировании артерий головы, шеи и конечностей.
Сообщалось о возможности пренатальной диагностики с обнаружением артериальных кальцификаций, водянки, аномальной сократительной способности сердца и гиперэхогенности почек.
Дифференциальный диагноз
Дифференциальный диагноз инфантильного артериосклероза включает эндокардиальный фиброэластоз, миокардит, болезни накопления, инфаркт, аномальное отхождение коронарных артерий, сердечные аномалии, метастатическую кальцификацию в результате почечной недостаточности, гипервитаминоз D и инфекции. Генерализованную артериальную кальцификацию у младенцев следует также учитывать в дифференциальном диагнозе неиммунной водянки плода.
Специфического лечения инфантильного артериосклероза нет.
Прогноз неблагоприятный. Большинство младенцев умирают от инфаркта миокарда в течение первого года жизни, причем наибольшее количество смертей происходит в течение первых шести месяцев жизни.

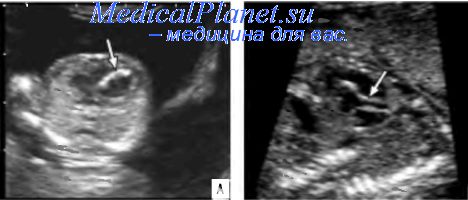
Рис. 15.75. ИАК. А - поперечное сечение. Б - продольное сечение. Отчетливо видно выраженное повышение эхогенности стенок аорты (стрелка).
Первое описание пренатальной диагностики ИАК в 1990 г. принадлежит R. Spear и соавт. [1]. В опубликованном ими наблюдении была обнаружена не только кальцификация аорты, но и самого сердца. В последующие годы было опубликовано еще несколько случаев пренатальной ультразвуковой диагностики ИАК 5, но во всех наблюдениях диагноз был установлен только во второй половине беременности (рис. 15.75).
В опубликованном нами наблюдении ИАК была заподозрена уже в 13 нед [7]. При оценке сердца плода была обнаружена гиперэхогенная во всех отделах межжелудочковая перегородка (рис. 15.76). Ее эхогенность была настолько высокой, что она была сравнима с эхогенностью костей плода. При этом размеры желудочков и предсердий были практически оди-

Рис. 15.76. ИАК. А - четырехкамерный срез сердца плода в 13 нед. Отмечается повышение эхогенности межжелудочковой перегородки (стрелка). Б - срез через аорту в 20 нед. Отчетливо видно повышение эхогенности стенок гипоплазиро- ванной аорты (стрелка). В - срез через три сосуда в 20 нед. 1 - легочная артерия; 2 - аорта; 3 - верхняя полая вена.

наковыми, так же как и диаметры главных артерий. Нарушений кровотока через атриовентрикулярные клапаны и клапаны главных артерий не было зарегистрировано не было. Сочетанных пороков не обнаружено. Полученные данные не укладывались ни в одну из описанных нозологических форм, диагностированных в ранние сроки беременности [8].
Наиболее вероятный предположительный диагноз, высказанный консультативно, сводился к ИАК, но она обычно сопровождается изменением аорты, а в представленных цифровых материалах аорта была не изменена. На основании полученных данных и их обсуждения было решено провести контрольное обследование в динамике. В 16 нед беременности отмечено выраженное превалирование диаметра легочной артерии над аортой, что свидетельствовало о формировании ее гипоплазии. В 20 нед беременности на фоне сохраняющейся гиперэхогенной межжелудочковой перегородки зарегистрировано выраженное повышение эхогенности стенок аорты, диаметр которой был даже меньше диаметра верхней полой вены. Соответственно было обнаружено превалирование размеров правого желудочка над левым. Таким образом, в 20 нед беременности были зарегистрированы характерные изменения аорты, что дало основание установить диагноз ИАК.
Учитывая неблагоприятый прогноз, беременность прервана в 23 нед по медицинским показаниям. При микроскопическом исследовании было обнаружено, что эндокард в области перегородки и левых отделов сердца резко утолщен (в 10-15 раз) за счет разрастания эластических волокон и в меньшей степени коллагеновых, располагающихся параллельными слоями. Внутренняя оболочка аорты утолщена за счет разрастания эластических волокон и очагов петрификации.
1. Spear R., Mack LA., BenedettiT.J. etal. Idiopathic infantile arterial calcification: In utero diagnosis// J. Ultrasound Med. 1990. V. 9.
2. Crum A.K., Lenington W., Jeanty Ph. Aortic calcinosis // TheFetus.net
3. Hajdu J., Marton Т., Papp С. etal. Calcification of the fetal heart- 6.
four case reports and a literature review// Prenat. Diagn. 1998. 7.
V. 18. № 11. P. 1186-1190.
4. Haug K., Kohlschmidt N., Dereser-Dennl M. etal. Familial fatal 8.
fetal cardiomyopathy with isolated myocardial calcifications:
a new syndrome? // Am. J. Med. Genet. 2001 . V. 101. № 3. P.255-258.
Eronen М., Pohjavuori М., Heikkila P. Fatal outcome of two siblings with idiopathic arterial calcification of infancy diagnosed in utero// Pediatr. Cardiol. 2001. V. 22. N° 2. P. 167-169.
Читайте также:


