Хламидийный артрит у ребенка
Одной из актуальных проблем современной педиатрии является диагностика и лечение воспалительных заболеваний суставов. Наиболее распространен среди ревматических заболеваний детского возраста реактивный артрит (РеА), который встречается
Одной из актуальных проблем современной педиатрии является диагностика и лечение воспалительных заболеваний суставов. Наиболее распространен среди ревматических заболеваний детского возраста реактивный артрит (РеА), который встречается у 86,9 на 100 000 детского населения [1].
В настоящее время к РеА относят воспалительные негнойные заболевания суставов, развивающиеся вследствие иммунных нарушений, после кишечной или урогенитальной инфекции. В преобладающем большинстве случаев РеА ассоциируется с острой или персистирующей кишечной инфекцией, вызываемой энтеробактериями (Yersinia enterocolitica, Yersinia pseudotuberculosis, Salmonella enteritidis, Salmonella typhimurium, Shigella flexneri, Shigella sonnei, Shigella Newcastle, Campylobacter jejuni), и с острой или персистирующей урогенитальной инфекцией, вызываемой Chlamydia trachomatis. Инфекции респираторного тракта, связанные с Mycoplasma pneumoniae, и особенно Chlamydophila pneumonia, также могут служить причинами развития РеА. Имеются также данные о связи РеА с кишечной инфекцией, вызванной Clostridium difficile и некоторыми паразитарными инфекциями.
РеА, ассоциированный с кишечной инфекцией и инфекцией, вызванной Chlamydia trachomatis, развивается преимущественно у генетически предрасположенных лиц (носителей HLA-B27) и относится к группе серонегативных спондилоартритов [2, 3, 6]. Было обнаружено, что антитела к ряду микроорганизмов перекрестно реагируют с HLA-B27. Это объясняется феноменом молекулярной мимикрии, согласно которой белки клеточной стенки ряда кишечных бактерий и хламидий имеют структурное сходство с отдельными участками молекулы HLA-B27. Предполагается, что перекрестно реагирующие антитела способны оказывать повреждающее действие на собственные клетки организма, которые в наибольшей степени экспрессируют молекулы HLA-B27. Но при этом считают, что такое перекрестное реагирование может препятствовать осуществлению адекватного иммунного ответа, способствуя персистированию и хронизации инфекции. Имеются данные, что у носителей НLA-B27 после перенесенной кишечной и урогенитальной инфекции РеА развивается в 50 раз чаще, чем у лиц, не имеющих этого антигена гистосовместимости.
Диагноз РеА ставится в соответствии со следующими диагностическими критериями, принятыми на III Международном совещании по РеА в Берлине в 1996 г. [7].
– Олигоартрит (поражение до 4 суставов).
– Преимущественное поражение суставов ног.
– Время возникновения: за 2–4 нед до развития артрита.
Лабораторное подтверждение инфекции:
– Необязательно, но желательно при наличии клинических проявлений инфекции.
– Обязательно, при отсутствии явных клинических проявлений инфекции.
Критерии исключения — установленная причина развития моно- или олигоартрита:
Вместе с тем в реальной практике термин РеА ошибочно используется ревматологами гораздо шире и включает артриты после перенесенной вирусной инфекции, поствакцинальные артриты, постстрептококковый артрит и некоторые другие.
В настоящее время одной из наиболее распространенных причин развития РеА является хламидийная инфекция.
В структуре РеА хламидийные артриты составляют до 80% [8, 9, 10]. Это связано с пандемией хламидиоза в мире, особенностями путей передачи хламидийной инфекции, цикла развития хламидий и реакции на терапию. Восприимчивость к хламидиям всеобщая, существует множество путей передачи инфекции в том числе и контактно-бытовой путь (в отношении Chlamydia pneumonia). Триггерная роль кишечной инфекции в развитии РеА также остается актуальной.
Классическим проявлением РеА является болезнь Рейтера или уретро-окуло-синовиальный синдром, впервые описанный Бенджамином Броди, а затем Гансом Рейтером, под именем которого синдром и вошел в медицину. Болезнь Рейтера в настоящее время рассматривается как особая форма РеА и характеризуется классической триадой клинических симптомов: уретрит, конъюнктивит, артрит. При наличии кератодермии говорят о тетраде болезни Рейтера. Синдром Рейтера чаще всего начинается с симптомов поражения урогенитального тракта через 2–4 нед после перенесенной инфекции или предполагаемого заражения хламидиями или бактериями кишечной группы. При синдроме Рейтера триггерными инфекционными факторами чаще всего являются Chlamydia trachomatis, Shigella flexneri 2а, либо их сочетание.
Болезнь Рейтера, ассоциированная с хламидийной инфекцией, характеризуется менее выраженной остротой клинической картины [8, 10]. Поражение урогенитального тракта характеризуется стертостью клинической картины. У мальчиков могут развиваться баланит, инфицированные синехии, фимоз. У девочек поражение урогенитального тракта может ограничиваться вульвитом, вульвовагинитом, лейкоцитурией и/или микрогематурией, а также клиникой цистита. Поражение урогенитального тракта может на несколько месяцев опережать развитие суставного синдрома.
Поражение глаз характеризуется развитием конъюнктивита: чаще катарального, невыраженного, непродолжительного, но склонного к рецидивированию. У 1/3 больных может развиться острый иридоциклит, угрожающий слепотой. Поражение глаз также может на несколько месяцев или лет опережать развитие суставного синдрома.
Экссудативный артрит (моно- или олигоартрит) при болезни Рейтера хламидийной этиологии может протекать без боли, скованности, выраженного нарушения функции, но с большим количеством синовиальной жидкости и непрерывно рецидивируя. Поражение суставов при этом характеризуется длительным отсутствием деструктивных изменений, несмотря на рецидивирующий синовит.
Нередко РеА протекает без отчетливых внесуставных проявлений, относящихся к симптомокомплексу синдрома Рейтера (конъюнктивит, уретрит, кератодермия). В таких случаях ведущим является суставной синдром, который также характеризуется преимущественным поражением суставов нижних конечностей, асимметричного характера. Несмотря на отсутствие внесуставных проявлений у этих детей также имеется высокий риск развития ювенильного спондилоартрита. Наличие характерного суставного синдрома, сопровождающегося выраженной экссудацией и связанного с перенесенной кишечной или урогенитальной инфекцией или с наличием серологических маркеров кишечной или урогенитальной инфекции, позволяет с большой долей вероятности отнести заболевание к разряду реактивных артритов.
Диагностика РеА основывается на клинико-анамнестических данных, включающих наличие характерного суставного синдрома, связанного с инфекционным процессом. В связи с тем, что инфекция, предшествующая развитию РеА, не всегда бывает ярко выражена, в процессе диагностики особую значимость приобретают данные дополнительных лабораторных исследований. Для постановки точного диагноза необходимо выделение возбудителя, вызвавшего инфекцию, и/или обнаружение в сыворотке крови высоких титров антител к нему. Для идентификации триггерных инфекций используют различные микробиологические, иммунологические и молекулярно-биологические методы. Этиологическая диагностика включает следующее.
1.1. Выявление антигена хламидий в эпителиальных клетках, полученных в результате соскобов из уретры и конъюнктивы, а также в синовиальной жидкости (прямой иммунофлюоресцентный анализ и др.).
1.2. Выявление антител к антигенам хламидий в сыворотке крови и в синовиальной жидкости (реакция связывания комплемента, прямая и непрямая иммунофлюоресценция):
- острая фаза хламидиоза или обострение хронического процесса — наличие иммуноглобулин (Ig) M в течение первых 5 дней, IgA — в течение 10 дней, IgG — через 2–3 нед;
- реинфекция или реактивация первичной хламидийной инфекции — повышение уровня IgG, определяются IgA, могут быть единичные IgM;
- хроническое течение хламидиоза — наличие постоянных титров IgG и IgA;
- бессимптомное течение хламидиоза, персистенция возбудителя — низкие титры IgA;
- перенесенная хламидийная инфекция — низкий титр IgG.
1.3. Выявление антител к бактериям кишечной группы в сыворотке крови (при помощи реакции прямой гемагглютинации и реакции связывания комплемента).
Наиболее доказательным является выделение триггерных микроорганизмов классическими микробиологическими методами (посевы кала, перенос соскоба с эпителия уретры и/или конъюнктивы на культуру клеток). Чаще удается выделить хламидии из урогенитального тракта, значительно реже — энтеробактерии из кала.
Трудности диагностики РеА часто обусловлены стертым субклиническим течением первичного инфекционного процесса. Артрит развивается чаще при нетяжелых формах кишечной или урогенитальной инфекций, и к моменту развития артрита признаки триггерной инфекции в большинстве случаев проходят. Кроме того, в условиях нарушенного иммунного ответа возможно развитие хронических персистирующих форм инфекции. Поэтому в дебюте суставного синдрома необходимо в первую очередь исключить скрытую кишечную и хламидийную инфекции. Кроме того, диагностику РеА затрудняет сочетание предшествовавших инфекционных процессов различной локализации. Установлено также, что поражение кишечника и мочевыводящих путей может быть как первичным по отношению к РеА, так и развиваться одновременно с ним и даже позже, что нередко затрудняет определение причинно-следственных связей.
Дифференциальный диагноз РеА от других видов ювенильных артритов часто бывает затруднен. Наиболее распространенной патологией, требующей дифференциальной диагностики с РеА, являются инфекционные артриты, заболевания, связанные с инфекцией, сопровождающиеся артритами, а также ортопедическая патология и разные формы ювенильного идиопатического артрита.
Вирусный артрит. В настоящее время известно, что около 30 вирусов могут вызывать развитие острого артрита. К ним относятся: вирусы краснухи, парвовирус, аденовирус, вирус гепатита В, вирусы герпеса различных типов, вирус паротита, энтеровирусы, Коксаки-вирусы и др. Диагностика основана на связи с вирусной инфекцией или проведенной вакцинацией. Клиническая картина чаще представлена артралгиями, чем артритами. Клинические симптомы наблюдаются в течение 1–2 нед и исчезают без остаточных явлений.
Диагностические критерии постстрептококкового артрита включают:
- появление артрита на фоне или спустя 1–2 нед после перенесенной носоглоточной инфекции (стрептококковой этиологии);
- одновременное вовлечение в процесс преимущественно средних и крупных суставов;
- возможную торпидность суставного синдрома к действию нестероидных противовоспалительных препаратов (НПВП), нерезкие сдвиги в лабораторных показателях;
- наличие повышенных титров постстрептококковых антител;
- выявление хронических очагов инфекции в носоглотке (хронический тонзиллит, фарингит, гайморит).
Клещевой боррелиоз (болезнь Лайма). Диагностика боррелиоза основана на данных анамнеза: пребывание пациента в эндемичной зоне, наличие в анамнезе факта укуса клеща, а также характерную клиническую картину. Подтверждают диагноз серологическими методами, которые выявляют антитела к Borrelia burgdorferi.
Диагноз септического артрита ставится на основании клинической картины инфекционного процесса, определения характера синовиальной жидкости, результатов посева синовиальной жидкости на флору с определением чувствительности к антибиотикам, а также рентгенологических данных (в случае развития остеомиелита).
Клиническая картина туберкулезного артрита представлена общими симптомами туберкулезной инфекции: интоксикацией, субфебрильной температурой, вегетативными нарушениями и локальными симптомами — боли в суставах, преимущественно в ночное время, явления артрита. Для подтверждения диагноза необходимы рентгенологические данные, анализ синовиальной жидкости, биопсия синовиальной оболочки.
Ювенильный спондилоартрит. Данное заболевание является возможным исходом хронического течения РеА у предрасположенных лиц (HLA-B27 носителей). Суставной синдром так же, как и при РеА, представлен асимметричным моно- или олигоартритом с преимущественным поражением суставов ног. Кардинальными признаками, позволяющими поставить диагноз ювенильного спондилоартрита, являются рентгенологические данные, свидетельствующие о наличии сакроилеита (одно- или двустороннего).
Выделяют три вида терапии: этиотропную, патогенетическую, симптоматическую.
Этиотропное лечение РеА, ассоциированного с хламидийной инфекцией. Поскольку хламидии являются внутриклеточными паразитами, то выбор антибактериальных препаратов ограничивается только теми, которые способны накапливаться внутриклеточно. К таким препаратам относятся макролиды, тетрациклины и фторхинолоны. Однако тетрациклины и фторхинолоны достаточно токсичны, их применение ограничено в детской практике. В связи с этим для лечения хламидийного артрита у детей используются макролиды. Азитромицин — для детей в первый день приема доза препарата составляет 10 мг/кг, а в последующие 5–7 дней — 5 мг/кг в один прием. Лучший эффект достигается при использовании антибиотика в течение 7–10 дней. Рокситромицин — для детей суточная доза составляет 5–8 мг/кг массы тела. Джозамицин (вильпрафен) суточная доза препарата составляет 30–50 мг/кг массы тела, разделенные на три приема. Кларитромицин используется у детей старше 6 мес — 15 мг/кг/сут в 2 приема, спирамицин — детям массой более 20 кг из расчета 1,5 млн МЕ/10 кг массы тела в сутки. Кратность приема — 2–3 раза.
У подростков возможно применение тетрациклинов и фторхинолоновых препаратов.
В отношении РеА, связанных с кишечной инфекцией, однозначных рекомендаций по антибактериальной терапии не существует. Наличие антител к бактериям кишечной группы и особенно бактериологическое подтверждение кишечной инфекции является основанием для назначения антибиотиков. Используются аминогликозиды — амикацин в/м или в/в — до 15 мг/кг/сут в одно-два введения, 7 сут, гентамицин в/м или в/в 5–7 мг/кг/сут в два введения, 7 сут, фторхинолоновые препараты (для детей старше 12 лет).
Патогенетическая терапия. Монотерапия антибиотиками оказывает недостаточный эффект при затяжном и хроническом течении РеА, неадекватности иммунного ответа. Целесообразно для лечения хронического хламидийного артрита использовать различные иммуномодулирующие средства (тактивин, ликопид, полиоксидоний) в сочетании с антибиотиками.
Наиболее эффективной, по результатам многолетних контролируемых исследований, оказалась схема с использованием ликопида [8, 10, 13].
Схема комбинированной терапии ликопидом и антибиотиками у больных с хроническим течением РеА, ассоциированного с хламидийной инфекцией, следующая.
- Ликопид применяется в виде сублингвальных таблеток. Детям до 5 лет целесообразно назначать ликопид по 1 мг 3 раза в день, дети старше 5 лет — ликопид по 2 мг 3 раза в день. Курс лечения составляет 24 дня.
- На 7-й день приема ликопида назначается антибиотик. Возможно использование любого антибиотика, обладающего противохламидийной активностью. Так как необходимо перекрыть 2–3 жизненных цикла хламидий, курс лечения антибиотиком должен составлять не менее 7–10 дней.
- После завершения курса антибактериальной терапии дети продолжают получать ликопид до 24 дня.
Использование иммуномодуляторов противопоказано при трансформации РеА в спондилоартрит, высокой иммунологической активности.
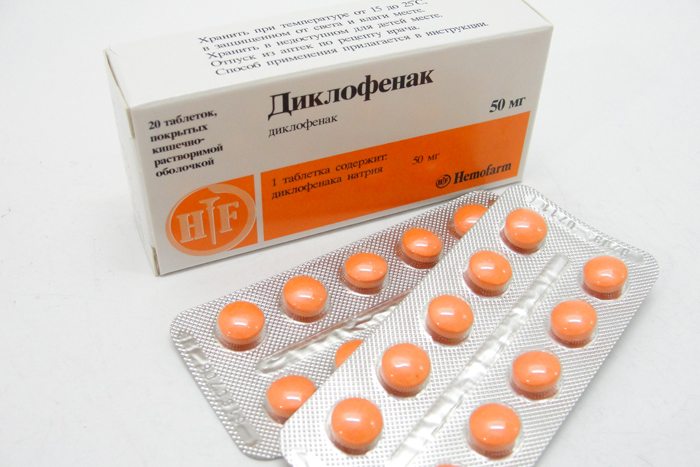
Симптоматическая терапия. С целью лечения суставного синдрома при РеА применяют НПВП. Диклофенак внутрь 2–3 мг/кг/день в 2–3 приема или напроксен внутрь 15–20 мг/кг/день в 2 приема или ибупрофен внутрь 35–40 мг/кг в 2–4 приема или нимесулид внутрь 5 мг/кг в 2–3 приема или мелоксикам внутрь 0,3–0,5 мг/кг в 1 прием.
Глюкокортикостероиды как наиболее мощные противовоспалительные средства используются в период обострения суставного синдрома. Их применение ограничивается преимущественно внутрисуставным способом введения. При необходимости можно воспользоваться коротким курсом пульс-терапии метилпреднизолоном, который предполагает быстрое (в течение 30–60 мин) внутривенное введение больших доз метилпреднизолона (5–15 мг/кг в течение 3 дней).
При тяжелом и торпидном течении заболевания, появлении признаков спондилоартрита, высокой клинической и лабораторной, в том числе иммунологической, активности возможно применение иммуносупрессивных препаратов. Наиболее часто используется сульфасалазин (в дозе 30–40 мг/кг массы в сутки), реже метотрексат ( в дозе 10 мг/м 2 в неделю).
У большинства детей РеА заканчивается полным выздоровлением. У части больных эпизоды РеА рецидивируют и в дальнейшем появляются признаки спондилоартрита, особенно у HLA-B27 позитивных больных. Мерами профилактики являются своевременное выявление хламидийной инфекции у ребенка и членов его семьи, адекватная терапия урогенитальной инфекции.
Е. С. Жолобова, доктор медицинских наук, профессор
Е. Г. Чистякова, кандидат медицинских наук, доцент
Д. В. Дагбаева
ММА им. И. М. Сеченова, Москва
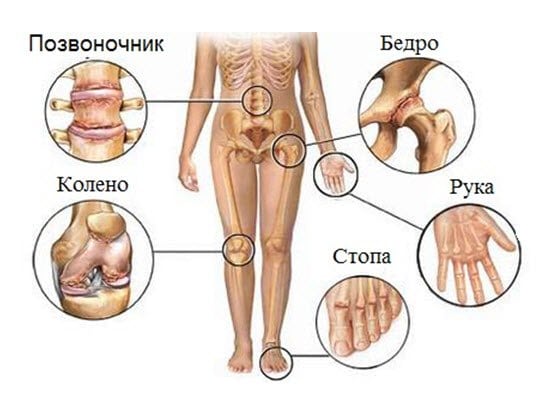
Хламидийный артрит — ревматическая патология, для которой характерно сочетанное поражение урогенитального тракта, суставов, слизистых оболочек глаз. Одновременное повреждение этих структур диагностируется редко. Заболевание клинически проявляется постепенно, провоцируя дизурические расстройства, конъюнктивиты, артралгии, тугоподвижность суставов. Хламидийный артрит возникает в результате аутоиммунного процесса, развивающегося на фоне урогенитальной инфекции.
Для обнаружения патологии используются лабораторные методы — ПЦР, исследование синовиальной жидкости, серологические реакции. Установить возникшие повреждения в синовиальной оболочке, суставной капсуле, связочно-сухожильном аппарате помогают рентгенография, МРТ, КТ. В терапии используются препараты различных клинико-фармакологических групп — антибиотики, НПВС, иммуномодуляторы, глюкокортикостероиды. При своевременном обращении за медицинской помощью прогноз на полное выздоровление благоприятный.
Причины
Важно знать! Врачи в шоке: "Эффективное и доступное средство от АРТРИТА существует. " Читать далее.
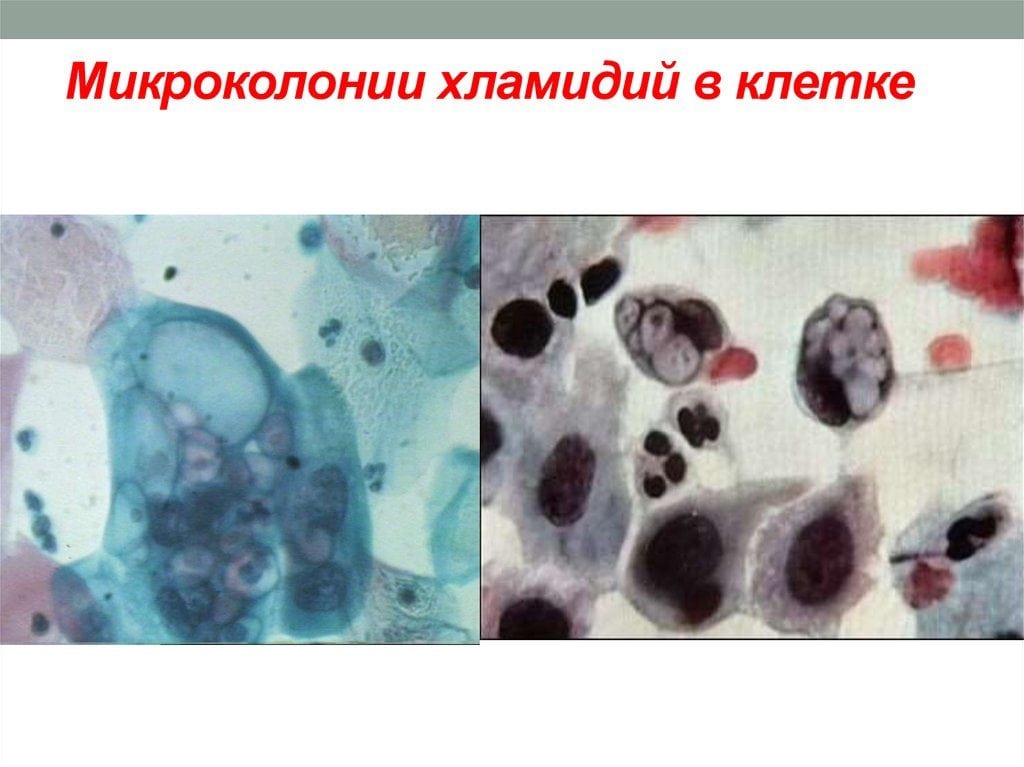
Ведущий этиологический агент хламидийного артрита — хламидии. Эти возбудители урогенитального хламидиоза — Chlamidia trachomatis — представляют собой мелкие бактерии, паразитирующие в клетках человека. После проникновения в организм они долгое время находятся в нем, никак не проявляясь. Но при резком снижении иммунитета патогенные микроорганизмы начинают активно размножаться, выделяя в окружающее пространство токсичные продукты своей жизнедеятельности. Хламидиоз чаще всего передается половым путем, а одноименный артрит диагностируется у 80% мужчин и 15-20% женщин. Патология выявляется у детей крайне редко.
Роль инфекционных агентов в этиопатогенезе реактивных асептических артритов заключается в молекулярном сходстве их антигенов с аутоантигенами человека. Проникнув в суставы, микроорганизмы начинают усиленно размножаться, но не это становится причиной развития воспалительного процесса. После их обнаружения иммунной системой вырабатываются специфические белки — антитела, необходимые для уничтожения болезнетворных бактерий. Но сходство белковых структур микроорганизмов с тканями хрящей, синовиальных оболочек, связок, сухожилий приводит к атаке антителами собственных клеток организма. Это и становится толчком к развитию хламидийного артрита, имеющего аутоиммунную этиологию. Таким образом, воспалительный процесс в суставах вызывают не сами инфекционные агенты, а реакция иммунной системы на их вторжение.
Хламидийный артрит развивается далеко не у каждого зараженного человека. Проникновению и персистенции микробов способствует анатомо-гистологическая уникальность суставных тканей. Миграция антигенпрезентирующих клеток из системного кровотока облегчается:
- фенестрированными (с тонким эндотелием и порами в эндотелиоцитах) капиллярами синовия;
- наличием молекул клеточной адгезии.
Происходит фиксация хондроцитами и синовиоцитами антигенов, что приводит к различным иммунологическим реакциям — продуцируются факторы клеточного роста, цитокины, медиаторы воспаления, повышается концентрация токсичных кислородных радикалов и оксида азота. Хламидийный артрит диагностируется у пациентов, наследственно предрасположенных к нему, имеющих особое строение суставных тканей.
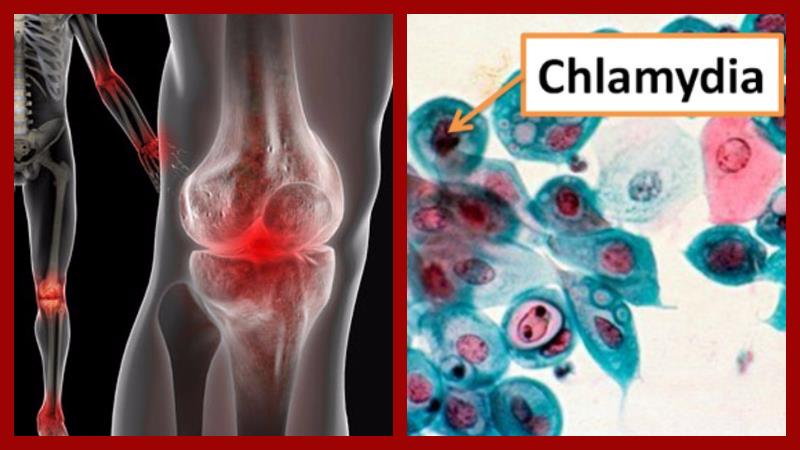
Клиническая картина
Хламидийная инфекция длительное время протекает бессимптомно. В дальнейшем она может клинически проявляться у женщин цервицитами, сальпингитами, аднекситами, циститами, проктитами, вялотекущими эндометритами, спаечными процессами в органах малого таза. Также обнаруживается фарингит, конъюнктивит, увеит. У женщин часто возникают тянущие тупые боли внизу живота, особенно во время полового контакта. Симптоматика хламидиоза у мужчин отличается. Они часто страдают от конъюнктивита, увеита, уретрита, баланита или баланопостита, простатита, проктита и эпидидимита во время сексуальной активности.
Хламидийный артрит нередко сопровождается внутрисуставными симптомами. Это специфические признаки миокардита, перикардита, нарушения ритма, проводимости, относительная недостаточность аортального клапана, бронхиолит. Патогенные микроорганизмы провоцируют развитие пиелонефрита, узловатой эритемы, амилоидоза почек. Характерные симптомы суставной патологии:
- боли в одном или нескольких суставах, усиливающиеся во время движения или при подъеме тяжестей;
- болезненные ощущения различной вариабельности в состоянии покоя при прогрессировании патологии;
- отечность, покраснение кожных покровов в области пораженных суставов;
- кожа постоянно горячая на ощупь из-за вовлечения в воспалительный процесс мягких тканей;
- болезненность при пальпации;
- развитие защитных контрактур — ограничения пассивных движений в суставе, неполноценное его сгибание или разгибание;
- спазмированность скелетной мускулатуры в области поражения;
- накопление патологического экссудата в суставе;
- утренняя припухлость и скованность движений.
Симптомы хламидийного артрита выражены слабо на стадии ремиссии. Во время рецидивов их интенсивность существенно возрастает. Нередко возникают признаки общей интоксикации организма — температура тела повышается, усиливается потоотделение, появляются озноб и холодная испарина. Человек страдает от желудочно-кишечных расстройств — избыточного газообразования, тошноты, отсутствия аппетита. Могут возникать головные боли, головокружения, слабость, быстрая утомляемость, расстройства сна.
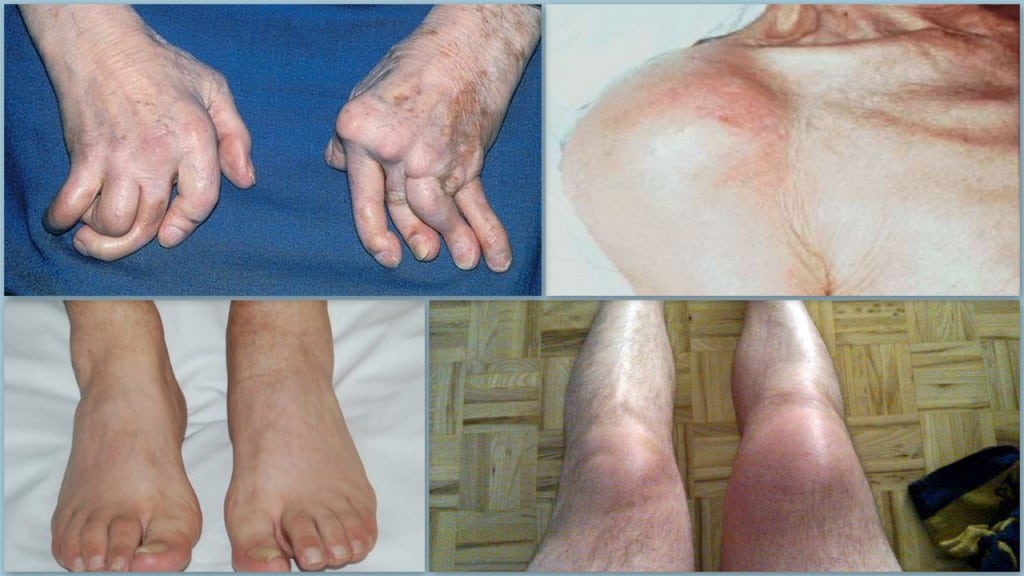
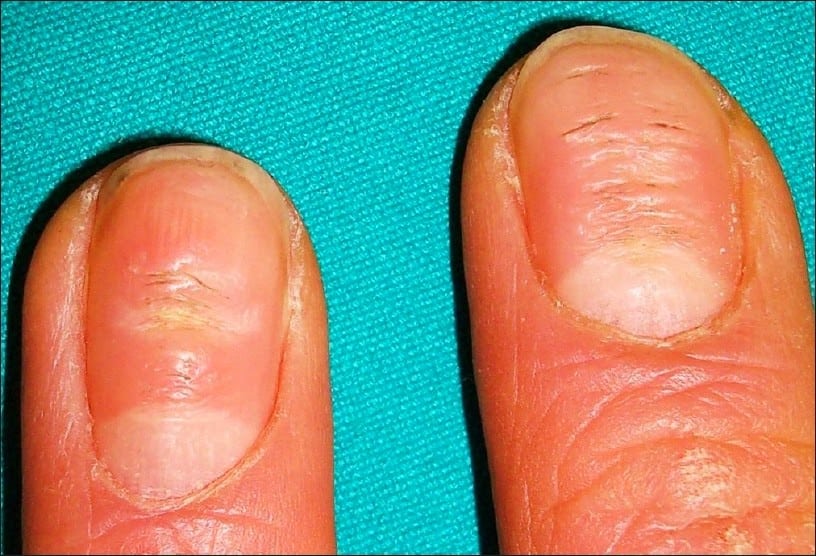
Для хламидийного артрита характерно ассиметричное поражение суставов. Сначала повреждается одно сочленение, чаще голеностоп или колено. Если больной не обращается за медицинской помощью, то вскоре у него диагностируется полиартрит — множественное сочетанное повреждение суставов. Нередко поражаются кожные покровы ладоней и подошв по типу кератодермии. Происходит ороговение дермы с формированием плотных бляшек. При хламидийном артрите также изменяется структура и цвет ногтевых пластинок, увеличиваются лимфатические узлы, особенно паховой локализации.
Диагностика
К диагностированию суставной патологии часто подключаются ревматолог, венеролог, уролог офтальмолог, гинеколог. Подозрение на развитие хламидийного артрита возникает при осмотре пациента по характерным внешним признакам — покраснению глаз, припухлости пораженных суставов и лимфоузлов. Назначаются развернутые общеклинические исследования крови и мочи. После проведения трехстаканной пробы, проб Аддиса-Каковского, Нечипоренко выявляется гной в моче, что указывает на наличие патогенных микроорганизмов (лейкоцитурия). При исследовании простатического секрета выявляется повышенная концентрация лейкоцитов на фоне снижения количества лецитиновых телец. В крови пациента с хламидиозом всегда повышено число альфа- и бета-глобулинов, фибрина, серогликоидов, С-реактивного протеина. При этом анализ на присутствие ревматоидного фактора отрицательный. Обязательно проводятся цитологические исследования следующих биологических образцов:
- соскобы мочеиспускательного канала, шейки матки;
- часть слезного секрета конъюнктивы;
- синовиальный экссудат;
- сперма;
- секрет простаты.
В образцах обнаруживаются хламидийные внутриклеточные цитоплазматические включения. Методом полимеразной цепной реакции выявляется ДНК инфекционного агента в биологическом материале. Установить наличие микроорганизмов в крови можно проведением одной из серологических реакций.
После взятия с помощью пункции синовиальной жидкости из пораженных патологией суставов обнаруживаются изменения ее качественного и количественного состава. Муциновый остаток рыхлый, увеличена концентрация лейкоцитов и доля нейтрофильных гранулоцитов. В крови выявляются цитофагоцитирующие макрофаги, хламидийные антигены и антитела, повышенная активность комплимента.
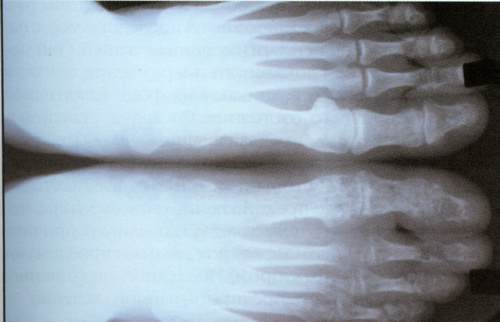
Параартикулярный несимметричный остеопороз, сужение суставных щелей, эрозивная деструкция костей устанавливаются по рентгенографическим снимкам. Чаще всего дегенеративным изменениям подвергаются стопы, тела позвонков. У трети пациентов диагностируется воспаление крестцово-подвздошных сочленений.
Основные методы лечения
Даже "запущенный" АРТРИТ можно вылечить дома! Просто не забывайте раз в день мазать этим.
Для исключения повторного инфицирования проводится одновременная терапия полового партнера. Основными целями лечения хламидийного артрита становятся:
- уничтожение болезнетворных микроорганизмов — хламидий, активизировавшихся бактерий и (или) грибков условно-патогенного биоценоза;
- снижение, а затем полное устранение выраженности суставных и внесуставных клинических проявлений;
- терапия возникших негативных последствий.
Для устранения инфекционных агентов пациентам назначается антибиотикотерапия Доксициклином. В лечебные схемы включаются антибактериальные средства из других групп. Это фторхинолоны (Ломефлоксацин, Офлоксацин, Ципрофлоксацин), макролиды (Эритромицин, Кларитромицин, Азитромицин), полусинтетические пенициллины с клавулановой кислотой (Панклав, Аугментин, Амоксиклав).
После антибиотикотерапии для стимуляции роста полезных лакто- и бифидобактерий применяются эубиотики — Хилак Форте, Бифидумбактерин, Лактобактерин, Линекс, Аципол. Так как хламидии поражают вместе с суставами внутренние органы, пациентам рекомендован прием гепатопротекторов (Эссенциале Форте, Карсил, Эссливер Форте), протеолитических ферментов (Панкреатин, Трипсин, Химотрипсин).

Активность патогенных грибков часто повышается на фоне изменившегося состава кишечной, вагинальной микрофлоры. Для коррекции этого состояния применяются антимикотические средства, обычно Флуконазол, Нистатин, Клотримазол.

Для нормализации иммунного ответа на внедрение инфекционных агентов проводится иммунокоррегирующая терапия. Используются препараты с интерфероном или те, которые стимулируют его выработку. Пациентам назначаются адаптогены (женьшень, элеутерококк), повышающие устойчивость организма к воздействию внешних и внутренних негативных факторов. С этой же целью рекомендован курсовой прием сбалансированных комплексов витаминов и микроэлементов (Центрум, Витрум, Селмевит, Компливит, Мультитабс).

Тяжелые атаки хламидийного артрита купируются проведением дезинтоксикационной, антигистаминной терапии. В особо сложных случаях применяется экстракорпоральная гемокоррекция (плазмаферез, каскадная фильтрация плазмы, криоаферез). Для устранения суставных симптомов хламидийного артрита используются препараты различных клинико-фармакологических групп:
- нестероидные противовоспалительные средства — Диклофенак, Нимесулид, Целекоксиб, Мелоксикам, Кетопрофен, Ибупрофен;
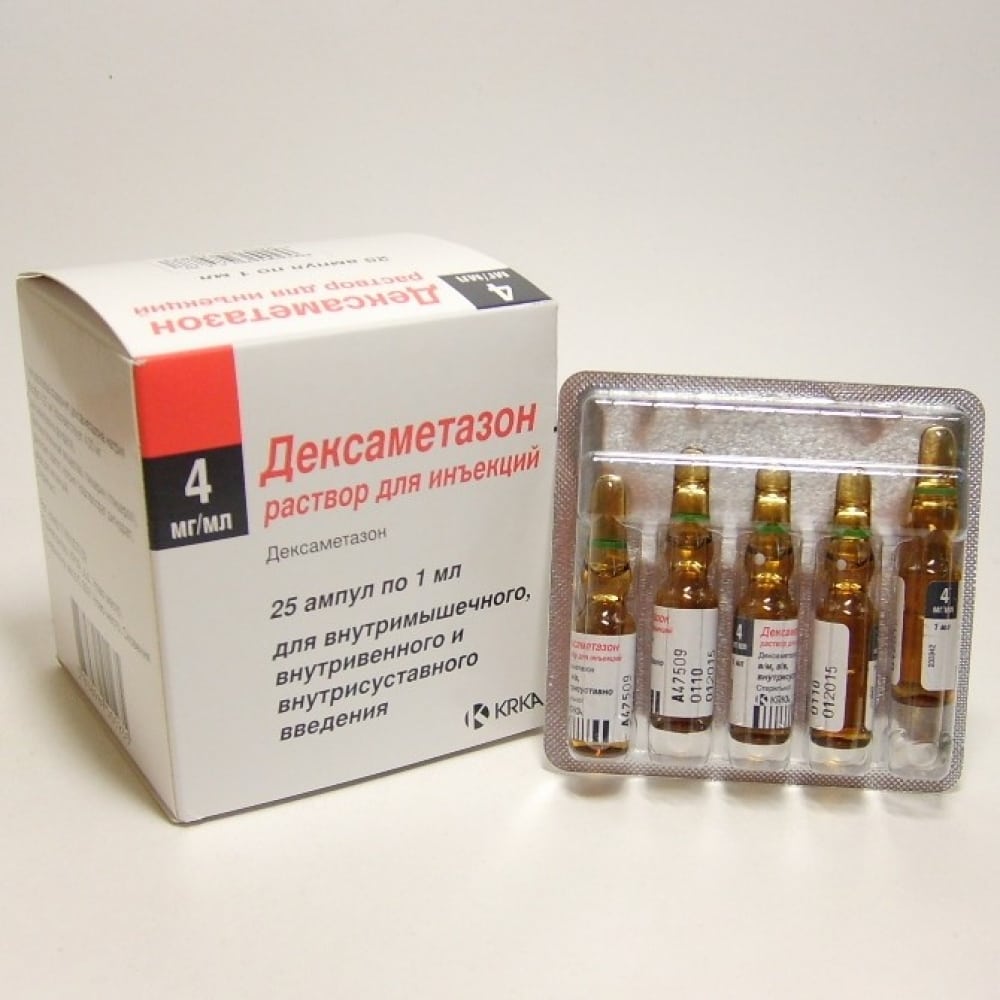
- глюкокортикостероиды — Триамцинолон, Дексаметазон, Дипроспан, Флостерон, Кеналог в виде медикаментозных блокад в сочетании с анестетиками Лидокаином или Новокаином;
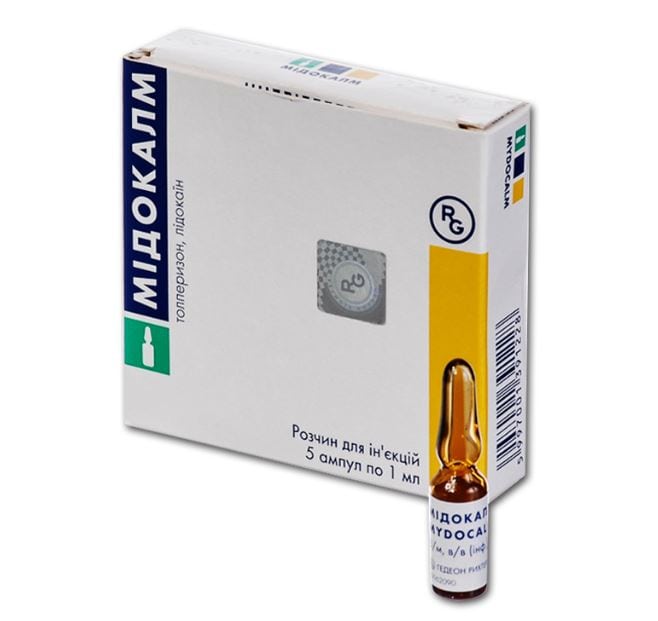
- миорелаксанты — Баклосан, Сирдалуд, Мидокалм при мышечных спазмах, контрактурах;
- базовые средства — Сульфосалазин, Метотрексат для устранения ревматоидных клинических проявлений;
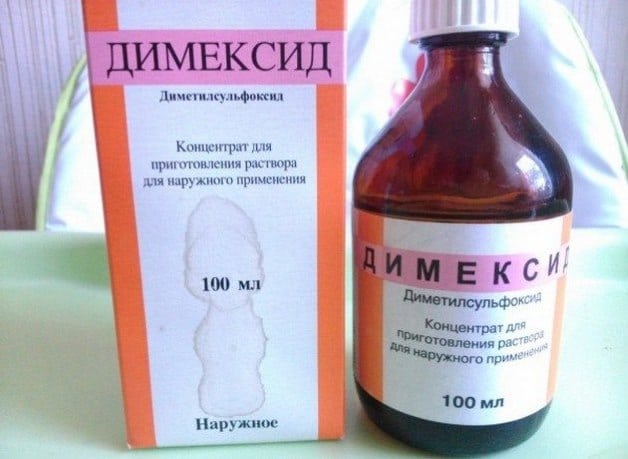
- Димексид в виде компрессов от воспалительных отеков;
- мази с обезболивающим и противовоспалительным действием (Финалгель, Найз, Фастум, Вольтарен, Нурофен);
- хондропротекторы — Терафлекс, Структум, Артра для регенерации хрящей, связок, сухожилий.

Терапия дополняется физиотерапевтическими процедурами — это фонофорез с одним из протеолитических ферментов, электрофорез с анальгетиками, магнитотерапия, лазеротерапия, УВЧ-терапия. На этапе реабилитации пациентам показаны массаж, ежедневные занятия лечебной физкультурой или гимнастикой.

Хламидийный артрит хорошо поддается терапии, особенно при своевременном обращении за медицинской помощью. При соблюдении всех врачебных рекомендаций он полностью излечивается в течение нескольких недель.
Как забыть о болях в суставах и артрите?
- Боли в суставах ограничивают Ваши движения и полноценную жизнь…
- Вас беспокоит дискомфорт, хруст и систематические боли…
- Возможно, Вы перепробовали кучу лекарств, кремов и мазей…
- Но судя по тому, что Вы читаете эти строки - не сильно они Вам помогли…
Но ортопед Валентин Дикуль утверждает, что действительно эффективное средство от АРТРИТА существует! Читать далее >>>
Читайте также:


