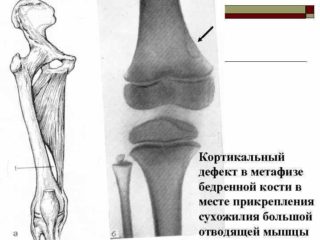
Фиброзный кортикальный дефект метафиза большеберцовой кости
Фиброзный кортикальный дефект бедренной кости – опухолеподобное поражение, преимущественно солитарное, которое встречается у 30-40% детей в возрасте от 4 до 8 лет и в подавляющем большинстве случаев не требует медицинского вмешательства. Патология развивается и протекает абсолютно бессимптомно и обычно выявляется случайно при проведении рентгенологического обследования костей таза и нижних конечностей. По своим гистологическим показателям фиброзный кортикальный дефект сходен с неоссифицируемой фибромой.
Причины возникновения дефекта
Причины образования патологии на сегодняшний день остаются не до конца изученными. Выявлена некоторая связь с генетически обусловленными системными заболеваниями соединительной ткани, в частности, крупные очаги поражения часто сопутствуют нейрофиброматозу I типа, фиброзной дисплазии, синдрому Яффе-Кампаначчи. Также отдельные исследования выявляют связь развития кортикального фиброзного дефекта с гипофосфатемическим витамин Д-резистентным рахитом.
В большинстве случаев этиология заболевания остается неясной. Патология выявляется случайно при рентгенологическом обследовании. Дефект нельзя отнести к редким: согласно статистике, у 30-40% детей в возрасте от 3 до 10 лет выявляются фиброзные очаги в метафизе и диафизе большеберцовой кости. Мальчики подвержены заболеванию вдвое чаще, чем девочки. У взрослых после закрытия ростковых зон костей фиброзный дефект не развивается. Как правило, к 13-14 годам наблюдается ремиссия патологии, и очаги фиброзной ткани замещаются нормальной костной тканью.
Случаев озлокачествления фиброзных новообразований в медицинской литературе не описано.
Клиническая картина
Фиброзный кортикальный дефект обнаруживается чаще всего в метафизе и диафизе большеберцовых костей, в местах прикрепления активных мышц, и представляет собой опухолеподобное очаговое перерождение тканей. Очаги представлены волокнистой фиброзной тканью с включениями гигантских клеток, а в некоторых случаях – рассеянных в фиброзной ткани веретенообразных и ксантомных клеток: нагруженных холестериновым эфиром макрофагов, перерожденных моноцитов. Также внутри фиброзных очагов могут быть обнаружены лимфоциты и плазменные клетки как следы воспалительной реакции.
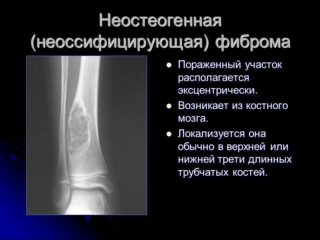
Очаги чаще всего возникают первично на периостальной поверхности, с течением времени распространяются интра- и субкортикально. В редких случаях новообразование заполняет весь поперечник кости. Если очаги имеют склонность к быстрому росту и распространению, заболевание классифицируют как неоссифицирующую фиброму и причисляют к доброкачественным новообразованиям, подлежащим оперативному лечению.
Отмечались ситуации, когда у пациента в кости одной конечности наблюдался фиброзный кортикальный дефект, а в другой – неоссифицирующая фиброма, что позволяет высказать предположение об общей природе их возникновения. При дифференциации фиброзного кортикального дефекта от неоссифицирующей фибромы принимают во внимание степень вовлечения в патологию костномозгового канала: ФКД не затрагивает его, а неоссифицируущая фиброма имеет тенденцию к прорастанию внутрь канала.
В отличие от кортикального дефекта, не выявляемого при прощупывании, фиброма может проявлять себя как припухлость плотной консистенции, неподвижная, не спаянная с кожей, слегка болезненная при пальпации.
При наличии фиброзного дефекта большеберцовой кости и при неоссифицируемой фиброме общее состояние больного остается удовлетворительным. Клинические анализы крови не позволяют выявить никаких характерных особенностей данных состояний.
Стоит отметить, что в медицинских кругах нет единого мнения о дифференциации ФКД и неоссифицирующей фибромы. Ряд специалистов считают их двумя разновидностями течения одной патологии, другие относят фиброму к опухолевым заболеваниям костной ткани, а ФКД не патологией, а дефектом или особенностью развития и роста костной ткани. Существует также мнение, что ФКД и неоссифицирующая фиброма являются разными стадиями течения одного заболевания.
Патология развивается бессимптомно и не сопровождается болевыми ощущениями или нарушениями подвижности конечностей. Однако в случаях масштабного замещения костной ткани фиброзной существенно снижается прочность кости, что может привести к патологическим переломам.
Диагностика кортикального дефекта
На рентгенологическом снимке обнаруживаются светлые очаги с четко очерченными границами склерозированной ткани, также наблюдается вздутие кортикального слоя. В случае неоссифицирующей фибромы в патологический процесс включен костномозговой канал.
Сцинтография при диагностике кортикального дефекта в большинстве случаев оказывается неэффективной и не позволяет выявить патологию. В отдельных случаях наблюдаются очаги умеренного поглощения и умеренной гиперемии. При обнаружении выраженного поглощения и гиперемии можно заподозрить перелом.
Патологию следует дифференцировать от других опухолевых образований костной ткани.
- Доброкачественная фиброзная гистоцитома отличается от фиброзного кортикального дефекта тем, что на рентгенографическом снимке не выявляется. Также фиброзная гистоцитома может вызывать болезненные ощущения.
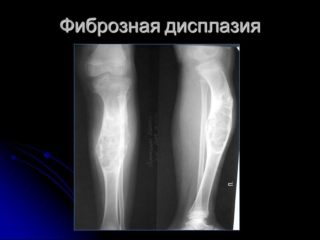
- Фиброзная дисплазия имеет везикулярную форму, развивается от центра кости.
- Периостальный десмоид выявляется в значительно более позднем возрасте – от 12 до 20 лет.
Процесс заживления очагов фиброзной ткани на рентгенографическом снимке следует отличать от процесса злокачественной резорбции тканей.
Лечение патологии
В большинстве случаев при выявлении патологии выбирается выжидательная тактика. Назначаются регулярные обследования для отслеживания динамики роста новообразований. Проведение биопсии при фиброзном кортикальном дефекте не рекомендуется.
В том случае, если очаг занимает более 50% поперечного сечения кости и возникает угроза спонтанного перелома, проводится хирургическая операция. Путём кюретажа (выскабливания) фиброзная ткань удаляется и замещается ауто- или аллотрансплантатом.
Прогноз
В большинстве случаев прогноз заболевания благоприятный даже при отсутствии какого-либо лечения. Фиброзный кортикальный дефект бедренной кости у детей имеет тенденцию к самопроизвольному исчезновению в 100% случаев — очаги замещаются здоровой костной тканью.
В исключительно редких случаях отмечались рецидивы заболевания с повторным формированием новых фиброзных очагов на месте старых.
Неоссифицируемая фиброма также имеет положительный прогноз, как правило, после операции остеокоррекции формирование очагов отмечается в редких случаях. Функция конечности полностью сохраняется, ортопедических нарушений ни у одного из прооперированных пациентов выявлено не было: оси, длина и геометрия костей остаются сохранными.
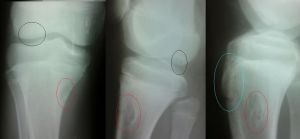
Доброкачественное образование костей и суставных хрящей.
Эпидемиология метафизарного фиброзного дефекта кости
Метафизарный фиброзный дефект кости обнаруживается почти исключительно в метафизах длинных трубчатых костей у детей и подростков при рентгенографии, выполненной часто без всяких предшествующих жалоб по разным поводам (травма или для сравнения при жалобах со стороны противоположного сустава).
Гистология и патогенез метафизарного фиброзного дефекта кости
Метафизарный фиброзный дефект кости (другие названия: фиброзный корковый дефект, неоссифицирующая фиброма, кортикальная лакуна) — явно неопухолевый дефект костной ткани. Такие новообразования встречаются очень часто, могут протекать бессимптомно и бывают случайной находкой при рентгенологическом исследовании. Морфологически эти очаги состоят из волокнистой соединительной ткани с фибробластами и рассеянными гигантскими клетками, в части случаев, особенно при длительно существующих очагах, содержат примесь ксантомных клеток.
Характер метафизарного фиброзного дефекта кости не соответствует представлениям об опухолях и позволяет рассматривать эти находки как очаговую перестройку костной ткани, начинающуюся с резорбции и завершающуюся ее воссозданием. Причина такой перестройки не выяснена. Метафизарный фиброзный дефект кости в 90% случаев возникает в метафизах длинных костей, чаще всего нижних конечностей. Они начинаются на периостальной поверхности и, увеличиваясь в размерах, смещаются интракортикально, а затем субкортикально, сохраняя эксцентрическое положение даже при значительных размерах. Только в более тонких костях (малоберцовой) они могут занимать весь поперечник.
В некоторых случаях очаги с такой гистологической картиной достигают больших размеров, продолжают увеличиваться при динамическом наблюдении. При этом они могут потребовать более активной тактики вплоть до хирургической резекции. Очаги с такими особенностями расценивают как опухоли — неоссифицирующие фибромы.
Противопоставление неоссифицирующих фибром как опухолей типичным МФД как неопухолевым поражениям нельзя считать оправданным, учитывая одинаковую гистологическую картину и тот факт, что во всех таких очагах может восстанавливаться нормальная костная структура.
Озлокачествление метафизарного фиброзного дефекта кости и неоссифицирующих фибром не описано.
Некоторые авторы выделяют фиброзную гистиоцитому, которая гистологически идентична неоссифицирующей фиброме.
Симптомы и лучевая диагностика метафизарного фиброзного дефекта кости
Как правило, МФД бессимптомны, представляют собой случайную рентгенологическую находку и чаще всего заживают без всякого лечения.
Фиброзные ксантомы костей, которые встречаются в несколько более позднем возрасте, чем МФД, вероятнее всего, представляют собой результат ксантоматозной трансформации не подвергшихся заживлению МФД с массивными скоплениями ксантомных пенистых клеток, в цитоплазме которых содержится много липидов.
Неоссифицирующие фибромы могут вызвать стойкую боль и привести к резкому истончению кортикального слоя, угрожая патологическим переломом.
Фиброзная гистиоцитома встречается у пациентов старше 20 лет и обычно сопровождается болью.
Чаще всего на рентгенограммах выявляется четко очерченный овальный или вытянутый в длину субкортикальный дефект костной ткани типичной локализации, с ровными или волнистыми очертаниями и склеротическим ободком. В более крупных очагах прослеживаются элементы ячеисто-трабекулярного рисунка. Изредка отмечается легкое вздутие кортикального слоя. Периостальная реакция отсутствует. Очаги могут появляться в нескольких типичных местах.
В редких случаях описано повторное появление МФД на месте ранее заживших. Более длительно существующие очаги могут отодвигаться в сторону диафиза и частично заполняться склерозированной костной тканью, оставляя после себя на некоторое время эностозы.
Рентгенологическая картина патогномонична. Обнаруженные метафизарные фиброзные дефекты кости подлежат динамическому наблюдению с интервалом не меньше 0,5 года. Хотя дополнительные методы визуализации обычно не требуются, возможно случайное выявление МФД при применении этих методов по другим показаниям. При остеосцинтиграфии может наблюдаться слабое накопление РФП. При МРТ-изображениях чаще всего отмечается сниженный на Т1- и Т2-взвешенном изображениях сигнал в очаге, обусловленный гемосидерином и фиброзной тканью, а отчасти также костеобразованием. Часто обнаруживаются участки жирового сигнала, а также кистозные очаги. Возможно образование вторичной АКК с горизонтальными уровнями. После контрастирования почти в 90% случаев отмечается интенсивное диффузное усиление сигнала, а в остальных случаях — усиление по краям септ.
Рентгенологическая картина в случаях фиброзной гистиоцитомы вариабельна и часто не позволяет отличить эту форму от неоссифицирующей фибромы, особенно при метафизарной локализации, как и от ряда других доброкачественных образований.
Заслуживает упоминания также редко встречающийся синдром Джеффи-Кампанаги — множественные фокальные кортикальные дисплазии (не менее 3) в сочетании с внескелетными изменениями, включая кожные пятна цвета кофе с молоком, умственную отсталость, гипогонадизм, изменения глаз и сердечно-сосудистые мальформации.
Что важно знать о кортикальном дефекте и фиброме кости у ребенка
- Фиброзный дефект кортикального слоя и неоссифицированная фиброма - наиболее частые поражения костей.
- Возрастной пик - 7-8 лет
- Частота 30% у детей и подростков
- Мальчики поражаются в 2 раза чаще, 3 чем девочки
- Обычно возникает до закрытия § зон роста
- Пенетрация кортикального слоя надкостницей
- Предрасположенность к развитию в длинных трубчатых костях
- При кортикальном дефекте поражение ограничено кортикальным слоем
- Неоссифицироеанная фиброма распространяется на костный мозг
- Гистология: веретеновидные клетки и гистиоциты, многоядерные гигантские клетки, сходные с остеокластами, лимфоциты, плазматические клетки
- Предрасположенность к поражению дистальных медиальных отделов малоберцовой кости, проксимальных отделов большеберцовой кости и малоберцовой кости, проксимальных отделов плеча.
Какой метод диагностики фибромы кости у детей выбрать: МРТ, КТ, рентген, УЗИ
- Кистозное поражение кости
- Обычно возникает как эксцентрическое поражение метафизов
- Легкий краевой склероз, иногда напоминающий морскую раковину
- Овальная форма
- Продольная ось опухоли параллельна продольной оси кости
- Истончение кортикального слоя
- Первоначально возникает в проксимальных закрытых зонах роста
- Типичные признаки злокачественного поражения отсутствуют
- Физиологический рост кости увеличивает расстояние между поражением и зоной роста, поражение становится более склерозированным (оссифицированная фиброма).
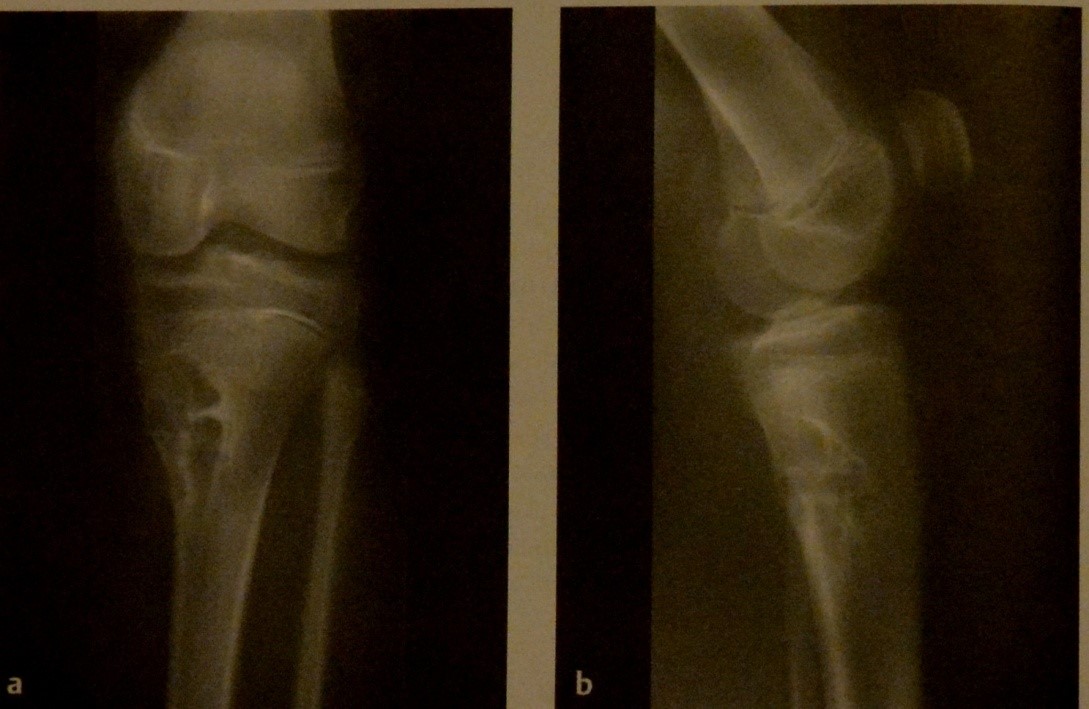
Неоссифицироеанная фиброма. Рентгенография колена в двух проекциях. Классический рентгенографический вид неоссифицированной фибромы в проксимальном заднемедиальном метафизе большеберцовой кости
- Четко ограниченный дефект кости
- Заполнен гипоэхогенным материалом
- Допплеровский режим выявляет выраженную васкуляризацию внутри поражения
- В динамике эхогенность поражения увеличивается, а размеры уменьшаются.
- Не требуется для подтверждения диагноза
- Обычно является случайной находкой
- Определяется изоинтенсивной по отношению к мышцам на Т1-взвешенных изображениях
- Гиперинтенсивное поражение на Т2-взве- шенных изображениях
- Т1- и Т2-взвешенные изображения визуализируют гипоинтенсивное кольцо краевого склероза
- Легкое контрастное усиление, особенно в краевой области
- Отсутствие периостальной реакции.
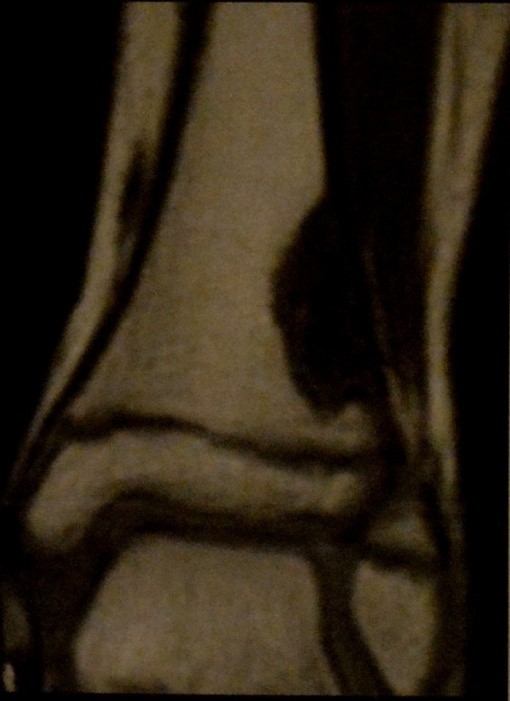
МРТ, неусиленное Т1 -взвешенное изображение. Неоссифицироеанная фиброма дистального бокового метафиза большеберцовой кости.
Клинические проявления
- Бессимптомное течение
- Обычно обнаруживается случайно
- Крупные поражения могут приводить к патологическим переломам.
Тактика лечения
- Выскабливание и имплантация решетчатого трансплантата показаны, если поражение занимает более 50% поперечного сечения полости костного мозга.
Течение и прогноз
- Большинство поражений спонтанно исчезают путем окостенения в течение 2-4 лет
- Может наблюдаться дальнейший рост
- Поражения не рецидивируют после хирургического удаления.
Осложнения
- патологические переломы.
Какие заболевания имеют симптомы, схожие с фиброзом кости у детей
Доброкачественная фиброзная гистиоцитома
- обычно возникает в возрасте до 25 лет;
- может вызывать боли;
- может рецидивировать после кюретажа;
- рентгенологически не различимы.
Периостальный десмоид
- первично возникает в возрасте 12-20 лет;
- предрасположенность к поражению задней части медиальной лодыжки малоберцовой кости;
- сходен с фиброзным кортикальным дефектом;
- может проявлять признаки злокачественного процес-
- обычно спонтанно исчезает;
Фиброзная дисплазия
- поражение одной или нескольких костей;
- предрасположенность к поражению бедра, болыпеберцевой кости и ребер;
- образуется от центра кости;
- возникает при таких состояниях, как синдром Мак-Кьюна-Олбрайта.
Советы и ошибки
- Заживление неоссифицированной фибромы можно ошибочно принять за остеосклеротический злокачественный процесс кости
- МРТ и КТ не показаны для оценки фиброзного кортикального дефекта
- Биопсия фиброзного кортикального дефекта противопоказана.
Аннотация научной статьи по клинической медицине, автор научной работы — Чигвария Николай Георгиевич, Поздеев Александр Павлович, Бергалиев Артур Нуралиевич
В статье отражены результаты комплексного обследования и лечения 158 детей и подростков с метафизарными фиброзными дефектами (МФД) и неоссифицирующимися фибромами (НФ) скелета, обращавшихся за специализированной медицинской помощью в клинику Научно-исследовательского детского ортопедического института имени Г. И. Турнера в период с 1980 по 2013 г. Определены диагностическая ценность и критерии идентификации очагов поражения при использовании рентгенологического, компьютерно-томографического и радионуклидного методов исследования. Сделан акцент на динамическую вариабельность клинико-рентгенологических проявлений лежащего в основе МФД и НФ патологического процесса и связанные с этим трудности диагностики , обозначены четкие показания к консервативному и хирургическому лечению .
Похожие темы научных работ по клинической медицине , автор научной работы — Чигвария Николай Георгиевич, Поздеев Александр Павлович, Бергалиев Артур Нуралиевич
METAPHYSEAL FIBROUS DEFECTS AND NONOSSIFYING BONE FIBROMA IN CHILDREN: CLINICAL TYPES AND TREATMENT
The paper presents the results of a comprehensive examination and treatment of 158 children and adolescents with nonossifying bone fibroma and skeleton, who referred for specialized medical aid in clinic of Scientific and Research Institute for Children''s Orthopedics n. a. G. I. Turner from 1980 to 2013. We defined diagnostic value and the criteria for identifying lesions using X-ray, computed tomography and radionuclide methods. We emphasized the dynamic variability of clinical and radiological manifestations of the pathological process in nonossifying bone fibroma and skeleton and related difficulties in the diagnosis . Accurate indications for the conservative and surgical treatment were pointed out.
МЕТАФИЗАРНЫЕ ФИБРОЗНЫЕ ДЕФЕКТЫ И НЕОССИФИЦИРУЮЩИЕСЯ ФИБРОМЫ КОСТЕЙ У ДЕТЕЙ: ВАРИАНТЫ ТЕЧЕНИЯ, ЛЕЧЕНИЕ
■ Резюме. В статье отражены результаты комплексного обследования и лечения 158 детей и подростков с метафизарными фиброзными дефектами (МФД) и неоссифицирующимися фибромами (НФ) скелета, обращавшихся за специализированной медицинской помощью в клинику Научно-исследовательского детского ортопедического института имени Г. И. Турнера в период с 1980 по 2013 г. Определены диагностическая ценность и критерии идентификации очагов поражения при использовании рентгенологического, компьютерно-томографического и радионуклидного методов исследования. Сделан акцент на динамическую вариабельность клинико-рентгенологических проявлений лежащего в основе МФД и НФ патологического процесса и связанные с этим трудности диагностики, обозначены четкие показания к консервативному и хирургическому лечению.
■ Ключевые слова: метафизарный фиброзный дефект, неоссифицирующаяся фиброма, диагностика, варианты течения, лечение.
Метафизарный фиброзный дефект и неоссифицирующаяся фиброма относятся к одним из наиболее часто встречающихся опухолеподобных поражений скелета в детском возрасте и, по данным ряда авторов, выявляются у трети обследованных детей и подростков [6, 7, 18, 19]. Из представленного к международной классификации костных опухолей комментария [10, 17] следует, что оба термина с позиций гистопатологии могут рассматриваться как синонимы, учитывая идентичность патоморфологической картины в обоих случаях. Наряду с этим, в клинической практике уже с середины прошлого столетия костные очаги, имеющие характерную рентгенологическую картину и располагающиеся в кортикальном слое грубчатой кости, расцениваются как МФД (синоним: фиброзный кортикальный дефект), а в случае распространения патологической ткани на губчатое вещество метафиза или в костномозговую полость предпочитают говорить о НФ (синонимы: неостеогенная фиброма, гистиоцитарная фиброма) [7, 9, 11, 13].
В клинической практике актуальность проблемы определяется нередкими диагностическими ошибками [2, 4, 6, 7, 11, 14, 16], обусловленными отсутствием систематизированных данных о возможных вариантах течения патологического процесса и связанной с этим неоправданной
лечебной тактикой, в частности расширением по казаний к оперативному лечению.
Цель исследования: выработать дифференци рованную лечебную тактику у детей с МФД и НФ скелета с учетом особенностей течения лежащего в их основе патологического процесса.
Материал и методы
Проведен анализ результатов обследования и лечения 158 детей и подростков с МФД (95 па циентов) и НФ (63 пациента) скелета, обращав
Результаты исследования и их обсуждение
Анализ клинического материала показал, что с жалобами за медицинской помощью обратились только 33 пациента с МФД и НФ, что составило 20,9 % от всей группы наблюдения. В порядке убывающей частоты предъявляемые жалобы распределились следующим образом: 22 пациентов (13,9 %) беспокоили повышенная утомляемость и чувство дискомфорта в пораженной конечности во время и после физических нагрузок, 9 (5,7 %) — боль, усиливающаяся при физических нагрузках, 2 (1,3 %) — локальная припухлость в проекции расположения костного очага.
Большая часть пациентов — 125 человек (79,1 %) — не предъявляла каких-либо жалоб. В этих случаях обнаружение МФД и НФ было связано с прицельным рентгенологическим обследованием скелета ребенка, выполненным либо по причине травматического повреждения конечности, в том числе патологического перелома трубчатой кости, либо в связи с заболеванием опорно-двигательного аппарата.
По результатам анализа собственного материала в возрасте от 0 до 3 лет пациентов с МФД и НФ не зарегистрировано. Самому младшему пациенту с МФД на момент его выявления было 4 года 11 мес., самому старшему — 17 лет 5 мес. В большинстве случаев (74,7 %) МФД впервые выявлены в препубертатный (35,8 %) и пубертатный
Рис. 1. Локализация и количество выявленных МФД: всего пациентов — 95, всего очагов — 155, верхние конечности — 4 (2,5 %), нижние конечности — 151 (97,5 %),
бедренная кость (дистальный метадиафиз) — 62 (40,0 %), большеберцовая кость (проксимальный метадиафиз) — 60 (38,7 %), большеберцовая кость (дистальный метадиафиз) — 13 (8,4 %), малоберцовая кость (проксимальный метадиафиз) — 11 (7,2 %), малоберцовая кость (дистальный метадиафиз) — 5 (3,2 %), плечевая кость (проксимальный метадиафиз) — 3 (1,9 %), лучевая кость (дистальный метадиафиз) — 1 (0,6 %)_
(38,9 %) возрастные периоды, на которые пришлось и преобладающее количество впервые за регистрированных больных с НФ скелета (68,3 %)
Локальных проявлений патологического процесса у детей с МФД выявлено не было, они зафиксированы только в группе пациентов с НФ Наиболее частыми из них были определяемое визуально и при пальпации безболезненное опу холевидное образование в проекции расположе ния костного очага, преимущественно у детей астенической конституции на участках со слабо-выраженным слоем покровных мягких тканей в частности по переднемедиальной поверхности проксимального отдела голени. Хромота, укорочение и гипотрофия мышц пораженной конечно-^ сти зафиксированы всего лишь у одного ребенка 13 мм с множественными НФ костей голени.
Рентгенологический метод исследования являлся основным и в большинстве случаев един ственным диагностическим методом, позволя ющим при знании типичной рентгенсемиотики безошибочно распознать патологический про цесс. Сведения о пораженных трубчатых костях и количестве выявленных МФД и НФ представлены на рис. 1 и 2, на которых видно, что в группе из 95 детей и подростков с МФД зафиксиро вано 155 типичных костных очагов, а в группе из 63 больных с НФ — 70 очагов поражения
Это объясняется наличием множественных форм поражения скелета, при которых у одного пациента были выявлены два и более костных очага.
При рентгенологическом исследовании установлено, что типичным местом расположения МФД и НФ была область метафизов и метадиафи-зов длинных трубчатых костей, на уровне которых очаги поражения чаще всего располагались эксцен-
Рис. 2. Локализация и количество выявленных НФ: всего пациентов — 63, всего очагов — 70, верхние конечности — 5 (7,1 %), нижние конечности — 65 (92,9 %),
большеберцовая кость (дистальный метадиафиз) — 23 (32,9 %), большеберцовая кость (проксимальный метадиафиз) — 16 (22,9 %), бедренная кость (дистальный метадиафиз) — 14 (20,0 %), малоберцовая кость (дистальный метадиафиз) — 7 (10,0 %), малоберцовая кость (проксимальный метадиафиз) — 5 (7,1 %), лучевая кость (дистальный метадиафиз) — 3 (4,3 %), плечевая кость (проксимальный метадиафиз) — 1 (1,4 %), локтевая кость (дистальный метадиафиз) — 1 (1,4 %)
трично (рис. 3). Не выявлено ни одного случая, при котором бы патологический процесс распростра нялся на эпифиз трубчатой кости и практически всегда между хрящевой ростковой зоной и смежным краем костного очага определялся участок неизмененной костной ткани метафиза.
Рис. 4. Рентгенограммы левого коленного сустава в прямой и боковой проекциях пациента К. в возрасте 11 лет 10 мес. (а) и 13 лет (б). Диагноз: МФД проксимального метадиафиза левой большеберцовой кости. В течение 1 года 2 мес. расстояние от хрящевой зоны роста до смежной границы очага увеличилось в два раза
На рентгенограммах НФ чаще всего имели округлую, овальную или неправильно вытянутую форму. Аналогично выглядела и большая часть МФД, при этом основное различие сводилось лишь к размерам очагов поражения. Нередко эксцентрично расположенные МФД приобретали полосовидную или серповидную форму. В подавляющем числе наблюдений вертикальный размер МФД и НФ превалировал над их горизонтальным размером, и поэтому на рентгенограммах костные очаги выглядели вытянутыми соответственно продольной оси трубчатой кости.
Анализ рентгенограмм пациентов с МФД и НФ, выполненных в динамике, показал, что такие характеристики рентгенсемиотики, как контуры границ и внутренняя структура костных очагов, определяются в первую очередь продолжительностью существования патологического процесса.
Установлено, что у всех пациентов контуры границ МФД и НФ были достаточно четкими. Однако в случаях продолжающегося роста патологической ткани четкость границ определялась в основном контрастом между самим очагом и окружающей его костной тканью (рис. 12, а). По мере стабилизации процесса происходило склерозирование приграничного контура, интенсивность которого со временем нарастала. При этом контур границы из относительно пологого становился полициклическим, фестончатым (рис. 12, б).
Во всех наблюдениях окружающая патологический очаг губчатая костная ткань метафиза сохра няла нормальную рентгенологическую структуру. Состояние смежных с очагом отделов кортикаль ного слоя трубчатой кости служило своеобразным индикатором активности патологического процесса. Подтверждением выраженности послед него было резкое истончение и выбухание прилежащего кортикального слоя кости.
Реакция надкостницы при рентгенологическом исследовании выявлена только в случаях па тологического перелома или микроперелома. Она носила характер линейного периостита. В осталь ных наблюдениях надкостница в зоне патологиче ского очага оставалась интактной.
Компьютерная томография является един ственным диагностическим методом, который позволяет получить максимально достоверную информацию о степени поражения поперечника трубчатой кости и, соответственно, четко с пози ций врача-клинициста объективизировать представление о МФД и НФ. Исследование проведено 26 пациентам с МФД и НФ. Из них 14 были с со литарными костными очагами, а 12 — с множественной формой поражения скелета.
На основании анализа аксиальных срезов выявлены следующие варианты расположения пато логической ткани: субпериостальный (рис. 8, б) интракортикальный (рис. 6, б), субкортикальный с распространением на губчатое вещество мета физа и(или) в костномозговую полость (рис. 12, в)
Первые два варианта соответствовали представлению преимущественно о МФД, последний характеризовал НФ.
Метод компьютерной томографии позволил дать объективную оценку состояния смежной с патологическим очагом компактной кости и, соответственно, сделать вывод о прочностных характеристиках пораженного отдела. В этом отношении прослеживалась корреляция между данными компьютерной томографии и рентгенографии (рис. 5).
Определение относительной плотности содержимого очагов поражения показало, что значения данного параметра напрямую зависели от ана лизируемого участка аксиального среза. При об работке данных компьютерно-томографического исследования подтверждался мягкотканый харак тер основного субстрата патологического очага (см. рис. 5), а средняя величина показателя от носительной плотности ткани при МФД и НФ составила (М ± т) 64,8 ± 2,1 ед. Ни при среднем квадратическом отклонении (а) ± 9,5. Обнаруже-
Рис. 5. Рентгенограммы дистального отдела правого бедра в прямой и боковой проекциях (я) и компьютерные томограммы нижней трети обоих бедер (б, в, г, д) пациента Х., 17 лет. Диагноз: НФ дистального отдела правой бедренной кости. Представленные аксиальные срезы (б, в, г) и реконструкции изображения в режиме МРЯ (д^ демонстрируют нормальную толщину кортикального слоя на уровне очага поражения. На аксиальных срезах (б) и (в) отображены результаты измерения относительной плотности (Лу.) различных структур в единицах Ни патологической ткани (71,0 и 78,0 ед. Ни); содержимого костномозговой полости (41,0 ед. Ни), зоны оссифи-кации (328,0; 666,0; 1261,0 ед. Ни), компактной кости (1641,0 ед. Ни). Эти же срезы демонстрируют участок, на котором патологическая ткань непосредственно контактирует с содержимым костномозговой полости
ние участков с отрицательным значением относительной плотности являлось подтверждением процесса липидизации патологической ткани, обусловленного депонированием в ней нейтральных жиров. При спонтанной оссификации выявлялись зоны повышенной плотности, по значениям равной или превышающей плотность губчатой и компактной кости (см. рис. 5). Данные компью-герно-томографического исследования позволили установить, что наиболее выраженные признаки реактивного костеобразования отмечались на тех участках, где патологическая ткань граничила непосредственно с эндостальной поверхностью компактной кости (см. рис. 5).
С целью изучения состояния регионарного кровообращения, а также функциональной активности костной ткани в зоне расположения очага поражения использовалась двухфазная сцинти-графия скелета. В качестве радиофармпрепарата (РФП) использовался комплексон 99тТс-технефор. Всего по методике двухфазной остеосцинтигра-фии обследовано 39 детей и подростков в возрасте от 4 до 18 лет. Из них 25 (64,1 %) — с МФД, а 14 (35,9 %) — с НФ.
Результаты радионуклидного исследования пациентов с МФД и НФ скелета представлены в табл. 1.
Из таблицы видно, что в первую группу вошло 8 детей (20,5 %) без каких-либо изменений регионарного кровообращения и функциональной активности костной ткани в проекции расположения патологического очага (КОП и КОН составили 100,0 %, что соответствовало норме). Во вторую группу было включено 10 обследованных (25,6 %) с отсутствием локальных очагов гиперемии в фазу перфузии (КОП — 100,0 %), но с гиперфиксацией радиофармпрепарата (РФП) в проекции очага поражения в костную фазу исследования (КОН — 149,2 ± 7,6 %). Третью группу составил 21 пациент (53,9 %), у которых зафиксированы изменения как со стороны регионарного кровообращения пораженной конечности (КОП — 153,9 ± 9,7 %), так и со стороны функциональной активности костной ткани в проекции расположения патологического очага (КОН — 206,3 ± 17,3 %).
Показатели фиксации радиофармпрепарата у пациентов с МФД и НФ (М ± т ± о)
Читайте также:


