Дисплазия костного мозга сколько с ним живут
Миелодиспластическим синдромом называют группу гетерогенных клональных заболеваний крови, объединенных следующими признаками: неэффективный гемопоэз, периферическая цитопения, дисплазия в одном или более ростке кроветворения с высоким потенциалом трансформации в острый миелоидный лейкоз.
Недостаточное кроветворение проявляется анемией, повышенной кровоточивостью и подверженностью инфекциям. Миелодиспластический синдром (МДС) встречается у людей любого возраста, в том числе и детского, но в большей степени ему подвержены люди после 60 лет.
По МКБ-10 миелодиспластическим синдромам присваивается код D46.
Причины
Клетки крови синтезируются и созревают главным образом в костном мозге (этот процесс называется миелопоэзом, а ткань, в которой он происходит, называется миелоидной), затем, выполнив свою функцию и состарившись, уничтожаются селезенкой, а на их место приходят новые. При миелодиспластическом синдроме костный мозг теряет способность к воспроизводству клеток крови (всех – эритроцитов, лейкоцитов, тромбоцитов или только некоторых) в необходимом организму количестве, в кровь попадают незрелые клетки (бласты), в результате чего она хуже выполняет свои функции. Это проявляется характерной для МДС симптоматикой. Примерно в 30% случаев процесс миелопоэза становится со временем полностью бесконтрольным, количество бластных форм кровяных клеток увеличивается, вытесняя нормальные, зрелые клетки. Когда количество бластов в крови превышает 20% (ранее пороговым значением было 30%), ставится диагноз острого миелоидного лейкоза.
В зависимости от того, известна ли причина нарушения функции костного мозга, или нет, МДС делится на первичный, или идиопатический, и вторичный. Вторичный возникает в результате угнетения костномозговой функции после химиотерапевтического или лучевого воздействия. Такое воздействие обычно является частью противоопухолевой терапии, т. е. проводится по поводу какого-либо вида рака. В этом случае МДС можно рассматривать как осложнение.
Первичный, или идиопатический МДС возникает спонтанно, без какой-либо предшествующей патологии и по неизвестной причине. Возможно, предрасполагающим фактором является генетический, поскольку при некоторых видах синдрома обнаруживаются хромосомные изменения.
Факторами, способствующими развитию МДС, являются:
- курение;
- контакт с канцерогенными химическими веществами (пестициды, гербициды, бензол);
- воздействие ионизирующей радиации;
- пожилой возраст.
Формы заболевания
Как уже указывалось выше, МДС делится на два вида, первичный и вторичный.
Чаще встречается первичный МДС (около 80% всех случаев), большинство заболевших – пожилые люди (65-75 лет). Вторичным МДС также в основном страдают пожилые люди, по той причине, что и злокачественные опухоли, а значит, и их осложнения, у них встречаются чаще. Вторичный МДС хуже поддается терапии и связан с худшим прогнозом.
Кроме того, МДС делится на клинические типы в зависимости от типа бластных клеток, их количества и наличия хромосомных изменений, эта классификация предложена Всемирной Организацией Здравоохранения (ВОЗ). Согласно классификации ВОЗ, выделяют следующие формы МДС:
- рефрактерная (т. е. устойчивая к классической терапии) анемия;
- рефрактерная цитопения с мультилинейной дисплазией;
- МДС с изолированной делецией 5q;
- МДС неклассифицируемый;
- рефрактерная анемия с кольцевидными сидеробластами;
- Рефрактерная цитопения с мультилинейной дисплазией и кольцевыми сидеробластами;
- рефрактерная анемия с избытком бластов-1;
- рефрактерная анемия с избытком бластов-2.
Стадии заболевания
В протекании МДС выделяют три стадии, которые, однако, не всегда клинически четко отличаются между собой, различия определяются лабораторно. Это стадия анемии, стадия трансформации (промежуточная между анемией и острым лейкозом), и острый миелоидный лейкоз. Не все исследователи согласны с определением острого миелоидного лейкоза как стадии миелодиспластического синдрома, поскольку он относится к миелопролиферативным нарушениям (т. е. тем, которые характеризуются бесконтрольным клеточным ростом), тем самым не полностью соответствуя характеристикам МДС.
Симптомы
Основные симптомы МДС связаны с проявлениями анемии. Пациенты предъявляют жалобы на повышенную утомляемость, приступы головокружения, одышку при физической нагрузке, которая ранее переносилась легко. Анемия связана с нарушением продукции эритроцитов, следствием чего является низкий уровень гемоглобина в крови.
В некоторых случаях развивается геморрагический синдром, который характеризуется повышенной кровоточивостью. Пациент начинает замечать, что даже незначительные поверхностные повреждения вызывают длительно не останавливающееся кровотечение, может появиться кровоточивость десен, частые и спонтанные носовые кровотечения, петехии на коже и слизистых оболочках, а также множественные гематомы (синяки) либо без связи с какой-либо запоминающейся пациенту травмы, либо после незначительного ушиба или даже надавливания. Геморрагический синдром связан с нарушениями тромбоцитопоэза.
У больных с МДС также обнаруживается подверженность инфекционным болезням. Они часто болеют простудными заболеваниями, кожными бактериальными и грибковыми инфекциями. Такое состояние обусловлено нейтропенией (недостаточностью нейтрофилов).
Кроме того, признаками МДС могут быть:
- беспричинное повышение температуры, часто до высоких значений (38 °С и выше);
- снижение веса, уменьшение аппетита;
- гепатомегалия;
- спленомегалия;
- болевой синдром.
В ряде случаев МДС ничем себя не проявляет и обнаруживается случайно во время лабораторного исследования крови по другому поводу.
Диагностика
Основной метод диагностики МДС – лабораторный. При подозрении на миелодисплазию проводятся:
- Клинический анализ крови. При этом обнаруживается анемия (макроцитарная), ретикулоцитопения, лейкопения, нейтропения, при синдроме 5q – тромбоцитоз. Примерно у половины пациентов выявляется панцитопения.
- Биопсия костного мозга. Цитоз обычно в норме или увеличен, но примерно у 10% пациентов он снижен (гипопластический вариант МДС), есть признаки нарушенного гемопоэза одного или нескольких ростков кроветворения, может обнаруживаться повышенное содержание бластных форм, патологических сидеробластов (эритроциты, содержащие отложения железа). Для идентификации аномальных фенотипов проводят исследование иммунофенотипа костномозговых клеток, это позволяет проводить дифференциальную диагностику МДС и неклональных цитопений, что важно для прогноза.
- Цитогенетический анализ. У 40–70 % пациентов обнаруживаются клональные цитогенетические аномалии, особенно часто наблюдается делеция (моносомия) 7 хромосомы (7q), которая является прогностически неблагоприятной.
- Определение уровня железа и феритина в сыворотке. Уровни повышены.
- Определение эндогенного эриропоэтина (при Диагностика МДС проводится лабораторными методами
Для определения МДС разработаны специальные критерии, т. е. условия, при соблюдении которых ставится данный диагноз. Диагностические критерии следующие:
- 1-, 2- или 3-ростковыя периферическая (т. е. обнаруживаемая в периферической крови) цитопения;
- дисплазия: признаки нарушения гемопоэза не менее 10% клеток не менее одного кроветворного ростка;
- характерные цитогенетические изменения (наличие патологического клона).
Цитопения должна быть стабильной и наблюдаться в течение не менее шести месяцев, однако если обнаруживается специфический кариотип, или ей сопутствует дисплазия не менее двух ростков кроветворения, достаточно двух месяцев.
Для постановки диагноза должны быть исключены другие заболевания, сопровождающиеся клеточной дисплазией и цитопенией.
При выявлении цитопении без других признаков МДС диагностируют идиопатическую цитопению, значение которой не установлено; при выявлении дисплазии без цитопении – идиопатическую дисплазию, значение которой не установлено. При этом требуется постоянное наблюдение пациента с повторным исследованием костного мозга через 6 месяцев, поскольку оба этих диагноза способны прогрессировать до МДС и острого миелоидного лейкоза (или другого миелопролиферативного заболевания).
МДС дифференцируется со следующими заболеваниями:
- анемии (прежде всего, мегалобластическая, сидеробластическая и апластическая);
- острый миелоидный лейкоз;
- лейкопения с нейтропенией;
- первичная иммунная тромбоцитопения;
- клональный гемопоэз с неопределенным потенциалом;
- первичный миелофиброз;
- ВИЧ;
- тяжелая интоксикация различной этиологии.
Лечение
В 1997 году была разработана специальная шкала, называемая шкалой IPSS (International Scoring Prognostic System, Международная шкала оценки прогноза), разделяющая пациентов на группы риска. В соответствии с определенной группой риска выбирается лечебная тактика, и, что следует из названия, оценивается прогноз.
Баллы присваиваются с учетом трех факторов:
- количество бластных форм;
- количество пораженных кроветворных ростков;
- цитогенетическая категория.

Костный мозг — важный кроветворный орган, в котором происходят процессы образования, развития и созревания клеток крови, то есть осуществляется гемопоэз. Этот орган также принимает участие в иммунопоэзе — процессе созревания иммунокомпетентных клеток. У взрослого человека в костном мозге содержатся незрелые, недифференцированные и низкодифференцированные клетки – стволовые.

Цитопения — клиническое проявление патологий системы кроветворения. Симптоматика недуга определяется поражением определенной клеточной линии. У больных возникает слабость, утомляемость, бледность, головокружение, лихорадка, кровоточивость, кровоизлияния. Специфические признаки при этом отсутствуют. Диагностика патологии основывается на результатах гемограммы и гистологического исследования биоптата костного мозга. Лечение заключается в переливании основных компонентов крови, проведении химиотерапии, иммуносупрессивной терапии и пересадке костного мозга.

цитопения с нарушением созревания клеток крови по нескольким росткам
Эффективное лечение МДС – одна из самых сложных проблем современной медицины. Его проводят специалисты в области онкогематологии. Синдром в запущенных случаях приводит к онкологии. Но так происходит не всегда. Легкие формы недуга типа рефракционной анемии обычно не заканчиваются формированием рака. Недостаток клеток крови приводит к анемии, кровоточивости, сердечной дисфункции, увеличению риска развития инфекционных заболеваний. Прогноз МДС определяется особенностями течения патологического процесса, своевременностью диагностических и общетерапевтических мероприятий. Своевременная терапия – единственный реальный шанс сохранить и продлить жизнь больных.
Этиология и патогенез
Гемопоэз – процесс кроветворения, который заключается в образовании и созревании клеток крови. Он происходит непрерывно, что связано с коротким сроком жизни клеток: от нескольких дней до 3-4 месяцев. Ежедневно в живом организме синтезируется огромное количество новых кровяных телец из клеток-предшественников. В процессе миелопоэза образуются миелоидные клетки – эритроцитарные, лейкоцитарные и тромбоцитарные клеточные элементы. Под воздействием негативных экзогенных и эндогенных факторов в костном мозге происходят патологические изменения, возникает расстройство кроветворения.

Этиология и патогенез МДС в настоящее время полностью не изучены. Ученые установили факторы, провоцирующие развитие патологии:
- загрязнения окружающей среды,
- радиоактивное излучение,
- табакокурение,
- опасные и вредные производственные факторы,
- контакты с агрессивными веществами,
- длительное проведение иммуносупрессивной терапии,
- врожденные генетические заболевания.
Первичный или идиопатический синдром — недуг невыясненной этиологии, который развивается в 80% случаев у лиц в возрасте 60-65 лет.
Вторичный синдром обусловлен воздействием на организм химиотерапевтических препаратов или лучевой терапии. Эта форма обычно развивается у молодых людей, быстро прогрессирует, отличается высокой устойчивостью к лечению и максимальным риском развития острого лейкоза.
В костном мозге вырабатываются все клеточные элементы крови. Там они находятся в незрелом состоянии, то есть являются предшественниками зрелых форм. По мере необходимости каждая из них превращается в полноценные клетки и выполняет жизненно важные функции, от которых зависит процесс дыхания, гемостаз, иммунная защита. При МДС стволовые клетки погибают до выхода в кровяное русло и не достигают своей функциональной зрелости. Это приводит к дефициту нормальных клеточных форм в крови и нарушению их функций, связанному с клеточной дисплазией.
МДС часто называют тлеющей лейкемией или предлейкозом, обусловленном генной мутацией стволовых клеток. Клональная пролиферация эритроидных, миелоидных и мегакариоцитарных форм приводит к неэффективному гемопоэзу и панцитопении. В костном мозге и крови происходят характерные морфологические изменения, обусловленные аномальной клеточной продукцией. У больных увеличивается печень и селезенка. Нестабильность синдрома обусловлена тенденцией к переходу в острый миелобластный лейкоз.
Симптоматические проявления
МДС не имеет специфической симптоматики. Его клинические проявления определяются степенью тяжести и формой недуга.
![]()
Анемический синдром — постоянный и обязательный признак патологии. Для него характерны гиперхромия и макроцитоз. Большой размер эритроцитов и их интенсивное окрашивание, зависящее от повышенного содержания гемоглобина, – признаки анемии при МДС и остром лейкозе. При анемии больные быстро утомляются, плохо переносят физические нагрузки, жалуются на головокружение, одышку, боль в груди, костях и суставах, невозможность сосредоточится. Их кожа становится бледной, ухудшается аппетит, снижается вес и работоспособность, возникает нервозность, цефалгия, дрожь в теле, шум в ушах, сонливость, тахикардия, обмороки. Плохо переносят анемию престарелые больные, а также лица с сердечно-легочной патологией. У них могут развиться тяжелые последствия – стенокардия, инфаркт миокарда, аритмии.- Нейтропения характеризуется лихорадкой, снижением сопротивляемости организма к патогенным биологическим агентам, частым развитием инфекционных заболеваний бактериальной и вирусной этиологии. У больных повышается температура тела, потливость, возникает слабость, увеличиваются лимфоузлы. Сепсис и пневмония у таких пациентов часто заканчиваются летальным исходом.
- При тромбоцитопении кровоточат десна, появляются гематомы и петехии, часто течет кровь из носа, возникают длительные кровотечения после мелких хирургических вмешательств и различных инвазивных манипуляций. Возможно развитие внутренних кровотечений, меноррагий, кровоизлияний в головной мозг. Массивная потеря крови часто становится причиной смерти пациентов.
- У больных возникает лимфаденит, гепатомегалия, спленомегалия, специфическое поражение кожи — лейкемиды.
МДС долгое время может протекать бессимптомно или иметь стертое течение. Больные часто не обращают внимание на слабовыраженные клинические проявления и не посещают своевременно врача. Обычно МДС обнаруживают случайно во время проведения очередного медосмотра.
Диагностика
Диагноз МДС ставят после проведения лабораторного исследования периферической крови и гистологического исследования биоптата костного мозга. Специалисты изучают образ жизни больного, его анамнез, наличие профессиональных вредностей.

наиболее достоверный диагностический метод – трепанбиопсия костного мозга
Диагностические методы при МДС:
- гемограмма — анемия, лейкопения, нейтропения, моноцитоз; панцитопения – абсолютное показание для цитологического исследования костного мозга;
- биохимия крови – определение уровня железа, фолиевой кислоты, эритропоэтина, ЛДГ и АСТ, АЛТ, щелочной фосфатазы, мочевины;
- иммунограмма – специальный комплексный анализ, позволяющий определить, в каком состоянии находится иммунная система;
- гистология костного мозга выявляет деструкцию ткани, очаги поражения, наличие аномальных клеток, дисбаланс кроветворной и жировой ткани, гиперплазию всех ростков кроветворения, признаки дисплазии клеток;
![]()
- цитохимическое исследование – нарушение обмена микроэлементов и витаминов: щелочной фосфатазы в лейкоцитах, миелопероксидазы, железа;
- цитогенетический анализ – выявление хромосомных аномалий;
- дополнительные инструментальные исследования, позволяющие оценить состояние внутренних органов — УЗИ, КТ и МРТ.
Только после полноценной диагностики и постановки правильного диагноза можно переходить к лечению недуга.
Лечение
Интенсивное лечение МДС заключается в применении целого комплекса мероприятий. В тяжелых случаях медикаментозную терапию проводят в условиях стационара. Больные с более легкими формами синдрома лечатся амбулаторно или на дневном стационаре. Основными среди общетерапевтических мероприятий являются химиотерапия и иммуносупрессивные методики. Трансплантация костного мозга проводится при тяжелом течении болезни и повышает шансы больных на выздоровление.

Лечение МДС проводится с целю нормализации показателей периферической крови, устранения симптомов патологии, предупреждения трансформации недуга в острый лейкоз, улучшения и продления жизни больных.
Симптоматическая терапия направлена на устранение клинических проявлений синдрома и сопутствующих заболеваний, осложняющих течение основного недуга.
Схема лечения и дозировка препаратов зависят от возраста пациента, степени тяжести заболевания и общего состояния здоровья. Эффективность медикаментозной терапии достаточно низкая и непродолжительная. Единственный способ спасти больного — выполнить пересадку костного мозга. В тяжелых случаях также проводят трансплантацию стволовых клеток. Несмотря на свою эффективность, эти способы лечения имеют много недостатков: являются дорогостоящими, имеют высокую вероятность отторжения трансплантата, требуют дополнительной подготовки пациента к операции, вызывают трудности в поиске подходящего донора.
В настоящее время развитие генной инженерии и культивирование клеток крови достигли нового уровня. С их помощью процесс кроветворения можно регулировать. Специалисты определяют сколько клеток недовырабатывается индивидуально у каждого больного, а затем переходят непосредственно к лечению.
С помощью любого из вышеперечисленных методов можно добиться полной ремиссии синдрома.
Профилактика
Специфической профилактики синдрома не существует. Профилактические мероприятия, не допускающие ухудшения состояния больных и предупреждающие трансформацию синдрома в лейкоз:
- укрепление иммунитета,
- сбалансированное питание,
- поддержание гемоглобина на оптимальном уровне,
- частые прогулки на свежем воздухе,
- своевременное обращение к врачу при появлении первых признаков синдрома,
- периодическая сдача анализов и прохождение необходимых исследований,
- гигиена кожи,
- защита от контактов с химическими веществами,
- защита от радиации,
- ограничение активной физической нагрузки,
- своевременное лечение простудных и инфекционных заболеваний.
Прогноз
Прогноз МДС неоднозначный. Он зависит от тяжести патологии и своевременности лечения. Продолжительность жизни при легких формах синдрома составляет 15 лет, при наличии тяжелого течения недуга она не превышает 10 месяцев. При отсутствии или неэффективности лечения МДС трансформируется в острый лейкоз. Адекватная терапия обеспечивает максимальное продление жизни. Наблюдение за больными, имеющими стертую клиническую картину и относительно благоприятное течение недуга, осуществляют постоянно, даже в период стабильных показателей крови и костного мозга.
У пожилых людей синдром протекает особенно тяжело и плохо лечится. Это связано с наличием у них хронических заболеваний и подавлением иммунитета. Их организм не справляется, и процесс выздоровления затягивается.
Видео: базовая информация о миелодиспластическом синдроме
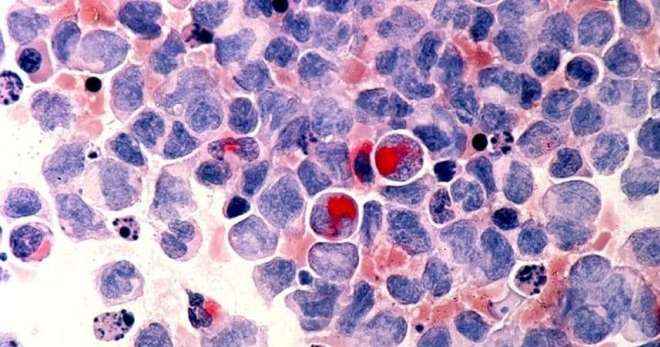
Миелодиспластический синдром – группа патологических состояний, сопровождающихся нарушением процесса кроветворения. Заболевание приводит к изменению основных форменных элементов крови. При отсутствии терапии существует высокий риск развития лейкоза (рака крови).
Миелодиспластический синдром – что это значит?
Миелодиспластический синдром, МДС – болезнь, сопровождающаяся нарушением кроветворения миелоидной ткани. При заболевании происходит нарушение выработки зрелых клеток крови, в результате чего возникает дефицит отдельных видов. Сами клетки крови подвергаются видоизменению, плохо функционируют. Длительное течение болезни приводит к возникновению острого миелоидного лейкоза.
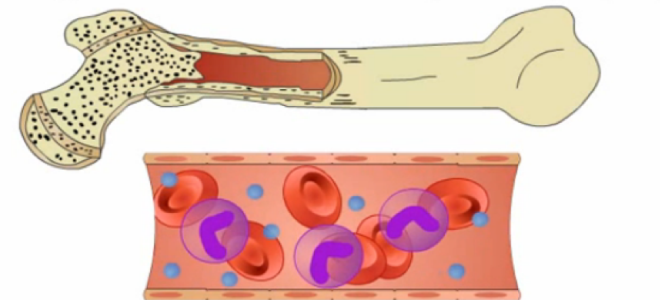
Миелодиспластический синдром – классификация
В зависимости от характера изменений, повреждаемого типа клеток различают следующие разновидности МДС:
- Миелодиспластический синдром, рефрактерная анемия – длится больше 6 месяцев. При проведении анализа крови фиксируются единичные бласты. В костном мозге обнаруживается дисплазия эритроидного ростка.
- Рефрактерная цитопения с многолинейной дисплазией – характеризуется наличием единичных бластов, фиксируются панцитопения, рост уровня моноцитов. В костном мозге изменениям подвержено меньше 10 % клеток.
- Миелодиспластический синдром с мультилинейной дисплазией – цитотпения, без увеличения бластных клеток.
- Неклассифицируемый миелодиспластический синдром – характеризуется цитопенией, наличием единичных бластов. Концентрация их не превышает 5 %.
- Миелодиспластический синдром с избытком бластов – цитопения без моноцитоза, без увеличения бластных клеток в периферической крови.
- Миелодиспластический синдром, ассоциированный с изолированной делецией 5q – форма, обусловленная нарушением генного аппарата. В анализе прослеживаются анемия, тромбоцитоз; концентрация бластов превышает 5 %. При цитогенетическом исследовании обнаруживается изолированная делеция 5q гена.
Причины миелодиспластического синдрома
Зачастую специалистам, диагностировавшим миелодиспластический синдром (МДС), не удается установить конкретную причину возникновения патологии. При этом они всегда стараются выявить первопричину болезни. В зависимости от этого фактора принято выделять две формы миелодиспластического синдрома:
- Идиопатический (первичный) – в большинстве случаев развивается без видимой причины, при отсутствии предпосылок.
- Вторичный – является результатом присутствия других патологий (лимфома, лимфогранулематоз). В отдельных случаях патология может провоцироваться проводимыми накануне лучевой или химиотерапией.
Проводимый онкологами ряд исследований доказал повышенную вероятность развития МДС у людей с генетическими аномалиями:
- синдромом Дауна;
- нейрофиброматозом;
- анемией Фанкони.
Диагноз МДС первичной формы составляет 80–90 % всех случаев миелодиспластического синдрома. Этот тип патологии чаще регистрируется у пациентов зрелого возраста, пожилых людей после 60 лет. Однозначно назвать причины развития патологии медикам не удается. Одновременно с этим они выделяют ряд факторов, повышающих риск развития МДС в разы. Среди таковых:
- курение;
- проживание в зонах с повышенным радиоактивным фоном;
- вредные условия труда (постоянный контакт с нефтепродуктами, ядохимикатами);
- врожденные патологии (болезнь Дауна, синдром Фанкони).
Вторичный МДС встречается в 10–20 % случаев заболевания. Возникает патология в любом возрасте. Частой причиной врачи называют побочный эффект от проводимой химиотерапии и радиоволнового лечения. Кроме того, спровоцировать изменения в картине крови способны некоторые лекарственные препараты:
- Циклофосфамид;
- ингибиторы топоизомеразы (Топотекан, Иринотекан).

Миелодиспластический синдром – симптомы
Симптомы и клиническая картина болезни напрямую зависят от степени нарушения, стадии патологического процесса. В некоторых случаях возможно практически бессимптомное течение. У таких пациентов только во время профилактического осмотра диагностируется миелодиспластический синдром, анемия как один из признаков заболевания крови. При этом пациенты жалуются на наличие неспецифических симптомов патологии:
- слабость;
- утомляемость;
- одышка при малейших нагрузках;
- побледнение кожных покровов;
- головокружения;
- обморочное состояние.
Когда миелодиспластический синдром сопровождается снижением концентрации тромбоцитов в кровяном русле, у пациентов могут фиксироваться периодические носовые кровотечения, обильная кровоточивость десен. Женщины могут отмечать появление меноррагии – обильных месячных. На поверхности кожных покровов появляются кровоподтеки. МДС с выраженным снижением нейтрофилов и агранулоцитозом сопровождается развитием частых простудных болезней, стоматитом. В тяжелых случаях у пациентов развивается пневмония.
Осложнения при миелодиспластическом синдроме
Нарушение работы системы кроветворения отрицательно сказывается на функционировании внутренних систем и органов. Снижение концентрации красных кровяных клеток провоцирует развитие кислородного голодания. В результате таких изменений первыми страдают нервная система и головной мозг. Однако главным из осложнений, которыми сопровождается миелодиспластический синдром, рефрактерная анемия с избытком бластов, является миелоидный лейкоз.
Патология характеризуется разрушением клеток крови, трудно поддается лечению, часто приводит к гибели пациентов. Выходом из ситуации является аллогенная трансплантация костного мозга. Среди других возможных осложнений МДС:
- тромбозы;
- анемия;
- инфекционные заболевания.
Миелодиспластический синдром – диагностика
Перед тем как выставить диагноз миелодиспластический синдром, анализ крови проводят неоднократно. Развернутое исследование помогает установить, какой непосредственно тип клеток подвергается патологическим изменениям. Эта информация используется для назначения курса терапии в дальнейшем. Комплексное обследование пациента должно включать:
- Исследование костного мозга – морфологическое обследование аспирата, трепанобиопсия с гистологией.
- Генетический тест для выявления возможных хромосомных мутаций (цитогенетический анализ).

Миелодиспластический синдром – лечение
Лечение миелодиспластического синдрома должно осуществляться комплексно. Тактика терапии определяется клинической картиной, симптоматикой, характером лабораторных показателей. При отсутствии признаков анемии, инфекционных патологий специалисты занимают выжидательную тактику. При МДС с выраженной анемией, нейтропенией и тромбоцитопенией, при повышенном риске лейкоза назначают сопроводительную терапию. В тяжелых случаях показана пересадка костного мозга.
При поздних формах болезни, выраженной клинике показан курс химиотерапии. Общепринятых стандартов данного типа лечения не существует. Специалисты активно занимаются разработкой новых лекарственных средств и препаратов. В отдельных случаях для остановки прогресса болезни, облегчения состояния пациента прибегают к иммуносупрессии.
Как лечить миелодиспластический синдром, какие препараты, в какой концентрации использовать – врачи определяют индивидуально.
- Сопроводительное лечение является самой распространенной методикой терапии МДС. Оно предусматривает частые инфузии компонентов крови.
- Длительное применение этой группы препаратов способно спровоцировать повышение концентрации железа в крови. Для исключения такой возможности назначают одновременно прием хелаторов, которые связывают железо и выводят его из организма.
- При терапии МДС с отсутствием хромосомных мутаций используют иммуносупрессоры. Они подавляют иммунитет, способствуют снижению воспалительного процесса.
- Невозможность трансплантации костного мозга является одним из показаний для проведения химиотерапии. Высокие дозировки этих препаратов используют, когда миелодиспластический синдром переходит в лейкоз или имеет место рефрактерная анемия (увеличение концентрации бластов при гиперклеточном костном мозге).
Лечение МДС включает в себя несколько направлений. В комплексной терапии заболевания зачастую применяется множество лекарственных средств. Среди основных препаратов:
- Иммуносупрессоры – помогают ликвидировать нарушения в иммунной системе, которые проявляются образованием аутоантител, развитием аутореактивных клонов Т-клеток. Представители этой группы: Циклоспорин, иммуноглобулин антитимоцитарный.
- Ингибиторы гиперметилирования – назначаются при МДС высокого риска, с большой концентрацией бластов: Децитабин, Азацитидин.
- Химиотерапия – применяется при повышенном риске перехода в лейкоз: Цитозар.
- Стимуляторы тромбопоэза – применяется при выраженном снижении концентрации тромбоцитов, различных кровотечениях: Ромиплостим, Лонифарниб, Типифарниб.
Лечение миелодиспластического синдрома народными средствами не приносит результатов. Заболевание трудно поддается медикаментозной терапии, поэтому врачи утверждают об отсутствии эффекта от использования лекарственных растений. Самостоятельный прием народных средств, отваров, настоек может отрицательно сказаться на состоянии здоровья пациента.
Миелодиспластический синдром – диета
Специальная диета при миелодиспластическом синдроме не предусмотрена. Врачи рекомендуют составлять свое меню, придерживаясь стола №15. Рацион должен обладать калорийностью 3000 ккал, объем жидкости должен составлять 1,5–2 л. Ежедневное меню должно содержать следующие продукты:
- отварные яйца;
- крупы, макаронные изделия;
- овощи и фрукты, зелень;
- пшеничные отруби;
- масло сливочное.
Миелодиспластический синдром – прогноз жизни
Предположительная продолжительность жизни при миелодиспластическом синдроме рассчитывается по разработанной системе WSS. При ее использовании учитывают три основных фактора, за каждый насчитывают 0–3 балла:
- кариотип (плохой, средний, хороший) – 0–2 балла;
- вид заболевания – 0–3 балла;
- необходимость проведения гемотрансфузии: присутствует – 1 балл, нет – 0 баллов.
Полученные показатели суммируются, и определяется группа риска. На основе нее строятся предположения относительно возможной продолжительности жизни:
- 0 баллов – 10–11 лет;
- 1 балл – 5 лет;
- 2 балла – 3–4 года;
- 3-4 балла – 1,5 года;
- 5-6 баллов – 8 месяцев.
Читайте также:




