Болезнь бехчета клинический случай
Болезнь Бехчета – редкое мультисистемное генетически детерминированное воспалительное заболевание из группы системных васкулитов, протекающих с поражением артерий и вен мелкого и среднего калибра [1, 2]. Болезнь впервые была описана в 1937 году турецким дерматологом Хулуси Бехчетом. Этиология заболевания неизвестна. Доказана ассоциация с антигенами HLA В51 [3] и DRw52 [2], в последнее время спектр генетических маркёров болезни Бехчета расширился. Показатели заболеваемости варьируют в зависимости от географического региона, так высокая распространённость болезни Бехчета регистрируется в странах Ближнего и Дальнего Востока, в Средиземноморье и регионах, относящихся к Великому шёлковому пути [4, 5]. Как правило, манифестация заболевания приходится на возраст 30 – 40 лет, крайне редко болезнь Бехчета возникает в детстве [6].
Международные критерии болезни Бехчета, предложенные в 2014 г. включают семь критериев, имеющих определённую балльную оценку. Таким критериям как афтозный стоматит, афтозное поражение гениталий и патология органа зрения присваивается по 2 балла, остальным признакам, включающим поражения кожи, вовлечение центральной нервной системы и сосудов, положительный тест патергии присваивается 1 балл за каждый признак. Диагностически значимым является сумма из 4-х и более баллов [7].
Для лечения болезни Бехчета применяют кортикостероиды, иммунодепрессанты, факторы-ингибиторы некроза опухолей и симптоматическое лечение.
Приводим наше наблюдение.
Пациентка В., 10 лет обратилась с жалобами на болезненные высыпания на слизистой оболочке полости рта, затрудняющие приём пищи и воды.
Заболела два года назад, когда на слизистой полости рта стали появляться глубокие длительно существующие язвочки, сопровождающиеся резкой болезненностью. Неоднократно обращалась к педиатру, дерматологу по месту жительства. Выставлялись диагнозы афтозный стоматит, кандидоз слизистой оболочки полости рта. Назначаемое лечение к улучшению не приводило. Дерматологом по месту жительства девочка была направлена в клинику Оренбургского государственного медицинского университета для установления диагноза.
При осмотре общее состояние девочки удовлетворительное. Кожный патологический процесс локализован на слизистой оболочке полости рта, где имеются 7 язвенных дефектов, диаметром от 0,3 до 0,6 см, дно которых покрыто сероватым налётом. Кожный покров и слизистая оболочка генитальной области свободны от высыпаний.
Выставлен предположительный диагноз болезнь Бехчета (рис 1).
Для подтверждения диагноза выполнен тест на патергию. После обработки кожи внутренней поверхности левого предплечья ватным тампоном, смоченным 70°С спиртом был выполнен укол стерильной иглой на глубину 5 мм. Оценка результата теста проведена через 48 часов. На месте укола имелась папула 1,5 мм, окружённая эритематозным венчиком (рис. 2).
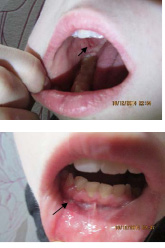
Рис. 1. Язвы на слизистой оболочке полости рта
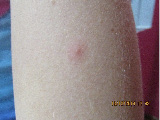
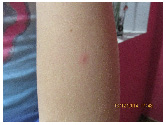
Рис. 2. Положительный тест на патергию (папула на внутренней поверхности правого предплечья)
Пациентка была осмотрена ревматологом, который также предположил болезнь Бехчета. Окулистом выставлен диагноз подострый иридоциклит и деструкция стекловидного тела левого глаза. Осмотр невролога патологических симптомов не выявил. Основываясь на современных диагностических критериях, общая сумма баллов у пациентки при оценке всех признаков составила 5 баллов, на основании чего был выставлен окончательный диагноз болезни Бехчета. Для дальнейшего обследования и лечения девочка была госпитализирована в детское ревматологическое отделение.
Описанный клинический случай представляет интерес как редко встречающаяся нозологическая форма с манифестацией в детском возрасте.
Анализ жалоб и объективных данных показал, что головные боли наблюдались у 86% больных, тошнота и рвота – у 57%. С одинаковой частотой наблюдались головокружение и психоэмоциональные расстройства – 71%. В меньшей степени были отмечены двигательные и когнитивные нарушения – 29 и 14% соответственно (рис. 2).
Средний возраст больных с неврологическими расстройствами составил 25,0±4,3 года.
Мы сочли необходимым определить время появления неврологических симптомов от момента начала болезни (рис. 3).
Сопоставление неврологических симптомов с системными проявлениями показало, что у большинства (65%) больных системные проявления (стоматит, увеит, узловатая эритема, язвенно-некротические поражения гениталий) опережали мозговые. У 10% больных неврологическая симптоматика отмечена в дебюте болезни, а у каждого четвертого больного (25%) неврологические и системные симптомы развивались одновременно (рис. 4).
Несмотря на тяжелые клинические проявления мозговой симптоматики у обследованных нами больных, глазные проявления наблюдались редко. Однако у одной больной наряду с тяжелым течением мозговых нарушений отмечалось одинаково тяжелое течение таких проявлений ББ, как язвенно-некротические повреждения слизистых полости рта, гениталий и кожи.
Всем больным (n=28) с установленным диагнозом ББ нами было проведено МРТ-исследование структур головного мозга. Результаты представлены на рисунке 5.
Объективно: больной заторможен, отмечаются бледность кожных покровов, лицо гиперемированно, в полости рта визуализируются единичные афты. Местами отмечаются папуло-пустулезные высыпания на коже живота, верхних и нижних конечностей (рис. 6). Суставы без особенностей. Со стороны внутренних органов без особых отклонений от нормы.
Данные дополнительных методов исследования
Клинический анализ крови: эритроциты – 4,5×1012/л, гемоглобин – 129 г/л, лейкоциты – 10×109/л (палочкоядерные нейтрофилы 6%, сегментоядерные 62%), тромбоциты – 141×109/л, СОЭ – 21 мм/ч.
Общий анализ мочи: без отклонений.
Биохимический анализ крови: общий белок – 68 г/л; холестерин – 4,6 ммоль/л; общий билирубин – 14,9 мкмоль/л (прямой – 4,4 мкмоль/л); тимоловая проба – 4,0 (тимол-вероналовая проба – 1,2; йодная проба – отрицательная, формоловая проба – слабоположительная); мочевина – 7,0 ммоль/л; креатинин – 82 мкмоль/л; К+ – 4,2 ммоль/л; Ca2+ – 144 ммоль/л; АЛТ – 57 Ед/л; АСТ – 45 Ед/л; глюкоза – 5,2 ммоль/л; СРБ+++. Кровь на RW – отрицательно. Время свертывания крови по Сухареву: начало – 336 c, конец – 551 c. Протромбиновый индекс – 98,7%, фибриноген плазмы – 2,75 г/л, время рекальцификации – 132 с, тромботест – 4.
ЭКГ: ритм синусовый, без отклонений от нормы.
УЗИ органов брюшной полости и почек: без отклонений.
МРТ головного мозга: инфаркт Варолиева моста (подострая стадия) (рис. 7). В области Варолиева моста слева визуализируется зона повышенного сигнала на Т2-ВИ и пониженного сигнала на Т1-ВИ 2,1×1,2×1,2 см. Перивентрикулярно и субкортикально с обеих сторон очаги высокого и повышенного сигнала на Т2-ВИ до 0,6 см, местами сливного характера, с наличием отека у задних рогов боковых желудочков. Желудочки мозга, субарахноидальное пространство умеренно расширены.
Рентгеноскопия органов грудной клетки: без отклонений.
Осмотр окулиста: без отклонений.
Осмотр невролога: болезнь Бехчета. Хроническая недостаточность мозгового кровообращения. Синдром демиелинизации мозга.
Лечение. Больному назначено: 1) комбинированная пульс-терапия метилпреднизолоном (в суммарной дозе 1500 мг) в сочетании с циклофосфаном (в дозе 600 мг) в/в капельно на физиологическом р-ре № 3; 2) НПВП (диклофенак 3,0 в/м № 7); 3) ипидакрин 10 мг в/м № 10; 3) варфарин 2,5 мг/сут. перорально № 10. По завершении пульс-терапии больной был переведен на пероральный прием метилпреднизолона 8 мг/сут и азатиоприна 150 мг/сут.
После проведенного лечения состояние больного значительно улучшилось до относительно удовлетворительного, сознание – ясное, температура тела 36,7–36,8° С; жалоб на головные, суставные боли и диспептические явления нет.
Больной выписан домой со следующими рекомендациями: 1) наблюдение у ревматолога и невролога по месту жительства; 2) метилпреднизолон 8 мг/сут; 3) азатиоприн 150 мг/сут.
Данный клинический случай демонстрирует позднюю диагностику ББ. Несмотря на наличие классических симптомов болезни в дебюте, диагноз ББ своевременно не был выставлен, не была назначена адекватная патогенетическая терапия. Это, в свою очередь, привело к развитию тяжелых проявлений ББ, обусловленных поражением центральной нервной системы.
Таким образом, возникает необходимость развития междисциплинарного подхода практических врачей к выявлению ранних симптомов ББ и совместному ведению этой категории больных.
![]()
Системный васкулит, впервые описанный Хулуси Бехчетом, турецким дерматологом, или же синдром Бехчета, наиболее часто встречается в Турции, Израиле, странах Средиземноморья, Восточной Азии (больше всего случаев фиксируется в Южной Корее и Японии). Он может вызывать поражения кожи и слизистых оболочек, увеит, обширное поражение артерий и вен, проявления со стороны желудочно-кишечного тракта и неврологические проявления. Симптомы могут комбинироваться и проявляться у пациентов по-разному.
Этиология неизвестна. Изучение семейного анамнеза указывает на возможную генетическую предрасположенность. Усиленные воспалительные реакции и иммунные механизмы играют роль, однако до сих пор неизвестно, является болезнь аутоиммунной или же аутовоспалительной.
Аутовоспалительные заболевания — это группа наследственных заболеваний, которые характеризуются рецидивами системного воспаления при отсутствии явной аутоиммунной патологии, такой как высокий титр патогенетически значимых ауто-антител или антигенспецифических Т-лимфоцитов. В отличие от других аутоиммунных заболеваний, синдром Бехчета, как правило, связан с ауто-антителами, болезнью Рейно, тромбоцитопенией, гемолитической анемией, вовлечением серозных оболочек или повышенным риском прочих аутоиммунных заболеваний. Черты, которые отделяют его от аутовоспалительных заболеваний, включают склонность ослабевать со временем, отсутствие мутаций, характерных для аутовоспалительных заболеваний, а также более высокая распространенность, чем у аутовоспалительных болезней, таких как семейная средиземноморская лихорадка. Может вовлекаться как врожденный, так и приобретенный иммунитет.
Патогенез неизвестен. Присутствует нейтрофильная гиперактивность, однако непонятно, является ли это состояние первичным или вторичным к цитокин-обусловленной активации. Также на основании ретроспективных групповых исследований были найдены определенные доказательства, что существуют различные типы презентации болезни, и каждый тип может иметь свой патогенез.
Диагностика основывается на определенных клинических критериях: у пациентов практически всегда наблюдаются рецидивирующие язвы и 2 других клинических проявления (повторяющиеся генитальные язвы, кожные поражения, поражения глаз, положительный тест патергии).
Дополнительные клинические проявления могут вовлекать разные системы органов, включая глаза, ЖКТ, сосудистую систему, легкие и ЦНС. Историю пациента стоит изучать с особым вниманием к наличию подобных состояний в семейном анамнезе. Лабораторные исследования бесполезны для диагностирования синдрома Бехчета, однако они играют роль в исключении альтернативных диагнозов или оценки осложнений после синдрома Бехчета, таких, как нарушения со стороны сосудов и ЦНС.
-
Многие пациенты сообщают о повторных язвах; афтозные язвы являются наиболее распространенным типом. Генитальные язвы могут быть болезненными и обычно встречаются на мошонке или малых половых губах. Большие язвы при заживании могут образовывать шрамы, в особенности язвы на мошонке. Кожные поражения могут быть папулезно-пустулезными или узловыми. Угревидные поражения похожи на обычное акне, однако могут возникать в нетипичных местах (на руках и ногах). Более чем у половины пациентов наблюдаются узловые эритемы; в отличие от обычных, при поражениях, обусловленных синдроме Бехчета эритемы могут переходить в язвы. Поверхностный тромбофлебит может быть по ошибке принят за узловую эритему.
-
Производится путем подкожной инъекции стерильной иглой, после чего выжидается 48 часов, чтобы увидеть, не образовались ли в месте укола папулезные или пустулезные формы. В Турции точность теста патергии составляет >60%, однако в США
Патергия
-
Примерно у половины пациентов наблюдается увеит. Более остро проявляется у мужчин. Гипопион, оседание гноя в передней камере глазного яблока, наблюдается у 20% пациентов и является маркером острого воспаления.
-
Наиболее часто встречается в Восточной Азии; около трети пациентов сталкиваются с реакциями со стороны ЖКТ. Диарея, спастическая боль в животе и изъязвление слизистых оболочек.
-
Редко. Возможные варианты включают тромбофлебит, глубокий венозный тромбоз, тромбоз синусов твёрдой мозговой оболочки и развитие аневризмы. Аневризмы могут быть состоянием, которое угрожает жизни человека, в особенности в легочной сосудистой системе; кровохарканье будет характерным признаком.
-
Наиболее часто встречается ослабление памяти. Могут наблюдаться нарушения речи, пространственной ориентации или движений.
-
Чаще всего поражаются колени; маленькие суставы также могут вовлекаться, но как правило болезнь нацелена на крупные суставы.
Для самого синдрома не существует специфических лабораторных тестов. Анализы могут быть полезными для дифференциальной диагностики.
-
Ревматоидный фактор, антиядерные антитела и антинейтрофильные цитоплазматические антитела как правило негативны при синдроме Бехчета. СОЭ и СРБ могут быть немного повышены, однако эти находки не являются специфичными и бесполезны для диагностики. HLA-B51 может быть положительным. Эта связь зависит от этнической принадлежности, и несмотря на то, что порой наблюдается у здоровых пациентов, она более характерна для пациентов с синдромом Бехчета, в особенности среди людей из стран Средиземноморья и Азии. Может указывать на тяжесть болезни, однако, это до сих пор не подтверждено. У пациентов с симптомами со стороны ЖКТ Антитела к сахаромицетам, иммуноглобулины класса IgA могут быть повышены, однако требуются дальнейшие исследования.
При синдроме Бехчета единственным симптомом, который указывает на легочные аневризмы, может быть кровохаркание. Рекомендуется КТ грудной клетки с высоким разрешением. КТ-ангиография и инвазивная ангиография являются альтернативными методами, если КТ грудной клетки не подтверждает диагноз. КТ с высоким разрешением или КТ-ангиография, выбранные в зависимости от наличия и квалификации специалистов, используются для сканирования на наличие легочных аневризм у пациентов с тромбофлебитом или другими аневризмами (напр.,в полой вене, печеночной вене).
Признаки того, что болезнь затронула глаза, могут включать: боль в глазах, затуманенность зрения, светобоязнь, краснота или слезоточивость; однако, задний увеит может проявляться минимальными симптомами. При любых изменениях зрения или симптомах со стороны глаз требуется консультация офтальмолога для того, чтобы определить тип их поражения, такой как увеит.
У пациента наблюдаются рекуррентные язвы в ротовой полости и 2 из нижеуказанных проявлений, в отсутствие других симптоматических заболеваний.
-
Рекуррентное генитальное афтозное изъязвление или образование шрамов фиксируется врачом или же о нем сообщает сам пациент. Врач наблюдает кожные поражения (включая поражения, напоминающие узловую эритему, псевдофолликулит, папуллезно-пустулезные поражения или угревидные узлы) у пациента пост-пубертатного возраста, не получающего кортикостероиды. Офтальмолог наблюдает поражение глаз с передним/задним увеитом или ретинитом. Тест патергии дает положительный результат; врач под углом вводит ≤21G стерильную иглу и осматривает результат спустя 48 часов.
Лечение зависит от типа и тяжести поражения; основная цель — предотвратить долгосрочные поражения. Большинство новых поражений проявляются в течение первых 5 лет после появления симптомов, и у большинства пациентов болезнь характеризуется затуханием симптомов, после чего следует внезапная ремиссия.
Наиболее острые проявления болезни должны определить выбор лечения, вне зависимости от наличия менее острых проявлений.
При легких симптомах, топическая терапия с использованием кортикостероидов (напр., пасты с триамцинолоном) как правило является достаточной. Повреждения, устойчивые к местному лечению, могут потребовать системного лечения колхицином, пероральным кортикостероидом, другим иммуносупрессором (например, азатиоприном, гидроксихлорохином, талидомидом, апремиластом) или ингибитором фактора некроза опухоли альфа (ФНО) (например, инфликсимабом, этанерцептом). Контрольный анализ по итогам предыдущих клинических исследований подтвердил, что использование колхицина не снижало потребности в последующем использовании иммуносупрессоров.
Поражение глаз требует неотложного и агрессивного лечения коротким курсом кортикостероидов, а также продолжительным курсом иммуносупрессантов. У большинства пациентов кортикостероиды можно отменить после того, как прошла активная фаза болезни, в то время как курс иммуносупрессантов, как правило, рассчитан на 1 год.
Пациентам с увеитом диагностику и лечение должен проводить офтальмолог. Этому типу пациентов требуется неотложное и агрессивное лечение иммуносупрессорами. Наиболее распространенной схемой лечения является азатиоприн плюс кортикостероид. Для контроля активности болезни можно использовать циклоспорин или ингибитор ФНО-альфа (например, инфликсимаб), также в сочетании с системными кортикостероидами и азатиоприном. Еще одним вариантом является монотерапия интерфероном (например, пегинтерферон альфа 2b). Кортикостероиды никогда не должны использоваться в качестве монотерапии, их всегда следует применять в комбинации с системным иммуносупрессором.
Симптомы со стороны ЦНС и кровеносных сосудов требуют самого агрессивного типа терапии с использованием интенсивной иммуносупрессии и кортикостероида, а также либо азатиоприна, циклофосфамида или ингибитора ФНО-альфа (например, инфликсимаб). Однако не существует контролируемых исследований, на которые можно было бы опираться для корректирования терапии. Продолжительность лечения может быть меньше, чем при более тяжелых проявлениях.
Профилактику тромбоза вен при синдроме Бехчета проводят путем контроля системного воспаления с помощью иммуносупрессоров, а не за счет использования антикоагулянтов. Однако если тромбоз вен все же наблюдается, можно назначить пациенту стандартную антикоагулянтную терапию (как правило, варфарин), при условии низкого риска кровотечения и отсутствия сосуществующих аневризм легочной артерии. Тромболитическую терапию используют редко, однако она может потребоваться некоторым пациентам. Использования циклоспорина следует избегать у пациентов с вовлечением нервной системы, даже если заболевание не активно.
Вовлечение желудочно-кишечного тракта следует правильно диагностировать, чтобы избежать ненужного использования иммуносупрессоров. Лечение кортикостероидом в сочетании с иммуносупрессором, таким как азатиоприн или инфликсимаб.
![]()
Системный васкулит, впервые описанный Хулуси Бехчетом, турецким дерматологом, или же синдром Бехчета, наиболее часто встречается в Турции, Израиле, странах Средиземноморья, Восточной Азии (больше всего случаев фиксируется в Южной Корее и Японии). Он может вызывать поражения кожи и слизистых оболочек, увеит, обширное поражение артерий и вен, проявления со стороны желудочно-кишечного тракта и неврологические проявления. Симптомы могут комбинироваться и проявляться у пациентов по-разному.
Этиология неизвестна. Изучение семейного анамнеза указывает на возможную генетическую предрасположенность. Усиленные воспалительные реакции и иммунные механизмы играют роль, однако до сих пор неизвестно, является болезнь аутоиммунной или же аутовоспалительной.
Аутовоспалительные заболевания — это группа наследственных заболеваний, которые характеризуются рецидивами системного воспаления при отсутствии явной аутоиммунной патологии, такой как высокий титр патогенетически значимых ауто-антител или антигенспецифических Т-лимфоцитов. В отличие от других аутоиммунных заболеваний, синдром Бехчета, как правило, связан с ауто-антителами, болезнью Рейно, тромбоцитопенией, гемолитической анемией, вовлечением серозных оболочек или повышенным риском прочих аутоиммунных заболеваний. Черты, которые отделяют его от аутовоспалительных заболеваний, включают склонность ослабевать со временем, отсутствие мутаций, характерных для аутовоспалительных заболеваний, а также более высокая распространенность, чем у аутовоспалительных болезней, таких как семейная средиземноморская лихорадка. Может вовлекаться как врожденный, так и приобретенный иммунитет.
Патогенез неизвестен. Присутствует нейтрофильная гиперактивность, однако непонятно, является ли это состояние первичным или вторичным к цитокин-обусловленной активации. Также на основании ретроспективных групповых исследований были найдены определенные доказательства, что существуют различные типы презентации болезни, и каждый тип может иметь свой патогенез.
Диагностика основывается на определенных клинических критериях: у пациентов практически всегда наблюдаются рецидивирующие язвы и 2 других клинических проявления (повторяющиеся генитальные язвы, кожные поражения, поражения глаз, положительный тест патергии).
Дополнительные клинические проявления могут вовлекать разные системы органов, включая глаза, ЖКТ, сосудистую систему, легкие и ЦНС. Историю пациента стоит изучать с особым вниманием к наличию подобных состояний в семейном анамнезе. Лабораторные исследования бесполезны для диагностирования синдрома Бехчета, однако они играют роль в исключении альтернативных диагнозов или оценки осложнений после синдрома Бехчета, таких, как нарушения со стороны сосудов и ЦНС.
-
Многие пациенты сообщают о повторных язвах; афтозные язвы являются наиболее распространенным типом. Генитальные язвы могут быть болезненными и обычно встречаются на мошонке или малых половых губах. Большие язвы при заживании могут образовывать шрамы, в особенности язвы на мошонке. Кожные поражения могут быть папулезно-пустулезными или узловыми. Угревидные поражения похожи на обычное акне, однако могут возникать в нетипичных местах (на руках и ногах). Более чем у половины пациентов наблюдаются узловые эритемы; в отличие от обычных, при поражениях, обусловленных синдроме Бехчета эритемы могут переходить в язвы. Поверхностный тромбофлебит может быть по ошибке принят за узловую эритему.
-
Производится путем подкожной инъекции стерильной иглой, после чего выжидается 48 часов, чтобы увидеть, не образовались ли в месте укола папулезные или пустулезные формы. В Турции точность теста патергии составляет >60%, однако в США
Патергия
-
Примерно у половины пациентов наблюдается увеит. Более остро проявляется у мужчин. Гипопион, оседание гноя в передней камере глазного яблока, наблюдается у 20% пациентов и является маркером острого воспаления.
-
Наиболее часто встречается в Восточной Азии; около трети пациентов сталкиваются с реакциями со стороны ЖКТ. Диарея, спастическая боль в животе и изъязвление слизистых оболочек.
-
Редко. Возможные варианты включают тромбофлебит, глубокий венозный тромбоз, тромбоз синусов твёрдой мозговой оболочки и развитие аневризмы. Аневризмы могут быть состоянием, которое угрожает жизни человека, в особенности в легочной сосудистой системе; кровохарканье будет характерным признаком.
-
Наиболее часто встречается ослабление памяти. Могут наблюдаться нарушения речи, пространственной ориентации или движений.
-
Чаще всего поражаются колени; маленькие суставы также могут вовлекаться, но как правило болезнь нацелена на крупные суставы.
Для самого синдрома не существует специфических лабораторных тестов. Анализы могут быть полезными для дифференциальной диагностики.
-
Ревматоидный фактор, антиядерные антитела и антинейтрофильные цитоплазматические антитела как правило негативны при синдроме Бехчета. СОЭ и СРБ могут быть немного повышены, однако эти находки не являются специфичными и бесполезны для диагностики. HLA-B51 может быть положительным. Эта связь зависит от этнической принадлежности, и несмотря на то, что порой наблюдается у здоровых пациентов, она более характерна для пациентов с синдромом Бехчета, в особенности среди людей из стран Средиземноморья и Азии. Может указывать на тяжесть болезни, однако, это до сих пор не подтверждено. У пациентов с симптомами со стороны ЖКТ Антитела к сахаромицетам, иммуноглобулины класса IgA могут быть повышены, однако требуются дальнейшие исследования.
При синдроме Бехчета единственным симптомом, который указывает на легочные аневризмы, может быть кровохаркание. Рекомендуется КТ грудной клетки с высоким разрешением. КТ-ангиография и инвазивная ангиография являются альтернативными методами, если КТ грудной клетки не подтверждает диагноз. КТ с высоким разрешением или КТ-ангиография, выбранные в зависимости от наличия и квалификации специалистов, используются для сканирования на наличие легочных аневризм у пациентов с тромбофлебитом или другими аневризмами (напр.,в полой вене, печеночной вене).
Признаки того, что болезнь затронула глаза, могут включать: боль в глазах, затуманенность зрения, светобоязнь, краснота или слезоточивость; однако, задний увеит может проявляться минимальными симптомами. При любых изменениях зрения или симптомах со стороны глаз требуется консультация офтальмолога для того, чтобы определить тип их поражения, такой как увеит.
У пациента наблюдаются рекуррентные язвы в ротовой полости и 2 из нижеуказанных проявлений, в отсутствие других симптоматических заболеваний.
-
Рекуррентное генитальное афтозное изъязвление или образование шрамов фиксируется врачом или же о нем сообщает сам пациент. Врач наблюдает кожные поражения (включая поражения, напоминающие узловую эритему, псевдофолликулит, папуллезно-пустулезные поражения или угревидные узлы) у пациента пост-пубертатного возраста, не получающего кортикостероиды. Офтальмолог наблюдает поражение глаз с передним/задним увеитом или ретинитом. Тест патергии дает положительный результат; врач под углом вводит ≤21G стерильную иглу и осматривает результат спустя 48 часов.
Лечение зависит от типа и тяжести поражения; основная цель — предотвратить долгосрочные поражения. Большинство новых поражений проявляются в течение первых 5 лет после появления симптомов, и у большинства пациентов болезнь характеризуется затуханием симптомов, после чего следует внезапная ремиссия.
Наиболее острые проявления болезни должны определить выбор лечения, вне зависимости от наличия менее острых проявлений.
При легких симптомах, топическая терапия с использованием кортикостероидов (напр., пасты с триамцинолоном) как правило является достаточной. Повреждения, устойчивые к местному лечению, могут потребовать системного лечения колхицином, пероральным кортикостероидом, другим иммуносупрессором (например, азатиоприном, гидроксихлорохином, талидомидом, апремиластом) или ингибитором фактора некроза опухоли альфа (ФНО) (например, инфликсимабом, этанерцептом). Контрольный анализ по итогам предыдущих клинических исследований подтвердил, что использование колхицина не снижало потребности в последующем использовании иммуносупрессоров.
Поражение глаз требует неотложного и агрессивного лечения коротким курсом кортикостероидов, а также продолжительным курсом иммуносупрессантов. У большинства пациентов кортикостероиды можно отменить после того, как прошла активная фаза болезни, в то время как курс иммуносупрессантов, как правило, рассчитан на 1 год.
Пациентам с увеитом диагностику и лечение должен проводить офтальмолог. Этому типу пациентов требуется неотложное и агрессивное лечение иммуносупрессорами. Наиболее распространенной схемой лечения является азатиоприн плюс кортикостероид. Для контроля активности болезни можно использовать циклоспорин или ингибитор ФНО-альфа (например, инфликсимаб), также в сочетании с системными кортикостероидами и азатиоприном. Еще одним вариантом является монотерапия интерфероном (например, пегинтерферон альфа 2b). Кортикостероиды никогда не должны использоваться в качестве монотерапии, их всегда следует применять в комбинации с системным иммуносупрессором.
Симптомы со стороны ЦНС и кровеносных сосудов требуют самого агрессивного типа терапии с использованием интенсивной иммуносупрессии и кортикостероида, а также либо азатиоприна, циклофосфамида или ингибитора ФНО-альфа (например, инфликсимаб). Однако не существует контролируемых исследований, на которые можно было бы опираться для корректирования терапии. Продолжительность лечения может быть меньше, чем при более тяжелых проявлениях.
Профилактику тромбоза вен при синдроме Бехчета проводят путем контроля системного воспаления с помощью иммуносупрессоров, а не за счет использования антикоагулянтов. Однако если тромбоз вен все же наблюдается, можно назначить пациенту стандартную антикоагулянтную терапию (как правило, варфарин), при условии низкого риска кровотечения и отсутствия сосуществующих аневризм легочной артерии. Тромболитическую терапию используют редко, однако она может потребоваться некоторым пациентам. Использования циклоспорина следует избегать у пациентов с вовлечением нервной системы, даже если заболевание не активно.
Вовлечение желудочно-кишечного тракта следует правильно диагностировать, чтобы избежать ненужного использования иммуносупрессоров. Лечение кортикостероидом в сочетании с иммуносупрессором, таким как азатиоприн или инфликсимаб.
Читайте также:


