Болевой синдром при деформирующем артрозе
Артропатии чаще поражают костные сочленения нижних конечностей. Факторы, провоцирующие заболевание различны. Боли при артрозе являются основным признаком болезни. Резкие и интенсивные болевые проявления возникают не случайно. Им предшествует длительный дискомфорт при ходьбе, физических нагрузках. Именно постепенное нарастание болевых ощущений является главным признаком негативных изменений в суставных тканях.

Причины болей при артрозе
Артропатия начинается с нарушения местной гемодинамики в суставе. Мелкие сосуды теряют пропускную способность, результатом чего является нарушение трофики хряща. Он ссыхается — становится тоньше, уменьшается его эластичность. Потеря внутрисуставной жидкости приводит к уменьшению щели между костями сочленения. В результате этого костные образования механически взаимодействуют друг с другом, что провоцирует болезненность и характерный хруст. Со временем на костях появляются остеофиты, приводящие к боли в мышцах.
При артрозе болевые ощущения отличаются многообразием — скоротечные, интенсивные, постоянные, ноющие.
Сила проявления болезненных ощущений указывает на стадию развития болезни. Правильная диагностика позволяет подобрать адекватную тактику лечения. Поэтому необходимо узнать причину, провоцирующую боль под коленом. Врачи классифицируют артроз на первичный и вторичный. Первопричиной первичной артропатии являются травмы, продолжительная физическая нагрузка. Вторичная же форма — это следствие:
- инфекционных заболеваний;
- нарушения метаболических реакций;
- болезней сосудов и почек.
В любой ситуации болевые ощущения могут предвещать артроз коленного сустава. Поэтому не стоит медлить с визитом к врачу. Потребуется комплексное обследование для выяснения причины болезненности. На разных стадиях артроза боли проявляются по-разному. Обычно дискомфортные ощущения связаны с болевым синдромом, возникающим после активных физических нагрузок, во время ходьбы и уменьшающимися в покое.
Характер болевого симптома
Боль в колене при артрозе на 1-м этапе недуга возникает по утрам, после ночного сна. Ощущения постепенно проходят при двигательной активности. При энергичных движениях сочленение издает характерный хруст, но болезненность отсутствует. Болит колено на этой стадии при длительных и значительных нагрузках. В покое боли исчезают, поэтому на начальном этапе заболевания пациенты не обращаются к врачу.
Обострение артроза на этой стадии приводит к появлению резей и прострелов. Хруст в сочленении слышен при любом движении. Наблюдается значительная контрактура костного соединения, нарушение механизма движения, но сустав сохраняет свою подвижность. Это симптомы артроза второй стадии, при которой проявляется острая продолжительная боль в начале двигательной активности. На 2-м этапе уменьшаются амортизирующие способности хрящей, снижается трудоспособность.
На 3 ст. боль при артрозе коленного сустава носит постоянный режущий характер при движении или в покое. Болевые проявления связаны со спазмом близлежащих мышечных волокон и развитием синовита. Движения резко ограничены. Суставы чувствительны к изменениям погодных условий, что выражается нарастанием боли в левой или правой ноге. Третья степень артроза ведет к стойкой инвалидности.
Как устранить симптом?
Облегчить боль в колене при артрозе и приостановить деструктивные процессы в пораженном суставе на начальном этапе недуга еще возможно. Для этого больному врачом рекомендуются медпрепараты:
- хондропротекторы, улучшающие состояние хрящей;
- поливитаминные комплексы;
- обезболивающие мази;
- бальнеологические процедуры.

Целесообразно подобрать комплексный подход к лечению.
Лечение второй стадии артроза не всегда успешно. Главная задача терапевтических мероприятий сводится к купированию сильных болей лекарственными средствами, уменьшению проявлений воспалительного процесса, по возможности произведению восстановления соединительной ткани. Для снятия болей на 3-й стадии используют анальгезирующие средства, которые принимают перорально, в виде внутримышечных или внутривенных уколов, новокаиновых блокад. Для кардинального решения проблемы необходима операция на сочленении. Хирургическим путем заменяют изношенный сустав эндопротезом. С его помощью пациенту возвращают былую подвижность суставного соединения.
Лечить проявления болевого синдрома помогают НПВС и анальгезирующие средства. Если подобная тактика не дает положительной динамики, то сильные боли купируют кортикостероидами. Их вводят в сустав инъекционно. Уменьшить боль сможет сочетание анальгезирующих средств, седативных медикаментов и миорелаксантов. Дозировку любого препарата назначает врач. Все обезболивающие препараты следует принимать через 30 мин. после еды, потому что медикаменты негативно воздействуют на слизистую ЖКТ.
Безопасно снять боль смогут мази, гели, растирки, в состав которых входят обезболивающие компоненты, а также природные вещества — эфирные масла, змеиный или пчелиный яд.
Полезными для снятия болезненности будут согревающие или холодные компрессы. Делать процедуру следует в одно и то же время. Чтобы унять боль в ноге можно сделать солевую ванну с добавлением эфирного масла. Лечение народными средствами суставной боли зачастую дает положительные результаты. Фитотерапевты советуют использовать следующие растения:
- душицу;
- зверобой;
- боярышник;
- череду;
- тысячелистник.
Из растительного сырья готовят настои. В период обострения недуга необходима ударная доза фитопрепарата. Берут 5 ст. л. измельченного сырья, настаивают в полулитровом заварнике. Употребляют внутрь в течение дня перед едой. Через 30 дней, если самочувствие улучшилось необходимо снизить дозировку ингредиентов до 3 ст. ложек на 500 мл воды. Терапия дает стойкий результат.
Рассмотрены патофизиология болевого синдрома при остеоартрозе и подходы к терапии с применением нестероидных противовоспалительных препаратов (НПВП). Описаны клиническая эффективность и безопасность применения нимесулида для лечения боли при остеоартрозе.
Pathophysiology of pain syndrome in osteoarthrosis and approaches to the therapy using non-steroidal anti-inflammatory preparations (NAIP) were considered. Clinical efficiency and safety of nemisulide application for relief of pain in osteoarthrosis were described.
Остеоартроз (ОА) — одно из самых распространенных заболеваний опорно-двигательного аппарата, основная причина постоянного болевого синдрома [1] и инвалидизации [2].
Болевой синдром при ОА представляется важной клинической проблемой. Манифестация боли возможна на разных стадиях процесса и не имеет четкой корреляции с рентгенологической картиной: рентгенологические проявления ОА отмечаются примерно у 30% взрослого населения, а болевой синдром развивается у 10–12% [3].
Боль может сохраняться даже после хирургического лечения. Примерно 15% больных, которым проведено эндопротезирование коленного сустава в связи с выраженным ОА, продолжают испытывать боль, несмотря на отсутствие хирургических осложнений и нормальную рентгенологическую картину [4].
В основе успешного управления симптомами ОА лежит понимание патофизиологии и тщательная клиническая оценка болевого синдрома.
Любой сустав, вне зависимости от его размеров, — это сложный орган, в состав которого входят синовиальная мембрана, синовиальная жидкость, хрящ, кость и мягкие ткани. При этом сустав — это еще и орган с едиными нейротрофическими, метаболическими, иммунными и функциональными составляющими, играющими важную роль как в патогенезе самого ОА, так и болевого синдрома при нем.
Известно, что прогредиентно протекающие дегенеративные процессы при ОА отмечаются во всех суставных структурах и объединяют потерю матрикса гиалинового хряща, ремоделирование подлежащей кости, поражение костного мозга, вовлечение связок, растяжение капсулы сустава, ослабление прилегающих к суставу мышц [5]. По мере прогрессирования ОА существенно меняется биомеханика сустава.
При ОА в процесс активно вовлекается периост из-за обнажения костной суставной поверхности [6]. Поверхность костной ткани внутри сустава, лишенная амортизирующих свойств из-за деструкции хряща, испытывает избыточную и неравномерную механическую нагрузку. В субхондральной кости появляются зоны динамической перегрузки, в которых развиваются изменения микроциркуляции. Это способствует возникновению субхондрального остеосклероза, кистовидной перестройки, изменению кривизны суставных поверхностей и образованию остеофитов. Повышение внутримедуллярного давления в субхондральной кости — это еще один источник боли при ОА.
Изменения также затрагивают связки, сухожилия, с развитием лигаментитов, теносиновитов, а также бурситов околосуставных сумок [7]. Прилегающие к суставу мышечные структуры страдают как от реактивного воспаления, развивающегося в суставах, так и от нарушения биомеханики больного сустава. В итоге повышенная механическая нагрузка на мышечный аппарат приводит к гипертонусу мышц, что также способствует нарастанию боли.
Значимая роль в патогенезе ОА отводится синовиту, деструктивно воздействующему на суставные структуры за счет активации фагоцитарных, воспалительных и иммунных реакций, способствующих высвобождению значительного числа медиаторов (цитокинов, простагландинов, матриксных металлопротеиназ, супероксидных радикалов, оксида азота и др.), играющих ключевую роль как в моделировании воспаления, так и восприятии боли [8, 9]. Воспаление синовиальной оболочки вносит существенный вклад в развитие боли, поскольку в ней достаточно широко представлены нервные окончания.
К настоящему времени накоплены данные о роли субстанции Р — нейропептида, способствующего возникновению и поддержанию боли за счет усиления продукции медиаторов воспаления в области суставов [10, 11]. По данным исследований при ОА субстанция Р обнаруживается в синовиальной жидкости и синовиальной оболочке [12, 13], периосте, подхрящевых участках костей, суставных капсулах, где синтезируется в немиелинизированных чувствительных нейронах [14], то есть в тех суставных структурах, из которых чаще и больше происходит болевых импульсов [15]. В хрящевой ткани сустава субстанция Р не обнаружена.
Еще одним проявлением ОА, усиливающим боль, является синовиальный выпот, способствующий растяжению богатой нервными окончаниями капсулы сустава [16, 17].
Кроме того, в качестве весьма специфического для суставов фактора, способствующего развитию болевого синдрома при ОА, рассматривается ангиогенез, при котором помимо роста сосудов отмечается значительный рост новых немиелинизированных чувствительных нервных окончаний [18]. При ОА процесс ангиогенеза наблюдается в синовиальной оболочке, некальцифицированных участках внутрисуставных хрящей и в остеофитах. Интересно, что в периваскулярных немиелинизированных нервных волокнах также обнаруживается субстанция Р и пептид, связанный с геном кальцитонина (CGRP), которые в совокупности способствуют медиации устойчивой жгучей боли, как ее описывают больные ОА [19].
Поскольку внутрисуставной гиалиновый хрящ не имеет ноцицепторов, он, несмотря на существенные дегенеративные процессы в нем, не может служить источником болевой импульсации. Очевидно, что боль при ОА полиэтиологична и происходит из всех выполняющих сустав структур, за исключением хряща [10, 11].
Болевой синдром при ОА может быть острым и хроническим: с периодическими обострениями и их уменьшением. Острая боль является следствием раздражения болевых рецепторов, расположенных в коже, связках, сухожилиях, сумках, костях, синовиальной оболочке, мышцах. Механизмы трансформации острой боли в хронический болевой синдром при ОА изучены недостаточно полно. Предполагается, что хронизации боли при ОА может способствовать длительное раздражение периферической ноцицептивной системы с постоянным вовлечением задних рогов спинного мозга [20]. При этом включаются принципиально иные механизмы формирования болевых импульсов. Ключевой вопрос касается связи между периферическим повреждением и воспалением структур суставов и стимуляцией выработки ЦОГ-2 в центральной нервной системе (ЦНС), где могут иметь значение как нервные, так и гуморальные механизмы. В частности, показано, что довольно продолжительная активность небольших сенсорных нейронов, обусловленная периферическим воспалением, сопровождается высвобождением глутамата/аспартата и субстанции Р в спинном мозге с последующей активацией рецепторов NMDA (N-метил-D-аспартата) в нейронах задних рогов спинного мозга [21]. Доказательством этого является повышенное содержание субстанции Р в спинномозговой жидкости больных ОА [22]. Стимуляция этих рецепторов может вызвать повышение экспрессии ряда ферментов, включая ЦОГ-2, в спинном мозге, что в итоге ведет к усилению болевого синдрома. Гуморальный же механизм воспалительной реакции, связанной с повреждением периферических суставных структур, приводит к высвобождению провоспалительных цитокинов (ФНО-α, ИЛ-1β), которые в свою очередь усиливают экспрессию ЦОГ-2.
Исходя из представлений о патогенезе ОА и болевого синдрома при нем, становится очевидным, что подавление воспаления и предотвращение деструкции суставных структур, с целью снижения синтеза провоспалительных цитокинов, простагландинов (в особенности ПГE2), ферментов синовиальной оболочки, металлопротеиназ, деградации коллагеновых волокон, протеолитической активности и т. п., является одним из приоритетных направлений в терапии ОА. Несомненно, назначение противовоспалительных препаратов не просто желательно, но и показано больным с ОА, испытывающим боль, особенно в тех случаях, когда развитие болевого синдрома тесно связано с тканевым воспалением, а простой анальгетик не оказывает должного эффекта. Подобный терапевтический подход соответствует ведущим рекомендациям национальных и международных руководств по купированию болевых синдромов у пациентов с ОА, где подчеркивается, что терапевтическим методом в таких случаях является использование парацетамола. При этом важно подчеркнуть, что парацетамол не оказывает действия на периферические ЦОГ, а посему не обладает противовоспалительным эффектом. И, кроме того, чтобы реализовать свою функцию, парацетамол должен достичь достаточного уровня концентрации в ликворе, поскольку оказывает комплексное воздействие на ЦНС, усиливая нисходящие от периферии к ЦНС процессы торможения. А это требует применения достаточной дозировки и обязательного соблюдения временного интервала между приемами (1 г трижды в день), чтобы полностью использовать потенциал препарата [27]. Эти аспекты оправдывают применение таких лекарственных препаратов, как НПВП, с учетом соотношения пользы и риска.
Нестероидные противовоспалительные препараты (НПВП) — наиболее назначаемый класс лекарственных средств, предназначенных для лечения болевых синдромов. Общими фармакологическими свойствами НПВП являются подавление биосинтеза простагландинов (ведущих факторов активации болевых рецепторов) за счет блокады изоферментов циклооксигеназы, в частности ЦОГ-2, и нормализация сниженного болевого порога. При назначении НПВП подавление синтеза простагландинов имеет место как на периферическом, непосредственно в месте повреждения и воспаления, так и на центральном уровнях, свидетельствуя о том, что и периферические и центральные механизмы принимают участие в антиноцицептивном действии этих препаратов. Центральный эффект НПВП связан с угнетением синтеза простагландинов, которые образуются в ЦНС и способствуют усилению болевого сигнала. Таким образом, ЦНС является дополнительным местом проявления антиноцицептивных эффектов НПВП.
Одним из наиболее популярных средств среди НПВП является нимесулид. Многочисленные исследования и более чем 30-летний клинический опыт применения показали, что нимесулид (Найз) обладает высокой эффективностью и хорошей переносимостью [28].
В контексте данной статьи хотелось бы прежде остановиться на бесспорных достоинствах нимесулида как препарата выбора для лечения болевых синдромов при ОА, принимая во внимание данные об их механизмах, рассмотренные ранее.
Интересны, прежде всего, ЦОГ-зависимые механизмы действия, обусловливающие эффективность и безопасность нимесулида. Поскольку нимесулид оказывает преимущественное действие на ЦОГ-2, то его эффекты очевидны как на периферии, в суставных структурах, затронутых деструктивным процессом и связанным с ним воспалением, так и в ЦНС [29, 30]. Причем исключительной особенностью нимесулида является способность не только подавлять активность ЦОГ-2, но и блокировать ее образование [31].
Хотя нимесулид и обладает преимущественным эффектом в отношении ЦОГ-2, он оказывает сбалансированное влияние на обе изоформы ЦОГ. В терапевтических концентрациях нимесулид ингибирует 88% активности ЦОГ-2 и 45% активности ЦОГ-1. При этом если воздействие на ЦОГ-1 прекращается через 24 часа после введения, то воздействие на ЦОГ-2 продолжается намного дольше [32], и это различие сохраняется при длительном применении [33, 34].
Неоспоримым преимуществом нимесулида является способность молекулы уменьшать высвобождение ФНО-α, ИЛ-6 и субстанции Р [35–37].
Примечательны ЦОГ-независимые эффекты нимесулида. В частности, в терапевтических концентрациях нимесулид влияет на продукцию токсичных окислительных радикалов и других компонентов нейтрофильной активации [38], ß-глюкуронидазы [39], что может усилить противовоспалительный и анальгетический эффект и потенциально уменьшать вероятность гастроинтестинальной ульцерогенности.
Наконец, трудно переоценить протективное действие нимесулида на суставной хрящ. Известно, что неселективные в отношении ЦОГ НПВП усугубляют тяжесть ОА при длительном применении. В наибольшей степени отрицательно влияют на хрящ производные индолуксусной кислоты (индометацин), чуть меньше — производные пропионовой кислоты (ибупрофен, напроксен и др.), что подтверждается данными рентгенографии. При этом доказано, что селективные ингибиторы ЦОГ-2, в частности нимесулид, не оказывают отрицательного влияния на синтез протеогликанов хрящевой тканью, даже при применении высоких доз [40, 41]. Напротив, нимесулид обнаруживает способность снижать в синовиальной жидкости, полученной из воспаленного сустава, уровень коллагеназы, вызывающей деградацию коллагена и протеогликанов [42].
С клинической точки зрения, многоплановость механизмов действия нимесулида, связанных или не связанных с ЦОГ, выражается в эффективности и быстром модулировании сложного воспалительного процесса и сопряженной с ним боли.
Клиническая эффективность нимесулида показана в многочисленных исследованиях. Известно, что препарат превосходит или как минимум столь же эффективен, как и классические НПВП, в отношении купирования значительного числа болевых синдромов, включая ревматоидный артрит, скелетномышечные боли в спине, послеоперационную и зубную боль, дисменорею. Преимущества нимесулида показаны и при лечении ОА. Так, использование нимесулида позволило добиться значимого уменьшения боли и улучшения самочувствия у подавляющего большинства пациентов с ОА, включенных в двойное слепое сравнительное исследование эффективности и безопасности нимесулида и диклофенака при гонартрозе и коксартрозе [43]. Этот результат представляется более значимым еще и потому, что примерно половина больных до назначения нимесулида получали другие НПВП и не отмечали при этом существенного улучшения своего состояния.
М. И. Шупина* , 1 , кандидат медицинских наук
Г. И. Нечаева*, доктор медицинских наук, профессор
Е. Н. Логинова*, кандидат медицинских наук
Т. В. Кропотина**, кандидат медицинских наук
Ю. В. Арбузова**
* ГБОУ ВПО ОмГМУ МЗ РФ, Омск
** БУЗОО ОКБ, Омск
Многие с этим живут долгие годы, особенно в пожилом возрасте. Боли в тазобедренных суставах, боли при ходьбе в голеностопном суставе, боли в кистях рук, в плечах при движении. Все это можно отнести к хроническим изменениям в суставах, которые объединены одним диагнозом — деформирующий остеоартроз или остеоартрит. По официальным данным, во всем мире болеют 5-7 процентов мужчин и женщин. Мужчины заболевают раньше, в возрасте 45 лет, женщины после 55 лет, это связано с гормональными особенностями, женщины чаще заболевают после климакса.
Что происходит с суставами при остеоартрозе

Уменьшается количество смазки внутри сустава, меньше обновляется хрящ. При интенсивных нагрузках, травмах случаются микропереломы, надрывы связок, на хряще образуются эрозии. Нагрузку может давать и лишний вес, который усиливает давление на суставы. Переохлаждение, артриты в прошлом дают повреждение костной и хрящевой ткани. Остеопороз (вымывание кальция из костей) также усиливает явления артроза.
Диагноз очевиден. Деформирующий остеоартроз отличается от ревматоидного артрита, артритов при аутоиммунных заболеваниях или реактивных артритов тем, что изменения в крови минимальны. Тут нет аутоиммунного компонента. Основные тесты, которые мы используем для выявления воспаления в общем анализе крови – это скорость оседания эритроцитов (СОЭ), количество лейкоцитов. В биохимическом анализе крови назначают такие тесты как С-реактивный белок, ревматоидный фактор, при остеоартрозе они почти не отличаются от нормы.
Обязательно назначается рентгенологическое исследование сустава, чтобы выявить стадию заболевания. Потому что изменения в суставе могут не соответствовать симптомам заболевания. Тяжелые изменения в суставе могут протекать почти без боли, в то же время пациент может жаловаться на сильные боли, хотя в самом суставе изменения минимальны. Чтобы выявить нарушения связочного аппарата, воспаление синовии – суставной оболочки, назначают УЗИ сустава. КТ или МРТ назначают для уточнения изменений. А также когда требуется хирургическое вмешательство.
Поражаться могут разные суставы, как крупные – тазобедренные, коленные, плечевые, локтевые, так и мелкие суставы – кистей и стоп. Зависит от того, какой сустав был перегружен. Если лишний вес – больше страдают суставы ног, тазобедренные, позвоночник. Если нагрузка на кисти рук при работе, поражаются фаланги пальцев и лучезапястный сустав.
Лечение остеоартроза
Основные цели лечения – сохранить и улучшить функции суставов, уменьшить боль. На начальном этапе это терапевтическая помощь, по мере прогрессирования требуется помощь физиотерапевтов, врачей ЛФК, хирургов и ортопедов.
Для больного важно снизить нагрузку на пораженный сустав, обязательно снизить массу тела, при ходьбе лучше использовать трости, ходунки.
ЛФК (лечебная физкультура) – просто необходима для суставов. Существует много разных систем для укрепления мышц и для увеличения подвижности. Конечно, если болят суставы, без специальных упражнений никак нельзя. Много упражнений для суставов и в восточной традиции, например Дарума-тайсо – одна из эффективных и простых систем.
Как вспомогательное и отвлекающее средство используют согревающие или противовоспалительные мази и гели, такие как капсикам, быструм-гель, фастум-гель. Полностью вылечиться ими невозможно, но облегчить состояние они могут. Из старых проверенных методов помогают компрессы с димексидом, особенно в первые дни при обострении.
При болях врач назначает приём группы нестероидных противовоспалительных препаратов в таблетках и инъекциях. В виде уколов чаще – диклофенак, кетопрофен. В таблетках или капсулах – кетопрофен, нимесулид, ибупрофен и более современные препараты – нальгезин, дилакса. НПВП приходится принимать длительно, но нужно не забывать о том, что длительный приём может спровоцировать язву слизистой оболочки желудка и ДПК и кровотечения из этих язв. Поэтому обычно приём НПВП совмещают с приемом препаратов группы омепразола (рабепразол, пантопразол) или антацидов (альмагель).
Длительными курсами от 2 до 6 месяцев принимают хондропротекторы. Это препараты, содержащие хондроитин и глюкуроновую кислоту – строительные материалы для хряща (артра, дона, алфлутоп). Это могут быть лекарственные препараты или БАДы (биологически активные добавки). Могут быть препараты как в таблетках, так и в инъекциях. Хирурги делают инъекции хондропротекторов в суставы.
Эффективность хондропротекторов наукой не доказана. Из своего опыта могу сказать, что людям с сердечными заболеваниями, особенно принимающие сложные схемы препаратов, лучше от них отказаться. Остальным же неплохо принимать 1-2 курса в год, особенно тем, кто страдает дефектом соединительной ткани, при условии, что они сами видят эффект от лечения.
Как вспомогательное противовоспалительное средство используют гормоны – глюкокортикоиды, чаще всего в виде инъекций в суставы.
При интенсивных болях врач назначает комбинированные препараты типа пенталгина. При неэффективности этих препаратов, выписывают более сильные опиоидные анальгетики (трамадол, золдиар).
Физиотерапия, в частности ультразвук, согласно исследованиям наиболее эффективная процедура для лечения остеоартроза. С его помощью разбиваются маленькие наросты на поверхностях суставов и отложения солей. Для противовоспалительного эффекта ультразвук делают с гормональными мазями.
По результатам тех же исследований магнит малоэффективен, а во многих случаях и вреден, особенно для людей в возрасте. Его частое и бесконтрольное применение может стимулировать онкологический процесс.
Диета направлена на снижение избыточной массы тела. Также она должна включать вещества, содержащие хондропротекторы — хрящи, особенно рыбные, желе, холодец.
Хирургическое лечение остеоартроза — это эндопротезирование, то есть замена сустава. Показаниями к операции может быть нарушение функции сустава, выраженность болей, которые не проходит при лечении физиотерапией, анальгетиками.
Многое в плане здоровья суставов зависит от нас, нужно не лениться делать гимнастику, следить за своим весом, щадить свои суставы, вовремя обратиться к врачу, пройти обследование и начать лечение.
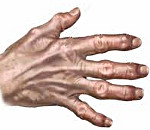
Деформирующий остеоартроз – прогрессирующее дистрофическое изменение костных суставов с первичным повреждением хрящевых тканей и последующей дегенерацией всего комплекса костно-суставного аппарата. Деформирующий остеоартроз характеризуется артралгией, функциональной недостаточностью суставов и выраженными изменениями их формы. Фармакотерапия деформирующего остеоартроза направлена на замедление прогрессирования дегенеративных процессов, уменьшение боли и улучшение функционирования суставов; в некоторых случаях показано эндопротезирование суставов. Течение деформирующего остеоартроза медленно прогрессирующее с развитием анкилоза или патологической нестабильности сустава.
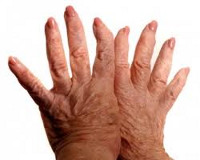
- Классификация
- Симптомы деформирующего остеоартроза
- Осложнения
- Диагностика
- Лечение деформирующего остеоартроза
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Деформирующий остеоартроз - частая патология суставов, при которой нарушение регенерации соединительнотканных структур приводит к преждевременному старению суставного хряща – его истончению, шероховатости, растрескиванию, потере прочности и эластичности. Субхондральная кость обнажается и уплотняется, в ней происходят остеосклеротические изменения, образуются кисты и краевые разрастания - остеофиты.
Деформирующий остеоартроз по первичному типу развивается в изначально здоровом хряще при врожденном снижении его функциональной выносливости. Случаи вторичного деформирующего остеоартроза возникают на фоне имеющихся дефектов суставного хряща, вызванных травматизацией, воспалением костно-суставных тканей, асептическим некрозом костей, гормональными или обменными нарушениями.

Классификация
В соответствии с клинико-рентгенологической картиной в развитии деформирующего остеоартроза выделяют 3 стадии:
Авторы Kellgren и Lawrence выделяют 0 стадию деформирующего остеоартроза с отсутствием рентгенологических проявлений.
Симптомы деформирующего остеоартроза
К проявлениям деформирующего остеоартроза относятся крепитация (хруст) в суставах при движении; ограниченность подвижности суставов, связанная с уменьшением суставной щели, разрастанием остеофитов и спазмом периартикулярных мышц; необратимая деформация суставов, вызванная дегенерацией субхондральных костей.
Деформирующий остеоартроз с заинтересованностью коленных суставов (гонартроз) проявляется болью при длительной ходьбе, подъеме в лестницу, хрустом и затруднением при выполнении сгибательных и разгибательных движений. При артрозе мелких суставов кистей рук появляются плотные узелки по краям межфаланговых проксимальных и дистальных суставов (узелки Гебердена и Бушара), сопровождающиеся болезненностью и скованностью.
При генерализованной форме деформирующего остеоартроза (болезни Келлгрена, полиостеоартрозе) отмечаются множественные изменения периферических и межпозвонковых суставов. Полиостеоартроз обычно сочетается с остеохондрозом межпозвоночных дисков, спондилёзом в шейном и поясничном отделах позвоночника; периартритами и тендовагинитами.
Осложнения
Длительное прогрессирование деформирующего остеоартроза может осложняться развитием вторичного реактивного синовита, спонтанного гемартроза, анкилоза, остеонекроза мыщелка бедра, наружного подвывиха надколенника.
Диагностика
В ходе диагностики деформирующего остеоартроза пациент проходит консультацию ревматолога и исследования, позволяющие определить состояние и степень функциональной полноценности сустава по характерным клиническим критериям. Основными являются данные рентгенодиагностики, показывающие сужение суставных щелей, разрастание остеофитов, деформацию суставных участков кости: наличие кист, субхондрального остеосклероза. Для более детальной оценки изменений хряща при деформирующем остеоартрозе дополнительно проводят УЗИ, КТ позвоночника и МРТ больного сустава.
По показаниям выполняют пункцию сустава. В сложных случаях выполняют артроскопию с прицельным забором материала и морфологическим изучением биоптатов синовиальной оболочки, суставной жидкости, хрящевой ткани, выявляющим дистрофические и дегенеративные изменения сустава.
Лечение деформирующего остеоартроза
Терапия деформирующего остеоартроза включает комплексный подход с учетом этиологических обстоятельств, систематичность и длительность лечения. В первую очередь требуется разгрузить больной сустав (особенно опорный), снизить двигательную активность, избегать длительной ходьбы, фиксированных поз и ношения тяжестей, при ходьбе пользоваться тростью.
Уменьшение воспаления и боли в суставах при деформирующем остеоартрозе достигается назначением НПВС: диклофенака, нимесулида, индометацина. Сильный болевой синдром снимают внутрисуставными блокадами с введением гормональных препаратов. При риске развития язвенной болезни показаны препараты мелоксикам, лорноксикам, местно - противовоспалительные мази, гели. При медленном рассасывании внутрисуставного выпота выполняют его пункционную эвакуацию.
В начальной стадии деформирующего остеоартроза эффективны хондропротекторы (гидрохлорид глюкозамина и хондроитинсульфат), помогающие приостановить дальнейшее разрушение хряща и восстановить его структуру. При деформирующем остеоартрозе назначают локальную физиотерапию - аппликации парафина и озокеритолечение, высокочастотную электротерапию, электрофорез с новокаином и анальгином, магнитотерапию и лазеротерапию. Для укрепления мышечно-связочных структур и улучшения двигательной функции суставов показана лечебная гимнастика, кинезотерапия, регулярное санаторное лечение и бальнеотерапия.
При тяжелом инвалидизирующем поражении тазобедренного или коленного суставов выполняют эндопротезирование, в случае развития деформирующего остеоартроза голеностопных суставов эффективна операция полного обездвиживания сустава (артродез). Инновационным в лечении деформирующего остеоартроза является применение стволовых клеток, замещающих собой поврежденные клетки хрящевой ткани и активизирующих регенеративные процессы.
Прогноз и профилактика
Скорость и степень прогрессирования деформирующего остеоартроза определяется его формой, локализацией, а также возрастом и общим фоном здоровья пациента. Коксартроз может серьезно нарушить функции конечности, стать причиной нетрудоспособности и даже инвалидности. При многих формах деформирующего остеоартроза достигается устранение болевой реакции, улучшение функционирования сустава, однако полного восстановления хряща у взрослого пациента достичь невозможно.
Профилактика деформирующего остеоартроза состоит в ограничении перегрузок суставов, своевременном лечении травм (растяжений связок, ушибов), заболеваний костного аппарата (дисплазии, плоскостопия, сколиоза), регулярных занятиях гимнастикой, поддержании оптимальной массы тела.
Читайте также:


