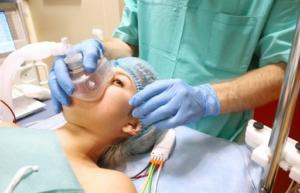
Спинальная анестезия при болезни паркинсона
Паркинсонизм — это синдром, характеризующийся тремором, акинезией, ригидностью и постуральной нестабильностью. Этиология неизвестна, но паркинсонизм может быть индуцирован некоторыми лекарствами (особенно нейролептиками) или быть последствием травмы/энцефалопатии.
Патофизиология
Паркинсонизм является следствием дисбаланса взаимно антагонистических дофаминэргической и холинэргической систем базальных ганглиев. Пигментированные клетки черного вещества исчезают, что ведет к снижению дофаминэргической активности. Снижение холинэргической активности не происходит. Цель медикаментозной терапии паркинсонизма — восстановление этого баланса, либо повышение допаминовой или допаминоподобной активности, либо снижение холинэргической активности в мозге.
Медикаментозная терапия
Лекарственное лечение паркинсонизма ограничено в связи с тяжелыми побочными эффектами (тошнота и спутанность сознания), особенно у пожилых. До 20% пациентов эффекта от лечения не имеют.
- L-допа является инактивированной формой допамина, которой для эффективного действия в мозге необходима конверсия в допамин при помощи декарбоксилаз. Это препарат первого выбора при идиопатическом паркинсонизме. Он более полезен пациентам с брадикинезией и ригидностью, чем с тремором, и обычно назначается с ингибиторами декарбоксилазы (например, бензеразид, кардидопа), которые не проникают в мозг и снижают периферическую конверсию допамина, таким образом снижая его дозу и риск побочных эффектов.
- Ингибиторы моноаминооксидазы-В (ингибиторы МАО-В; например, селегилин), действуют, снижая центральный обратный захват допамина. Селегилин менее выраженно взаимодействует с другими препаратами, чем неспецифические ингибиторы МАО, но все же может вызнать гипертензивную реакцию на петидин и опасное возбуждение ЦНС на селективные ингибиторы обратного захвата серотонина и трициклические антидепрессанты.
- Дериваты спорыньи, такие как бромокриптин, каберголин, лизурид и перголид, действуют прямо, стимулируя допаминовые рецепторы. Обычно их оставляют для дополнительной терапии уже получающим L-допа или пациентов с побочными эффектами от последнего.
- Энтакапон — вспомогательное средство, способное снизить дозу L-допа и удлинить его действие. Обычно его оставляют для пациентов, испытывающих ухудшение после длительной допаминэргической терапии.
- Другие вспомогательные препараты, ропинироль, прамипексоль, амантадин, апоморфин и тонкапон.
- В настоящее время парентеральных форм препаратов для лечения паркинсонизма нет.
К наиболее часто используемым препаратам этой группы относятся бензтропин, проциклидин, бензгексол и орфенадрин. Они являются препаратами первого выбора только при средневыраженной симптоматике с доминированием тремора. Ригидность и повышенная саливация могут быть смягчены этими препаратами, но на брадикинезию они не подействуют. Они могут быть полезны при лекарственно индуцированном паркинсонизме, но не при медленной дискинезии. Существуют парентеральные формы проциклидина и бензтропина, что делает их полезными при острых лекарственных дистониях.
Хирургическое лечение
Операции для лечения вызванной паркинсонизмом инвалидности пользуются растущей популярностью. В норме они выполняются пациентам в сознании с использованием стереотаксической техники:
- Таламотомия применяется в случаях, когда доминирующей причиной инвалидности является тремор, особенно если тремор унилатеральный. Передняя таламотомия иногда применяется при ригидности
- Паллидотомия применяется в первую очередь при ригидности и брадикинезии, хотя тремор (если он есть) тоже может уменьшиться.
Большинство пациентов с тяжелыми формами заболевания получают несколько поддерживающих препаратов, и лекарственные взаимодействия могут быть потенциально опасными.
- Анальгетики: петидин, синтетические опиаты (фентанил, альфентанил) – Гипертензия и мышечная ригидность с селегилином. Мышечная ригидность – Может провоцировать злокачественную гипертермию Более очевидно в больших дозах
- Ингаляционные анестетики – Потенциируют аритмии, индуцируемые L-допа – Если на предоперационной ЭКГ есть желудочковая аритмия, галотан применять нельзя
- Противорвотные средства: метоклопрамид, дроперидол, прохлоперазин – Могут вызвать экстрапирамидные расстройства или ухудшить симптомы паркинсонизма – По схеме ведения ПОТР. Метоклопрамид может повышать концентрацию L-допа в плазме
- Антидепрессанты: трициклические (амитриптилин) – Потенциируют аритмии, индуцируемые L-допа (только трициклические)
- Ингибиторы обратного захвата серотонина (флюоксетин) – Гипертонический криз и церебральное возбуждение с селегилином (селективные ингибиторы обратного захвата серотонина и трициклические)
- Антигипертензивные (все классы) – Выраженный антигипертензивный эффект при леченном и нелеченном паркинсонизме. Связан с постуральной гипотензией и относительной гиповолемией – Наиболее выражено с клонидином и резерпином
Анестезия
Идеально, если пациент с тяжелым заболеванием находится под наблюдением врача, имеющего специальный опыт в лечении болезни Паркинсона, с привлечением его к ведению больного в периоперационном периоде. Особый интерес представляют следующие обстоятельства:
- Дисфагия и избыточная саливация (сиалоррея) указывают на повышенный риск аспирации и возможность проблем с контролем дыхательных путей в периоперационном периоде. Для этой группы пациентов типичен гастроэзофагальный рефлюкс.
- Постуральная гипотензия может быть результатом нарушения вегетативной регуляции (семейная вегетативная дисфункция) и медикаментозно индуцированной гиповолемии, требующих настороженности в отношении возможной гипотензии при индукции анестезии или изменения положения во время операции.
- Медикаментозно индуцированные аритмии, особенно желудочковая экстрасистолия, типичны, но клинического значения обычно не имеют.
- Респираторная функция может быть скомпрометирована брадикинезией и мышечной ригидностью, равно как и задержкой мокроты. Могут быть показаны исследования рентгенограмм грудной клетки, функциональных легочных тестов и газов крови.
- Затруднения мочеиспускания могут потребовать катетеризации мочевого пузыря. Послеоперационная задержка мочи потенциально может быть причиной послеоперационной спутанности сознания.
- Следует определить тяжесть основного заболевания и других, вероятно, ожидаемых проблем, таких как акинезия, ригидность мышц, тремор, спутанность сознания, депрессия, галлюцинации и нарушения речи.
- Терапию паркинсонизма следует продолжать вплоть до начала анестезии. Симптоматика заболевания может проявиться через какие-нибудь 3 ч после пропущенной дозы.
- В премедикации необходимости обычно нет, если нет опасной сиалорреи. К средствам лечения последней относится атропин (10 мкг/кг в/м до 1 мг) или гликопирролат (200-400 мкг в/м).
- Наличие сиаллореи и дисфагии до операции свидетельствуют о наличии дисфункции ЖКТ. В этом случае показаны контроль дыхательных путей и быстрое введение в наркоз.
- Во избежание дрожи необходимо поддерживать нормотермию.
- Нет данных о преимуществе какой-либо из анестезиологических методик.
- Анальгезия: морфин используется внутривенно, если региональная или местная анальгезия невозможны (АКП для этих пациентов может оказаться трудной). Оральная анальгезия может быть затруднена в связи с дисфагией (может потребоваться назогастральный зонд).
Послеоперационное ведение
- В принципе, чем выраженнее инвалидизация пациента до операции, тем выше надобность в респираторной поддержке и в переводе в ПИТ после операции.
- Если инвалидизирующим фактором является ригидность, то должна быть организована послеоперационная физиотерапия.
- Если нарушена функция ЖКТ, то может потребоваться введение назогастрального зонда для скорейшего возврата к применению пероральных препаратов.
- Затягивающаяся дисфункция ЖКТ после операции может стать причиной тяжелых осложнений в связи с отсутствием в настоящее время парентеральных препаратов для лечения паркинсонизма.
Противорвотные средства
- Домперидон (10-20 мг через 4-6 орально или 30-60 мг через 4-6 ч ректально). Препарат первого выбора при ПОТР у пациентов с паркинсонизмом. Не преодолевает гематоэнцефалический барьер (ГЭБ) в сколько-нибудь существенной степени, таким образом, не вызывает значительных экстрапирамидных нарушении.
- Антагонисты серотонина однасетрон 4 мг в/в или гранисетрон 1 мг в/в медленно, могут быть препаратами первой помощи при ПОТР если домперидон не эффективен.
- Антигистаминные деривативы (например, циклизин 50 мг в/в или в/м).
Вопросы обезболивания больных с болезнью Паркинсона рассмотрены Shalkh S.I., Verma H. (1). Основные положения следующие.
Паркинсонизм – наименование клинического синдрома, основными компонентами которого являются нарушение произвольного движения (гипокинезия), ригидность, тремор. В основе – разрушение допамин-содержащих нервных клеток в черном веществе (substantia nigra) базальных ганглиев.
Перед операцией необходим анализ следующих позиций:
1. Точность диагноза и продолжительность заболевания.
2. Анализ сопутствующих отклонений в различных органах и системах.
3. Планируемое хирургическое вмешательство (плановое, ургентное).
4. Принимаемые больным антипаркинсонические препараты, их эффективность, возможность взаимодействия с препаратами для наркоза.
5. Продолжение леводопы в предоперационном периоде.
6. Премедикация и профилактика аспирации желудочным содержимым.
Диагноз болезнь Паркинсона может быть поставлен с определенной долей уверенности больным с наличием как минимум двух из трех основных симптомов – тремор в покое, ригидность, брадикинезия.
Болезнь Паркинсона характерна для больных преклонного и пожилого возраста. Вследствие этого у таких пациентов возможны традиционные гериатрические проблемы: патология предстательной железы, катаракта, оперативные вмешательства в анамнезе и т.д.
У пациентов с болезнью Паркинсона обычно имеет место дисфункция вегетативной нервной системы. Возможные проявления разнообразны: ортостатическая гипотензия, слюнотечение, запоры, недержание кала, чрезмерное потоотделение, возможность внезапного непредсказуемого ответа на центральные нейроаксиальные блокады.
Дисфункция дыхательных путей являются следствием некоординируемых несознательных движений, ригидности и слабости скелетной мускулатуры. Слабость мышц глотки ведет к увеличению нарушению эвакуации секрета дыхательных путей, что может предрасполагать к аспирационной пневмонии.
Нарушения со стороны желудочно-кишечного тракта являются следствием утраты аппетита вследствие преклонного возраста, депрессии, тошноты и рвоты в результате приема соответствующих лекарственных средств. В совокупности это может вести к утрате массы тела. Увеличена вероятность стаза желудочного содержимого и желудочно-пищеводного рефлюкса. В силу этого желательна профилактика аспирации желудочным содержимым в предоперационном периоде.
Проявлениями нейропсихологических нарушений являются отклонения настроения (депрессия), когнитивные дисфункции, нарушения поведения. Возможны галлюцинации. В послеоперационном периоде нейропсихологические нарушения могут приводит к различным психотическим реакциям, которые одновременно с тремором и ригидностью могут вести к затруднениям в переводе на самостоятельное дыхание и экстубации.
ВЗАИМОДЕЙСТВИЯ ЛЕКАРСТВЕННЫХ СОЕДИНЕНИЙ
В случае приема леводопы у больных возможны тошнота и рвоты, на фоне депрессии и пожилого возраста это ведет к увеличению предрасположенности к дегидратации и гиповолемии. В периоперативном периоде необходима адекватная волемическая поддержка.
Леводопа действует центральным механизмом, что предрасполагает к гипотензии. Непосредственные агонисты допамина бромокриптин и лизурид могут усугублять гипотензию, вызывая периферическую вазодилатацию. Применение антидепрессантов старого поколения (амитриптилина и других трициклических антидепрессантов) может становиться причиной ортостатической гипотензии.
Больным, получающим леводопу, ингибиторы моноаминоксилазы (МАО) противопоказаны, симпатомиметики должны использоваться с осторожностью, поскольку они могут индуцировать резкий подъем артериального давления. На фоне применения леводопы галотан, вызывающий сенститизацию сердца к катехоламинам, следует избегать, поскольку он может усугублять аритмии.
Ингибиторы МАО подавляют метаболизм наркотических аналгетиков в печени, поэтому их рекомендуется использовать в дозе 20–25% от обычной. При назначении меперидина больным, получающим антидепрессанты (ингибиторы МАО, флюоксетин) возможно развитие серотонинового синдрома (нарушение функции вегетативной нервной системы с гипертензией, тахикардией, гипертермией, гиперрефлексией, нарушением сознания, возбуждением, чрезмерным потоотделением). Имели место сообщения о возбуждении, мышечной ригидности, гипертермии у больных, получающих меперидин и селегилин, такую комбинацию препаратов лучше избегать.
Препараты, которые вызывают или усугубляют болезнь Паркинсона, следует избегать, включая фенотиазины, бутирофеноны, метоклопрамид.
Хирургические вмешательства при болезни Паркинсона осуществляют в случаях, когда медикаментозное лечение теряет эффективность или прием препаратов сопровождается опасными для здоровья и жизни человека побочными эффектами.
Среди показаний к выполнению операции выделяют ригидность мышц, акинезию или брадикинезию, трудности при ходьбе, неконтролируемый тремор конечностей и головы.
Операцию назначают после стойкого снижения эффекта от применения лекарственных препаратов, при угнетении функций ЦНС в процессе консервативной терапии, резком развитии заболевания.
Виды нейрохирургических вмешательств
Операция при болезни Паркинсона направлена на восстановление двигательной функции, снижение скорости прогрессирования патологии, улучшение когнитивных способностей и стабилизацию психических нарушений.

В процессе хирургического вмешательства проводится разрушение пораженной области мозга или стимуляция мозговых центров. Операцию проводят стереотаксическим методом, подразумевающим точное проникновение хирургических инструментов к очагу вмешательства, что позволяет избежать травматизации тканей.
Прежде чем лечь на хирургический стол, пациент проходит тщательное обследование и предоперационную подготовку, в процессе которой подбирают оптимальный метод вмешательства и средства анестезии.
Операция включает несколько этапов. На первом этапе проводят компьютерную визуализацию структур головного мозга с использованием специальных маркеров. Голову больного неподвижно фиксируют, а благодаря стереотаксической раме осуществляется выведение изображения. На основе данных хирург определяет точные координаты мишени, составляет план последовательности действий.
Второй этап предусматривает использование местной анестезии в области трепанации черепа, образование трепанационного отверстия, деструкцию области мозга и имплантацию стимулирующей системы. Применяется местное обезболивание, пациент пребывает в сознании. Во время манипуляций врач разговаривает с больным, задает ему вопросы, периодически проверяет чувствительность и подвижность конечностей, мимические движения.
Учитывая то, что кинетические нарушения возникают из-за повреждения таламуса, хирургическое лечение подразумевает использование двух инвазивных методик его коррекции – таламотомии и паллидотомии.
Таламотомия – представляет собой частичную деструкцию структур таламуса, которые генерируют и передают неправильные импульсы к мышцам. Человека неподвижно фиксируют, обезболивают место трепанации, после чего проделывает отверстие в черепной коробке, через которое получают доступ к таламусу. Криодеструкцию проводят при помощи специального зонда, с наконечником, к которому подается жидкий азот.
Проведение разрушения нервной ткани возможно под воздействием высокой температуры (термодеструкция). Наконечник зонда нагревает ткани до 93 градусов Цельсия, что приводит к их коагуляции. Одностороннее вмешательство на противоположной симптоматике стороне. Таламотомия справа приводит к нормализации двигательной функции в левой части тела, наоборот.
Используют неинвазивную таламотомию с помощью ультразвука. Фокусированные ультразвуковые волны, под контролем МРТ проникают сквозь черепную коробку к мишени, ее нагревая. Абаляция части таламуса при помощи ультразвука позволяет существенно уменьшить клинические проявления паркинсонизма щадящим способом.
Двухсторонняя деструкция таламуса не выполняется, т.к. приводит к негативным последствиям – ухудшению памяти и когнитивных способностей, проблемам с речью.
Независимо от выбранного метода, таламотомия приводит к результатам:
- человек в два раза лучше контролирует движения;
- прекращается тремор;
- снижаются дозы препаратов для медикаментозной терапии.
Таламотомия при использовании методов криодеструкции или термодеструкции дает стойкий многолетний или пожизненный эффект. Абаляция клеток таламуса при помощи ультразвуковых волн улучшает состояние больного на срок 1 год и более.
После таламотомии пациент остается в условиях стационара в течение двух суток. Если в процессе операции возникли осложнения, сроки пребывания в больнице врач устанавливает индивидуально. Процесс восстановления занимает от двух месяцев, а период постепенного снижения симптоматики занимает до полугода.
Паллидотомия – деструкция медиальной области бледного шара (структурной части базальных ядер). При паркинсонизме данный участок мозга становится чрезмерно активным, что подавляет работу областей ЦНС, отвечающих за двигательные функции. Частичное разрушение бледного шара позволяет пациентам избавится от локомоторной скованности и устранить тремор.
Хирургическое лечение болезни Паркинсона посредством паллидотомии показано при:
- кинетических нарушениях, которые не поддаются консервативной терапии;
![]()
- непроизвольных движениях конечностей и тела, спровоцированных длительным приемом препаратов леводопы;
- как альтернатива нейростимуляции.
Техника проведения паллидотомии сходна с таламотомией, однако воздействие осуществляется на разные области мозга. Помимо криодеструкции, для разрушения участков бледного шара возможно применение электрокоагуляции. Воздействие жидким азотом или током на мозговое вещество занимает не более одной минуты.
После устранения патологического участка зонд извлекают, а на кожу в местах трепанации черепа накладывают швы. В течение двух месяцев после паллидотомии пациент должен избегать травм головы, психоэмоционального напряжения, работ, требующих применения физической силы.
Двухстороннее разрушение бледного шара ухудшает симптоматику, нарушает речь, провоцирует депрессивные состояния, поэтому обычно осуществляют одностороннюю паллидотомию.
Глубокая стимуляция мозга
Когда прием лекарственных средств не в состоянии остановить развитие симптоматики болезни Паркинсона, операция становится неизбежной. Таламотомия и паллидотомия осуществляются только односторонне, поэтому их применение не всегда приводит к желаемым результатам. Кроме того, разрушение структур центральной нервной системы сопряжено с вероятностью появления необратимых осложнений. Эффективным и щадящим способом хирургического лечения считается нейростимуляция.
Нейростимуляция – внедрение электростимулятора в определенные области головного мозга. Глубокая стимуляция позволяет заблокировать нездоровые импульсы, что положительно отражается на двигательных функциях пациента.
Глубокая стимуляция мозга назначается при ригидности мускулов, сильном треморе конечностей, замедленности движений. По сравнению с медикаментозным лечением, нейростимуляция дает стойкий эффект.
Среди преимуществ стимуляции отмечают:
- снижение доз лекарственных препаратов, а в некоторых случаях прекращение их приема;
- возможность изменения настроек в зависимости от этапа терапии;
- возможность полного извлечения системы в случае возникновения осложнений.
Вживление системы нейростимуляции проводится опытным хирургом. Процесс включает два этапа – имплантацию электродов в мозговую структуру, а также установку устройства нейростимуляции и его удлинителя под кожу в районе грудной клетки. При помощи удлинителя осуществляется доставка сигнала от стимулятора к мозгу. Возможно двухстороннее осуществление стимуляции, при этом устанавливается два комплекта электродов и удлинителей.
Электрод представляет собой тонкий провод диаметром до полутора миллиметров. Его имплантируют в область мозговой коры, куда через специальные контакты поступают сигналы от нейростимулятора. Хирург вживляет один или несколько электродов, в зависимости от тяжести состояния пациента.
Генератор импульсов имплантируется под кожу в районе грудной клетки, как правило, спустя 2-5 дней после первого этапа операции. Устройство небольшого размера включает в себя электронный генератор и аккумулятор (или батарею).
Врач настраивает устройство устанавливая полярность и частоту, амплитуду и длительность импульсов. В процессе настройки пациент сообщает врачу о своих ощущениях, что позволяет подобрать оптимальные параметры. После включения и настройки, стимулятор начинает подавать электронные импульсы в ЦНС по системе проводов.
Пульт пациента служит для включения и выключения устройства, выбора программ, проверки уровня заряда аккумулятора или батареи. Замену устройства, работающего от батарейки, осуществляют каждые 5 лет, от аккумулятора 10. Заряжают аккумулятор через каждые 1-2 недели, в течение двух часов.
Эффект после нейростимуляции наступает в течение двух месяцев. Некоторые пациенты отмечают положительную динамику уже через пару дней после включения стимулятора. Болезнь переходит в стабильное состояние на срок пять лет и более, в отдельных случаях эффект сохраняется пожизненно.
Ограничения после глубокой стимуляции
Установка нейростимулятора ограничивает диагностику МРТ, а также лечебные процедуры, осуществляемые при помощи электротоков.
Нейростимулятор может послужить причиной проблем при прохождении систем контроля на границе, в аэропортах, государственных учреждениях. Системы контроля могут повлиять на настройки устройства, поэтому если оно включено, нельзя подходить к металлоискателям или детекторам.
Пациенту выдается специальное медицинское удостоверение с идентификационным штрих-кодом. Удостоверение содержит данные о личности больного, контакты лечащего врача и информацию, которая позволяет медицинским работникам оперативно получить доступ к истории болезни.
Наркоз при болезни Паркинсона и проведение анестезии
Операции, направленные на лечение паркинсонизма, осуществляются преимущественно под местной анестезией. Общий наркоз сопровождается повышенным риском, связанным со спецификой заболевания, а также применяемыми больным медикаментами.
До оперативного вмешательства требуется провести анализ сопутствующих заболеваний, возмо жность совмещения анестезии с принимаемыми препаратами. Прием противопаркинсонических средств перед деструкцией или стимуляцией не прекращают.
В случае необходимости полного расслабления пациента, следует отдать предпочтение легким седативным препаратам. Чтобы избежать дрожи, в операционной необходимо поддерживать комфортную температуру, не допускать переохлаждения пациента.
Местное обезболивание при болезни Паркинсона предпочтительно. Во время хирургических манипуляций на мозге, больной должен быть в сознании, чтобы врач мог контролировать его речевые и двигательные функции.
Использование противорвотных средств
Чтобы устранить рвотный рефлекс врач назначает препараты на основе домперидона, антагонисты серотонина или антигистаминные деривативы. Лекарственные средства на основе метоклопрамида противопоказаны.
Результаты операции при болезни Паркинсона
Первые сутки после вмешательства больные испытывают общую слабость, неприятные ощущения в области трепанации, головокружение. В норме эти симптомы проходят спустя 12-24 часа после операции.
Уменьшение симптоматики паркинсонизма, улучшение двигательной функции наступает спустя несколько дней или недель после деструкции пораженных участков. Иногда процесс восстановления занимает 2-6 месяцев, после чего состояние пациента стабилизируется.
Уменьшается или исчезает тремор конечностей, возвращается способность нормально передвигаться, снижается ригидность мышц. Степень улучшений зависит от стадии болезни и индивидуальных особенностей пациента. Согласно исследованиям, больные отмечают улучшение своего состояния на 50-80%.
Операция не избавит от заболевания, а только снизит проявление симптомов. Несмотря на значительные улучшения состояния, следует придерживаться врачебных рекомендаций, продолжать прием лекарственных средств. Больному рекомендуется пройти курс реабилитации и не допускать инфицирования послеоперационного шва до его полного заживления.
Противопоказания
К противопоказаниям хирургического лечения относят:
- старческий возраст;
- возможность лечения консервативными методами;
- завышенные ожидания от операции;
- тяжелые формы депрессии, деменция;
- наличие кардиостимулятора.
При болезни Паркинсона оперативное лечение не назначается людям с тяжелыми сердечно-сосудистыми расстройствами, декомпенсированными поражениями печени, почек и других внутренних органов.
Последствия после операции при Паркинсона
Деструкция пораженных участков мозга может привести к вербальным нарушениям, что проявляется замедлением скорости речи и потерей четкости произношения. Больные могут испытывать общую слабость, локальное снижение чувствительности.
В ходе операции вероятны такие осложнения как инсульт, гематомы, отек тканей мозга. Эти поражения вызывают усиление тремора, нарушение зрения, паралич конечностей и другие неврологические патологии.
Опасность представляют инфекции, провоцирующие послеоперационные менингиты.
Статистические данные свидетельствуют об успешном выполнении 95% оперативных вмешательств. В 5 % случаев возникают осложнения, 1% из которых заканчивается летально.
Сколько стоит операция
Цена за выполнение односторонней паллидотомии стартует от 95 тысяч рублей, таламотомии от 100 тысяч, глубокая стимуляция мозга обойдется больному приблизительно в 1,5 миллиона рублей. Стоимость варьируется в зависимости от вида и сложности операции, условий клиники где ее выполняют, квалификации хирурга.
Это заболевание характеризуется поражением экстрапирамидной системы мозга, сопровождается истощением дофаминергической и преобладанием холинергической активности. Больные постоянно получают стимуляторы дофаминергической активности мозга (левадопа, мидантан и др.) и холинолитики (циклодол, норакин и др.).
Специфика анестезиологического пособия зависит от физиологических сдвигов, вызванных болезнью, и от медикаментозного фона.
При выборе средств для премедикации надо учитывать, что фенотиазиновые препараты снижают активность дофамина; лучше их не применять. То же самое относится к производным бутирофенона (дроперидол, галоперидол и др.), поэтому проводить нейролепсию с помощью дроперидола у больных паркинсонизмом надо осторожно [Ngai S. Н., 1972].
Учитывая вмешательство болезни и медикаментозной терапии в тонус симпатической нервной системы, в ходе анестезиологического пособия можно ожидать возникновения аритмий, несчабильной гемодинамики, более выраженных мостуральных реакций кровообращения. Лучше воздержаться от применения кетамина, тщательно контролировать ОЦК, своевременно возмещая кровопотерю и секвестрацию крови.
Применение миорелаксантов у больных паркинсонизмом не имеет особенностей, хотя описаны редкие случаи гиперкалиемии при первом введении дитилина [Gravlee G. Р., 1980].
- Вступление
- Патология нервной системы
- Болезнь Паркинсона
- Рассеянный склероз
- Боковой амиотрофический склероз
- Синдром Ландри--Гийена--Барре--Штроля
- Полиомиелит и полирадикулоневриты
- Парезы и параличи
- Тетраплегия
Похожие главы из других работ:
Врачи используют два основных подхода к лечению паркинсонизма. У каждого есть свои преимущества и недостатки, однако оба лишь смягчают симптомы заболевания, не устраняя его причины.
Болезнь Паркинсона -- прогрессирующее нейродегенеративное заболевание, которое наблюдается не так редко и составляет 1-2% у пожилых людей. Как самостоятельная нозологическая форма.
Болезнь Паркинсона (паркинсонизм) -- хроническое нейродегенеративное заболевание, сопровождающееся прогрессирующим разрушением и гибелью дофаминовых нейронов в ЦНС.
У многих больных, умерших от паркинсонизма, при вскрытии в черной субстанции обнаруживаются белковые скопления (они называются тельцами Леви по фамилии немецкого патологоанатома, открывшего их в 1912 г.).
Болезнь Рейтера (или синдром Рейтера) -- инфекционное заболевание, передающееся половым путем и характеризующееся сочетанным поражением мочеполовых органов, суставов и глаз. Причина. Болезнь Рейтера вызывается некоторыми типами хламидий.
Эпидемиология В Российской Федерации артериальная гипертензия (АГ) остаётся одной из самых актуальных медицинских проблем. Это связано и с чрезвычайно большой распространенностью заболевания (около 40% взрослого населения).
Мочекаменная болезнь является причиной 20% всех случаев гематурии. Гематурия при ней носит интермиттирующий или персистирующий характер и может быть представлена как микро-, так и макрогематурией.
Почечнокаменная болезнь часто протекает скрыто и обнаруживается случайно при рентгенологическом исследовании по другому поводу или ее первые признаки появляются тогда, когда камень имеет уже большие размеры.
Мочекаменная болезнь (нефролитиаз, уролитиаз, почечнокаменная болезнь) - хроническое заболевание, характеризующееся нарушением обменных процессов в организме и местными изменениями в мочевой системе с образованием камней.
Выделяют четыре периода тече-ния ожоговой болезни: -- ожоговый шок; -- острая ожоговая токсемия; -- септикотоксемия; -- период выздоровления (реконвалесценция).
Гранулематозное поражение желудочно-кишечного тракта локализуется чаще в одном или нескольких сегментах тонкой или толстой кишки, реже в пищеводе и желудке. Встречается у детей любого возраста.
Аддисонова болезнь (бронзовая болезнь) обусловлена прекращением или уменьшением продукции гормонов коры надпочечников. Наиболее характерным признаком заболевания является специфическая пигментация кожи (цвета загара.
Гипертоническая болезнь (эссенциальная гипертония) составляет до 90 % всех случаев хронического повышения артериального давления. В экономически развитых странах 18-20 % взрослых людей страдают гипертонической болезнью.
Гипертоническая болезнь - патология сердечно-сосудистого аппарата, развивающаяся в результате дисфункции высших центров сосудистой регуляции, нейрогуморального и почечного механизмов и ведущая к артериальной гипертензии.
Читайте также: