Позвоночник это хрящ или
Общее описание позвоночника. Первый, второй, седьмой шейный позвонок, грудной, поясничный, крестцовый и копчиковый позвонки. Соответствующие отделы.
Строение и функции позвоночного столба
Позвоночный столб, или позвоночник является частью скелета туловища и выполняет защитную и опорную функции для спинного мозга и выходящих из позвоночного канала корешков спинномозговых нервов. Главной составляющей позвоночника является позвонок. Верхний конец позвоночника поддерживает голову. Скелет верхней и нижней свободных конечностей прикрепляется к скелету туловища (позвоночник, грудная клетка) посредством поясов. В результате, позвоночник передает тяжесть тела человека поясу нижних конечностей. Таким образом, позвоночный столб выдерживает значительную часть тяжести человеческого тела. Следует обратить внимание на то, что будучи весьма прочным, позвоночный столб удивительно подвижен.
Позвоночник человека представляет длинный изогнутый столб, состоящий из ряда лежащих один над другим позвонков. Наиболее типично следующее их количество:
- шейных позвонков (С — от лат. cervix — шея) — 7,
- грудных (Th — от лат. thorax — грудь) — 12,
- поясничных (L — от лат. lumbalis — поясничный) — 5,
- крестцовых (S — от лат. sacralis — крестцовый) — 5,
- копчиковых (Со — от лат. coccygeus — копчиковый) — 4.
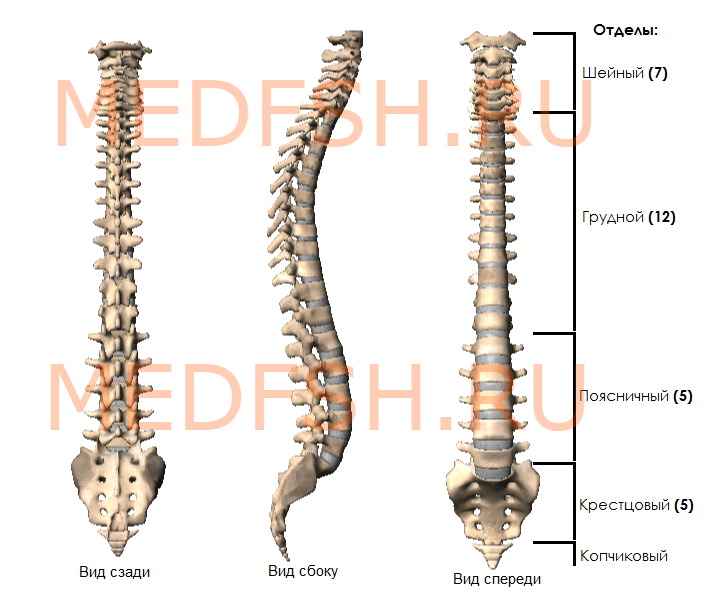
У новорожденного ребенка число отдельных позвонков 33 или 34. У взрослого человека позвонки нижнего отдела срастаются, образуя крестец и копчик.
Позвонки разных отделов отличаются по форме и величине. Однако все они имеют общие признаки. Каждый позвонок состоит из главных элементов: расположенного спереди тела позвонка и сзади дуги. Таким образом, дуга и тело позвонка ограничивают широкое позвоночное отверстие. Позвоночные отверстия всех позвонков образуют длинный позвоночный канал, в котором залегает спинной мозг. У позвоночного столба между телами позвонков находятся межпозвоночные диски, построенные из волокнистого хряща.
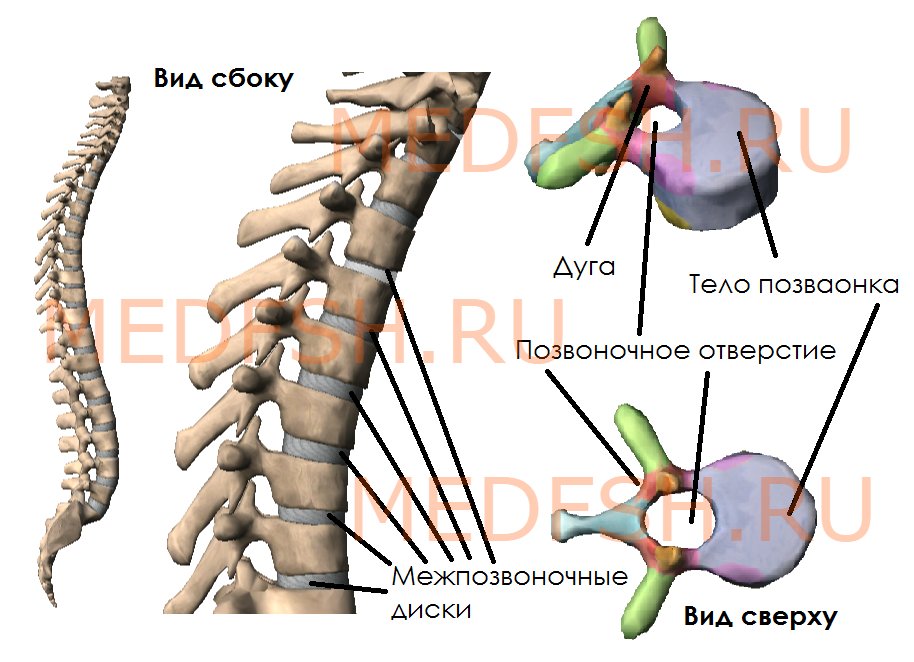
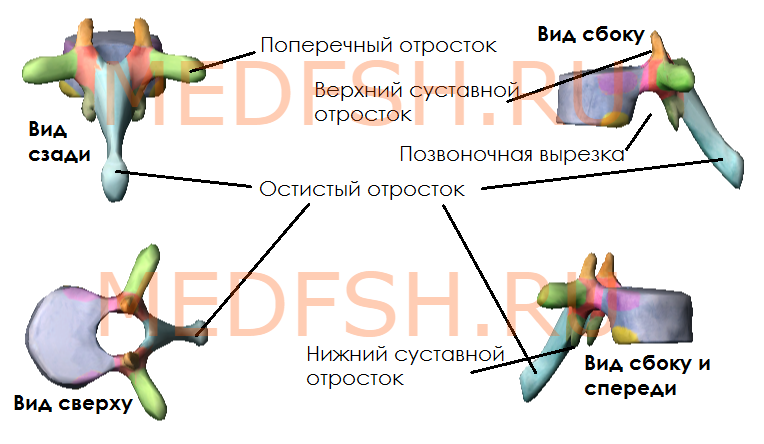
От дуги позвонка отходят отростки, кзади направляется непарный остистый отросток. Вершина многих остистых отростков легко прощупывается у человека по средней линии спины. В стороны от дуги позвонка отходят поперечные отростки и по две пары суставных отростков: верхние и нижние. При помощи их позвонки соединяются между собой. На верхнем и нижнем краях дуги вблизи ее отхождения от тела позвонка имеется по вырезке. В результате, нижняя вырезка вышележащего и верхняя вырезка нижележащего позвонков образуют межпозвоночное отверстие, через которое проходит спинномозговой нерв.
Итак, позвоночный столб выполняет опорную и защитную функцию, состоит из позвонков, разделённых на 5 групп:
- Шейные позвонки — 7
- Грудные позвонки — 12
- Поясничные — 5
- Крестцовые — 5
- Копчиковые — 1-5 (чаще 4)
Каждый позвонок, в свою очередь, имеет следующие костные образования:
- тело (расположено спереди)
- дугу (расположено сзади)
- остистый отросток (отходит назад)
- поперечные отростки (по бокам)
- две пары суставных отростков (сбоку сверху и снизу)
- верхняя и нижняя вырезки (образуются на месте отхождения суставного отростка от тела)
Шейные позвонки, особенности строения первого, второго и седьмого шейного позвонка
Число шейных позвонков у человека, как почти у всех млекопитающих, — семь.
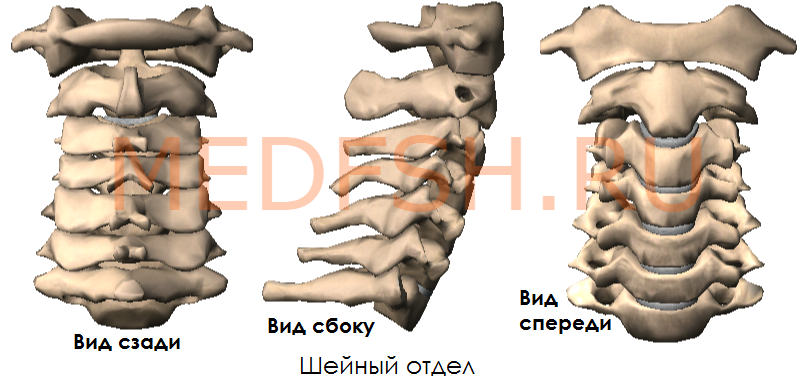
Шейные позвонки человека отличаются от других своими небольшими размерами и наличием небольшого округлого отверстия в каждом из поперечных отростков. При естественном положении шейных позвонков эти отверстия, накладываясь один на другой, образуют своеобразный костный канал, в котором проходит позвоночная артерия, кровоснабжающая мозг. Тела шейных позвонков невысокие, их форма приближается к прямоугольной.
Суставные отростки имеют округлую гладкую поверхность, у верхних отростков она обращена кзади и вверх, у нижних — вперед и вниз. Длина остистых отростков увеличивается от II к VII позвонку, концы их раздвоены (кроме VII позвонка, остистый отросток которого самый длинный).
Первый и второй шейные позвонки сочленяются с черепом и несут на себе его тяжесть.
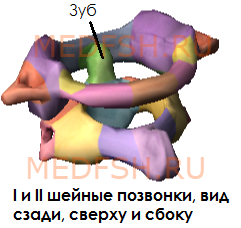
Не имеет остистого отростка, его остаток — небольшой задний бугорок выступает на задней дуге. Средняя часть тела, отделившись от атланта, приросла к телу II позвонка, образовав его зуб.
Тем не менее, сохранились остатки тела — латеральные массы, от которых отходят задняя и передняя дуги позвонка. На последней имеется передний бугорок.
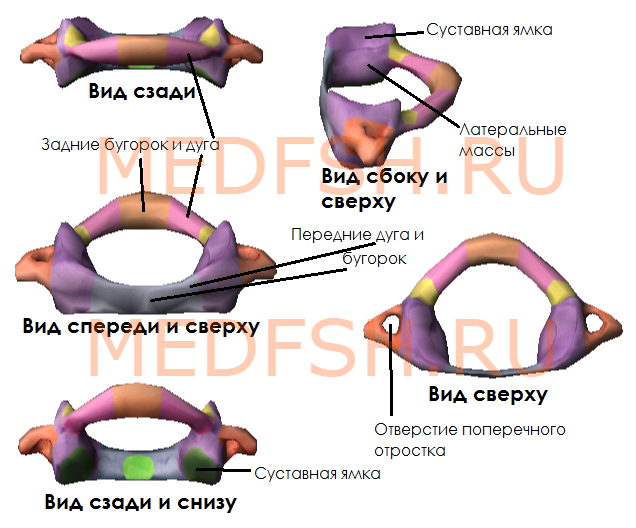
Атлант не имеет суставных отростков. Вместо них на верхней и нижней поверхностях латеральных масс находятся суставные ямки. Верхние служат для сочленения с черепом, нижние — с осевым (вторым шейным) позвонком.
При поворотах головы атлант вместе с черепом вращается вокруг зуба, который отличает II позвонок от других. Латерально от зуба на верхней стороне позвонка расположены две суставные поверхности, обращенные вверх и вбок. Они сочленяющиеся с атлантом. На нижней поверхности осевого позвонка имеются нижние суставные отростки, обращенные вперед и вниз. Остистый отросток короткий, с раздвоенным концом.
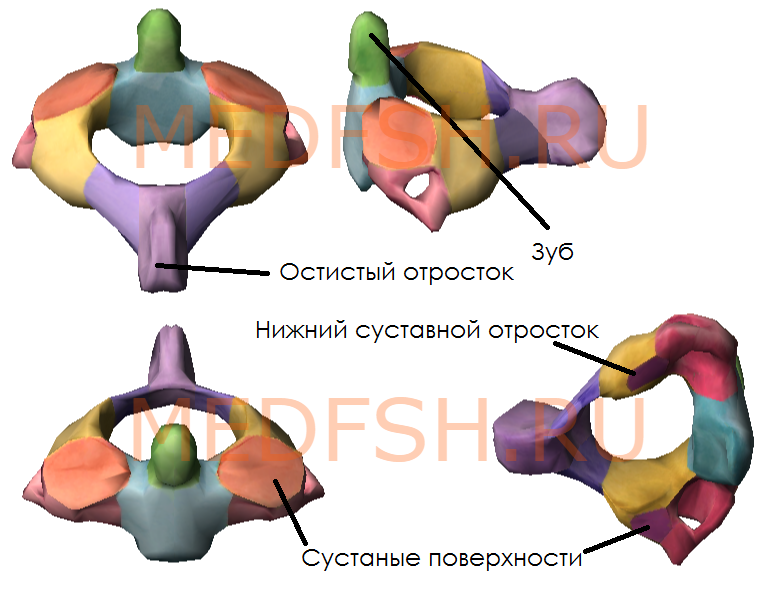
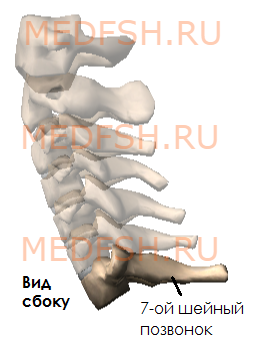
Имеет длинный остистый отросток, который прощупывается под кожей на нижней границе шеи.
Итак, шейные позвонки (7) имеют небольшой размер, на поперечных отростках имеются отверстия поперечного отростка.
Особенным строением обладает первый шейный позвонок, или атлант, а также второй и седьмой шейные позвонки.
Грудные позвонки
Двенадцать грудных позвонков соединяются с ребрами. Это накладывает отпечаток на их строение.
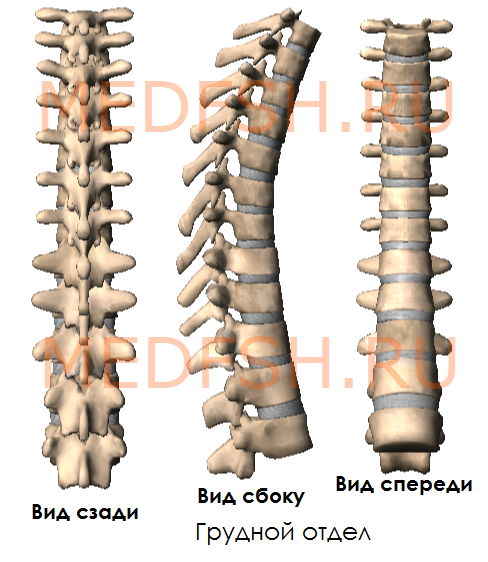
На боковых поверхностях тел имеются реберные ямки для сочленения с головками ребер. Тело I грудного позвонка имеет ямку для I ребра и половину ямки для верхней половины головки II ребра. А во II позвонке имеется нижняя половина ямки для II ребра и пол-ямки для III. Таким образом, II и нижележащее ребра, по X включительно, присоединяются к двум смежным позвонкам. К XI и XII позвонкам прикрепляются лишь те ребра, которые соответствуют им по счету. Их ямки располагаются на телах одноименных позвонков.
На утолщенных концах поперечных отростков десяти верхних грудных позвонков имеются реберные ямки. С ними сочленяются соответствующие им по счету ребра. Таких ямок нет на поперечных отростках XI и XII грудных позвонков.
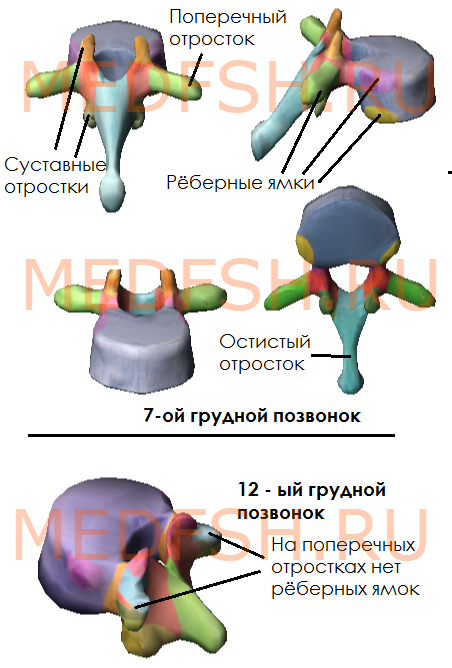
Суставные отростки грудных позвонков расположены почти во фронтальной плоскости. Остистые отростки значительно длиннее, чем у шейных позвонков. В верхней части грудного отдела они направлены более горизонтально, в средней и нижней частях опускаются почти вертикально. Тела грудных позвонков увеличиваются в направлении сверху вниз. Позвоночные отверстия имеют округлую форму.
Итак, особенности грудных позвонков:
- имеются рёберные ямки, расположенные на боковых поверхностях тела, а также на концах поперечных отростков 10-ти верхних грудных позвонков
- суставные отростки почти во фронтальной плоскости
- длинные остистые отростки
Поясничные позвонки
Пять поясничных позвонков отличаются от других крупными размерами тел, отсутствием реберных ямок.
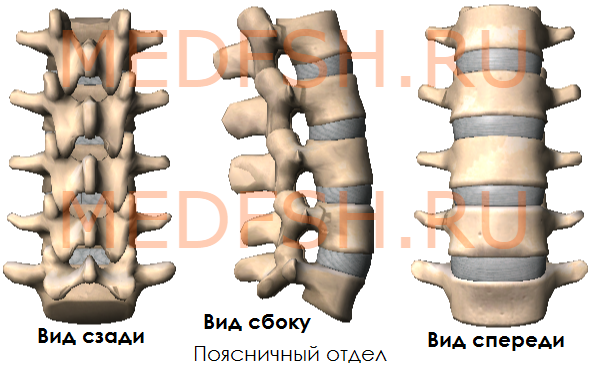
Поперечные отростки сравнительно тонкие. Суставные отростки лежат почти в сагиттальной плоскости. Позвоночные отверстия треугольной формы. Высокие, массивные, но короткие остистые отростки расположены почти горизонтально. Таким образом, строение поясничных позвонков обеспечивает большую подвижность этой части позвоночника.
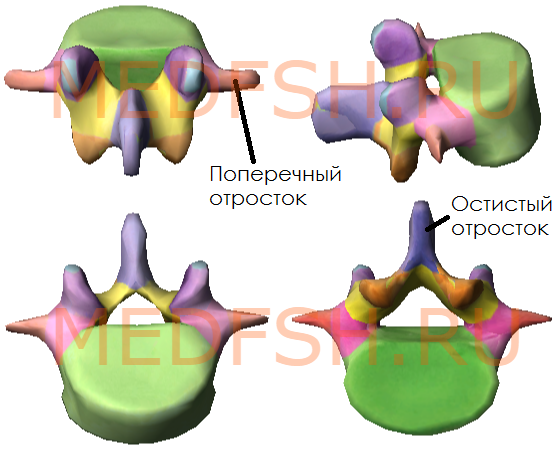
Крестцовые и копчиковые позвонки
Наконец, рассмотрим строение крестцовых позвонков у взрослого человека. Их 5, и они, срастаясь, образуют крестец, который у ребенка еще состоит из пяти отдельных позвонков.
Примечательно то, что процесс окостенения хрящевых межпозвоночных дисков между крестцовыми позвонками начинается в возрасте 13-15 лет и заканчивается только к 25 годам. У новорожденного ребенка задняя стенка крестцового канала и дуга V поясничного позвонка еще хрящевые. Сращение половин костных дуг II и III крестцовых позвонков начинается с 3-4-го года, III-IV — в 4-5 лет.
Передняя поверхность крестца вогнутая, в ней различают:
- среднюю часть, образованную телами, границы между которыми хорошо видны благодаря поперечным линиям
- затем два ряда круглых тазовых крестцовых отверстий (по четыре с каждой стороны); они отделяют среднюю часть от латеральных.
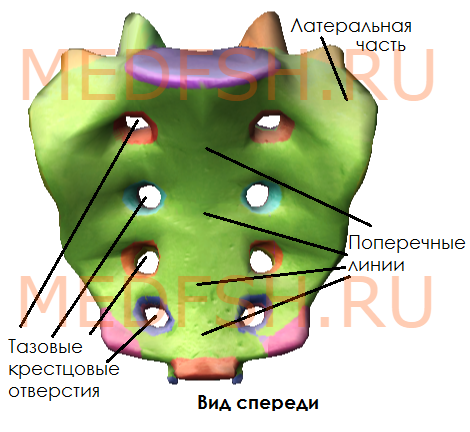
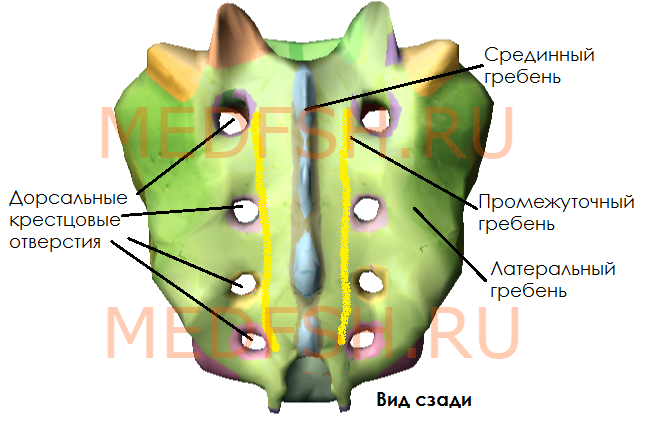
Задняя поверхность крестца выпуклая и имеет:
- пять продольных гребней, образовавшихся благодаря слиянию отростков крестцовых позвонков:
- во-первых, остистых отростков, образующих срединный гребень,
- во-вторых, суставных отростков, образующих правый и левый промежуточные гребни
- и в-третьих, поперечных отростков позвонков, образующих латеральные гребни
- а так же четыре пары дорсальных крестцовых отверстий, расположенных кнутри от латеральных гребней и сообщающихся с крестцовым каналом, который является нижней частью позвоночного канала.
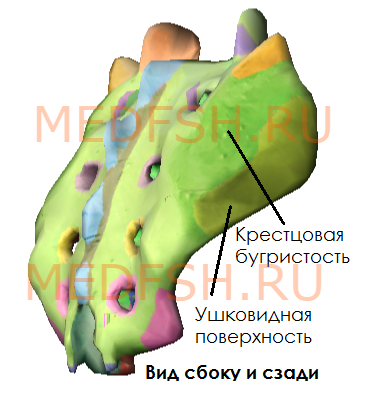
На латеральных частях крестца находятся ушковидные поверхности для сочленения с тазовыми костями. На уровне ушковидных поверхностей сзади расположена крестцовая бугристость, к которой прикрепляются связки.
В крестцовом канале находятся терминальная нить спинного мозга и корешки поясничных и крестцовых спинномозговых нервов. Через тазовые (передние) крестцовые отверстия проходят передние ветви крестцовых нервов и кровеносные сосуды. В свою очередь, через дорсальные крестцовые отверстия — задние ветви тех же нервов.
Копчик образован 1-5 (чаще 4) сросшимися копчиковыми позвонками. Копчиковые позвонки срастаются в возрасте от 12 до 25 лет, причем этот процесс идет в направлении снизу вверх.
Хрящевая ткань – одна из основных соединительных тканей, выполняющих опорные функции в организме. Она защищает наши кости от травм. Но, когда хрящ начинает деградировать, растрескиваться, терять свойства упругости, костная ткань остается без защиты.
В последствии постоянного её травмирования (удары позвонков друг о друга), в позвоночнике могут формироваться остеоартрозы и остеохондрозы. Обсудим, как же можно избежать подобных последствий и какие лекарства для восстановления хрящевой ткани позвоночника существуют.
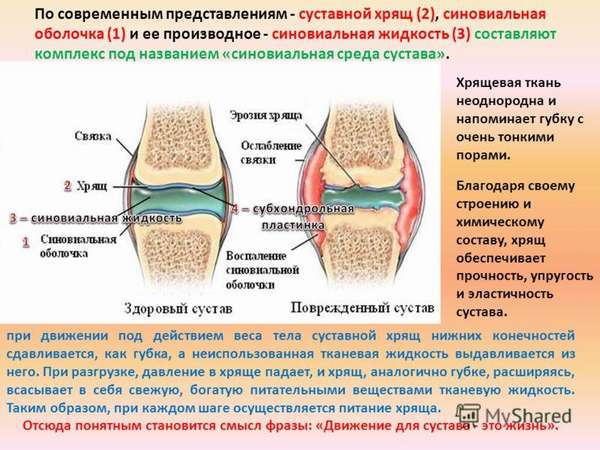
Особенности строения хрящевой ткани позвоночника
Хрящ в суставах оголен и смазан синовиальной жидкостью, которая не позволяет трению между суставами (межпозвоночными дисками) повредить структуру ткани.
Его строение способствует обратимой деформации и клеточному обмену веществ, благодаря таким компонентам в его составе как:
- Хондроциты (хрящевые клетки).
- Матрикс – межклеточное пространство, которое состоит из основного вещества и волокон.
- Межклеточное вещество, составляющее большую часть самого хряща.
Само межклеточное вещество состоит из:
- глюкозамина, отвечающего за эластичность и подвижность суставов,
- молекул протеогликанов, заполняющих промежутки между волокнами коллагена,
- хондроитина сульфат, отвечающего за эластичность межпозвоночных дисков,
- гиалуроновой кислоты, обеспечивающей упругость тканей,
- коллагена – основного белка соединительной ткани, создающего, так называемый, каркас для хрящевых молекул,
- большого количества воды.
Обновление ткани хряща происходит за счёт синовиальной жидкости внутри сустава, которая содержит все вышеперечисленные вещества, так необходимые для хрящевой ткани. Без них просто невозможна работа самого хряща.
Если сравнивать с другими тканями в организме, то особенностью строения хрящевой ткани будет то, что она содержит очень мало клеток, которые, в свою очередь, окружены огромным количеством матрикса. Также, в хрящевой ткани полностью отсутствуют кровеносные сосуды. А диски питаются веществами, содержащимися в синовиальной жидкости. Питания этого им недостаточно, и они начинают усыхать.
Позвоночник становится менее гибким и более хрупким. И именно из-за недостатка клеток, способных размножаться путем деления и медленного межклеточного обмена веществ, процесс восстановления данного вида ткани происходит очень тяжело.
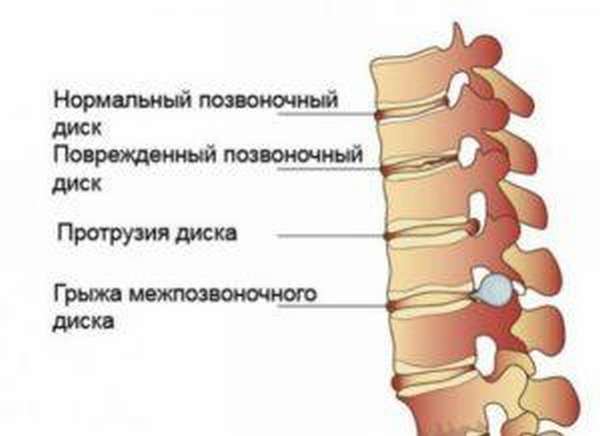
Поскольку сила трения и давления постоянно направлены на хрящевую ткань, то она с годами начинает изнашиваться. А в результате старения, вполне возможны такие заболевания как:
- межпозвоночные грыжи,
- артрозы,
- протрузии межпозвоночных дисков,
- остеоартрозы.
Вылечить подобные недуги достаточно сложно, и, как правило, удается добиться лишь временного облегчения. Поэтому так важно, чтобы хрящевая ткань восстанавливалась, воспроизводила новые клетки взамен поврежденных.
Да, регенерация – один из самых важных процессов для всего организма. Но, к сожалению, в хрящевых тканях позвоночника она происходит лишь наполовину. Полностью, именно эта ткань, не восстанавливается. Стоит также отметить, что и процесс этот довольно длительный, может достигать и десяти лет.
Узнайте, как лечить остеоартроз коленного и плечевого сустава.
Методы восстановления
Главное в лечении заболеваний позвоночника – вовремя спохватиться. Тогда велика вероятность реабилитации его функций. Для восстановления хрящевой ткани позвоночника используют и народные средства, проверенные временем, и новаторские подходы. Но все эти методики направлены на:
- активизацию кровообращения,
- восстановление и питание соединительных тканей скелета позвоночника,
- снятие нагрузки с поврежденного участка,
- изменение рациона питания,
Реабилитационные методики следующие:
- отказ от вредных привычек и смена режима питания,
- применение лекарственных препаратов,
- занятие умеренными физическими нагрузками,
- применение гормональной терапии,
- курсы массажа и физиотерапии,
- использование экспериментальных методов.
Рассмотрим как можно восстановить межпозвоночные хрящи при помощи вышеперечисленных методик.
Без изменения режима питания и образа жизни, в целом, никакие препараты не помогут. Само собой, просто необходимо избавление от таких вредных привычек, как употребление алкоголя или курение. Но, и не менее важным будет пересмотр своего рациона. Из него следует исключить:
- все кондитерские изделия, сахар и сдобу,
- соленья,
- консервированные продукты,
- копчёности,
- бобовые,
- острую, жирную пищу,
- дрожжесодержащие продукты, а также вызывающие процесс брожения в желудке,
- кофе, чай и всё, что содержит кофеин,
- алкогольные и неалкогольные газированные напитки (минеральную воду, по назначению врача, можно).
В свой рацион необходимо добавить продукты, содержащие мукополисахариды, способствующие поддержанию эластичности в тканях позвоночника:
- наваристые бульоны на мясе,
- холодец,
- кисели,
- молочные продукты,
- морепродукты и нежирную морскую рыбу,
- овощи, все фрукты, кроме винограда, и зелень,
- фруктовые желе (блюда с желатином),
- заливная рыба,
- злаки, кунжут,
- сухофрукты,
- яичный желток.
Ваш рацион должен быть полностью сбалансированным и богатым кальцием, витамином D, фосфором и другими жизненно необходимыми микроэлементами и витаминами. Также не забывайте выпивать достаточное количество жидкости для улучшения кровообращения.
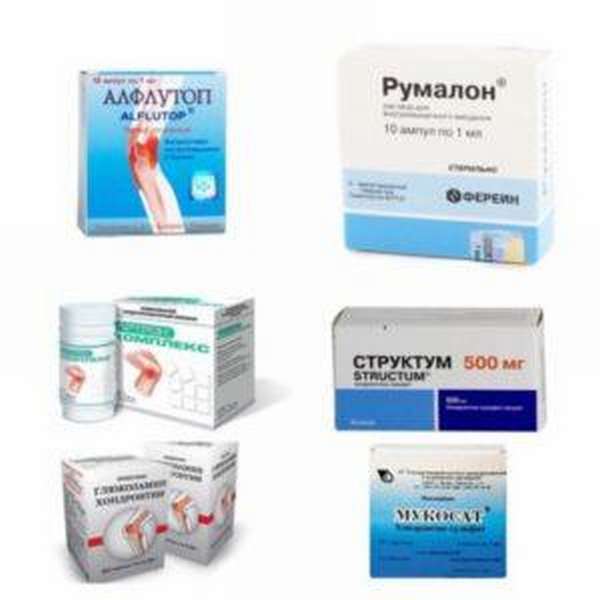
Одним из основных методов является приём препаратов для восстановления хрящевой ткани межпозвоночных дисков. Они, в свою очередь, в зависимости от химического состава, делятся на различные группы, такие как:
- хондропротекторы,
- витаминные комплексы и микроэлементы,
- гормоны.
Все они имеют и положительные и отрицательные моменты. У абсолютно всех лекарств есть побочные последствия. Назначить их может только ваш врач. Никогда не занимайтесь самолечением.
Хороший восстанавливающий эффект оказывает применение препаратов из группы хондропротекторов. Они не дают развиваться и прогрессировать дегенеративно-дистрофическим процессам, восстанавливают и наращивают хрящевую ткань.
Препараты на основе хондропротекторов подразделяются на следующие подгруппы:
- содержащие только хондроитин сульфат: Мукосат, Хондролол, Хондроксид.
- с глюкозамином – предшественником ходроитина: Флексамин, Артрон,
- с мукополисахаридом в составе: Артепарон,
- содержащие природные компоненты (костную ткань телят и морские организмы): Афлутол, Румалон,
- с комбинированным составом: Терафлекс, Триактив, Мовекс.
Положительные стороны препаратов данной группы:
- возможность выбора лекарственной формы: гели, мази, таблетки, уколы,
- эффективность от длительного приёма препаратов клинически доказана,
- хорошая переносимость препаратов,
- устраняют дефицит собственных метаболитов и оказывают положительное влияние на вещественный обмен.
Недостатки хондропротекторов:
- завышенная стоимость препаратов,
- длительность применения: от трёх до шести месяцев,
- снижение симптомов только после месяца приёма,
- трудности с проникновением действующих веществ в ткань позвоночного столба,
- необходимость комбинирования с физиопроцедурами и симптоматическими средствами.
Врач должен индивидуально подобрать препарат на основе состояния пациента и результатов клинических испытаний.
Хороший эффект, согласно клиническим испытаниям, дают уколы анаболических гормонов, таких как:
- Соматотропин, ответственный за развитие и рост молодого организма. Вырабатывается в гипофизе, но с возрастом его уровень значительно падает.
- Тиреокальцитонин, тоже гормон гипофиза, усиливающий анаболический эффект.
Особенно эффективно вводить эти два гормона одновременно. Но, как любые гормональные препараты, они имеют массу побочных эффектов. Нарушают работу почек и печени, вызывают диспропорции скелета. Поэтому данные препараты используют крайне редко и их всё еще клинически испытывают.

Умеренное применение витаминов и микроэлементов, несомненно, благоприятно сказывается на всём организме, включая соединительную ткань позвоночника. Именно для восстановления этой ткани используют такие препараты как:
Рекомендуется комплексное применение вышеперечисленных препаратов.
Медицина не стоит на месте, используя достаточно смелые экспериментальные методы для восстановления тканей позвоночника. Перечислим некоторые из них:
- Применение таких препаратов, стимулирующих адренергические рецепторы, как, например, кленбутерол. Их действия схожи с анаболическими гормонами, но не имеют таких выраженных побочных эффектов.
- Использование стволовых клеток, которые, попадая в хрящевую ткань, трансформируются в хондроциты.
- Использование поливинилпиролидона для замещения синовиальной жидкости. Этот метод сложно применим при повреждении сразу нескольких межпозвоночных дисков.
- Применение готовых хондроцитов для введения в хрящевую ткань. Но, этому может препятствовать реакция иммунитета организма на вторжение чужеродных клеток.
- Хирургическая коррекция: удаление грыж или самого межпозвоночного диска, а также замена его протезом.
ЛФК уже очень давно успешно применяют в качестве реабилитационной терапии после различных заболеваний и травм. Умеренные упражнения способствуют укреплению мышечного корсета, улучшению метаболизма и кровообращения, регенерации тканей.
Перечислим физические упражнения, которые будут полезны в реабилитационный период:
- плавание,
- пешие прогулки,
- йога,
- упражнения для вытягивания позвоночника с помощью перекладины или инверсионного стола (тренажер, который можно установить даже дома),
- упражнения на растяжку,
- расслабляющие упражнения.
Внимание! Заниматься при сильной боли или в период обострения заболеваний строго запрещено. При серьезных повреждениях позвоночника занятия должны проходить исключительно под присмотром тренера. В конце статьи вы сможете посмотреть видео с упражнениями для позвоночника.
Заключение
Когда скелет человека уже сформирован, восстановить хрящевую ткань достаточно сложно, а в некоторых случаях, и вовсе невозможно. Но, регулярно применяя различные методики, представленные в данной статье, можно добиться неплохих результатов. Главное – вовремя начать лечение. Тогда есть шанс прекратить разрушение хрящевых тканей.
Все наши кости в процессе эмбрионального (зародышевого) развития образуются из хрящей. У взрослого человека они составляют не более 2% массы тела. Кости растут благодаря диафизарному хрящу, удлиняются они до тех пор, пока не закрываются так называемые зоны роста1. Однако некоторые из них увеличиваются в течение всей жизни человека. Установлено, что постоянно растут, хотя и малыми темпами, нижняя челюсть, нос, ушные раковины, ступни ног и кисти рук.
Наиболее часто, спортсмены покидают спорт из-за травм суставно-связочного аппарата. Его слабое место — хрящ. Проблемы с позвоночником также обусловлены в основном патологией межпозвоночных хрящей.
Можно сказать, что в спортивной травматологии лечение хрящей является заботой № 1. При этом некоторые авторы считают, что восстанавливаются они не более чем на 50%, ставя, таким образом, под сомнение возможность полного восстановления спортивной работоспособности. Попробуем более подробно рассмотреть, что же такое хрящ и определить пределы и методы его регенерации.
Хрящевая ткань — одна из разновидностей соединительной ткани, которая выполняет в организме опорные функции. Непременным атрибутом хряща, за исключением суставного, является надхрящница, обеспечивающая его питание и рост. В суставах хрящ обнажен и контактирует непосредственно с внутренней средой сустава — синовиальной жидкостью. Она выполняет роль своеобразной смазки между трущимися поверхностями суставов, покрытых гладким глиаиновым хрящом. Хрящи костей и позвоночника постоянно испытывают как статическую, так и динамическую нагрузки. Хрящи носа, гортани, бронхов, фиброзных треугольников в сердце осуществляют также и опорную функцию.
Структура хряща позволяет ему испытывать обратимую деформацию и в то же время сохранять способность к обмену веществ и размножению. Главные его компоненты — хрящевые клетки (хендроциты) и внеклеточный матрикс, состоящий из волокон и основного вещества. Причем, большую часть массы хряща составляет именно межклеточное вещество.
В зависимости от преобладания коллагеновых, эластических волокон или основного вещества различают гиалиновый, эластический и волокнистый хрящ.
Особенностью хряща, по сравнению с другими видами тканей в организме является то, что в нем мало клеток и они окружены большим количеством межклеточного пространства — матрикса. Хрящ так плохо восстанавливается после повреждений именно потому, что в нем очень мало клеток, способных размножаться и основная часть репарации (восстановления) идет за счет внеклеточного матрикса. В эластическом хряще (гортани, носа, ушной раковины) содержится много эластина (из него, например, на 30% состоит ухо человека ).
Биомеханические свойства хрящей делают их высокоспецифическими и по существу уникальными компонентами опорно-двигательного аппарата.
Они:
а) принимают на себя действие внешних механических сил сжатия и растяжения; распределяют эти силы равномерно, поглощают и рассеивают их, переводя аксиально направленные силы в тангенциальные (в суставах конечностей, позвоночника и т.д.);
б) образуют устойчивые к износу поверхности сочленений скелета, участвуют в формировании смазочного аппарата в синовиальных суставах;
в) являются местом прикрепления и опорой для мягких тканей и мышц; образуют полости в местах контакта с внешней средой (хрящи носа, ушей, органов дыхания).
Считается, что хрящевой матрикс состоит из 3-х основных компонентов:
1) волокнистый коллагеновый каркас, который образует трехмерную сеть переплетений;
2) молекулы протеогликанов, которые заполняют петли волокнистого каркаса;
3) вода, свободно перемещающаяся между переплетениями каркаса и молекулами протеогликанов.
У суставного хряща нет кровеносных сосудов. Он питается диффузно, поглощая питательные вещества из синовиальной жидкости.
В чем причина низкой метаболической активности хряща? Только в одном — в малом количестве клеток (1-10%) в единице объема ткани. В пересчете на чистую клеточную массу уровень метаболизма хондроцитов ничуть не меньше, чем у других клеток организма. Особенно низким метаболизмом отличаются суставные хрящи и пульподные ядра межпозвонковых дисков. Именно эти структуры отличаются самым малым количеством хондроцитов (1% от общей массы хряща) и именно они хуже всех других восстанавливаются после повреждений.
Окислительные процессы в хряще протекают в основном анаэробным (бескислородным) путем. Так, например, хондроциты пульпозных ядер межпозвоновых дисков на 99% питаются анаэробно и лишь на 1% аэробно. В среднем же кислородные окисление в хрящевой ткани как минимум в 50 раз менее интенсивно, чем в обычных тканях организма. Анаэробный характер окисления в хондроцитах — это защитно-приспособительная реакция, сложившаяся в процессе эволюции. И это неудивительно, если учесть, что хрящ не имеет (глаиновый, фиброзный) или почти не имеет (эластический) кровоснабжения. Если начать введение кислорода в пространство, пограничное с хрящом, то диффузия в хрящ О2 не только не улучшает его трофику, но, наоборот, резко ухудшает ее.
Насколько низка метаболическая активность хряща, можно понять из следующего сравнения. Белковый состав печени полностью обновляется за 4(!) дня. Коллаген хрящей обновляется всего лишь на 50% за 10(!) лет. Поэтому становится понятным, что любая травма хрящевой ткани практически неизлечима, если только не принять специальных мер, направленных на увеличение числа хондроцитов, которые сформируют новый матрикс.
Регенерация хрящевой ткани как физиологическая, так и репаративная (восстановительная) напрямую зависит от гормонального фона и модулирующего действия тех или иных гормонов. Так, например, глюкокортикоидные гормоны угнетают анаболические реакции в хондроцитах, ингибируют синтез коллагена и протеогликанов, вызывают дефицит глауроновой кислоты в синовиальной жидкости и в матриксе. И это угнетающее действие глюкокортикоидов более выражено, если оно сочетается со сдавлением (компрессией) хряща. В принципе, в этом нет ничего удивительного, если учесть, что глюкокортикоиды подавляют гликолиз — анаэробное окисление глюкозы в хряще. Регенерация без энергетического обеспечения становится попросту невозможной. Инсулин стимулирует синтез коллагена в матриксе хрящевой ткани, однако эта стимуляция невелика и носит опосредованный характер.
Самым сильным фактором, стимулирующим как физиологический, так и репаративный синтез в хрящевой ткани является соматотропный гормон. Сродство хрящей к соматотропному гормону отсутствует как таковое. Однако под действием соматотропного гормона в печени образуется инсулиноподобный фактор роста (ИРФ-1), который и обладает собственно анаболическим действием на все ткани, включая хрящевую. Сам по себе гормон роста способен оказывать анаболическое действие на клетки лишь в том случае, если его концентрация в 2000 раз превышает физиологическую. Такое возможно только в пробирке и полностью исключается в реальной жизни. Применяя соматотропин с репаративной целью необходимо помнить, что его влияние на синтез ИРФ-1 возможно лишь в условиях нормальной работы печени, при отсутствии серьезных заболеваний, иначе ИРФ-1 просто не будет синтезироваться и введение соматотропина не даст никакого результата. Способность соматомедина усиливать регенерацию хрящевой ткани в 100 раз превышает эффект от введения в организм инсулина и тестостерона. ИРФ-1 — это единственный фактор, вызывающий деление (размножение) хондроцитов. Другие анаболические факторы организма (а их довольно много) такой способностью не обладают.
Тестостерон — основной андроген организма умеренно стимулирует биосинтетические процессы в хрящах, а эстрогены — женские половые гормоны, наоборот, тормозят ее.
Анаболические стероиды обладают способностью вызывать регенерацию хряща в намного большей степени, нежели чистый тестостерон и это неудивительно, если учесть, что они обладают анаболическим действием в несколько раз превышающим анаболическое действие тестостерона.
Интересно, что матрикс — порождение хондроцитов — живет своей самостоятельной жизнью. Он способен модулировать действие различных гормонов на хондроциты, ослабляя, либо усиливая их действие. Воздействуя на матрикс, можно изменить состояние хондроцитов как в лучшую, так и в худшую сторону. Удаление части матрикса вызывает немедленную интенсификацию биосинтеза недостающих в нем макромолекул. Более того, одновременно усиливается пролиферация (разрастание) хондроцитов. Количественные изменения в матриксе способны вызвать их качественные изменения.
Длительное ограничение движений в суставе (гипсовая иммобилизация и др.) приводит к уменьшению массы хрящей. Причина на удивление проста: в неподвижном суставе отсутствует перемешивание синовиальной жидкости. При этом диффузия молекул в хрящевую ткань замедляется и питание хондроцитов ухудшается. Недостаток прямой компрессивной нагрузки (на сжатие) так же приводит к ухудшению питания хондроцитов. Хрящу нужна хотя бы минимальная компрессионная нагрузка для поддержания нормальной трофики. Чрезмерная нагрузка на растяжение в эксперименте вызывает перерождение хряща с развитием грубых фиброзных волокон.
Очень сложное влияние на состояние внутрисуставных хрящей оказывает синовиальная оболочка. Она может как усиливать анаболизм хрящевой ткани, так и усиливать ее катаболизм. Удаление синовиальной оболочки резко ухудшает трофику хрящей, которая восстанавливается лишь после ее отрастания.
Хондроциты способны и к ауторегуляции. Они синтезируют специальные факторы роста, стимулирующие разрастание соседних хондроцитов. Пока их структура полностью не расшифрована. Известно лишь то, что они имеют полипептидную природу.
Если в шейном отделе позвоночника негативные явления развиваются с подросткового возраста, то в поясничном отделе, где нагрузка на единицу поперечного сечения намного ниже — начиная с 25-30 лет. В целом они носят такой же морфологический характер, как и в шейном отделе, но отличаются клиническими (медицинскими) признаками. В шейном отделе позвоночника сквозь поперечные отростки шейных позвонков проходят крупные артерии, питающие все основание мозга и его стволовую часть, где находится жизненно важные центры (дыхания, кровообращения и т.д.). С развитием шейного остеохондроза происходит постепенное незаметное сдавливание этих артерий с развитием недостаточности мозгового кровообращения. При этом практически не бывает (или они бывают очень редко) никаких болевых признаков процесса. В поясничном отделе позвоночника картина несколько иная. Из этого отдела выходят нервные корешки, несущие чувствительные волокна от нижних конечностей и двигательные волокна к мышцам ног. Поясничный остеохондроз прежде всего проявляется различными болевыми симптомами, нарушением чувствительности и двигательной сферы. При этом никаких жизненно важных функций организма он не нарушает. Шейный остеохондроз никакими болевыми признаками себя не обнаруживает и особых неудобств не доставляет, однако может привести к серьезным нарушениям мозгового кровообращения, вплоть до инсультов с развитием параличей.
Возрастные изменения эластических хрящей не носят фатального характера. Они выражаются в основном в оссификации — накоплении кальция и не приводят ко сколько-нибудь заметному нарушению функций.
В глиаминовых хрящах суставов уже начиная с 30-летнего возраста обнаруживается фибриляция — разволокнение хрящевой поверхности. При микроскопическом исследовании на поверхности хряща обнаруживаются разломы и расщепления. Расщепление хряща происходит как вертикальном, так и в горизонтальном направлении. При этом местами встречаются скопление клеток хрящевой ткани как ответная реакция организма на разрушение хряща. Иногда отмечается возрастное увеличение (!) толщины суставных хрящей как ответное действие на действия механических (тренировка) факторов. Возрастную эволюцию хрящей коленного сустава многие исследователи отмечают начиная уже с 40-летнего возраста. Наиболее существенное изменение, отмечаемое при старении хряща — это уменьшение содержания воды, что автоматически приводит к снижению его прочности.
Потенциальные возможности регенерации хряща достаточно велики. Он может регенерировать за счет собственного потенциала (размножение хондроцитов и рост матрикса) и, что не менее важно, за счет других видов соединительной ткани, которые имеют общее с ним происхождение. Примыкающие к хрящу ткани обладают способностью к переориентации своих клеток и превращению их в хрящеподобную ткань, которая неплохо справляется со своими функциями. Возьмем для примера самый частый вид повреждений — повреждение внутрисуставного хряща.
При поверхностных повреждениях можно добиться полного восстановления хряща применяя сильнодействующие фармакологические средства. За последние 40 лет экспериментальных и клинических работ свою высокую эффективность доказал лишь один единственный препарат — соматотропный гормон (СТГ). Он стимулирует рост хрящевой ткани в 100 раз сильнее, чем введение тестостерона и инсулина. Еще больший эффект оказывает комбинированное введение СТГ и тиреокальцитонина — особого рода гормона щитовидной железы, который усиливает репарацию как костной, так и хрящевой ткани. Исключительная эффективность действия СТГ на репарацию хряща обусловлено тем, что он стимулирует непосредственно деление хондроцитов. Используя СТГ теоретически можно довести количество хондроцитов до любого нужного количества. Они, в свою очередь, восстанавливают матрикс до необходимого объема, синтезируя все его компоненты, начиная с коллагеновых волокон и кончая протеогликанами. Недостатком СТГ является то, что его нельзя применять местно, вводя непосредственно в зону поражения хрящевой ткани, поскольку действует он опосредованно. СТГ вызывает образование в печени инсулиноподобного фактора роста (ИРФ-1) который и оказывает сильнейший анаболический эффект. Парентеральное (инъекционное) его введение вызывает рост не только поврежденных хрящей, но и нормальных тоже, а это нежелательно, ведь в организме существуют кости, в которых хрящевые зоны роста не закрываются на протяжении всей жизни. Длительное введение больших доз СТГ в сформировавшийся организм может вызвать диспропорции скелета. Хотя следует отметить, что на пораженный хрящ он действует сильнее, и явных деформаций скелета при лечении СТГ в научной литературе не встречается.
В последние годы синтезирована лекарственная формы ИРФ-1, которую все шире применяют инъекционно вместо соматотропина. Поскольку ИРФ-1 действует непосредственно на ткани (в т.ч. и на хрящевую), то возникает заманчивая перспектива использовать его для местного введения (электрофорез, ультразвук и т.д.). Такое применение ИРФ-1 позволило бы локализовать его действие местом пораженного хряща и исключить действие на здоровые хрящи организма.
Неплохое действие на восстановление хряща и окружающего его соединительной ткани оказывают анаболические стероиды (АС). По эффективности они стоят на втором месте после ИРФ-1 и соматотропного гормона, хотя непосредственно деления хондроцитов они не вызывают. Анаболические стероиды, однако, ускоряют физиологическую регенерацию и потенцируют анаболическое действие инсулина и других эндогенных анаболических факторов, блокируют действие катаболических гормонов (глюкокортикоидов). Практическое применение АС в хирургической и травматологической практике доказало их высокую эффективность. Очень жаль, что до сих пор не разработаны лекарственные формы АС для локального применения. Это позволило бы создавать высокие концентрации лекарственного вещества именно в месте повреждения и предотвращать системные (на уровне всего организма) побочные действия. К сожалению, исследования в данной сфере никем не финансируются из-за причисления АС к допинговым средствам в спорте.
Некоторые исследователи в области молекулярной биологии представили очень убедительный материал, доказывающий, что стимуляторы (2-адренергических рецепторов способны симулировать анаболические эффекты соматомединов и, в частности, по отношению к хрящевой ткани. Механизм такого действия не вполне ясен. Не исключено, что просто повышается чувствительность печени к эндогенному соматотропному гормону и возрастает синтез в печени ИРФ-1. Одним из наиболее сильных избирательных стимуляторов (2-адренергических рецепторов является кленбутерол. Этот препарат не обладает гормональными эффектами и, в то же время, оказывает хорошее анаболическое действие. Подобно ИРФ-1 он стимулирует рост хрящевой ткани и может с успехом применяться в посттравматическом восстановительном периоде. Препаратов, стимулирующих (2-адренорецепторы много, но особо хотелось бы отметить такое старое и проверенное средство как адреналин. Адреналин — гормон мозгового вещества надпочечников даже при длительном курсовом применении не вызывает привыкания. В больших дозах адреналин воздействует в основном на а-адренорецепторы. Происходит сужение сосудов кожи, повышение артериального давления, подъем уровня сахара в крови. Малые дозы адреналина не затрагивают а-адренорецепторов, стимулируют (2-адренорецепторы. Расширяются сосуды мышц, снижаются уровень сахара в крови и артериальное давление. Развивается общее анаболическое действие и, в особенности по отношению к хрящевой ткани. Ежедневное введение малых (именно малых!) доз адреналина хорошо зарекомендовало себя как средство, способствующее регенерации.
Некоторые витамины в больших фармакологических дозировках способны существенно увеличить выброс в кровь эндогенного соматотропина. Пальму первенства здесь держит никотиновая кислота (витамин РР). Внутривенное введение сравнительно небольших доз никотиновой кислоты способно увеличить базальную секрецию СТГ в 2-3 раза. Увеличивает секрецию гормона роста витамин К, только применять его необходимо в умеренных дозах, чтобы не повысить чрезмерно свертываемость крови.
1 Прекращение роста большинства костей в длину могут служить признаком того, что уже возможно лечение, например, анаболическими стероидами, которые приводят к преждевременному закрытию ростовой зоны хряща, если ростовые зоны узе закрыты, (что явствует из рентгеновского снимка лучевой кости молодого человека), то уже отсутствует опасность слишком быстро закрыть зоны роста применения стероиды, а значит, их применение можно начинать.
Читайте также:


