Оссификат в теле позвонка
а) Терминология:
1. Сокращения:
• Рекомбинантный человеческий костный морфогенетический протеин 2 (rhBMP-2)
• Тотальное замещение диска (ТЗД)
• Трансфораминальный поясничный межтеловой спондилодез (TLIF)
• Задний поясничный межтеловой спондилодез (PLIF)
2. Синонимы:
• Гетеротопическая оссификация (ГО)
• Эктопическое костеобразование
• Эктопическая оссификация
• Экстрадисковая оссификация
3. Определения:
• Нетипичная локализация новообразованной костной ткани
• Три основных варианта развития:
о Связанная с применением rhBMP-2
о Связанная сТЗД
о Поражение смежного сегмента после спондилодеза шейного отдела позвоночника
б) Визуализация:
1. Общие характеристики:
• Наиболее значимый диагностический признак:
о Тонкосрезовая КТ: плотные костные остеофиты, распространяющиеся в спинномозговой канал или невральное отверстие и вызывающие их стеноз
• Локализация:
о Поясничный отдел позвоночника
о В зоне хирургического доступа после перенесенного TLIF/PLIF в вентролатеральном отделе эпидурального пространства
о Источником оссификации являетсядугоотростчатый сустав, который становится причиной в той или иной мере выраженного стеноза неврального отверстия
• Размеры:
о От нескольких мм до нескольких см
• Морфология:
о Вариабельна, округлая форма и ровные края либо неправильная форма, напоминающая остеофиты
2. КТ при гетеротопической оссификации позвоночника:
• Бесконтрастная КТ:
о Участок костной плотности, расположенный в просвете неврального отверстия или спинномозгового канала
о Гетеротопическую оссификацию (ГО) необходимо отличать от случаев экструзии костного трансплантата или остеофитов
о Гетеротопическая оссификация (ГО) на аксиальных изображениях бывает сложно увидеть, поскольку ее нередко ошибочно принимают за нормальный корень дуги:
- На сагиттальных КТ-срезах особое внимание обращайте на костные островки, связанные с областью межпозвонкового диска
3. МРТ при гетеротопической оссификации позвоночника:
• Т1-ВИ:
о Обращайте внимание на признаки стеноза дурального мешка или неврального отверстия
о При наличии в составе оссификата жирового костного мозга в Т1-режиме его бывает сложно увидеть, так как его сигнал смешивается с сигналом окружающей жировой клетчатки
• Т2-ВИ:
о Вариабельная интенсивность сигнала в зависимости от того, насколько в составе оссификата представлены красный/желтый костный мозг
4. Рекомендации по визуализации:
• Наиболее оптимальный метод диагностики:
о КТ позволяет оценить распространенность ГО
о МРТ используется для диагностики сдавления корешков/дурального мешка
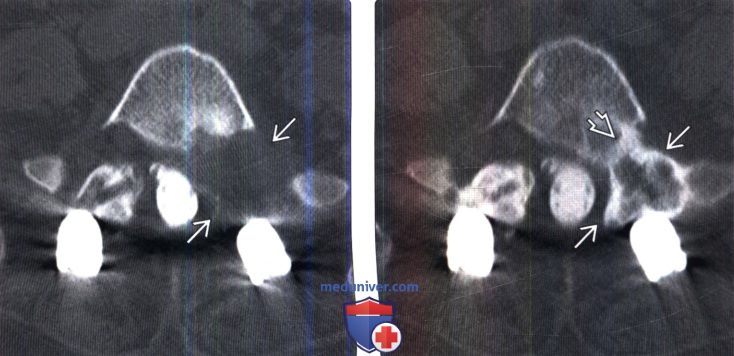
(Слева) Гетеротопическая оссификация после фасетэктомии и заднего спондилодеза напоминает картину нормального суставного отростка. Первичная КТ-миелография: крупный дефект левых задних элементов L5 позвонка после фасетэктомии.
(Справа) КТ-миелограммаэтого же пациента через два года после операции: послеоперационный дефект заполнен новообразованной костной тканью, которая поминает форму резецированного дугоотростчато-го сустава. Левое невральное отверстие стенозировано оссификатом.
в) Дифференциальная диагностика гетеротопической оссификации позвоночника:
1. Миграция или экструзия трансплантата:
• Обращайте внимание на рентгеннегативные маркеры, которыми помечены края межтеловых спейсеров
• Отсутствие костного трансплантата там, где он должен быть (межтеловое пространство)
2. Дегенеративные изменения смежных сегментов:
• Остеофиты, связанные с дегенеративным поражением смежных позвоночно-двигательных сегментов
3. Кальцифицированная грыжа диска:
• Ограниченное, округлое и/или частично кальцифицированное образование, исходящее из межпозвонкового диска
4. Кальцифицирующий миозит:
• Связь с ранее перенесенной травмой мышц
• Эпицентр кальцификации находится в толще мышцы
о Отсутствие кальцинатов в эпидуральном пространстве
5. Экзостоз:
• Кортикальные границы образования являются продолжением кортикальных стенок задних элементов позвонков
• Хрящевой колпачок (виден не всегда)
6. Костный фрагмент при переломе:
• Связь с интраоперационной травмой костных структур
• Чаще всего возникают при коррекционных маневрах в ходе коррекции деформаций позвоночника
7. Первичная остеогенная опухоль:
• Агрессивное новообразование, характеризующееся признаками деструкции и пролиферации костной ткани
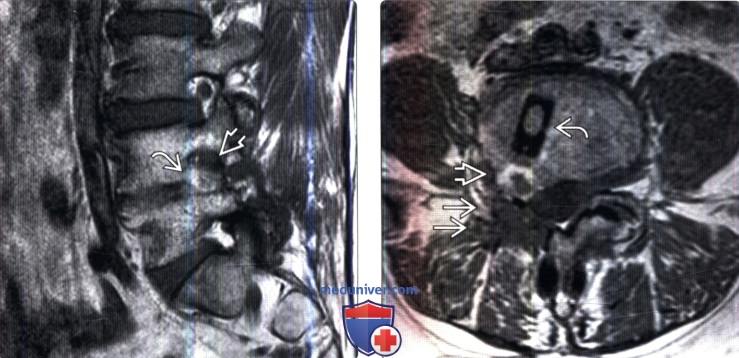
(Слева) Случай тяжелого фораминального стеноза на фоне гете-ротопической оссификации. На сагиттальном Т1-ВИ на уроне неврального отверстия отмечается выраженный стеноз отверстия на уровне L4-L5 справа со сдавлением расположенного в нем корешка L4.
(Справа) На аксиальном Т1-ВИ (этот же пациент) видны траектория хирургического доступа после выполненной ранее фасетэктомии и заднего межтелового спондилодеза, межтеловой спейсер и гетеротопический оссификат, стенозирующий невральное отверстие. Оссификат характеризуется усилением Т1-сигнала, связанным с наличием в его толще жирового костного мозга.
г) Патология:
1. Общие характеристики:
• Этиология:
о Операции на поясничном отделе позвоночника:
- Гетеротопическое новообразование костной ткани, связанное в первую очередь попаданием BMP из средства его доставки в эпидуральное пространство:
С возможным развитием центрального или фораминального стеноза
- Согласно данным одного из исследований, частота этого осложнения при одноуровневом PLIF достигает 75%:
Установка межтелового кейджа таким образом, что задний край его находился в пределах 2 мм от заднего края тела позвонка, в 77% случаев сопровождалась новообразованием костной ткани в спинномозговом канале
Четкая связь с клинической симптоматикой не установлена
- В другом исследовании частота гетеротопической оссификации (ГО) при PLIF и TLIF составила 21%:
Оссификация в области неврального отверстия наблюдалась только при TLIF
- Гетеротопическая оссификация у пациентов, перенесших ALIF, PLIF или TLIF:
4-12 мг BMP из расчета на один уровень
- Следует отметить, что на сегодняшний день не опубликовано ни одного исследования, которое бы касалось частоты ГО при межтеловых спондилодезах без использования rh-BMP-2
о Операции на шейном отделе позвоночника:
- Оссификация вдоль передней поверхности сегментов, смежных с оперированными сегментами:
11 % в группе пациентов, у которых применялся rhBMP-2, против 6% в контрольной группе
2% пациентов в другом исследовании
- Количество используемого BMP при передних спондилодезах шейного отдела позвоночника составляет 0,6-7 мг на один уровень
о Тотальное эндопротезирование межпозвонкового диска:
- Шейный отдел: Prodisc™ С (Synthes; West Chester, РА):
Достаточно значительная ГО в 45% случаев имплантации
Сегментарный анкилоз еще в 18% случаев через 4 года после операции
Отсутствие клинически значимых последствий
- Шейный отдел: Bryan® disc (Spine Experts; Los Angeles, CA):
В 60% случаев — формирование костного блока через пять лет после имплантации
Отсутствие клинически значимых последствий
Убедительное свидетельство против теории о защите смежных сегментов при ТЗД
- Шейный отдел: Mobi-C® (LDR; Troyes, France):
Частота гетеротопической оссификации (ГО) 8%
2. Стадирование, степени и классификация гетеротопической оссификации позвоночника:
• Классификация ГО:
о 0 степень: отсутствие новых оссификатов после имплантации протеза
о I степень: вновь формирующие оссификаты, которые не достигают межтелового пространства
о II степень: оссификаты достигают межтелового пространства, однако не ограничивают подвижность сегмента
о III степень: мостовидная оссификация, ограничивающая подвижность сегмента (но не полностью)
о IV степень: костный блок сегмента
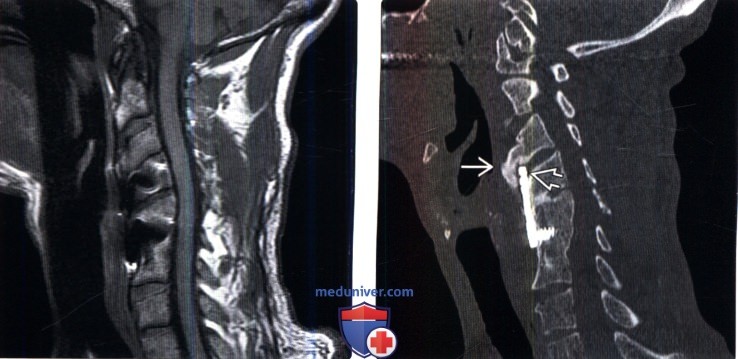
(Слева) Случай гетеротопической оссификации на уровне смежного сегмента, которая фактически привела к удлинению костного блока еще на один уровень вверх. На сагиттальном Т1-ВИ визуализируются металлоконструкции после выполненного на уровне С4-С6 переднего спондилодеза. Шейный лордоз сглажен, однако в остальном костный блок выглядит обычно. Костные аномалии в области бывшего вмешательства при МРТ нередко экранированы металлическими артефактами.
(Справа) Сагиттальный КТ-срез (этот же пациент): признаки гетеротопической оссификации, распространяющейся от тела СЗ вниз на верхний край пластинки. Пластинка в этом случае установлена не совсем корректно, верхний край ее перекрывает межпозвонковый диск.
д) Клинические особенности:
1. Клиническая картина:
• Наиболее распространенные симптомы/признаки:
о Большинство случаев гетеротопической оссификации (ГО) остаются бессимптомными
о Опубликован ряд исследований, в которых говорилось о клинически значимых случаях гетеротопической оссификации (ГО):
- Wong et al в своем исследовании отмечали наличие клинически значимой гетеротопической оссификацией (ГО) у пяти пациентов после PLIF/TLIF:
У всех из них имела место неврологическая симптоматика, трем из пяти понадобилось ревизионное вмешательство
- Chen et al. отмечали наличие клинически значимой гетеротопической оссификацией (ГО) у четырех пациентов после TLIF:
Новые жалобы у этих пациентов появились в сроки 23-51 месяц после первичного вмешательства
Боль в спине и радикулопатия
2. Лечение гетеротопической оссификации (ГО):
• Симптоматическое лечение либо ревизионное вмешательство с резекцией гетеротопических оссификатов
е) Диагностическая памятка. Следует учесть:
• Гетеротопические оссификации (ГО), содержащие жировой костный мозг легко пропустить на Т1-ВИ, на которых интенсивность сигнала жирового костного мозга может быть аналогична сигналу эпидуральной и фораминальной жировой клетчатки
• Гетеротопические оссификации (ГО) в области хирургического доступа после PLIF или TLIF на аксиальных изображениях бывает сложно увидеть, поскольку ее нередко ошибочно принимают за нормальный корень дуги:
о На сагиттальных КТ-срезах особое внимание обращайте на костные островки, связанные с областью межпозвонкового диска
ж) Список использованной литературы:
1. Simmonds МС et al: Safety and effectiveness of recombinant human bone morphogenetic protein-2 for spinal fusion: a meta-analysis of individualparticipant data. Ann Intern Med. 158(12):877-89, 2013
2. Singh К et al: Clinical sequelae after rhBMP-2 use in a minimally invasive transforaminal lumbar interbody fusion. Spine J. 13(9): 1118-25, 2013
3. Du J et al: Early follow-up outcomes after treatment of degenerative disc disease with the discover cervical disc prosthesis. Spine J. 1 1 (4):281 -9, 2011
4. Mannion RJ et al: Promoting fusion in minimally invasive lumbar interbody stabilization with low-dose bone morphogenic protein-2--but what is the cost? SpineJ. 11(6):527-33, 2011
5. Quan GM et al: Eight-year clinical and radiological follow-up of the Bryan cervical disc arthroplasty. Spine (Phila Pa 1976). 36(8):639-46, 201 1
6. Chen NF et al: Symptomatic ectopic bone formation after off-label use of recombinant human bone morphogenetic protein-2 in transforaminal lumbar interbody fusion. J Neurosurg Spine. 12(1):40-6, 2010
7. Coric D et al: Prospective study of cervical arthroplasty in 98 patients involved in 1 of 3 separate investigational device exemption studies from a single investigational site with a minimum 2-year follow-up. Clinical article. J Neurosurg Spine. 13(6):715-21,2010
8. Kim PD et al: Ectopic bone formation in the pelvis after combined anterior and posterior fusion of the spine with osteogenic protein -1 use: a case report. J Spinal Disord Tech. 23(3):21 5-20, 2010
9. Ryu. KS et al: Radiological changes of the operated and adjacent segments following cervical arthroplasty after a minimum 24-month follow-up: comparison between the Bryan and Prodisc-C devices. J Neurosurg Spine. 13(3):299-307, 2010
10. Suchomel P et al: Clinical results and development of heterotopic ossification in total cervical disc replacement during a 4-year follow-up. Eur Spine J. 19(2):307-15, 2010
11. Traynelis VC: Ectopic bone. J Neurosurg Spine. 12( 1 ):39, 2010 12. Yi S et al: Difference in occurrence of heterotopic ossification according to prosthesis type in the cervical artificial disc replacement. Spine (Phila Pa 1976). 35(16): 1 556-61, 2010
13. Beaurain J et al: Intermediate clinical and radiological results of cervical TDR (Mobi-C) with up to 2 years of follow-up. Eu rSpine J. 18(6):841 -50, 2009
14. Geibel PT et al: The use of recombinant human bone morphogenic protein in posterior interbody fusions of the lumbar spine: a clinical series. J Spinal Disord Tech. 22(5):315-20, 2009
15. Kerr EJ et al: Implant design may influence delayed heterotopic ossification after total disk arthroplasty in lumbar spine. Surg Neurol. 72(6):747-51; discussion 751,2009
16. Wong DA et al: Neurologic impairment from ectopic bone in the lumbar canal: a potential complication of off-label PLIF/TLIF use of bone morphogenetic protein-2 (BMP-2). Spine J. 8(6): 1011 -8, 2008
17. Joseph V et al: Heterotopic bone formation with the use of rhBMP2 in posterior minimal access interbody fusion: a CT analysis. Spine (Phila Pa 1976). 32(25):2885-90, 2007
18. Mehren C et al: Heterotopic ossification in total cervical artificial disc replacement. Spine (Phila Pa 1976). 31 (24):2802-6, 2006
19. Haid RW Jr et al: Posterior lumbar interbody fusion using recombinant human bone morphogenetic protein type 2 with cylindrical interbody cages. Spine J. 4(5):527-38; discussion 538-9, 2004
20. McAfee PC et al: Classification of heterotopic ossification (HO) in artificial disk replacement. J Spinal Disord Tech. 16(4):384-9, 2003
Редактор: Искандер Милевски. Дата публикации: 19.9.2019
Фибродисплазия характеризуется врожденной костной патологией и прогрессирующим гетеротопическим окостенением мышц, сухожилий, связок, апоневрозов [1, 2]. Нет расовой, половой или географической предрасположенности. Заболевание чаще возникает как результат спонтанной новой мутации. Наследственная передача — аутосомно-доминантная, возможен материнский мозаицизм.
Мутация c.617G>A приводит к замене аргинина на гистидин в кодоне 206 (p.R206H). Структурное гомологичное моделирование белков предсказывает, что замена аминокислоты приводит к конформационным изменениям рецептора, что вызывает изменение его чувствительности и активности [3].
При ФОП предполагается активная выработка КМП-4 сверх порога, что объясняет избыточную оссификацию и эктопическое образование кости постнатально [4].
Врожденные фенотипы, вызванные ФОП-метаморфозом, включают ряд врожденных уродств (деформаций) и скелетных аномалий: деформированный большой палец ноги (основной диагностический признак болезни), дисплазию метафизов, короткие фаланги, короткие большие пальцы рук, синостозы — симфалангизм пальцев, сращение поверхностей шейных суставов, сращение реберно-позвоночных суставов, проксимальные медиальные берцовые остеохондромы, короткие широкие шейки плечевой кости, редкие волосы, глухоту и др. [1, 4, 5].
В отечественной литературе имеются единичные работы о развитии ФОП у детей преимущественно в школьном возрасте [6–8].
В данном сообщении мы представляем наиболее типичные клинические и рентгенологические проявления ФОП у 30 детей в возрасте от 1,5 до 14 лет, наблюдавшихся в клинике детских болезней Первого МГМУ им. И. М. Сеченова в 1968–2010 гг. и два наблюдения с выявленным геном ФОП.
Дети поступали с жалобами на появление на голове мягких эластичных образований, которые постепенно распространялись вниз и уплотнялись. Начало болезни нередко сопровождалось недомоганием, субфебрилитетом, болезненностью очагов, постепенным их уплотнением, нарастанием общей скованности и контрактурами в области крупных суставов. Быстрота распространения процесса колебалась от 2–3 месяцев до 3–5 лет.
.jpg)
.jpg)
.jpg)
Основные лабораторные параметры, включая общие и биохимические анализы крови и мочи (в т. ч. ферменты и показатели минерального обмена), уровень гормонов щитовидной и паращитовидных желез, оставались нормальными.
Лечение проводили кортикостероидными гормонами (преднизолоном или метилпреднизолоном в дозе 0,5–1 мг/кг массы в сутки) короткими курсами, нестероидными противовоспалительными препаратами (НПВП), внутривенным введением 5% раствора динатриевой соли этилендиаминтетрауксусной кислоты (Na2 ЭДТА), 10% раствора Ксидифона внутрь и/или местно путем электрофореза или мази с Ксидифоном. В последние годы использовали бисфосфонаты нового поколения (динатрия памидронат или Аредиа, Бонефос, Бонвива и др.), антилейкотриеновые препараты (монтелукаст) и блокаторы мастоцитов (кромолин натрия).
Приводим представляющие интерес наблюдения двух пациентов, обследованных генетически в 2010 году.
Артем Т. в 14 лет обратился в клинику в июне 2010 года.
Беременность у матери протекала нормально, но в конце появились отеки ног, А/Д — 150/100 мм рт. ст, прибавка веса 10 кг. Из-за запрокидывания головки ребенка проведено кесарево сечение (12-часовой безводный период). Вес при рождении 3200 граммов, длина 53 см, окружность головки 36 см. Рос и развивался удовлетворительно. Сидит с 6 месяцев, начал ходить с 10 месяцев, первый зуб прорезался в 4 месяца. Вес в один год 11 кг, речь с 1 года 3 месяцев. Грудное вскармливание 2 месяца, далее искусственное, диагностирована анемия легкой степени.
Перенесенные болезни до школы — ветряная оспа, мононуклеоз, позже — ОРВИ.
В два года поставлен диагноз врожденная вальгусная деформация больших пальцев стоп, сделана операция выправления подвывиха первого пальца левой ноги (вставлена спица).
В 5 лет — диагноз болезнь Пертеса, экзостозная болезнь.
В 9 лет из-за ушиба (падение с велосипеда) стала плохо сгибаться в колене левая нога, стал прихрамывать.
С 11 лет выявлена двухсторонняя нейросенсорная тугоухость.
В 14 лет (апрель 2010 г.) появилось уплотнение на шее слева. На операции в кивательной мышце выявлен тяж хрящевой плотности. Материал биопсии консультирован в РОНЦ АМН РФ: данных за опухоль нет.
Консультирован в ЦИТО в мае 2010 г., установлены экзостозы и ограничение движений в левой кивательной мышце.
УЗИ левой кивательной мышцы (21.05.2010) — в средних ее отделах определяется участок измененной структуры, захватывающий всю толщу мышцы на протяжении 5,2 см с уплотнением, понижением эхогенности, не имеющий характерной волокнистой структуры; выше и ниже в мышечной ткани есть участки гиперэхогенных мышечных включений (послеоперационные изменения на фоне специфического миозита). Справа — аналогичные включения.
УЗИ передней поверхности правого бедра — на уровне верхней трети — оссификат (2,8 × 0,3 см толщины), в мягких тканях спины справа, на уровне нижних грудных позвонков — оссификат, аналогичный по структуре.
По завершении обследования и очной консультации в РОНЦ им. Н. Н. Блохина в мае 2010 года заподозрен прогрессирующий оссифицирующий миозит.
В клинике детских болезней обследован амбулаторно (15–17.06.2010 г.).
При осмотре мальчик хорошего роста, повышенного питания (рост 160 см, вес 60 кг). Жалуется на затруднение при поворотах шеи и наклонах туловища вперед. Ощущает неловкость в спине и тазе при ходьбе и ощупывании, прихрамывает на правую ногу.
Кожа чистая со следами загара. Укорочение больших пальцев стоп и кистей с подвывихом на ногах — halux valgus (рис. 4). На шее в области левой кивательной мышцы уплотнение с рубцом в центре. Поворот влево затруднен. Наклон туловища вперед лишь до горизонтального уровня. Справа на передней поверхности бедра — уплотнение в толще мышцы. На спине справа на уровне 6-го грудного позвонка определяется костный тяж длиной около 5–7 см, вне связи с позвоночником. Лимфатические узлы не увеличены. Со стороны легких, сердца, органов брюшной полости без патологии.
На R-грамме стоп: справа — вальгусная деформация первого пальца, основная фаланга значительно укорочена, утолщена, смещена латерально (подвывих). Слева — деформация головки плюсневой кости и проксимальной фаланги первого пальца (после операции). Суставная щель неравномерно сужена (рис. 4).
.jpg)
На рентгенограмме тазобедренных суставов с захватом 2/3 бедренных костей — головки бедренных костей уплощены, левая смещена латерально. Слева крыша вертлужной впадины скошена. Утолщение кортикального слоя в бедренных костях. В проекции шейки и верхней половины диафиза бедренной кости слева в мягких тканях определяются тени костной плотности. Справа — единичные тени в проекции шейки бедренной кости (рис. 5).
На рентгенограммах кистей соотношение костей не нарушено. Отмечается метаэпифизарный остеопороз. Пястные кости укорочены. Слева основная фаланга первого пальца укорочена, гипоплазия эпифиза. Средние фаланги V пальцев с искривленностью.
ЭхоКГ (17.06.2010 г). Размеры полостей сердца, толщина миокарда в пределах нормы. Систолическая и диастолическая функции левого желудочка не нарушены. Давление в легочной артерии в норме. По передней стенке правого желудочка минимальное расхождение листков перикарда в диастолу 1,3–1,5 мм. МАРС: добавочные базальные хорды и трабекула в полости левого желудочка. Удлинен евстахиев клапан.
Клинический диагноз: «Фибродисплазия оссифицирующая прогрессирующая. Классическая форма. Поздняя стадия. Врожденные аномалии больших пальцев стоп: укорочение и утолщение основных фаланг с подвывихом (Halux valgus) и кистей (укорочение пястных костей и основной фаланги первого пальца слева с гипоплазией эпифиза. Искривление средних фаланг V пальцев). Костно-хрящевые экзостозы слева на уровне нижней и верхней третей бедренной кости. Укорочение и расширение шейки бедренных костей. Множественные внескелетные костные образования (оссификаты) в толще мышц спины, бедер, шеи.
МАРС: добавочные базальные хорды и трабекула в полости левого желудочка, удлинение евстахиевого клапана. Двусторонняя нейросенсорная тугоухость.
Заключение. Ребенок наблюдался длительно с диагнозами врожденной вальгусной деформации больших пальцев стоп, экзостозной болезни, болезни Пертеса, подозрением на опухоль шеи с биопсией измененного участка кивательной мышцы; получал все прививки и вакцинации, несмотря на высокую лихорадку на каждое введение вакцин, не соблюдал необходимого щадящего двигательного режима, многократно травмировался, подвергался многочисленным лучевым исследованиям, операциям и лишь через 14 лет диагноз ФОП верифицирован и подтвержден генетически.
В настоящее время ему рекомендованы щадящий двигательный режим, отвод от всех внутримышечных инъекций, манипуляций в области нижней челюсти, профилактика ОРВИ (Арбидол, санация полости носа — промывание морской водой, капли — Маример, вакцинация при эпидемии гриппа подкожно или интраназально), плавание в бассейне с морской водой или в море, применение преднизолона (2 мг/кг 5–7 дней) и бисфосфонатов (Аредиа) при возникновении новых оссификатов, оформление инвалидности и динамическое наблюдение в специализированном стационаре.
Второй пациент — Алеша О. под наблюдением клиники с 1 года 3 месяцев.
В возрасте 5 месяцев упал с дивана без последствий. Позже в 12 месяцев повторное падение, ударился лбом. На месте ушиба возник отек размером с куриное яйцо. Получал гидрокортизон, примочки местно с эффектом.
При рентгенографии и томографии выявлена врожденная аномалия С1–С2 — деформация тел позвонков в виде платиспондилии, незаращение на уровне задних отделов (spina difida posterior), гипоплазия зубовидного отростка С2.
При ЭхоКГ размеры камер сердца выше возрастной нормы (мальчик повышенного питания: вес в 1 год 2 месяца 15 кг). Дополнительная хорда в левом желудочке.
Имеются диагностические признаки классической формы ФОП — укороченные с подвывихом большие пальцы стоп (рис. 6), а также врожденная патология шейных позвонков и гипоспадия.
.jpg)
Общие анализы крови и мочи, биохимическое исследование крови в пределах нормы.
Генетическое обследование выявило наличие мутации Arg206His в гене ACVR1, характерное для классического варианта ФОП.
Таким образом, наши наблюдения свидетельствуют о недостаточном знакомстве с ФОП врачей различных специальностей — педиатров, хирургов, ортопедов, что приводит к длительной верификации диагноза, ненужным вмешательствам и травмам мягких тканей (операции, биопсии, внутримышечное введение лекарств, вакцинации).
Обобщая литературные и собственные данные, следует считать для диагноза главным наличие врожденной патологии больших пальцев стоп (нередко в сочетании с патологией пальцев кистей) и внескелетные оссификаты. У детей дошкольного возраста, как правило, они возникают на шее, плечевом поясе и постепенно распространяются вниз. У старших детей оссификаты могут появляться в любых участках мягких тканей (мышцах, сухожилиях и др.), чаще вследствие травм любого генеза или на фоне гриппа и ОРВИ. При подозрении на ФОП необходим поиск мутаций в гене ACVR1.
К сожалению, прогноз болезни неудовлетворительный. Очень важно соблюдать все профилактические меры для избежания любых травм мягких тканей и проводить профилактику ОРВИ и гриппа, которые могут ускорить прогрессирование болезни и спровоцировать легочно-сердечную недостаточность.
В настоящее время содружеством ученых активно разрабатываются и апробируются (в эксперименте и на животных) препараты, обладающие способностью блокировать мутации в гене ACVR1, что позволит предупредить или прервать гетерогенную оссификацию и улучшить состояние пациентов.
Литература
- Mc Kusick V. A. Heritable Disorders in Connective Tissue. St. Louis C. V. Mosby (pub) (4 th ed.), 1972.
- Kaplan F. S., Le Merrer M., Glaser D. L., Pignolo R. J., Goldsby R. E., Kitterman J. A., Groppe J., Shore E. M. Fibrodysplasia ossificans progressiva // Best Pract Res Clin Rheumatol. 2008, 22: 191–205.
- Shore E. M., Xu M., Feidman G. J. еt al. A recurrent mutation in the BMP type 1 receptor ACVR1 causes inherited and sporadic fibrodisplasia ossificans progressive // Nature Genetics. 2006, 38: 525–527.
- Koster B., Pauli R. M., Reardon W., Zaidi S., Zasloff M., Morhart R., Mundios S., Groppe J., Shore E. M. Classic and atypical fibrodysplasia ossificans progressiva (FOP) phenotypes are caused by mutations in the bone morphogenetic protein (BMP) type I receptor ACVR1 // Hum Mutat. 2009, 303: 79–90.
- Kaplan F. S., Glaser D. L., Shore E. M., Deimengian G. K., Gupta R., Delai P., Morhart R., Smith R., Le Merrer M., Rogers J. G., Connor M., Kitterman J. A. The phenotype of fibrodysplasia ossificans progressiva // Clin Rev Bone Miner Metab. 2005, 3–4: 183–188.
- Борисова Т. С., Рябова Т. В., Иванова К. В. К вопросу о прогрессирующем оссифицирующем дерматомиозите у детей // Вестн. дерматол. и венерол. 1966, № 12, 15–19.
- Ложбанидзе Т. Б., Антелава О. А., Никишина И. П. и др. Прогрессирующая оссифицирующая фибродисплазия // РМЖ. 2005, № 8: 560–564.
- Рябова Т. В., Баяндина Г. Н., Утюшева М. Г., Геппе Н. А. и др. Прогрессирующий оссифицирующий полимиозит у детей. В кн.: Сложный больной в практике педиатра-ревматолога. М.: МИА. 2008. С. 86–104.
Первый МГМУ им. И. М. Сеченова, Медико-генетический научный центр РАМН, Москва
Стеноз или патологическое сужение позвоночного канала – опасное заболевание, часто сопровождающее межпозвоночные грыжи и другие патологии позвоночника. Он провоцирует сильные боли в спине, парезы и параличи, а стеноз позвоночного канала на поясничном уровне может вызывать нарушения работы тазовых органов и сопровождаться непроизвольной дефекацией и мочеотделением.
Болезнь серьезно снижает качество жизни и грозит развитием тяжелых осложнений. В короткие сроки она может приводить к возникновению компрессионной миелопатии и миелорадикулопатии. Поэтому при возникновении симптомов стеноза лечение нужно начинать незамедлительно.
Виды стеноза позвоночного канала
Существует несколько классификаций заболевания. В основу основной легло изменение сагиттального размера спинномозгового канала. Выделяют:
- Абсолютный стеноз позвоночного канала – диагностируется при его сужении до 10 мм, а площади до 75 кв. мм. Это неизменно сопровождается компрессией нервных корешков конского хвоста.
- Относительный – размер спинномозгового канала составляет не менее 12 мм, площадь – до 100 кв. мм. Признаки относительного стеноза позвоночного канала проявляются при присоединении другого фактора, провоцирующего сдавление нервных окончаний.

Возможно сочетание абсолютного и относительного стеноза позвоночного канала поясничного и шейного отдела. В таких ситуациях говорят о смешанной форме патологии.
В зависимости от расположения участка сужения различают латеральный и центральный стеноз. В первом случае наблюдается уменьшение корешковых каналов до 4 мм, во втором же происходит сокращение расстояния от задней поверхности тела позвонка до расположенного напротив него основания остистого отростка.

Также различают врожденную и приобретенную форму заболевания. Первая возникает в результате воздействия инфекционных и токсических факторов во время внутриутробного развития плода на 3–6 неделе. В таких ситуациях чаще диагностируется умеренно выраженный центральный стеноз позвоночного канала .
Приобретенный или вторичный имеет место при:
- травмах;
- дегенеративно-дистрофических изменениях межпозвоночных дисков и фасеточных суставов;
- спондилолизстезе;
- уплотнении желтых связок;
- болезни Бехтерева;
- перенесении операций на позвоночнике;
- опухолевых процессах и пр.
Вторичный дегенеративный стеноз позвоночного канала может быть как абсолютным, так и относительным. Чаще он формируется в пояснично-крестцовом отделе позвоночника на уровне L5–S1. В зависимости от причины его развития и сопутствующих признаков выделают дискогенный, дискоартрогенный и т. д.

Точное определение вида патологии с помощью МРТ-исследования позволяет выбрать лучший вариант лечения и методику проведения операции. Для получения полной картины больным также назначается рентгенография и КТ.
Методы лечения
Лечение стеноза позвоночника может проводиться консервативным или хирургическим путем. Но неумолимая медицинская статистика свидетельствует о том, что только у 32–45 % больных наблюдается положительная динамика на фоне применения лекарственных препаратов, физиопроцедур и ЛФК. Но и в таких ситуациях лечение стеноза без операции не приводит к выздоровлению, а лишь способствует незначительному улучшению состояния, особенно если диагностирован стеноз левого или правого корешкового канала L5–S1 или другого сегмента.

Консервативная терапия включает:
- прием индивидуально подобранных препаратов из группы НПВС, миорелаксантов, витамин, средств для улучшения кровотока, хондропротекторов и т. д.;
- блокады с анестетиками;
- инъекции кортикостероидов;
- фонофорез;
- магнитотерапию;
- СМТ-терапию;
- ЛФК.
Поэтому сегодня единственным способом избежать развития осложнений и добиться полного устранения неприятных симптомов является хирургическое лечение. Операция при стенозе призвана в первую очередь устранить те факторы, которые привели к сдавлению спинного мозга и его нервных корешков. С этой целью выполняются декомпресионные операции. В ходе них удаляется провоцирующая стеноз канала грыжа диска или дужки позвонков. При необходимости выполняется стабилизация позвоночника, чтобы зафиксировать позвонки в анатомически правильном положении и избежать их смещения в дальнейшем, т. е. не допустить рецидив.
Изначально применяются декомпрессионные вмешательства для устранения эффекта сдавливания позвоночного канала. Сегодня в арсенале спинальных хирургов присутствует 3 типа методик, которые применяются при грыже диска со стенозом, в том числе L5-S1:
- Классическая дискэктомия – операция, подразумевающая удаление всего межпозвоночного диска через разрез величиной до 10 см. Она показана при передней компрессии спинного мозга грыжевым выпячиванием межпозвоночного диска, в том числе если присутствует 2 грыжи и стеноз. Хотя существуют более щадящие методики удаления патологического образования, открытая дискэктомия не оставляет шансов для их повторного формирования на том же участке позвоночника, что полностью устраняет риск рецидива заболевания. На место удаленного диска устанавливается титановый имплантат (кейдж), обеспечивающих надежную поддержку позвонков.
- Микрохирургическая дискэктомия – хирургическое вмешательство преследует те же цели, что и открытая операция, но осуществляется специальными инструментами через миниатюрный разрез, длина которого не превышает 3 см. Поэтому после нее пациенты восстанавливаются легче и быстрее. Но микрохирургическая дискэктомия не позволяет произвести фиксацию позвонков системами передней стабилизации, что необходимо, когда стеноз и грыжа позвоночника взаимосвязаны.
- Декомпрессионная ламинэктомия – эта операция применяется при задней компрессии спинного мозга. Она заключается в частичном удалении дуг позвонков в области поражения с последующей стабилизацией позвоночного столба специальными конструкциями.

После того как будет снята компрессия спинного мозга хирурги должны зафиксировать позвоночник в физиологическом положении и создать оптимальные условия для правильного распределения нагрузки во время физической работы. В зависимости от локализации сужения могут использоваться:
- Системы, стабилизирующие передние опорные столбы – представляют собой кейджи с костной крошкой.
- Системы задней стабилизации – применяются для неподвижного соединения тел позвонков, титановые конструкции для транспедикулярной фиксации.

Оба варианта стабилизирующих систем считается оптимальным вариантом лечения заболевания. Межтеловые кейджи позволяют надежно крепить переднюю колонну позвоночного столба и предотвратить рецидив заболевания, а тренспедикулярные импланты надежно стабилизируют позвоночник не позволяя ему смещаться.
Так же применяют специальные системы динамической стабилизации. Существует несколько видов таких конструкций, каждая из которых имеет свою строго ограниченную область применения. Это:
- Межостистые U-имплантаты – системы такого рода созданы для динамической фиксации остистых отростков поясничного отдела, в том числе стеноз позвоночного канала на уровне L3–L4, L4–L5 может выступать показанием для их установки. U-система позволяет незначительно снизить нагрузку на задние опорные столбы и увеличить площадь позвоночного канала, благодаря чему купируются боли, спровоцированные спондилезными суставами позвонка.
- Система транспедикулярной фиксации с нетиноловыми стержнями – так же показана для установки в поясничном отделе позвоночника для надежного соединения тел смежных позвонков. Такая система дает возможность сохранить большой объем движений, благодаря чему двигательные способности практически не ограничиваются.
- Имплантат межтеловой динамический – предназначен для установки на место удаленного диска, когда диагностирован стеноз позвоночного канала шейного или поясничного отделов позвоночника. Его конструктивные особенности позволяют сохранить достаточно хороший объем движений.
Их недостатком можно считать невозможность применения при нестабильности позвоночника, так как они не обеспечивают выраженный лечебный эффект и неспособны удерживать позвонки в нужном положении.
Так же со временем их подвижность утрачивается.
Декомпрессионная операция на шейном отделе
При стенозе позвоночного канала шейного отдела симптомы практически отсутствуют. Они начинают проявляться на запущенных стадиях заболевания в виде:
Хирургическое лечение стеноза позвоночного канала шейного отдела проводится через передний или задний доступ. Выбор зависит от характера сложившейся ситуации и наличия сопутствующих патологий шеи.
Операция по устранению стеноза позвоночного канала шейного отдела передним доступом предполагает выполнение разреза на фронтальной поверхности шеи. Она выполняется из микрохирургического доступа и не травматична, требует высокого уровня мастерства от вертебролога . Обычно хирург пытается сделать его в естественной кожной складке, чтобы со временем послеоперационный рубец стал незаметным.
Показаниями для такого вида вмешательства являются:
- кифоз ;
- точно определенная на МРТ передняя компрессия;
- серьезная нестабильность позвоночника;
- дегенеративный стеноз позвоночного канала шейного отдела, охватывающий более 2-х позвонков.
Суть лечения стеноза шеи состоит в проведении дискэктомии и спондилодеза. После удаления межпозвоночного диска на его место устанавливается межтеловой имплантат который надежно удерживает позвонки.
Операции с задним доступом отличаются так же малотравматичностью и поэтому они безопасны в опытных руках. Предпологается выполнение ламинэктомии или ламинопластики, при наличии показаний также может проводиться спондилодез, а стабильность позвоночника обеспечивается установкой подходящих конструкций.

Показаниями для проведения операции задним доступом выступают:
- подтверждение результатами МРТ задней компрессии;
- конгенитальный стеноз;
- шейный кифоз ;
- обнаружение остификации задней или передней продольной связки.
Традиционно все манипуляции проводятся через задний доступ при диагностировании остеопороза, недостаточности связочного аппарата или риске развития псевдоартроза.
Декомпрессионные операции при стенозе на поясничном отделе
Признаки стеноза позвоночного канала поясничного отдела заключаются в возникновении постепенно усиливающейся боли в спине и ногах. Изначально они проявляются при ходьбе или физической работе, но впоследствии могут сохраняться и в состоянии покоя. Дискомфорт не имеет четкой локализации, поэтому больные часто описывают его как неприятное ощущение в ногах. Ноги ломят особенно ночью. Появляется симптом беспокойных ног.

Также симптомы стеноза позвоночного канала поясничного отдела могут проявляться:
До разработки и введения в спинальную практику систем стабилизации позвоночника, лечение стеноза позвоночного канала поясничного отдела осуществлялось путем проведения декомпрессионной ламинэктомии без фиксации. На сегодняшний день декомпрессивная операция в сочетании с фиксацией позвонков задними или передними системами стабилизации является золотым стандартом.

При стенозе позвоночного канала поясничного отдела операция чаще всего проводится с использованием систем транспедикулярных. Благодаря их установке удается добиться высокой функциональности прооперированной области и значительно сократить период реабилитации.
В пользу таких систем свидетельствуют и статистические данные. Согласно им, центральный и латеральный позвоночный стеноз поясничного отдела с 90% эффективностью поддается лечению путем задней декомпрессии с последующей стабилизацией.
Лечение осложненного стеноза
Наиболее часто встречаемым сопутствующим заболеванием является нестабильность позвоночника. В таких ситуациях применение лишь систем межостистой фиксации или декомпрессионных вмешательств невозможно. Это приведет к усилению расшатывания позвонков и ухудшит состояние больного. В подобных ситуациях могут применяться исключительно системы передней и задней стабилизации.

- Выполнение микродискэктомии или открытой дискэктомии в сочетании с установкой транспедикулярных имплантов.
- Стабилизация позвоночника титановым кейджем.
При своевременном проведении операции пациенты имеют высокие шансы на полное выздоровление и возвращение к полноценной жизни.
Особенности реабилитации
При завершении хирургического вмешательства пациентам разрешается подниматься на ноги в тот же день или на следующее утро. При нормальном течении восстановительного периода выписка из стационара осуществляется через 3–4 суток. Каждый пациент получает подробные рекомендации от врача, точное следование которым является залогом получения максимально выраженного эффекта от проведенных операций.
Всем пациентам рекомендовано:
- в течение всего периода реабилитации не поднимать ничего, тяжелее 3 кг;
- важно избегать вибрации, встрясок, резких движений, поворотов, однообразных движений;
- недопустимы серьезные физические нагрузки ;
- легкая бытовая работа разрешена, но при возникновении болей, слабости или других симптомов стоит обратиться к лечащему врачу;
- по рекомендации врача необходимо приступить к выполнению специальных упражнений и в дальнейшем регулярно заниматься ЛФК под руководством реабилитолога;
- через 4 недели после оперативного вмешательства следует начинать заниматься плаванием.
В среднем длительность восстановительного периода составляет 6–8 недель. Точное выполнение всех врачебных рекомендаций позволяет сократить его и ускорить возвращение пациента к привычному образу жизни.
Дети, не менее взрослых, подвержены заболеваниям позвоночника. Примерно в 6% случаев диагностирования стеноза он имеет врожденную природу. В остальных ситуациях сужение спинномозгового канала возникает вследствие дегенеративных изменений и травм. Особенности анатомии детского организма обуславливают возможность развития патологии даже в результате падения с высоты собственного роста на колени или при кувырке.
Поэтому нередко при исследовании ранее абсолютно здоровых детей, с недавних пор жалующихся на кратковременную слабость в ногах, обнаруживался стеноз позвоночного канала L4–S1. Также нередко заболевание провоцирует сколиоз и спондилез .
Основная трудность в лечении детей состоит в ранней диагностике нарушения. Поскольку они не всегда могут точно описать, что их беспокоит, или не придают тревожным симптомам должного значения, родители могут долгое время не подозревать о развитии заболевания. Часто направление на МРТ пациенты получают после выполнения ряда других исследований, проводимых по поводу возникающей хромоты или других проявлений патологии.

Лечение стеноза у детей осуществляется силами консервативной терапии. В случае ее неэффективности или угрозе развития осложнений требуется помощь хирургов. При легких формах безоперационное лечение часто дает неплохие результаты, но присутствие деформаций позвоночного столба практически всегда требует проведения хирургических вмешательств. Они направлены не только на устранение стеноза, но и ликвидацию предпосылок для его развития. Поэтому часто одновременно или в несколько этапов выполняют хирургическое лечение спондилолистеза и исправление сколиоза.
Операция при стенозе
В нашей клинике проводиться полный спектр хирургических вмешательств, показанных при стенозе, включая установку систем транспедикулярной стабилизации.
Стоимость хирургического лечения стеноза начинается от 450 000 руб и зависит от:
— Фирмы производителя имплантов;
— Клиники (где будет проведена операция) и класса палаты.
Цена включает в себя:
— Прибывание в клинике до и после операции;
— Импланты.
— Операцию;
— Наркоз;
— Послеоперационное наблюдение.
— Наблюдение и консультация на период реабилитации.
Все услуги клиники и стоимость приведены в прайсе
Читайте также:


