Локальная атрофия спинного мозга что это

МРТ позвоночника. Т2-взвешенная сагиттальная МРТ. Компрессия спинного мозга. Цветовая обработка изображения.
Изменение клинической симтоматики в хроническом периоде травмы, такое как наростание симптомов миелопатиии, повышение уровня неврологического дефицита, боли и увеличение мышечного спазма служат признаками развития поздних осложнений. Для оценки их характера показана МРТ позвоночника. Вместе с тем, надо иметь ввиду, что у таких пациентов часто имплантированы металлические конструкции, создающие артефакты. Осторожности требует исследование пациентов с нейростимуляторами.
Типичными для хронической травмы изменениями при МРТ позвоночника являются миеломаляция, киста и атрофия спинного мозга. Посттравматический отёк спинного мозга приводит к его ишемии, с последующей демиелинизаций и глиозом. Патогенетической основой формирования кисты служит интрамедуллярная гематома. При ее резорбции остаётся локальная киста. Соединение кисты со спинномозговым каналом приводит к его расширению, а адгезия к нарушению оттока ликвора.

МРТ шейного отдела спинного мозга. Миеломаляция. Т2-взвешенная сагиттальная МРТ.
Локальная киста обычно наблюдается в месте наибольшего сдавления спинного мозга кистой или грыжей диска. Чаще они наблюдаются при травмах шейного отдела позвоночника. Киста при МРТ позвоночника имеет типичный ликворный сигнал в спинном мозге и может быть окружена зоной миеломаляции.

МРТ шейного отдела позвоночника. Локальная киста. Т2-взвешенная сагиттальная МРТ.
Атрофией считается уменьшение передне-заднего измерения спинного мозга по результатам МРТ меньше 7 мм в шейном отделе и меньше 6 мм в грудном. Участок атрофии при МРТ может быть локальным или протяжённым, если он распространяется более чем на 2 позвонковых сегмента. Граница атрофии на Т2-взвешенных МРТ нечёткая. Распространённая атрофия является типичным отдалённым последствием спинальной травмы.

МРТ шейного отдела позвоночника. Компрессия и атрофия спинного мозга. Т2-взвешенная сагиттальная МРТ.
Сирингомиелитические кисты как отдалённое последствие спинальной травмы встречаются у 3-4% пациентов с неврологическими нарушениями. В целом, они относятся к отдалённым последствиям трамы, хотя известны случаи раннего формирования сирингомиелитических кист. Чаще кисты выявляются при МРТ грудном отделе спинного мозга. Замечена связь сирингомиелитических кист с деформацией позвоночного канала и посттравматическим его стенозом. В отличие от истинной сирингомиелии они развиваются на фоне атрофии и обычно не сопровождаются вздутием спинного мозга. Кисты наблюдаются с одинаковой частотой как выше, так и ниже уровня травмы. Протяжённость кисты может быть любой. Содержимое кисты обычно ликворное, но бывает и с примесью белка, что повышает сигнал от её содержимого на Т1-зависимых МРТ. На Т2-зависимых МРТ в кисте могут быть зоны потери сигнала, что отражает повышенное давление внутри неё. Отмечено, что дренаж кист в этих случаях наиболее эффективен. Изредка при МРТ в кистах встречаются перегородки.

МРТ шейного отдела позвоночника. Кистозно-атрофические изменения. Т2-взвешенная сагиттальная МРТ.
Под разрывом спинного мозга понимают отсутствие его изображение при МРТ на протяжении участка на уровне травма или ниже его. Разрывы чаще наблюдаются в грудном отделе с частотой около 4%. Полный перерыв нередко сочетается при МРТ позвоночника с миеломаляцией и атрофией окружающего спинного мозга.

МРТ грудного отдела позвоночника. Полный разрыв спинного мозга.
Спинной мозг может прикрепляться прочно к к стенке позвоночного канала, что даже приводит к его продольным разрывам. Часто при МРТ наблюдается весь комплекс изменений спинного мозга : диффузная атрофия, кисты и расщепление.
МРТ СПб позволяет выбирать место томографии, при этом специализированное нейрохирургическое учреждение – лучший выбор. При МРТ в СПб мы чаще смотрим последствия спинальной травмы в в том числе и в открытом МРТ,
Магниторезонансная томография — это неинвазивное исследование, проводимое с помощью магнитных полей и компьютера. МРТ спинного мозга — наиболее точное средство анализа здоровья позвоночника.
Зачем делается МРТ позвоночника
Магнитно-резонансная томография спинного мозга — практически единственный надежный метод исследования всех отделов позвоночника. Мельчайшие элементы на полученных снимках позволяют увидеть достоверную картину здоровья пациента. Специалист видит все нюансы анатомического строения каждого позвонка, пространства между ними, нервных пучков, межпозвоночных дисков, спинного мозга.
Магнитно-резонансную томографию спинного мозга назначают с целью анализа преимущественно мягких тканей, а компьютерную томографию (КТ) — для исследования костной системы, позвонков. Диагностика с помощью КТ не является альтернативой МРТ, так как у этих способов разное назначение. Что касается второй, то привлекает ее безопасность, ввиду отсутствия радиоактивного излучения. Исследование костей лучше проводить с помощью компьютерной томографии.
Причинами назначения на МРТ являются:
- грыжа дисков между позвонков, т. к. удается точно определить ее размер, локализацию;
- опухоли и метастазы от них в других частях тела;
- наблюдения до или после операций, особенно после удаления опухолей;
- оценка здоровья суставов, межпозвонковых дисков, дегенеративных изменений;
- травмы и переломы позвоночника;
- травмы спинного мозга (сотрясения, сдавливания, кровоизлияния, ушибы);
- инфекционные заболевания, затрагивающие позвоночник;
- врожденные аномалии и нарушения;
- болевые синдромы в спине, когда боль отдает в ноги;
- спинальные, цереброспинальные демиелинизирующие заболевания.
![]()
МРТ помогает не только диагностировать болезнь, но и анализировать состояние пациента во время лечения. В соответствии с поставленным диагнозом МРТ может быть назначена для обследования всего позвоночника или его отделов:
- шейного;
- грудного;
- пояснично-крестцового;
- копчиковой зоны.
Что показывает МРТ при исследовании спинного мозга
МРТ спинного мозга делается для диагностирования таких заболеваний, как новообразования в спинном мозге, воспалительные процессы, метастатические и первичные опухоли, сосудистые миелопатии (инфаркт спинного мозга, аномальное состояние сосудов). Кроме того, МРТ позвоночника позволяет:
- проанализировать анатомические особенности позвоночника;
- вовремя заметить патологию;
- держать под контролем введение стероидных препаратов;
- иметь полную картину состояния позвоночного столба накануне операции;
- вовремя увидеть новообразования;
- узнать о причинах появления болей в спине;
- отслеживать состояние позвоночника после операций.
МРТ для исследования головного мозга

Проводится при исследовании сосудов, нарушения кровообращения, причин возникновения болей и головокружений, проблем с координацией, при рвоте и тошноте неясного характера, потере функции слуха или зрения, нарушении памяти и интеллекта, при сбоях в мозговой активности, параличах, судорогах, болях в шейном отделе.
Кроме того, с помощью магнитно-резонансной томографии исследуются черепно-мозговые травмы, контролируется состояние больного на протяжении послеоперационного периода.
Патологии, выявляемые при обследовании головного мозга: болезнь Альцгеймера, рассеянный склероз, инсульты, нарушения функции гипофиза, болезни внутреннего уха, орбит, опухоли. При обследовании с помощью МРТ головного мозга врач получает детальную информацию о состоянии больших полушарий, мозжечка, сосудов, ликворопроводящих путей.
Заболевания раком распространяются по всему миру, поражая людей всех возрастов. МРТ головного мозга способствует обнаружению ранней стадии рака. Метод определяет место локализации опухоли, ее распространение. Желательно воспользоваться методом МРТ на ранней стадии заболевания раком с целью обнаружения метастаз.
Для наиболее глубокой проверки обследование проводится с использованием контрастного препарата. Таким способом можно выявить характер новообразования; понять, злокачественная опухоль или доброкачественная; найти метастазы, воспаления мозга, степень распространения патологии.
Атрофия в спинном мозге
Атрофией спинного мозга — это одно из изменений, типичных для хронической травмы позвоночника. Результаты МРТ показывают уменьшение параметров спинного мозга: менее 7 мм в шее и менее 6 мм в груди. Атрофированная часть спинного мозга, которая может быть растянута на два позвонка и более, называется протяженной. Меньшая величина атрофии является локальной. Атрофия представляет собой типичное последствие спинальной травмы.
МРТ шейного отдела

Шейный отдел позвоночника имеет семь позвонков, последовательно расположенных друг за другом. Целью проведения МРТ является выявление патологических изменений тканей столба позвоночника, в частности, спинного мозга и межпозвонковых грыж.
Исследование также помогает оценить физико-химические и патофизиологические процессы шейного отдела. МРТ является практически единственным приемлемым способом проанализировать здоровье шейного отдела. На полученных снимках можно увидеть:
- сдавливание спинного мозга;
- проблемы в хрящевых дисках;
- аномалии сосудов;
- злокачественные опухоли;
- патологические изменения мышечной и суставной системы;
- проблемы в нервных корешках.
Томография шейного отдела дает трехмерное изображение нервных стволов, сосудистой сети позвоночного столба. Она выявляет не заболевание остеохондрозом, а морфологические нарушения межпозвонковых дисков. Снимки срезов тканей шейного отдела, сделанные через каждые пять миллиметров, показывают патологические индексы кровоснабжения позвоночного столба. Назначается обследование в случаях:
- предположения о наличии метастаз;
- развития грыжи и протрузии дисков;
- сосудистых аномалий;
- туберкулеза;
- аутоиммунных состояний;
- стеноза спинного мозга;
- остеохондроза, спондилеза;
- травмирования шеи со смещением структуры шейного отдела и сдавления в районе спинного мозга;
- необходимости нейрохирургической операции.
Расширение центрального канала спинного мозга на МРТ
Существует врожденное расширение центрального канала спинного мозга — гидромиелия. Это проявляется в виде дистрофических процессов в спинном мозге, в толще которого формируются полости, накапливающие жидкость. Заболевание характеризуется мышечной слабостью в руках и атрофией, ограничением подвижности суставов и позвоночника, холодными конечностями. МРТ позволяет выявить расширение канала в спинном мозге на уровне шеи.
Сирингомиелия — образование пустот в продолговатом мозге, а также в веществе спинного мозга, вызванное хроническим заболеванием нервной системы. Характеризуется потерей чувствительности кожи верхней части туловища и рук. МРТ позвоночника позволяет точно диагностировать этот вид заболевания.
Сирингомиелитическая полость выглядит как веретеновидное образование с ровными контурами. Содержимое полости похоже по сигнальным свойствам на цереброспинальную жидкость. Спинной мозг в поперечном разрезе имеет увеличенный размер на уровне кистозного образования. При использовании контраста накопления вещества не происходит. МРТ гидромиелитической полости выявляет совпадение сигнальных характеристик с ликвором. Поперечник спинного мозга в районе полости не увеличен.
МРТ спинного мозга с применением контраста
Контрастное усиление процедуры МРТ позволяет оценить структуру тканей и клеток. Обычно метод с контрастом назначается при наличии онкологических заболеваний. Опухоль обнаруживается на начальной стадии, проявляются ее четкие границы, структура и консистенция.
Информативность исследования МРТ головного и спинного мозга повышается за счет контрастного вещества. Вводится препарат на основе металла гадолиния: омнискан, дотарем, магневист, гадовист. Процесс введения контрастного препарата в вену идет синхронно с ходом выполнения сканирования МРТ. Человек ощущает прохладу или прилив крови, но это длится не более двух минут. Возможен небольшой металлический привкус во рту после процедуры.
- в период реабилитации после удаления грыж в межпозвоночных дисках, рубцовая ткань проверяется на возможность рецидивов;
- когда есть доброкачественные и злокачественные новообразования;
- для обнаружения метастаз.
Правила проведения МРТ
Не разрешается проводить МРТ при беременности. Если необходимо кормление грудью, то делать это можно лишь спустя сутки или двое после процедуры сканирования. Наличие металла в виде имплантатов и приборов в теле является причиной для отказа от процедуры.
Клаустрофобия может вызвать страх перед процедурой у пациента, но для этого случая медики предлагают успокоительные средства. Иногда появляются признаки аллергии на контрастное вещество, в этом случае используют медикаменты для снятия симптомов.
Для получения качественного изображения пациент должен выдержать неподвижное состояние 15–30 минут. Излишний вес пациента может стать препятствием для прохождения томографии. Проведение МРТ после получения острых травм не рекомендуется.
Процесс проведения МРТ
Пациента укладывают на подвижный столик и фиксируют нужное положение тела специальными ремнями и валиками. Обследуемый участок тела окружают устройства с проводами, проводящими радиоволны. Это может быть какой-то отдельный участок: шейный отдел, грудной или поясничный.
При необходимости применения контрастирования медсестра вводит катетер в вену на руке пациента. Физиологический раствор во флаконе, подключенном к катетеру, отвечает за промывку системы во избежание ее закупорки. Когда приготовления закончены, стол с пациентом задвигается внутрь аппарата, а весь медперсонал выходит из кабинета.
Получив снимки, врач анализирует результат и просит пациента подождать, так как может понадобиться дополнительная серия снимков. После этого катетер вынимают. Исследование проводится на протяжении 45 минут. Оно не причиняет никакой боли. Стук и гудение аппарата могут беспокоить больного, но он вправе попросить беруши или наушники.
Обычно не требуется никакого восстановительного периода. При возникновении аллергических проявлений на контрастное вещество медперсонал оказывает необходимую помощь.
Магнитно-резонансная томография позволяет сделать высококачественную диагностику, увидеть состояние мягких тканей, содержащих воду, и позвоночника в целом. Это очень чувствительный метод исследования, позволяющий диагностировать патологии головы и спинного мозга. Он способен обозначить точные границы между здоровыми тканями и больными.
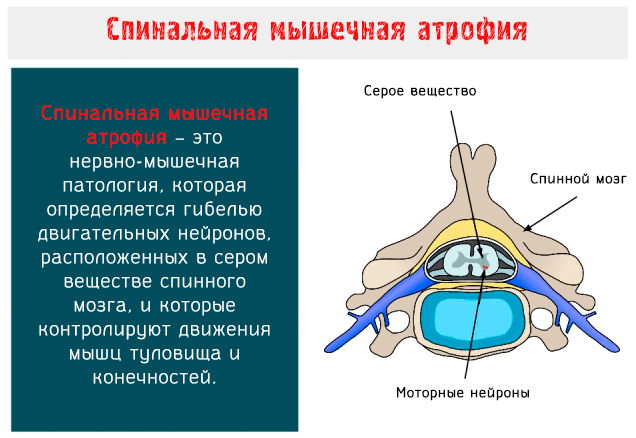
Спинальная мышечная атрофия является основной генетической причиной смерти в детском возрасте. Давайте разберемся в причинах и способах изменения жизни ребенка, а также узнаем, какие методы лечения доступны на сегодняшний день.
Что такое спинальная мышечная атрофия
Спинальная мышечная атрофия (SMA: Spinal Muscular Atrophy) – это нервно-мышечное заболевание аутосомно-рецессивного типа, характеризуется гибелью двигательных нейронов, расположенных в переднем роге серого вещества спинного мозга и в нижней части ствола головного мозга.
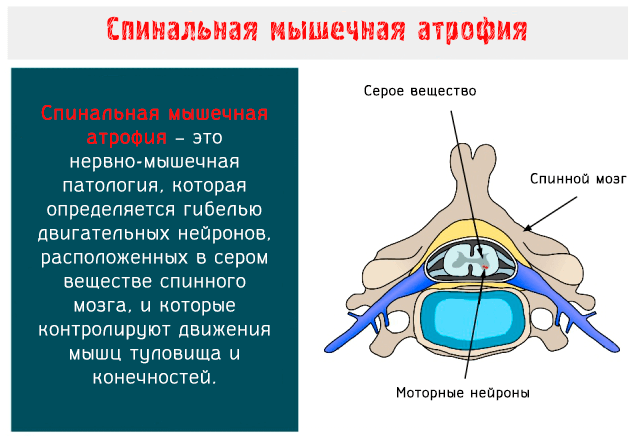
Моторные нейроны – это клетки, из которых образуются нервы, предназначенные для управления скелетными и поперечно-полосатыми мышцами глотки и гортани: когда они вырождаются, целые группы волокон подвергаются атрофии и, соответственно, результатом является мышечная слабость.
Работы глазных мышц, хотя и управляется моторными нейронами энцефального ствола мозга, не нарушается при этой болезни.
Частота спинальной мышечной атрофии колеблется от 1:6000 до 1:10000, и подвержены ей все этнические группы; является редким заболеванием, является одним из самых распространенных нервно-мышечных заболеваний, точнее вторым после дистрофии Дюшенна.
Причина спинально мышечной атрофии
Причина спинально мышечной атрофии была обнаружена в середине 90-х годов, спустя сто лет после первого описания болезни. В 95% случаев речь идёт о делеции в гене SMN1, локализованном на длинном плече хромосомы 5 (делеция – это потеря последовательности ДНК).
Поскольку спинально мышечная атрофия наследуется по аутосомно-рецессивному типу, для развития болезни человек должен получить обе копии плохого SMN1 – от матери и от отца. Таких родителей называют гетерозиготными или носителями, и они не имеют симптомов заболевания. Носители встречаются с частотой 1:50.
Ген SMN1 кодирует белок SMN, который используется в цитоплазме и ядре всех клеток и имеет решающее значение для формирования snRNP, малых ядерных рибонуклеопротеидов, компонентов сплайсинг машин.
Почему же вездесущий белок SMN является критическим фактором для выживания и надлежащего функционирования моторных нейронов?
В 2012 году Лотти и соавторы показали, что белки SMN имеют имеют важное значение для дифференциации и бесперебойной работы моторных нейронов.
Другие гипотезы были сформулированы для объяснения антиапоптической роли SMN:
- потребность в этом белке выше у моторных нейронов, чем в других тканях.
- по мнению других авторов, это можно объяснить тем, что белок SMN участвует в транспортировке вдоль аксонов РНК-связывающих белков.
Несмотря на все предположения, в настоящее время ещё неясно, какая из многих функций протеина SMN связана с развитием спинально мышечной атрофии.
4 типа спинально мышечной атрофии
Спинально мышечную атрофию классифицируют на четыре типа, в соответствии:
- с возрастом появления симптомов
- с максимальной двигательной активностью, на которую способен больной
У 25% лиц избегают точной классификации. Кроме того, у людей, страдающих от одного типа заболевания, симптомы могут существенно различаться.
Это самая тяжелая форма спинально мышечной атрофии, составляет 50% от всех случаев.
Главные её особенности:
- проявляется до 6-го месяца жизни
- ребенок имеет плохую и дряблую мышечную массу: он мало движется, потому что не может противостоять силе тяжести, не в состоянии держать голову в вертикальном положении и сидеть без поддержки
- кости хрупкие и подвержены переломам, кроме того, в позвоночнике развивается сколиоз. Проблемы с костями у пациента со спинально мышечной атрофией не удивляют, так как именно физическая активность способствует минерализации костей
- рефлекс сосания и глотания слабый, поэтому такого ребёнка трудно кормить
- грудная клетка ребенка меньше нормы из-за слабости дыхательных мышц. Кашлевый рефлекс слабый, что нарушает процесс избавления от выделений (слизи и твердые частицы, включая микробов)
У детей, страдающих от спинально мышечной атрофии 1 типа, часто развивается пневмония, так как они не в состоянии избавиться от каких-либо патогенных микроорганизмов с кашлем, а также из-за потери контроля глотательных мышц, которые не могут предотвратить попадание слюны и кусочков пищи в легкие. Повторяющие пневмонии ведут, к сожалению, к дыхательной недостаточности.
Для тех, кто страдает от этой формой патологии прогноз неблагоприятный: смерть наступает в течение 2 лет, даже самое хорошее лечение продлевает жизнь только до 5 лет.
Промежуточная форма спинальной мышечной атрофии.
Давайте посмотрим характеристики:
- проявляется между 6 и 18 месяцами
- ребенок показывает задержку в развитии моторики: не в состоянии сидеть, ему нужна поддержка, чтобы стоять, и никогда не научится ходить. Может иметь легкий тремор рук
- при этом типе также отмечается склонность к развитию сколиоза и хрупкости костей
- у некоторых маленьких пациентов дисфагия становится препятствием для поглощения достаточного для развития количества калорий
- кашлевый рефлекс может ослабнуть, облегчая возникновение респираторных инфекций
При спинальной мышечной атрофии 2 типа также высок риск развития дыхательной недостаточности. Прогрессирование симптомов настолько разнообразно, что некоторые пациенты умирают в младенчестве, другие в состоянии достичь зрелости.
Детская форма спинальной мышечной атрофии, которая:
- может возникнуть в возрасте от полутора лет
- по сравнению с предыдущими случаями, дети могут стоять и ходить самостоятельно, эта способность в некоторых случаях сохраняется до зрелого возраста
- наблюдается тремор рук и могут возникнуть проблемы с суставами и сколиоз
- нарушения дыхания и глотания проявляются менее часто, чем при 1 и 2 типе
У людей, страдающих от 3 типа спинальной мышечной атрофии, средняя продолжительность жизни сравнима со здоровыми людьми. Но, из-за проблем с питанием и низкой физической активность, часто имеют избыточный вес.
Продолжительность жизни нормальная.
Как распознать спинальную мышечную атрофию
Специалист по детской неврологии задаст ряд вопросов, чтобы получить подробный отчет о медицинской истории ребенка и его семьи, после процедуры физического обследования, чтобы оценить физическое состояние маленького пациента.
Подтверждение диагноза спинальной мышечной атрофии достигается благодаря генетическому тесту: берут образец крови и исследуют на наличие аномального гена SMN1. Тест можно использовать, чтобы найти носителей.
Поиск неисправного SMN1 также может осуществляться путём биопсии ворсинок хориона, которые являются частью плаценты, что делает возможным пренатальную диагностику в случае:
- если у пары уже был ребёнок, пострадавший от спинальной мышечной атрофии
- партнеры обнаруживают, что являются носителями, но все равно хотя родить ребёнка
Иногда бывает, что нельзя точно утверждать, что это спинальная мышечная атрофия. Тогда используют другие тесты, которые помогают провести дифференциальный диагноз между спинальной атрофией и другими патологиями нервов и мышц:
- электромиография, которая измеряет электрическую активность мышц
- мышечная биопсия, то есть изучение образцов мышечной ткани
- оценка концентрации креатина киназы, фермента уровень которого повышается при повреждении мышц
Как облегчить симптомы спинальной атрофии
На данный момент не существует лекарств для лечения спинальной мышечной атрофии, поэтому пациенты могут воспользоваться только поддерживающим лечением.
- физиотерапия
- диетология
- дыхание
Для пациентов школьного возраста важно, чтобы они активно участвовали в школьных мероприятиях, потому что их физическая инвалидность никак не влияет на способности к обучению.
Физиотерапия необходима независимо от возраста человека. Упражнения позволят максимизировать амплитуду движений, чтобы предотвратить или замедлить потерю мелкой моторики. Дети со спинальной мышечной атрофией 1 и 2 типа получают огромную пользу от гимнастики в бассейне, поскольку вода помогает стимулировать всю мышечную массу.
Пациентам с 3 типом спинальной мышечной атрофии нужны ортопедические устройства (инвалидные коляски, параподы и т.д.), которые обеспечивают удобство и мобильность. Упражнения также важны, поскольку помогают предотвратить сколиоз, который усугубляет проблемы с дыханием и движениями.
Каждый человек, страдающий от спинальной мышечной атрофии, должен иметь свой индивидуальный план питания, чтобы предотвратить последствия недостаточного или избыточного питания.
У тех детей, которые имеют большие трудности при грудном кормлении, пережевывании пищи и глотании, нужно принять меры, чтобы избежать таких осложнений, как аспирационная пневмония.
- Вы можете прибегнуть к использованию назогастрального зонда, который проходит через нос и доставляет пищу в желудок. Его относительно легко установить и снять, но он может протекать, тогда его следует заменить
- Другой вариант – гастростомия, то есть вывод трубки из желудка; является более простым в обслуживании, но процедура выполняется в операционной под наркозом.
Дыхание
Есть в этом случае для со спинальной мышечной атрофией существует три цели:
- пациенты и всех люди, которые вступают в контакт с ними, должны быть вакцинированы, например, против вируса гриппа, пневмококковой инфекции и бактерии коклюша, потому что инфекции дыхательных путей могут быть очень опасными для таких пациентов
- если кашлевый рефлекс слабым, это можно исправить с помощью специального устройства (Cough Assist): оно создает быстрое изменение давления снаружи и внутри легких, и быстрое прохождение воздуха по дыхательным путям, что имитирует кашель, освобождая дыхательные пути от секрета и микробов
- наконец, важна оценка дыхательной функции этих субъектов по степени сатурации кислорода в крови. Если количества кислорода меньше потребностей, стоит серьёзно рассмотреть идею использования механического респиратора. Изначально он используется в случае инфекции дыхательных путей и во время сна; с развитием атрфоии – весь день.
Открытие причины заболевания открыло для исследовательских групп большое направление для поиска методов лечения, направленных на максимально возможное замедление прогрессирования симптомов: повышение уровня белка SMN.
- Поскольку спинальная мышечная атрофия является моногенным заболеванием, это позволяет вмешаться в корень недуга, предоставляя пациентам функционирующий ген SMN1 (генная терапия)
- У лиц, страдающих от спинальной атрофии, но имеющих ген SMN2, можно увеличить экспрессию этого гена и заблокировать исключение экзона 7 во время сплайсинга незрелой мРНК.
В обоих случаях количество функционирующего белка SMN увеличивается.
AVXS-101 – экспериментальный препарат, разработанный биотехнологической компании Авексис, которому удалось достичь 1 этапа экспериментов на людях, при оценке безопасности лечения, и он начинает проверку эффективности.
Авексис сосредоточились на детях, страдающих от спинальной мышечной атрофии 1 типа, потому что это самый распространенный и смертельный тип заболевания.
AVXS-101 состоит из большого числа частиц адено-ассоциированного вируса серотипа 9, неспособного к репликации, но содержащего одну копию нормального гена SMN1.
Вводится в организм внутривенно, в состоянии преодолеть гематоэнцефалический барьер и достичь моторных нейронов.
Молекула ДНК, переносимая каждым вирусным вектором, производится в лаборатории. Она не изменяет ДНК пациента; содержит промотор, т.е. последовательность, которая способствует транскрипции ДНК в РНК, и гарантирует постоянное производство протеина SMN.
Анализ промежуточных данных, опубликованных Авексис в апреле 2016 года показывает, что:
Спинальная мышечная атрофия – одно из самых опасных генетически обусловленных заболеваний, которое обнаруживается у младенцев, подростков, взрослых.

Страшно узнать, что малыш никогда не будет сидеть, стоять, бегать. Еще страшнее видеть, как нормально растущий и развивающийся ребенок вдруг начинает медленно угасать, постоянно падать, через несколько месяцев не может подняться по лестнице, а однажды теряет способность просто встать.
Спинальная мышечная атрофия — что это
Врачи объединяют несколько видов наследственных заболеваний, характеризующихся нарушением движения, в одну группу под названием спинальная мышечная атрофия. В МКБ-10 они идут под кодом G12 с дополнительными указаниями на тип болезни.
Спинальная мышечная атрофия — это разнородная группа наследственных заболеваний, протекающих с поражением / потерей двигательных нейронов передних рогов спинного мозга.
По данным исследователей, около 0,01-0,02% детей рождаются с диагнозом СМА. Чаще патология встречается у мальчиков и мужчин.
Обнаруживается спинальная мышечная атрофия преимущественно у детей в раннем возрасте. Однако некоторые формы заболевания начинают проявляться только у подростков или уже взрослых людей. Коварство патологии заключается в том, что она постепенно, день за днем отбирает у больных то, что они сумели добиться.
Впервые патологию описал Г. Вердниг. Он обратил внимание на равностороннюю атрофию спинного мозга, его передних рогов, корешков периферических нервов в 1891 г. Уже в следующем году Дж. Хоффман сумел доказать, что речь идет о самостоятельном заболевании. В середине XX в. исследователи Е. Кугелберг и Л. Веландер описали патологию, которая возникает в позднем возрасте и имеет более благоприятный прогноз.
Симптомы
Каждый вид СМА имеет свои особенные признаки, однако существуют некоторые симптомы, которые позволяют объединить разнородные заболевания в одну группу. Это:
- Нарастающая слабость мышц и их атрофия.
- При заболевании, проявившемся после 1-2 лет, заметна деградация уже достигнутых способностей, например, бега, ходьбы.
- Тремор пальцев. Дрожь наблюдается и на языке.
- Деформация скелета.
- Сохранность интеллектуального и психического здоровья у большинства больных.

Виды СМА
Возраст, время проявления симптомов, особенности течения патологии, прогноз позволяют выделять несколько видов заболеваний.
Данная форма патологии описывается редко, часто его объединяют с первым типом СМА. Болезнь – врожденная. Характеризуется полным отсутствием движений, сухожильных рефлексов, слабостью мышц, ограниченным движением суставов коленей. С самого рождения наблюдаются дыхательные нарушения.
Часто диагноз путают с перинатальной энцефалопатией или родовыми травмами. Однако в последних двух случаях дети достаточно быстро адаптируются, их состояние становится лучше. У детей со СМА улучшения не возникают, в большинстве случаев они умирают, не дожив до месяца, от осложнений.
Патология первого типа имеет очень тяжелое течение. Ее называют также болезнью Верднига-Гоффмана. Диагностирован этот тип может быть от рождения до 6 месяцев. Отмечается слабость мышц, их периодическое подергивание – последнее увидеть достаточно трудно из-за достаточно большого слоя жирового слоя. Дрожь может периодически пробегать по языку малыша.
Наблюдается ухудшение рвотного, сосательного, глотательного рефлекса, нарушение слюноотделения. Младенец не может кашлять, громко кричать. Часто сопровождается тяжелыми дыхательными нарушениями, пневмонией.
Грудная клетка у таких детей имеет более плоскую форму из-за слабо развитых мышц груди.
Малышей со спинальной амиотрофией Верднига-Гоффмана легко узнать по позе лягушонка. Бедра и плечи отведены, локти и колени согнуты.
К 6 месяцам ребенок может научиться держать головку, но практически никогда не сможет самостоятельно сесть, встать, ходить. Проблемы с глотанием вызывают сложности в кормлении.
Часто именно это заболевание сопровождается олигофренией, врожденными нарушениями работы сердца, небольшим размером головы.
Патология второго типа обнаруживается у малышей в возрасте от полугода до полутора-двух лет. Болезнь Дубовица характеризуется слабостью и тремором в глубоких отделах мышц, дрожью пальцев, языка, ограничением объема движения конечностей. Детей отличает маленький вес, задержка развития. Они сидят, сами кушают, но вставать и ходить не могут.
Болезнь носит прогрессирующий характер. Со временем слабеют мышцы груди, шеи, исчезают сухожильные рефлексы, отмечаются нарушения глотания, слабый голос. Больного можно узнать по свисающей головке.

Патологию Кугельберга-Веландера диагностируют часто после 2 лет. Она считается относительно легкой формой СМА, многие больные доживают до 30-40 лет. Человек стоит, однако дается ему это с трудом из-за очень слабых мышц. Происходит постепенная атрофия мышц.
Ребенок до 10-12 лет развивается нормально, потом начинает спотыкаться, падает, теряет способность заниматься спортом, бегать, выходить из дома, просто перемещаться без инвалидного кресла. Больного мучают периодические судороги конечностей. Развивается сильный сколиоз, изменяется форма грудной клетки.
Часто у таких пациентов происходят переломы, отмечается ограниченный объем движения суставов.
К четвертому типу относят бульбоспинальную амиотрофию Кеннеди, дистальную амиотрофию Дюшенна-Арана, а также перонеальную амиотрофию Вюльпиана. Заболевания обычно диагностируются в возрасте 35-40 лет, иногда возрастные границы расширяются от 16 до 60 лет. Больной отмечает постепенную потерю мышечной силы, угасание рефлексов сухожилий, видимые сокращения мышц.
При атрофии Дюшенна-Арана прежде всего поражаются кисти рук. Амиотрофию Вюльпиана можно узнать по формированию крыловидных лопаток.
Причины и механизм развития заболевания
Спинальная амиотрофия развивается из-за мутировавшего SMN гена пятой хромосомы. Если оба родителя – его носители, существует 25%-ная вероятность, что ребенок родится больным.
Мутация гена SMN приводит к нарушению синтеза белка, в результате чего происходит разрушение мотонейронов спинного мозга. Нервные импульсы не проходят к мышцам, которые из-за бездействия атрофируются, человек теряет способность двигаться.
Считается, что теряет работоспособность сначала глубоко расположенная мускульная ткань.
Диагностика
Наиболее точным методом определения спинально-мышечной атрофии у детей является анализ ДНК. Он проводится как у родившегося малыша, так и во время внутриутробного развития. Дополнительно проводятся следующие исследования:

Если у молодых людей, планирующих рождение ребенка, есть родственники с патологией СМА, им рекомендовано пройти генетическую экспертизу.
Лечение
Основная цель исследований, направленных на терапию спинальной мышечной амиотрофии, связана с повышением уровня белка SMN. В настоящее время лекарственные препараты проходят испытания, и официальная российская медицина их не использует.
Лечение сегодня включает лекарства, которые улучшают прохождение нервных импульсов. Назначаются ноотропные препараты, основная задача которых – улучшение работы головного мозга. Назначаются биологически активные добавки, способствующие улучшению обмена веществ. Показана витаминотерапия, в частности, прием витаминов группы Б.
Средства влияющие на нервно-мышечную проводимость:
- Альфа-липоевая кислота
- Ацетил Л-карнитин
- Альфа-глицерофосфохолин
Витамины и витаминные комплексы:
- Тиамин (B-1)
- Пиридоксин (B-6)
- B-комплекс

Важными методами лечения являются массаж, физиотерапия, нейромышечная стимуляция. Назначается ЛФК. Физические упражнения помогают поддержать силу, с другой стороны, выполнение их в обществе, походы в бассейн помогают социализироваться, общаться с другими людьми.
Больным СМА рекомендовано соблюдение диеты. Продукты питания – источник веществ, необходимых мышцам. Так, необходимые аминокислоты содержатся в зерновых, мясе, рыбе, грибах, орехах, кисломолочных продуктах. Рекомендованы блюда из овса и пшеницы, бурого риса.
Естественному поддержанию и росту мышц поможет шпинат, брокколи, сельдь, лук, грейпфрут, арбуз. Для повышения тестостерона мужчинам рекомендуют принимать укроп, пастернак, женьшень, петрушку.
Прогноз
То, как будет развиваться болезнь, сколько лет проживет ребенок, зависит от ее типа.
При атрофии типа один прогноз крайне неблагоприятен. Около 50% малышей не доживают и до двух лет. Не больше 10% детей с болезнью Верднига-Гоффмана могут дожить до пяти лет. Причиной гибели чаще всего становится воспаление легких, остановка дыхания, сердца.
Пациенты, которым диагностирована болезнь Дубовица, живут в среднем до 10, иногда 12 лет. Около 30% малышей умирают, не достигнув четырех лет.
При SMA III типа детская смертность встречается реже. У многих пациентов симптомы появляются в предподростковом-подростковом возрасте. Через несколько лет они перестают ходить. Далее, по нарастающей, отмечается атрофия мышц внутренних органов, в том числе дыхательных.
Считается, что заболевание IV типа не влияет на продолжительность жизни, тем не менее, оно ведет к инвалидизации.
Профилактика
Мер, направленных на профилактику и предотвращение развития СМА, не существует. Женщина, ожидающая рождения ребенка, может заподозрить проблему, обратив внимание на слабость шевелений плода. Проведенный ДНК-анализ может подтвердить или развеять подозрения. При необходимости проводится медицинская комиссия, которая может порекомендовать прерывание беременности. Врач обязательно рассказывает о заболевании, его течении и последствиях.
После диагностики заболевания у уже родившегося ребенка его окружают заботой и вниманием. Использование системы искусственной вентиляции легких, отсасывателей мокроты, специальных приспособлений для движения малыша, который может передвигаться, помогают улучшить качество жизни и помочь ребенку жить. Рекомендовано регулярно делать массаж, физиопроцедуры. Детей даже с ограниченными движениями возят в бассейн.
Спинальная амиотрофия – опасная, пока не поддающаяся лечению патология. Она характеризуется атрофией мышц. Возникает в разном возрасте. Прогноз в большинстве случаев неблагоприятный.
Для подготовки статьи использовались следующие источники:
Селиверстов Ю. А., Клюшников С. А., Иллариошкин С. Н. Спинальные мышечные атрофии: понятие, дифференциальная диагностика, перспективы лечения // Журнал Нервные болезни — 2015
Лепесова М. М., Ушакова Т. С., Мырзалиева Б. Д. Дифференциальная диагностика спинальной мышечной амиотрофии первого типа // Вестник Алматинского государственного института усовершенствования врачей — 2016
Читайте также:



