Левобупивакаин для спинальной анестезии
Русское название
Латинское название вещества Левобупивакаин
Химическое название
(2S)-1-бутил-N-(2,6-диметилфенил)пиперидин-2-карбоксамид
Брутто-формула
Фармакологическая группа вещества Левобупивакаин
Нозологическая классификация (МКБ-10)
Код CAS
Фармакология
Фармакодинамика
Левобупивакаин является местным анестезирующим средством и анальгетиком длительного действия. Средство блокирует передачу импульсов в сенсорных и моторных нервных волокнах в основном за счет влияния на потенциалзависимые натриевые каналы клеточной мембраны, хотя также вызывает блокаду калиевых и кальциевых каналов. Кроме того, левобупивакаин препятствует передаче и проведению импульсов в других тканях: наиболее важную роль в развитии клинических нежелательных реакций играет его действие на ССС и ЦНС .
В исследованиях клинической фармакологии с использованием модели блокады локтевого нерва было продемонстрировано, что левобупивакаин обладает таким же клиническим эффектом, что и бупивакаин.
Данные по безопасности левобупивакаина при его введении на протяжении более 24 ч ограничены.
Фармакокинетика
Распределение. В клинических исследованиях у человека показано, что распределение левобупивакаина после в/в введения в основном такое же, как и у бупивакаина. Концентрация левобупивакаина в плазме крови зависит от дозы и пути введения, поскольку на его абсорбцию из места введения влияет васкуляризация ткани.
Исследования in vitro показали, что связывание левобупивакаина с белками плазмы крови у человека составляет >97% при концентрациях от 0,1 до 10 мкг/мл.
В исследованиях клинической фармакологии при в/в введении 40 мг левобупивакаина средний T1/2 составил приблизительно (80±22) мин, Cmax — (1,4±0,2) мкг/мл и AUC — (70±27) мкг·мин/мл.
При эпидуральном введении 75 мг (0,5%) и 112,5 мг (0,75%) левобупивакаина, а также при блокаде плечевого сплетения левобупивакаином в дозе 1 мг/кг (0,25%) и 2 мг/кг (0,5%) средние Cmax и AUC0–24 приблизительно пропорциональны вводимой дозе. После эпидурального введения 112,5 мг (0,75%) левобупивакаина средние значения Cmax и AUC составляют 0,58 мкг/мл и 3,56 мкг·ч/мл соответственно.
Vd после в/в введения составляет 67 л.
Метаболизм. Левобупивакаин в значительной степени подвергается метаболизму, в моче и кале неизмененный левобупивакаин не обнаруживается. Основной метаболит левобупивакаина — 3-гидроксилевобупивакаин — выделяется в мочу в виде конъюгатов с глюкуроновой кислотой и сернокислого эфира. В исследованиях in vitro было показано, что в метаболизме левобупивакаина участвуют изоферменты цитохрома CYP3A4 и CYP1A2 , при этом образуются дисбутиллевобупивакаин и 3-гидроксилевобупивакаин соответственно. Данные исследования показали, что метаболизм левобупивакаина и бупивакаина сходен.
Рацемизации левобупивакаина in vivo не выявлено.
Выведение. После в/в введения левобупивакаин выводится в среднем в течение 48 ч на 95%, причем 71% выводится через почки, 24% — через кишечник.
При введении в виде в/в инфузии общий плазменный клиренс левобупивакаина равен 39 л/ч, а конечный T1/2 — 1,3 ч.
Особые группы пациентов
Нарушение функции почек. Данных по фармакокинетике левобупивакаина у пациентов с нарушением функции почек нет. Левобупивакаин в значительной степени подвергается метаболизму, в неизмененном виде в моче не обнаруживается.
Применение вещества Левобупивакаин
Анестезия при хирургических вмешательствах:
- при больших хирургических вмешательствах, например эпидуральная (включая анестезию во время операции кесарева сечения), интратекальная, блокада периферических нервов;
- при малых хирургических вмешательствах, например инфильтрационная анестезия, перибульбарная блокада (в глазной хирургии).
Купирование болевого синдрома: продолжительная эпидуральная инфузия, однократное или многократное болюсное эпидуральное введение для купирования болевого синдрома, особенно в послеоперационном периоде или во время родов.
Обезболивание: подвздошно-паховая и подвздошно-подчревная блокада.
Противопоказания
Дозировка 7,5 мг/мл противопоказана в акушерской практике из-за повышенного риска развития кардиотоксичности при введении бупивакаина.
Ограничения к применению
Введение левобупивакаина длительностью >24 ч; у пациентов, получающих антиаритмические ЛС со свойствами местных анестетиков (мексилетин) и антиаритмические ЛС III класса (при применении последних могут развиться аддитивные токсические эффекты); регионарная анестезия у пациентов с сердечно-сосудистыми заболеваниями, в частности с тяжелыми нарушениями ритма сердца; у пациентов с предшествующими заболеваниями ЦНС; у пациентов, получающих другие местные анестетики или ЛС , схожие по структуре с местными анестетиками амидного типа; у пациентов с заболеваниями печени или снижением печеночного кровотока (например при циррозе или алкогольной болезни печени).
Применение при беременности и кормлении грудью
Левобупивакаин нельзя применять для парацервикальной блокады у беременных. Учитывая случаи брадикардии у плода при введении бупивакаина, нельзя исключить такое же действие левобупивакаина.
Клинических данных по применению левобупивакаина в I триместре беременности нет. В исследованиях на животных тератогенное действие левобупивакаина зарегистрировано не было. В то же время, при системном уровне экспозиции левобупивакаина, который достигается в клинической практике у человека, у животных были зафиксированы эмбриотоксические эффекты. Потенциальный риск для человека неизвестен. Таким образом, при отсутствии явной необходимости женщинам в I триместре беременности левобупивакаин вводить не следует.
В настоящее время существует обширный опыт применения бупивакаина при акушерских хирургических вмешательствах (при беременности и родоразрешении), при этом эмбриотоксическое действие бупивакаина не зарегистрировано. Дозировка 7,5 мг/мл противопоказана в акушерской практике из-за повышенного риска развития кардиотоксичности при введении бупивакаина.
Сведений о том, проникает ли левобупивакаин в грудное молоко, нет. Однако левобупивакаин, по всей видимости, выделяется при лактации в меньшей степени, чем бупивакаин. Грудное вскармливание возможно после проведения местной анестезии.
Побочные действия вещества Левобупивакаин
Нежелательные реакции на левобупивакаин согласуются с таковыми при применении ЛС данного класса. Наиболее частыми нежелательными реакциями являются снижение АД , тошнота, анемия, рвота, головокружение, головная боль, повышение температуры тела, боль во время процедуры введения препарата, боль в спине и дистресс-синдром плода (при применении в акушерской практике).
Нежелательные реакции, зарегистрированные в клинических исследованиях и пострегистрационных наблюдениях, приведены в соответствии с поражением органов и систем органов и частотой возникновения: очень часто (≥1/10); часто (≥1/100, 1 .
Со стороны органа зрения: неизвестно — нечеткость зрения, птоз 2 , миоз 2 , энофтальм 2 .
Кардиологические нарушения: неизвестно — AV-блокада, остановка сердечной деятельности, желудочковые тахиаритмии, тахикардия, брадикардия.
Со стороны сосудов: очень часто — снижение АД; неизвестно — гиперемия 2 .
Со стороны дыхательной системы, органов грудной клетки и средостения: неизвестно — остановка дыхания, отек гортани, апноэ, чихание.
Со стороны ЖКТ : очень часто — тошнота; часто — рвота; неизвестно — гипестезия слизистой оболочки полости рта, нарушение контроля функции сфинктеров 1 .
Со стороны кожи и подкожных тканей: неизвестно — ангионевротический отек, крапивница, зуд, гипергидроз, ангидроз 2 , эритема.
Со стороны скелетно-мышечной системы и соединительной ткани: часто — боль в спине; неизвестно — подергивание мышц, мышечная слабость.
Со стороны почек и мочевыводящих путей: неизвестно — дисфункция мочевого пузыря 1 .
Беременность, послеродовые и перинатальные состояния: часто — дистресс-синдром плода.
Со стороны половых органов и молочной железы: неизвестно — приапизм 1 .
Общие расстройства и нарушения в месте введения: часто — повышение температуры тела.
Лабораторные и инструментальные данные: неизвестно — снижение сердечного выброса, изменения на ЭКГ .
Травмы, интоксикации и осложения манипуляций: часто — боль во время процедуры.
1 Может быть симптомом или признаком синдрома конского хвоста.
2 Может быть симптомом или признаком преходящего синдрома Горнера.
При применении местных анестезирующих средств нежелательные реакции развиваются редко, однако они могут возникать при передозировке или случайной внутрисосудистой инъекции, и при этом носят серьезный характер.
Описаны случаи перекрестной чувствительности к различным анестезирующим средствам группы амидов.
Случайное интратекальное введение левобупивакаина может привести к спинальной анестезии на очень высоком уровне.
Влияние левобупивакаина на ССС связано со снижением проводимости, возбудимости и сократимости миокарда. Обычно этому предшествуют признаки токсического поражения ЦНС , например судороги, в то же время в редких случаях остановка сердца возникает без какой-либо продромальной неврологической симптоматики.
Поражение нервной системы — редкое, но хорошо диагностируемое осложнение регионарной, в частности эпидуральной и спинальной, анестезии. Оно может быть связано с прямым повреждением спинного мозга или спинномозговых нервов, синдромом передней спинномозговой артерии, введением раздражающего вещества или нестерильного раствора. В редких случаях изменения сохраняются постоянно.
Существуют данные о сохраняющейся слабости или сенсорных нарушениях, ассоциированных с введением левобупивакаина. Иногда эти явления могут быть постоянными. Сложно определить, возникают ли такие длительные эффекты вследствие токсического действия или являются признаками недиагностированного травматического повреждения во время хирургического вмешательства, либо при влиянии других механических факторов, в частности установки катетера и манипуляций с ним.
Однако невозможно определить, были ли эти явления связаны с действием левобупивакаина, механической травмой спинного мозга либо корешков спинномозговых нервов или взятием крови в области основания позвоночника.
Также описаны редкие случаи преходящего синдрома Горнера (птоз, миоз, энофтальм, односторонняя потливость и/или гиперемия), связанного с применением местных анестезирующих средств, включая левобупивакаин. После прекращения терапии эти явления исчезают.
Взаимодействие
В исследованиях in vitro показано, что в метаболизме левобупивакаина участвуют изоферменты цитохрома Р450 CYP3A4 и CYP1A2 . На превращения левобупивакаина могут влиять ингибиторы изофермента CYP3A4 (в частности кетоконазол) и CYP1А 2 (например метилксантины), хотя клинические исследования таких взаимодействий не проводились.
Левобупивакаин следует с осторожностью применять у пациентов, получающих антиаритмические ЛС со свойствами местных анестетиков (мексилетин) и антиаритмические ЛС III класса (при применении последних могут развиваться аддитивные токсические эффекты).
Клинические исследования по оценке действия левобупивакаина в комбинации с эпинефрином не проводились.
Передозировка
После случайной внутрисосудистой инъекции местного анестезирующего средства может возникнуть немедленная токсическая реакция. При передозировке левобупивакаина Cmax достигается только через 2 ч после введения (в зависимости от места инъекции), таким образом, симптомы токсического поражения могут быть отсроченными. Возможно продление его эффекта.
Системные нежелательные реакции после передозировки или непреднамеренного внутрисосудистого введения местного анестезирующего средства длительного действия включают в себя симптомы поражения ССС и ЦНС .
Воздействие на ЦНC. При развитии судорог следует немедленно ввести в/в тиопентал натрия или диазепам, титруя дозу соответствующим образом. Тиопентал натрия и диазепам тоже могут оказывать угнетающее действие на ЦНС , дыхательную и сердечно-сосудистую деятельность. Таким образом, при введении этих ЛС может развиваться апноэ. ЛС , блокирующие нервно-мышечную передачу, следует применять только в том случае, если есть возможность поддержания проходимости дыхательных путей и лечения пациента с полной миорелаксацией.
При отсутствии своевременного лечения судороги, последующие гипоксия и гиперкапния, а также угнетение сердечной деятельности под влиянием местных анестезирующих средств могут вызвать нарушения сердечного ритма, фибрилляцию желудочков и остановку сердца.
Воздействие на ССС . Предварительное введение жидкости и/или применение вазопрессоров позволяет предотвратить или уменьшить снижение АД . При снижении АД показана в/в инфузия кристаллоидов и коллоидов и/или введение вазопрессоров в возрастающих дозах (например эфедрин 5–10 мг). Также следует как можно быстрее устранить все другие причины снижения АД .
При развитии тяжелой брадикардии целесообразно введение атропина в дозе 0,3–1 мг, что позволяет увеличить ЧСС до допустимых значений. При возникновении нарушений сердечного ритма следует проводить соответствующее лечение, фибрилляция желудочков требует экстренной кардиоверсии.
Пути введения
Инъекционно.
Меры предосторожности вещества Левобупивакаин
Все виды местной или регионарной анестезии следует выполнять в хорошо оснащенном медицинском учреждении, персонал должен иметь опыт проведения регионарной анестезии, а также уметь диагностировать возможные нежелательные реакции и проводить соответствующее лечение.
Левобупивакаин может вызывать аллергические реакции, нарушения со стороны ССС и неврологические нарушения.
У пациентов с сердечно-сосудистыми заболеваниями, в частности с тяжелыми нарушениями ритма сердца, регионарную анестезию левобупивакаином нужно проводить с осторожностью.
У пациентов с предшествующими заболеваниями ЦНС попадание местного анестезирующего средства в ЦНС при эпидуральном введении может повлечь за собой обострение этих заболеваний. Поэтому при планировании эпидуральной анестезии у таких пациентов необходимо проводить соответствующую клиническую оценку.
Эпидуральная анестезия. Концентрированный раствор левобупивакаина (0,5–0,75%) при эпидуральной анестезии нужно вводить дробно по 3–5 мл, постепенно увеличивая дозу, при этом интервал между введениями должен быть достаточным, для того чтобы успеть определить токсические проявления в случае попадания ЛС в просвет сосуда или интратекально.
Описаны случаи тяжелой брадикардии, снижения АД и дыхательной недостаточности с остановкой сердечной деятельности при применении местных анестезирующих средств (некоторые из этих случаев закончились летальным исходом). При необходимости введения большой дозы левобупивакаина, например при эпидуральной блокаде, рекомендуется ввести предварительную тестовую дозу с 3–5 мл лидокаина с эпинефрином. Непреднамеренное попадание левобупивакаина в сосудистое русло можно распознать по временному нарастанию ЧСС , а случайное попадание его в подоболочечное пространство — по симптомам спинальной блокады. При продолжительном (интермиттирующем) введении левобупивакаина через катетер необходимо выполнять аспирационную пробу (перед первой и каждой последующей дополнительной инъекцией). Попадание левобупивакаина внутрь сосуда возможно даже при отсутствии крови в шприце во время аспирационной пробы. При выполнении эпидуральной анестезии рекомендуется вначале ввести тестовую дозу и отслеживать действие левобупивакаина до начала введения всей дозы целиком.
При введении любого местного анестезирующего средства необходимо выполнять аспирацию крови или спинномозговой жидкости (когда это необходимо) перед инъекцией основной и каждой последующей доз, чтобы избежать попадания ЛС в просвет сосуда или интратекально. Однако отрицательная аспирационная проба не гарантирует от попадания ЛС в сосудистое русло или подоболочечное пространство. У пациентов, получающих другие местные анестетики либо ЛС , схожие по структуре с местными анестетиками амидного типа, левобупивакаин следует применять с осторожностью из-за аддитивного токсического действия этих ЛС .
Регионарная блокада крупных нервных стволов. В целях обеспечения функционального венозного доступа пациенту должны в/в поступать жидкости через постоянный катетер. Чтобы в плазме крови не создавалась высокая концентрация левобупивакаина и не развивались серьезные нежелательные реакции, следует применять наименьшую дозу, позволяющую достичь эффективной анестезии. Нельзя вводить большой объем анестезирующего средства с высокой скоростью, по возможности левобупивакаин нужно вводить фракционно, постепенно увеличивая дозу.
Местная анестезия в области головы и шеи. Введение даже небольших доз левобупивакаина в область головы и шеи (при ретробульбарной блокаде, при блокаде во время стоматологических вмешательств и при блокаде звездчатого ганглия) может вызвать тяжелые нежелательные реакции, сходные с таковыми при системных токсических эффектах после случайной внутрисосудистой инъекции в большей дозе. Введение левобупивакаина требует предельной осторожности.
Возможно развитие реакций, вызванных в/а инъекцией анестезирующего средства и попаданием его в церебральный кровоток ретроградным путем. Нежелательные реакции также могут быть связаны с пункцией твердой мозговой оболочки зрительного нерва при ретробульбарной блокаде с диффузией какого-либо местного анестезирующего средства по субдуральному пространству в средний мозг. Необходимо проводить постоянное наблюдение и тщательное мониторирование показателей дыхательной и сердечной деятельности у пациентов, которым выполняются эти виды блокад. Также должны быть доступны оборудование для реанимационных мероприятий и персонал, имеющий соответствующую подготовку.
Применение в хирургической офтальмологии. Специалисты, выполняющие ретробульбарную блокаду, должны помнить о возможности развития остановки дыхания при местном введении анестезирующего средства. Как и при других вариантах регионарной анестезии, перед проведением ретробульбарной блокады необходимо убедиться в наличии оборудования, персонала и ЛС для лечения таких нарушений, как угнетение или остановка дыхания, судороги, возбуждение или подавление сердечной деятельности. Как и в случае других видов анестезии, после проведения ретробульбарной блокады необходимо постоянное наблюдение для отслеживания описанных нежелательных реакций.
Особые группы пациентов
Применение у ослабленных и пожилых пациентов, а также пациентов с острыми заболеваниями. Левобупивакаин у ослабленных и пожилых пациентов, а также пациентов с острыми заболеваниями следует применять с осторожностью.
Влияние на способность управлять транспортными средствами и работу с механизмами. Левобупивакаин может оказывать значительное влияние на способность управлять транспортными средствами и работать с механизмами. Необходимо предупредить пациентов о недопустимости управления транспортными средствами и работы с механизмами до разрешения всех эффектов анестезии и немедленных эффектов хирургического вмешательства.
M. Gozdemir 1 , B. Muslu 1 , H. Sert 1 , B. Usta 1 , R. I. Demircioglu 1 ,
O. F. Karatas 2 и O. Surgit 3
Departments of 1 Anesthesiology,
2 Urology and 3 General Surgery,
Faith University School of Medicine, Ankara, Turkey.
Транзиторные неврологические симптомы ( TNS ) после спинальной анестезии часто возникают на фоне применения лидокаина. Но подобные нарушения наблюдаются при применении и других анестетиков. Целью данного проспективного, рандомизированного, двойного слепого исследования было определить частоту TNS после спинальной анестезии после применения левобупивакаина или лидокаина.
Методы. В исследовании принимали участие пациенты, которым планировались операции по поводу паховой грыжи, аппендэктомия, операции по поводу варикозной болезни или малые ортопедические операции (60 пациентов, 47 мужчин, 13 женщин, средний возраст 30 лет). По системе ASA все пациенты входили в I или II класс. Всем пациентам выполнялась спинальная анестезия либо 20 мг изобарического левобупивакаина (5 мг/мл), либо 80 мг изобарического лидокаина (20 мг/мл). Отмечалось время начала сенсорного и моторного блоков и наличие побочных эффектов. На 1, 2 и 3 день после операции пациенток опрашивал анестезиолог, который не знал, к какой группе относится пациент. Диагноз TNS ставился, если после анестезии у пациента наблюдались боли в ягодицах, бедрах и/или нижних конечностях.
Результаты. В группе левобупивакаина TNS наблюдались у одного пациента (3,33%), в группе лидокаина у восьми (26,6%) (Р = 0,002). Максимальная скорость наступления сенсорного блока была меньше в группе лидокаина (Р ≤ 0,001). Группы не отличались по показателю наивысшего дерматома сенсорного и моторного блоков.
Заключение. После спинальной анестезии левобупивакаином частота TNS была гораздо ниже, чем в группе лидокаина. Однако видно, что TNS могут возникнуть и на фоне применения левобупивакаина.
При исследовании TNS чаще всего использовался спинальный анестетик лидокаин. Несколько исследований указывают на то, что лидокаин является причиной TNS после спинальной анестезии (4). По сравнению с лидокаином, бупивакаин в меньшей степени приводит к TNS после спинальной анестезии (2, 5-9). Целью данного проспективного, рандомизированного было определить частоту TNS у пациентов, которые выполнялась субарахноидальная анестезия либо левобупивакаином 5 мг/мл, либо лидокаином 20 мг/мл.
После получения одобрения местного этического комитета, в исследовании приняло участие 60 пациентов (47 мужчин, 13 женщин, средний возраст 30 лет (20-81 год)). Исследование проспективное, рандомизированное, двойное-слепое. Исследование проходило в период с января 2008 по декабрь 2008 года. По шкале ASA все пациенты относились к I или II классу. Они получали спинальную анестезию перед ортопедической операцией, вмешательством по поводу варикозной болезни, паховой грыжи или аппендицита. Все операции выполнялись при положении пациента на спине. Критериями исключения являлись: острая или хроническая патология, такая как тяжелая деформация позвоночника, операции на спине в анамнезе, неудачные попытки спинальной анестезии в анамнезе, неврологическая патология (рассеянный склероз, повреждения спинного мозга), сахарный диабет, ожирение – ИМТ более 30, аллергия на используемые лекарственные препараты. Все пациенты подписали информированное согласие. Первичной целью исследования было определение частоты TNS после спинальной анестезии, по критериям которые будут описаны ниже. Вторичной целью являлось определение других побочных эффектов спинальной анестезии.
Пациенты случайно распределялись по двум группам, в которых получали либо изобарический левобупивакаин HCI (Chirocaine 5 мг/мл, Abbott , Nycomed Pharma , Elverum , Norway ), либо изобарический лидокаин (20 мг/мл) ( рисунок 1 ).
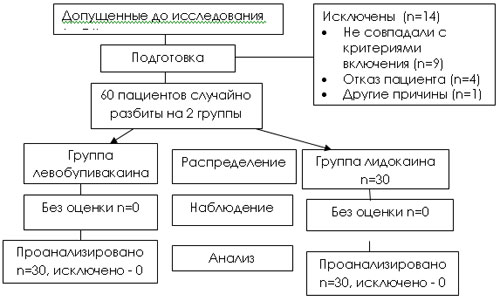 |
| Рисунок 1 . Диаграмма изучения транзиторных неврологическим симптомов у пациентов на фоне спинальной анестезии левобупивакаином или лидокаином. |
Оба препарата были приготовлены в дозе по 4 мл таким образом, что анестезиолог не знал, какой препарат он вводит. Так как исследование являлось рандомизированным и двойным-слепым, то доза анестетика была подобрана таким образом, что ее хватало для проведения любой манипуляции (малая ортопедическая, варикозная болезнь, паховая грыжа, аппендэктомия). Пациенты были проинформированы о том, что действие анестезии длится в течение нескольких часов и после операции. Премедикация ни одному пациенту не выполнялась. До операции начиналась внутривенная инфузия раствора Рингера и она продолжалась во время операции со скоростью 10 мл/кг/час. Рутинно выполнялись ЭКГ, контроль АД и пульс оксиметрия.
Спинальная анестезия проводилась следующим образом: в положении сидя пациенту обрабатывали кожу 10% раствором повидон-йода в изопропиле алкоголя. В промежуток L2-3 или L3-4 вводилась 25G single–orifice Quincke cutting-point-type игла (Spinocan, B. Braun Melsungen AG, Melsungen , Germany ). После свободного получения спинномозговой жидкости осуществлялось введение анестетика. После этого немедленно изменялось положение тела пациента в положение лежа с небольшим возвышением головного конца. Во время спинальной анестезии при возникновении гипотонии (снижение среднего АД более чем на 25%) проводилась инъекция 5 или 10 мг эфедрина и болюсное введение 200 мл раствора Рингера. При брадикардии (снижении ЧСС ниже 50 ударов в минуту) вводилось 0,5 мг атропина.
Все пациенты находились в больнице до следующего утра после операции и опрашивались одним из исследователей перед выпиской. Через 2 дня опрос проводился по телефону. Исследователи не знали, к какой группе относится пациент. С использованием стандартного списка симптомов, пациентов спрашивали, испытывали ли они следующие симптомы: головную боль, боль в спине, боль не связанную с операцией, сенсорные нарушения, изменения мышечной силы, трудности в физиологических отправления. Особое внимание уделялось симптомам, которые были связаны с нижними конечностями, типам боли и распространению боли ( таблица 1 ).
Таблица 1 . Послеоперационный перечень симптомов после спинальной анестезии,
связанных с нижними конечностями.
Бедро (передняя поверхность)
Бедро (задняя поверхность)
Пациенты оценивали боль по визуальной аналоговой шкале. TNS диагностировали при боли и/или дизестезии в области ягодиц, бедер и/или нижних конечностях после восстановлении от анестезии в том случае, если болевой синдром не был связан с операцией. Отмечалось время от начала блока до появления TNS . Послеоперационный болевой синдром, включая связанный с TNS , лечили с помощью dexketoprofen trometamol 25 мг по 2 таблетки 2 раза в день.
Через одну неделю после спинальной анестезии, пациентов с TNS вновь опрашивали по телефону. Особое внимание уделяли головной боли, боли в спине, боль в области послеоперационной раны, боли в бедрах, ягодицах, икрах и в других областях. Оценивались симптомы и их продолжительность. У пациентов также спрашивали о степени их удовлетворения после спинальной анестезии.
Первичной целью было определить общую частоту TNS в группах левобупивакаина и лидокаина. Продолжительность наблюдения составила 3 дня. Для сравнения использовалась работа Hampl и коллег (8) о частоте TNS на фоне применения лидокаина. Для обеспечения 80% степени с использованием двустороннего t-теста с α = 0,05 необходима группа из, как минимум, 28 пациентов. Статистический анализ проводился с использованием SPSS , версия 11.0 (SPSS Inc ., Chicago , IL). Демографические характеристики групп сравнивались посредством t-теста и Mann - Whitney U -тест. Общая частота случаев TNS сравнивалась между группами с использованием х 2 -теста. Данные выражались как среднее и диапазон значений (%). Статистическая разница определялась как Р ≤ 0,05.
Группы левобупивакаина и лидокаина значительно не отличались по времени достижения максимального блока ( таблица 2 ). Время развития максимального сенсорного блока было значительно дольше в группе левобупивакаина (Р = 0,01, таблица 2 ). Группы не различались по максимальным показателям сенсорного и моторного блоков ( таблица 2 ).
Таблица 2. Характеристика пациентов и показатели спинальной анестезии.
Группа левобупивакаина (n=30)
Группа лидокаина
(n=30)
Во время операции, 2 пациента из группы левобупивакаина и 3 из группы лидокаина жаловались на боль во время операции. В этих случаях спинальная анестезия дополнялась внутривенным введением фентанила, общего обезболивания не потребовалось. Гипотония и брадикардия наблюдалась у двоих пациентов в каждой группе.
TNS развились у одного пациента (1/30, 3,33%) в группе левобупивакаина и у восьми пациентов (8/30, 26,6%) в группе лидокаина (Р = 0,002, таблица 3 ). У девяти пациентов с TNS развилась двусторонняя симптоматика. Через неделю клиники TNS отмечено не было. Распределение болевого синдрома представлено в таблице 3 . У более чем половины пациентов боль распространялась на различные зоны, включая ягодицы, бедра и нижние отделы ног ( таблица 3 ). Среди восьми пациентов в группе лидокаина, которые испытывали TNS , выраженность болевого синдрома варьировала от 1/10 до 6/10 (в среднем 3/10).
Таблица 3. Транзиторные неврологические симптомы
после спинальной анестезии в обеих группах
Один пациент, у которого развилась TNS после анестезии на фоне левобупивакаина, получал 20 мг препарата для удаления варикоцеле. Уровень боли составил 6/10 с иррадиацией в ягодицы и бедра. Боль возникла на следующий день после операции и купировалась через 72 часа. Нарушений мочеиспускания и дефекации отмечено не было. Холодовой тест и тест с булавкой не показал гиперальгезии или потери чувствительности, глубокие рефлексы сухожилий не нарушены. Радиограммы поясничного отдела позвоночника не выявили патологии. Эти данные совпадают с TNS . Все пациенты с TNS в группе лидокаина хорошо ответили на терапию НПВП (dexketoprofen trometamol).
У двух пациентов из группы левобупивакаина наблюдались затруднения в пассаже мочи в течение первых 24 часов после спинальной анестезии. Умеренная послеоперационная тошнота в день операции наблюдалась у трех пациентов из группы левобупивакаина и у четырех в группе лидокаина. Через неделю у одного пациента в каждой группе наблюдался постпункционный болевой синдром, который был купирован консервативно. Эти пациенты не жаловались на боли в спине.
Возникновение TNS связано с анестетиком, который используется во время анестезии (4). Было показано, что лидокаин связан с TNS больше, чем другие анестетики (4). Как результат темой обсуждения является поиск альтернативных препаратов. Например, применение бупивакаина приводит к снижению частоты TNS (2, 4-9). Левобупивакаин, который является одним из стереоизомеров бупивакаина (10), похож на бупивакаин по обезболивающим свойствам (11) и должен обладать меньшей частотой развития TNS . При обзоре литературы была найдена лишь одна публикация о частоте TNS на фоне приема левобупивакаина (12). Данное исследование было разработано специально для ликвидации подобного пробела.
Авторы обнаружили, что частота TNS на фоне спинальной анестезии левобупивакаином была гораздо ниже, чем после применения лидокаина (3% против 27%). Эти данные совпадают с исследованиями бупивакаина (2, 3, 5, 6, 9), а также с данными единственного исследования левобупивакаина (12). В ходе данного исследования, у 30 пациентов на фоне применения левобупивакаина TNS не развилась, а в группе лидокаина таких пациентов было 3. Симптомы купировались в течение 24 часов.
Частота TNS после спинальной анестезии лидокаином составляет 0-40% (9, 13-16). В ходе настоящего исследования данная частота составила 26,6%. Авторы использовали дозировку в 20 мг/мл (2%) раствора лидокаина. В предыдущих исследованиях концентрация была следующей: 2% или 5% (5, 17), 1% или 5% (18), 2%, 1% или 0,5% (5). Концентрация не влияет на частоту TNS , поэтому следует искать другие причины.
Физиологический механизм TNS до конца не ясен. В 1993 году Schneider и коллеги (1) описали четырех пациентов с транзиторной болью в ягодицах и/или нижних конечностях после спинальной анестезии гипербарическим 5% лидокаином на 7,5% декстрозе. Авторы полагали, что симптомы возникали вследствие высокой концентрации и гипертонуса раствора анестетика. Дальнейшие исследования концентрации лидокаина (5, 17-20), концентрации глюкозы (5) и осмолярности (17) показали, что данные показатели не влияют на риск развития TNS .
К факторам риска развития TNS на фоне лидокаина относятся литотомическое положение и амбулаторный статус (6), а ранняя мобилизация не оказывает влияния (21, 22). TNS также может развиться на фоне спинальной анестезии с другими анестетиками (4). Исследования на животных показали, что местные анестетики обладают нейротоксичным действием (23-26), но исследования на волонтерах, которые получали лидокаин при спинальной анестезии, не показали постоянных электрофизиологических аномалий у пациентов с TNS (27).
Ограничением данного исследования являлось небольшой размер группы. В эпидемиологическом исследовании пациентов после спинальной анестезии было показано, что из 744 пациентов, которые получали бупивакаин, лишь у 10 (1,3%) развилась TNS (6). Частота TNS на фоне применения левобупивакаина также кажется низкой, поэтому необходимы крупные исследования с большим количеством пациентов. Также полезно проспективно сравнить левобупивакаин и бупивакаин, что является следующим этапом в нашем институте.
В заключении можно сказать, что частота TNS на фоне применения левобупивакаина ниже, чем на фоне применения лидокаина. Однако, все-таки, TNS может развиваться на фоне использования левобупивакаина.
- Schneider M, Ettlin T, Kaufmann M, Schumacher P, Urwyler A, Hample K, Arthur AV. Transient neurologic toxicity after hyperbaric subarachnoid anesthesia with 5% lidocaine. Anesth Analg 1993; 76: 1154–7.
- Hampl KF, Schneider M, Ummenhofer W, Drewe J. Transient neurologic symptoms after spinal anesthesia. Anesth Analg 1995; 81: 1148–53.
- Tarkkila P, Huhtala J, Tuominen M. Transient radicular irritation after spinal anaesthesia with hyperbaric 5% lignocaine. Br J Anaesth 1995; 74: 328–9.
- Zaric D, Pace NL. Transient neurologic symptoms (TNS) after spinal anesthesia with lidocaine versus other local anesthetics. Cochrane Database Syst Rev 2009; 15: CD003006.
- Pollock JE, Neal JM, Stephenson CA ,Wiley CE. Prospective study of the incidence of transient radicular irritation in patients undergoing spinal anesthesia. Anesthesiology 1996; 84: 1361–7.
- Freedman JM, Li D-K, Drasner K, Jaskela M, Larsen B,Wi S. Transient neurologic symptoms after spinal anesthesia: an epidemiologic study of 1,863 patients. Anesthesiology 1998; 89: 633–41.
- Tarkkila K, Huhtala J, Tuominen M. Transient radicular irritation after bupivacaine spinal anesthesia. Reg Anesth 1996; 21: 26–9.
- Hampl KF, Heinzmann-Wiedmer S, Luginbuehl I, Harms C, Seeberger M, Schneider MC, Drasner K. Transient neurologic symptoms after spinal anesthesia: a lower incidence with prilocaine and bupivacaine than with lidocaine. Anesthesiology 1998; 88: 629–33.
- Keld DB, Hein L, Dalgaard M, Krogh L, Rodt SA. The incidence of transient neurologic symptoms (TNS) after spinal anaesthesia in patients undergoing surgery in the supine position. Hyperbaric lidocaine 5% versus hyperbaric bupivacaine 0.5%. Acta Anaesthesiol Scand 2000; 44: 285–90.
- McLeod GA, Burke D. Levobupivacaine. Anaesthesia 2001; 56: 331–41.
- Glaser C, Mayrhofer P, Zimpfer G, Heinz MT, Sitzwohl C, Kapral S, Schindler I. Levobupivacaine versus racemic bupivacaine for spinal anesthesia. Anesth Analg 2002; 94: 194–8.
- Breebaart MB, Vercauteren MP, Hoffmann VL, Adriaensen HA. Urinary bladder scanning after day-case arthroscopy under spinal anaesthesia: comparison between lidocaine, ropivacaine, and levobupivacaine. Br J Anaesth 2003; 90: 309–13.
- Ostgaard G, Hallara°ker O, Ulveseth OK, Flaatten H. A randomised study of lidocaine and prilocaine for spinal anaesthesia. Acta Anaesthesiol Scand 2000; 44: 436–40.
- Salazar F, Bogdanovich A, Adalia R, Chaba?s E, Gomar C. Transient neurologic symptoms after spinal anaesthesia using isobaric 2% mepivacaine and isobaric 2% lidocaine. Acta Anaesthesiol Scand 2001; 45: 240–5.
- Pollock JE. Transient neurologic symptoms: etiology, risk factors, and management. Reg Anesth 2002; 27: 581–6.
- Fanelli G, Daneli G, Zasa M, Baciarello M, Di Cianni S, Leone S. Intrathecal ropivacaine 5mg/ml for outpatient knee arthroscopy: a comparison with lidocaine 10 mg/ml. Acta Anaesthesiol Scand 2009; 53: 109–15.
- Hampl KF, Schneider MC, Pragger H, Gut J, Drewe J, Drasner K. A similar incidence of transient neurologic symptoms after spinal anesthesia with 2% and 5% lidocaine. Anesth Analg 1996; 83: 1051–4.
- Tong D,Wong J, Chung F, Friedlander M, Bremang J, Mezei G, Streiner D. Prospective study on incidence and functional impact of transient neurologic symptoms associated with 1% versus 5% hyperbaric lidocaine in short urologic procedures. Anesthesiology 2003; 98: 485–94.
- Pollock JE, Liu SS, Neal JM, Stephenson CA. Dilution of spinal lidocaine does not alter the incidence of transient neurologic symptoms. Anesthesiology 1999; 90: 445–50.
- Imbelloni LE, Gouveia MA, Cordeiro JA. Low dose of lidocaine: comparison of 15 with 20 mg/ml with dextrose for spinal anesthesia in lithotomy position and ambulatory surgery. Acta Anaesthesiol Scand 2008; 52: 856–61.
- Silvanto M, Tarkkila P, Makela MJ, Rosenberg PH. The influence of ambulation time on the incidence of transient neurologic symptoms after lidocaine spinal anesthesia. Anesth Analg 2004; 98: 642–6.
- Cramer BG, Stienstra R, Dahan A, Arbous MS, Veering BTh, Van Kleef JW. Transient neurological symptoms with subarachnoid lidocaine: effect of early mobilization. Eur J Anaesthesiol 2005; 22: 35–9.
- Drasner K, Sakura S, Chan VW, Bollen AW, Ciriales R. Persistent sacral sensory deficit induced by intrathecal local anesthetic infusion in the rat. Anesthesiology 1994; 80: 847–52.
- Lambert LA, Lambert DH, Strichartz GR. Irreversible conduction block in isolated nerve by high concentrations of local anesthetics. Anesthesiology 1994; 80: 1082–93.
- Huang YF, Pryor ME, Mather LE, Veering BT. Cardiovascular and central nervous system effects of intravenous levobupivacaine and bupivacaine in sheep. Anesth Analg 1998; 86: 797–804.
- Marganella C, Bruno V, Matrisciano F, Reale C, Nicoletti F, Melchiorri D. Comparative effects of levobupivacaine and racemic bupivacaine on excitotoxic neuronal death in culture and N-methyl-D-aspartate-induced seizures in mice. Eur J Pharmacol 2005; 518: 111–5.
- Pollock JE, Burkhead D, Neal JM, Liu SS, Friedman A, Stephenson C, Polissar NL. Spinal nerve functions in five volunteers experiencing transient neurologic symptoms after lidocaine subarachnoid anesthesia. Anesth Analg 2000; 90: 658–65.
Address:
Muhammet Gozdemir
Department of Anaesthesiology
Fatih University School of Medicine
Alparslan TurkeS Caddesi No. 57
06510 Ankara
Turkey
Читайте также:


